
第五章第一节求质量、化学式及确定元素种类学校:___________姓名:___________班级:___________考号:___________
一、简答题
1.【最新】5月,某市自来水有股奇怪的味道,经专家多轮综合检测,基本认定引起此次异味的主要物质是邻叔丁基苯酚。将30克邻叔丁基苯酚完全燃烧,生成88克CO2
和25.2克H2O(无其他产物)。已知邻叔丁基苯酚的相对分子质量为150,求:
(1)30克邻叔丁基苯酚中含碳元素_____克,氢元素______克。
(2)邻叔丁基苯酚的化学式为____________。
二、填空题
2.某有机物W和氧气置于完全封闭的容器中引燃,充分反应后,生成二氧化碳和水。实验测得反应前后物质质量如表所示:
根据上表数据回答问题:
(1)反应后x的值为_______;已知W的相对分子质量为46,则W物质化学式为_______。(2)反应生成的二氧化碳和水分子个数比为_______。
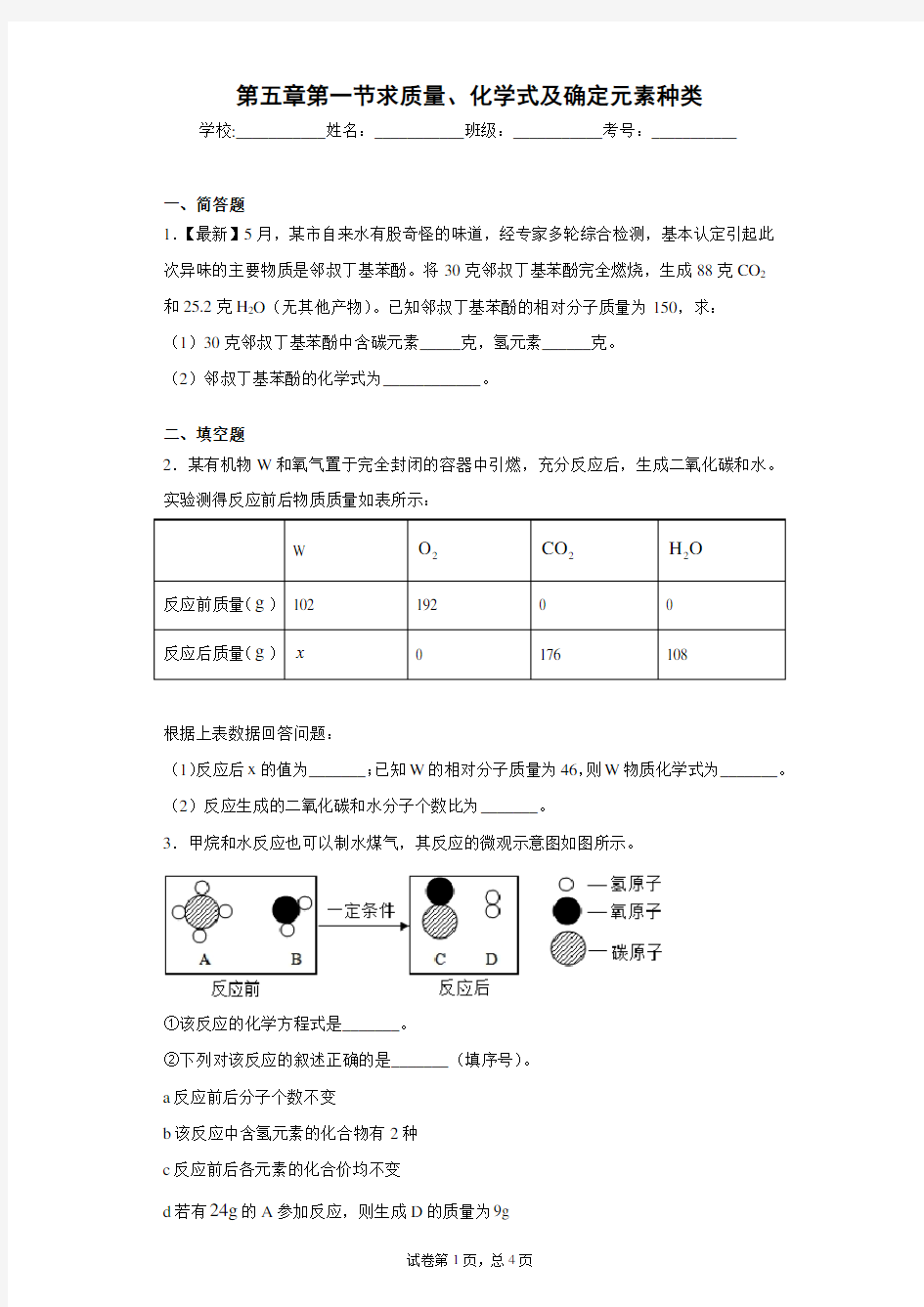
3.甲烷和水反应也可以制水煤气,其反应的微观示意图如图所示。
①该反应的化学方程式是_______。
②下列对该反应的叙述正确的是_______(填序号)。
a反应前后分子个数不变
b该反应中含氢元素的化合物有2种
c反应前后各元素的化合价均不变
d若有24g的A参加反应,则生成D的质量为9g
4.工业上用甲、乙制备化学肥料丙,同时有丁生成。根据下列微观示意图得出的结论中,正确的( )
①甲的化学式为NH3②乙、丙、丁都是氧化物
③丙中氮、氢元素质量比为7:1 ④参加反应的甲、乙质量比为17:44
A.①B.①③C.①④D.②④
5.某反应A+B C+D,若A和B的混合物35g,恰好完全反应生成5g C。而生成C和D的混合物7g需要5g A,则4g B和足量A充分反应能生成_______g的D。6.化学用语帮助我们建立起宏观世界与微观世界的联系:
(1)用化学符号表示出“两个氢原子”:_______。
H O”的各种表达正确的是_______。
(2)下列对于化学式“2
A表示水这种物质
B表示水分子由氢元素和氧元素组成
C表示1个水分子
D表示水分子由2个氢原子和1个氧原子构成
C H O,它是由_______种元素组成的,其中氢、氧元素的质(3)二甲醚的化学式为26
量比为_______。(写最简整数比)
(4)在一个密闭容器中放入X、Y、Z、W四种物质,在一定条件下发生化学反应,一段时间后,测得有关数据如表所示,则关于此反应的认识不正确的是_______。
A 物质Y 可能是该反应的催化剂
B 该反应的基本类型为分解反应
C 参加反的Z 与W 的质量比为2:3
D 反应后容器中Z 与Y 的质量比为6:1
(5)A 、B 、C 、D 表示4种物质,其微观示意图见表。A 和B 在一定条件下反应可生成C 和D 。下列说法正确的是_______(填数字序号)。
①4种物质均由分子构成 ②该反应属于置换反应
③反应中C 、D 两种物质的质量比为11:7 ④4种物质中属于氧化物的是A 、B ⑤若有28g A 完全反应,则有14g D 生成
三、单选题
7.某物质在空气中完全燃烧生成8.8g 二氧化碳和5.4g 水,则关于这种物质的组成描述正确的是( )
A .该物质只含有碳元素和氢元素
B .该物质中碳元素与氢元素的质量比为12:1
C .该物质一定含有碳元素和氢元素,可能含有氧元素
D .该物质的分子中碳原子与氢原子的个数比为1:2 8.某物质(用R 表示)在空气中燃烧的方程为222R+3O 2CO +3H O 点燃
,则R 的化
学式为( )。 A .3CH COOH
B .25
C H OH
C .3CH OH
D .4CH
9.在反应A +B→C +D 中,A 与B 参加反应的质量比为4∶3,生成的C 和D 的质量和为2.8g ,则参加反应的B 的质量为( )。 A .0.3 g
B .0.9g
C .1.2g
D .1.6g
10.有机物X 在足量的氧气中燃烧,生成二氧化碳和水的质量比为44:27,则X 的化学式可能( )。 A .4CH
B .3CH OH
C .24C H
D .26C H O
11.在反应4A+3B
2C 中,2.7g A 完全反应后生成5.1g C 。已知B 的相对分子质
量为32,则C 的相对分子质量是( )。 A .34 B .68
C .102
D .204
参考答案
1.24 2.8 C 10H 14O 【详解】
根据质量守恒定律可知生成物二氧化碳中的碳元素和水中的氢元素即为30g 邻叔丁基苯酚中碳元素和氢元素的质量。 (1)碳元素的质量=88g×
12100%44?=24g ;氢元素的质量=25.2g×2
100%18
?=2.8g ;根据24g+2.8g=26.8g<30g ,所以邻叔丁基苯酚中含有的元素为碳、氢、氧三种元素,氧元素的质量=30g-24g-2.8g=3.2g ;
(2)邻叔丁基苯酚中碳、氢、氧的原子个数比为:24g 2.8g 3.2g
::=10:14:112116
,故其化学式为:C 10H 14O 。
2.10 26C H O 2:3 【解析】 【详解】
(1)根据质量守恒定律可以知道待测值x=102g+192g-176g-108g=10g ;反应中生成二氧化碳中碳元素的质量为:12
176g 100%=48g 44
?
?,生成水中氢元素的质量为2
110800g 12g 8
%=1?
?,W 参加反应的质量为102g-10g=92g ,+1248g g<92g ,则可以知道W 中一定含有碳元素、氢元素、氧元素,氧元素质量为()102g-10g -48g-12g=32g ,
C H O 、、原子个数比为
48g 12g 32g
::=4:12:2=2:6:112116
,由W 的相对分子质量为46可知,W 的化学式为26C H O ;
(2)根据二氧化碳和水的质量为176g 108g 、
和其相对分子质量为44、18,则反应生成二氧化碳和水的分子个数比为2:3。 3.224O CO+3CH H H +一定条件下
bd
【详解】
①由反应的微观示意图可知,反应前的物质是甲烷和水,反应后的物质是一氧化碳和氢气,反应的方程式为:224O
CO+3CH H H +一定条件下
;
②根据化学方程式判断选项是否正确;
A、根据反应方程式可见,反应前后分子数目发生改变,叙述错误;
B、含氢元素的化合物是甲烷和水2种,叙述正确;
C、反应后碳元素和氢元素反应前后的化合价发生改变,叙述错误;
D、根据反应方程式计算,624g
=9g
16
?
,24g的A能生成9g的D,叙述正确。
故填:bd。
4.B
【详解】
观察微观示意图,可知反应物、生成物甲、乙、丙、丁分别是:NH3、CO2、CO(NH2)2、
H2O,因此反应的方程式是:2NH3+CO2一定条件
CO(NH2)2+H2O,由此可知:
①甲的化学式为:NH3,故正确;
②4种物质中只有CO2、H2O属于氧化物,而CO(NH2)2不是氧化物,故错误;
③丙为CO(NH2)2,其中氮、氢元素的质量比为(14×2):(1×4)=7:1,故正确;
④参加反应的甲、乙的质量比为:(2×17):44=34:44,故错误;
所以,①③正确,②④错误。
故选B。
5.12
【详解】
根据质量守恒定律可以知道,35g A和B混合物恰好完全反应生成D的质量为:
35g-5g=30g。则当生成C和D的混合物7g时,消耗B的质量为7g-5g=2g,D的质量为
30g
7g=6g
35g
?,
设第二次生成D的质量为x,则
A B C D
2g6g
4g x
+=+
2g 4g =x=12g 6g x
?。 故填:12。
6.2H AC 3 3:8 BC ①⑤ 【详解】
(1)两个氢原子为2H 。
(2)考查化学式的意义,2H O 可以表示水这种物质,可以表示水是由氢元素和氧元素组成,
可以表示一个水分子,表示一个水分子由两个氢原子和一个氧原子构成。 (3)二甲醚是由三种元素组成,其中氢元素和氧元素的质量之比为3:8;
(4)A 、因X 增加的质量等于Z 和W 减少的质量之和,则Y 的质量在该反应中不发生变化,Y 可能做催化剂,认识正确,不符合题意;
B 、该反应是Z 和W 反应生成X ,符合两种物质反应生成一种物质,则属于化合反应,不是分解反应,认识错误,符合题意;
C 、反应的Z 和W 的质量比为()()16-6g:16-11g=2:1,认识错误,符合题意;
D 、反应后Z 为6g ,Y 为1g ,则Z 和Y 的质量比为6:1,认识正确,不符合题意。 故填:BC 。
(5)
A 和
B 反应生成
C 和
D 反应的化学反应方程式为222CO+2NO CO N 2+一定条件下
,
①四种物质均由分子构成,说法正确;
②反应前是两种化合物该反应不是置换反应,说法错误; ③反应中C 和D 的质量之比22:7,说法错误; ④四种物质中属于氧化物的是ABC ,说法错误;
⑤A 和D 的相对质量之比为56:28,所以28g 的A 能生成14g 的D ,说法正确。 故①⑤说法正确,故填:①⑤。 7.C 【详解】
A 、这种物质中一定有碳元素和氢元素,氧元素可能有也可能没有,描述错误;
B 、该物质中碳元素质量等于二氧化碳中碳元素的质量,该物质中氢元素质量即为水中氢元
素质量,故该物质中碳元素与氢元素的质量比122
=(8.8g ):(5.4g )=4:14418
?
?,描述错误; C 、该物质中一定有碳元素和氢元素,氧元素可能有也可能没有,描述正确; D 、该物质的分子中碳原子和氢原子的个数比 2.4g 0.6g :=1:3121
=,描述错误。 故选C 。 8.B 【分析】
通常提供化学方程式,考查化学反应中原子守恒的应用,所谓原子守恒是指反应前后各种元素的原子总数相等,依此确定某一反应物或生成物的化学式。 【详解】
根据原子守恒:反应前后各种元素的原子总数相等,则R 中碳原子个数=2,氢原子个数=6,氧原子个数=4+3-6=1,各选项中只有25C H OH 符合条件。 故选B 。 9.C 【详解】
根据质量守恒定律,参加反应的A 和B 的质量和等于生成的C 和D 的质量总和相等,所以参加反应的B 的质量=3
2.8g 1.27
g ?=,故选C 。 10.D 【详解】
根据题意“生成的2CO 与水的质量比为44:27”,则生成物中碳元素和氢元素的质量比
12= (44100%):(2
271100%)=4:18
44???
?,碳原子和氢原子的数目之比为1:3。 A 、4CH 中碳原子与氢原子的数目比为=1:4,不符合题意; B 、碳原子和氢原子的数目之比是1:4,不符合题意; C 、24C H 中碳原子与氢原子的数目之比是1:2,不符合题意; D 、25C H OH 中碳元素与氢元素的数目比为=1:3,符合题意。 故选D 。 11.C 【详解】
根据质量守恒定律,B 的质量=5.1g-2.7g=2.4g 设C 的相对分子质量为a 。
4A +3B =2C
3322a 2.4g 5.1g ? 332 2.4g
=a=1022a 5.1g
??。 故选C 。
花卉品种大全鲜花图片花卉图片大全大花惠兰 大花惠兰品种多样,黄的、粉的、红的等花色繁多。棵型较大,株高在1.3米左右,适宜摆放在面积较大的空间。通常放在花架上,显得大方,温馨。大花惠兰抗寒性能好,易养护,正常浇水即可。花期较长,一般在二、三个月,但花败后,一般不易再养出花来。大花惠兰属中高档花卉,价格与花剑的数量有关系,花剑越多,则价格越高,一般每加一个花剑,价格要增加30元左右,而如果几株组合在一起,价格会更高。 彩色马蹄莲 彩色马蹄莲是现在石家庄花卉市场上的花卉新品,但数量较少,新颖、高档,是送礼的佳品。一般的马蹄莲以白色居多,彩色马蹄莲是因为嫁接了其他花卉的基因,从而培育出了各种颜色。棵型较小,株高在40厘米左右,适合放在桌子、茶几、角柜上,作为家具的点缀。花期在一个月左右,一般三、四天浇一次水,并要一次浇透,叶片上可以喷水,平时可以用水或啤酒擦拭叶片,亮亮的叶片更能衬托出彩色马蹄莲花瓣的高贵。花瓣的颜色一般有渐变的效果,叶型美观且多种多样,并带着一些小斑点,花败后可以观叶。 百合 百合是今年的流行,相比去年却不太流行。百合的花冠较大,香味浓郁,如果在房间的一角放上一盆,整个室内都能闻到它的香味。百合格调高雅,但不能因为百合好看而摆放过多,否则效果会适得其反,一般可以选择5株一盆的组合,放在门、窗附近等上风口,以利于香味的扩散,但百合怕风,不能被风吹到。百合的花期较短,在15度左右的室内温度下,大概在半个月左右,花败后,叶子的观赏价值不大,一般的家庭也不易再养出花来。室内温度严重影响百合的花期,养百合主要是控制好室内温度,如果室内温度过高,从花苞到开花,可能只用一个晚上。百合花在似开非开、手指能伸进去时,应该把花蕊轻轻摘下,以防止花粉掉到花瓣上形成橙色斑点。百合的花苞很漂亮,一盆百合中如果既有有盛开的花瓣,又有待放的花苞,百合的格调会被释放得淋漓尽致。 郁金香 郁金香也是今年比较流行的品种,相比去年也不太流行,今年的数量也多一些。与其他花卉相比,郁金香的花色、品种丰富多样,花型的大小差距较大,大小、株高的变化较多,
1. 初中化学常用的30种元素的元素符号 HHeLiBeB 氢氦锂铍硼 CNOFNe 碳氮氧氟氖 NaMgAlSiP 钠镁铝硅磷 SClArKCa 硫氯氩钾钙 MnFeCuZnAg 锰铁铜锌银 IBaPtAuHg 碘钡铂金汞2.化合价口诀 负一硝酸氢氧根,负二硫酸碳酸根。 负三记住磷酸根,正一价的是铵根。 一价氢氯钾钠银;二价氧钙钡镁锌。 三铝四硅五价磷,二三铁,二四碳。 二四六硫价都齐全,铜汞二价最常见。 单质零价永不变。
3.离子符号 硝酸根离子:NO3- 氢氧根离子:OH- 硫酸根离子:SO42- 碳酸根离子:CO32- 氢离子:H+ 氯离子:Cl- 钾离子:K+钠离子:Na+ 银离子:Ag+ 氧离子:O2-钙离子:Ca2+钡离子:Ba2+ 镁离子:Mg2+锌离子:Zn2+铝离子:Al3+亚铁离子:Fe2+ 铁 离子:Fe3+ 硫离子:S2- 铜离子:Cu2+ 4.俗名 生石灰:CaO 熟石灰:Ca(OH)2 火碱、烧碱、苛性钠:NaOH 纯碱、苏打:Na2CO3 小苏打:NaHCO3 5. 化学式(正前负后,标价化简,交叉检验) 单质 氢气H2氦气He氧气O2氮气N2氖气Ne钠Na硅Si铝Al 硫S氯气Cl2钾K氩气Ar 锰Mn铁Fe铜Cu锌Zn 镁Mg银Ag镉Cd锡Sn 氙气Xe钡Ba铂Pt金Au 硒Se碘I2臭氧O3铅Pb 氧化物 水H2O过氧化氢H2O2一氧化碳CO 一氧化氮NO二氧化氮NO2氧化钠Na2O 氧化铝Al2O3二氧化硅SiO2五氧化二磷P2O5三氧化硫SO3二氧化硫SO2氧化钙CaO 氧化亚铁FeO氧化铁Fe2O3四氧化三铁Fe3O4氧化铜Cu O氧化镁MgO二氧化碳CO2 酸 硝酸HNO3盐酸HCl硫酸H2SO4碳酸H2CO3乙酸CH3COOH 碱
元素质量分数试题例析 一、根据化合物中某元素的质量分数求化学式 例1:已知锰元素的一种氧化物中氧元素的质量分数为50.5%,此氧化物的化学式为( )。 A .M nO B .Mn O 23 C .MnO 2 D .Mn O 27 分析:设氧化物的化学式为Mn O x y ,则有5516495%505%x y ::=..,解得 x y ::=27。故选D 。 二、根据化合物中某元素的质量分数求相对分子质量 例2:“骨质疏松症”是人体缺钙引起的,可服用补钙剂来治疗。乳酸钙是一种常见的补钙剂,测知乳酸钙分子中含有一个钙原子,钙元素的质量分数为18.34%,则乳酸钙的相对分子质量为______________。 分析:根据化合物中,某元素的质量分数=??n 相对原子质量相对分子质量 ,100%则有: 1834%140100%.=??相对分子质量 ,解得相对分子质量为218。 故答案为218。 三、根据混合物中一种元素的质量分数,求另一种元素的质量分数 例3:由Na S Na SO Na SO 22324、、三种物质组成的混合物中,测得硫元素的质量分数为32%,则氧元素的质量分数为____________。 分析:观察三种物质的化学式的特征可知,所含Na 与S 的原子个数比均为2:1,由此可知,两种元素有固定的质量比,其质量比等于相对原子质量之和的比,还等于质量分数比,因此有2323232% ?=Na 的质量分数,解得钠元素的质量分数为46%,氧元素的质量分数为:132%46%22%--=。 故答案为22%。 四、根据混合物中某元素的质量分数,确定物质的组成 例4:某气体由CO CH SO 、、42中的一种或几种组成,已知氧元素的质量分数为50%,则该气体的组成可能有____________种,分别为____________。 分析:三种化合物中氧元素的质量分数分别为57.14%、0.50%,如果该气体由一种物质组成,只能为SO 2;如果由两种物质组成,根据平均值法,其中一种物质中氧元素的质量分数应小于50%,另一种物质中氧元素的质量分数应大于50%。故该气体应由CO 和CH 4组成;三种物质都含有也符合要求。 故答案为3种,分别为SO CO CH CO CH SO 2442;、;、、。
元素、元素符号、化合价和化学式 1. 下列选项中的元素都属于非金属元素的是( ) A .H 、S 、C B .Ca 、F 、Cl C .O 、Br 、Al D .P 、K 、N 2、下列符号表示两个氮原子的是( ) A .N B .2N C .N 2 D . N 2+ 4、下列物质中硫元素化合价最高的是( ) A .S B .K 2SO 4 C .SO 2 D .H 2S 5、下列符号既表示一种元素,又表示一个原子,还表示一种物质的是( ) A .2N B .O C .SO 2 D .Zn 6、10个H 2O 和10个H 2SO 4分子中一样多的是( ) A .氢分子个数 B .氢原子个数 C .氢元素个数 D .氢气 7、下列物质的化学式书写正确的是( ) A .氖气Ne 2 B .氧化铁FeO C .硫酸钠Na 2SO 4 D .硝酸钙CaNO 3 8、A 、B 、C 三种元素的化合价分别为+1、+2、-2,这三种元素组成的化合物分子式可能是( ) A 、ABC 4 B 、A 4B C 3 C 、A 2BC 3 D 、A 3BC 3 9、我国最新研制的高温超导材料氮化硼,经测定该材料中两种元素的原子个数比为1∶1。该材料的化学式为( ) A 、BN B 、B 3N 2 C 、NB D 、B 2N 3 10、对Mg 和Mg 2+认识不正确的是 ( ) 是同一种元素和、+2Mg Mg A 化合价不同与、+2Mg Mg B 多两个质子比、+2Mg Mg C 多两个电子比、+2Mg Mg D 11、元素中文名称大多数都是使用形声造字法,根据元素名称的汉字可判断金属元素、非金属元素。下列各组元素属于非金属元素的一组是( ) A 、汞、铁、铝、锕 B 、氪、铹、镧、碘 C 、溴、氟、砷、碲 D 、汞、溴、砹、氡 12、下列符号通常用来表示微观意义而不表示宏观意义的是( ) A 、 H B H 2 C 2H D H 2O 13、下列化学式书写错误的是( ) A 、 Na 2SO 4 B AlO C ZnCl 2 D K 2O 14、下列五种物质中均含有碘元素,它们按下列顺序排列:①KI ②I 2 ③HIO ④X ⑤NaIO 4根据这种排列规律,X 不可能是( ) A 、 I 2O 4 B 、 I (IO 3)3 C 、 AgI D 、 I 2O 5 15、在下列各组物质中,锰元素的化合价由高到低排列的是( ) A 、 K 2MnO 4 KMnO 4 MnO 2 Mn B 、 KMnO 4 K 2MnO 4 MnCl 2 MnO 2 C 、 KMnO 4 K 2MnO 4 MnO 2 MnCl 2 D 、 MnO 2 MnCl 2 Mn KMnO 4 1、已知有机化学中将只含有C 、H 元素的化合物称为烃。其中甲烷的分子式为CH 4,乙烷的分了式为C 2H 6,丙烷的分子式为C 3H 8,则丁烷的分子式为____。若用n 表示这类物质的一个分子中碳原子个数,则这类物质分子式的通式可表示为___。 3、用元素符号和相应的数字表示:①3个水分子 ;②2个硫原子 ; ③+2价的镁元素 ;④2个镁离子 ;⑤m 个硫酸根离子 。
种类介绍花卉品种大全 以下为部分花卉图片鲜花图片花卉图片大全 栀子花图 别名:栀子、黄栀子、山栀子、薝卜花、野桂花、白蟾花、雀舌花、玉瓯花、玉荷花 朱顶红图 别名:百枝莲、对红、对对红、柱顶红、朱顶兰、孤挺花、华胄兰、百子莲 紫罗兰 别名:草紫罗兰、草桂花、夏紫罗兰、秋紫罗兰、冬紫罗兰、香紫罗兰 紫薇 别名:百日红、痒痒树、满堂红 紫茉莉图 别名:草茉莉、胭脂花、夜娇娇、夜晚花、洗澡花、状元红、官粉花、潮来花
紫背万年青 别名:紫锦兰、蚌花 朱蕉 别名:红竹、红叶铁树、千年木 藏红花图 别名:西红花、番红花、泪夫兰 醉蝶花图 别名:紫龙须、蜘蛛花、凤蝶草、西洋白花菜 紫鸭跎草图 别名:紫锦草、紫竹梅
紫鹅绒 别名:天鹅绒三七、土三七、橙黄土三七、红凤菊 月季图 别名:长春花、月月红、四季花、斗雪红、瘦客 夜来香图 别名:夜香花、夜香树、夜丁香、晚香玉、夜兰香 秋海棠 别名:洋海棠、四季海棠、瓜子海棠、虎耳海棠 郁金香图 别名:洋荷花、草康香、旱荷花
叶子花图 别名:三角梅、贺春红、室中花、三角花、九重葛、三叶梅、南美紫茉莉、肋杜鹃 鸳鸯茉莉图 别名:二色茉莉 虞美人图 别名:李春花、丽春花、赛牡丹、小种罂粟花、苞米罂粟、蝴蝶满园春 一叶兰 别名:蜘蛛抱蛋、箬兰、苞米兰 迎春花图 别名:金腰带、小黄花
玉簪图 别名:玉春棒、白鹤花、白玉簪、玉泡花 一品红 别名:圣诞树、象牙红、老来娇、圣诞花、圣诞红、猩猩木 一串红图 别名:西洋红、象牙红、墙下红、爆仗红、拉尔维亚 樱花 别名:山樱花、山樱桃、福岛樱、青肤樱 榆叶梅图 别名:榆梅、小桃红、榆叶鸾枝
离子符号 原子团 原子团形成的离子 元素的化合价
1:单质的化学式 2:化合物的化学式
化学符号周围数字的含义大盘点 一、符号(化学式、元素符号、离子符号)前面的数字只表示粒子(分子、原子、离子)的个数。 ① 2H ──2个氢原子;【元素符号前面的数字只表示原子的个数】 注意:千万别理解为两个氢元素。元素是宏观概念,只讲种类,不讲个数。 ② 2H2O ──2个水分子;【化学式前面的数字只表示分子的个数】 ③ 2Mg2+──2个镁离子;【离子符号前面的数字只表示离子的个数】 ④ 2SO42-──2个硫酸根离子;【离子符号(原子团) 前面的数字只表示离子的个数】 二、符号右下角的数字只表示一个(或每个)粒子中某元素原子的个数或原子团的个数。 ① H2──1个氢分子由2个氢原子构成;【化学式中元素右下角的数字只表示一个分子中所含原子的个数】 ② 2H2O──每个水分子由2个氢原子和1个氧原子构成;前面的2只表示2个水分子 ③ SO4──1个硫酸根原子团中含有1个硫原子和4个氧原子; 注意:原子团只是化合物的组成部分,不能把原子团符号当成化学式。 三、元素符号右上角的数字只表示离子所带的电荷。 ① Mg2+──1个镁离子带2个单位的正电荷; ② SO42-──每个硫酸根离子带2个单位的负电荷;(不要理解为两个硫酸根离子带两个单位的负电荷) 四、元素符号正上方的数字只表示某物质中元素或原子团的化合价。 化学式的计算 1、化学式用元素符号和数字的组合表示物质组成的式子,叫做化学式。例如O2,H2,HCl等都是化学式。 2、相对原子质量由于原子实际数值太小,书写和使用都不方便,所以采用相对原子质量。以一种碳原子质量的1/12为标准,其他原子的质量跟他相比较所得到的比,作为这种原子的相对原子质量。 3、相对原子质量与质子数、中子数之间的关系:相对原子质量≈质子数+中子数 4、纯净物中各元素质量比=纯净物中各元素原子的相对原子质量总和之比 5、质量分数=纯净物中某元素的质量分数=该元素原子的相对原子质量总和/相对分质量×100% 6、原子个数比化学式中各元素原子个数比等于元素质量除以该元素的相对原子质量的商之比
花的种类大全 关于花2010-05-22 14:52:04 阅读5997 评论7 字号:大中小订阅 矮樱艾菊芭蕉白鲜白芨百合薄荷宝巾宝绿贝母碧桃滨菊巢蕨稠李雏菊春兰慈姑 刺槐刺桐葱兰翠菊大蓟大青大薸大戟地肤地锦帝冠吊兰蝶豆丁香冬青杜鹃杜梨 番薯繁缕肺衣粉藤扶桑桂花海棠海桐海芋含笑荷花合欢红花红蕉红桑红蓼花葵 花忍花烛黄蝉黄翁黄杨黄芩黄栌黄橘幌菊火棘鸡麻继木嘉兰荚蒾姜黄角蒿结香 金柑金琥锦葵景天菊花菊蒿卷耳决明款冬葵菊蜡花蜡菊腊梅兰花梨花莲翘铃兰 凌霄柳兰龙胆芦竹芦荟绿萝落葵络石马兰玫瑰梅花米兰魔芋牡丹母菊木瓜木棉 木香木槿泡桐菩提蒲桃莕菜蔷薇球兰瑞香瑞云砂仁沙参山茶山柰山楂商陆芍药 蛇莓射干肾蕨石榴石蒜石竹石楠石斛蜀葵水鳖水苏水仙水芋水蕹睡莲硕葱丝兰 松霞苏铁酸浆蒜松桃花田菁铁兰王莲卫矛文竹翁柱乌头希稗细辛霞草仙茅襄荷 小檗械葵星球杏花旋花雪松岩芋依兰银花银杏银叶樱草樱花迎春油桐雨菊玉兰 玉竹玉簪郁金郁李圆柏月桂月季云实泽兰泽泻知母珠兰朱蕉著草紫荆紫藤紫苑 紫珠紫菀紫薇棕竹赪桐芙蓉芸香茉莉茑萝茜草荭草菖蒲萱草蒿菊蒺瑰猬实溲疏 缬草珙桐杓兰栀子枸骨枸杞柽柳栾树桉树桫椤棣棠榕树昙花鸢尾 矮牵牛矮泽米矮棕竹艾琳季安星桃安祖花澳洲茄八仙花霸王鞭白布菊白鹤芋白鹃梅 白兰花白千层白软木白穗花白头翁白玉兰白云锦百合竹百里香百脉根百日草百子莲 斑鸠菊半边莲半支莲报春花贝壳花贝母兰闭鞘姜扁叶芋变叶木玻璃菊波斯菊博落回 卜若地补血草彩叶草菜豆树草海桐草珊瑚草菖蒲常春藤长春花长寿花巢凤梨晨雾草 串金鱼垂盆草春黄菊翠雀花翠云草大花葱大幌菊大火草大丽花大岩桐袋鼠花灯台树 滇丁香点地梅电灯花吊竹梅钓钟柳冬红花冬珊瑚豆瓣绿独丽花独蒜兰独尾花杜鹃花 断肠草堆心菊多榔菊蛾蝶花鹅掌柴俄耳甫番红花非洲菊非洲堇飞燕草费利菊风车草 风铃草风信子凤凰木凤仙花凤眼莲伏牛花福禄考富贵草富贵竹高代花高雪轮沟头花
元素符号和分子式 班级姓名学号 一、选择题: 1、下列微粒能决定元素种类的是() A.质子数B.中子数C.电子数D.原子量 2、在水(H2O)中含有() A.氢元素和氧元素B.氢分子和氧原子 C.氢原子和氧原子D.氢气和氧气 3、下列说法正确的是() A.由同种元素组成的物质叫单质 B.由不同种元素组成的纯净物叫化合物 C.由一种元素组成的物质叫纯净物 D.由不同种元素组成的物质叫混合物 4、下列各组物质中,前者是氧化物,后者是单质的是() A.镁粉硫磺粉B.水银氧化汞 C.二氧化硫氧气D.水蒸气冰 5、蒸馏水不宜养鱼,是因为蒸馏水中几乎不含() A.氧元素B.氧分子C.氢元素D.氧原子 6、关于氯酸钾、二氧化硫、五氧化二磷、氧化镁四种物质中,下列叙述正确的是()A.都是氧化物B.都含有氧分子 C.都是化合物D.都含有氧元素 7、下列物质中含氧分子的是() A.二氧化碳(CO2)B.二氧化锰(MnO2) C.氯酸钾(KClO3)D.液氧(O2) 8、在K2SO4、K2CO3、K2O的化学式中() A.都含有2个钾元素B.都含有2个钾原子 C.都含有1个钾分子D.钾元素的质量分数相同 9、下列铁的化合物中,铁元素的质量分数最大的是() A.FeO B.Fe2O3C.Fe3O4D.Fe2(SO4)3二、填空题: 10、用元素符号表示: 氧元素1个氧原子6个氧原子 铜元素10个铜原子m个铜原子 13、下列符号中“2”的意义: (1)SO2:(2)2O2: (3)2Mg:(4)2P2O5: 14、已知某元素R与氢元素的化合物的化学式为RH4,含氢为25%,已知该元素R的原子核中有6个中子,则这种元素的原子量是,原子核内的质子数是,元素符号是。 15、某种化合物的化学式为H n RO2n+1,式量为M,则R的原子量为,R在该化合物中的质量百分比为。 三、计算题: 16、计算硫酸钾(K2SO4)和碳酸钾(K2CO3)中钾元素的质量分数。87克碳酸钾与多少克硫酸钾的含有钾的质量相同? 17、有xy2和x2y两种化合物;x2y的式量为44,x元素的质量分数为63.6%,则化合物xy2的式量是多少?x元素在xy2中的质量分数为多少?
物质中某元素的质量分数及其计算 定义: 物质中某元素的质量分数,就是该元素的质量与组成该物质的各元素的___________之比。 公式: 某元素的质量分数 = 一、根据化合物的化学式求某元素的质量分数 1. 计算硝酸铵(NH4NO3)中氮元素的质量分数。 2. 水果中含有柠檬酸,可促进消化,柠檬酸的化学式为C6H8O7。计算檬酸的相对分子质量___________;檬酸中碳原子的质量分数为___________。 二、根据化合物中某元素的质量分数求相对分子质量 3. “骨质疏松症”是人体缺钙引起的,可服用补钙剂来治疗。乳酸钙是一种常见的补钙剂,测知乳酸钙分子中含有一个钙原子,钙元素的质量分数为18.34%,则乳酸钙的相对分子质量为______________。 三、根据化合物中某元素的质量分数求化学式 4. 已知锰元素的一种氧化物中氧元素的质量分数为50.5%,此氧化物的化学式为()。 A.MnO B.Mn O 23 C.MnO 2 D.Mn O 27
5. 已知NH4NO3和KH2PO4固体混合物中氮元素的质量分数为28%,则混合物中KH2PO4的质量分数为多少? 五、其它计算 6. 已知 4.6g某物质在纯氧中完全燃烧生成8.8g二氧化碳和5.4g水,经计算,该物质是由____________元素组成?知该物质相对分子质量为46,则该物质的化学式为____________。
例3:由Na S Na SO Na SO 22324 、、三种物质组成的混合物中,测得硫元素的质量分数为32%,则氧元素的质量分数为____________。 分析:观察三种物质的化学式的特征可知,所含Na与S的原子个数比均为2:1,由此可知,两种元素有固定的质量比,其质量比等于相对原子质量之和的 比,还等于质量分数比,因此有232 3232% ? = Na的质量分数 ,解得钠元素的质量分 数为46%,氧元素的质量分数为:132%46%22% --=。 故答案为22%。 物质中某元素的质量分数 定义: 物质中某元素的质量分数,就是该元素的质量与组成物质的各元素总质量之比。公式: 某元素的质量分数 = ×100%。 一、根据化合物的化学式求某元素的质量分数 1.计算硝酸铵(NH4NO3)中氮元素的质量分数。 分析:利用定义法进行计算 解:先根据化学式计算出 NH4NO3的相对分子质量=14+1x4+14+16x3=80 再计算氮元素的质量分数: N的相对原子质量=xN的原子数/NH4NO3的相对分子质量x100%=14x2/80x100% =35% 2.水果中含有柠檬酸,可促进消化,柠檬酸的化学式为C6H8O7。计算檬酸的相对分子质量___________;檬酸中碳原子的质量分数为___________。 3.“骨质疏松症”是人体缺钙引起的,可服用补钙剂来治疗。乳酸钙是一种常见
常见的元素符号: 氢氦锂铍硼,碳氮氧氟氖,钠镁铝硅磷,H He Li Be B C N O F He Na Mg Al Si P 硫氯氩钾钙, 锰铁铜锌银,钡铂金汞碘S Cl Ar K Ca Mn Fe Cu Zn Ag Ba Pt Au Hg I 常见元素的化合价: 钾钠银氢+1价, 氟氯溴碘-1价, 钙镁钡锌汞+2价, 正一亚铜,正二铜,正二亚铁,正三铁,+3铝来+4硅, 单质零价永不变,氧硫负二要记住。 碳酸根、硫酸根负二价,硝酸根、氢氧根负一价,只有铵根正一价。 单质的化学式: 化合物的化学式: 氧化物:一氧化碳CO , 二氧化碳CO2, 五氧化二磷P2O5 二氧化硫SO2, 二氧化锰MnO2 , 三氧化二铁Fe2O3 , 氧化亚铁FeO ,四氧化三铁Fe3O4 , 氧化镁MgO , 氧化钙CaO , 三氧化二铝Al2O3氧化汞HgO , 氧化铜CuO 酸:盐酸HCl 硫酸H2SO4硝酸HNO3碳酸H2CO3 磷酸H3PO4 碱:氢氧化钠NaOH , 氢氧化钙Ca(OH)2, 氢氧化钡Ba(OH)2氢氧化钾KOH , 氢氧化铁(红褐色)Fe(OH)3 氢氧化铜(蓝色)Cu(OH)2, 氢氧化镁(白色)Mg(OH)2盐:盐酸盐:氯化钠NaCl , 氯化镁MgCl2, 氯化铝AlCl3氯化钾KCl , 氯化铁FeCl3, 氯化亚铁FeCl2, 氯化锌ZnCl2 氯化钡BaCl2, 氯化铜CuCl2, 氯化银AgCl
碳酸盐:碳酸钙CaCO3, 碳酸钠Na2CO3, 碳酸钾K2CO3碳酸钡BaCO3 硫酸盐: 硫酸亚铁FeSO4, 硫酸铁Fe2(SO4)3, 硫酸钠Na2SO4 硫酸镁MgSO4, 硫酸铝Al2(SO4)3, 硫酸铜CuSO4 硫酸锌ZnSO4, 硫酸钡BaSO4 硝酸盐:硝酸银AgNO3硝酸汞Hg(NO3)2硝酸锌Zn(NO3)2 硝酸钡Ba(NO3)2硝酸铝Al(NO3)3硝酸铁Fe(NO3)3 硝酸铜Cu(NO3)2硝酸钙Ca(NO3)2 常见的离子: 钾离子K+,钠离子Na+,银离子Ag+,氢离子H+ , 氟离子F-,氯离子Cl-,钙离子Ca2+,镁离子Mg2+,钡离子Ba2+ , 锌离子Zn2+,汞离子Hg2+,铜离子Cu2+,亚铁离子Fe2+ , 铁离子Fe3+,铝离子Al3+,氧离子O2-, 硫离子S2-, 碳酸跟离子CO32-, 硫酸根离子SO42- , 硝酸根离子NO3- 氢氧根离子OH- , 铵根离子NH4+, 磷酸根离子PO43- 化学方程式 一、化合反应 1、镁在空气中燃烧:2Mg+ O2点燃2MgO 2、铁在氧气中燃烧:3Fe +2O2点燃Fe3O4 3、铝在空气中燃烧:4Al+ 3O2点燃2Al2O3 4、铜在空气中受热:2Cu+ O2加热2CuO 5、氢气在空气中燃烧:2H2 +O2点燃2H2O 6、红磷在空气中燃烧:4P +5O2点燃2P2O5 7、硫粉在空气中燃烧:S+ O2点燃SO2 8、碳在氧气中充分燃烧:C +O点燃CO2 二、分解反应 1、实验室用双氧水制氧气:2H2O2 MnO2 2H2O +O2↑ 2、加热高锰酸钾:2KMnO加热K2MnO4 + MnO2+O2↑
1.用化学符号表示: ⑴钠元素______ ⑵三个磷原子 _______ ⑶氩气⑷氮气⑸两个氧分子 ⑹2个钙离子 ________ ⑺-2价的硫元素 ____________ 2.(5分写出下列化学用语: 一个氢分子两个氧原子3个铁离子碳酸根二氧化锰中锰元素的化合价为+4价 3.用化学符号表示:⑴钠元素______ (6)2个钙离子 _____________ ⑺-2价的硫元素______________ 4..用符号表示: ⑴空气中体积分数最大的气体_______ ;⑵2个水分子____________ ;35个五氧化二磷分子______________ ⑷3个钠离子______________ 。; 锌元素_、氯离子_。①两个氩原子___________;②三个氮分子__________ 5.用数字和化学符号表示: 两个氮原子_____________ ; 三个铁原子________________ ;四个水分子______________ ; 6.用化学符号表示: (1)X个二氧化碳分子_; (2) 2个镁离子 (3)空气中含量最多的物质的化学式_;( 4) 2个硫酸根离子_; (5)人类生命活动离不开的气态单质是______________ ; ( 6)液态氧化物是 _____________ ; (7)绿色植物发生光合作用所需的气体是_ (写化学式)。 -2 2H2O 7 . ( 3分)写出下列符号中“ 2 ”的含义: ;;。 8.下列符号中“ 2”所表示的意义: ①2CC2、; +2 CaO ②2C1 ;③; ④2CC32-、。 ⑤ 2H2_;
,属于原子的是 _____ 。 ⑵电子层数相同,最外层电子数也相同的粒子有 _________ 。 10. 某元素在人体内能调节体液平衡等,缺乏该元素会造成心律不齐,过量时会使人恶心腹泻 该元素的原子结构示意图为 ,则X= _________ ,该原子有 __________个电子层,最外层 有 个电子,容易 (得或失)电子,此元素应属于 _______ (填“金属”、“非金属”)元素。 11. (8分)元素周期表和原子结构示意图是学习和研究化学的重要工具。请根据下图示意图回答问题。 _______ A B C (1) 根据 A 图可查岀该元素的相对原子质量为 ,根据 B 图可判断该元素原子的质子数 为 ,根据C 图可判断该元素原子的最外层电子数为 ; (2) 上述三个图表示的三种元素最本质的区别是 ___________ ________ __ ; (3) 写出符合下列要求的化学用语: 相对分子质量最小的物质 地壳中含量最多的金属元素 污染空气的有害气体 空气中含量最多的 气体 12、 _______________________________________________________________________________________ (1能直接构成纯净物的是 (2能保持物质化学性质的是 。(3化学变化中的最小粒子是 (4带正电荷的粒子 是。(5带负电荷的粒子是。不带电的粒子是(7质量与氢原子质量近似相等的粒子是 。(8决定原子质量 大小的粒子是 。(9在同一原子中数目相等的粒子是 。 13、水是由 组成的;水是由 构成的;水分子是由 构成的; 一个水分子是由构成的 9.下面是部分元 素原子或离子的结构示意图。请你仔细观察、 ⑴上述粒子中,属于同一种元素的是 的是 _______ (填序号,下同),属于阳离子的是 ________ ,属于阴离子 2: S 分析,再回答问题: 2 S- H
第四节物质组成的表示方法 作者:吴正兴文章来源:本站原创点击数:284 更新时间:2009-10-23 第四节物质组成的表示方法 第2课时元素的质量分数、化学式计算 班级学号姓名成绩 第Ⅰ卷(选择题) 一、选择题(每小题只有一个 ....选项符合题意。) 1.(2008年苏州市)有关尿素[CO(NH 2) 2 ]的说法正确的是 ( ) A.尿素的相对分子质量为:12+16+14+1×2×2=46 B.尿素是一种有机氮肥 C.尿素中碳、氧、氮、氢四种元素的质量比为:12:16:14:1 D.尿素中氮元素质量分数的计算式为:×l00%2.某气体单质和氧气的相对分子质量比为7:8,则该气体可能是 ( ) A.CO B.CO 2 C.N 2 D.Cl 2 3.世界卫生组织(WHO)将某氧化物RO 2 列为A组高效安全灭菌消毒剂,它在食 品保鲜、饮用水消毒等方面有着广泛应用。实验测得该氧化物中R与O的质量 比为71:64,R 2 O的化学式为 () A.CO 2B.ClO 2 C.SO 2 D.NO 2 4.氮元素的一种氧化物中氮元素与氧元素质量之比为7:12,则该氧化物的化学式为 () A.NO B.N 2O 3 C.NO 2 D.N 2 O 5 5.下列几种化合物,含铁元素的质量分数最高的是( ) A.Fe 3O 4 B.Fe 2 O 3 C.FeO D.FeS 6.(07北京市)在一氧化碳中,碳元素与氧元素的质量比是 ( ) A.1∶1 B.1∶2 C.3∶4 D.3∶8 7.3.2g某种铁的氧化物含有2.24g铁元素,则这种铁的氧化物的化学式为( )
A.FeO B.Fe 2O 3 C.Fe 3 O 4 D.Fe 3 O 2 8.当硝酸铵(NH 4NO 3 )和尿素[CO(NH 2 ) 2 ]中所含氮元素的质量相同时,它们的质量 比 为 ( ) A.1︰1 B.2︰3 C.4︰3 D.8︰3 9.农村经常使用氮肥硝酸铵,化学式NH 4NO 3 ,经过测定含氮量为37%,已知该 化肥中只含有一种杂质,则该化肥中可能混有下列物质中的哪种氮肥( ) A.氯化铵(NH 4Cl) B.硫酸铵[(NH 4 ) 2 SO 4 ] C.尿素[CO(NH 2) 2 ] D.碳铵(NH 4 HCO 3 ) 10.已知某种NH 4NO 3 样品中混有不含氮元素的杂质,测得该NH 4 NO 3 样品中含氮的 质量分数为24.5%,则样品中NH 4NO 3 的质量分数为 ( ) A.24.5% B.49% C.70% D.80% 11.(07北京市)水中氢元素的质量分数为 A.5.6% B.9.9% C.11.1% D.12.1% 12.化学式为H 2R 2 O 3 的物质,其相对分子质量为114,则R的相对原子质量为 ( ) A.32g B.64g C.32 D.64 13.山茶油是一种绿色保健品,其主要成分是柠檬醛。现从山茶油中提取76g 柠檬醛,将其在氧气中完全燃烧,生成二氧化碳220g,水72g,则柠檬醛的组成中(相对原子质量:H-1 C-12 O-16) ( ) A.只含有碳、氢元素 B.一定含有碳、氢、氧元素 C.一定含有碳、氢元素,可能含有氧元素 D.一定含有碳、氧元素,可能含有氢元素
初中化学常考元素符号+化学式 元素符号前20号元素: 氢H 、氦He、锂Li、铍Be、硼B、碳C、氮N、氧O、氟F、氖Ne、钠Na、镁Mg、铝Al、硅Si、磷P、硫S、氯Cl、氩Ar、钾K、钙Ca、锌Zn、铁Fe、铜 Cu、汞Hg、银Ag。 化学式 单质:氢气H 2、氮气N 2 、氧气O 2 、氯气Cl 2 、氦He、碳C 、钠Na、镁Mg、 铝Al、硅Si、磷P、硫S、氩Ar、钾K、钙Ca、锌Zn、铁Fe、铜Cu、汞Hg、银Ag。 非金属氧化物: 水H 2O、二氧化碳CO 2 、一氧化碳CO、五氧化二磷P 2 O 5 、二氧化硫SO 2 、 三氧化硫SO 3、过氧化氢(双氧水)H 2 O 2 、二氧化氮NO 2 。 金属氧化物: 氧化铁Fe 2O 3 (赤铁矿,铁锈的主要成分)、 四氧化三铁Fe 3O 4 (磁铁矿的主要成分)、 氧化铝Al 2O 3 (铝土矿的主要成分)、 氧化铜CuO、氧化钙CaO、二氧化锰MnO 2 、氧化镁MgO。 酸:盐酸HCl(胃酸的主要成分)、硫酸H 2SO 4 、硝酸HNO 3 、 碳酸H 2CO 3 、乙酸CH 3 COOH(俗称醋酸)。 碱: 氢氧化钠NaOH(俗称火碱、烧碱、苛性钠,易溶于水)、氢氧化钡Ba(OH) 2 (易溶于水)、
氢氧化钙 Ca(OH)2(俗称熟石灰、消石灰。微溶于水,水溶液俗称澄清石灰水)、 氢氧化镁Mg(OH)2(不溶于水,白色沉淀)、 氢氧化铁 Fe(OH)3(不溶于水,红褐色沉淀)、 氢氧化铜 Cu(OH)2(不溶于水,蓝色沉淀)、一水合氨NH 3?H 2O (水溶液俗称氨水)。 盐: 氯化钠NaCl (食盐的主要成分,易溶于水)、 氯化钾KCl (易溶于水)、氯化钡BaCl 2(易溶于水)、 氯化钙CaCl 2(易溶于水)、 氯化亚铁FeCl 2(易溶于水,形成浅绿色溶液)、 氯化铁FeCl 3(易溶于水,形成黄色溶液)、 氯化银AgCl (不溶于水,不溶于酸,白色沉淀)、 硫酸钠Na 2SO 4(易溶于水)、硫酸钙CaSO 4(微溶于水)、 硫酸钡BaSO 4(不溶于水,白色沉淀)、硫酸锌ZnSO 4(易溶于水)、 硫酸亚铁FeSO 4(易溶于水,形成浅绿色溶液)、 硫酸铁Fe 2(SO 4)3(易溶于水,形成黄色溶液)、 硫酸铜CuSO 4(易溶于水,形成蓝色溶液)、 碳酸钠Na 2CO 3(俗称纯碱、苏打,易溶于水)、 碳酸钙CaCO 3(大理石、石灰石的主要成分,不溶于水,白色固体)、碳酸钡BaCO 3(不溶于水,白色沉淀)、 硝酸钠NaNO 3(易溶于水)、硝酸钾KNO 3(易溶于水)、 硝酸铵NH 4NO 3(易溶于水)、硝酸钡Ba(NO 3)2(易溶于水)、 硝酸银AgNO 3(易溶于水)、碳酸氢钠NaHCO 3(俗称小苏打,易溶于水)、高锰酸钾 KMnO 4(暗紫色晶体)、锰酸钾 K 2MnO 4、 氯酸钾 KClO 3(白色粉末状固体)、 亚硝酸钠NaNO 2(工业用盐,有毒,易溶于水)。 有机物:甲烷CH 4、醋酸CH 3COOH 、乙醇C 2H 5OH 、葡萄糖 C 6H 12O 6。
初中化学常见符号和化学式 一、写出与元素名称相对应的元素符号(或原子团)以及常见化合价。钾钠银氢 氟氯溴碘 氧铝硫、、 铜、汞硅 镁钡锌钙 碳、铁、 氢氧根铵根硝酸根 氯酸根碳酸根硫酸根 磷酸根 二、用化学符号表示以下离子。 镁离子铜离子银离子铝离子 铁离子亚铁离子氧离子氯离子 钙离子钠离子钾离子钡离子 锌离子氢氧根离子铵根离子 氯酸根离子碳酸根离子硫酸根离子 磷酸根离子硝酸根离子 三、常见物质的化学式 (非金属单质) 氢气氮气氧气氯气 氟气溴碘 氦气氖气氩气 磷硫碳 (金属单质) 钠镁铝钾 钙铁锌铜 钡钨汞金 (氧化物) 水一氧化碳二氧化碳五氧化二磷 氧化钠二氧化硅二氧化氮二氧化硫 三氧化硫一氧化氮氧化镁 氧化铜氧化钡氧化亚铜 氧化亚铁三氧化二铁、氧化铁(铁红) 四氧化三铁氧化铝二氧化锰
(氯化物盐酸盐) 氯化钾氯化镁氯化钠(食盐) 氯化钙氯化铜氯化锌氯化银 氯化钡氯化铝氯化亚铁氯化铁 (常见的酸) 盐酸硫酸硝酸 碳酸磷酸亚硫酸 硫化氢乙酸(醋酸)溴化氢 (常见的盐) 硫酸铜硫酸钡硫酸钙 硫酸钾硫酸镁硫酸亚铁硫酸铁 硫酸铝硫酸氢钠硫酸氢钾亚硫酸钠 硝酸钠硝酸钾硝酸银硝酸镁 硝酸铜硝酸钙亚硝酸钠 碳酸钠碳酸氢钠碳酸镁 碳酸钙碳酸钾氯酸钾 高锰酸钾锰酸钾 (常见的碱)氢氧化钠氢氧化钙氢氧化钡 氢氧化镁氢氧化铜氢氧化钾 氢氧化铝氢氧化铁氢氧化亚铁 三、常见物质的化学式 (常见有机物)甲烷甲醇乙醇乙酸 (常见结晶水合物)碱式碳酸铜 (常见化肥)尿素CO(NH2)2硝酸铵NH4NO3硫酸铵(NH4)2SO4碳酸氢铵NH4HCO3磷酸二氢钾KH2PO4 红褐色絮状沉淀——Fe(OH)3 蓝色絮状沉淀——Cu(OH)2 白色沉淀——Mg(OH)2 AgCl, BaSO4(其中BaSO4、AgCl是不溶于HNO3的白色沉淀) CaCO3、BaSO3是溶于HNO3的白色沉淀 微溶于水——Ca(OH)2, CaSO4
必记一 物质构成的奥秘 一、中考必记元素 1.前20 号元素 : :钠镁铝 硅 磷 硫 氯氩钾 钙 Na Mg Al Si C1 Kr 2.其他常见元素 元素名称锰铁 钢 锌淡银 领金汞 元素符号Mn Fe CuZnEAgBa Au Hg 二、元素周期表 1.元素周期表中的规律 (1)同一横行(第一周期除外)的元素原子最外层电子数: 自左向 右由1依次递增至8。 (2)元素种类:从左到右依次为金属元素、非金属元素和稀有气体 元素。 (3 )同一横行的元素的原子电子层数相同,最外层电子数依次增多。 (4) 同一纵行的元素的原子最外层电子数相同,化学性质相似,电 子层数从上到下依次增多。 2.由元素周期表中的一格获得的信息 元素符号0 原子序数一8 千国家家 1 元素名称一氧 相对原子质量(单位为“1”,常省略不写)16,00 (1)数量关系 Q 原子序数=核电荷数= 核内质子数= 核外电子数:再 2相对原子质量一质子数+ 中子数。 根据化学式计算化合价的计算步骤(以P2O5 为例): 国写出化学式
P:O, 标出化合物中已知元素的化合价 P.O 设设出未知元素的化合价为x 根据化合物中各元素正负化合价 代数和为零,列等式2x+5x( -2)=0. 求求出未知元素化合价,解得x =+5 四、中考常考离子和原子团 1.常考离子 氢离子一H 氯离子一CI 镁离子一Mg 亚铁离子一Fe2+ 钙离子一Ca2+ (浅绿色) 铜离子一Cu2+ (蓝色) 钠离子一Na+ 钡离子一Ba2+ 钾离子一K+ 铁离子一Fe3+(黄色)锌离子一Zn2+ 铝离子一Al3+ 银离子一Ag+ 2.常考带电原子团 氢氧根一OH 碳酸根一CO3 硫酸根一SO4 碳酸氢根一HCO3 硝酸根一NO3 铵根一NH4 高锰酸根一MnO4 (紫红色) (注意]表示几个某离子(或带电原子团)时只需在离子符号前加。 应的数字即可。如三个钾离子表示为3K*,三个碳酸根离子表示为3C0 五、化学式的书写和读法 1.单质 (1)用元素符号和数字表示,如: 氯气一Cl2 氮气一N 2 氧气一O2 氢气一H 2 (2)直接由元素符号表示,如: @金属单质 铁一Fe 铝一Al 镁一Mg 钠一-Na 钾一K 钙一Ca 锌一Zn 铜一CU 锰一M n 钡一Ba 银一Ag 固态非金属单质 硅一Si 磷一P 硫3稀有气体:氖气Ne 氦气He 2.化合物 ()常见的氧化物( 均含氧元素,氧元素在右) 0读法与化学式不一致,如: 水一H2O 氧化铁( 三氧化二铁)一Fe2O3 过氧化氢一H2O2
初中化学元素以及化学式相对分子质量的计算 【同步教育信息】 一. 本周教学内容: (一)元素元素符号 1. 了解元素概念 2. 元素、原子、单质之间的区别和联系 3. 运用元素概念区分单质和化合物 4. 了解元素符号的意义,学会元素符号的正确书写 5. 熟记常见的元素符号 (二)化学式相对分子质量 1. 理解化学式和相对分子质量概念 2. 掌握化学式的书写和读法 3. 理解化学式前和化学式中有关数字的意义 4. 掌握根据化学式的有关计算 二. 重点、难点: 1. 元素、单质、化合物、氧化物的概念 2. 物质的简单分类 3. 元素符号的涵义和书写方法 4. 化学式的写法和读法 4. 有关化学式的计算 三. 教学过程 (一)元素元素符号 1. 元素的概念 世界是由物质组成的。人类已知物质有一千多万种,而这么多物质是由一百多种元素组成。元素的概念是:元素是具有相同核电荷数(即质子数)的同一类原子的总称。元素只有一百多种,物质有一千多万种,说明一种元素能形成许多种物质,或者说许多种物质里可以含有同一种元素。例如水、二氧化碳、氧化汞、氧气里都含有氧元素。比如,英文字母有26个,而英文单词有成千上万个。元素是宏观概念,是同一类原子的总称,只讲种类,不讲个数。决定元素种类的是质子数。原子是具体的微观粒子,既讲种类,又讲个数。如同人类和人。我们不能说几个人类,但可以说几个人。我们可以说鸟类、人类等等,不能说几个鸟类,我们可以说几只鸟或几个人。元素用于描述物质宏观组成,原子用于描述物质的微观组成。如二氧化碳是由碳元素和氧元素组成,一个二氧化碳分子是由一个碳原子和二个氧原子构成。氧气是由氧元素组成,一个氧分子由两个氧原子构成。 元素与原子的比较
家居饰品的种类繁多,而最雅致、最有生活气息的,要属绿叶鲜花了。为方便消费者选配花卉,记者采访了设计师杨桦,杨桦就目前花卉市场的特点,推荐了9种适合家居摆放的花卉,涵盖了适合不同消费人群的高、中、低档,并不失时尚。 大花惠兰 大花惠兰品种多样,黄的、粉的、红的等花色繁多。棵型较大,株高在1.3米左右,适宜摆放在面积较大的空间。通常放在花架上,显得大方,温馨。大花惠兰抗寒性能好,易养护,正常浇水即可。花期较长,一般在二、三个月,但花败后,一般不易再养出花来。大花惠兰属中高档花卉,价格与花剑的数量有关系,花剑越多,则价格越高,一般每加一个花剑,价格要增加30元左右,而如果几株组合在一起,价格会更高。 彩色马蹄莲 彩色马蹄莲是现在石家庄花卉市场上的花卉新品,但数量较少,新颖、高档,是送礼的佳品。一般的马蹄莲以白色居多,彩色马蹄莲是因为嫁接了其他花卉的基因,从而培育出了各种颜色。棵型较小,株高在40厘米左右,适合放在桌子、茶几、角柜上,作为家具的点缀。花期在一个月左右,一般三、四天浇一次水,并要一次浇透,叶片上可以喷水,平时可以用水或啤酒擦拭叶片,亮亮的叶片更能衬托出彩色马蹄莲花瓣的高贵。花瓣的颜色一般有渐变的效果,叶型美观且多种多样,并带着一些小斑点,花败后可以观叶。 百合 百合是今年的流行,相比去年却不太流行。百合的花冠较大,香味浓郁,如果在房间的一角放上一盆,整个室内都能闻到它的香味。百合格调高雅,但不能因为百合好看而摆放过多,否则效果会适得其反,一般可以选择5株一盆的组合,放在门、窗附近等上风口,以利于香味的扩散,但百合怕风,不能被风吹到。百合的花期较短,在15度左右的室内温度下,大概在半个月左右,花败后,叶子的观赏价值不大,一般的家庭也不易再养出花来。室内温度严重影响百合的花期,养百合主要是控制好室内温度,如果室内温度过高,从花苞到开花,可能只用一个晚上。百合花在似开非开、手指能伸进去时,应该把花蕊轻轻摘下,以防止花
初中化学需要记住的元素符号和化学式 化学是一门比较特殊的科学,而元素符号和化学式是我 们打开化学这扇神秘大门的钥匙!掌握元素符号和化学式的 知识是我们学好化学的基础。现将这部分知识总结如下,希 望对大家有所帮助! 元素符号 前20号元素: 氢H 、氦He、锂Li、铍Be、硼B、碳C、氮N、氧O、氟F、氖Ne、钠Na、镁 Mg、铝Al、硅Si、磷P、硫S、氯Cl、氩Ar、钾K、钙Ca、锌 Zn、铁Fe、铜 Cu、汞Hg、银Ag。 化学式 单质: 氢气H2、氮气N2、氧气O2、氯气Cl2、氦He、碳C 、钠Na、镁Mg、铝Al、硅Si、磷P、硫S、氩Ar、钾K、钙Ca、锌Zn、铁Fe、铜Cu、汞Hg、银Ag。 非金属氧化物: 水H2O、二氧化碳CO2、一氧化碳CO、五氧化二磷P2O5、二氧化硫SO2、三氧化硫SO3、过氧化氢(双氧水)H2O2、二氧化氮NO2。 金属氧化物:
氧化铁Fe2O3(赤铁矿,铁锈的主要成分)、 四氧化三铁 Fe3O4(磁铁矿的主要成分)、 氧化铝 Al2O3(铝土矿的主要成分)、 氧化铜CuO、氧化钙CaO、二氧化锰MnO2、氧化镁MgO。 酸: 盐酸HCl(胃酸的主要成分)、硫酸H2SO4、 硝酸HNO3、碳酸H2CO3、乙酸CH3COOH(俗称醋酸)。 碱: 氢氧化钠NaOH(俗称火碱、烧碱、苛性钠,易溶于水)、氢氧化钡Ba(OH)2(易溶于水)、 氢氧化钙 Ca(OH)2(俗称熟石灰、消石灰。微溶于水, 水溶液俗称澄清石灰水)、 氢氧化镁Mg(OH)2(不溶于水,白色沉淀)、 氢氧化铁 Fe(OH)3(不溶于水,红褐色沉淀)、 氢氧化铜 Cu(OH)2(不溶于水,蓝色沉淀)、 一水合氨NH3?H2O(水溶液俗称氨水)。 盐: 氯化钠NaCl(食盐的主要成分,易溶于水)、 氯化钾KCl(易溶于水)、 氯化钡BaCl2(易溶于水)、 氯化钙CaCl2(易溶于水)、 氯化亚铁FeCl2(易溶于水,形成浅绿色溶液)、