一些常用氢氧化物沉淀形成和再溶解所需的pH值
- 格式:doc
- 大小:27.50 KB
- 文档页数:1
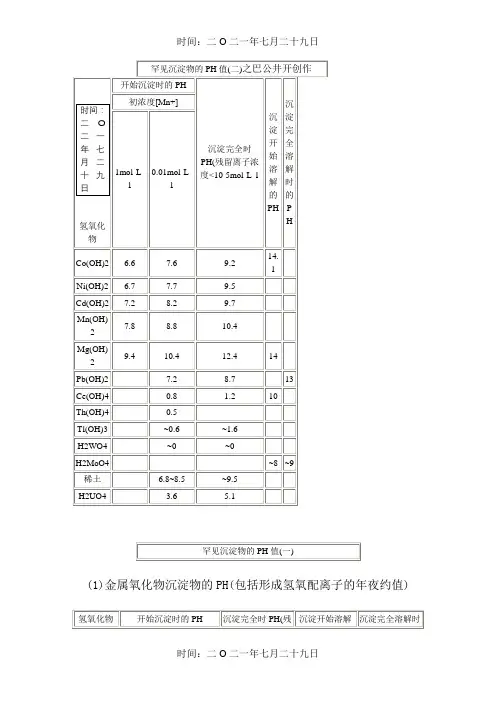
(1)金属氧化物沉淀物的PH(包括形成氢氧配离子的年夜约值)初浓度[Mn+]留离子浓度<10-5mol·L-1的PH的PH1mol·L-10.01mol·L-1Sn(OH)400.511315TiO(OH)200.5 2.0--Sn(OH)20.9 2.1 4.71013.5ZrO(OH)2 1.3 2.3 3.8--HgO 1.3 2.4 5.011.5-Fe(OH)3 1.5 2.3 4.114Al(OH)3 3.3 4.0 5.27.810.8Cr(OH)3 4.0 4.9 6.81215Be(OH)2 5.2 6.28.8--Zn(OH)2 5.4 6.48.010.512~ 13 Ag2O 6.28.211.212.7-Fe(OH)2 6.57.59.713.5-废水中重金属离子在碱性条件下可形成氢氧化物沉淀,然后通过固液分离装置除失落沉渣.但各金属氢氧化物沉淀析出的最佳pH值有所分歧.根据文献报道[1],镍氢氧化物沉淀析出的理论pH值范围分别为8.49~9.49、、铅氢氧化物沉淀析出的理论pH值范围分别为7.88~8.88<18.3>重金屬廢水處理重金屬廢水處理最經濟而簡單的處理方法為化學沉澱,就是加入石灰提高廢水之PH,使重金屬離子變成氫氧化物沉澱去除重金屬離子之沉澱作用與PH的關係如下表所示:重金屬離子適合沉澱之PH 最佳沉澱之PHFe^3+,Sn^2+,Al^2+ 4 7Cu^2+,Zn^2+,Cr^3+,Be^2+ 6 9Fe^2+ 7 10Cd^2+,Ni^2+,Co^2+,Cu^2+(濃) 8 11Ag^+,Mn^2+,Hg^+ 9 12。
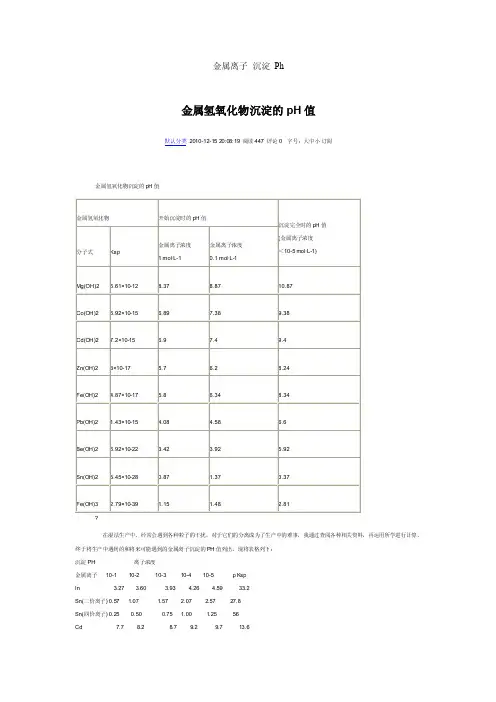
金属离子沉淀Ph金属氢氧化物沉淀的pH值默认分类2010-12-15 20:08:19 阅读447 评论0 字号:大中小订阅金属氢氧化物沉淀的pH值在湿法生产中,经常会遇到各种粒子的干扰,对于它们的分离成为了生产中的难事,我通过查阅各种相关资料,再运用所学进行计算,终于将生产中遇到的和将来可能遇到的金属离子沉淀的PH值列出,现将表格列下:沉淀PH 离子浓度金属离子10-1 10-2 10-3 10-4 10-5 p KspIn 3.27 3.60 3.93 4.26 4.59 33.2Sn(二价离子) 0.57 1.07 1.57 2.07 2.57 27.8Sn(四价离子) 0.25 0.50 0.75 1.00 1.25 56Cd 7.7 8.2 8.7 9.2 9.7 13.6Pb(二价离子) 7.04 7.54 8.04 8.54 9.04 14.9Pb(四价离子) --- --- --- --- - 1.13 65.53Tl -0.27 0.06 0.39 0.72 1.05 43.8Fe(二价离子) 7.0 7.5 8.0 8.5 9.0 15.1Fe(三价离子) 1.9 2.2 2.5 2.9 3.2 37.4Co(二价离子) 7.15 7.65 8.15 8.65 9.15 14.7Co(三价离子) -0.23 0.1 0.43 0.76 1.09 43.7Al 3.4 3.7 4.0 4.4 4.7 32.88Cr 4.3 4.6 4.9 5.3 5.6 30.2Cu 4.7 5.2 5.7 6.2 6.7 19.6Ni 7.2 7.7 8.2 8.7 9.2 14.7Mn 8.1 8.6 9.1 9.6 10.1 12.73Mg 9.1 9.6 10.1 10.6 11.1 10.74Zn 6.04 6.54 7.04 7.54 8.04 16.92Sb 0.53 0.86 1.19 1.52 1.85 41.4Ti 1.00 1.33 1.66 2.00 2.33 40Bi 4.20 4.53 4.86 5.19 5.52 30.4“--”代表数值很大,生产工艺中不可能存在,未用括号标出价态的离子是正常价态。
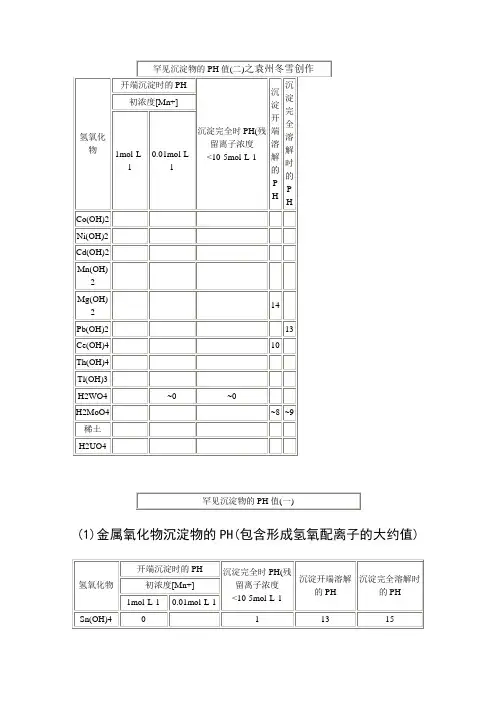
(1)金属氧化物沉淀物的PH(包含形成氢氧配离子的大约值)
TiO(OH)20--
Sn(OH)210
ZrO(OH)2--
HgO-
Fe(OH)314
Al(OH)3
Cr(OH)31215
Be(OH)2--
Zn(OH)212~ 13
Ag2O-
Fe(OH)2-
废水中重金属离子在碱性条件下可形成氢氧化物沉淀,然后
通过固液分离装置除掉沉渣.但各金属氢氧化物沉淀析出的
最佳pH值有所分歧.根据文献报导[1],镍氢氧化物沉淀析
出的实际pH值范围分别为8.49~9.49、、
<18.3>重金屬廢水處理
重金屬廢水處理最經濟而簡單的處理方法為化學沉澱,就是
加入石灰提高廢水之PH,使重金屬離子變成氫氧化物沉
澱去除重金屬離子之沉澱作用與PH的關係如下表所示:
重金屬離子適合沉澱之PH
最佳沉澱之PH
Fe^3+,Sn^2+,Al^2+ 4 7
Cu^2+,Zn^2+,Cr^3+,Be^2+ 6 9
Fe^2+ 7 10
Cd^2+,Ni^2+,Co^2+,Cu^2+(濃) 8 11
Ag^+,Mn^2+,Hg^+ 9 12。

金属氢氧化物沉淀的ph值1. 引言嘿,朋友们!今天咱们要聊聊一个听起来有点高大上的话题——金属氢氧化物沉淀的pH值。
别害怕,这可不是化学课上的枯燥内容,而是个很有趣的话题,跟咱们日常生活其实有很多关联哦。
你可能会想,金属氢氧化物?那是什么鬼?其实,简单来说,这就是一些金属元素和氢氧根结合后形成的沉淀物,通常在咱们的实验室里或者水处理过程中会碰到。
1.1. 金属氢氧化物的定义好吧,让我们先捋一捋什么是金属氢氧化物。
想象一下,你在厨房做饭,锅里一堆水在沸腾。
然后,你往里加点氢氧化钠(就是我们常说的小苏打),瞬间,那水就变得浑浊了。
这个浑浊就是氢氧化物的沉淀哦,水中金属离子与氢氧根结合形成了小颗粒,悬浮在水里,样子还蛮好玩的。
不同的金属离子,比如铝、铁、锌,它们跟氢氧根的反应可各有各的特点,真是个五光十色的化学世界。
1.2. pH值的基本概念那么,pH值又是什么呢?说白了,就是测量溶液酸碱性的一个指标。
pH值范围从0到14,7是中性,低于7是酸性,高于7则是碱性。
想象一下,pH值就像是一个气温计,告诉你水的“脾气”。
如果你往水里加点酸,比如醋,那pH值就会降到6以下,水就开始变得有点“酸”,而加点碱性物质,像小苏打,pH值又会上升,变得“温暖”起来。
2. 金属氢氧化物沉淀的形成好啦,咱们回到金属氢氧化物沉淀。
它的形成过程有点像一场化学派对,金属离子和氢氧根就像两个恋爱中的小情侣,碰到一起就会产生化学反应。
比如说,铝离子加上氢氧根,就会生成氢氧化铝沉淀。
想象一下,铝离子穿着西装,氢氧根则打扮得漂漂亮亮,俩人一见钟情,瞬间就形成了沉淀。
这个沉淀的颜色、性质与环境的pH值密切相关,像是气氛的变化,搞得一场化学派对的精彩纷呈。
2.1. pH值对沉淀的影响pH值变化就像是一种调料,不同的pH值会影响沉淀的形成和颜色。
例如,在碱性环境中,铁离子容易形成红色的氢氧化铁沉淀,而在酸性环境中,这个沉淀就不容易形成了。
这就像是在说,如果把派对的音乐调得太高,可能大家都兴奋得忘乎所以,反而不利于“相亲”啦!2.2. 影响因素分析不仅如此,温度、金属离子的浓度等等也会影响沉淀的形成。

氢氧化铝沉淀溶解的ph范围氢氧化铝沉淀的溶解,哎呀,这可是个有趣的话题!想象一下,你在厨房里忙活,突然发现了一个不明的白色粉末,这可不是你的小孩留下的面粉,而是氢氧化铝的沉淀。
它在水里就像个小调皮,酸碱环境一变,它就开始展现自己的特技,活泼得很呢!所以,咱们得聊聊它的“性格”,尤其是它喜欢的pH范围。
氢氧化铝这位小家伙,在中性环境下就像个乖宝宝,基本不吭声,安静得很。
但一旦pH值开始往酸性方向跑,它就开始有点不乐意了。
你想啊,pH值如果低于5.5,氢氧化铝就开始觉得自己被压迫,慢慢溶解,仿佛在说:“我受不了了,放我出去!”所以,酸性环境让它不再沉默,溶解得可快呢!这就像那种在派对上被冷落的人,突然找到了自己的舞池,嘿,活跃得很。
而在碱性环境中,氢氧化铝又是一副不同的面孔。
pH值高于7时,尤其是当它遇到强碱时,哇塞,简直是如鱼得水!这时候,它可不再沉淀了,反而是想要表现得更加闪亮,溶解得像春水一样。
它就像那种在学校里成绩优异的学生,得到了老师的赞赏,心里美滋滋的,真是个快乐的小家伙。
说到这里,咱们得提一下这个pH范围。
大概在4到8之间,氢氧化铝的情绪变化真是戏剧性。
pH值低于5.5,它开始情绪低落,没什么精神;而在6到8之间,它就开始稳定,简直像是找到了人生的意义。
这个pH范围就像是它的“家”,在这里它最安心,能乖乖待着。
你知道吗?氢氧化铝可不是个简单的家伙,它的存在不仅仅是为了沉淀,它还有很多用处。
比如说,在水处理方面,它可是个小能手。
它能把水里的杂质吸附掉,清清爽爽,真是给环境做了不少贡献。
就像你家里打扫卫生,氢氧化铝就是那个勤劳的小工人,把脏东西都清理掉,让水变得清澈透明。
在这过程中,pH值对它的影响就像调味品,少了不行,过了也不行,得恰到好处。
科学家们也早就发现了这一点,所以在水处理的过程中,得时刻监测pH值。
这就像是烹饪,盐放多了就咸,放少了又没味,得拿捏得当,才行啊。
有趣的是,氢氧化铝在不同的pH条件下,其沉淀和溶解之间的转变,真像是人性的一面。
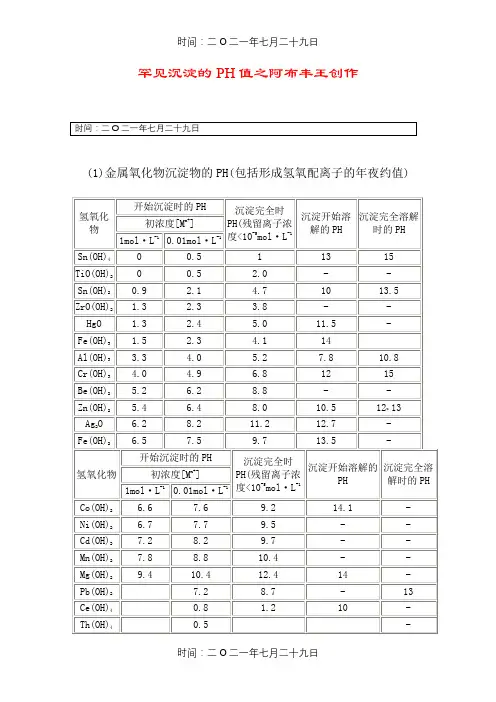
作者:非成败作品编号:92032155GZ5702241547853215475102时间:2020.12.13(1)金属氧化物沉淀物的PH(包括形成氢氧配离子的大约值)1mol·L-10.01mol·L-1度<10-5mol·L-1Sn(OH)40 0.5 1 13 15TiO(OH)20 0.5 2.0 - -Sn(OH)20.9 2.1 4.7 10 13.5ZrO(OH)21.32.33.8 - -HgO 1.3 2.4 5.0 11.5 -Fe(OH)31.52.3 4.1 14Al(OH)33.34.05.2 7.8 10.8Cr(OH)34.0 4.9 6.8 12 15Be(OH)25.26.2 8.8 - -Zn(OH)25.4 6.4 8.0 10.5 12~13Ag2O 6.2 8.2 11.2 12.7 -Fe(OH)26.57.5 9.7 13.5 -废水中重金属离子在碱性条件下可形成氢氧化物沉淀,然后通过固液分离装置除掉沉渣。
但各金属氢氧化物沉淀析出的最佳pH值有所不同。
根据文献报道[1],镍氢氧化物沉淀析出的理论pH值范围分别为8.49~9.49、、铅氢氧化物沉淀析出的理论pH值范围分别为7.88~8.88<18.3>重金屬廢水處理重金屬廢水處理最經濟而簡單的處理方法為化學沉澱,就是加入石灰提高廢水之PH,使重金屬離子變成氫氧化物沉澱去除重金屬離子之沉澱作用與PH的關係如下表所示:重金屬離子適合沉澱之PH 最佳沉澱之PHFe^3+,Sn^2+,Al^2+ 4 7 Cu^2+,Zn^2+,Cr^3+,Be^2+ 6 9 Fe^2+ 7 10 Cd^2+,Ni^2+,Co^2+,Cu^2+ (濃) 8 11 Ag^+,Mn^2+,Hg^+ 9 12作者:非成败作品编号:92032155GZ5702241547853215475102时间:2020.12.13。