
中学化学中的三角关系
中学化学中的三角形关系比较多,掌握这些三角形关系有助于我们对化学知识有一个系统的认识,有助于对物质之间的转化记忆。现对中学化学中出现的三角形关系总结如下,供大家参考。
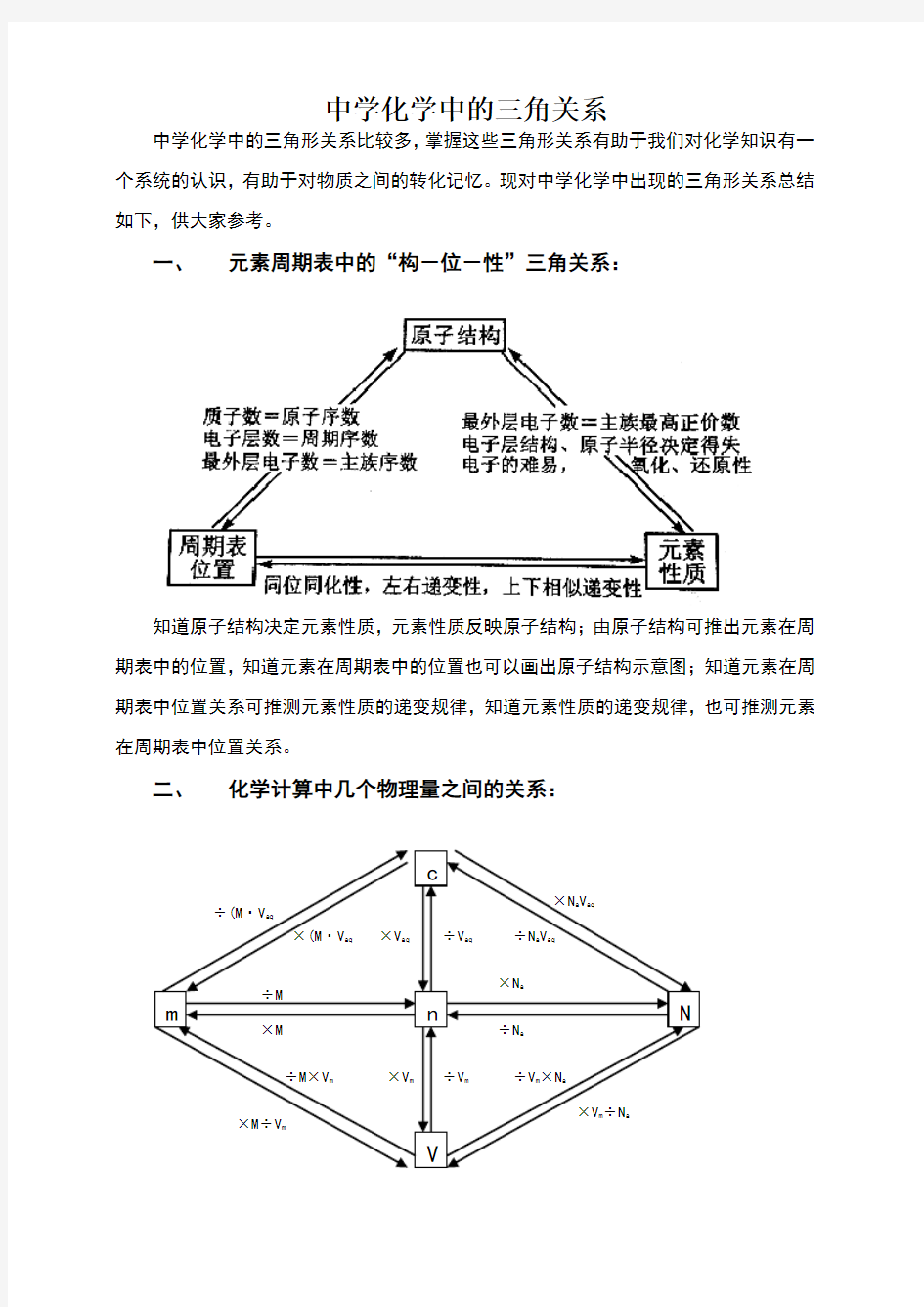
一、 元素周期表中的“构-位-性”三角关系:
知道原子结构决定元素性质,元素性质反映原子结构;由原子结构可推出元素在周期表中的位置,知道元素在周期表中的位置也可以画出原子结构示意图;知道元素在周期表中位置关系可推测元素性质的递变规律,知道元素性质的递变规律,也可推测元素在周期表中位置关系。
二、
化学计算中几个物理量之间的关系:
c
n
V
m
N
÷M ×M
÷(M·V aq
×(M·V aq
×V aq
÷V aq
÷V m
×V m
÷N a ÷N a V aq ×M÷V m
÷M×V m
×N a V aq ÷V m ×N a
×V m ÷N a
×N a
三、 物质之间的三角形转化关系:
1、 钠及其化合物之间的转化
2Na + O 2
点燃
Na 2O 2
2Na + 2H 2O == 2NaOH + H 2↑ 2Na 2O 2 + 2H 2O == 4NaOH + O 2↑ 2NaOH +CO 2 ==Na 2CO 3 + H 2O NaOH +CO 2==NaHCO 3
NaHCO 3 +Ca(OH)2 ==CaCO 3↓+ NaOH + H 2O 2NaHCO 3
△
Na 2CO 3 + H 2O
Na 2CO 3 + H 2O + CO 2==NaHCO 3
Na 2CO 3 + Ca(OH)2 == 2NaOH + CaCO 3↓
2、 钙的化合物之间的转化
Ca(OH)2 + CO 2 == CaCO 3↓+ H 2O CaCO 3
高温
CaO + CO 2↑
CaO + CO 2 ==CaCO 3 CaO + H 2O== Ca(OH)2
3、 铝及其化合物之间的转化
Ca(OH)2
CaCO 3 CaO
Al AlO 2
-
Al(OH)3
Al
3+
2Al + 6H + == 2Al 3+
+ 3H 2↑ 2Al + OH -
+ H 2O== 2AlO 2-
+ 3H 2↑ Al 3+
+4OH -
== AlO 2-
+ 2H 2O Al 3+
+3OH -
== Al(OH)3↓ AlO 2-
+ 4H +
== Al 3+
+ 2H 2O AlO 2-
+ H +
+ H 2O == Al(OH)3↓ Al(OH)3 + 3H +
== Al 3+
+ 3H 2O Al(OH)3 + OH -
== AlO 2-
+ 2H 2O
Al(Ⅲ)的三种形态在水中存在的量与溶液的pH 的关系如图所示:
4、碳及其化合物之间的转化关系: 2C + O 2
点燃
2CO
7
14NaHCO 3
CO
CO 2
C Na 2CO 3
C + O 2
点燃
CO 2 CO + O2
点燃
CO2
CO 2 +2NaOH == Na 2CO 3 + H 2O CO 2 +NaOH == NaHCO 3 Na 2CO 3 + H 2O + CO 2 == 2NaHCO 3 Na 2CO 3 + 2HCl == 2NaCl + CO 2↑+ H 2O 2NaHCO 3
△
Na 2CO 3 + H 2O + CO 2↑
NaHCO 3 + NaOH == Na 2CO 3 + H 2O NaHCO 3 + HCl == NaCl + H 2O + CO 2↑
5、 氮及其化合物之间的转化关系:
N 2 + 3H 2
催化剂 高温高压
2NH 3
N 2 + O 2
通电
2NO
4NH 3 + 5O 2 催化剂
△ 4NO + 6H 2O
2NO + O 2 == 2NO 2 3NO 2 + H 2O == 2HNO 3 + NO
4HNO 3 (浓)+ Cu == Cu(NO 3)2 + 2NO 2 + 2H 2O 8HNO 3 (稀)+ 3Cu == 3Cu(NO 3)2 + 2NO 2 + 4H 2O
6、 硫及其化合物之间的转化关系:
NH 3
N 2
NO HNO 3
NO 2
S + H 2 △
H 2S S + O 2
点燃
SO 2
2H 2S + O 2
点燃
2S + 2H 2O 2H 2S + 3O 2
点燃
2 SO 2 + 2H 2O
2H 2S + SO 2 == 3S + H 2O 2SO 2 + O 2
催化剂 加热
2SO 3
SO 3 + H 2O == H 2SO 4
H 2SO 4 +Na 2SO 3 == Na 2SO 4 + SO 2↑+ H 2O
7、 氯及其化合物之间的转化关系:
Cl 2 + H 2O == HCl + HClO MnO 2+4HCl(浓)MnCl 2+Cl 2↑+2H 2O
2HClO
△
2↑
8、 “铁三角”关系:
H 2S S
SO 2 H 2SO 4
SO 3
HCl
HClO
Cl 2 Fe
2+
Fe
3+
Fe
NaOH ,醇
Fe +2H + == Fe 2+
+ H 2 2Fe +3Cl 2
点燃
2FeCl 3
2Fe 2+
+ Cl 2 ==2 Fe 3+
+ 2Cl -
2 Fe 3+
+Fe == 3Fe
2+
Fe 2+
+ Zn == Zn 2+
+ Fe 2Fe 3+
+ 3Zn == 3Zn 2+
+ 2Fe
9、 烃及其衍生物之间的转化关系
CH 2=CH 2 + HBr
催化剂
CH 3CH 2Br CH 2=CH 2
+ H 2O
催化剂
CH 3CH 2OH
CH 3CH 2Br CH 2=CH 2+ HBr
CH 3CH 2Br + H 2O CH 3CH 2OH + HBr
CH 3CH 2OH
浓硫酸 170℃
CH 2=CH 2↑+ H 2O CH 3CH 2OH + HBr
CH 3CH 2Br + H 2O
CH 2=CH 2
CH 3CH 2Br CH 3CH 2OH
NaOH