
配位化学课程考试题-开卷
姓名:
学号:
问题一(14分)
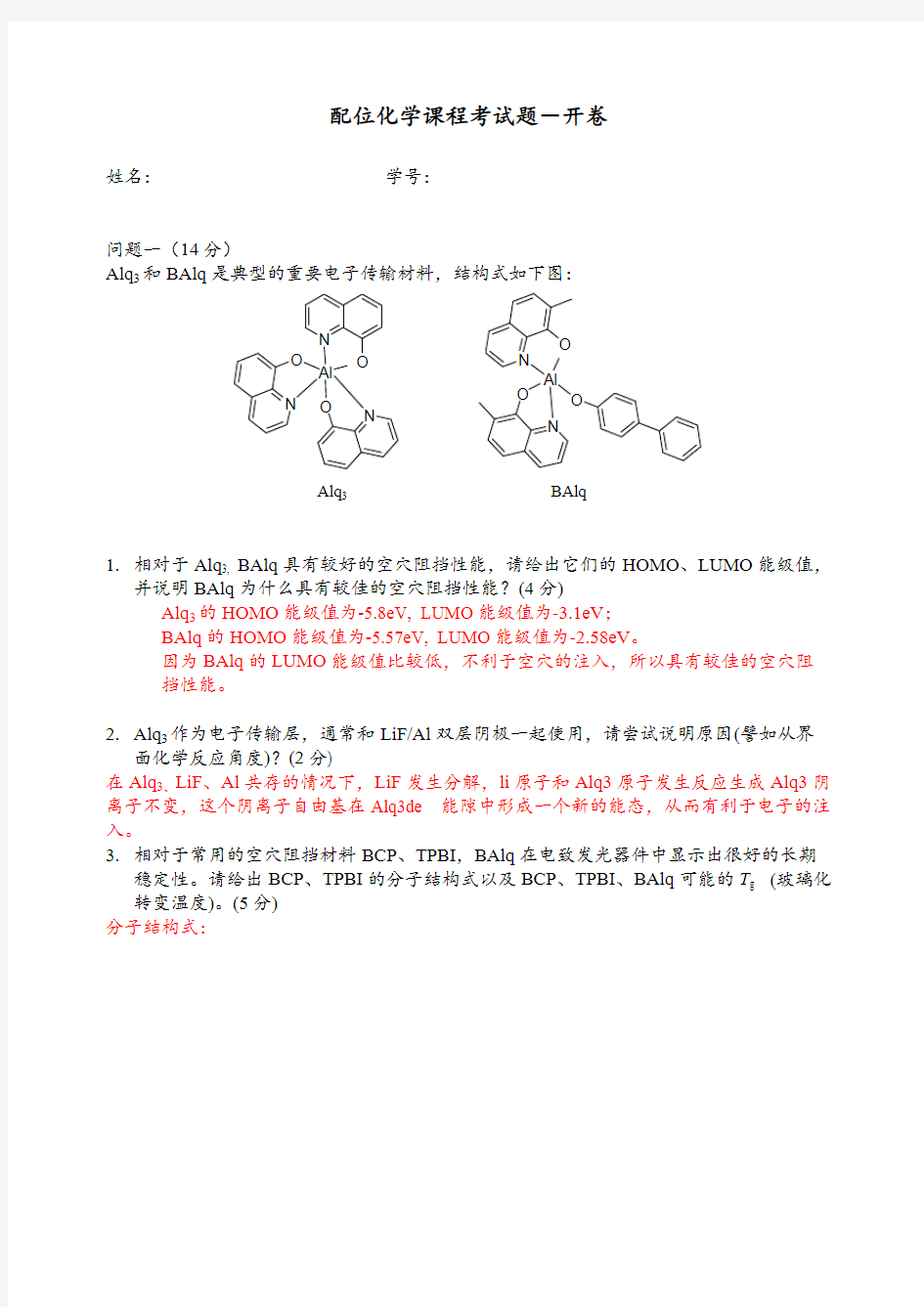
Alq 3和BAlq 是典型的重要电子传输材料,结构式如下图:
N O Al
N O
N
O
N
O
Al N
O
O
Alq 3
BAlq
1.相对于Alq 3, BAlq 具有较好的空穴阻挡性能,请给出它们的HOMO 、LUMO 能级值,并说明BAlq 为什么具有较佳的空穴阻挡性能?(4分) Alq 3的HOMO 能级值为-5.8eV, LUMO 能级值为-3.1eV ;
BAlq 的HOMO 能级值为-5.57eV, LUMO 能级值为-2.58eV 。
因为BAlq 的LUMO 能级值比较低,不利于空穴的注入,所以具有较佳的空穴阻挡性能。
2.Alq 3作为电子传输层,通常和LiF/Al 双层阴极一起使用,请尝试说明原因(譬如从界面化学反应角度)?(2分)
在Alq 3、LiF 、Al 共存的情况下,LiF 发生分解,li 原子和Alq3原子发生反应生成Alq3阴离子不变,这个阴离子自由基在Alq3de 能隙中形成一个新的能态,从而有利于电子的注入。
3.相对于常用的空穴阻挡材料BCP 、TPBI ,BAlq 在电致发光器件中显示出很好的长期稳定性。请给出BCP 、TPBI 的分子结构式以及BCP 、TPBI 、BAlq 可能的T g (玻璃化转变温度)。(5分)分子结构式:
N
N
N
N
N
N
N
N
BCP TPBI
BCP 、TPBI 、BAlq 可能的T g 分别为:80℃、100℃、200℃
4.给出BCP 、TPBI 、Alq 3电子迁移率大小顺序。(3分)
问题二(34分)
有机磷光金属配合物及电致磷光器件是当前有机电致发光研究领域的热点之一:
1 说明基于磷光材料的电致发光器件的内量子效率,理论上,能够达到100%。(4分) 再临光器件的发光层,主发光体的单重激发态与三重激发态的能量都可以分别由Foster 能
量转移和Dexter 能量转移到磷光发光体的单重激发态和三重激发态中,再经由磷光发光体内部快速的系间窜越将单重激发态的能量转换到三重激发态,进而放出磷光,因而内部量子效率可接近100%。
2 假定电致磷光器件的外量子为100%, 通常情况下,外量子效率为多少?为什么?(4
分)?试分析提高外量子效率的途径?(4 分)p315
内量子效率100%,光耦合输出效率ηe=20%,最大外量子效率EQE=ηe*IQE=20%1 发光层具有较高的光致发光的效率
2磷光材料(磷光材料可以通过采用重原子效应、降低体系温度和向体系内引入顺磁分子
的方法提高量子产率)
3在发光层内,实现电荷以及激子限制4提高发射光耦合出射效率
3 以非离子、分子型电致磷光铱配合物为例,当前,蓝、天蓝、绿、黄、红、近红外发
光材料都已报道。请举例说明,写出相应蓝、天蓝、绿光、黄光、红光、近红外发光铱配合物的化学结构式,并阐述上述铱配合物为什么发光颜色可调?(14分)P338P337
天蓝:
FIrPic 绿光:
N
F
F
Ir
2
N
O
O
N
Ir
2
N
黄光: 红光: 近红外发光:
C 8H 17C 8H 17
N
Ir
2
O
O
N
Ir
2
O
O
S
N
O
O
S
N
Ir
2
O
O
铱配合物发光颜色可调是因为可以通过改变铱配合物的配体,增加或减少配体的
共轭长度,从而改变配合物的LUMO 和HOMO 能级值,进而增大或减小带隙,调节其发光颜色。
4
有机磷光配合物在高效白光照明器件上具有重要应用前景。其中,流明效率是衡量“白光照明器件”性能重要的指标之一,与器件的工作电压直接相关。如何有效降低器件工作电压?(4分)
1)电荷传输材料具有较高的载流子迁移率
2)空穴传输材料的HOMO 能级与阳极功函数相匹配,电子传输层的LUMO 能及与阴极
功函数相匹配
3)发光层材料具有适当的HOMO 和LUMO 能级(发光颜色纯度)以及载流子迁移率。5 试分析“有机白光照明器件”面临的挑战。 (4 分)P378
由于目前很难设计单个分子能够在整个可见光范围内都有高效发射,所以常常采用将多个掺杂剂进行组合,从而产生有机白光器件。在这种情况下,有机白光器件会面临以下问题:1.材料的宽发射光谱分布
2.由于材料的纯度关系到器件的发光效率、稳定性和重复性,故而需要高纯度的材料,但是提纯需要高的成本,长的操作操作时间,步骤繁琐。
3.有机白光器件的成本大。能得到最高效率的白光器件常采用的热蒸发源技术成本大。
4.寿命短。问题三(6 分)
能量转移在设计新型发光化合物以及电致发光器件过程中起着重要作用,试回答下述问题?1 什么是F?rster 和 Dexter 能量转移?(4分)p44. p2 136
处于激发态的激子能量可以以辐射复合或非辐射复合的形式退激发,也可以将能量以光的 发射——再吸收的形式转移给别的激子,或者在直接将电子或空穴转移到另外的分子上形成新的激子的同时完成能量的传递。后两种能量的转移方式分别叫做F?rster 和 Dexter 能量转移。
2磷光材料可以通过F?rster 能量转移,敏化荧光材料发光;在荧光-荧光材料,磷光-
磷光材料之间也能发生F?rster 能量转移,前提条件是什么?(2分)主发光体的放射和客发光体的吸收可以重叠,而且两者的跃迁是被允许的
定设备调试高中资料试卷方案。
问题四(8 分)
稀土配合物是一类重要磷光材料:
1.说明稀土离子有效发光为什么需要敏化(2分) ?P393
稀土离子本身几乎不被直接激发,所以需要敏化。
2.给出敏化示意图(4分)。P322
稀土配合物发光的机理是配体激发到单重激发态后,要经过系间窜越到三重激发态,再由三重激发态将能量转移给中心离子,使中心离子受到激发,跃迁到激发态,当中心离子由激发态回到基态时产生荧光。
3.在敏化过程中,哪一种能量转移过程起主要作用?(2分)
敏化是Dexter能量转移。
问题五(8 分)
在电致磷光器件中,电荷捕获(Charge trapping)被认为是主要发光机理:
1说明电荷捕获的含义。(2 分)
激发的能量除了有主发光体转移到客发光体的方式外,也可以经由载流子的方式来激发客发光体,就是电子与空穴直接在客发光体上复合形成Frenkel形式的激子,进而激发客发光体来放光。一般来说,在高掺杂龙都和低电流密度下,载流子捕捉是主要的发光机制。
2结合具体实例分析。(6 分)
在电致发光与光致发光中,发光分子从基态被激发到激发态的过程不同,但到达激发态后,激子辐射发光的过程是相同的。通常掺杂体系的能量转移效率与外加电场无关,因此如果在电致发光中客体获得能量的途径仅为能量转移,那么光致发光光谱和电致发光光谱中母体和客体的发光强度比例将不会改变。但是很多情况下EL谱中客体发光明显强于PL谱中客体的发光,这说明客体除了通过能量转移从母体获得能量外还有其它能量获得的途径。客体获得其它能量的最有可能的途径是载流子通过电荷捕获直接在客体
分子上复合形成激子。这也是荧光客体除通过能量转移从母体获得能量外的唯一能量获得的途径。
图2.1是典型的客体发光在EL谱中明显强于PL谱的文献报道。器件结构为ITO/PEDOT/PF:PBD:Ir/Ba/Al,在PL光谱中母体PF在客体掺杂浓度为16%还能看见发光,但在EL光谱中当客体掺杂浓度为0.5%时,母体发光已经被完全猝灭了。PL光谱和EL光谱如此明显的差别最好的解释就是此器件在电致发光中存在电荷捕获发光。
图2.1 PF:PBD:Ir掺杂体系的PL光谱和EL光谱对比。
问题六(6 分):
三基色发光材料对于实现全彩有机电致发光显示至关重要。试分析在单组分电致发光材料的设计方面,需要注意的问题。
1)具备高量子效率的荧光特性,且自吸收小;
2)要求材料的荧光光谱主要分布在400~700 nm可见光范围内;
3)具有良好的半导体特性,亦即应具有较高的电导率, 能传导电子,或能传导空穴,或两者兼有。
4)具有良好的成膜特性,容易采用某种途径(甩涂、旋涂、真空沉积
等)制膜,且膜厚度在几百个纳米甚至几十个纳米的范围内无针孔;
5)具有优良的溶解性能,以保证加工的便利性;
6)材料稳定。
问题七(10 分)
相比于非离子型磷光配合物,还有一类离子型磷光配合物用于发光电化学池(LECs):
1.给出离子型磷光配合物用于发光电化学池的可能机理(4 分)?
在基于离子型过渡金属配合物的发光电化学池机理研究中,Slinker 等[35]提出了电动力学模型由图2a 可知电极和材料没有接触时相对的能级位置,可以看出电极的费米能级与发光层的HOMO 和LUMO 能级不匹配此时,发光层离子成对分布在施加一定偏压时,有机层的阴阳离子分别向阳极和阴极移动,在电极表面形成内建电场( 图2b) 通过离子的重新分布克服了发光层HOMO- LUMO 能带,促进电子和空穴注入,然后复合产生光子
2.试分析发光电化学池潜在优缺点、未来发展趋势或应用前景?(6分)
聚合物发光电化学池(polymer light-emitting electrochemical cell,简称LEC)是依据聚合物发光二极管(PLED)的发光特性,通过在聚合物发光层中掺入聚合物电解质而制备得出的。LEC工作时,在外电场作用下,功能层中的离子迁移形成对聚合物的掺杂,最后形成p-i-n结构,电子和空穴在i型区复合发光。与PLED相比,LEC有着起亮电压低、发光量子效率高等优点,但也具有发光响应速度慢,最大亮度低,启亮时间长,工作寿命短等诸多缺点。共轭聚合物同时具有离子导电和电子导电的性能,避免了聚合物和盐类的之间由于极性不同的相容性差导致的分相问题。
由于LEC中的发光层是一层含有可氧化还原掺杂的荧光共轭聚合物和
离子导电的聚合物固体电解质的复合膜所组成,共轭发光聚合物一般都是非
极性分子,而聚合物固体电解质则是强极性的材料,因此相容性很差,影响
了器件的性能。所以如何提高荧光共轭聚合物相和导电聚合物相之间的相容
性是进一步提高发光器件性能的一个非常关键的因素。另外,LEC器件还存
在复合膜的离子电导率低、响应时间慢等不足,所以近年来的研究工作主要
集中在这几个方面,并取得了一些可喜的成果.
由于PLEC薄膜制作相对简单,有望在平板显示和大面积照明方面或得商业应用
问题八(14分)
钌配合物较早地用于有机染料敏化太阳能电池器件,请回答下述问题:
1.给出有机染料敏化太阳能电池机理(电解质为I2/I3-)(6分)
当在Tio:表面吸附一层具有很好吸收可见光特性的染料光敏化剂时,染料分子吸收可见光后变为激发态。这是,如果染料分子的激发态能级高于Tiq的导带能级,且两者能级
匹配,那么激发态的染料分子就将光生电子注入到二氧化钦的导带而完成载流
子的分离。注入导带中的电子在多孔薄膜传输十分迅速,可瞬间到达导电玻璃
上,然后电子再经过外部回路传输到对电极。电解质溶液中的Is3-在对电极上得
到电子被还原成I一,厂传输到氧化钦的染料分子表面,给出电子将氧化态染料
分子还原成基态染料分子,同时自身被氧化成Is3-,从而完成整个电子循环(如
图2一1所示)。
D+h v→D*(燃料激发)
D*→D++e-(CB)(燃料氧化,光电子产生并注入二氧化钛的导带(CB))
e-(CB) →e-(CE)(二氧化钛导带的电子传输到对电极(CE))
I3-+2 e-→3 I- (电解质被还原)
3 I-+ 2D+→2D+ I3-(燃料分子被还原)
D为染料分子,D*为激发态染料分子
2.为了提高有机染料敏化太阳能电池的效率,在有机染料的设计方面需要注重哪些问题?
(4分)?
1紧密吸附在TiO2纳米薄膜表面,能够快速达到吸附平衡,而且不易脱落
2具有很宽的可见光谱吸收,易吸收尽可能多的太阳光
3激发态氧化还原电势比二氧化钛导带更负,以保证燃料激发态电子注入二氧化钛导带,且激发态寿命足够长且具有较高的电荷传输效率
4基态的燃料敏化剂不与溶液中的氧化还原离子对发生降解作用
5在氧化还原过程中要有相对低的势垒,以便在初级和次级电子转移中的自由能损失最小6具有长期的稳定性
3.试分析有机有机染料敏化太阳能电池的发展趋势(4分)
目前来看,有机染料敏化太阳能电池的转换效率和稳定性制约其发展,使用固态电解质代替现在液态的电解质已经是发展的趋势,同时解决二氧化钛对染料的光催化降解问题也是研究的重点。
(2)染料敏化剂要研究多种染料的协同敏化以及纯有机染料和无机量子点染料。
(3)良好性能的准固态电解质和固态有机空穴传输材料作为电解质,需要在现有的基础上取得突破。
配位化学试题 1. 利用Pt (Ⅱ)配合物中的反位效应,试说明如何以 K 2PtCl 为原料制备 :(1) [ PtPyNH 3Cl ] 所有可能的异构体,(2)下列配合物: Pt Cl NH 3H 3N Py Pt Cl Py H 3N H 3N Pt Cl NH 3C 2H 4Cl 2. 下列各组中,哪种配位体与同一中心离子形成的配合物稳定性高,为什么? C l -,F -和AL 3+;I -,Br --和Hg 2+;2CH 3NH 2,en 和Cu 2+ 3. 从常数手册上查出 [Cu (gly )2 ] 的lgk 1=9.76,lgk 2=2.47。测定条件是: T=25℃,[ NaClO 4 ]=1.0 mol/L ,此常数代表什么意义?具有什么性质?如测定 的方法是pH 法,叙述此方法的原理以及测定过程(gly :甘氨酸)。 4. 解释下列各胺与 Cu (Ⅱ)形成配离子稳定性的差别: 配体 lgk 1(25℃,I=0.1) 乙二胺 1055 1,2—二氨基丙烷 10.65 1,3—二氨基丙烷 9.98 1,2,3—三氨基丙烷 11.1 5. 下列二组试剂与同一金属离子形成螯合物时,估计lgk 大小次序: M(en)3M(Pn)3M(dien)2(1), ,,(2)N OH Cl N OH N OH CH 3N OH CH(CH 3)2 6、试为制备下列各化合物写出适合的配平方程式,并给出大致的反应条件。 (1)以 [Ir(NH 3)5H 2O]3+ 为原料,制备 [Ir(NH 3)5ONO]2+ (2)以 K 2PtCl 4 为原料,制备 [Pt(NH 3)4Cl 2] (3)以 CoBr 2·6H 2O 为原料,制备 [Co(NH 3)5Br]Br 2 (4)以 [Co(NH 3)5Cl]Cl 2 为原料,制备 [Co(en) 3]Cl 3 (5)以 [Pt(NH 3)4SO 4 为原料,制备 trans-[Pt(NH 3)4(OH)2]SO 4 7、何谓配位场谱项?它是如何产生的? 8、为什么Mn(NO 3)2的水溶液是很淡的粉红色?请解释。
传热学试题 第一章概论 一、名词解释 1.热流量:单位时间所传递的热量 2.热流密度:单位传热面上的热流量 3.导热:当物体有温度差或两个不同温度的物体接触时,在物体各部分之间不发生相对位移的情况下,物质微粒(分子、原子或自由电子)的热运动传递了热量,这种现象被称为热传导,简称导热。 4.对流传热:流体流过固体壁时的热传递过程,就是热对流和导热联合用的热量传递过程,称为表面对流传热,简称对流传热。 5.辐射传热:物体不断向周围空间发出热辐射能,并被周围物体吸收。同时,物体也不断接收周围物体辐射给它的热能。这样,物体发出和接收过程的综合结果产生了物体间通过热辐射而进行的热量传递,称为表面辐射传热,简称辐射传热。 6.总传热过程:热量从温度较高的流体经过固体壁传递给另一侧温度较低流体的过程,称为总传热过程,简称传热过程。 7.对流传热系数:单位时间单位传热面当流体温度与壁面温度差为1K是的对流传热量,单位为W/(m2·K)。对流传热系数表示对流传热能力的大小。 8.辐射传热系数:单位时间单位传热面当流体温度与壁面温度差为1K是的辐射传热量,单位为W/(m2·K)。辐射传热系数表示辐射传热能力的大小。 9.复合传热系数:单位时间单位传热面当流体温度与壁面温度差为1K是的复合传热量,单位为W/(m2·K)。复合传热系数表示复合传热能力的大小。 10.总传热系数:总传热过程中热量传递能力的大小。数值上表示传热温差为1K时,单位传热面积在单位时间的传热量。 二、填空题 1.热量传递的三种基本方式为、、。 (热传导、热对流、热辐射) 2.热流量是指,单位是。热流密度是指,单位是。 (单位时间所传递的热量,W,单位传热面上的热流量,W/m2) 3.总传热过程是指,它的强烈程度用来衡量。 (热量从温度较高的流体经过固体壁传递给另一侧温度较低流体的过程,总传热系数) 4.总传热系数是指,单位是。 (传热温差为1K时,单位传热面积在单位时间的传热量,W/(m2·K)) 5.导热系数的单位是;对流传热系数的单位是;传热系数的单位是。 (W/(m·K),W/(m2·K),W/(m2·K))
驾校科目一考试题库 总分100分(90分过关) 采用公安部2013年新版考试题库,本站在全国率先提供最新版的科目一试题 1、风、雨、雪、雾等复杂气象条件,遇前车速度较低时,应开启前照灯,连续鸣喇叭迅速超越。 对错 2、交通事故仅造成重伤且驾驶人愿意承担全部责任的,可自行协商处理。 对错 3、图中警察手势为示意车辆靠边停车信号。 对错 4、车辆下坡行驶,要适当控制车速,充分利用发动机进行制动。 对错 5、违反道路交通安全法律、法规的规定,发生重大交通事故,构成犯罪的,依法追究刑事责任,并由公安机关交通管理部门吊销驾驶证。 对错 6、行车途中,仪表板上的“ ”灯亮起,表示车内温度异常。 对错 7、如图所示黄色双向两车道路面中心虚线,用于分隔对向行驶的交通流,在保证安全的情况下,应许车辆越线超车或向左转弯。 对错 8、造成交通事故后逃逸的,由公安机关交通管理部门吊销机动车驾驶证,且终生不得重新取得机动车驾驶证。 对错 9、图中警察手势为停止信号。 对错 10、自动挡汽车在平路行驶时使用“L”挡。 对错 11、发现高速公路上突然有人或动物横穿时,紧急避险措施不应超过必要的限度,造成不应有的损害。 对错 12、通过窄路、窄桥时,不得超车。 对错 13、车辆进入山区道路后,要特别注意“连续转弯”标志,并主动避让车辆及行人,适时减速和提前鸣喇叭。 对错
14、在高速公路变更车道时,应提前开启转向灯,观察情况,确认安全后,缓转转向盘,驶入需要变更的车道。 对错 15、机动车在高速公路上遇前方堵塞或交通不畅时,可以在应急车道内行驶或停车。 对错 16、机动车驾驶人在驾驶证暂扣期间,不得驾驶机动车。 对错 17、当车辆不慎落水后,驾驶人应保持冷静,并告知乘员不要慌张,做好深呼吸,待水快浸满车厢时,开启车门或摇开车窗逃生。 对错 18、驾驶人一边驾车,一边吸烟对安全行车无影响。 对错 19、机动车通过没有交通信号灯控制也没有交通警察指挥的交叉路口,相对方向行驶的右转弯的机动车让左转弯的车辆先行。 对错 20、驾驶车辆变更车道时,应提前开启转向灯,注意观察,保持安全距离,驶入要变更的车道。 对错 21、遇儿童在公路嬉戏打闹时,应连续鸣喇叭,快速通过。 对错 22、在没有中心隔离设施或者没有中心线的道路上,机动车遇相对方向来车时应当减速靠右行驶,并与其他车辆、行人保持必要的安全距离。 对错 23、图中是注意行人标志。 对错 24、机动车行驶中,车内人员不得将头伸出窗外,但可以将手伸出窗外。 对错 25、当事人对道路交通事故认定有异议的,可以向上一级公安交通管理部门提出书面复核申请。 对错 26、公安机关交通管理部门调解期间,当事人向人民法院提起民事诉讼的,调解终止。 对错 27、行车中发生交通事故时,应先保护自己,其次保护乘车人。 对错
分裂能: 中心离子的d轨道的简并能级因配位场的影响而分裂成不同组能级之间的能量差。晶体场稳定化能:在配体静电场的作用下, 中心金属离子的d轨道能级发生分裂, 其上的电子一部分进入分裂后的低能级轨道, 一部分进入高能级轨道。进入低能级轨道使体系能量下降, 进入高能级轨道使体系能量上升。根据能量最低原理, 体系中的电子优先进入低能级。如果下降的能量多于上升的能量, 则体系的总能量将下降。这样获得的能量称为晶体场稳定化能。光谱项:配位场光谱是指配合物中心离子的电子光谱。这种光谱是由d电子在d电子组态衍生出来的能级间跃迁产生的, 所以又称为d-d跃迁光谱或电子光谱。求某一电子组态的能级, 就是推导其光谱项, 实质上就是推算该电子组态的不同L和S的组合。空穴规则:在多于半满的壳层中, 根据静电观点, “空穴”可理解成正电子, 正电子也象电子那样会产生相互排斥作用。 二、命名结构式 1、[Co(NH3)6]Cl3 2、顺-二氯·二氨合铂(II) 反-二氯·二氨合铂(II) 顺-四氯·二氨合铂(Ⅳ) 反-四氯·二氨合铂(Ⅳ) 面-三氯·三氨合钴(III ) 经-三氯·三氨合钴(III ) 3、二(μ- 氯) ·四氯合二铁(III) 二(μ- 氯) ·二(二氯合铁(III)) 4、[(CO)5Mn-Mn(CO)5] 二(五羰基合锰) 5、二茂铁
三、简答 1.异构体异构现象是配合物的重要性质之一。所谓配合物的异构现象是指分子式(或实验式)相同,而原子的连接方式或空间排列方式不同的情况。化学结构异构(构造异构)结构异构是因为配合物分子中原子与原子间成键的顺序不同而造成的, 常见的结构异构包括电离异构, 键合异构, 配位体异构和聚合异构电离异构:在溶液中产生不同离子的异构体。[Co(NH3)5Br]SO4紫红色和[Co(NH3)5SO4]Br(红色), 它们在溶液中分别能产生SO42-和Br-。键合异构有些单齿配体可通过不同的配位原子与金属结合, 得到不同键合方式的异构体, 这种现象称为键合异构。配位异构在阳离子和阴离子都是配离子的化合物中, 配体的分布是可以变化的, 这种异构现象叫配位异构。配位体异构这是由于配位体本身存在异构体, 导致配合单元互为异构。立体异构实验式相同,成键原子的联结方式也相同,但其空间排列不同,由此而引起的异构称为立体异构体一般分为非对映异构体(或几何异构)和对映异构体(或旋光异构)两类 2.配合物稳定性、软硬酸碱理论、举例说明、应用配合物在溶液中的稳定性是指配离子或分子在溶液中解离为水合金属离子和配体达到平衡时,其解离程度的大小。稳定性是配合物在溶液中的一个重要性质,通常用相应的稳定常数来衡量。软酸或软碱是其价电子容易被极化或容易失去的酸或碱,而硬酸或硬碱则是其价电子与原子核结合紧密且不容易被极化或不容易失去的酸或碱。或者说,软酸、软碱之所以称为软,是形象地表明他们较易变形,硬酸、硬碱之所以称为硬,是形象地表明他们不易变形。举例:硬酸中接受电子的原子较小、正电荷高,其价电子轨道不易变形(用一句话说就是硬酸是受体原子对外层电子的吸引力强的酸)。像Al3+离子以及BF3之类的化合物都是硬酸的例子。软酸中接受电子的原子较大、正电荷数目低或者为0, 以易变形的价电子轨道去接受电子(也用一句话说就是软酸是受体原子对外层电子的吸引力弱的酸)。金属原子、Hg2+离子及InCl3之类化合物即是典型的软酸。硬碱中的价电子结合紧密(半径小),软碱中的价电子容易被极化(半径大)。典型的硬碱是一些较小的阴离子如F-离子,对称的含氧酸阴离子, 如ClO4-, 以及具有小的给予体原子的分子如NH3等。典型的软碱是一些较大的阴离子如I-、H-,或者含有较大的给予体原子的分子。应用:软硬酸碱原则在无机化学中有许多定性的应用:①由于一种元素的硬度通常随着其氧化态的增大而增大,氧化态越高硬度越大。因此,为了使一种处于高氧化态的元素稳定,就必须使之与硬碱如O2-、OH-或F-配位:如Fe(VI)和Pt(VI)这样的高价态能够分别在化合物 K2FeO4和PtF6中得到。相反,为了使一种元素处于低氧化态,则必须用软碱如CO或PR3与元素配位。如Na[Co-1(CO)4]和Pt0[P(CH3)3]4这样的化合物中可以见到Co(-1)和Pt(0)。 ②软硬酸碱原理还用来判断离子性盐在水中的溶解度。 3.价键理论、配位场理论、分子轨道理论优缺点价键理论提出配位共价模型,考虑了中心原子和配体的结构,能较好地说明许多配合物的配位数、几何构型、磁性质和一些反应活性等问题。但这个价键理论只能说明配合物在基态时的性质,而不能说明与激发态有关的性质(如配合物的各种颜色和光谱),也不能说明同一过渡金属系列中不同配合物的相对稳定性等。配位场理论人们在晶体场理论的基础上, 吸收了价键理论的若干成果, 既适当考虑中心原子与配体化学键的共价性, 又仍然采用晶体场理论的计算方法, 发展成为一种改进了的晶体场理论, 特称为配体场理论。分子轨道理论用于说明双原子分子和芳香烃的结构。1935年Van Vleck首先用分子轨道理论方法来处理配合物的化学键问题,遵循成键三原则:能量近似、最大重叠和对称性匹配原则。在理论上比晶体场理论等方法更为严谨,所得的结果常用来补充晶体场理论的不足。晶体场理论晶体场理论是一种静电理论, 它把配合物中中心原子与配体之间的相互作用, 看作类似于离子晶体中正负离子间的相互作用。但配体的加入, 使得中心原子五重简并的 d 轨道(见图)失去了简并性。在一定对称性的配体静电场作用下, 五重简并的d轨道将解除简并, 分裂为两组或更多的能级组, 这种分裂将对配合物的性质产生重。
第一部分选择题 一、单项选择题(本大题共 10 小题,每小题 2 分,共 20 分)在每小题列出的四个选项中只有一个选项是符合题目要求的,请将正确选项前的字母填在题后的括号内。 1 .对于过热器中:高温烟气→外壁→内壁→过热的传热过程次序为() A .复合换热、导热、对流换热 B .导热、对流换热、复合换热 C .对流换热、复合换热、导热 D .复合换热、对流换热、导热 2 .温度对辐射换热的影响对对流换热的影响。() A .等于 B .大于 C .小于 D .可能大于、小于 3 .对充换热系数为 1000W/(m 2 · K) 、温度为 77 ℃的水流经 27 ℃的壁面,其对流换热的热流密度为() A . 8 × 10 4 W/m 2 B . 6 × 10 4 W/m 2 C . 7 × 10 4 W/m 2 D . 5 × 10 4 W/m 2 4 .流体流过管内进行对流换热时,当 l/d 时,要进行入口效应的修正。() A .> 50 B .= 80 C .< 50 D .= 100 5 .炉墙内壁到外壁的热传递过程为() A .热对流 B .复合换热 C .对流换热 D .导热 6 .下述哪个参数表示传热过程的强烈程度?() A . k B .λ C .α c D .α 7 .雷诺准则反映了的对比关系?() A .重力和惯性力 B .惯性和粘性力 C .重力和粘性力 D .浮升力和粘性力 8 .下列何种材料表面的法向黑度为最大? A .磨光的银 B .无光泽的黄铜 C .各种颜色的油漆 D .粗糙的沿
9 .在热平衡的条件下,任何物体对黑体辐射的吸收率同温度下该物体的黑度。() A .大于 B .小于 C .恒等于 D .无法比较 10 .五种具有实际意义的换热过程为:导热、对流换热、复合换热、传热过程和() A .辐射换热 B .热辐射 C .热对流 D .无法确定 二、填空题(本大题共 10 小题,每小题 2 分,共 20 分) 11 .已知某大平壁的厚度为 10mm ,材料导热系数为 45W/(m · K) ,则通过该平壁单位导热面积的导热热阻为。 12 .已知某换热壁面的污垢热阻为 0.0003 ( m 2 · K ),若该换热壁面刚投入运行时的传热系数为340W ( m 2 · K ),则该换热壁面有污垢时的传热系数为。 13 .采用小管径的管子是对流换热的一种措施。 14 .壁温接近换热系数一侧流体的温度。 15 .研究对流换热的主要任务是求解,进而确定对流换热的热流量。 16 .热对流时,能量与同时转移。 17 .导热系数的大小表征物质能力的强弱。 18 .一般情况下气体的对流换热系数液体的对流换热系数。 19 .在一定的进出口温度条件下,的平均温差最大。 20 .是在相同温度下辐射能力最强的物体。 三、名词解释(本大题共 5 小题,每小题 4 分,共 20 分) 21 .稳态导热 22 .稳态温度场 23 .热对流 24 .传热过程 25 .肋壁总效率 四、简答题(本大题共 2 小题,每小题 8 分,共 16 分)
2018科目一内部题库 第1页 1、机动车仪表板上(如图所示)亮表示什么? A 、驻车制动解除 B 、制动踏板没回位 C 、行车制动器失效 D 、制动系统出现异常 答案:D 2、驾驶人有下列哪种违法行为一次记6分? A 、使用其他车辆行驶证 B 、饮酒后驾驶机动车 C 、车速超过规定时速50%以上 D 、违法占用应急车道行驶 答案:D 3、下列哪种违法行为的机动车驾驶人将被一次记12分? A 、驾驶故意污损号牌的机动车上道路行驶 B 、机动车驾驶证被暂扣期间驾驶机动车的 C 、以隐瞒、欺骗手段补领机动车驾驶证的 D 、驾驶机动车不按照规定避让校车的 答案:A 4、在道路与铁路道口遇到一个红灯亮时要尽快通过道口。 答案:错 5、这个标志是何含义? A 、向左急转弯 B 、向右急转弯 C 、向左绕行 D 、连续弯路 答案:A 6、驾驶机动车遇到这种信号灯亮时,如果已越过停止线,可以继续通行。 答案:对 7、这个标志是何含义? A 、双向交通 B 、分离式道路 C 、潮汐车道 D 、减速让行 答案:A 8、机动车仪表板上(如图所示)亮,表示驻车制动器操纵杆可能没松到底。 答案:错 9、在路口右转弯遇同车道前车等候放行信号时如何行驶? A 、从前车左侧转弯 B 、从右侧占道转弯 C 、鸣喇叭让前车让路 D 、依次停车等候 答案:D 10、机动车发生正面碰撞时,安全气囊加上安全带的双重保护才能充分发挥作用。 答案:对 11、灯光开关在该位置时,前雾灯点亮。 答案:对 12、这个开关控制机动车哪个部位? A 、风窗玻璃除雾器 B 、风窗玻璃刮水器 C 、危险报警闪光灯 D 、照明、信号装置
配合物的化学键理论 摘要:化学键理论在配位化学中有着重要的运用,它现在主要有三大流派。本文就回顾化学键的发展历程,并对三大化学键理论做出仔细的阐述。 关键字:化学键价键理论分子轨道理论晶体场理论配位场理论 十八世纪后半叶,欧洲的化学家开始了定量的化学实验的研究。法国化学家普劳斯特通过测定部分化合物的重量组成而提出了定组成定律即一个化合物不管它是天然的还是人工合成的组成该化合物的各元素的重量百分比是固定不变的这一定律促使人们进一步研究化合物是怎样组成的和靠什么力结合在一起的。化合物的定组成结构和性质有什么关系。由此化学键理论产生和逐步发展起来。 1 化学键的发展历程 最早化学家假设原子和原子之间是用一个神秘的钩钩住的,这种设想至今仍留下痕迹,化学键的“键”字就有钩的意思。 1916年,德国科学家柯塞尔考察大量的事实后得出结论:任何元素的原子都要使最外层满足8 电子稳定结构。柯塞尔的理论能解释许多离子化合物的形成,但无法解释非离子型化合物。1923 年,美国化学家路易斯发展了柯塞尔的理论,提出共价键的电子理论:两种元素的原子可以相互共用一对或多对电子,以便达到稀有气体原子的电子结构,这样形成的化学健叫做共价健。 柯塞尔和路易斯的理论常叫原子价电子理论。它只能定性地描述分子的形成,化学家更需要对化学键做定量阐述。 1927 年,海特勒和伦敦用量子力学处理氢分子,用近似方法计算出氢分子体系的波函数和能量获得成功,这是用量子力学解决共价键问题的首例。1930 年,鲍林更提出原子成键的杂化理论(杂化轨道理论)。1932 年,洪德把单键、多键分成δ和∏键两类。δ健是指在沿着连接两个原子核的直线(对称轴)上电子云有最大重叠的共价键,这种键比较稳定。∏键是指沿电子云垂直于这条直线方向上结合而成的键,这种键比较活泼。这就使价键理论进一步系统化,使经典的化合价和化学键有机地结合在一起了。 由于上述的价键理论对共扼分子、氧气分子的顺磁性等事实不能有效解释,因此本世纪30 年代后又产生一种新的理论——分子轨道理论。 分子轨道理论在1932 年首先由美国化学家马利肯提出。他用的方法跟经典化学相距很远,一时不被化学界接受,后经密立根、洪德、休克尔、伦纳德等人努力,使分子轨道理论得到充实和完善。它把分子看作一个整体,原子化合成分子时,由原子轨道组合成分子轨道,
1、机动车仪表板上(如图所示)亮表示什么? A、驻车制动解除 B、制动踏板没回位 C、行车制动器失效 D、制动系统出现异常 答案:D 2、驾驶人有下列哪种违法行为一次记6分? A、使用其他车辆行驶证 B、饮酒后驾驶机动车 C、车速超过规定时速50%以上 D、违法占用应急车道行驶 答案:D 3、下列哪种违法行为的机动车驾驶人将被一次记12分? A、驾驶故意污损号牌的机动车上道路行驶 B、机动车驾驶证被暂扣期间驾驶机动车的 C、以隐瞒、欺骗手段补领机动车驾驶证的 D、驾驶机动车不按照规定避让校车的 答案:A 4、在道路与铁路道口遇到一个红灯亮时要尽快通过道口。 答案:错 5、这个标志是何含义? A、向左急转弯 B、向右急转弯 C、向左绕行 D、连续弯路 答案:A 6、驾驶机动车遇到这种信号灯亮时,如果已越过停止线,可以继续通行。 答案:对 7、这个标志是何含义? A、双向交通 B、分离式道路 C、潮汐车道 D、减速让行 答案:A 8、机动车仪表板上(如图所示)亮,表示驻车制动器操纵杆可能没松到底。 答案:错 9、在路口右转弯遇同车道前车等候放行信号时如何行驶? A、从前车左侧转弯 B、从右侧占道转弯 C、鸣喇叭让前车让路 D、依次停车等候 答案:D 10、机动车发生正面碰撞时,安全气囊加上安全带的双重保护才能充分发挥作用。答案:对 11、灯光开关在该位置时,前雾灯点亮。 答案:对 12、这个开关控制机动车哪个部位? A、风窗玻璃除雾器 B、风窗玻璃刮水器 C、危险报警闪光灯 D、照明、信号装置 答案:B 13、安装防抱死制动装置(ABS)的机动车制动时,制动距离会大大缩短,因此不必保持安全车距。答案:错 14、机动车仪表板上(如图所示)亮表示什么? A、前照灯开启 B、危险报警闪光灯开启 C、前后位置灯开启 D、前后雾灯开启
文档来源为:从网络收集整理.word 版本可编辑.欢迎下载支持. 1 1、机动车仪表板上(如图所示)亮表示什么? A 、驻车制动解除 B 、制动踏板没回位 C 、行车制动器失效 D 、制动系统出现异常 答案:D 2、驾驶人有下列哪种违法行为一次记6分? A 、使用其他车辆行驶证 B 、饮酒后驾驶机动车 C 、车速超过规定时速50%以上 D 、违法占用应急车道行驶 答案:D 3、下列哪种违法行为的机动车驾驶人将被一次记12分? A 、驾驶故意污损号牌的机动车上道路行驶 B 、机动车驾驶证被暂扣期间驾驶机动车的 C 、以隐瞒、欺骗手段补领机动车驾驶证的 D 、驾驶机动车不按照规定避让校车的 答案:A 4、在道路与铁路道口遇到一个红灯亮时要尽快通过道口。 答案:错 5、这个标志是何含义? A 、向左急转弯 B 、向右急转弯 C 、向左绕行 D 、连续弯路 答案:A 6、驾驶机动车遇到这种信号灯亮时,如果已越过停止线,可以继续通行。 答案:对 7、这个标志是何含义? A 、双向交通 B 、分离式道路 C 、潮汐车道 D 、减速让行 答案:A 8、机动车仪表板上(如图所示)亮,表示驻车制动器操纵杆可能没松到底。 答案:错 9、在路口右转弯遇同车道前车等候放行信号时如何行驶? A 、从前车左侧转弯 B 、从右侧占道转弯 C 、鸣喇叭让前车让路 D 、依次停车等候 答案:D 10、机动车发生正面碰撞时,安全气囊加上安全带的双重保护才能充分发挥作用。 答案:对 11、灯光开关在该位置时,前雾灯点亮。 答案:对 12、这个开关控制机动车哪个部位? A 、风窗玻璃除雾器 B 、风窗玻璃刮水器 C 、危险报警闪光灯 D 、照明、信号装置 答案:B 13、安装防抱死制动装置(ABS )的机动车制动时,制动距离会大大缩短,因此不必保持安全车距。 答案:错 14、机动车仪表板上(如图所示)亮表示什么? A 、前照灯开启 B 、危险报警闪光灯开启 C 、前后位置灯开启 D 、前后雾灯开启 答案:C 15、机动车仪表板上(如图所示)亮时,防抱死制动系统处于打开状态。 答案:错 16、公安交通管理部门对驾驶人的交通违法行为除依法给予行政处罚外,实行下列哪种制度? A 、奖励里程制度 B 、违法登记制度 C 、累积记分制度 D 、强制报废制度 答案:C
配位化学习题 1.命名下列配合物的配离子(任选4个) (1)(NH4)3[SbCl6]; (2) [Co(en)3] Cl3; (3)[Co(NO2)6]3-; (4)[Cr(H2O)4Br2] Br·2H2O; (5) [Cr(Py)2 (H2O) Cl3] ; (6)NH4[Cr(SCN)4(NH3)2] 答案:(1) 六氯合锑(III)酸铵; (2) 三氯化三(乙二胺)合钴(III); (3)六硝基合钴(III)配阴离子; (4)二水合溴化二溴·四水合铬(III); (5)三氯·水·二吡啶合铬(III); (6)四硫氰根·二氨合铬(III)酸铵 2. 根据下列配合物和配离子的名称写出其化学式(任选4个) (1)四氯合铂(II)酸六氨合铂(II); (2)四氢合铝(III)酸锂; (3)氯化二氯·四水合钴(III);(4)羟基·水·草酸根·乙二胺合铬(III); (5)氯·硝基·四氨合钴(III)配阳离子;(6)二氨·草酸根合镍(II) 答案: 3.叙述化学热力学和化学动力学对无机合成的指导作用。 避免和减少合成工作的盲目性,必须掌握化学热力学和化学动力学。
1化学热力学作用: 1)能否发生,2)极限如何。 2. 化学动力学作用: 1)反应速度。反应有多快,2)反应机理。如何进行反应, 3. 理论指导 通过热力学和动力学的分析,预测能否反应和反应多快,制定相应的实验方案度。 4.根据学习经验,说明配合物合成后需要进行的表征手段有那些? 答案:(1) 熔点的测定;(2)红外光谱;(3)元素分析;(4) 核磁共振;(5)差热及热重分析;(6)X-射线粉末衍射; (7)扫描电子显微镜; (8)透射电子显微镜; (9)气体吸附实验分析。 5. 有两种钴(III)配合物组成均为Co(NH3)5Cl(SO4),但分别只与AgNO3和BaCl2发生沉淀反应。写出两个配合物的化学结构式,并指出他们属于哪一类异构现象? 答案:前者与AgNO3反应生成AgCl沉淀者,Cl-为外界,化学结构式为[CoSO4(NH3)5] Cl;能与BaCl2反应生成BaSO4沉淀者外界为SO2-4,化学结构式为[CoCl(NH3)5] SO4,二个配合物之间属解离异构关系。 6.向Hg2+溶液中加入KI溶液时有红色HgI2生成,继续加入过量的KI溶液时HgI2溶解得无色的HgI2-4配离子。请说明HgI2有颜色而HgI2-4无色的原因。
《传热学》试题库 第一章概论 一、名词解释 1.热流量:单位时间所传递的热量 2.热流密度:单位传热面上的热流量 3.导热:当物体有温度差或两个不同温度的物体接触时,在物体各部分之间不发生相对位移的情况下,物质微粒(分子、原子或自由电子)的热运动传递了热量,这种现象被称为热传导,简称导热。 4.对流传热:流体流过固体壁时的热传递过程,就是热对流和导热联合用的热量传递过程,称为表面对流传热,简称对流传热。 5.辐射传热:物体不断向周围空间发出热辐射能,并被周围物体吸收。同时,物体也不断接收周围物体辐射给它的热能。这样,物体发出和接收过程的综合结果产生了物体间通过热辐射而进行的热量传递,称为表面辐射传热,简称辐射传热。6.总传热过程:热量从温度较高的流体经过固体壁传递给另一侧温度较低流体的过程,称为总传热过程,简称传热过程。7.对流传热系数:单位时间单位传热面当流体温度与壁面温度差为1K是的对流传热量,单位为W/(m2·K)。对流传热系数表示对流传热能力的大小。 8.辐射传热系数:单位时间单位传热面当流体温度与壁面温度差为1K是的辐射传热量,单位为W/(m2·K)。辐射传热系数表示辐射传热能力的大小。 9.复合传热系数:单位时间单位传热面当流体温度与壁面温度差为1K是的复合传热量,单位为W/(m2·K)。复合传热系数表示复合传热能力的大小。 10.总传热系数:总传热过程中热量传递能力的大小。数值上表示传热温差为1K时,单位传热面积在单位时间的传热量。 二、填空题 1.热量传递的三种基本方式为、、。 (热传导、热对流、热辐射) 2.热流量是指,单位是。热流密度是指,单位是。 (单位时间所传递的热量,W,单位传热面上的热流量,W/m2) 3.总传热过程是指,它的强烈程度用来衡量。 (热量从温度较高的流体经过固体壁传递给另一侧温度较低流体的过程,总传热系数) 4.总传热系数是指,单位是。 (传热温差为1K时,单位传热面积在单位时间的传热量,W/(m2·K)) 5.导热系数的单位是;对流传热系数的单位是;传热系数的单位是。 (W/(m·K),W/(m2·K),W/(m2·K)) 6.复合传热是指,复合传热系数等于之和,单位是。 (对流传热与辐射传热之和,对流传热系数与辐射传热系数之和,W/(m2·K)) 7.单位面积热阻r t的单位是;总面积热阻R t的单位是。 (m2·K/W,K/W) 8.单位面积导热热阻的表达式为。 (δ/λ) 9.单位面积对流传热热阻的表达式为。 (1/h) 10.总传热系数K与单位面积传热热阻r t的关系为。 (r t=1/K) 11.总传热系数K与总面积A的传热热阻R t的关系为。 (R t=1/KA) 12.稳态传热过程是指。 (物体中各点温度不随时间而改变的热量传递过程。) 13.非稳态传热过程是指。
2013年_C1驾照考试科目一考试题库驾考宝典2013年C1驾照考试科目一考试题库 第一章路交通安全法律、法规和规章章节练习试题 1、驾驶机动车在道路上违反道路交通安全法的行为,属于什么行为, A、违章行为 B、违法行为 C、过失行为 D、违规行为本题答案:B 2、机动车驾驶人违法驾驶造成重大交通事故构成犯罪的,依法追究什么责任, A、刑事责任 B、民事责任 C、经济责任 D、直接责任本题答案:A 3、机动车驾驶人造成事故后逃逸构成犯罪的,吊销驾驶证且多长时间不得重 新取得驾驶证, A、5年内 B、10年内 C、终生 D、20年内本题答案:C 4、驾驶机动车违反道路交通安全法律法规发生交通事故属于交通违章行为。 本题答案:错 5、驾驶机动车在道路上违反道路通行规定应当接受相应的处罚。本题答案:对 6、对未取得驾驶证驾驶机动车的,追究其法律责任。本题答案:对 7、对违法驾驶发生重大交通事故且构成犯罪的,不追究其刑事责任。本题答案:错 8、造成交通事故后逃逸且构成犯罪的驾驶人,将吊销驾驶证且终生不得重新 取得驾驶证。本题答案:对 9、驾驶机动车在道路上违反交通安全法规的行为属于违法行为。本题答案:对 10、驾驶机动车应当随身携带哪种证件, A、工作证 B、驾驶证 C、身份证 D、职业资格证本题答案:B 11、未取得驾驶证的学员在道路上学习驾驶技能,下列哪种做法是正确的,
A、使用所学车型的教练车由教练员随车指导 B、使用所学车型的教练车单独驾 驶学习C、使用私家车由教练员随车指导 D、使用所学车型的教练车由非教练员的驾驶人随车指导本题答案:A 12、机动车驾驶人初次申领驾驶证后的实习期是多长时间, A、6个月 B、12个月 C、16个月 D、18个月本题答案:B 13、在实习期内驾驶机动车的,应当在车身后部粘贴或者悬挂哪种标志, A、注意新手标志 B、注意避让标志 C、统一式样的实习标志 D、注意车距标志 本题答案:C 14、以欺骗、贿赂等不正当手段取得驾驶证被依法撤销驾驶许可的,多长时间 不得重新申请驾驶许可, A、3年内 B、终身 C、1年内 D、5年内本题答案:A 15、驾驶人要按照驾驶证载明的准驾车型驾驶车辆。本题答案:对 16、上路行驶的机动车未随车携带身份证的,交通警察可依法扣留机动车。本 题答案:错 17、上路行驶的机动车未放置检验合格标志的,交通警察可依法扣留机动车。 本题答案:对 18、伪造、变造机动车驾驶证构成犯罪的将被依法追究刑事责任。本题答案: 对 19、机动车驾驶人在实习期内驾驶机动车不得牵引挂车。本题答案:对 20、驾驶拼装机动车上路行驶的驾驶人,除按规定接受罚款外,还要受到哪种 处理, A、处10日以下拘留 B、暂扣驾驶证 C、吊销驾驶证 D、追究刑事责任本题答 案:C 21、驾驶报废机动车上路行驶的驾驶人,除按规定罚款外,还要受到哪种处理,
泰山学院课程考试专用 泰山学院化学化工学院2010级化学专业本科 2012~2013学年第一学期 《配位化学》试卷A (试卷共6页,答题时间120分钟) 一、选择题(每小题 2 分,共 20 分。请将答案填在下面的表格内) 1、关于影响配位数的主要因素的叙述,正确的是( ) A. 不论何种配体,中心离子的电荷越高、半径越小,配位数越大 ; B. 不论何种中心原子,配体的体积都是对配位数影响最大的因素 ; C. 讨论配位数的大小要从外部条件、中心离子、配体等方面考虑 ; D. 中心离子的电荷与半径,决定了形成配合物的配位数高低 ; 2、下面关于中心离子的描述,正确的是( ) A. Nb(V)、La(III)、Co(III) 为外层具有9-17电子结构的过渡金属离子; B. Cu(I)、Sn(II)、Hg(II) 为外层具有18 电子结构的离子 ; C. Ge(II)、Sn(II)、Pb(II) 为外层具有18+2电子结构的离子 ; D. Al(III)、Si(IV)、Ti(III) 为外层具有8电子结构的离子; 3、说明Zn 2+,Cd 2+,Hg 2+形成配合物的稳定性顺序,错误的是( ) A. [ZnI 4]2- > [HgI 4]2- ; B. [ZnCl 4]2- < [CdCl 4]2- ;
C. [CdF4]2-< [HgF4]2-; D. [CdF4]2-< [ZnF4]2-; 4、下列光谱化学序列中配体强弱顺序排列,正确的是( ) A. en > NO2-; B. F-< C2O42-; C. NH3> en ; D. OH-> CN-; 5、下列有关配合物的立体结构与配位数的描述,不正确的是( ) A. 配位数为3的配合物,有平面三角形和三角锥型两种构型; B. 一维无限链式结构的Cs[CuCl3]n的配位数为4 ; C. 具有角锥形结构的[SnCl3]-配位数为3 ; D. 配合物[(Ph3P)3Cu2Cl2]中铜(I)的配位数有3、4两种模式; 6、下列有关配位数与配合物的结构描述,不正确的是( ) A. 配离子[PdCl4]2-和[AuCl4]-都具有平面四方形结构; B. 配合物[VO(acac)2] 和[Cu(NH3)4]SO4·H2O都具有四方锥结构; C. 配离子[Ni(CN)5]3-和[CdCl5]3-都具有三角双锥构型; D. 配离子Cd(CN)4]2-和[Cu(CN)4]2-都具有四面体结构; 7、下列关于配合物几何异构体的叙述,正确的是( ) A. 配合物[Co(NO2)3(NH3)3] ,有2种几何异构体; B. 配离子[Co(en)2Cl2]+,有5种几何异构体; C. 配离子[Co(NH3)2(H2O)2(Py)2]3+,共有6种几何异构体; D. 配合物[Cr(gly)3] ,有4种几何异构体; 8、外文期刊Angew.Chem.Int.Ed可从哪个数据库网址中查得?() A. https://www.doczj.com/doc/e49272772.html, ; B. https://www.doczj.com/doc/e49272772.html, ; C. https://www.doczj.com/doc/e49272772.html, ;
《传热学》考试试题库汇总 第一章概论 一、名词解释 1.热流量:单位时间所传递的热量 2.热流密度:单位传热面上的热流量 3.导热:当物体有温度差或两个不同温度的物体接触时,在物体各部分之间不发生相对位移的情况下,物质微粒(分子、原子或自由电子) 的热运动传递了热量,这种现象被称为热传导,简称导热。 4.对流传热:流体流过固体壁时的热传递过程,就是热对流和导热联合用的热量传递过程,称为表面对流传热,简称对流传热。 5.辐射传热:物体不断向周围空间发出热辐射能,并被周围物体吸收。同时,物体也不断接收周围物体辐射给它的热能。这样,物体发出和接收过程的综合结果产生了物体间通过热辐射而进行的热量传递,称为表面辐射传热,简称辐射传热。 6.总传热过程:热量从温度较高的流体经过固体壁传递给另一侧温度较低流体的过程,称为总传热过程,简称传热过程。 7.对流传热系数:单位时间单位传热面当流体温度与壁面温度差为1K 是的对流传热量,单位为 W /(m2·K) 。对流传热系数表示对流传热能力的大小。 8.辐射传热系数:单位时间单位传热面当流体温度与壁面温度差为1K 是的辐射传热量,单位为 W /(m2·K) 。辐射传热系数表示辐射传热能力的大小。 9.复合传热系数:单位时间单位传热面当流体温度与壁面温度差为1K 是的复合传热量,单位为 W /(m2·K) 。复合传热系数表示复合传热能力的大小。 10.总传热系数:总传热过程中热量传递能力的大小。数值上表示传热温差为 1K 时,单位传热面积在单位时间的传热量。 二、填空题 1. 热量传递的三种基本方式为 (热传导、热对流、热辐射) 2. 热流量是指单位是。热流密度是指 ,单位是。 (单位时间所传递的热量, W ,单位传热面上的热流量, W/m2) 3. 总传热过程是指 (热量从温度较高的流体经过固体壁传递给另一侧温度较低流体的过程,总传热系数 ) 4. 总传热系数是指 (传热温差为 1K 时,单位传热面积在单位时间的传热量, W /(m2·K) ) 5. 导热系数的单位是 ;传热系数的单位是。 (W /(m·K) , W /(m2·K) , W /(m2·K) ) 6. 复合传热是指 ,复合传热系数等于之和,单位是。 (对流传热与辐射传热之和,对流传热系数与辐射传热系数之和, W /(m2·K) ) 7. 单位面积热阻 r t 的单位是 ;总面积热阻 R t 的单位是。 (m 2·K/W, K/W) 8. 单位面积导热热阻的表达式为 (δ/λ) 9. 单位面积对流传热热阻的表达式为 (1/h) 10. 总传热系数 K 与单位面积传热热阻 r t 的关系为。 (r t =1/K) 11. 总传热系数 K 与总面积 A 的传热热阻 R t 的关系为。
2020年最新科目一考试试题库 1.机动车仪表板上(如图所示)亮表示什么? a.驻车制动解除 b.制动踏板没回位 c.行车制动器失效 d.制动系统出现异常 答案:d 2.驾驶人有下列哪种违法行为一次记6分? a.使用其他车辆行驶证 b.饮酒后驾驶机动车 c.车速超过规定时速50%以上 d.违法占用应急车道行驶 答案:d 3.有下列哪种违法行为的机动车驾驶人将被一次记12分? a.驾驶故意污损号牌的机动车上道路行驶 b.机动车驾驶证被暂扣期间驾驶机动车的 c.以隐瞒、欺骗手段补领机动车驾驶证的 d.驾驶机动车不按照规定避让校车的 答案:a 4.在道路与铁路道口遇到一个红灯亮时要尽快通过道口。 答案:错 5.这个标志是何含义?
a.向左急转弯 b.向右急转弯 c.向左绕行 d.连续弯路 答案:a 6.驾驶机动车遇到这种信号灯亮时,如果已越过停止线,可以继续通行。 答案:对 7.这个标志是何含义? a.双向交通 b.分离式道路 c.潮汐车道 d.减速让行 答案:a 8.机动车仪表板上(如图所示)亮,表示驻车制动器操纵杆可能没松到底。 答案:错
9.在路口右转弯遇同车道前车等候放行信号时如何行驶? a.从前车左侧转弯 b.从右侧占道转弯 c.鸣喇叭让前车让路 d.依次停车等候 答案:d 10.机动车发生正面碰撞时,安全气囊加上安全带的双重保护才能充分发挥作用。答案:对 11.灯光开关在该位置时,前雾灯点亮。 答案:对 12.这个开关控制机动车哪个部位? a.风窗玻璃除雾器 b.风窗玻璃刮水器 c.危险报警闪光灯 d.照明、信号装置
13.安装防抱死制动装置(ABS)的机动车制动时,制动距离会大大缩短,因此不必保持安全车距。 答案:错 14.机动车仪表板上(如图所示)亮表示什么? a.前照灯开启 b.危险报警闪光灯开启 c.前后位置灯开启 d.前后雾灯开启 答案:c 15.机动车仪表板上(如图所示)亮时,防抱死制动系统处于打开状态。 答案:错 16.公安交通管理部门对驾驶人的交通违法行为除依法给予行政处罚外,实行下列哪种制度? a.奖励里程制度 b.违法登记制度 c.累积记分制度 d.强制报废制度 答案:c 17.驾驶人的驾驶证损毁后不得驾驶机动车。
科目一模拟考试2016最新版 总分100分(90分及格),考试时间45分钟 1、如图所示,B车具有优先通过权。 ? ? 2、驾驶机动车在路口遇到这种信号灯亮时,不能右转弯。 ? ? 3、机动车仪表板上(如图所示)亮表示启用地板及前风窗玻璃吹风。
? ? 4、女驾驶人穿高跟鞋驾驶车辆,不利于安全行车。 ? ? 5、机动车仪表板上(如图所示)一直亮,表示发动机控制系统故障。 ? ? 6、如图所示,A车在这种情况下应适当减速。
? ? 7、在道路上遇到这种情况可以从两侧超车。 ? ? 8、一个合格的驾驶人,不仅表现在技术的娴熟上,更重要的是应该具有良好的驾驶行为习 惯和道德修养。 ? ? 9、这个标志的含义是提醒前方左侧行车道或路面变窄。 ? ?
10、驾驶人的驾驶证损毁后不得驾驶机动车。 ? ? 11、驾驶人在实习期内驾驶机动车时,应当在车身后部粘贴或者悬挂统一式样的实习标志。 ? ? 12、如图所示,驾驶机动车接打电话容易导致发生交通事故。 ? ? 13、驾驶机动车发生财产损失交通事故,当事人对事实及成因无争议的可先撤离现场。 ? ? 14、驾驶机动车通过窄路、窄桥时的最高速度不能超过每小时30公里。 ? ? 15、如图所示,驾驶机动车遇到没有行人通过的人行横道时不用减速慢行。
? ? 16、驾驶人将机动车交给驾驶证被暂扣的人驾驶的,交通警察给予口头警告。 ? ? 17、其他车辆不准进入专用车道行驶,其目的是为了不影响专用车的正常通行。 ? ? 18、伪造、变造或者使用伪造、变造驾驶证的驾驶人构成犯罪的,将依法追究刑事责任。 ? ? 19、机动车之间发生交通事故,不管是否有人员伤亡,只要双方当事人同意,都可自行协商 解决 ? ? 20、在道路与铁路道口遇到一个红灯亮时要尽快通过道口。
级《配位化学》期末考试试题(A 卷)
————————————————————————————————作者:————————————————————————————————日期: 2
泰山学院化学与环境科学系2007级化学系各专业本科 2009~2010学年第二学期 《配位化学》试卷 A (试卷共6页,答题时间120分钟) 题号 一 二 三 四 五 总分 统分人 复核人 得分 一、选择题(每小题 2 分,共 20 分。请将答案填在下面的表格内) 1、中心原子具有18+2电子结构的是( ) A. Al(III); B. Zn(II); C. Pb(II); D. Fe(III); 2、下列关于配合物几何异构体数目的叙述,正确的是( ) A.[Co(NO 2)3(NH 3)3]配合物有3种几何异构体; B.平面四边形配合物[M(abcd)]型配合物,只有1种几何异构体 ; C. [M(a 2b 2b 2]型的八面体配合物存在5种几何异构体; D.八面体[M(ab)3]配合物,不存在几何异构体; 3、配合物晶体场稳定化能的计算结果,错误的是( ) A. [Fe(H 2O)6]2+ 的CFSE=-0.4Δo B. [Mn(H 2O)6]2+ 的CFSE=-2.0Δo 得分 阅卷人 题号 1 2 3 4 5 6 7 8 9 10 答案
C. [Ni(H2O)6]2+的CFSE=-1.2Δo D. [Cu(H2O)6]2+的CFSE=-0.6Δo 4、指出下列配体的光谱化学序列中错误的排列顺序( ) A. en < NO2-; B. SCN- > CN-; C. NH3 < en ; D. H2O > C2O42-; 5、配合物荷移跃迁能排列顺序存在错误的是:() A. [OsCl6]2- > [OsBr6]2- > [OsI6]2- B. [Ru III Cl6]3- > [Ru IV Cl6]2- C. VO43 > CrO42- > MnO4- D. HgCl42- < HgBr42- < HgI42- 6、期刊https://www.doczj.com/doc/e49272772.html,mun.主要收录在哪个数据库网址中?() A. https://www.doczj.com/doc/e49272772.html, ; B. https://www.doczj.com/doc/e49272772.html, ; C. https://www.doczj.com/doc/e49272772.html, ; D. https://www.doczj.com/doc/e49272772.html, ; 7、找出有关d n组态自由离子基谱项,错误的是:( ) A. d1组态的自由离子基谱项是2D ; B. d2组态的自由离子基谱项是1P; C. d3组态的自由离子基谱项是4F; D. d4组态的自由离子基谱项是5D; 8、配合物的立体结构与配位数的描述,错误的是( ) A. [Ag(NH3)2]+的配位数为2; B. 配位数为4的配合物,主要有四面体和平面四边形两种构型; C. 配位数为3的配合物只有平面三角形结构; 2 / 8