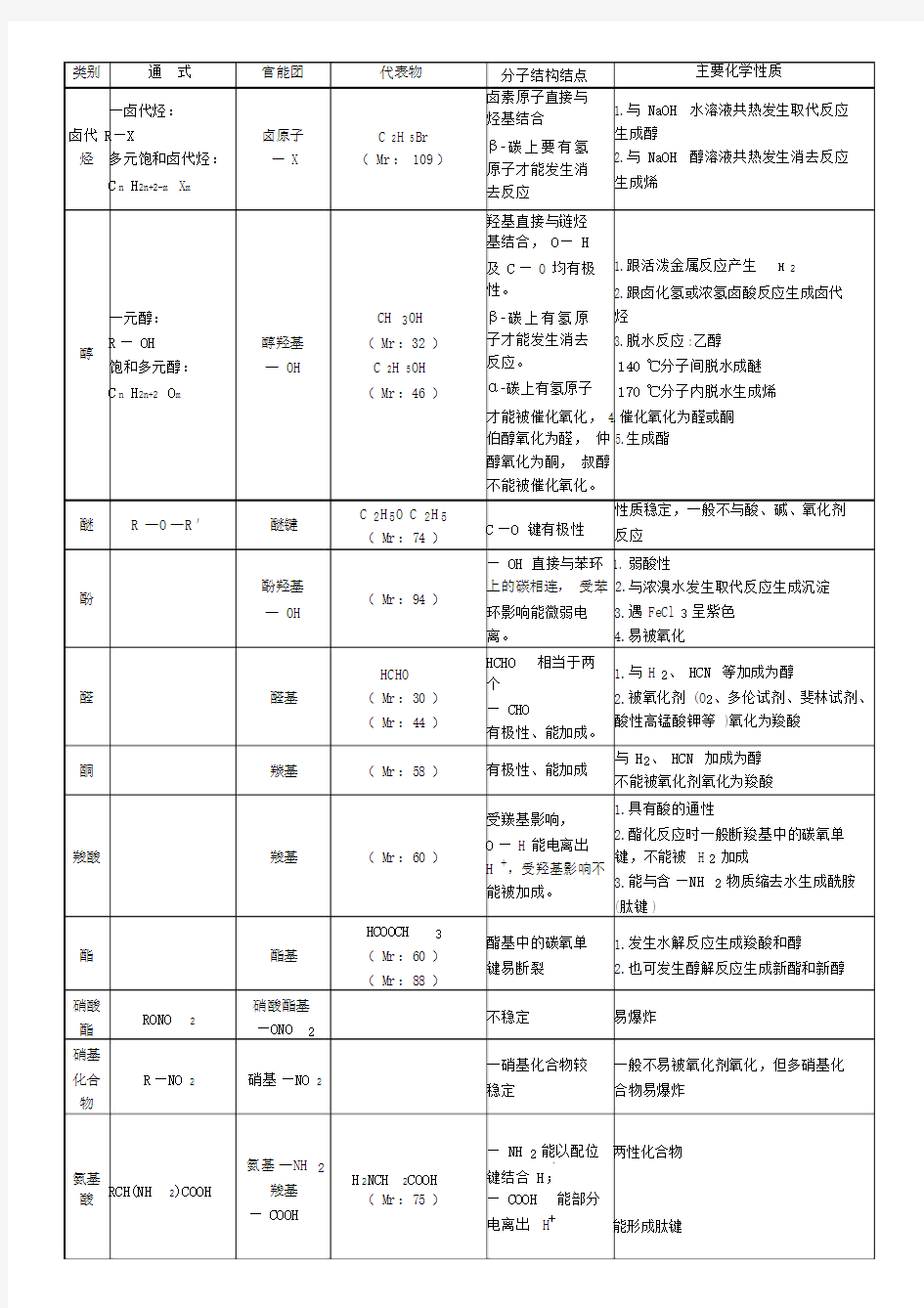
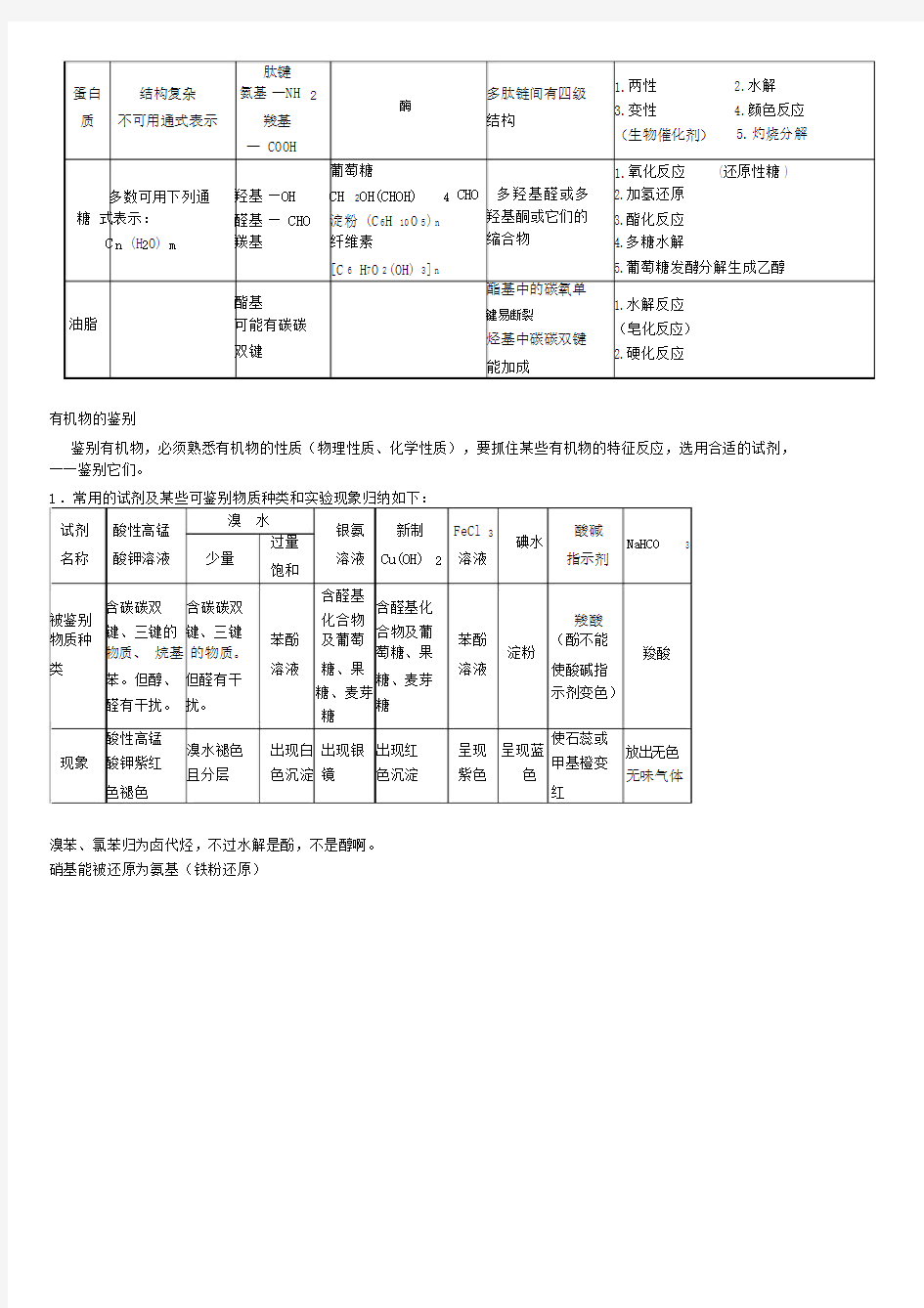
类别通式官能团代表物
一卤代烃:
卤代 R—X卤原子 C 2H 5Br
烃多元饱和卤代烃:— X( Mr : 109 )
C n H2n+2-m X m
一元醇:CH 3OH
醇R— OH醇羟基( Mr :32 )
饱和多元醇:— OH C 2H 5OH
C n H2n+2 O m( Mr :46 )
分子结构结点
卤素原子直接与
烃基结合
β-碳上要有氢
原子才能发生消
去反应
羟基直接与链烃
基结合, O— H
及C— O 均有极
性。
β-碳上有氢原
子才能发生消去
反应。
α-碳上有氢原子
主要化学性质
1.与 NaOH 水溶液共热发生取代反应
生成醇
2.与 NaOH 醇溶液共热发生消去反应
生成烯
1.跟活泼金属反应产生H 2
2.跟卤化氢或浓氢卤酸反应生成卤代
烃
3.脱水反应 :乙醇
140℃分子间脱水成醚
170℃分子内脱水生成烯
醚R —O—R′醚键C 2H5O C 2H5( Mr :74 )
酚酚羟基
( Mr :94 )— OH
HCHO
醛醛基( Mr :30 )
( Mr :44 )酮羰基( Mr :58 )
羧酸羧基( Mr :60 )
HCOOCH 3酯酯基( Mr :60 )
( Mr :88 )
硝酸
RONO 2硝酸酯基
酯—ONO 2硝基
化合R—NO2硝基—NO2物
氨基
氨基—NH 2
H2NCH 2COOH RCH(NH 2)COOH羧基
酸( Mr :75 )
— COOH 才能被催化氧化, 4.催化氧化为醛或酮
伯醇氧化为醛,仲 5.生成酯
醇氧化为酮,叔醇
不能被催化氧化。
性质稳定,一般不与酸、碱、氧化剂C—O 键有极性反应
— OH 直接与苯环 1.弱酸性
上的碳相连,受苯 2.与浓溴水发生取代反应生成沉淀
环影响能微弱电 3.遇 FeCl 3呈紫色
离。 4.易被氧化
HCHO 相当于两
1.与 H 2、 HCN 等加成为醇
个
2.被氧化剂 (O2、多伦试剂、斐林试剂、— CHO
酸性高锰酸钾等 )氧化为羧酸
有极性、能加成。
有极性、能加成
与 H2、 HCN 加成为醇
不能被氧化剂氧化为羧酸
受羰基影响,
1.具有酸的通性
2.酯化反应时一般断羧基中的碳氧单O— H 能电离出
键,不能被 H 2加成
H +,受羟基影响不
3.能与含—NH 2物质缩去水生成酰胺能被加成。
(肽键 )
酯基中的碳氧单 1.发生水解反应生成羧酸和醇
键易断裂 2.也可发生醇解反应生成新酯和新醇
不稳定易爆炸
一硝基化合物较一般不易被氧化剂氧化,但多硝基化
稳定合物易爆炸
— NH 2能以配位两性化合物
+
键结合 H;
— COOH 能部分
电离出 H+能形成肽键
肽键
蛋白 结构复杂 氨基 —NH 2
多肽链间有四级
质
不可用通式表示
羧基 酶
结构
— COOH
葡萄糖
1. 两性
2.水解
3. 变性
4.颜色反应 (生物催化剂)
5. 灼烧分解 1. 氧化反应 (还原性糖 )
多数可用下列通糖 式表示:
C n (H 2O) m
羟基 —OH
CH 2OH(CHOH) 醛基 — CHO 淀粉 (C 6H 10O 5) n
羰基 纤维素
[C 6 H 7O 2(OH) 3] n
4 CHO 多羟基醛或多
羟基酮或它们的缩合物
2.加氢还原
3.酯化反应
4.多糖水解
5.葡萄糖发酵分解生成乙醇
酯基中的碳氧单
酯基
油脂
键易断裂
可能有碳碳
烃基中碳碳双键
双键
能加成
1.水解反应
(皂化反应)
2.硬化反应
有机物的鉴别
鉴别有机物,必须熟悉有机物的性质(物理性质、化学性质),要抓住某些有机物的特征反应,选用合适的试剂,一一鉴别它们。
1 .常用的试剂及某些可鉴别物质种类和实验现象归纳如下:
试剂
酸性高锰 溴 水
银氨
新制
FeCl 3
酸碱
过量
碘水
Cu(OH) 2 NaHCO
3
名称
酸钾溶液
少量
饱和 溶液
溶液
指示剂
含碳碳双
含碳碳双
含醛基
含醛基化
被鉴别
化合物
羧酸
键、三键的 键、三键
合物及葡
物质种
苯酚 及葡萄
苯酚
(酚不能
物质、 烷基 的物质。
萄糖、果
淀粉
类
溶液
糖、果
溶液
羧酸
苯。但醇、 但醛有干 糖、麦芽
使酸碱指
糖、麦芽
示剂变色)
醛有干扰。 扰。
糖
糖
酸性高锰
溴水褪色 出现白 出现银 出现红 呈现 呈现蓝 使石蕊或
现象 酸钾紫红
放出无色
且分层
色沉淀 镜
色沉淀
紫色
色
甲基橙变
色褪色
无味气体
红
溴苯、氯苯归为卤代烃,不过水解是酚,不是醇啊。
硝基能被还原为氨基(铁粉还原)
有机物的鉴别 鉴别有机物,必须熟悉有机物的性质(物理性质、化学性质),要抓住某些有机物的特征反应,选用合适的试剂,一一鉴别它们。 1.常用的试剂及某些可鉴别物质种类和实验现象归纳如下: 试剂名称酸性高锰 酸钾溶液 溴水银氨 溶液 新制 Cu(OH)2 FeCl3 溶液 碘水 酸碱 指示剂 Na NaOH Na2CO3 NaHCO3 被鉴别物质种类含碳碳双 键、三键的 物质、烷基 苯。但醇、 醛有干扰。 含碳碳双 键、三键 的物质。 但醛有干 扰。 苯酚 溶液 含醛基 化合物 及葡萄 糖、果 糖、麦芽 糖 含醛基化 合物及葡 萄糖、果 糖、麦芽 糖 苯酚 溶液 淀粉 羧酸 (酚不能 使酸碱指 示剂变色) 羧酸 现象酸性高锰 酸钾紫红 色褪色 溴水褪色 且分层 出现白 色沉淀 出现银 镜 出现红 色沉淀 呈现 紫色 呈现 蓝色 使石蕊或 甲基橙变 红 放出无色 无味气体 溴苯、氯苯归为卤代烃,不过水解是酚,不是醇啊。硝基能被还原为氨基(铁粉还原) 类型概念举例(化学方程式) 反应 物类 属 取代反应分子里 某些原 子或原 子团被 其它原 子或原 子团所 代替 卤代反应 CH 4 + Cl 2 CH 3 Cl + HCl 烷烃、 环烃、 芳烃 硝化反应 芳烃、 苯酚 磺化反应 芳烃 酯化反应 酸、醇 分子间脱水 2C 2 H 5 OH C 2 H 5 OC 2 H 5 + H 2 O 醇 水解反应 CH 3 CH 2 X + H 2 O CH 3 CH 2 OH + HX 卤代 烃、酯
加成反应有机物 分子中 的双键 (或三 键)两 端的碳 原子与 其它原 子或原 子团直 接结合 生成新 的化合 物 加氢气 芳烃、 烯烃、 炔烃 加卤素 烯烃、 炔烃 加水 CH 2 =CH 2 + H 2 O CH 3 -CH 2 OH(工业制醇) CH 2 ≡CH 2 + H 2 O CH 3 -CHO(工业制醛) 烯烃、 炔烃 加卤代烃 CH≡CH + HCl CH 2 =CHCl 烯烃、 炔烃 加氢气 CH 3 CHO + H 2 CH 3 CH 2 OH 醛 聚合反应由相对 分子质 量小的 化合物 互相结 合成相 对分子 质量大 的高分 子化合 物 加聚反应 烯烃、 炔烃、 醛、酚 等 缩聚反应:生成高分子的同时还 有小分子 消去反应有机化 合物在 一定的 条件 下,从 一个分 子中脱 去一个 小分子 而生成 不饱和 (含双 键或三 键)的 分之内脱水 CH 3 CH 2 OH CH 2 =CH 2 ↑+ H 2 O 醇、 烃、卤 代烃 等 卤代烃脱卤化氢 CH 3 CH 2 CH 2 Br + NaOH CH 3 CH=CH 2 + NaBr + H 2 O 裂化(深度裂化也叫裂解) C 4 H 10 CH 4 + C 3 H 6
有机官能团及性质 【学习目标】 1.掌握常见的有机官能团的结构及性质。 2.能根据结构推导有机物的性质,能根据有机物的性质推导可能的结构。 【典型例题】 [例题1]在下列反应式中的括号里填上恰当的反应物 [例题2]吗丁啉是一种常见的胃药,其有效成分的结构简式可用下图表示。关于该物质的 下列说法不正确...的是( ) A 、该物质的分子式为C 22H 25ClN 5O 2 B 、该物质具有碱性,能与酸反应 C 、该物质能发生水解反应 D 、该物质能发生取代反应和加成反应 【课堂练习】 1.(多选) 下列物质中,不能与小苏打反应的是( ) A.甲酸 B.乙酸 C.碳酸 D.苯酚 2.(多选)将阿司匹林放入足量的NaOH 溶液中煮沸,能发生反应的化学键是( ) 3. 有机物(1)CHO )OH(CHOH CH 42(2)OH CH CH CH 223(3)=2CH OH CH CH 2 (4)32COOCH CH CH = (5)COOH CH CH 2=中,既能发生加成反应、酯化反 应,又能发生氧化反应的是( ) A .(3)(5) B .(1)(3)(5) C .(2)(4) D .(1)(3) 4.(多选)在烃分子中去掉2个氢原子形成一个双键是吸热反应,大约需 1mol kJ 125~117-?.的热量,但1,3-环己二烯失去2个氢原子变成苯是放热反应,反应 热1mol kJ 23.4-?,以上事实表明( ) A .1,3-环己二烯加氢是吸热反应 B .1,3-环己二烯比苯稳定 C .苯加氢生成环己烷是放热反应 D .苯比1,3-环己二烯稳定 5. 与醛基相邻的碳原子上的氢原子叫α—H ,无α—H 的醛在强碱作用下,发生分子间氧化 —还原反应生成酸和醇,叫做康尼查罗反应,例如+→+OH CH NaOH 2HCHO 3 HCOONa ,则下列化合物中不发生康尼查罗反应的是( ) ① ② ③ ④ A .①② B .①②④ C .③④ D .①②③④
1.酚羟基 (1)配位反应 具有酚羟基的药物在中性或弱酸条件下,与FeCl 3试液反应显色。 OH 3 中性或弱酸条件 O 3 Fe 3 如:对乙酰氨基酚显蓝紫色;苯乙胺类药物与FeCl 3试液反应显色,再加入碱性溶液,随即被高铁离子氧化而显紫色或紫红色。 在碱性条件下,Fe 3+与OH 反应成Fe (OH )3沉淀;强酸条件下,酚羟基以分子形式存在,不与Fe 3+反应。因此,规定在中性或弱酸条件下反应。 (2)弱还原性 具有酚羟基的苯乙胺类药物,可被碘、过氧化氢、铁氰化钾等氧化剂氧化而显色。 如肾上腺素在酸性条件下,被过氧化氢氧化显红色,放置可变为棕色多聚体;盐酸异丙肾上腺素在偏酸性条件下,被碘迅速氧化,再用硫代硫酸钠消退碘的颜色,溶液显淡红色。 2.芳伯氨基 具有芳伯氨基或潜在芳伯氨基的药物,均可发生重氮化-偶合反应生成有色的偶氮染料。 NH 2 2N N HO 如:贝诺酯反应后生成橙红色沉淀;苯佐卡因和盐酸普鲁卡因视供试品不同,生成橙黄到猩红色沉淀;对乙酰氨基酚加酸水解后,再发生重氮化-偶合反应,显红色。 3.羰基 含羰基的物质可与羰基试剂反应生成沉淀。 O R 1R 2 H 2NOH HCl NOH R 1R 2 白色肟类化合物 O R 1R C NNHR R 1R 2黄色腙类化合物 如黄体酮与异烟肼缩合生成黄色异烟腙。
4.脂肪胺及含N杂环 (1)与生物碱显色剂的反应 脂肪胺及含N显色 生物碱纯度不同,显色就有差别。常用的生物碱显色剂包括:Mandelin试剂(1%钒酸铵的浓硫酸溶液)、Frohde试剂(1%钼酸钠或5%钼酸铵的浓硫酸溶液)、Marquis试剂(30%甲醛溶液0.2ml与10ml浓硫酸混合)、浓硫酸、浓硝酸及浓盐酸。 如肾上腺素与甲醛-硫酸显红色;盐酸异丙肾上腺素与甲醛-硫酸显棕色至暗紫色; (2)与生物碱沉淀剂的反应 大多数生物碱类药物在酸性水溶液中,可与生物碱沉淀剂反应生成沉淀。常用的生物碱沉淀剂有碘化铋钾、碘化汞钾、碘-碘化钾(碘试液)、三硝基苯酚(苦味酸)、硅钨酸、二氯化汞、磷钨酸等。 如盐酸利多卡因与三硝基苯酚反应生成沉淀;盐酸布比卡因与三硝基苯酚反应,生成黄色沉淀;维生素B1与碘化汞钾反应生成淡黄色沉淀、与碘-碘化钾反应生成红色沉淀、与硅钨酸反应生成白色沉淀、与苦酮酸反应生成扇形白色结晶。 (3)亚硝基铁氰化钠反应 亚硝基铁氰化钠反应(Rimini试验)是脂肪伯胺的专属反应。如:重酒石酸间羟胺反应后显红紫色。 红紫色 亚硝基铁氰化钠又称硝普钠,化学式:Na2[Fe(CN)5NO]·2H2O,为强有力的血管扩张剂,用于高血压急症和在外科手术时产生控制性低血压,也用于急性心脏衰竭。亚硝基铁氰化钠与胺的反应称为Rimini试验,由E. Rimini于1898年发现,发生在硝普钠和C1-C4的脂肪伯胺、二乙胺或二戊胺之间。与脂肪伯胺的反应产生红色化合物,最低检出限量为50μg;与二级胺的反应则生成蓝色化合物。 5.酯基 (1)酯基水解 酯基水解本身无明显反应现象,一般利用水解产物的性质来鉴别。 如阿司匹林的鉴别:加碳酸钠水解后,再加过量的稀硫酸,即析出白色沉淀,并发生醋酸的臭气。
有机物官能团与性质[知识归纳] —R —OH 其中: 1、能使KMnO4褪色的有机物: 烯烃、炔烃、苯的同系物、醇、酚、醛、葡萄糖、麦芽糖、油脂 2、能使Br2水褪色的有机物:烯烃、炔烃、酚、醛、葡萄糖、麦芽糖、油脂 3、能与Na反应产生H2的有机物:醇、酚、羧酸、氨基酸、葡萄糖 4、具有酸性(能与NaOH、Na2CO3反应)的有机物:酚、羧酸、氨基酸 5、能发生银镜反应或与新制Cu(OH)2反应的有机物: 醛、甲酸{HCOOH}、甲酸盐、甲酸酯、葡萄糖、麦芽糖 6、既有氧化性,又有还原性的有机物:醛、烯烃、炔烃 7、能发生颜色(显色)反应的有机物: 苯酚遇FeCl3显紫色、淀粉遇I2变蓝、蛋白质遇浓硝酸变黄、葡萄糖遇Cu(OH)2显绛蓝 [有机合成的常规方法] 1.引入官能团: ①引入-X的方法:烯、炔的加成,烷、苯及其同系物的取代 ②引入-OH的方法:烯加水,醛、酮加氢,醛的氧化、酯的水解、卤代烃的水解、糖分解为乙醇和CO2 ③引入C=C的方法:醇、卤代烃的消去,炔的不完全加成,*醇氧化引入C=O 2.消除官能团 ①消除双键方法:加成反应 ②消除羟基方法:消去、氧化、酯化 ③消除醛基方法:还原和氧化 3.有机反应类型 常见的有机反应类型有取代(包括酯化、水解)、加成、加聚、消去、氧化、还原等。能够发生各种反应类型的常见物质如下: ①烷烃、芳香烃与X2的反应 (1)取代反应②羧酸与醇的酯化反应 C H 2 CH 2 C H COOH O O O O 33325 C H 2 CH 2 C H 2 CH O O C OCH 2 CH 2 O []n 32 CHO 1
2 ③酯的水解反应 ①不饱和烃与H 2、 X 2、HX (2)加成反应 的反应 ②醛与H 2的反应 {与H 2发生加成反应生成醇} (3)加聚反应:烯烃、炔烃在一定条件下的聚合反应。 (4)消去反应:某些醇在浓H 2SO 4作用下分子内脱水生成烯烃的反应。 (5)还原反应:含 C=C 、—C ≡C —、 有机物与H 2的加成反应。 ①任何有机物的燃烧 (6)氧化反应 ②KMnO 4与烯烃的反应 ③醇、醛的催化氧化 一.考点梳理 1.各类烃的衍生物的结构与性质 二.方法归纳 有机物中羟基(—OH )上的氢电离难易程度:羧酸>酚>醇 1.决定有机物的种类 有机物的分类依据有 组成、碳链、官能团 和同系物等。烃及烃的衍生物的分类依据有所不同,可由下列两表看出来。 烃的分类法: 烃的衍生物的分类法: 2.产生官能团的位置异构和种类异构 中学化学中有机物的同分异构种类有碳链异构、官能团位置异构和官能团的种类异构三种。对于同类有机物,由于官能团的位置不同而引起的同分异构是官能团的位置异构,如下面一氯乙烯的8种异构体就反映了碳碳双键及氯原子的不同位置所引起的异构。 对于同一种原子组成,却形成了不同的官能团,从而形成了不同的有机物类别,这就是官能团的种类异构。如:相同碳原子数的醛和酮,相同碳原子数的羧酸和酯,都是由于形成不同的官能团所造成的有机物种类不同的异构。 3.决定一类或几类有机物的化学性质 官能团对有机物的性质起决定作用,-X 、-OH 、-CHO 、-COOH 、-NO2、-SO3H 、-NH2、RCO-,这些官能团就决定了有机物中的卤代烃、醇或酚、醛、羧酸、硝基化合物或亚硝酸酯、磺酸类有机物、胺类、酰胺类的化学性质。因此,学习有机物的性质实际上是学习官能团的性质,含有什么官能团的有机物就应该具备这种官能团的化学性质,不含有这种官能团的有机物就不具备这种官能团的化学性质,这是学习有机化学特别要认识到的一点。例如,醛类能发生银镜反应,或被新制的氢氧化铜悬浊液所氧化,可以认为这是醛类较特征的反应;但这不是醛类物质所特有的,而是醛基所特有的,因此,凡是含有醛基的物质,如葡萄糖、甲酸及甲酸酯等都能发生银镜反应,或被新制的氢氧化铜悬浊液所氧化。 4.影响其它基团的性质 有机物分子中的基团之间存在着相互影响,这包括官能团对烃基的影响,烃基对官能团的影响,以及含有多官能团的物质中官能团之间的的相互影响。 ① 醇、苯酚和羧酸的分子里都含有羟基,故皆可与钠作用放出氢气,但由于所连的基团不同,在酸性上存在差异。 R-OH 中性,不能与NaOH 、Na2CO3反应;与苯环直接相连的羟基成为酚羟基,不于苯环直接相连的羟基成为醇羟基。 C6H5-OH 极弱酸性,比碳酸弱,但比HCO3-(碳酸氢根)要强。不能使指示剂变色,能与NaOH 反应。 苯酚还可以和碳酸钠反应,生成苯酚钠与碳酸氢钠; R-COOH 弱酸性,具有酸的通性,能与NaOH 、Na2CO3反应。 显然,羧酸中,羧基中的羰基的影响使得羟基中的氢易于电离。 ② 醛和酮都有羰基(>C=O),但醛中羰基碳原子连接一个氢原子,而酮中羰基碳原子上连接着烃基,故前者具有还原性,后者比较稳定,不为弱氧化剂所氧化。 ③ 同一分子内的原子团也相互影响。如苯酚,-OH 使苯环易于取代(致活),苯基使-OH 显示酸性(即电离出H+)。果糖中,多羟基影响羰基,可发生银镜反应。 由上可知,我们不但可以由有机物中所含的官能团来决定有机物的化学性质,也可以由物质的化学性质来判断它所含有的官能团。如葡萄糖能发生银镜反应,加氢还原成六元醇,可知具有醛基;能跟酸发生酯化生成葡萄糖五乙酸酯,说明它有五个羟基,故为多羟基醛。 5.有机物的许多性质发生在官能团上 有机化学反应主要发生在官能团上,因此,要注意反应发生在什么键上,以便正确地书写化学方程式。 乙酸 —C —H O
1、卤代烃 官能团:卤原子(-X)。 性质:在碱的溶液中发生“水解反应”,生成醇。在碱的醇溶液中发生“消去反应”,得到不饱和烃 2、醇 官能团,醇羟基(-0H)。 性质:能与钠反应,产生氢气能发生消去得到不饱和烃(与羟基相连的碳直接相连的 碳原子上如果没有氢原子,不能发生消去)③能与羧酸发生酯化反应④能被催化氧化成醛 (伯醇氧化成醛,仲醇氧化成酮,叔醇不能被催化氧化) 3、醛 官能团:醛基.(-CHO)O 性质:能与银氨溶液发生银镜反应能与新制的氢氧化铜溶液反应生成红色沉淀③能被氧化成羧酸④能被加氢还原成醇 4、酚 官能团:酚羟基(-0H) 性质:具有酸性能钠反应得到氢气酚羟基使苯环性质更活泼,苯环上易发生取代,酚 羟基在苯环上是邻对位定位基③能与羧酸发生酯化 5、羧酸 官能团:羧基(-COOH) 性质:具有酸性(一般酸性强于碳酸)能与钠反应得到氢气不能被还原成醛(注意是 “不能”)③能与醇发生酯化反应 6、酯 官能团:酯基(-COOR) 性质:能发生水解得到酸和醇醇、酚:羟基(-OH);伯醇羟基可以消去生成碳碳双键,酚羟基可以和NaOH反应生成水, 与Na2CO3反应生成NaHCO3,二者都可以和金属钠反应生成氢气 7.、醛
官能团:醛基(-CHO ); 性质: 可以发生银镜反应, 可以和斐林试剂反应氧化成羧基。③与氢气加成生成羟基。 8.、酮: 官能团:羰基(> C=O ); 性质:可以与氢气加成生成羟基。不能被高锰酸钾氧化。 9.、羧酸: 官能团:羧基(-COOH ); 反应生成水,与 NaHCO3、Na2CO3反应生成二氧化碳 酯化反应。 10、硝基化合物: 11、胺: 16、腈:官能团:氰基(-CN ) 性质: 酸性,与NaOH 官能团:硝基(-NO2); 性质:一定条件下,硝基可被还原为 -NH 2 官能团:氨基(-NH2). 性质:弱碱性 12、烯烃:官能团: 碳碳双键(> C=C <) 性质: 加成反应 能被高锰酸钾等强氧化剂氧化,使高锰酸钾溶液褪色 13、炔烃:官能团: 碳碳三键(-C 三C-) 性质: 加成反应 能被高锰酸钾等强氧化剂氧化,使高锰酸钾溶液褪色 14、醚:官能团:醚键( 毛-O-C 茅 性质:可以由醇羟基脱水形成。 15、磺酸:官能团:磺基(-SO3H ) 酸性,可由 浓硫酸取代生成
高中常见有机化合物结构与性质总结 物质类别特征结构(官能团)断键位置反应类型试剂条件反应产物烷烃取代X2,光照 烯烃 加成 X2的CCl4溶液 HX H2O,催化剂 加成,还原H2,催化剂 加聚一定条件 ——氧化酸性KMnO4溶液酸性KMnO4溶液褪色 炔烃或 加成 X2的CCl4溶液或 HX,催化剂,加热或加成,还原H2,催化剂或 ——氧化酸性KMnO4溶液酸性KMnO4溶液褪色 芳香烃 取代 X2,FeX3 HNO3,浓H2SO4,加热 加成3H2H2,Ni,加热 取代 HNO3,浓H2SO4,加热 C C H H C C C C X X C C X H C C OH H C C H X NO2 R R NO2 NO2 O2N R H H H C H H C H H C H X C H X C X X C X X C C H H C C H X C C X X C C C C C C C C H C X C C ]n [ C
氧化 酸性KMnO 4溶液 卤代烃 —X 取代 NaOH 水溶液(催),加热 消去 NaOH 乙醇溶液(催), 加热 醇 —OH 取代、置换 Na 取代、酯化 羧酸—COOH ,浓H 2SO 4,加热 氧化 O 2,Cu ,加热 取代 浓HX 溶液,加热 消去 浓H 2SO 4,加热 —CH 2—OH —— 氧化 酸性KMnO 4溶液(或酸性K 2Cr 2O 7溶液) —COOH 酚 取代 溴水 取代、置换 Na 中和 NaOH 溶液 —— 氧化 空气 —— 醛 氧化 O 2,催化剂,加热 (或银氨溶液, 或新制 Cu(OH)2 浊液) 羧 加成、还原 H 2,催化剂,加热 羧酸 取代、置换 Na 中和 NaOH 溶液 取代、酯化 醇,浓H 2SO 4,加热 O H ONa OH OH H H H OH Br Br Br C H C H COOH O C H ONa C O O C C C C X C O C H H H C O OH C C OH C H O C O H ONa C O OH C O O C R O OH C O H C OH H H C O H C O OH C O C O H C C X C OH C C C X H
有机物官能团与性质 [知识归纳] —R —OH 其中: 1、能使KMnO4褪色的有机物: 烯烃、炔烃、苯的同系物、醇、酚、醛、葡萄糖、麦芽糖、油脂 2、能使Br2水褪色的有机物:烯烃、炔烃、酚、醛、葡萄糖、麦芽糖、油脂 3、能与Na反应产生H2的有机物:醇、酚、羧酸、氨基酸、葡萄糖 4、具有酸性(能与NaOH、Na2CO3反应)的有机物:酚、羧酸、氨基酸 5、能发生银镜反应或与新制Cu(OH)2反应的有机物: 醛、甲酸、甲酸盐、甲酸酯、葡萄糖、麦芽糖 6、既有氧化性,又有还原性的有机物:醛、烯烃、炔烃 7、能发生颜色(显色)反应的有机物:
[有机合成的常规方法] 1.引入官能团: ①引入-X 的方法:烯、炔的加成,烷、苯及其同系物的取代 ②引入-OH 的方法:烯加水,醛、酮加氢,醛的氧化、酯的水解、卤代烃的水解、糖分解为乙醇和CO 2 ③引入C=C 的方法:醇、卤代烃的消去,炔的不完全加成,*醇氧化引入C=O 2.消除官能团 ①消除双键方法:加成反应 ②消除羟基方法:消去、氧化、酯化 ③消除醛基方法:还原和氧化 3.有机反应类型 常见的有机反应类型有取代(包括酯化、水解)、加成、加聚、消去、氧化、还原等。能够发生各种反应类型的常见物质如下: ①烷烃、芳香烃与X 2的反应 (1)取代反应 ②羧酸与醇的酯化反应 ③酯的水解反应 ①不饱和烃与H 2、X 2、HX (2)加成反应 的反应 ②醛与H 2的反应 (3)加聚反应:烯烃、炔烃在一定条件下的聚合反应。 C H COOH O O O O C H 2CH 2Br Br C H 2CH O O C OCH 2CH 2O C []n CHO
红外波谱 分子被激发后,分子中各个原子或基团(化学键)都会产生特征的振动,从而在特点的位置会出现吸收。相同类型的化学键的振动都是非常接近的,总是在某一范围内出现。 常见官能团的红外吸收频率 整个红外谱图可以分为两个区,4000~1350区是由伸缩振动所产生的吸收带,光谱比较简单但具有强烈的特征性,1350~650处指纹区。
通常,4000~2500处高波数端,有与折合质量小的氢原子相结合的官能团O-H, N-H, C-H, S-H 键的伸缩振动吸收带,在2500-1900波数范围内常常出现力常数大的三件、累积双键如:- C≡C-,- C≡N, -C=C=C-, -C=C=O, -N=C=O等的伸缩振动吸收带。在1900以下的波数端有-C=C-, -C=O, -C=N-, -C=O等的伸缩振动以及芳环的骨架振动。 1350~650指纹区处,有C-O, C-X的伸缩振动以及C-C的骨架振动,还有力常数较小的弯曲振动产生的吸收峰,因此光谱非常复杂。该区域各峰的吸收位置受整体分子结构的影响较大,分子结构稍有不同,吸收也会有细微的差别,所以指纹区对于用已知物来鉴别未知物十分重 要。
有机化学有机化合物红外吸收光谱 σ伸缩振动,δ面内弯曲振动,γ面外弯曲振动 一、烷烃 饱和烷烃IR光谱主要由C-H键的骨架振动所引起,而其中以C-H键的伸缩振动最为有用。在确定分子结构时,也常借助于C-H键的变形振动和C-C键骨架振动吸收。烷烃有下列四种振动吸收。 1、σC-H在2975—2845 cm-1范围,包括甲基、亚甲基和次甲基的对称与不对称伸缩振动 2、δC-H在1460 cm-1和1380 cm-1处有特征吸收,前者归因于甲基及亚甲基C-H 的σas,后者归因于甲基C-H的σs。1380 cm-1峰对结构敏感,对于识别甲基很有用。共存基团的电负性对1380 cm-1峰位置有影响,相邻基团电负性愈强,愈移向高波数区,例如,在CH3F中此峰移至1475 cm-1。 异丙基1380 cm-1裂分为两个强度几乎相等的两个峰1385 cm-1、1375 cm-1 叔丁基1380 cm-1裂分1395 cm-1、1370cm-1两个峰,后者强度差不多是前者的两倍,在1250 cm-1、1200 cm-1附近出现两个中等强度的骨架振动。 3、σC-C在1250—800 cm-1范围内,因特征性不强,用处不大。 4、γC-H分子中具有—(CH2)n—链节,n大于或等于4时,在722 cm-1有一个弱吸收峰,随着CH2个数的减少,吸收峰向高波数方向位移,由此可推断分子链的长短。 二、烯烃 烯烃中的特征峰由C=C-H键的伸缩振动以及C=C-H键的变形振动所引起。烯烃分子主要有三种特征吸收。 1、σC=C-H 烯烃双键上的C-H键伸缩振动波数在3000 cm-1以上,末端双键氢 C=CH2 在3075—3090 cm-1有强峰最易识别。 2、σC=C 吸收峰的位置在1670—1620 cm-1。随着取代基的不同,σC=C吸收峰的位置有所不同,强度也发生变化。 3、δC=C-H烯烃双键上的C-H键面内弯曲振动在1500—1000 cm-1,对结构不敏感,用途较少;而面外摇摆振动吸收最有用,在1000—700 cm-1范围内,该振动对结构敏感,其吸收峰特征性明显,强度也较大,易于识别,可借以判断双键取
苏教版高二有机化学官能团性质整理 分类:烷、烯、炔、苯、卤化烃、醇、酚、醚、醛、酮、羧酸、酯、氨基酸由结构(官能团)推测性质: 能发生取代反应的有:-C n H 2n-1 、苯环、-X、-OH、-COOH、-COO-(酯基) 其中:能酯化的有:-OH、-COOH 能水解的有:-X、-COO-(酯基) 苯环上的取代:①苯及其同系物:与液溴反应,FeBr 3 作催化剂②酚类:与浓溴水反应 能发生加成反应的有:苯环、C=C、C≡C、-CHO、羰基(后三个主要是与H 2 加成) 其中:能加聚的有: C=C、C≡C、(-CHO、羰基) 能发生消去反应的有:-X(β-C上有H)、-OH(β-C上有H) 能发生氧化反应的有:醇-OH(α-C上有H)、酚-OH、-CHO、C=C、C≡C、R-C 6H 5 (R为烃基;直 接与苯环相连的C上有H)燃烧除外(大部分有机物都能燃烧,均为氧化反应) 能与酸性高锰酸钾反应(使其褪色)的有:同上 能发生还原反应的有:苯环、C=C、C≡C、-CHO、羰基(以上均为上氢还原,属加成反应) 能与H 2 反应的有:同上 能与溴水反应的有:C=C、C≡C、酚类(苯环上-OH的邻、对位上至少有一个位置有H)、-CHO 能与Na反应的有:醇-OH、酚-OH、-COOH 能与NaOH反应的有:酚-OH、-COOH 能与Na 2CO 3 反应的有:酚-OH、-COOH 能与NaHCO 3 反应的有: -COOH 体现酸性的有:酚-OH(不能使指示剂变色)、-COOH(可使指示剂变色) 体现碱性的有:-NH 2 能与FeCl 3 反应的有:酚-OH 附下表
苏教版高二有机化学官能团性质整理
类别通式官能团代表物分子结构结点主要化学性质 卤代烃一卤代烃: R—X 多元饱和卤代烃: C n H2n+2-m X m 卤原子 —X C2H5Br (Mr:109) 卤素原子直接与烃基 结合 β-碳上要有氢原子才 能发生消去反应 1.与NaOH水溶液共热发生取代(水 解)反应生成醇 2.与NaOH醇溶液共热发生消去反应 生成烯 3.在碱性条件下,水解更彻底,若卤 原子与苯环相连,则难水解 醇一元醇: R—OH 饱和多元醇: C n H2n+2O m 醇羟基 —OH CH3OH (Mr:32) C2H5OH (Mr:46) 羟基直接与链烃基结 合,O—H及C—O 均有极性。 β-碳上有氢原子才能 发生消去反应。 α-碳上有氢原子才能 被催化氧化,伯醇氧 化为醛,仲醇氧化为 酮,叔醇不能被催化 氧化。 1.跟活泼金属反应产生H2 2.跟卤化氢或浓氢卤酸发生取代反应 生成卤代烃 3.脱水反应:存在浓H2SO4 140℃分子间脱水成醚 170℃分子内脱水生成烯 4.催化氧化为醛或酮 5.去掉氢,发生酯化反应 6.能被重铬酸钾酸性溶液氧化,由橙 红色变为绿色 醚R—O—R′醚键C2H5O C2H5 (Mr:74) C—O键有极性 性质稳定,一般不与酸、碱、氧化剂 反应 酚C n H n O 酚羟基 —OH (Mr:94)C6H5OH —OH直接与苯环上 的碳相连,受苯环影 响能微弱电离。 1.弱酸性,比碳酸还弱 2.与浓溴水发生取代反应生成白色沉 淀,在浓H2SO4存在下,可与硝酸 生成三硝基苯酚 3.遇FeCl3呈紫色 4.易被氧化 醛C n H2n O 醛基 HCHO (Mr:30) (Mr:44)CH3CHO HCHO相当于两个 —CHO 有极性、能加成 1.与H2、HCN等加成为醇 2.被氧化剂(O2、多伦试剂、斐林试剂、 酸性高锰酸钾溴水等)氧化为羧酸 3.能发生银镜反应,能与新制的氢 氧化铜悬浊液反应 酮CnH2n O 羰基(Mr:58) CH3COCH3 有极性、能加成 与H2、HCN加成为醇 不能被氧化剂氧化为羧酸 羧酸C n H2n O2羧基(Mr:60)CH3COOH (醋酸乙酸) 受羰基影响,O—H能 电离出H+,受羟基影 响不能被加成。 1.具有酸的通性 2.酯化反应时脱去羟基,不能被H2 加成 3.能与含—NH2物质缩去水生成酰胺 (肽键) 4.醋酸能使苯酚钠变浑浊 5.甲酸既有酸的性质,又有醛的性质 酯C n H2n O2酯基HCOOCH3 (Mr:60) 酯基中的碳氧单键易 断裂 1.发生水解反应生成羧酸和醇 2.也可发生醇解反应生成新酯和新醇 硝酸酯RONO2硝酸酯基 —ONO2 不稳定易爆炸 硝基化合 物R—NO2硝基—NO2一硝基化合物较稳定 一般不易被氧化剂氧化,但多硝基化 合物易爆炸 氨基酸RCH(NH)COOH 氨基—NH2 羧基 H2NCH2COOH —NH2能以配位键结 合H+;—COOH能部 两性化合物
常见有机物及官能团的性质总结 1。卤化烃:官能团,卤原子。 (1)在碱的水溶液中发生“水解反应”,生成醇。 (2)在碱的醇溶液中发生“消去反应”,得到不饱和烃 2。醇:官能团,醇羟基。 (1)能与钠反应,产生氢气。 (2)在浓硫酸作用下,加热到170度能发生分子内的脱水,消去得到不饱和烃(与羟基相连的碳直接相连的碳原子上如果没有氢原子,不能发生消去), (3)加热到140度能发生分子间的脱水生成醚。 (4)能与羧酸发生酯化反应。 (5)能被催化氧化成醛(伯醇氧化成醛,仲醇氧化成酮,叔醇不能被催化氧化) 3。醛:官能团,醛基。 (1)能与银氨溶液发生银镜反应 (2)能与新制的氢氧化铜溶液反应生成红色沉淀 (3)能被氧化成羧酸 (4)能被加氢还原成醇 4。酚,官能团,酚羟基。 (1)具有酸性能钠反应得到氢气
(2)酚羟基使苯环性质更活泼,苯环上易发生取代,酚羟基在苯环上是邻对位定位基,(以苯酚与溴的取代反应为例) (3)能与羧酸发生酯化 5。羧酸,官能团,羧基。 (1)具有酸性(一般酸性强于碳酸)能与钠反应得到氢气。 (2)能与醇发生酯化反应 **不能被还原成醛(注意是“不能”) 6。酯,官能团,酯基。 (1)能发生水解得到酸和醇 醇、酚:羟基(-OH);伯醇羟基可以消去生成碳碳双键,酚羟基可以和NaOH反应生成水,与Na2CO3反应生成NaHCO3,二者都可以和金属钠反应生成氢气 醛:醛基(-CHO);可以发生银镜反应,可以和斐林试剂反应氧化成羧基。与氢气加成生成羟基。 酮:羰基(>C=O);可以与氢气加成生成羟基 羧酸:羧基(-COOH);酸性,与NaOH反应生成水,与NaHCO3、Na2CO3反应生成二氧化碳 硝基化合物:硝基(-NO2); 胺:氨基(-NH2).弱碱性 烯烃:双键(>C=C<)加成反应。 炔烃:三键(-C≡C-)加成反应 醚:醚键(-O-)可以由醇羟基脱水形成
一、烷烃——无官能团: 1、一般C4及以下是气态,C5以上为液态。 2、化学性质稳定,不能使酸性高锰酸钾溶液(氧化)、溴水等褪色。 3、可以和卤素(如液溴、氯气)发生取代反应,生成卤代烃和相应的卤化氢,条件:光照 4、烷烃在高温下可以发生裂解,例如甲烷在高温下裂解为碳和氢气。 二、烯烃——官能团:碳碳双键 1、性质或拨,可使酸性高锰酸钾溶液褪色,可使溴水或溴的四氯化碳溶液褪色(加成,生成二溴代烷)。 2、酸催化下和水加成生成醇,如乙烯在浓硫酸催化下和水加成生成乙醇。 3、烯烃加成符合马氏规则,氢一般加在氢多的那个C上。 4、乙烯在银或铜等催化下可以被空气氧化为环氧乙烷。 5、烯烃可以在镍等催化剂存在下和氢气加成生成烷烃。 6、烯烃可以发生加聚反应生成高聚物,如聚乙烯、聚丙烯、聚苯乙烯等。 7、实验室制乙烯通过乙醇在浓硫酸作用下脱水生成,条件170℃。 三、炔烃——官能团:碳碳三键 1、性质与烯烃相似,主要发生加成反应。也可以让高锰酸钾,溴水等褪色。 2、炔烃加水生成的产物为稀醇,稀醇不稳定,会重排成醛或酮。如乙炔加水生成乙烯醇,乙烯醇不稳定会重排成乙醛。 3、乙炔和氯化氢加成的产物为氯乙烯,加聚反应后得到聚氯乙烯。 4、炔烃加成同样符合马氏规则。 5、实验室制乙炔主要通过电石水解制得(用的饱和食盐水)。 四、芳香烃——含有苯环的烃 1、苯的性质很稳定,类似烷烃,不与酸性高锰酸钾溶液,溴的四氯化碳反应,但可与溴水发生萃取(物理反应)。 2、苯可以发生一系列取代反应,主要有: 和氯,溴等卤素取代,生成氯苯或溴苯等相应的卤化烃(条件:液溴、铁或三溴化铁催化,不可用溴水)。 和浓硝酸,浓硝酸的混合物发生硝化反应,生成硝基苯和水。条件:加热。 和浓硫酸反应生成苯磺酸,条件:加热。 3、苯可以加氢生成环己烷。 4、苯的同系物的性质不同,取代基性质活波,只要和苯环直接相连的碳上有氢,就可以被酸性高锰酸钾溶液氧化为苯甲酸。如甲苯可以使酸性高锰酸钾溶液褪色,被氧化为苯甲酸。无论取代基有多长,氧化产物都为苯甲酸。 5、苯分子中所有原子都在同一平面上。 6、苯环中不存在碳碳双键,六个碳原子之间的键完全相同。是一种特殊的大π键。 五、卤代烃——官能团:卤素原子 1、全部难溶于水,除一氯甲烷,一溴甲烷为气体外,其余均为液体或固体。 2、卤代烃可在碱性的水溶液中水解,生成醇。如溴乙烷在氢氧化钠水溶液中水解,生成乙醇。 3、卤代烃可以在氢氧化钠醇溶液中发生消去反应,生成烯烃,前提是卤素原子连接的碳原
高中有机化学中各种官能团的性质 1。卤化烃:官能团,卤原子在碱的溶液中发生“水解反应”,生成醇在碱的醇溶液中发生“消去反应”,得到不饱和烃 2。醇:官能团,醇羟基能与钠反应,产生氢气能发生消去得到不饱和烃(与羟基相连的碳直接相连的碳原子上如果没有氢原子,不能发生消去)能与羧酸发生酯化反应能被催化氧化成醛(伯醇氧化成醛,仲醇氧化成酮,叔醇不能被催化氧化) 3。醛:官能团,醛基能与银氨溶液发生银镜反应能与新制的氢氧化铜溶液反应生成红色沉淀能被氧化成羧酸能被加氢还原成醇 4。酚,官能团,酚羟基具有酸性能钠反应得到氢气酚羟基使苯环性质更活泼,苯环上易发生取代,酚羟基在苯环上是邻对位定位基能与羧酸发生酯化 5。羧酸,官能团,羧基具有酸性(一般酸性强于碳酸)能与钠反应得到氢气不能被还原成醛(注意是“不能”)能与醇发生酯化反应 6。酯,官能团,酯基能发生水解得到酸和醇 醇、酚:羟基(-OH);伯醇羟基可以消去生成碳碳双键,酚羟基可以和NaOH反应生成水,与Na2CO3反应生成NaHCO3,二者都可以和金属钠反应生成氢气 醛:醛基(-CHO);可以发生银镜反应,可以和斐林试剂反应氧化成羧基。与氢气加成生成羟基。 酮:羰基(>C=O);可以与氢气加成生成羟基
羧酸:羧基(-COOH);酸性,与NaOH反应生成水,与NaHCO3、Na2CO3反应生成二氧化碳 硝基化合物:硝基(-NO2); 胺:氨基(-NH2). 弱碱性 烯烃:双键(>C=C<)加成反应。 炔烃:三键(-C≡C-)加成反应 醚:醚键(-O-)可以由醇羟基脱水形成 磺酸:磺基(-SO3H)酸性,可由浓硫酸取代生成 腈:氰基(-CN) 酯: 酯(-COO-) 水解生成羧基与羟基,醇、酚与羧酸反应生成 注: 苯环不是官能团,但在芳香烃中,苯基(C6H5-)具有官能团的性质。苯基是过去的提法,现在都不认为苯基是官能团 官能团:是指决定化合物化学特性的原子或原子团. 或称功能团。 卤素原子、羟基、醛基、羧基、硝基,以及不饱和烃中所含有碳碳双键和碳碳叁键等都是官能团,官能团在有机化学中具有以下5个方面的作用。 1.决定有机物的种类 有机物的分类依据有组成、碳链、官能团和同系物等。烃及烃的衍生物的分类依据有所不同,可由下列两表看出来。
有机物官能团的性质【学习目标】 1、掌握各类官能团的书写和基本性质 2、掌握各官能团之间的转化关系初步学会设计合理的有机合成路线。学习重点:官能团的性质和转化。 学习难点:官能团的性质和转化。 【学习过程】 一、知识准备 1、各类官能团的结构和主要化学性质
酯基 二、某些官能团(或结构)的共性 1、能和氢气发生加成: 2、能使溴水褪色(发生反应): 3、能使酸性高锰酸钾溶液褪色: 例1、白藜芦醇的结构简式如图所示, ⑴白藜芦醇中的官能团为 ; ⑵白藜芦醇的分子式为 ; ⑶1mol 白藜芦醇最多能和 molH 2反应,1mol 白藜 芦醇最多能消耗 molBr 2,1mol 白藜芦醇最多消耗 molNaOH 。 例2、香草醛是一种食品添加剂,可由愈创木酚作原料合成,合成路线如下图所示。 ⑴中间产物③中官能团的名称为 。 ⑵①→②的反应类型为 ,香草醛的分子式为 。 ⑶在氢氧化钠溶液中,②③分别消耗NaOH 物质的量之比为 ,分别和金属钠反应,②③分别消耗NaOH 的物质的量之比为 ,化合物③和H 2反应时, OCH 3OH OCH 3 COOH HO OCH 3 COOH O OH OCH 3 CHO ① ② ③ ④ 香草醛 愈创木酚 H + -CO 2 O 2 OH - COOH CHO
最多消耗 molH 2。 ⑷化合物②在浓硫酸的作用下能发生反应,形成一个具有3个六元环的有机物⑤,写出⑤ 的结构简式 。 例3、化合物Ⅲ是合成中药黄芩中的主要活性成分的中间体,合成方法如下: Cl OH O H 3CO H 3CO H 3CO H O H 3CO H 3CO H 3CO O + 一定条件 I II III +HCl ⑴I 的分子式为 ; ⑵Ⅱ中官能团的名称为 ; ⑶Ⅱ中最多有 个原子共平面; ⑷写出Ⅱ与NaOH 溶液反应的化学方程式 ; ⑸1mol 产物III 与足量的氢气反应,消耗H 2的物质的量为 ,与足量溴水反应,消耗Br 2的物质的量为 。 例4、CPAE 是蜂胶的主要活性成分,由咖啡酸合成 CPAE 路线如下: ⑴咖啡酸的分子式为 ,1mol 咖啡酸最多消耗 molNaOH 。 ⑵写出苯乙醇在浓硫酸加热条件下发生反应的化学方程式 。 ①A 是苯乙醇的相邻同系物,写出A 结构简式 。 ②B 与苯乙醇互为同分异构体,能与NaOH 反应,苯环上的一溴代物只有两种,写出符
高中常见官能团及其性质(详细版) 一、烷烃——无官能团: 1、一般C4及以下是气态, C5以上为液态。 2、化学性质稳定, 不能使酸性高锰酸钾溶液(氧化) 、溴水等褪色。 3、可以和卤素(如液溴、氯气)发生取代反应,生成卤代烃和相应的卤化氢,条件:光照 4、烷烃在高温下可以发生裂解,例如甲烷在高温下裂解为碳和氢气。 二、烯烃——官能团:碳碳双键 1、性质或拨, 可使酸性高锰酸钾溶液褪色,可使溴水或溴的四氯化碳溶液褪色(加成,生成二溴代烷) 。 2、酸催化下和水加成生成醇,如乙烯在浓硫酸催化下和水加成生成乙醇。 3、烯烃加成符合马氏规则,氢一般加在氢多的那个C 上。 4、乙烯在银或铜等催化下可以被空气氧化为环氧乙烷。 5、烯烃可以在镍等催化剂存在下和氢气加成生成烷烃。 6、烯烃可以发生加聚反应生成高聚物,如聚乙烯、聚丙烯、聚苯乙烯等。 7、实验室制乙烯通过乙醇在浓硫酸作用下脱水生成,条件170℃。 三、炔烃——官能团:碳碳三键 1、性质与烯烃相似,主要发生加成反应。也可以让高锰酸钾,溴水等褪色。 2、炔烃加水生成的产物为稀醇,稀醇不稳定,会重排成醛或酮。如乙炔加水生成乙烯醇, 乙烯醇不稳定会重排成乙醛。 3、乙炔和氯化氢加成的产物为氯乙烯,加聚反应后得到聚氯乙烯。 4、炔烃加成同样符合马氏规则。 5、实验室制乙炔主要通过电石水解制得(用的饱和食盐水) 。 四、芳香烃——含有苯环的烃 1、苯的性质很稳定,类似烷烃, 不与酸性高锰酸钾溶液,溴的四氯化碳反应, 但可与溴水发生萃取(物理反应) 。 2、苯可以发生一系列取代反应,主要有: 和氯, 溴等卤素取代, 生成氯苯或溴苯等相应的卤化烃(条件:液溴、铁或三溴化铁催化, 不可用溴水) 。 和浓硝酸,浓硝酸的混合物发生硝化反应,生成硝基苯和水。条件:加热。 和浓硫酸反应生成苯磺酸,条件:加热。 3、苯可以加氢生成环己烷。 4、苯的同系物的性质不同,取代基性质活波,只要和苯环直接相连的碳上有氢,就可以被酸性高锰酸钾溶液氧化为苯甲酸。如甲苯可以使酸性高锰酸钾溶液褪色,被氧化为苯甲酸。无论取代基有多长,氧化产物都为苯甲酸。 5、苯分子中所有原子都在同一平面上。 6、苯环中不存在碳碳双键,六个碳原子之间的键完全相同。是一种特殊的大π键。 五、卤代烃——官能团:卤素原子 1、全部难溶于水,除一氯甲烷,一溴甲烷为气体外,其余均为液体或固体。 2、卤代烃可在碱性的水溶液中水解,生成醇。如溴乙烷在氢氧化钠水溶液中水解,生成乙醇。 3、卤代烃可以在氢氧化钠醇溶液中发生消去反应,生成烯烃,前提是卤素原子连接的碳原 子的相邻碳原子上有氢。 4、卤代烃通常通过醇和卤化氢在酸催化下发生取代反应制备。如乙醇在氢溴酸中,用浓硫酸催化制得溴乙烷。
高中化学所有有机化学的官能团性质,反应类型,引入官能团,反应条件 一、卤基(卤原子):水解也称取代(氢氧化钠溶液),消去(氢氧化钠醇溶液) 酚羟基:显色(Fecl3) 羧基:与醇发生酯化(浓硫酸加热)还原(+H2)中与 醇羟基:酯化,取代,消去 CC双键与叁建:加成,聚合反应(加聚) 羰基:银镜 酯基:水解(生成醇与羧酸) 苯基:加成,取代,磺化,硝化 都能发生氧化反应(+O2点燃) 同时带羟基与羧基的化合物还能发生缩聚 取代反应:有机物分子里的某些原子或原子团被其她原子或原子团所代替的反应。 加成反应:有机物分子里不饱与的碳原子跟其她原子或原子团直接结合的反应。 聚合反应:一种单体通过不饱与键相互加成而形成高分子化合物的反应。 加聚反应:一种或多种单体通过不饱与键相互加成而形成高分子化合物的反应。 消去反应:从一个分子脱去一个小分子(如水、卤化氢),因而生成不饱与化合物的反应。 氧化反应:有机物得氧或去氢的反应。 还原反应:有机物加氢或去氧的反应。 酯化反应:醇与酸起作用生成酯与水的反应。 水解反应:化合物与水反应生成两种或多种物质的反应(有卤代烃、酯、糖等) 1、氧化反应:有机物得氧或去氢的反应。甲烷燃烧CH4+2O2→CO2+2H2O(条件为点燃) 甲烷隔绝空气高温分解甲烷分解很复杂,以下就是最终分解。CH4→C+2H2(条件为高温高压,催化剂) 乙烯燃烧 CH2=CH2+3O2→2CO2+2H2O(条件为点燃) 乙炔燃烧C2H2+3O2→2CO2+H2O (条件为点燃) 苯燃烧 2C6H6+15O2→12CO2+6H2O (条件为点燃) 乙醇完全燃烧的方程式C2H5OH+3O2→2CO2+3H2O (条件为点燃) 乙醇的催化氧化的方程式2CH3CH2OH+O2→2CH3CHO+2H2O(条件为催化剂)(这就是总方程式) 2、取代反应:有机物分子里的某些原子或原子团被其她原子或原子团所代替的反应。 甲烷与氯气发生取代反应CH4+Cl2→CH3Cl+HCl CH3Cl+Cl2→CH2Cl2+HCl CH2Cl2+Cl2→CHCl3+HCl CHCl3+Cl2→CCl4+HCl (条件都为光照。 ) 苯与液溴的取代C6H6+Br2→C6H5Br+HBr 苯与浓硫酸浓硝酸 C6H6+HNO3→C6H5NO2+H2O (条件为浓硫酸) 实验室制甲烷CH3COONa+NaOH→Na2CO3+CH4(条件就是CaO 加热) 3 加成反应:有机物分子里不饱与的碳原子跟其她原子或原子团直接结合的反应。 乙烯与溴水CH2=CH2+Br2→CH2Br-CH2Br 乙烯与水CH2=CH2+H20→CH3CH2OH (条件为催化剂) 乙烯与氯化氢CH2=CH2+HCl→CH3-CH2Cl 乙烯与氢气CH2=CH2+H2→CH3-CH3 (条件为催化剂) 乙炔与溴水C2H2+2Br2→C2H2Br4 乙炔与氯化氢两步反应:C2H2+HCl→C2H3Cl--------C2H3Cl+HCl→C2H4Cl2 乙炔与氢气两步反应:C2H2+H2→C2H4→C2H2+2H2→C2H6 (条件为催化剂) 苯与氢气C6H6+3H2→C6H12 (条件为催化剂) 4、聚合反应:一种单体通过不饱与键相互加成而形成高分子化合物的反应。 乙烯聚合nCH2=CH2→-[-CH2-CH2-]n- (条件为催化剂) 氯乙烯聚合nCH2=CHCl→-[-CH2-CHCl-]n- (条件为催化剂)