质 谱 分 析 练习题
1、 有机质谱的分析原理及其能提供的信息是什么?
2、 以单聚焦质谱仪为例,说明质谱仪的组成,各主要部件的作用及原理。
3、 有机质谱图的表示方法有哪些?是否谱图中质量数最大的峰就是分子离子峰,为什么?
4、 同位素峰的特点是什么?如何在谱图中识别同位素峰?
5、谱图解析的一般原则是什么?
6、有机化合物在离子源中有可能形成哪些类型的离子?从这些离子的质谱峰中可以得到一些什么信息?
7、某化合物相对分子量为116。其离子峰m/e 57(100)、43(27)、29(57)
A. (CH 3)2CHCO 2C 2H 5
B. C 2H 5CO 2(CH 2)2CH 3
C. CH 3(CH 2)2CO 2CH 3
以上三个酯,哪个是该化合物?
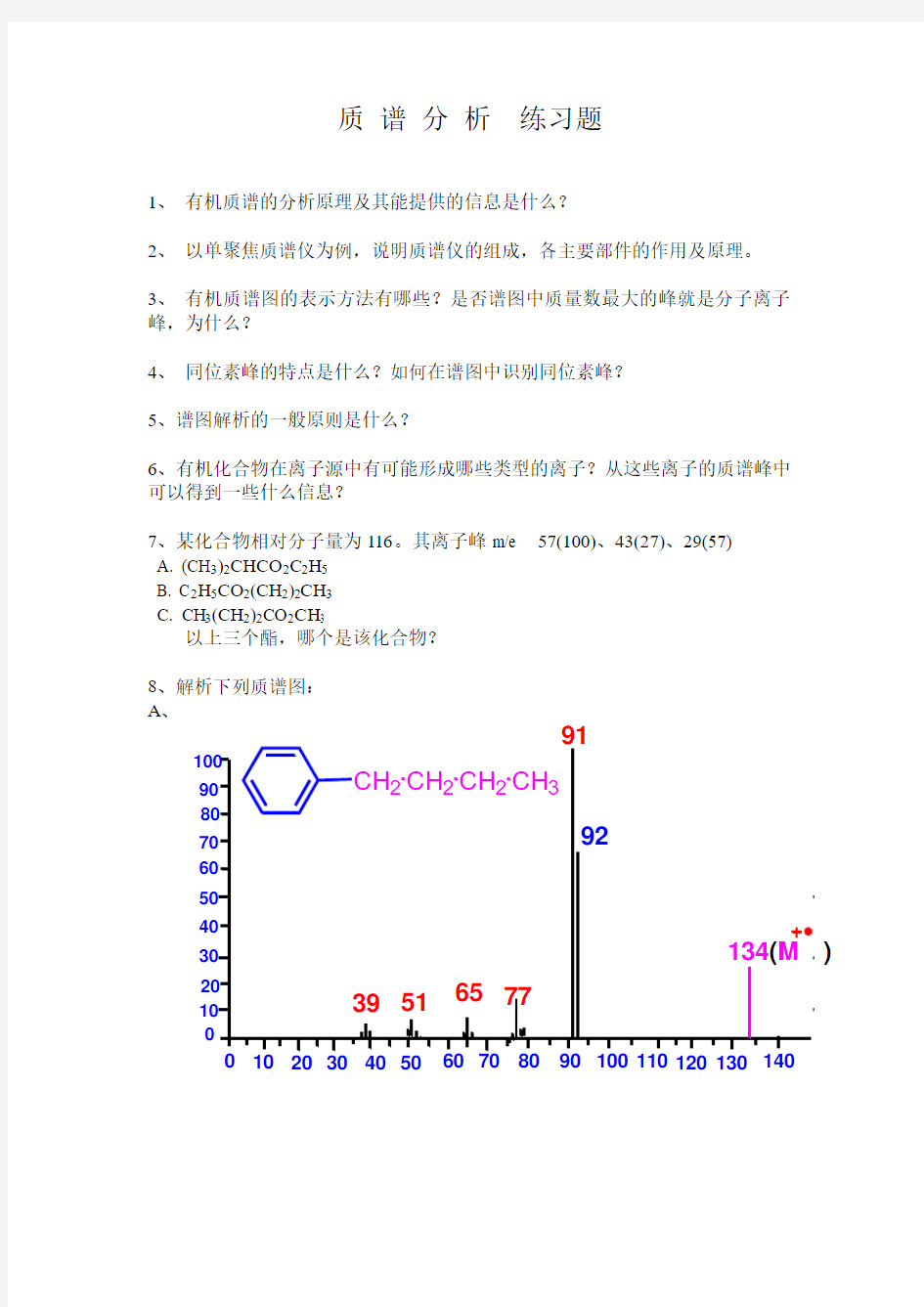
8、解析下列质谱图:
A 、
0% O F B A S E P E A K
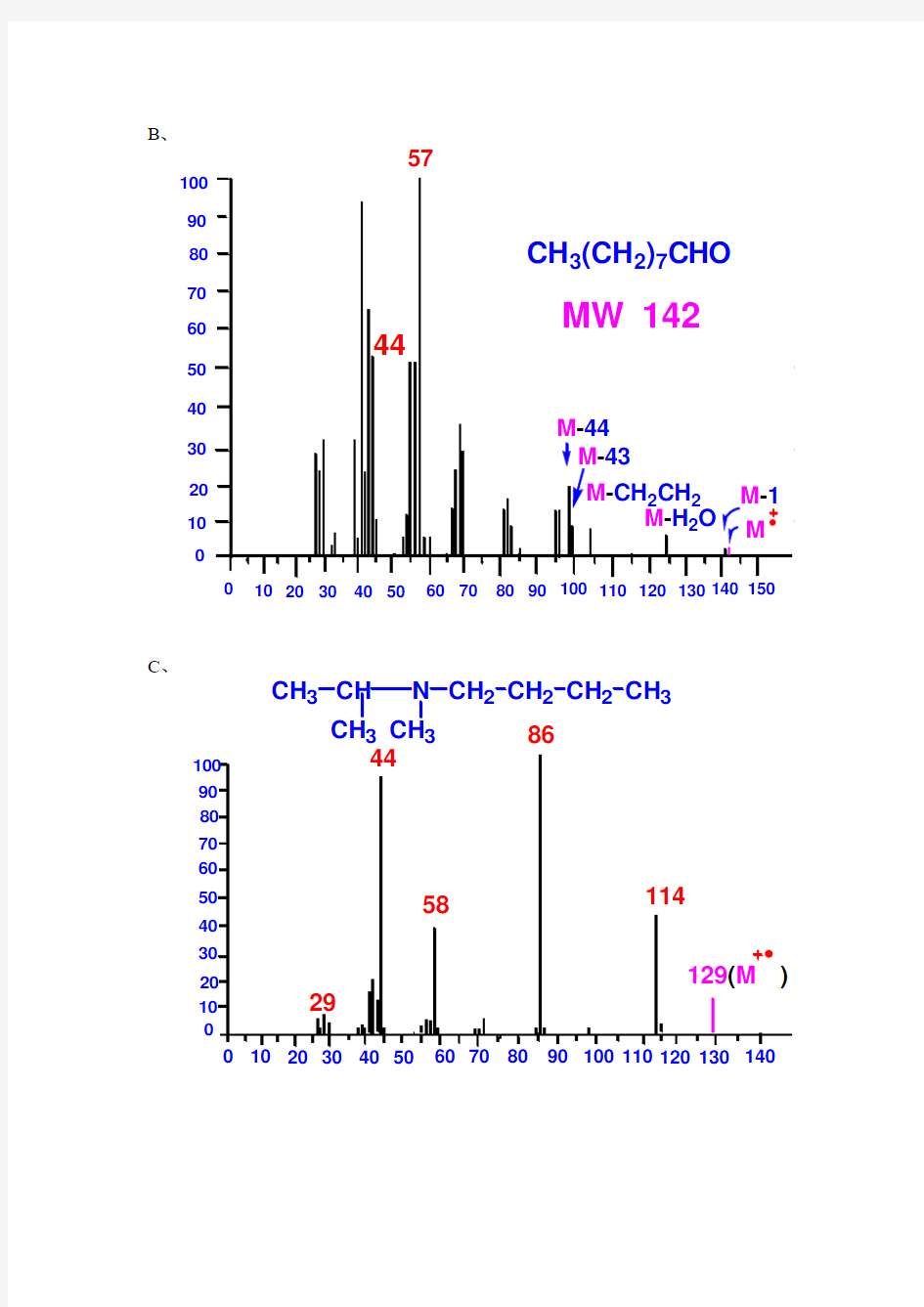
B 、
C 、
0% O F B A S E P E A K 86CH N CH CH 32CH 3CH 3CH
31008090100605030204070% O F B A S E P E A K 57406080120103050709011013020
习题课
一、判断正误 正确的在括号内画“√”,错误的画“×” 1、金属中典型的空间点阵有体心立方、面心立方和密排六方三种。 2、位错滑移时,作用在位错线上的力F的方向永远垂直于位错线并指向滑移面上的未滑移区。 3、只有置换固溶体的两个组元之间才能无限互溶,间隙固溶体则不能。 4、金属结晶时,原子从液相无序排列到固相有序排列,使体系熵值减小,因此是一个自发过程。 5、固溶体凝固形核的必要条件同样是ΔG<0、结构起伏和能量起伏。 6三元相图垂直截面的两相区内不适用杠杆定律。 7物质的扩散方向总是与浓度梯度的方向相反。 8塑性变形时,滑移面总是晶体的密排面,滑移方向也总是密排方向。 9.晶格常数是晶胞中两相邻原子的中心距。 10.具有软取向的滑移系比较容易滑移,是因为外力在在该滑移系具有较大的分切应力值。11.面心立方金属的滑移面是{110}滑移方向是〈111〉。 12.固溶强化的主要原因之一是溶质原子被吸附在位错附近,降低了位错的易动性。13.经热加工后的金属性能比铸态的好。 14.过共析钢的室温组织是铁素体和二次渗碳体。 15.固溶体合金结晶的过程中,结晶出的固相成份和液相成份不同,故必然产生晶内偏析。16.塑性变形后的金属经回复退火可使其性能恢复到变形前的水平。 17.非匀质形核时液体内部已有的固态质点即是非均匀形核的晶核。 18.目前工业生产中一切强化金属材料的方法都是旨在增大位错运动的阻力。 19、铁素体是α-Fe中的间隙固溶体,强度、硬度不高,塑性、韧性很好。 20、体心立方晶格和面心立方晶格的金属都有12个滑移系,在相同条件下,它们的塑性也相同。 21、珠光体是铁与碳的化合物,所以强度、硬度比铁素体高而塑性比铁素体差。 22、金属结晶时,晶粒大小与过冷度有很大的关系。过冷度大,晶粒越细。 23、固溶体合金平衡结晶时,结晶出的固相成分总是和剩余液相不同,但结晶后固溶体成分是均匀的。 24、面心立方的致密度为0.74,体心立方的致密度为0.68,因此碳在γ-Fe(面心立方)中的溶解度比在α-Fe(体心立方)的小。 25、实际金属总是在过冷的情况下结晶的,但同一金属结晶时的过冷度为一个恒定值,它与冷却速度无关。 26、金属的临界分切应力是由金属本身决定的,与外力无关。 27、一根曲折的位错线不可能是纯位错。 28、适当的再结晶退火,可以获得细小的均匀的晶粒,因此可以利用再结晶退火使得铸锭的组织细化。 29、冷变形后的金属在再结晶以上温度加热时将依次发生回复、再结晶、二次再结晶和晶粒长大的过程。 30、临界变形程度是指金属在临界分切应力下发生变形的程度。 31、无限固溶体一定是置换固溶体。 32、金属在冷变形后可形成带状组织。 33、金属铅在室温下进行塑性成型属于冷加工,金属钨在1000℃下进行塑性变形属于热加工。
L20 强弱电解质的判断和比较 课堂练习 1、下列状态时,不能导电的电解质是() A.液态氯化氢B.熔融食盐C.硫酸铜溶液D.氯水 解析:氯水是混合物,能导电;熔融的食盐能导电。 答案:A 2、BaSO4在熔化状态下能导电,其本质原因是() A.是电解质B.存在自由移动的离子 C.存在电子D.存在离子 3、关于强、弱电解质叙述正确的是() A.强电解质都是离子化合物,弱电解质都是共价化合物 B.强电解质都是可溶性化合物,弱电解质都是难溶性化合物 C.强电解质的水溶液中无溶质分子,弱电解质的水溶液中有溶质分子 D.强电解质的水溶液导电能力强,弱电解质的水溶液导电能力弱 解析:A项,部分共价化合物是强电解质;B项强电解质有些是难溶性的,如BaSO4;C项,强电解质在水中完全电离无溶质分子,弱电解质在水中部分电离,有溶质分子。D项,水溶液的导电能力取决于溶液中离子浓度大小,与电解质的强弱无关。 答案:C 4、分别向下列各溶液中加入少量NaOH固体,溶液的导电能力变化最小的是() A.水B.盐酸C.醋酸溶液D.NaCl溶液 5、下列电离方程式中书写正确的是() A.NaHSO 4Na++H++SO2-4 B.NaHCO 3Na++H++CO2-3 C.HClO===H++ClO- D.H 2S H++HS-,HS-++S2- 解析:A项,NaHSO4为强电解质,应用“===”;B项“HCO-3”不能拆开且用“===”;C项,HClO为弱酸,应用“”。 答案:D 6、下列电解方程式书写错误的是() A.(NH4)2SO4溶于水:(NH4)2SO4===2NH+4+SO2-4 B.H 3PO4溶于水:H3PO43H++PO3-4 C.HF溶于水:HF H++F- D.NaHS溶于水:NaHS===Na++HS-,HS-H++S2- 解析:H 3PO4溶于水要分步电离:H3PO4H++H2PO-4、H2PO-4H++HPO2-4、HPO2-4 H++PO3-4。
材料工程基础学习思考题(第二部分固态相变基础) 1、铸造的分类及特点? 2、焊接的分类及特点? 3、锻造的分类及特点? 4、粉末冶金的分类及特点? 5、材料表明工程领域常见的表面处理方法及特点? 6、复合材料的分类及特点? 7、材料热加工过程中可能发生的相变问题及相变与热加工方法之间的关系及控制问题? 基本概念: 奥氏体;马氏体;铁素体;珠光体;组织遗传;相遗传;起始晶粒度;本质晶粒度;实际晶粒度;珠光体团;相间析出;正方度;异常正方度;Ms,As,Md,Ad的含义;机械诱发马氏体相变;奥氏体稳定化;反稳定化;奥氏体热稳定化;奥氏体机械稳定化;热弹性马氏体;形状记忆效应;相变冷作硬化;淬透性;淬硬性;基元;魏氏组织;孕育期;淬火临界冷却速度;临界冷却速度;二次淬火;二次硬化;抗回火稳定性;红硬性;回火脆性;碳化物的原位形核;碳化物的独立形核;奥氏体的等温冷却转变;奥氏体的连续冷却转变;材料的冷脆转变温度;第一类回火脆性;第二类回火脆性。 二、论述说明题 1、以珠光体为原始组织的共析钢为例,说明奥氏体等温转变的过程如何?画图说明(图1-12) 2、画图说明加热速度对珠光体为原始组织的共析钢的奥氏体等温的影响如何?(图1-16)要求说明加热速度对转变机理的影响。 3、连续加热时,奥氏体形成有何特点? 4、为什么非平衡组织不宜直接加热淬火? 5、如何描述奥氏体晶粒度?各种晶粒度有何含义? 6、定性说明为什么第二相颗粒能阻碍奥氏体晶粒长大? 7、画图说明片状珠光体的长大过程?画图说明粒状珠光体的产生过程? 8、何为相间析出?相间析出产生的条件是什么?画图说明相间析出的基本过程? 9、比较珠光体转变和马氏体转变的特点有哪些不同? 10、马氏体转变有哪些特点? 11、画图说明T0,As,Ms,Md,Ad之间的关系并说明其含义是什么?(图3-19) 12、影响Ms点的主要因素有哪些? 13、何为爆发式马氏体转变?其转变特点有哪些? 14、影响马氏体形态及亚结构的主要因素有哪些?(要求说明是如何影响的) 15、何为奥氏体的稳定化?画图说明奥氏体热稳定化现象如何?(图3-92) 16、贝氏体转变的基本过程是什么?这种转变有何特点? 17、比较贝氏体、马氏体的亚结构有何差别? 18、大森等人将贝氏体分为哪几类?其主要依据是什么?(或者说其区分条件是什么)要求画图说明。 19、贝氏体的铁素体是如何长大的?有何特点? 20、关于贝氏体转变在理论上有何争论? 21、说明奥氏体的等温转变图是如何建立起来的?(或者说是如何实验绘制出来的)
- 第二章 思考题与例题 1. 离子键、共价键、分子键和金属键的特点,并解释金属键结合的固体材料的密度比离子键或共价键固体高的原因 2. 从结构、性能等方面描述晶体与非晶体的区别。 3. 何谓理想晶体何谓单晶、多晶、晶粒及亚晶为什么单晶体成各向异性而多晶体一般情况下不显示各向异性何谓空间点阵、晶体结构及晶胞晶胞有哪些重要的特征参数 4. 比较三种典型晶体结构的特征。(Al 、α-Fe 、Mg 三种材料属何种晶体结构描述它们的晶体结构特征并比较它们塑性的好坏并解释。)何谓配位数何谓致密度金属中常见的三种晶体结构从原子排列紧密程度等方面比较有何异同 5. 固溶体和中间相的类型、特点和性能。何谓间隙固溶体它与间隙相、间隙化合物之间有何区别(以金属为基的)固溶体与中间相的主要差异(如结构、键性、性能)是什么 6. 已知Cu 的原子直径为A ,求Cu 的晶格常数,并计算1mm 3Cu 的原子数。 ( 7. 已知Al 相对原子质量Ar (Al )=,原子半径γ=,求Al 晶体的密度。 8 bcc 铁的单位晶胞体积,在912℃时是;fcc 铁在相同温度时其单位晶胞体积是。当铁由 bcc 转变为fcc 时,其密度改变的百分比为多少 9. 何谓金属化合物常见金属化合物有几类影响它们形成和结构的主要因素是什么其性能如何 10. 在面心立方晶胞中画出[012]和[123]晶向。在面心立方晶胞中画出(012)和(123)晶面。 11. 设晶面(152)和(034)属六方晶系的正交坐标表述,试给出其四轴坐标的表示。反之,求(3121)及(2112)的正交坐标的表示。(练习),上题中均改为相应晶向指数,求相互转换后结果。 12.在一个立方晶胞中确定6个表面面心位置的坐标,6个面心构成一个正八面体,指出这个八面体各个表面的晶面指数,各个棱边和对角线的晶向指数。 13. 写出立方晶系的{110}、{100}、{111}、{112}晶面族包括的等价晶面,请分别画出。
解读电解质与非电解质强电解质与弱电解质 河北省宣化县第一中学栾春武 电解质与非电解质、强电解质与弱电解质都就是高中化学中十分重要得概念,正确理解非常重要,因此必须准确把握其内涵与外延,为了让同学们更好地、更准确理解,归纳如下: 电解质:在水溶液里或熔融状态下能够导电得化合物,如酸、碱、盐等、 非电解质:在水溶液里或熔融状态下都不够导电得化合物,如非金属氧化物、酒精、蔗糖等。 从树状分类这个角度上可以把化合物分为电解质与非电解质两类。电解质可分为强电解质与弱电解质两类。 一、电解质与非电解质 (1)金属能导电,但它们不就是化合物,因此金属即不就是电解质,也不就是非电解质。 (2)SO2、NH3溶于水,能导电,导电离子就是H2SO3、NH3·H2O电离出来得,故SO2、NH3不就是电解质。HCl、H2SO4等溶于水,能导电,导电离子就是自身电离出来得,故它们就是电解质、酸、碱、盐就是电解质,非金属氧化物都不就是电解质。 (3)活泼金属氧化物,如Na2O、Al2O3等,在熔融状态下能导电,就是因为它们自身能电离出离子,Al2O3(熔) 2 Al3+ + 3O2-,就是电解质、 (4)难容物(如CaCO3等)得水溶液导电能力很弱,但熔融状态能导电,就是电解质、
(5)酒精、蔗糖等大多数有机物就是非电解质、 (6)电解质不一定导电、强碱与盐等离子化合物在固态时,阴、阳离子不能自由移动,所以不能导电,但熔融状态下或溶于水时能够导电。酸在固态或液态(熔融状态)时只有分子,没有自由移动得离子,因而也不导电,在水溶液里受水分子得作用,电离产生自由移动得离子,而能够导电。 (7)不导电得物质不一定就是非电解质,能导电得物质不一定就是电解质。电解质、非电解质均指化合物、O2不导电,铁、铝能导电,但它们既不就是电解质,也不就是非电解质。 (8)电解质溶液得导电能力与溶液中离子浓度及离子所带电荷多少有关,离子浓度越大,离子所带电荷越多,导电能力越强。 (9)判断电解质就是否导电,关键瞧电解质就是否发生电离,产生了自由移动得离子,还要瞧电离产生得离子浓度得大小、如CaCO3在水中得溶解度很小,溶于水电离产生得离子浓度很小,故认为其水溶液不导电。 二、强电解质与弱电解质
主要的高分子材料的合成类型和方法;高分子单体、单元结构的概念以及与高分子组成和结构性质的关系;聚合物的反应掌握高分子链结构的长、柔和复杂的特点;掌握高分子分子量与分子量分布的表征,理解高分子聚集态结构的多样性、复杂性与多缺陷特点,掌握相变与转变温度的物理意义以及对加工性质和力学性质的影响;理解高聚物高弹性的特点 1.为什么说柔顺性是高分子独有的性质? 答:因为柔顺性是高分子链通过内旋转作用改变其构象的性能,分子内旋转是导致分子链柔顺性的根本原因,因此只有在高分子内部,具有一定的内旋转自由度,出现分子链的内部旋转,才会表现出柔顺性。 2.高分子的分子量相对于小分子和无机物有何特点,主要的表示和描述方法有 哪些? 高聚物分子量有两个特点:一是分子量大,二是分子量的多散性。 首先,从相对分子质量来看——小分子和无机化合物的相对分子质量只有几十到几百; 高聚物的相对分子质量相对高得多 其次,高聚物的晶态结构比小分子物质的晶态有序程度差得多,高聚物的非晶态结构比小分子物质液态的有序程度高。 综上,高分子的分子量可以用聚合物的多分散性、平均分子量、多分散系数来表示。 3.高分子的聚集体包括哪些内容,为什么聚合物不易形成100%的结晶以及宏观 单晶?另外试述高分子的聚集体有哪些特点,以及成型加工条件、性能的关系? 4.如何理解高分子材料拉伸的应力-应变的时温等效性和蠕变特性? 时温等效原理;时间温度等效原理;时间温度对应原理;time temperature correspondence 分子式:CAS号:性质:又称时间温度对应原理。观察高分子材料的某种力学响应(如力学松弛),既可在较低温度下通过足够长的观察时间来实现,也可在较高温度下短时间内观察来实现,简单地说,升高温度与延长观察时间具有相同的效果。 高分子材料蠕变指的是高分子材料在外界恒定应力作用下,由于材料内部分子的位移产生的应变(即外观形变)随着时间而变大。当应力去掉后,由于高分子材料有弹性记忆回复能力,形变可以部分回复。 5.高分子材料组成和结构的基本特征、高分子链的组成和结构、高分子链的聚 集态结构。 ①高分子材料组成和结构的基本特征是: 1、平均分子量大和存在分子量分布 2、具有多种形态 3、组成与结构的多层次性 ②高分子链的组成和结构主要指组成高分子链的结构单元的化学组成、键接方式、空间构 型和高分子链的形态等。 A、高分子链中的原子类型 根据主链上原子类型,高分子链可分为:碳链高分子、杂链高分子、元素有机高分子、无机高分子、梯形和螺旋形高分子。 B、结构单元的键接方式 共有三种可能的键接方式:头头接、尾尾接、头尾接。其造成的原子排列方式为:无规共聚、交替共聚、嵌段共聚和接枝共聚。
第2章习题 2-1 a )试证明均匀形核时,形成临界晶粒的△ G K 与其临界晶核体积 V K 之间的关系式为 2 G V ; b )当非均匀形核形成球冠形晶核时,其△ 所以 所以 2-2如果临界晶核是边长为 a 的正方体,试求出其厶G K 与a 的关系。为什么形成立方体晶核 的厶G K 比球形晶核要大? 解:形核时的吉布斯自由能变化为 a )证明因为临界晶核半径 r K 临界晶核形成功 G K 16 故临界晶核的体积 V K 4 r ; G V )2 2 G K G V b )当非均匀形核形成球冠形晶核时, 非 r K 2 SL G V 临界晶核形成功 3 3( G ;7(2 3cos 3 cos 故临界晶核的体积 V K 3(r 非)3(2 3 3cos 3 cos V K G V 1 ( 3 卸2 3 3cos cos )G V 3 3(書 (2 3cos cos 3 ) G K % G K 与V K 之间的关系如何? G K
G V G v A a3G v 6a2 3 得临界晶核边长a K G V
临界形核功 将两式相比较 可见形成球形晶核得临界形核功仅为形成立方形晶核的 1/2。 2-3为什么金属结晶时一定要有过冷度?影响过冷度的因素是什么?固态金属熔化时是否 会出现过热?为什么? 答:金属结晶时要有过冷度是相变热力学条件所需求的, 只有△ T>0时,才能造成固相的自 由能低于液相的自由能的条件,液固相间的自由能差便是结晶的驱动力。 金属结晶需在一定的过冷度下进行,是因为结晶时表面能增加造成阻力。固态金属熔 化时是否会出现过热现象,需要看熔化时表面能的变化。如果熔化前后表面能是降低的, 则 不需要过热;反之,则可能出现过热。 如果熔化时,液相与气相接触,当有少量液体金属在固体表面形成时,就会很快覆盖 在整个固体表面(因为液态金属总是润湿其同种固体金属 )。熔化时表面自由能的变化为: G 表面 G 终态 G 始态 A( GL SL SG ) 式中G 始态表示金属熔化前的表面自由能; G 终态表示当在少量液体金属在固体金属表面形成 时的表面自由能;A 表示液态金属润湿固态金属表面的面积;b GL 、CSL 、CSG 分别表示气液相 比表面能、固液相比表面能、固气相比表面能。因为液态金属总是润湿其同种固体金属,根 据润湿时表面张力之间的关系式可写出:b SG 》6GL + (SL 。这说明在熔化时,表面自由能的变 化厶G 表w o ,即不存在表面能障碍,也就不必过热。实际金属多属于这种情况。如果固体 16 3 3( G v )2 1 32 3 6 2 (G v )2 b K t K 4 G V )3 G V 6( 4 G v )2 64 3 96 3 32 r K 2 ~G ?, 球形核胚的临界形核功 (G v )2 (G v )2 (G v )2 G b K 2 G v )3 16 3( G v )2
电解质与非电解质 陕西吴亚南 物质的分类依据不同分法也就会不同,化合物根据组成和性质可以分为无机化合物和有机化合物;可以分为氧化物、酸、碱、盐等。化合物根据其在水溶液或熔融状态下是否可以导电又可以分为电解质和非电解质。本文着重讲解电解质与非电解质问题。 一、电解质和非电解质 1、电解质:在水溶液中或熔融状态下能导电的化合物。(如:氯化钠,硫 酸铜等) 理解时注意:电解质是在水溶液或熔融状态下可以导电的化合物。 也就是要抓住三点问题: (1)在水溶液或熔融状态下二者只具其一就可以,其中一种不可以,但是在另一种情况下却可以也满足要求。如:氯化氢在熔融状态下不能导 电,但是在水溶液中却可以,也就满足第一个要求。 (2)要能导电,不论导电的强弱只要能导电就可以,如:水虽然导电性很弱,但我们仍然认为水是电解质。 (3)一定要是化合物。如:金属也可以导电,但却不属于化合物(单质类)所以也就不是电解质了。再如:稀硫酸也可以导电,但稀硫酸是溶液 不是化合物(溶液都是混合物),所以稀硫酸也不是电解质。 2、非电解质:在水溶液中和熔融状态下都不能导电的化合物。(如:乙醇, 蔗糖等) 3、对电解质和非电解质概念的理解: (1)电解质和非电解质都首先是化合物,是化合物的分支。 (2)是看他们在水溶液中和熔融状态下是否能导电与其它状态无关。 (3)看它们导电时所形成的自由移动的离子是否来自于其自身的电离。例题:下列说法正确的是 1、氯水能导电,所以氯水是电解质。 错误:氯气是单质不属于化合物,所以氯气既不是电解质也不是非电解质。 2、盐酸能导电,所以盐酸是电解质。 错误:盐酸是氯化氢的水溶液,属于混合物,所以盐酸既不是电解质也不是非电解质。 3、铜能导电,所以铜是电解质。 错误:铜是金属单质,它即不是电解质也不是非电解质。 4、磷酸是电解质,所以磷酸在熔融状态下和溶于水后都能导电。 错误:磷酸是共价化合物,在熔融状态下不会形成自由移动的离子,所
材料工程基础及参考答案 材料工程基础习题 1、从粉碎过程来看,制粉方法可归纳为三大类:机械制粉、(物理制粉)和(化学制粉) 2衡量合金铸造性能的主要指标有流动性和。 3.高炉原料主要有() A铁矿石、脉石、焦碳;B铁矿石、熔剂、燃料;C碳质还原剂、燃料、脉石;D铁矿石、还原剂、熔剂 4.炼钢的基本任务() A脱碳、脱氧、脱硫,氧化生铁;B使生铁中C、Si、Mn、P、S 等元素合乎标准要求;C氧化生铁中C、Si、Mn等元素;D去除生铁中的杂质元素 5.铝土矿的浸出是拜耳法生产氧化铝的关键工序之一,浸出所用的循环母液中的主要成分为NaOH、NaAlO2、Na2CO3等,其中起主要作用的是() ANaOH;BNaAlO2;CNa2CO3;DNaAlO2和NaOH 7.下列哪种材料不适合挤压加工() A铝及铝合金;B铜及铜合金;C中碳钢;D高合金纲 8.保证冲压件质量的最重要因素是(A) A模具质量;B成形工序;C分离工序;D成形设备 9.下列热处理工艺中,哪种处理工艺常用来改善金属材料的切削加工性()A退火处理;B正火处理;C淬火处理;D时效处理
10.要使某种金属材料获得高弹性、高屈服强度的力学性能,可以采用的热处理工艺为() A退火处理;B淬火+中温回火;C淬火+低温回火;D淬火+高温回火 11.表面淬火用钢的含碳量范围一般为() A0.1—0.2%;B0.2—0.3%;C0.3—0.4%;D0.4—0.5% 12.汽车齿轮表面受严重磨损并受较大的交变冲击载荷而破坏,为了提高其使用寿命,必须提高其表面硬度、耐磨性及疲劳强度,同时齿轮心部要保持良好的韧性及塑性,可以采用的技术方案为() A低碳钢表面渗碳+淬火+高温回火;B低碳钢表面渗碳+淬火+ 低温回火C低碳钢表面渗氮+淬火+高温回火;D低碳钢表面渗氮+淬火+低温回火 13.为了防止飞机、车辆、冷冻设施等的观察窗在寒冷气候条件下表面不结冰,可以对玻璃表面进行()处理 A化学抛光;B涂层导电薄膜;C涂层憎水涂层;D涂层光学薄膜 14.()两种元素具有较强的脱氧能力,一般认为在钢中是有益的元素。 A、MnP; B、SiS; C、MnSi; D、PS 15.低温回火的温度范围是() A.350℃~500℃B.150℃~250℃C.500℃~650℃
查看文本 习题 一、名词解释 金属键; 结构起伏; 固溶体; 枝晶偏析; 奥氏体; 加工硬化; 离异共晶; 成分过冷; 热加工; 反应扩散 二、画图 1在简单立方晶胞中绘出()、(210)晶面及[、[210]晶向。 2结合Fe-Fe3C相图,分别画出纯铁经930℃和800℃渗碳后,试棒的成分-距离曲线示意图。 3如下图所示,将一锲形铜片置于间距恒定的两轧辊间轧制。试画出轧制后铜片经再结晶后晶粒大小沿片长方向变化的示意图。 4画出简单立方晶体中(100)面上柏氏矢量为[010]的刃型位错与(001)面上柏氏矢量为[010]的刃型位错交割前后的示意图。 5画图说明成分过冷的形成。 三、Fe-Fe3C相图分析 1用组织组成物填写相图。 2指出在ECF和PSK水平线上发生何种反应并写出反应式。 3计算相图中二次渗碳体和三次渗碳体可能的最大含量。 四、简答题 1已知某铁碳合金,其组成相为铁素体和渗碳体,铁素体占82%,试求该合金的含碳量和组织组成物的相对量。 2什么是单滑移、多滑移、交滑移?三者的滑移线各有什么特征,如何解释?。 3设原子为刚球,在原子直径不变的情况下,试计算g-Fe转变为a-Fe时的体积膨胀率;如果测得910℃时g-Fe和a-Fe的点阵常数分别为0.3633nm和0.2892nm,试计算g-Fe转变为a-Fe的真实膨胀率。 4间隙固溶体与间隙化合物有何异同? 5可否说扩散定律实际上只有一个?为什么? 五、论述题 τC 结合右图所示的τC(晶体强度)—ρ位错密度 关系曲线,分析强化金属材料的方法及其机制。 晶须 冷塑变 六、拓展题 1 画出一个刃型位错环及其与柏士矢量的关系。 2用金相方法如何鉴别滑移和孪生变形? 3 固态相变为何易于在晶体缺陷处形核? 4 画出面心立方晶体中(225)晶面上的原子排列图。 综合题一:材料的结构 1 谈谈你对材料学科和材料科学的认识。 2 金属键与其它结合键有何不同,如何解释金属的某些特性? 3 说明空间点阵、晶体结构、晶胞三者之间的关系。 4 晶向指数和晶面指数的标定有何不同?其中有何须注意的问题? 5 画出三种典型晶胞结构示意图,其表示符号、原子数、配位数、致密度各是什么? 6 碳原子易进入a-铁,还是b-铁,如何解释? 7 研究晶体缺陷有何意义? 8 点缺陷主要有几种?为何说点缺陷是热力学平衡的缺陷?
电解质溶液知识点总结 一、电解质和非电解质 电解质:在水溶液里或熔融状态下能导电的化合物。 非电解质:在水溶液里和熔融状态下都不能导电的化合物。 【注意】 1.电解质和非电解质的范畴都是化合物,所以单质既不是电解质也不是非电解质。 2.化合物为电解质,其本质是自身能电离出离子,有些物质溶于水时所得溶液也能导电,但这些物质自身不电离,而是生成了一些电解质,则这些物质不属于电解质。如:SO2、SO3、CO2、NO2等。 3.常见电解质的范围:酸、碱、盐、金属氧化物、水。 二.强电解质和弱电解质 强电解质:在溶液中能够全部电离的电解质。则强电解质溶液中不存在电离平衡。 弱电解质:在溶液中只是部分电离的电解质。则弱电解质溶液中存在电离平衡。 O _ 1.强、弱电解质的范围: 强电解质:强酸、强碱、绝大多数盐 弱电解质:弱酸、弱碱、水 2.强、弱电解质与溶解性的关系: 电解质的强弱取决于电解质在水溶液中是否完全电离,与溶解度的大小无关。一些难溶的电解质,但溶解的部分能全部电离,则仍属强电解质。如:BaSO4、BaCO3等。 3.强、弱电解质与溶液导电性的关系: 溶液的导电性强弱与溶液中的离子浓度大小有关。强电解质溶液的导电性不一定强,如很稀的强电解质溶液,其离子浓度很小,导电性很弱。而弱电解质溶液的导电性不一定弱,如较浓的弱电解质溶液,其电离出的离子浓度可以较大,导电性可以较强。 4.强、弱电解质与物质结构的关系: 强电解质一般为离子化合物和一些含强极性键的共价化合物,弱电解质一般为含弱极性键的化合物。5.强、弱电解质在熔融态的导电性: 离子型的强电解质由离子构成,在熔融态时产生自由移动的离子,可以导电。而共价型的强电解质以及弱电解质由分子构成,熔融态时仍以分子形式存在,所以不导电。 三、弱电解质的电离平衡: 强电解质在溶液中完全电离,不存在电离平衡。弱电解质在溶液中电离时,不完全电离,存在电离平衡。当弱电解质的离子化速率和分子化速率相等时,则建立了电离平衡。其平衡特点与化学平衡相似。(逆、等、动、定、变) 1.电离方程式: 书写强电解质的电离方程式时常用“==,书写弱电解质的电离方程式时常用“”。 2.电离平衡常数: 在一定条件下达到电离平衡时,弱电解质电离形成的各种离子的浓度的乘积与溶液中未电离的分子的浓度之比是一个常数,这个常数称为电离平衡常数,简称电离常数。
《土木工程材料》思考题答案 绪论 1、土木工程材料的研究在现代建筑业中有何意义? (1)建材在基建总费用中占很大比例(总投资的60%)(2)建筑形式、结构设计、施工方法等受建材品种、质量的制约(3)建材量大面广,涉及资源、能源、环境等各方面,具有综合的、巨大的社会经济效益。 2、土木工程材料可分为哪几类? 按组成:金属材料、无机非金属材料、有机材料、复合材料;按作用:结构材料、功能材料;按使用部位:墙体材料、屋面材料、地面材料等。 3、选用土木工程材料的基本原则是什么? (1)就地取材,选用技术成熟、经济实用的建材(2)遵照有关政策法规,合理使用利废、节能的新材料,淘汰粘土砖等落后传统建材(3)综合考虑材料性能、施工进度、热工及抗震等建筑性能要求、工程投资等因素。总之,要做到:价廉物美、满足使用要求、综合效益好。 4、对于传统土木工程材料与新品种材料的使用应抱什么态度? 传统建材有长久的历史、广泛的应用,但面临社会的发展、技术进步更新,也暴露出不足和落后,应结合地区特点、工程性质、市场规律进行合理利用和改进。新型建材既存在技术成熟、经济可行方面的问题,也面临人们观念更新、设计与施工、销售配套等问题,因此,既不要盲目照搬,也不要消极保守,应积极而慎重地推广使用。 第一章土木工程材料的基本性质 1、材料的密度、表观密度、体积密度、堆积密度有何区别?材料含水后对它们有何影响? (1)定义、测试方法;(2)大小:ρ> ρ’> ρ0 > ρ0’ (3)适用对象:块材,散粒状;(4)影响因素:孔隙率、含水率。 2、试分析材料的孔隙率和孔隙特征对材料的强度、吸水性、抗渗性、抗冻性、导热性及吸声性的影响? 孔隙率越大,表观密度越小、强度越低。开孔能提高材料的吸水性、透水性、吸声性,降低抗冻性。细小的闭孔能提高材料的隔热保温性能和耐久性。细小的开孔能提高材料的吸声性。 3、一块砖,外形尺寸240*115*53mm,从室外取来时重量为2700g,浸水饱和后重量为2850g,绝干时重量为2600g,求此砖的含水率、吸水率、干表观密度。W含=(2700-2600)/2600*100% W吸=(2850-2600)/2600*100%
《材料科学基础》习题与思考题
《材料科学基础教程》复习题与思考题 一、选择与填空 1-1下列组织中的哪一个可能不是亚稳态,即平衡态组织? a)马氏体+残余奥氏体b)上贝氏体c)铁素体+珠光体d)奥氏体+贝氏体 1-2下列组织中的哪一个可能不是亚稳态? a)铁碳合金中的马氏体b)铁碳合金中的珠光体+铁素体 c)铝铜合金中的a +GPZ d铁碳合金中的奥氏体+贝氏体 1-3单相固溶体在非平衡凝固过程中会形成成分偏析: a)若冷却速度越大,则成分偏析的倾向越大; b)若过冷度越大,则成分偏析的倾向越大; c)若两组元熔点相差越大,则成分偏析的倾向越小; d)若固相线和液相线距离越近,贝U成分偏析的倾向越小。 1-4有两要平等右螺旋位错,各自的能量都为E1,当它们无限靠近时,总能量为—a)2E1 b) 0 c) 4E1 1-13两根具有反向柏氏矢量的刃型位错在一个原子面间隔的两个平行滑移面上相向运动以后,在相遇处___________ 。 a)相互抵消b)形成一排间隙原子c)形成一排空位 1-15位错运动方向处处垂直于位错线,在运动过程中是可变的,晶体做相对滑动的方向—。 a)随位错线运动方向而改变b)始终是柏氏矢量方向c)始终是外力方向 1-16位错线张力是以单位长度位错线能量来表示,则一定长度位错的线张力具有— 纲。 a)长度的b)力的c)能量的 1-17位错线上的割阶一般通过—形成。
a)位错的交割b)共格界面c)小角度晶界 1-7位错上的割阶一般通过 _形成。 a)孪生b)位错的交滑移c)位错的交割 1-23刃形位错的割阶部分—。 a)为刃形位错b)为螺形位错c)为混合位错 1-24面心立方晶体中Frank不全位错最通常的运动方式是 _。 a)沿{111}面滑移b)沿垂直于{111}的面滑移c)沿{111}面攀移 1-25位错塞积群的一个重要效应是在它的前端引起______ 。 a)应力偏转b)应力松弛c)应力集中 1-26面心立方晶体中关于Shcockley分位错的话,正确的是_____ 。 a)Shcockle y分位错可以是刃型、螺型或混合型; b)刃型Shcockley分位错能滑移和攀移; c)螺型Shcockley分位错能交滑移。 1-27汤普森四面体中罗-罗向量、不对应罗-希向量、希-希向量分别有个。 a)12, 24, 8,12 b)24, 24, 8,12 c)12,24, 8,6 1-32 ______ ,位错滑移的派—纳力越小。 a)相邻位错的距离越大b)滑移方向上的原子间距越大c)位错宽度越大 1 —33层错和不全位错之间的关系是__ 。 a)层错和不全位错交替出现;b)层错和不全位错能量相同; c)层错能越高,不全位错柏氏矢量模越小;d)不全位错总是出现在层错和完整晶体的交界处。 1 —34位错交割后原来的位错线成为折线,若—。
强电解质和弱电解质 [教学重点]1、掌握强、弱电解质的概念及弱电解质的电离平衡。 2、了解电解质强弱与导电能力的一般关系。 [重点讲解] 一、强电解质和弱电解质 (一)电解质 1、定义:凡是在水溶液里或熔化状态下能导电的化合物 实质:在水溶液或熔化状态下能电离出自由移动的离子的化合物。 注意: (1)电解质和非电解质研究范畴均是化合物。 (2)某些化合物溶于水后其水溶液能导电但不一定是电解质。例:SO3溶于水后可以与水反应生成H2SO4而导电,但SO3为非电解质。 (3)离子化合物呈固态,共价化合物呈液态虽然是电解质但不导电,因为没有自由移动的离子。 (4)电解质和电解质的水溶液不同,前者为纯净物,后者为混合物。 2、中学常见的电解质 酸、碱、大多数盐(中学所学)均是电解质。 3、电解质导电 (1)原因:形成自由移动的离子。 (2)导电能力:相同条件下与溶液中的离子浓度大小有关。 (二)强电解质和弱电解质 1、比较:强电解质弱电解质 电离程度全部部分 电离方程式:H2SO4=2H++SO42- NaHCOO3=Na++HCO3- NaHSO4=Na++H++SO42- 溶质微粒离子分子为主,离子为辅 实例强酸:HCl,HNO3,H2SO4弱酸:HF,HClO,HCOOH,H2CO3 HBr,HI等
CH3COOH,,H2S, H2SO3,H2SiO3,H2O,H3PO4等强碱:KOH,NaOH,Ba(OH)2 弱碱:NH3·H2O,Al(OH)3 Ca(OH)2等不溶性碱 大多数盐:NaCl BaSO4 AgCl等 注意:强弱电解质的判断依据是,该电解质溶解后电离是否完全而不是该溶液中的离子浓度大小。例:BaSO4虽难溶于水,但溶解的部分完全电离,所以是强电解质。 2、弱电解质的电离平衡 (1)概念:在一定条件下弱电解质的电离速率与结合速率相等时,电离过程就达到了平衡状态,叫做电离平衡状态。 (2)特点:等,V电离=V结合; 定,离子浓度和分子浓度不变; 动,动态平衡; 变,条件改变电离平衡发生移动,电离为吸热过程。 (3)影响电离平衡移动的因素:因为电离平衡是动态平衡,其规律仍遵循化学平衡移动原理。 ①浓度:改变浓度电离平衡向削弱该改变的方向移动。加水,弱电解质电离平衡向电离方向移动,但离子浓度均减小。 ②温度:因为电离过程是吸热过程,所以升高温度,弱电解质的电离平衡向电离方向移动。 (4)多元弱酸,分步电离,第一步电离大于第二步电离,第二步电离远大于第三步电离……,例如,0.1mol/L H2S溶液中各步电离[H+]为: [H+]=1×10-4mol/L [H+]=1×10-13mol/L 电离难的原因为:a、一级电离出H+后,剩下的酸根阴离子带负电荷,增加了对H+的吸引力,使第二个H+离子电离困难的多;b、一级电离出的H+抑制了二级的电离。 [例题讲解] 1、把0.05mol NaOH分别加入到下列100mL溶液中,溶液的导电能力变化不大的是() A、自来水 B、0.5mol/L 盐酸 C、0.5mol/L醋酸 D、0.5mol/L氯化铵 分析:电解质溶液导电能力与该溶液中的离子浓度有关,离子浓度越大,导电能力就越强,导电能力变化不大,说明该溶液中在加入NaOH前后离子浓度无显著变化。A选项中自来水中加入NaOH后离子浓度发生显著变化。C选项中醋酸为弱电解质,反应前离子浓度较小,加入NaOH后发生CH3COOH+NaOH=CH3COONa+H2O反应后生成强电解质CH3COONa,离子浓度显著增大。故A、C不
《材料工程基础》复习思考题 第一章绪论 1、材料科学与材料工程研究的对象有何异同? 10、如何区分传统材料与先进材料? 18、什么是复合材料?如何设计和制备复合材料? 21、纳米材料与纳米技术的异同?它们对科技发展的作用?23、什么是生态环境材料?如何对其生命周期进行评价? 第二章材料的液态成形技术 3、影响液态金属充型能力的因素有哪些?如何提高充型能力? 4、铸件的凝固方式有哪些?其主要的影响因素? 6、什么是缩松和缩孔?其形成的基本条件和原因是什么? 9、试述铸件产生变形和开裂的原因及其防止措施。 13、常见的特种铸造方法有哪些?各有何特点? 第三章材料的塑性成形技术 1、金属为什么容易塑性变形?生产塑性变形的本质? 2、金属常见的塑性成形方法有哪些? 4、什么是金属的可煅性?其影响因素有哪些? 第四章材料的粉末工艺
1、粉末冶金工艺有何特点?其主要的工艺过程包括? 7、雾化制粉的方法有哪些?如何提高雾化制粉的效率? 13、粉体为什么能烧结?烧结的推动力是什么? 第五章材料的连接工艺 1、简述金属的可焊性及其影响因素。 2、简述焊接接头的组织结构。 5、简述钎焊的工艺特点及常用的钎焊材料。 第六章材料的表面处理 2、简述电镀和化学镀的异同(工艺及适应材料)。 6、三束表面改性技术的定义、特点和局限性。 第七章金属材料 1、金属材料的主要强化方式有哪些? 3、什么是钢的淬硬性和淬透性?其主要影响因素? 4、合金产生时效强化的条件是什么?如何进行时效强化? 第八章单晶与半导体工艺 1、简述芯片的主要制备工艺步骤。
第九章纤维的制备 1、为什么纤维通常具有高强度、高模量且韧性好的特点? 2、简述熔融纺丝和溶液纺丝的异同。 第十章复合材料制备工艺 3、什么是玻璃钢?它的制备工艺和主要应用? 4、简述复合材料的强韧化机理。 第十一章陶瓷材料 2、先进陶瓷是如何分类的? 4、简述陶瓷的主要成形方法。 8、为什么金属通常具有良好的塑性,而陶瓷却是脆性的? 10、简述陶瓷与玻璃在结构和性能上的差异。 11、什么是钢化玻璃?对玻璃进行钢化的主要方法有哪些? 第十二章高分子材料 1 何谓高分子化合物?它与一般有机化合物有什么不同? 2 聚合物的分子形状及其特点是什么? 3 合成高分子的化学反应有哪些?
蛋白质组学研究的完整解决方案 人体内真正发挥作用的是蛋白质,蛋白质扮演着构筑生命大厦的“砖块”角色,随着破译生命密码的人类基因组计划进入尾声,一个以蛋白质和药物基因学为研究重点的后基因组时代已经拉开序幕,蛋白质将是今后的重点研究方向之一。然而,蛋白质的分离和鉴定非常费时,目前测定蛋白质的技术远远落后于破译基因组的工具,最好的实验室每天只能分离和识别出100种蛋白质。据估计,人体内可能有几十万种蛋白质,这大概需要10年时间进行识别。 为了加快蛋白质组学研究进程,以专业生产蛋白质组学研究设备而著称的美国Genomic Solution Inc.公司开发了完整的蛋白质组学解决方案,由一系列机械手臂与软件,并结合了二维电泳实验设备与质谱仪,可以进行高效、自动化且具重复性的试验分析。在Genomic solution值得信赖的技术平台上,你的研究工作将更富成效,重复性更好。在这一整套Investigator平台上,各仪器之间配合无隙,由于它的整合性及标准性,使得研究进程大大加快,原来需要9—12个月才能获得数据结果发表的时间减少到9—12周。这套完整的系统具备蛋白质组研究所需的众多功能:2-D电泳、图像获取、2-D胶分析、蛋白样品切割、蛋白消化、MALDI样品准备、消化及点样、数据分析整合,再加上制备好的胶、试剂及附件,使研究工作可以立即展开。此套设备为进行蛋白质组学研究的利器,大大加速了蛋白质分离和鉴定的速度。该系统主要由以下几部分组成: 一、2-D电泳系统(Investigator? 2-D Electophoresis System) 该系统主要进行2D PAGE第一向等电聚焦凝胶电泳和第二向SDS-PAGE电泳,设备包括2-D电泳系统所需的各种设备,如pHaser?(IPG胶条电泳)、管状制胶设备、二维电泳装置、电源设备、半导体冷却器及各种相关的蛋白纯化试剂盒。 产品特征: * 提供2D PAGE电泳所需的各种设备,使电泳更加简便,大大节约研究时间 * 高分辨率:有效的第一向等电聚焦凝胶电泳和23cm X 23cm第二向SDS-PAGE大面积板胶提供清晰的电泳图像,有效提高单体、磷酸化和糖基化蛋白的分离 * 大容量:可同时容纳15块1mm一维管状胶,或8块2-3mm管状胶;10块IPG胶条和10块二维电泳板胶 * 灵活性:该系统用于管状胶、IPG 胶条、预制胶、自制胶和SDS PAGE胶使用 * 恒温:高效的半导体制冷装置保证电泳体系温度恒定,温度变化< 0.5℃ * 专门为高分辨率2D PAGE而设计的电源系统 * 提供超纯的相关化学试剂和药品
2-1 名词解释:配位数与配位体,同质多晶与多晶转变,位移性转变与重建性转变,晶体场理论与配位场理论 答:配位数:晶体结构中与一个离子直接相邻的异号离子数。 配位体:晶体结构中与某一个阳离子直接相邻、形成配位关系的各个阴离子中心连线所构成的多面体。 同质多晶:同一化学组成在不同外界条件下(温度、压力、pH值等),结晶成为两种以上不同结构晶体的现象 多晶转变:当外界条件改变到一定程度时,各种变体之间发生结构转变,从一种变体转变成为另一种变体的现象 位移性转变:不打开任何键,也不改变原子最邻近的配位数,仅仅使结构发生畸变,原子从原来位置发生少许位移,使次级配位有所改变的一种多晶转变形式 重建性转变:破坏原有原子间化学键,改变原子最邻近配位数,使晶体结构完全改变原样的一种多晶转变形式。 晶体场理论:认为在晶体结构中,中心阳离子与配位体之间是离子键,不存在电子轨道的重迭,并将配位体作为点电荷来处理的理论。 配位场理论:除了考虑到由配位体所引起的纯静电效应以外,还考虑了 共价成键的效应的理论。 2-2 面排列密度的定义为:在平面上球体所占的面积分数。 (a)画出MgO(NaCl型)晶体(111)(110)和(100)晶面上的原子排布(b )计算这三面的面排列密度 解:MgO晶体中O2-做紧密堆积,Mg2+填充在八面体空隙中。 (a)(111)(110)和(100)晶面上的氧离子排布情况如图2-1所示。 (b)在面心立方紧密堆积的单位晶胞中, (111)面:面排列密度 = (110)面:面排列密度 = (100)面:面排列密度 = 2-4 设原子半径为R,试计算体心立方堆积结构的(100)、(110)、(111)面的面排列密度和晶面族的面间距。解:在体心立方堆积结构中: (100)面:面排列密度 = 面间距 = (110)面:面排列密度 = 面间距 = (111)面:面排列密度 = 面间距 = 2-8 试根据原子半径R计算面心立方晶胞、六方晶胞、体心立方晶胞的体积。 解:面心立方晶胞: 六方晶胞(1/3): 体心立方晶胞: 2-9 MgO具有NaCl结构。根据O2-半径为0.140nm和Mg2+半径为0.072nm,计算球状离子所占据的体积分数和计算MgO的密度。并说明为什么其体积分数小于74.05%? 解:在MgO晶体中,正负离子直接相邻,a0=2(r++r-)=0.424(nm) 体积分数=4×(4π/3)×(0.143+0.0723)/0.4243=68.52% 密度=4×(24.3+16)/[6.023×1023×(0.424×10-7)3]=3.5112(g/cm3) MgO体积分数小于74.05%,原因在于r+/r-=0.072/0.14=0.4235>0.414,正负离子紧密接触,而负离子之间不直接接触,即正离子将负离子形成的八面体空隙撑开了,负离子不再是紧密堆积,所以其体积分数小于等径球体紧密堆积的体积分数74.05%。