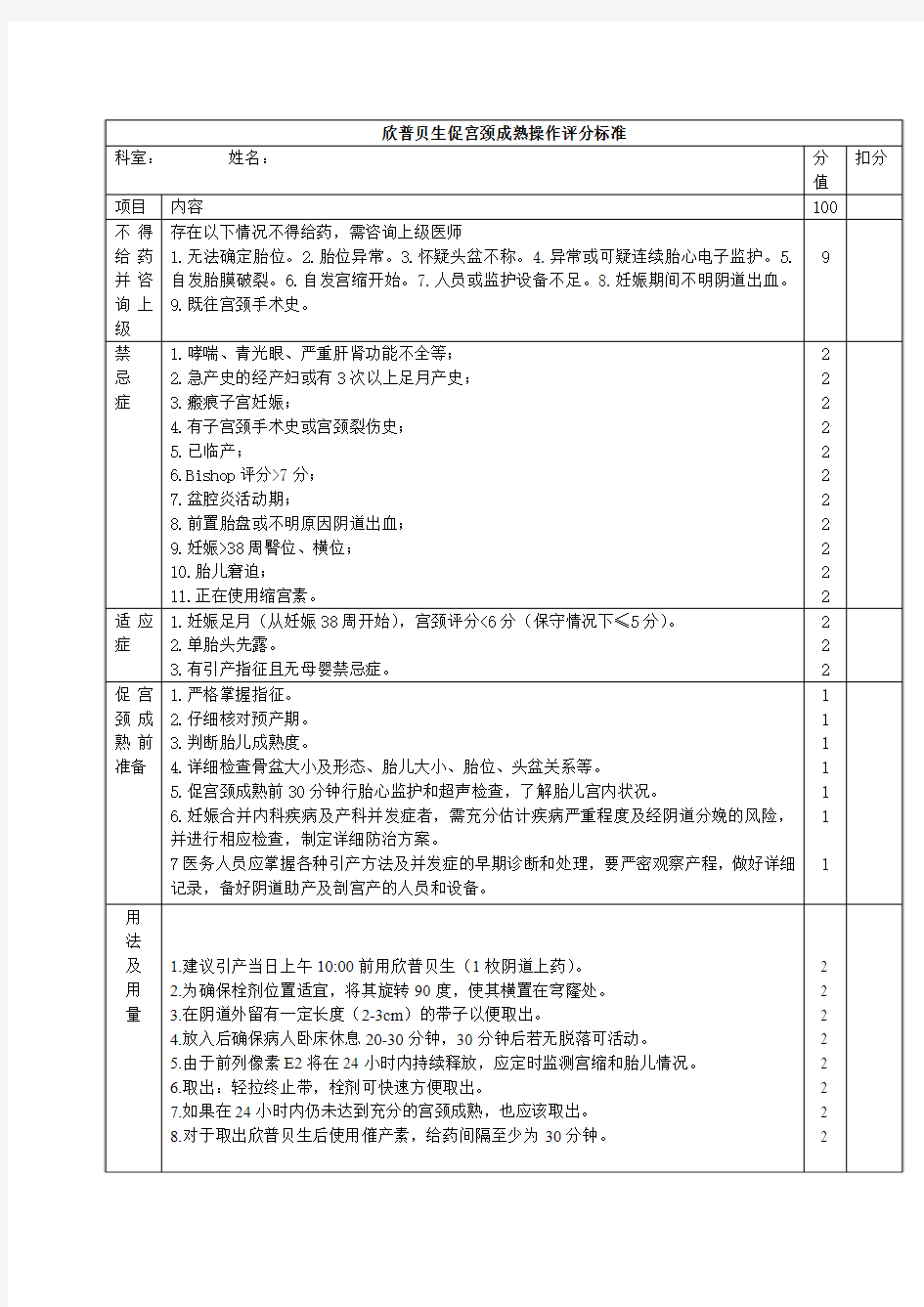
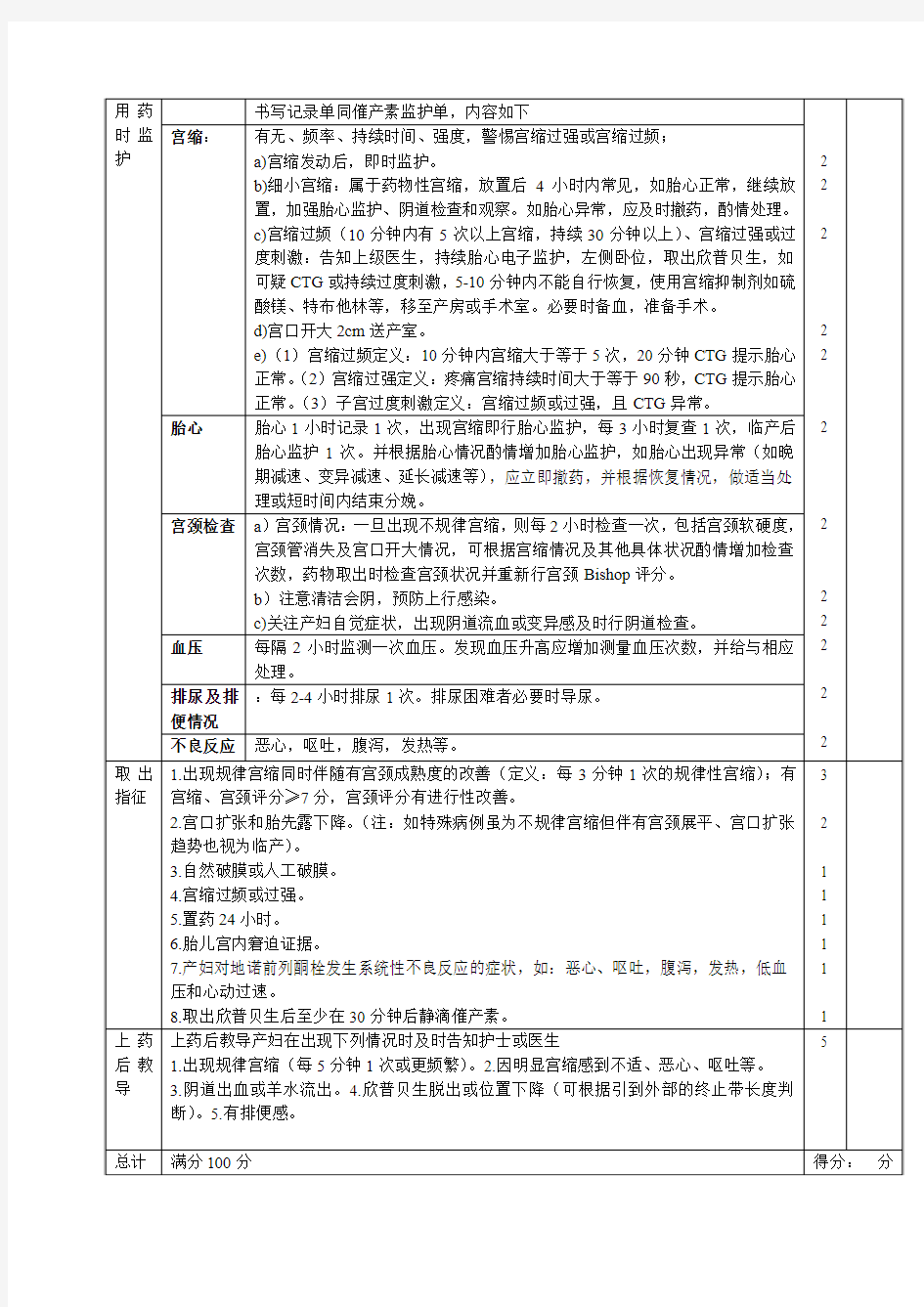
1.初产妇,27岁,妊娠40周,估计胎儿体重3500g,坐骨结节间径7cm,出口后矢状径 5cm,本例正确的处理措施应为 A.等待自然分娩 B.会阴后侧切开术 C.静脉滴注缩宫素 D.产钳术 E.剖宫产术 2.足月初产妇,羊水少,OCT正常,宫颈Bishop评分多少需要在引产前促宫颈成熟 A.5分 B.6分 C.7分 D.8分 E.9分 3.一初产妇,现妊娠41+周,主诉胎动少2天入院,检查宫底剑突下2指,LOA,先露已固定,胎心158次/分,尚规则,无宫缩。下一步的正确处理为: A、B超+胎心监护(NST) B、破膜引产 C、急诊剖宫产 D、催产素点滴引产 E、促宫颈成熟 4. 一孕足月初产妇临产后宫缩强,宫口开大9cm时自然破膜。破膜后不久突然发生烦躁不安、呼吸困难、呛咳、发绀,血压至0mmHg。此时急救措施首选__ A.静注地塞米松40mg B.加压给氧,准备气管切开 C.静脉缓慢注射罂粟碱90mg D.静注阿托品1mg E.立即结束分娩 5. 关于羊水过多合并正常胎儿的处理方法中错误的是 A.症状严重者穿刺放羊水 B.症状较轻者可继续妊娠 C.给予前列腺素合成酶抑制剂 D.一次放羊水量不超过1500mL E.妊娠已近37周,胎儿成熟,则行人工破膜 6. 23岁初孕妇,39周妊娠,近两周来胎动时常感腹痛。入院查体:宫高28cm,腹围85cm,子宫敏感性高,胎位LSA,胎心140次/分,B超检查:胎儿发育正常,羊水指数7cm。诊断为羊水过少。首选的处理方案是 A.尽快破膜引产 B.期待疗法
C.羊膜腔输液 D.立即剖宫产 E.观察 7. 足月分娩的概念是 A妊娠满28周至40足周之间分娩 B.妊娠满36周至41足周之间分娩 C.妊娠满36周至42足周之间分娩 D.妊娠满37周至不满42足周之间分娩 8. 静脉注射缩宫素加强宫缩一般每分钟不超过() A.10滴 B.20滴 C.30滴 D.40滴 E.50滴 9.孕42周产妇,给予缩宫素引产4h后,产妇主诉腹痛难忍。查体:子宫下段压痛明显,伴血尿。诊断先兆子宫破裂。首选护理措施是() A.配血备皮 B. 停缩宫素 C.陪伴产妇 D.通知家属 E.吸氧保暖 10. 应用催产素加强子宫收缩,下列哪项是错误的 A.稀释后静脉滴注 B.严密观察子宫收缩 C.定时听胎心,测量血压 D.胎位正常,无头盆不称者 E.高张性子宫收缩乏力 11. 一初产妇,现妊娠41+周,主诉胎动少2天入院,检查宫底剑突下2指,LOA,先露已固定,胎心158次/分,尚规则,无宫缩。下一步的正确处理为:() A、B超+胎心监护(NST) B、破膜引产 C、急诊剖宫产 D、催产素点滴引产 E、促宫颈成熟 12. 24岁初产妇,规律宫缩10小时,连续观察2小时,宫口由6cm开大至7cm,胎头+1,胎心140次/分。本例恰当的处置应是 A.严密观察产程进展 B.肌注哌替啶(杜冷丁) C.静脉滴注缩宫素 D.立即行人工破膜 E.立即行剖宫产术 13. 25岁初产妇,妊娠40周,规律宫缩4小时,枕左前位,估计胎儿体重3000g,胎心140次/分。阴道检查:宫口开大3cm,未破膜,S+l,骨盆外测量未见异常。若此后宫缩逐渐减弱,产程达16小时,胎膜已破,宫口开大7cm,此时恰当处理应是 A.静注地西洋
血液样本采集标准操作规程 1.目的 规范样本库采集人体血液样本的操作规程。 2.适用范围 适用于使用真空采血管采集人体血液样本的活动过程。 3.定义和术语 3.1知情同意 保证被收集者了解并理解研究的目的和内容,并自愿同意参加试验的原则。知情同意具有国际性,是对所有进行人体研究或人体取样调查的研究人员的伦理要求。在以人为研究/试验对象的科研领域,收集者必须获得研究对象/参与者的知情同意,保护被收集者合法权益的同时保护收集者免于诉讼。 3.2知情同意书 知情同意书,是每位被收集者表示自愿参加某一项试验而签署的文件。知情同意的具体体现是知情同意书的签署。知情同意书由收集者和被收集者共同签署,一式两份。正本由收集者保存,被收集者保存副本。 3.3真空采血管采血法 将有头盖胶塞的采血试管预先抽成不同的真空度,利用其负压自动定量采集静脉血样。 3.4血清和血凝块 指在凝血过程中,血浆中的纤维蛋白原转变为不溶的血纤维。血纤维交织成网,将很多血细胞网罗在内,形成血凝块。血液凝固后,血凝块又发生回缩,并释放出淡黄色液体,称为血清,其中已无纤维蛋白原。
3.5血浆 血浆是离开血管的全血经抗凝处理后,通过离心沉淀,所获得的不含细胞成分的液体,其中含有纤维蛋白原。 3.6白细胞 白细胞人体血液及组织中的无色细胞,是血液中的一类细胞,有细胞核。根据形态特征可分为粒细胞、淋巴细胞和单核细胞。 3.7枸橼酸钠(柠檬酸钠) 枸橼酸能与血液中的钙离子结合形成螯合物,阻止血液凝固。 3.8乙二胺四乙酸二钾(EDTA·K2) 与枸橼酸钠的抗凝机制相同,用21.5-2.2mg EDTA·K2可阻止1ml血液凝固。 3.9肝素 一种相对分子质量为15000,含硫酸基团的黏多糖,与抗凝血酶Ⅲ结合,促进其对凝血因子和凝血酶活性的抑制,抑制血小板聚集从而达到抗凝。 4.职责 4.1临床护理人员 按照标准操作规程采集血液。 4.2样本管理员 协助样本的采集,对样本进行处理和储存,并作相关记录。 5.设备和耗材 5.1个人防护装备 实验防护服、手套、口罩、护目镜及其它相关防护装备。 5.2设备
妊娠晚期促子宫颈成熟与引产指南(2014年) 中华医学会妇产科学分会产科学组妊娠晚期引产是在自然临产前通过药物等手段使产程发动,达到分娩的目的,是产科处理高危妊娠常用的手段之一。引产是否成功主要取决于子宫颈成熟程度。但如果应用不得当,将危害母儿健康,因此,应严格掌握引产的指征、规范操作,以减少并发症的发生。中华医学会妇产科学分会产科学组在2008年发表了《妊娠晚期促宫颈成熟与引产指南(草案)》, 现在此基础上结合国内外近年来的循证医学证据,再次进行了较大程度地修改,以提供妊娠晚期促子宫颈成熟和引产方面符合循证医学的建议。 本指南标出的循证医学证据的等级:Ⅰ级证据:来自至少一个设计良好的随机对照临床试验中获得的证据;Ⅱ-1级证据:来自设计良好的非随机对照试验中获得的证据;Ⅱ-2级证据:来自设计良好的队列研究或病例对照研究的证据;Ⅱ-3级证据:来自多个带有或不带有干预的时间序列研究得出的证据,非对照试验中得出的差异极为明显的结果也可作为这一等级的证据;Ⅲ级证据:来自临床经验、描述性研究、病例报告或专家委员会报告的权威意见。 本指南标出的推荐分类等级:A级:有充分的证据来推荐;B级:有合理的证据来推荐;C级:现有的证据相互矛盾,不允许做支持或反对的推荐;D 级:有合理的证据不推荐;E 级:有充分的证据不推荐;L级:没有足够的证据(数量或质量)做推荐。 一、引产的适应证 引产的主要适应证如下。 1. 延期妊娠:妊娠已达41周或过期妊娠的孕妇应予引产,以降低围产儿死亡率,及导致剖宫产率增高的胎粪吸入综合征的发生率(Ⅰ-A)。 2. 妊娠期高血压疾病:妊娠期高血压、轻度子痫前期患者妊娠满37 周,重度子痫前期妊娠满34 周或经保守治疗效果不明显或病情恶化,子痫控制后无产兆,并具备阴道分娩条件者。 3. 母体合并严重疾病需要提前终止妊娠:如糖尿病、慢性高血压、肾病等内科疾病患者并能够耐受阴道分娩者。 4. 胎膜早破:足月妊娠胎膜早破2 h以上未临产者。 5. 胎儿及其附属物因素:包括胎儿自身因素,如严重胎儿生长受限(FGR)、死胎及胎儿严重畸形;附属物因素如羊水过少、生化或生物物理监测指标提示胎盘功能不良,但胎儿尚能耐受宫缩者。 二、引产的禁忌证 1. 绝对禁忌证:(1)孕妇有严重合并症或并发症,不能耐受阴道分娩或不能阴道分娩者(如心功能衰竭、重型肝肾疾病、重度子痫前期并发器官功能损害者等)。(2)子宫手术史,主要是指古典式剖宫产术、未知子宫切口的剖宫产术、穿透子宫内膜的肌瘤剔除术、子宫破裂史等。(3)完全性及部分性前置胎盘和前置血管。(4)明显头盆不称,不能经阴道分娩者。(5)胎位异常,如横位、初产臀位估计经阴道分娩困难者。(6)子宫颈癌。(7)某些生殖道感染性疾病,如未经治疗的单纯疱疹病毒感染活动期等。(8)未经治疗的HIV感染者。(9)对引产药物过敏者。(10)生殖道畸形或有手术史,软产道异常,产道阻塞,估计经阴道分娩困难者。(11)严重胎盘功能不良,胎儿不能耐受阴道分娩。(12)脐带先露或脐带隐性脱垂。 2. 相对禁忌证:(1)臀位(符合阴道分娩条件者)。(2)羊水过多。(3)双胎或多胎妊娠。
土壤样品采集技术规范-标准化文件发布号:(9456-EUATWK-MWUB-WUNN-INNUL-DDQTY-KII
土壤样品采集技术规范 土壤样品的采集是土壤测试的一个重要环节,采集有代表性的样品,是如实反映客观情况,是测土配方施肥的先决条件。因此,应选择有代表性的地段和有代表性的土壤采样,为保证土壤样品的代表性,必须采取以下技术措施控制采样误差。 1、采样单元(严格按照已经给定大家的GPS定位为准,如果该点已经有建筑非农田,可以就近取土壤类型、种植作物一致的露天大田非大棚土壤,如玉米小麦是山东典型作物。如果就近实在没有作物地块,可以标注上是蔬菜地,如白菜地。非原始点位的,需要文字说明点位漂移的大致方位距离等) 点位漂移的另选取典型代表地块,采样地块的土壤要尽可能均匀一致。选取地势平坦,肥力均匀,采样单元一般为100平方米地块。采样单元应集中在典型地块,相对在中心部位,采一个混合样。 3、采样路线 采样时应“等量”和“多点混合”的原则进行采样。一般采用S形(下图)布点采样,能够较好地克服耕作、施肥等所造成的误差。或者梅花采样即取四个角加中心点。田块选取要避开路边(有交通工具汽车尾气扬尘等污染影响结果的准确性)、田埂、沟边、肥堆等特殊部位。 3、采样点数量 一个样点至少采集6个点位的土壤,然后混匀。(要保证足够的点,使之能代表采样单元的土壤特性),混匀后,用四分法(见下图)将多余的土壤弃去。方法是将采集的土壤样品混匀后放在盘子里或塑料布上、蛇皮袋上,剔除落叶石块等杂物后弄碎、混匀,铺成四方形,划对角线将土样分成四份,把对角的两份分别合并成一份,保留一份,弃去一份。如果所得的样品依然很多,可再用四分法处理,直至所需数量为止。一个混和土样以取土1公斤左右为宜。 4、采样点定位(必须有,尤其是点位漂移的)
1.初产妇,27岁,妊娠40周,估计胎儿体重3 500g,坐骨结节间径7cm,出口后矢状径 5cm,本例正确的处理措施应为 A.等待自然分娩 B.会阴后侧切开术 C.静脉滴注缩宫素 D.产钳术 E.剖宫产术 2.足月初产妇,羊水少,OCT正常,宫颈Bishop评分多少需要在引产前促宫颈成熟 A.5分 B.6分 C.7分 D.8分 E.9分 3.一初产妇,现妊娠41+周,主诉胎动少2天入院,检查宫底剑突下2指,LOA,先露已固定,胎心158次/分,尚规则,无宫缩。下一步的正确处理为: A、B超+胎心监护(NST) B、破膜引产 C、急诊剖宫产 D、催产素点滴引产 E、促宫颈成熟 4.一孕足月初产妇临产后宫缩强,宫口开大9cm时自然破膜。破膜后不久突然发生烦躁不安、呼吸困难、呛咳、发绀,血压至0mmHg。此时急救措施首选__ A.静注地塞米松40mg B.加压给氧,准备气管切开 C.静脉缓慢注射罂粟碱90mg D.静注阿托品1mg E.立即结束分娩 5.关于羊水过多合并正常胎儿的处理方法中错误的是 A.症状严重者穿刺放羊水 B.症状较轻者可继续妊娠 C.给予前列腺素合成酶抑制剂 D.一次放羊水量不超过1500mL E.妊娠已近37周,胎儿成熟,则行人工破膜 6.23岁初孕妇,39周妊娠,近两周来胎动时常感腹痛。入院查体:宫高28cm,腹围85cm,子宫敏感性高,胎位LSA,胎心140次/分,B超检查:胎儿发育正常,羊水指数7cm。诊断为羊水过少。首选的处理方案是 A.尽快破膜引产 B.期待疗法
C.羊膜腔输液 D.立即剖宫产 E.观察 7.足月分娩的概念是 A妊娠满28周至40足周之间分娩 B. 妊娠满36周至41足周之间分娩 C.妊娠满36周至42足周之间分娩 D. 妊娠满37周至不满42足周之间分娩 8.静脉注射缩宫素加强宫缩一般每分钟不超过() A.10 滴 B.20 滴 C.30 滴 D.40 滴 E.50 滴 9.孕 42 周产妇,给予缩宫素引产 4h 后,产妇主诉腹痛难忍。查体:子宫下段压痛明显,伴血尿。诊断先兆子宫破裂。首选护理措施是() A. 配血备皮 B.停缩宫素 C. 陪伴产妇 D. 通知家属 E. 吸氧保暖 10.应用催产素加强子宫收缩,下列哪项是错误的 A.稀释后静脉滴注 B.严密观察子宫收缩 C.定时听胎心,测量血压 D.胎位正常,无头盆不称者 E.高张性子宫收缩乏力 11.一初产妇,现妊娠41+周,主诉胎动少2天入院,检查宫底剑突下2指,LOA,先露已固定,胎心158次/分,尚规则,无宫缩。下一步的正确处理为: ( ) A、B超+胎心监护(NST) B、破膜引产 C、急诊剖宫产 D、催产素点滴引产 E、促宫颈成熟 12. 24岁初产妇,规律宫缩10小时,连续观察2小时,宫口由6cm开大至7cm,胎头+1,胎心140次/分。本例恰当的处置应是 A.严密观察产程进展 B.肌注哌替啶(杜冷丁) C.静脉滴注缩宫素 D.立即行人工破膜 E.立即行剖宫产术 13. 25岁初产妇,妊娠40周,规律宫缩4小时,枕左前位,估计胎儿体重3000g,胎心140次/分。阴道检查:宫口开大3cm,未破膜,S+l,骨盆外测量未见异常。若此后宫缩逐渐减弱,产程达16小时,胎膜已破,宫口开大7cm,此时恰当处理应是 A.静注地西洋
临床试验生物样本转运的标准操作规程 版本号 1.0 页数1页 起草人起草日期年月日审核人审核日期年月日批准人批准日期年月日颁布日期年月日起效日期年月日 威海市立医院 药物临床试验机构
临床试验生物样本转运的标准操作规程 一、目的 建立机构办公室对临床试验中生物样本转运的管理工作。确保生物样本转运规范、一致并符合方案要求,用以监督和提高临床试验质量,保障临床试验顺利进行。 二、范围 适用于在本机构开展的药物临床试验的生物样本转运。 三、内容 1. 生物样本采集处理后,按试验方案要求将标本立即交至试验人员或放至相应标本放置 点或标本冰箱。记录标本信息、交接/保存时间、标本状态。 2.转运样本时,递交/接收人员应核对如下项目: 1)检查样本的外包装是否完好; 2)标本包装的标识是否规范:标本名称、编号、数量等; 3)核对试验标本信息是否与交接单注明信息一致,核对无误后双方在交接记录单签上 姓名、日期; 3.如采取快递形式运送样本,样本接收时应有递交人员签字的交接单(一式两份),接 收人不仅需要核对以上信息,还要检查运输过程中的贮存条件是否与贮存要求相符,核 对无误后在交接记录单签上姓名、日期,复印快递单保留存档;并将其中一份交接单退 回给递交人。 4. 如果交接时的条件出现异常,需将该批样本按保存条件存放,向对方说明情况,等待 书面通知后决定后续处理,过程应详细记录。 四、参考资料 1国家食品药品监督管理总局令第3号发布《药物临床试验质量管理规范》,2003 2国家食品药品监督管理总局.卫生部文件,国食药监注[2011]482号.关于印发药物临床试验生物样本分析实验室管理指南(试行)的通知,2011 五、工作表格 1《临床试验标本交接表》(文件编号:JG-form-028-1.0)
妊娠晚期促子宫颈成熟与引产指南(完整版) 妊娠晚期引产是在自然临产前通过药物等手段使产程发动,达到分娩的目的,是产科处理高危妊娠常用的手段之一。引产是否成功主要取决于子宫颈成熟程度。但如果应用不得当,将危害母儿健康,因此,应严格掌握引产的指征、规范操作,以减少并发症的发生。中华医学会妇产科学分会产科学组在 2008 年发表了《妊娠晚期促宫颈成熟与引产指南(草案)》, 现在此基础上结合国内外近年来的循证医学证据,再次进行了较大程度地修改, 以提供妊娠晚期促子宫颈成熟和引产方面符合循证医学的建议。 本指南标出的循证医学证据的等级:Ⅰ级证据:来自至少一个设计良好的随机对照临床试验中获得的证据;Ⅱ-1 级证据:来自设计良好的非随机对照试验中获得的证据;Ⅱ-2 级证据:来自设计良好的队列研究或病例对照研究的证据;Ⅱ-3 级证据:来自多个带有或不带有干预的时间序列研究得出的证据,非对照试验中得出的差异极为明显的结果也可作为这一等级的证据;Ⅲ级证据:来自临床经验、描述性研究、病例报告或专家委员会报告的权威意见。 本指南标出的推荐分类等级:A级:有充分的证据来推荐;B 级:有合理的证据来推荐;C 级:现有的证据相互矛盾,不允许做支持或反对的推荐;D 级:有合理的证据不推荐;E 级:有充分的证据不推荐;L级:没有足够的证据(数量或质量)做推荐。 一、引产的适应证
引产的主要适应证如下: 1. 延期妊娠:妊娠已达 41 周或过期妊娠的孕妇应予引产,以降低围产儿死亡率,及导致剖宫产率增高的胎粪吸入综合征的发生率(Ⅰ-A)。 2. 妊娠期高血压疾病:妊娠期高血压、轻度子痫前期患者妊娠满 37 周,重度子痫前期妊娠满 34周或经保守治疗效果不明显或病情恶化,子痫控制后无产兆,并具备阴道分娩条件者。 3. 母体合并严重疾病需要提前终止妊娠:如糖尿病、慢性高血压、肾病等内科疾病患者并能够耐受阴道分娩者。 4. 胎膜早破:足月妊娠胎膜早破2h 以上未临产者。 5. 胎儿及其附属物因素:包括胎儿自身因素,如严重胎儿生长受限(FGR)、死胎及胎儿严重畸形;附属物因素如羊水过少、生化或生物物理监测指标提示胎盘功能不良,但胎儿尚能耐受宫缩者。 二、引产的禁忌证 1. 绝对禁忌证: (1)孕妇有严重合并症或并发症,不能耐受阴道分娩或不能阴道分娩者(如心功能衰竭、重型肝肾疾病、重度子痫前期并发器官功能损害者等)。 (2)子宫手术史,主要是指古典式剖宫产术、未知子宫切口的剖宫产术、穿透子宫内膜的肌瘤剔除术、子宫破裂史等。 (3)完全性及部分性前置胎盘和前置血管。 (4)明显头盆不称,不能经阴道分娩者。
妊娠晚期促子宫颈成熟与引产指南(2014) 妊娠晚期引产是在自然临产前通过药物等手段使产程发动,达到分娩的目的,是产科处理高危妊娠常用的手段之一。 中华医学会妇产科学分会产科学组妊娠晚期引产是在自然临产前通过药物等手段使产程发动,达到分娩的目的,是产科处理高危妊娠常用的手段之一。引产是否成功主要取决于子宫颈成熟程度。但如果应用不得当,将危害母儿健康,因此,应严格掌握引产的指征、规操作,以减少并发症的发生。中华医学会妇产科学分会产科学组在2008年发表了《妊娠晚期促宫颈成熟与引产指南(草案)》, 现在此基础上结合国外近年来的循证医学证据,再次进行了较大程度地修改,以提供妊娠晚期促子宫颈成熟和引产方面符合循证医学的建议。 本指南标出的循证医学证据的等级:Ⅰ级证据:来自至少一个设计良好的随机对照临床试验中获得的证据;Ⅱ-1级证据:来自设计良好的非随机对照试验中获得的证据;Ⅱ-2级证据:来自设计良好的队列研究或病例对照研究的证据;Ⅱ-3级证据:来自多个带有或不带有干预的时间序列研究得出的证据,非对照试验中得出的差异极为明显的结果也可作为这一等级的证据;Ⅲ级证据:来自临床经验、描述性研究、病例报告或专家委员会报告的权威意见。 本指南标出的推荐分类等级:A级:有充分的证据来推荐;B级:有合理的证据来推荐;C级:现有的证据相互矛盾,不允许做支持或反对的推荐;D 级:有合理的证据不推荐;E级:有充分的证据不推荐;L级:没有足够的证据(数量或质量)做推荐。 一、引产的适应证 引产的主要适应证如下: 1. 延期妊娠:妊娠已达41周或过期妊娠的孕妇应予引产,以降低围产儿死亡率,及导致剖宫产率增高的胎粪吸入综合征的发生率(Ⅰ-A)。 2. 妊娠期高血压疾病:妊娠期高血压、轻度子痫前期患者妊娠满37 周,
土壤样品采集技术规范 土壤样品的采集是土壤测试的一个重要环节,采集有代表性的样品,是如实反映客观情况的先决条件。因此,应选择有代表性的地段和有代表性的土壤采样,并根据不同分析项目采用相关的采样和处理方法。为保证土壤样品的代表性,必须采取以下技术措施控制采样误差。 1、采样单元 尽可能优先采用分区布点法进行监测点位的布设,每个采样单元的土壤要尽可能均匀一致。在分区时应重点考虑:①各场地实际使用过程中涉及的污染物种类及其对土壤造成污染的方式和途径在区块中分布的均匀性;②尽可能以场地使用时自然形成的分界作为监测分区的边界,且区块形状基本规则;③一个区块内同样深度层的土壤应属于同一种分类;④当一个拟划分的区块面积过大时,应认真推敲是否有拆分成小区块的必要。而对于占地面积较大、无法按使用功能划分区块或拆迁后造成场地内土壤迁移、原始状况遭破坏的场地,应根据调查的不同阶段分别采用系统随机布点法、系统布点法布设监测采样的点位。在设置系统网格布局时应重点考虑:①根据场地面积、土壤污染分布可能的均匀程度、监测样品控制数量等因素设置网格密度;②尽可能将网格设置成方形、长方形或三角形等则形状;③场地面积过大时,可根据前期调查的结果经分析后设置分区域不同密度和形状的网格,几种典型的监测布点方法见图. 本次取样网格大小基本可采取20m×20m,其中厂内办公区、生产车间及废料堆放点等典型位置都应设置取样点。 2、采样深度 在完成土壤样品采集点位平面布设后,应根据不同阶段调查的要求进行点位的纵向布设。土壤纵向结构一般可分为表层土壤(0~、浅层土壤~和深层土壤~)。根据国外通行的做法并结合国内典型场地监测实际案例的经验,表层和浅层的土壤可在各层的深度范围内采集1个样品。一般表层土壤常用的采样方法均可以保证样品在深度方向上样品的代表性。浅层土壤采样时可在规定的深度范围内连续或分上下2段采样后制成混合样。深层土壤应采用纵向分层的方法,分别采集每1层土壤的代表性样品。在环境调查判定污染物种类和初步探明污染程度、范围阶段,一般在3m深度以内时,每个样品的采样分层间隔为. 3、采样点数量 要保证足够的采样点,使之能代表采样单元的土壤特性。 4、采样点定位 有条件的可采用GPS定位,记录经纬度,精确到″。无条件的可在地图上标明采样点位置,并记录样点名称、固定参照物的距离和方位。 5、采样方法
微生物标本采集及保存要求 一、总则:用于培养的标本在收集时应注意严格无菌操作和及时送检,检测后标本应妥善保存。 二、临床标本的采集 (一)下呼吸道分泌物(痰液) 令患者早上起床后用清水濑口,不要刷牙,立即从下部呼吸道咳出第一口痰,吐在无菌塑料痰盒中,及时送检。 (二)、尿液(中段尿) 护理人员协助采取中段尿约3ml入无菌试管中,及时送检。 (三)、粪便:取有粘液、脓血部分的粪便置玻璃大便专用管中,如为稀水便,可直接收集于玻璃管中,及时送检。 (四)、眼、耳、鼻、喉拭子:将棉拭子沾取少许无菌生理盐水(如沾取的太多,可在无菌生理盐水瓶壁上挤去多余的水份),然后采取可疑部位的分泌物,倒悬于无菌试管内,及时送检。 (五)、脓液:用沾有生理盐水的棉拭子沾取脓液,要尽量多取一些,然后将棉拭置于无菌试管中,及时送检。 (六)、: 1、凡怀疑菌血症和败血病的患者,采血培养时,应尽量在未使用抗菌素前采血,如已使用抗菌素,应尽量选择抗菌素在体内浓度最低时采血,应在病人第二次使用抗菌素之前采集血培养标本。当然在病人发热或寒颤时采集也可。 2、成人每次采血5—10ml,小儿采血2—3ml; 3、严格消毒病人采血部位和血培养瓶口,抽一定量血液后,无菌注入血培养瓶内,轻轻摇匀, 4、从抽血到接种入瓶,动作要快,防止血液凝固,同时要及时送检。 (七)、穿刺液:胸腹水、心包液、关节腔液、鞘膜积液: 严格无菌抽取后,注入含肝素抗凝的无菌试管中,轻轻颠倒试管10余次,使肝素与穿刺液混匀达到抗凝的目的,或直接无菌注入血培养瓶内及时送检。 (八)、胆汁:由专科医生以无菌方法取引流液10ml注入无菌试管。 (九)、脑脊液:以无菌方法取脑脊液3-5ml,置无菌试管内,常温保存送检,如只做培养可直接无菌注入血培养瓶内,及时送检。 (十)、生殖器官标本:阴道、子宫颈及前列腺等分泌物应由医师采集,收集于无菌试管内送检。如疑为淋病奈瑟菌感染,做培养检查时,采集的标本应床旁接种并及时放入孵箱培养。(十一)、烧伤标本:以无菌棉拭子直接采取多个部位创面的脓汁分泌物放入无菌试管中. (十二)、支原体(解脲、人型)培养+药敏的标本采集 1、支原体对干、热抵抗力差,标本采集后应尽快接种支原体运送培养基送检。 2、男性:用细的无菌棉拭子沾取无菌盐水少许深入尿道口内2.5-3cm。 三、临床标本的保存 细菌室标本原则上要求及时送检、及时处理,不得保存。
生物样本库建设管理规定 第一章总则 第一条为加强和规范医院生物样本库建设、运行和管理,制定本规定。 第二条医院生物样本库应按照“顶层设计、统筹规划、共建共享”的原则,建立信息资源和利益共享机制以及相应的信息服务平台,建成资料完整、规范化、标准化、信息化、特色鲜明的综合型生物样本库,为临床转化医学研究提供平台支撑。 第三条医院生物样本库应遵循《中国医药生物技术协会生物样本库标准(试行)》和伦理规范,为临床科学研究提供高质量的样本、高质量的数据、高质量的服务。 第四条医院生物样本库在院党委的领导下,依托病理科建设,病理科主任兼任生物样本库主任,负责规范运行、质控、经费管理等。 第二章生物样本库组织构架与任务职责第五条组织构架 图一:组织构架
第六条生物样本库人员编配 生物样本库设主任、副主任各1人,采集组2人,加工处理组2人,冻存管理组1人;主任由病理科主任兼任,副主任及成员由医院招聘专职人员。 主任:负责生物样本库全面管理工作。 副主任:协助主任完成生物样本库的日常运行与管理工作。 采集组:负责组织样本的取材与运输等工作。 加工处理组:负责接收入库样本,并根据样本种类与研究需求进行分装、处理等。 冻存管理组:负责样本的出入库管理、追踪核实样本的库存情况与质量检测等工作。 具体岗位职责与要求,由生物样本库明确后报医院审定。 待遇:专职人员参照中心实验室招聘人员待遇执行。 第七条任务职责 一、学术委员会 (一)依托医院学术委员会。 (二)职责: 1.指导生物样本库建设及中长期发展规划。 2.对生物样本库的重大学术研究问题提供咨询和把关。 3.对生物样本采集与使用进行科学性审查。 4.检查监督生物样本库运行管理。 5.检查指导生物样本库年度预算拟制和落实情况。
妊娠晚期促宫颈成熟与引产指南 妊娠晚期促宫颈成熟与引产指南 ―――――中华医学会妇产科学分会产科学组 妊娠晚期引产是指在自然临产前通过药物等手段使产程发动,达到分娩的目的。主要是为了使胎儿及早脱离不良的宫内环境,解除与缓解孕妇合并症或并发症所采取的一种措施。妊娠晚期引产是产科处理高危妊娠最常用的手段之一,引产是否成功主要取决于宫颈成熟度。但如果应用不得当,将危害母儿健康,对母儿都存在潜在的风险,如增加剖宫产率、胎儿窘迫发生率等,因此,应严格掌握引产的指征、规范操作,以减少并发症的发生。本指南主要是提供妊娠晚期促宫颈成熟和引产方面、符合循证医学的建议。 一、引产的主要指征: 1.延期妊娠(妊娠已达41周仍未临产者)或过期妊娠。 2.母体疾病,如严重的糖尿病、高血压、肾病等。 3.胎膜早破,未临产者。 4.胎儿因素,如可疑胎儿窘迫、胎盘功能不良等。 5.死胎及胎儿严重畸形。 二、引产禁忌症: 1.绝对禁忌症:孕妇严重合并症及并发症,不能耐受阴道分娩者,如: (1)子宫手术史,主要是指古典式剖宫产术,未知子宫切口的剖宫产术,穿透子宫内膜的肌瘤剔除术,子宫破裂史等。 (2)前置胎盘和前置血管。 (3)明显头盆不称。 (4)胎位异常,横位,初产臀位估计不能经阴道分娩者。 (5)宫颈浸润癌。 (6)某些生殖道感染性疾病,如疱疹感染活动期。 (7)未经治疗的获得性免疫缺陷病毒感染者。 (8)对引产药物过敏者。 2.相对禁忌症:
(1)子宫下段剖宫产史。 (2)臀位。 (3)羊水过多。 (4)双胎或多胎妊娠。 (5)经产妇分娩次数大于等于5次者。 三、引产前准备 1.严格掌握引产指征。 3.仔细核对预产期,防止人为的早产和不必要的引产。 4.判断胎儿成熟度:如果胎肺未成熟,如情况许可,尽可能先促胎肺成熟后在引产。 5.详细检查骨盆大小即形态、胎儿大小、胎位、头盆关系等,排除阴道分娩禁忌症。 6.在引产前应行胎心监护和超声检查,了解胎儿宫内状况。 7.妊娠合并内科疾病及产科并发症者,在引产前,充分估计疾病严重程度及经阴道分娩的风险,并进行相应检查,制定详细的防治方案。 8.医护人员应熟练掌握各种引产方法及其并发症的早期诊断和处理,要严密观察产程,做好详细记录,引产期间需配备有阴道助产及剖宫产的人员和设备。四、评价宫颈成熟度 目前公认的评估成熟度常用的方法是Bishop评分法,评分大于等于6分提示宫颈成熟。评分越高,引产成功率越高。评分小于6分提示宫颈不成熟,需要促宫颈成熟。 五、促宫颈成熟的方法 (一)、前列腺素制剂促宫颈成熟 如果宫颈评分<6分,则应进行促宫颈成熟。常用的促宫颈成熟的药物主要是前列腺素制剂。PG促宫颈成熟的主要机制,一是通过改变宫颈细胞外基质成分,软化宫颈,如激活胶原酶,是胶原纤维溶解和基质增加;二是影响宫颈和子宫平滑肌,使宫颈平滑肌松弛,宫颈扩张,宫体平滑肌收缩,牵拉宫颈;三是促进子宫平滑肌细胞间缝隙连接的形成。 目前临床使用的前列腺素制剂有:
样本采集规范 ●接到手术信息后,通知负责医生与样本提供者签写知情同意书 并留取样本提供者的术前配对血(抗凝、非抗凝血各一管,每管3~5ml),放置4℃冰箱并通知生物样本库人员来取。 ●提前30分钟内进入手术室准备样本交接。 ●样本离体后在最短时间完成样本交接,填写样本交接单,将样 本即刻转移到样本取材室进行采集。 ●手术切除样本应在离体后30min内完成样本采集。 ●依据科研需求,样本采集包括正常组织(>癌灶周围3cm)、 癌旁(癌灶周围3cm内)和癌灶。样本采集顺序为“正常→癌旁→癌灶”,每个位置采集不少于3块,每块应≥0.5cm3或300mg或1×107细胞。采集部位应与石蜡切片相一致。癌灶、癌旁、正常组织分别置于-80℃2管、液氮2管、RNAlater 1管保存。 ●采集石蜡样本应≥0.5x0.5x0.2cm,样本和福尔马林的比例为1:8。 ●保存RNA需用RNA later,组织体积与RNA later之比≥1:5。 ●电镜样本采集将组织样本修成1mm3大小组织块,即刻投入4℃
固定液。样本和电镜保存液比例≥1:10。 ●样本的配对血(抗凝、非抗凝各一管)应在离体后尽快分离, 2000r/m离心10分钟,离心后取上清液(血清、血浆)各五管保存,每管200~500μl,如果不够分5管则应保证每管最少200μl。 ●将抗凝管上清液取走后,剩余血细胞加入人淋巴细胞分离液 2000r/m离心10分钟,洗脱后,1000r/m离心5分钟重复两次,用移液枪吹打贴壁细胞进行细胞计数分管,保证每管淋巴细胞数应不小于1x107个。根据科研需求,如需保证细胞活性,应加入冷冻保护剂,进行梯度降温后保存。 ●根据研究需要,采集治疗过程中和治疗后的空腹外周静脉血, 术后1周、2周、1个月各取一次,肿瘤患者术前血液样本采集应在放/化疗前进行。
上海生物样本库 最佳实践规范及标准操作流程 文件汇编 (第二版) 2010年5月
样本库最佳实践规范 第2章 样本 目 录 2.样本 (2) 2.1样本采集 (2) 2.1.1样本采集的要求 (2) 2.1.2样本的采集 (3) 2.1.3采集后处理 (8) 2.1.4采集的信息记录 (11) 2.2样本储存 (12) 2.2.1样本的储存 (12) 2.2.2样本储存的标识 (14) 2.2.3样本库存的追踪 (16) 2.2.4库存核实 (16) 2.2.5外部质量控制 (17) 2.3样本取用和运输 (20) 2.3.1样本的内部转移 (20) 2.3.2样本的使用 (20) 2.3.3样本运输 (24) 2.4样本销毁 (33) 2.4.1样本销毁的申请审核 (33) 2.4.2样本的销毁 (34)
2.样本 样本库采集和储存的样本是组织和血液等的人体生物样本,以及附着在这些样本上的所有相关信息。 样本库最基本的内容是在获得捐赠者的知情同意后对样本进行采集和储存,拥有对样本的保管权,并对样本的取用、运输和销毁进行管理,保护样本的质量和完整性。 样本在采集、储存、取用、运输和销毁上有着不同的目的和方法,都必须符合国家相关法律法规和伦理的要求。 2.1样本采集 2.1.1样本采集的要求 采集的样本应符合一定的要求,以保证样本的质量,使采集的样本成为具有价值的资源。样本的来源、用途、种类,采集的时间、地点、人员和方法都对样本的质量产生影响,采集前我们必须确认好相关的信息,做好充分的准备。 2.1.1.1符合伦理道德的要求 样本采集必须在捐赠者知情并且与样本库签订《知情同意书》后进行,得到的样本应首先满足捐赠者在病理诊断上的需求,剩余的部分才能作为样本由样本库进行处理和储存。 样本采集涉及捐赠者的隐私和其他保密的信息必须进行保密。 伦理道德相关的内容将在第5章中详细展开。 2.1.1.2采集有价值的样本 样本采集前应对计划采集样本的价值进行评估,避免重复采集和采集不需要的样本,保证捐赠者的利益和提高样本库的样本水平。
CCGC文件4 生物标本采集技术规范及 数据库建立指南 (讨论稿) 2006年12月制定 2009年12月修订 国家863 “肿瘤分子分型与个体化诊治”项目组 “肿瘤基因组”研究重大项目组 中国医药生物技术协会组织生物样本库分会
目录 简介 (1) 背景 (3) 指南概述 (4) 一、技术标准和标准化操作指南 (4) 二、伦理、法律和法规 (6) 生物样本采集和保存操作指南实施细则 (9) 一、采集的生物样本种类 (9) 二、生物样本的贮存和加工 (10) 三. 临床资料的收集和数据管理 (11) 四. 生物样本采集SOPs (Standard Operation Procedure)手册 (12) 附件1:关于使用组织样本开展科学研究的知情同意书 (14) 附件2:伦理委员会审核意见书 (17) 附件3:为何要使用生物样本进行科学研究的问答 (18) 附件4:生物样本交接协议书 (20) 附件5:肿瘤样本采集的基本技术标准 (23) 样本采集登记表 (24) 附件6:项目合作协议 (25) 附件7:临床研究队列入组标准 (26) 附件8:国际肿瘤基因组协作研究(ICGC)肿瘤组织样本质量标准 (27)
简介 目前在世界范围内开始进行肿瘤分子分型和个体化诊治的研究。这项研究能否获得实质性进展取决于一个最基本的问题,即研究用生物样本的质量和数量,包括符合临床诊治规范的临床研究队列,高质量、严格按照SOPs收集的组织样本和详细的临床、病理、治疗与随访等资料。 实际上做到这一点在操作上有相当的难度。以科技最发达的美国为例,为了保证高质量标本采集和完整数据库的建立,过去的多年中美国国立癌症研究(NCI )每年都投入约5000多万美金的专项基金用于生物资源标本库的建立; Relax — it's not your money they're after.近期,Folks at the National Cancer Institute (NCI) are heading up an effort to establish the US's first national biobank — a safe house for tissue samples, tumor cells, DNA and, yes, even blood — that would be used for research into new treatments for diseases.美国NCI正在为建立美国第一个国家“生物银行”而奔走努力。“生物银行”是一个存放组织样本,肿瘤细胞、DNA甚至血液的生物样本库----主要用于研究治疗疾病的新方法。目前,美国国立癌症研究所(NCI),生物资源和生物样本(OBBR)办公室正在努力从事这项工作。预计近期By fall, the group hopes to have mapped out a plan for a national biobank; the recent stimulus showered on the government by the Obama Administration might even accelerate that timetabl可制订出筹建国家“生物银行”的实施计划,奥巴马政府也在积极促成这一计划的实现。 其中还不包括大量研究课题本身具有采集生物样本的任务。其他发达国家均以类似的方式进行这项工作中。这项工作最大的问题是如何按照相对统一的标准进行样本采集和开展研究工作。因为,这样一项研究决不可能由一个单位或几个实验室完成,以近来发表在NATURE 的几种疾病基因变异相关性研究,所用的病例数达到14,000,共同对照3000,参与的医疗机构超过百余个。我国的一项发表在NATURE GENETICS的基因多态性与肿瘤相关性研究,采用的病例和对照分别达到近5000例。这一结果表明,研究队列和生物样本是决定我国在这一领域中自主创新能力和国际竞争力的关键问题。 已有事实表明,现代肿瘤研究是以规范化诊治的多中心临床队列建立为基础;以获得高质量肿瘤样本和系统临床随访资料为核心。这二项已成为国际生物医药领域竞争的决定性因素,也是转化医学研究的基础。 因此集成我国肿瘤资源、人才和技术的优势,发挥我国在肿瘤研究领域的作用,提升创新能力和参与国际竞争具有重要意义。 目前,我国在这一领域已具备一定的条件。许多大型医疗科研机构已开展了一些关于生物样本采集和临床数据库建立的工作。但是,这些生物样本采集工作基本上是科研人员自发的、零散的、缺乏系统的设计和规范。主要目的是为眼前的课题研究,无固定经费支持,缺少具有法律保障的伦理监督、缺乏长远打算,管理使用无序,低水平重复和浪费现象严重。 为了促进我国人口与健康领域战略目标的实现、建立和推动我国“组学及系统生物学”整合医学和转化医学的发展,特别是提升我国在这一领域的整体创新能力和国际竞争力。建立国家层面上的生物样本库,将包括肿瘤在内的重大疾病和高危人群研究队列建立、生物资
临床微生物学标本采取和处理的规范化要求 正确的采取、处理与运送用于细菌培养的标本是临床细菌检验成功的关键。标本采取与处理的规范化是准确、及时地向临床提供重要的临床感染信息的基础;而标本采取与处理不当将严重影响检验结果,给临床以误导,延误对患者的正确治疗。为此,我们提出初步的参考意见,并希望在实践中不断完善。 一、血液细菌培养标本的采集和处理 临床上疑为败血症、脓毒血症或其他血液感染的患者,需做血液细菌培养以明确病原。 1.采集方法:静脉采血,以无菌操作方法抽取血液后,直接注入血培养瓶中,轻轻颠倒混匀,以防血液凝固。如果同时作需氧和厌氧培养,应先将标本接种到厌氧瓶中,再注入需氧瓶,严格防止将空气注入厌氧瓶中。 2.采血时间以及血培养份数:在患者发热期间越早越好,最好在抗菌治疗前,用药前24小时内采集2~3次血液标本,可使细菌检出率高达99%。对间歇性寒战或发热的患者,应在寒战或体温高峰到来之前0.5~1小时采血,亦可在寒战或发热后1小时采集血液标本。特殊感染患者采血培养时应遵循以下原则: (1)可疑急性发热性菌血症、败血症患者:应在使用抗菌药物之前,在24小时内从不同部位采集2~3份血液标本培养。 (2)可疑细菌性心内膜炎患者、感染性心内膜炎患者:在1~2小时内采集3份血标本培养,如果24小时后阴性,再采集两份血标本培养。 (3)不明原因发热患者:先采集2~3份血标本,抽血间隔60 min,24~36小时后体温升高之前,再采集2份血标本进行培养。因为1次血培养不足以说明问题,可能会遗漏阳性结果。 (4)可疑菌血症但血培养持续阴性时;应改变血培养方法,以获得罕见或苛养的微生物。 (5)在急性发热性疾病如脑膜炎、细菌性肺炎,需马上做抗菌治疗;或急性骨髓炎、化脓性关节炎等要紧急手术的患者,应立即从两臂分别取2份标本。 3.采血部位:采血部位通常为肘静脉。疑为亚急性心内膜炎的患者,以肘动脉或股动脉采血为宜。疑为细菌性骨髓炎或伤寒患者,在病灶或髂前(后)上棘处严格消毒后抽取骨髓。多次采血应在不同部位的血管穿刺以排除皮肤菌丛污染的可能。要避免从血管插管内取血,因插管常被污染,其培养结果不能反映真实情况。
临床试验生物样本采集的标准操作规程 版本号 1.0 页数2页 起草人起草日期年月日审核人审核日期年月日批准人批准日期年月日颁布日期年月日起效日期年月日 威海市立医院 药物临床试验机构
临床试验生物样本采集的标准操作规程 一、目的 建立机构办公室对临床试验中生物样本采集的管理工作。确保生物样本采集规范、一致并符合方案要求,用以监督和提高临床试验质量,保障临床试验顺利进行。 二、范围 适用于在本机构开展的药物临床试验的生物样本采集。 三、内容 1.血液标本的采集: 1)核对:医嘱、采血点、标本容器与受试者身份证信息一致性。 2)评估:根据受试者病情、进食情况、正在进行的静脉药物治疗;肢体活动情况和静脉情况;穿刺部位皮肤情况;受试者沟通、理解及合作能力;手套、止血带、采血针、 采血管、消毒用物、弯盘,摆放位置合理等。 3)告知:受试者及其家属采集血样标本的目的和配合方法。 4)实施: ?选择合适的静脉、穿刺点,在穿刺上方约6cm处系止血带,常规消毒皮肤,嘱受 试者握拳。 ?戴手套:拔除采血针的护套,一手固定血管,另一手拇指和食指持穿刺针,按静 脉穿刺法穿刺血管;见回血后将胶塞穿刺针直接刺入血管的胶塞盖的中央,血液 被自动吸入采血管内;如须采多管血样,将刺塞针反折拔出后再次刺入另一采血 管。 ?嘱患者松拳,同时松止血带,迅速拔出针头,用干棉签按压穿刺点1-2分钟/次。 ?含抗凝剂的采血管要立即上下摇匀8次。 ?采用注射器采血的,拔出针头后须取下针头,将所需血量沿管壁注入采血容器中, 如有抗凝剂药充分摇匀。 5)整理记录: ?协助受试者取舒适体位。
?按《医疗废物处理条例》处置用物,脱手套、洗手。 ?再次核对医嘱、采血点、受试者身份、标本、条形码等信息,并记录在《生物样 本(血样)采集记录表》 2. 尿液标本的采集 1)核对:医嘱、采尿点、采尿管、标本容器与受试者身份证信息一致性。 2)评估:受试者沟通、理解与自理能力以及排尿情况及需求;采尿杯、标本容器。 3)告知:受试者及其家属采集尿标本的目的和配合方法。 4)实施: ?可下床活动的受试者,给予容器,嘱取清晨第一次尿液10-50ml于容器中送检。 ?行动不便的受试者,协助在床上使用便器后,留取足量的尿液于容器中送检。 ?留置导尿管的受试者留取尿标本时,先放空尿袋的尿,待重新有尿排出后再打开 尿袋下方引流孔处橡胶塞收集尿液送检。 5)整理记录: ?协助受试者取舒适体位。 ?按《医疗废物处理条例》处置用物,脱手套、洗手。 ?再次核对医嘱、采血点、受试者身份、标本、条形码等信息,并记录在《生物样 本(尿)采集记录表》 四、参考资料 1国家食品药品监督管理总局令第3号发布《药物临床试验质量管理规范》,2003 2国家食品药品监督管理总局.卫生部文件,国食药监注[2011]482号.关于印发药物临床试验生物样本分析实验室管理指南(试行)的通知,2011 五、工作表格 1《生物样本(血样)采集记录表》(文件编号:JG-form-029-1.0) 2《生物样本(尿)采集记录表》(文件编号:JG-form-030-1.0)