
北京大学2000年研究生入学考试试题
考试科目:物理化学(含结构化学)考试时间:1月23日上午 招生专业: 研究方向: 指导教师:
试 题:(答案一律写在另发的答题纸上)
常数 k B =1.38×10-23J ·K -1,h =6.62×10-34J ·s
一.(10分)将某纯物质液体用活塞封闭在一个绝热筒内,温度为T 0,活塞对液体的
压力正好是液体在T 0时的蒸汽压P 0,设该液体的物态方程为: V m =V m,0{1+α(T-T 0)-κ(P-P 0)}
式中V m,0是液体在T 0 、P 0时的摩尔体积,α与κ分别是体膨胀系数和等温压缩系数,并为常数。将液体经绝热可逆过程部分气化,使液体温度降至T ,此时液体蒸汽压为P ,试证明液体所气化的摩尔分数为
)}P P (V T
T ln C {H T
n m x 00,m 0l m ,P m g l --?==
α 式中n 为气化前液体物质的量,m 为变成蒸气的物质的量,l m ,P C 为液体物质的摩尔等压热容,m g l H ?是该物质在时的摩尔气化焓。
二.(6分)已知溶液A 、B 中的活度系数γA 和γB 满足下列关系 P T B
B
P T A A )lnx ln ()lnx ln (
,,γ=γ???? 当溶液的平衡气相(设为理想气体)中A 的分压P A 服从下列关系
})x 1exp{(x P P 2A A *A A α?-=
式中*A P 为纯A 液体的蒸气压,α为常数,请证明溶液中B 的活度系数γB 与x B 的
关系式为:})x 1exp{(2B B
αγ
?-=
三. (8分)银可能受到H 2S 气的腐蚀而发生下列反应:
)g (H )s (S Ag )s (Ag 2)g (S H 222+→+
298.2K 时,12m r mol kJ 25.40)s ,S Ag (G -θ?-=?,12m r mol kJ 93.32)g ,S H (G -θ?-=?
(1) 在298.2K ,P 0=101.3kPa 下,H 2S 与H 2混和气体中,H 2S 的摩尔分数低于多
少时便不致使Ag 发生腐蚀?
(2)该平衡体系的最大自由度f
max
为几?
四. (8分)1mol纯物质理想气体,分子的某内部运动形式只有三个可及能级,各能
级的能量(ε
i )和简并度(ω
i
)分别为其中ε
1
=0,ω
1
=1;ε
2
/k
B
=100K,ω
2
=3;ε
3/k
B
=300K,ω
3
=5,其中k
B
为Boltzmann常数。
(1)计算该内部运动形式在200K时之分子配分函数。
(2)计算200K时,能级ε
2
上在最概然分布时之分子数(总分子数为L=6.023×1023mol-1)
(3)当∞
→
T时,求三个能级上最概然分子数之比。
五.(8分)Nd-Fe-B是高性能永磁材料,但Nd和Fe的熔点很高,且Nd又很活泼,
故不能采用纯物质直接生产Nd-Fe-B磁性材料,而往往采用先制备富含Nd的Nd-Fe合金再掺合B。
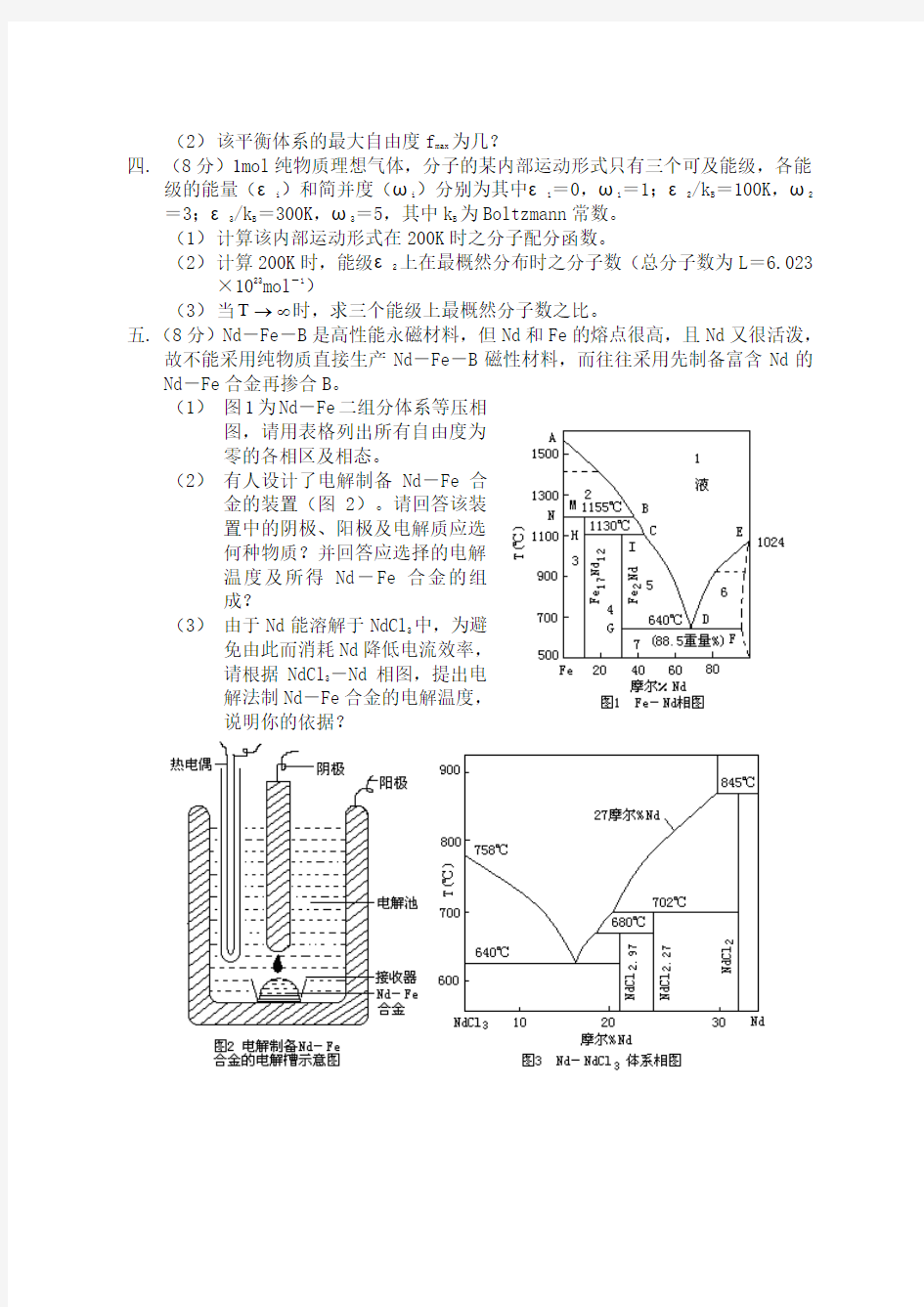
(1)图1为Nd-Fe二组分体系等压相
图,请用表格列出所有自由度为
零的各相区及相态。
(2)有人设计了电解制备Nd-Fe合
金的装置(图2)。请回答该装
置中的阴极、阳极及电解质应选
何种物质?并回答应选择的电解
温度及所得Nd-Fe合金的组
成?
(3)由于Nd能溶解于NdCl
3
中,为避
免由此而消耗Nd降低电流效率,
请根据NdCl
3
-Nd相图,提出电
解法制Nd-Fe合金的电解温度,
说明你的依据?
六.(10分)气相光气合成反应:CO (g )+Cl 2(g )=COCl 2(g )是一个二级反应(对
CO 及Cl 2各为一级反应)。CO 及Cl 2的初始压力均为100kPa 。在25.0℃及35.0℃反应的半衰期分别为60.0分钟和30.0分钟。 (1) 计算25.0℃时的速率常数k 。 (2) 计算反应的活化能E a 及指前因子A 。
(3) 设此反应为双分子反应,计算反应在25.0℃时的活化熵θ≠?m S 及活化焓
θ≠?m H
七.(10分)电池Ag|AgCl|HCl (m )|H 2(P )|Pt (1) 写出电极反应及电池反应。 (2) 导出电池电动势的计算式(含有活度系数及可测量的量)。 (3) 具体说明如何测量电池电动势的方法求氯化银电极的标准电极电势的标准
值,为此还需要哪些数据? (4) 请具体说明如何用电动势来计算K sp (AgCl ),为此还需要哪些具体数据? 上述问题中(3)、(4)都必需导出定量计算式,条件:T =298.2K ,P =101.325kPa 。 八.(12分)
(1) 角动量的z 轴分量为M z =xP y -yP x ,请写出其算符z M
?。 (2) 按原子单位写出核不动近似条件下Li +的Schr?dinger 方程,计算其能量。
(3) 计算氢原子5d 轨道的磁矩及其在z 轴方向上的最大分量。 (4) 判断下列分子或离子所属的点群,指明它们是否有旋光异构体。
42H C -3CH 624)CH (N +33)en (Co (en :乙二胺)
九.(12分) (1) 下图是近似等摩尔的CH 4、CO 2和CF 4的气态混合物的XPS (碳1S 信号),
请指明A 、B 、C 三个峰各代表什么化合物。
(2) 下图是平面周期性结构的一部分,请画出该结构的点阵素单位,指出结构
基元。
(3) 试画出CH 3CH 2Br 的NMR 的基本图形。 (4) 在下图中,圆圈内的数字1、2、3、4表示等径圆球在z 方向上的坐标分别
为0,41
,42,4
3。请指出在Z 方向上A 、B 两处各有什么微观对称元素。
十.(4分)
(1) 某共轭双烯分子的久期行列式如下:
0X
1011X 100
1X 11
01X =
请画出该分子的骨架,给碳原子编号。 (2) 用HMO 法求得该分子的π型分子轨道如下:
)+φ+φ+φ(φ=ψ4321121 )φφ+φ(φ=ψ4321221--
)+φφφ(φ=ψ4321321-- )φ+φφ(φ=ψ432142
1--
请计算1和4两碳原子间π键的键级。
十一.(12分)
某立方晶系的金属晶体,用CuK α射线(λ=154.2pm )摄取其粉末衍射图,测得各衍射线的2θ角如下:44.62o 51.90o 76.45o 93.06o 98.57o 122.12o 145.0o 156.16o (1) 将各衍射线指标化。
(2)确定该晶体的空间点阵型式。
(3)求算该晶体的晶胞参数。
(4)实验测得该金属的密度为8.908g·cm-3,若将其结构视为等径圆球的密堆
积结构,试计算其摩尔质量。
(5)用点阵面指标表示该金属密置层的方向,计算相应的点阵面间距。
(6)用分数坐标表明该金属晶体中八面体空隙中心的位置。
天津大学《物理化学》第五版习题及解答 目录 第一章气体的pVT性质 (2) 第二章热力学第一定律 (6) 第三章热力学第二定律 (24) 第四章多组分系统热力学 (51) 第五章化学平衡 (66) 第六章相平衡 (76) 第七章电化学 (85) 第八章量子力学基础 (107) 第九章统计热力学初步 (111) 第十一章化学动力学 (118)
第一章气体的pVT性质
1.1 物质的体膨胀系数与等温压缩率的定义如下 试推出理想气体的,与压力、温度的关系。 解:根据理想气体方程 1.5 两个容积均为V的玻璃球泡之间用细管连结,泡内密封着标准状态下的空气。若将其中的一个球加热到100 °C,另一个球则维持0 °C,忽略连接细管中气体体积,试求该容器内空气的压力。 解:由题给条件知,(1)系统物质总量恒定;(2)两球中压力维持相同。 标准状态: 因此, 1.9 如图所示,一带隔板的容器内,两侧分别有同温同压的氢气与氮气,二者均可视为理想气体。
(1)保持容器内温度恒定时抽去隔板,且隔板本身的体积可忽略不计,试求两种气体混合后的压力。 (2)隔板抽取前后,H2及N2的摩尔体积是否相同? (3)隔板抽取后,混合气体中H2及N2的分压立之比以及它们的分体积各为若干?解:(1)等温混合后 即在上述条件下混合,系统的压力认为。 (2)混合气体中某组分的摩尔体积怎样定义? (3)根据分体积的定义 对于分压 1.11 室温下一高压釜内有常压的空气,为进行实验时确保安全,采用同样温度的纯氮进行置换,步骤如下:向釜内通氮气直到4倍于空气的压力,尔后将釜内混合气体排出直至恢复常压。重复三次。求釜内最后排气至恢复常压时其中气体含氧的摩尔分数。 解:分析:每次通氮气后至排气恢复至常压p,混合气体的摩尔分数不变。 设第一次充氮气前,系统中氧的摩尔分数为,充氮气后,系统中氧的摩尔分数为 ,则,。重复上面的过程,第n次充氮气后,系统的摩尔分数为 , 因此 。 1.13 今有0 °C,40.530 kPa的N2气体,分别用理想气体状态方程及van der Waals方程计算其摩尔体积。实验值为。
北京大学教师职务聘任推荐审批表姓名徐风 工作证号76091 校内单位药学院 现任职务助理研究员 拟聘职务副教授 填表日期2017年7月10日
填表说明 1. 申请聘任北京大学教师、医师、研究系列职务时,均填写本表。 2. 填写的内容要具体、真实。用钢笔填写或打印,字迹要端正、清楚。打印或复印时请保持本表格式、A4纸双面复印,左侧装订。 3. 若加附页,请严格依照本表的格式与大小,附页页码标为“附页*a、附页*b”等,如第7页加附页,页码为“附页7a”、“附页7b”。 4. 本表1~8页由本人填写,由所在单位审核。 5. 第2页学历历史及工作经历请从中学填起,按自然时间顺序填写。学历分中学、大学本科、硕士、博士等阶段;工作经历按不同工作单位任不同职务经历的顺序填写;博士后阶段属于一个工作经历段。在职学习者,学历时间和工作经历时间可重复。 6. 第5页的教学情况中,课程类别指:本科生或研究生基础课、专业基础课、专业课、实验课、实践课等(可咨询教学管理部门)。 7. 第7页填写反映本人任现职以来所取得的学术成果,包括论(译)著、教材、研究报告等。各项成果请按顺序注明全部作者、论著名称、出版单位、出版时间或刊物名称(出版地)、卷、期、年份。被SCI、SSCI、EI收录或引用的,请注明收录、引用情况。 8. 第8页说明任现职以来承担过的科研项目的项目名称、起止时间、本人承担的工作部分、总经费及本人承担经费、项目完成情况。已验收的项目请注明验收结论,获奖项目请注明所有获奖者顺序、获奖名称和等级、授奖单位、授奖时间。 9. 第13~18页为活页,双面复印,不用装订,只填写带*的内容。
物理化学测验题(六) 一、选择题。在题后括号,填上正确答案代号。 1、接触角是指: (1)g/l界面经过液体至l/s界面间的夹角; (2)l/g界面经过气相至g/s界面间的夹角; (3)g/s界面经过固相至s/l界面间的夹角; (4)l/g界面经过气相和固相至s/l界面间的夹角; 2、朗缪尔公式克描述为:( )。 (1)五类吸附等温线; (2)三类吸附等温线; (3)两类吸附等温线; (4)化学吸附等温线。 3、化学吸附的吸附力是:( )。 (1)化学键力;(2)德华力; (3)库仑力。 4、温度与表面力的关系是: ( )。 (1)温度升高表面力降低; (2)温度升高表面力增加; (3)温度对表面力没有影响; (4)不能确定。 5、液体表面分子所受合力的方向总是:( ),液体表面力的方向总是:( )。 (1)沿液体表面的法线方向,指向液体部; (2)沿液体表面的法线方向,指向气相; (3)沿液体的切线方向; (4)无确定的方向。 6、下列各式中,不属于纯液体表面力的定义式的是: ( ); (1)p T A G ,??? ????; (2) p T A H ,??? ???? ; (3) V T A F ,? ?? ???? 。 7、气体在固体表面上吸附的吸附等温线可分为:( )。 (1)两类; (2)三类; (3)四类; (4)五类。 8、今有一球形肥皂泡,半径为r ,肥皂水溶液的表面力为σ,则肥皂泡附加压力是:( )。 (1)r p σ2=? ;(2)r p 2σ =?;(3)r p σ 4=?。 9、若某液体能在某固体表面铺展,则铺展系数?一定:( )。 (1)< 0; (2)> 0;(3)= 0。 10、等温等压条件下的润湿过程是:( )。 (1)表面吉布斯自由能降低的过程; (2)表面吉布斯自由能增加的过程;
关于北京大学政府管理学院-伦敦政经学院政府系 公共政策双硕士学位项目(英文授课)的说明 1.学位 (1)北京大学政府管理学院与伦敦政经学院政府系联合推出双硕士项目。这个双硕士项目将授予学生双学位,即北京大学管理学(公共政策)硕士学位(英文表述为Master of Management in Public Policy)和伦敦政经学院公共政策硕士学位。 (2)本项目授予学位为绑定学位,学生必须完成北大和伦敦政经全部课程并合格通过所有考核后才能获取北京大学管理学硕士学位和伦敦政经学院公共政策硕士学位,如果无法完成该项目的全部课程或不能达到两校的毕业要求,则不能单独获得北京大学公共政策硕士学位或伦敦政经学院公共政策硕士学位。如果学生想单独获得北京大学硕士学位,则须继续修满北京大学正常硕士学位要求的全部学分(10门课,共30学分)。 2.招生 2010-11年度计划在全球招生9至12人。中国籍学生必须首先通过正常的保研或考研程序被北京大学政府管理学院公共管理一级学科录取。 3.学制 学制为两学年(至三学年),即一学年在北京大学政府管理学院学习(简称北京学年),另一学年在伦敦政经学院政府系学习(简称伦敦学年),如有第三学年则为备用学年。 4.北京学年 (1)基本介绍 北京学年的学习由北京大学政府管理学院进行安排和管理。该项目的教职人员主要来自政府管理学院,同时也有来自北京大学其他院、系、中心的师资力量。 (2)基本要求 学生须修满6门3学分课程并完成硕士毕业论文以获得硕士学位。学生可选择以英文和中文授课的课程(6门中至少4门为英文授课的课程),并可以选择用英文或中文完成毕业论文。 (3)课程要求 必修课: Chinese Politics and Public Policy(中国政治与公共政策) Ch ina’s Economic Development and Reform(中国的经济发展与改革) A Research Design Course(一门研究设计课)
一、选择题 1、下列说法中不正确得就是:( C ) (A) 生成得新鲜液面都有表面张力 (B)平面液体没有附加压力 (C)弯曲液面得表面张力得方向指向曲率中心 (D)弯曲液面得附加压力指向曲率中心 2、 水在临界温度时得表面Gibbs自由能: (C ) (A)(A)大于零(B) 小于零 (C)等于零 (D)无法确定 3、 一个 U 型管得两臂直径不同,一端为1×10-3 m,另一端为 3×10—3 m,水得表 面张力为0、072 N·m-1。如用这个 U 型管装上水来测量压力,将引入得误差为: ( B ) (A) 72 Pa (B) 192 Pa (C) 96 Pa (D)288 Pa 4、 低压下,气体 A 在表面均匀得催化剂上进行催化转化反应,其机理为: A(g) + KA K ─→ B(g) + K 第一步就是快平衡, 第二步就是速控步,则该反应表观为几级? ( B ) (A)零级???? (B)一级 ?(C) 二级????(D) 无级数 5 、表面过程中ΔG(表面)=-W'得充要条件除了等温等压外,还有:(D) A,不做其它功; B,热力学可逆; C,组成不变; D,就是B与C。 6、物质表面张力得值与:( C ) A,温度无关; B,压力无关; C,表面大小无关; D,另一相物质无关。 7、以P平、P凸、P凹分别表示平面、凸面、凹面液体上得饱与蒸汽压,三者关系为: ( B ) A,P平>P凹>P凸;B,P凸〉P平>P凹; C,P凸〉P凹〉P平; D,三者相同. 8、常见亚稳态现象都与表面性质有关,下面说法正确得就是:(D ) A,过饱与蒸气就是由于小液滴得蒸气压小于大液滴得蒸气压所致; B,过热液体形成原因就是新相种子-—小气泡得附加压力太小; C,饱与溶液陈化、晶粒长大,因为小晶粒溶解度比大晶粒大; D,人工降雨时在大气中撒入化学物质主要得目得就是促进凝结中心形成 9、对亲水性固体表面,其相应接触角θ就是:( B ) A,θ>90°; B,θ<90°;C,θ=180°;D,θ可为任意角 1O、Langmuir吸附理论中说法符合基本假定得就是:( A )
第五章 化学平衡 5-1.在某恒定的温度和压力下,取n 0﹦1mol 的A (g )进行如下化学反应:A (g ) B (g ) 若0B μ﹦0 A μ,试证明,当反应进度ξ﹦0.5mol 时,系统的吉布斯函数G 值为最小,这时A ,B 间达到化学平衡。 解: 设反应进度ξ为变量 A (g ) B (g ) t ﹦0 n A , 0﹦n 0 0 ξ0﹦0 t ﹦t 平 n A n B ξ ξ﹦ B B n ν n B ﹦νB ξ,n A ﹦n 0-n B ﹦n 0-νB ξ,n ﹦n A +n B ﹦n 0 气体的组成为:y A ﹦ A n n ﹦00 B n n νξ-﹦01n ξ-,y B ﹦B n n ﹦0 n ξ 各气体的分压为:p A ﹦py A ﹦0 (1)p n ξ - ,p B ﹦py B ﹦ p n ξ 各气体的化学势与ξ的关系为:0 000ln ln (1)A A A A p p RT RT p p n ξμμμ=+=+- 0 000ln ln B B B B p p RT RT p p n ξμμμ=+=+? 由 G =n A μA +n B μB =(n A 0A μ+n B 0 B μ)+00ln (1)A p n RT p n ξ-+0 ln B p n RT p n ξ ? =[n 0-ξ0A μ+ξ0 B μ]+n 00ln p RT p +00()ln(1)n RT n ξξ--+0 ln RT n ξ ξ 因为 0B μ﹦0A μ,则G =n 0(0 A μ+0ln p RT p )+00()ln(1)n RT n ξξ--+0 ln RT n ξ ξ ,0()ln T p G RT n ξξξ?=?- 20,20()()T p n RT G n ξξξ?=-?-<0 令 ,( )0T p G ξ?=? 011n ξξξξ ==-- ξ﹦0.5 此时系统的G 值最小。
硕士研究生学位论文题目:标题 姓名: 学号: 院系: 专业: 研究方向: 导师姓名: 二〇一年月
版权声明 任何收存和保管本论文各种版本的单位和个人,未经本论文作者同意,不得将本论文转借他人,亦不得随意复制、抄录、拍照或以任何方式传播。否则,引起有碍作者著作权之问题,将可能承担法律责任。
摘要 摘要 某某问题是……. 本文①采用了…… 研究表明……. 关键词:关键词1,关键词2,关键词3…… ①本研究得到某某基金(编号:XXX)资助。
北京大学硕士学位论文 ENGLISH TITLE Author Name( Major ) Directed by your Supervisor ABSTRACT In environmental economics, environmental resources including environmental quality are categorized as amenity resources. Due to its importance to human welfare, the amenity resources theoretical study and valuation is an ongoing issue at the academic frontier in the environmental economics area. KEY WORDS: Keyword 1, Keyword 2, Keyword 3, ……
<目录 目录 摘要............................................................................... I ABSTRACT .......................................................................... II 目录............................................................................. III 第一章引言. (1) 1.1Ⅲ族氮化物(GaN 基半导体)材料的基本性质 (1) 1.1.1Ⅲ族氮化物半导体的晶体结构 (1) 第二章研究进展 (2) 2.1环境中黑炭的主要来源 (2) 第四章图表示例 (4) 第五章结论及展望 (5) 参考文献 (6) 附录A 附录示例 (8) 致谢 (9) 北京大学学位论文原创性声明和使用授权说明 (10) 注:目录从第1章开始,前边因页眉需要设置了标题,实际使用时更新后去掉前边部分。使用时请删除本注释。如本示例,更新目录后删除前边三项(摘要、ABSTRACT、目录)即可。
中南大学研究生考试试卷 2009— 2010学年二学期期末考试试题时间110分钟 表面物理化学化学课程32学时2.0学分考试形式:开卷 专业班级:姓名学号 卷面总分100分,占总评成绩 70 %,卷面得分 一、选择题(每小题2分,共20分) 1.液体表面最基本的特性是( A ) A.倾向于收缩 B.倾向于铺展 C.形成单分子吸附层 2.若将液体与毛细管壁间的接触角近似看作0°,则液体在毛细管中的液面可以看作( C ) A.凹型 B.凸型 C.球面 3.下列方程均为计算液a/液b界面张力γab的经验公式,其中Fowkes公式为( C ) A.γab =γa -γb B.γab =γa + γb -2(γaγb)1/2 C.γab =γa + γb -2(γa dγb d)1/2 4.吊片法测定液体表面张力时,要求尽可能采用表面粗糙的吊片材料,其目的是( A ) A.改善液体对吊片的润湿使θ接近于0° B. 改善液体对吊片的润湿使θ接近于90° C.改善液体对吊片的润湿使θ接近于180° 5.溶液中溶剂记为1、溶质记为2,则吸附量Γ2(1)的含义为( C ) A.单位面积表面相与含有相等总分子数的溶液相比较,溶质的过剩量 B.单位面积表面相与含有等量溶质的溶液相比较,溶剂的过剩量 C.单位面积表面相与含有等量溶剂的溶液相比较,溶质的过剩量 6.C12H25SO4Na(1)、C14H29SO4Na(2)、C16H33SO4Na(3)三种物质在水表面吸附达到饱和状态时,三种物质分子在表面所占面积a m存在下列关系( B ) A. a m,1> a m,2> a m,3 B. a m,1≈a m,2≈a m,3 C. a m,1< a m,2< a m,3 7.苯在水面上先迅速展开后又自动收缩成为小液滴漂浮在水面上,用于描述苯液滴形状的表化专业术语是( C ) A.二维液膜 B.多分子层 C.透镜 8.下列说法中不正确的是( C ) A.任何液面都存在表面张力 B.平面液体没有附加压力 C.弯曲液面的表面张力方向合力指向曲率中心 D.弯曲液面的附加压力指向曲率中心 9.运用过滤手段进行溶胶净化的目的是( B ) A.除掉反应过程中过量的副产物 B.除掉过量的电解质 C.除掉溶胶体系中的粗离子 10.对于胶体体系下列说法正确的是( B ) A.电解质引发胶体体系聚沉的主要原因是使扩散层变厚 B.低浓度的聚合物可以使胶体体系发生聚沉,而高浓度的聚合物却可以使胶体体系稳定 C.胶体体系属于热力学多相体系,由于界面自由能显著,所以无论采取何种措施都不可 能获得相对稳定的胶体溶液 二、填空题(每小题2分,共20分) 1.液-固润湿过程有_沾湿_ ,_ 浸湿_ , _铺展_ . 2.固体自溶液中吸附时,极性吸附剂易于从非极性溶液中吸附__极性_____物质,而非极 性吸附剂易于从极性溶液中吸附__非极性____物质。
1、用H3PO4(pKa1= 2.16,pKa2= 7.21,pKa3= 12.32)和NaOH所配成的pH = 7.35的缓冲溶液中,抗碱成分是()(4 分)A.H3PO4 B.H2PO4- C.HPO42- D.PO43- 我的答案:B 得分:4分 2、对于一个化学反应,下列说法中正确的是()(4 分)
A.越负,反应速率越大 B.越负,反应速率越大 C.活化能越大,反应速率越大 D.活化能越小,反应速率越大 我的答案:D 得分:4分 3、蛋白质发生盐析的主要原因是()(4 分)A.电解质离子强烈的水化作用使大分子去水化 B.蛋白质所带的电荷发生了变化
C.由于电解质的加入,使大分子溶液处于等电点 D.蛋白质上基团的解离情况发生了变化我的答案:A 得分:4分 4、已知某蛋白的pI = 5.6,欲使该蛋白移向正极,则电泳液的pH应()(4 分)A.<5.6 B.=5.6 C.>5.6 D.无法确定
我的答案:C 得分:4分 5、聚沉As2S3负溶胶,下列电解质中聚沉能力最强的是()(4 分) A.Ca(NO3)2 B.K2SO4 C.Na3PO4 D.AlCl3 我的答案:D 得分:4分
6、溶胶在一定时间内能稳定存在而不聚沉,主要原因是()(4 分) A.溶胶的分散相粒子很小 B.溶胶的分散相粒子很大,扩散速度慢C.溶胶的胶粒呈均匀分布,是均相系统D.胶粒带电,相互排斥;胶粒带有水化膜保护,阻止彼此碰撞时聚结沉淀 我的答案:D 得分:4分 7、溶胶的丁铎尔(Tyndall)现象的本质是胶粒对光的()(4 分) A.透射作用
北大考博辅导:北京大学会计学考博难度解析及经验分享根据教育部学位与研究生教育发展中心最新公布的第四轮学科评估结果可知,在在校友会版2017-2018会计学专业大学排名中,会计学专业排名第一的是清华大学,排名第二的是厦门大学,排名第三的是北京大学。 作为北京大学实施国家“211工程”和“985工程”的重点学科,光华管理学院的会计学一级学科在历次全国学科评估中均名列第三。 下面是启道考博整理的关于北京大学会计学考博相关内容。 一、专业介绍 会计学专业是以会计学、审计学、财务管理为基础的基本理论应用学科,以经济学、管理学的基本理论和知识为基础,主要学习财务会计的基础理论和基本技能,资本运营、资产重组、企业兼并方面的专业知识和国际会计核算的惯例,同时注重培养学生的实践能力,侧重于实务操作,通过会计手工模拟室和会计电算化实验室的基本训练能,培养学生分析和解决会计实际问题的基本能力和综合能力,同时注重强化学生财务管理、审计、经济法、税法方面知识的学习,为学生以后参加注册会计师考试打下坚实的专业基础。 北京大学光华管理学院的会计学专业在博士招生方面,不区分研究方向 120201 会计学 研究方向:00.不区分研究方向 此专业实行申请考核制。 二、考试内容 北京大学会计学专业博士研究生招生为资格审查加综合考核形式,由笔试+专业面试构成。其中,综合考核内容为: 学院组织所报考专业专家小组对申请人进行综合评议。同时根据招生计划,按照一定的比例择优确定复试名单。初审结果和复试名单将于2019年3月邮件通知。 1、复试时间及方式:一般安排在3月下旬。复试采取笔试加面试的方式进行差额甄选,对学生的学科背景、专业训练和素质、分析和操作技能、外语水平、思维能力、创新能力等各方面进行综合考察。 2、笔试:即基础能力测试,按报考专业分别测试。 (1)对于报考应用经济学专业的学生,第一部分是高级微观经济学;第二部分是高级宏观经济学和计量经济学;两部分分值各占50%。
物化第8-10试卷 一、选择题 1. 物质表面张力的值与:( C ) A.温度无关B.压力无关C.表面大小无关D.另一相物质无关 2.在液面上,某一小面积S周围表面对S有表面张力,下列叙述不正确的是( A )A.表面张力与液面垂直; B.表面张力与S的周边垂直; C.表面张力沿周边与表面相切; D.表面张力的合力在凸液面指向液体内部(曲面球心),在凹液面指向液体外部。 3. 表面活性物质的实质性作用是:( B ) A,乳化作用;B,降低表面张力;C,加溶作用;D,降低物质的溶解性 4.某温度压力下,有大小相同的水滴、水泡和气泡,其气相部分组成相同,见图。它们三者表面自由能大小为:(C) A.G a = G c < G b; B.G a = G b > G c ; C.G a < G b < G c ; D.G a = G b = G c 。 5.对于有略过量的KI存在的AgI溶胶,下列电解质中聚沉能力最强的是( D ) A . NaCl B. K3[Fe(CN)6] C. MgSO4 D. FeCl3 6.关于胶体和溶液的叙述中正确的是( C ) A. 胶体带电荷,而溶液呈电中性 B. 胶体加入电解质可产生沉淀,而溶液不能
C. 胶体是一种介稳性的分散系,而溶液是一种稳定的分散系 D. 胶体能够发生丁达尔效应,而溶液中不存在布朗运动 7.某化学反应的计量方程为A 2B C D k +??→+,实验测定得到其速率系数为3110.25(mol dm )s k ---=??,则该反应的级数为 ( C ) (A )零级反应 (B )一级反应 (C )二级反应 (D )三级反应 8.有一个平行反应,①1a,1,A B E k ???→;②2a,2,A D E k ???→。已知反应①的活化能大于反应②的活化能,即a,1a,2E E >,以下措施中哪一种不能改变获得产物B 和D 的比例? ( B ) (A) 提高反应温度 (B) 延长反应时间 (C) 加入适当催化剂 (D) 降低反应温度 9. 下列说法错误的是( D ) A. 一步完成的反应是基元反应。 B. 由一个基元反应构成的化学反应称简单反应。 C. 由两个或两个以上基元反应构成的化学反应称复杂反应。 D. 基元反应都是零级反应。 10. 加入正催化剂使反应速度加快,下列叙述不正确的是( C ) A. 使反应体系的活化分子百分数增高 B. 使反应体系的活化分子总数增多。 C. 使反应体系的活化分子百分数降低。 D. 使反应体系的活化能降低。 二、选择题 1.溶胶的动力性质包括 布朗运动 、 扩散作用 和 沉降作用 。
北京大学教育学院年博士研究生招生说明 北京大学教育学院年招收博士研究生将继续实行以综合素质能力为基础的“申请考核制”。申请人须按照我校博士生招生简章和教育学院的相关要求进行报名并提交申请材料。【教育领导与管理领域教育博士专业学位项目招生说明请参看《北京大学年教育领导与管理领域教育博士专业学位研究生招生简章》、教育经济与管理专业高级教育行政管理方向招生说明请参看《北京大学年教育经济与管理专业高级教育行政管理方向博士研究生招生简章》】。具体办法如下: 一、申请人基本条件 .品行端正,遵纪守法; .报名攻读博士学位研究生须符合下列条件之一: 1)已获得硕士或博士学位的人员; 2)应届硕士毕业生(须在录取年月日前取得硕士学位); 3)获得本科学士学位满年(到录取年的月日)的人员,可按照同等学力身份报考。以 同等学力身份报名者,须在报考学科、专业或相近研究领域的全国核心期刊上已发 表两篇以上学术论文(以第一或第二作者),或已获得省、部级以上与报考学科相 关的科研成果奖励(排名前五名); . 申请人对于教育应具有强烈的兴趣和科学研究的潜力; . 健康状况符合北京大学研究生入学体检标准; . 高等教育学、教育学原理、教育经济与管理(不含高级教育行政管理方向,下同)、教育技术学四个专业仅招收全日制转档生;教育领导与管理领域教育博士专业学位、教育经济与管理高级教育行政管理方向学习方式为非全日制。 二、报名申请 . 网上申报:年月日月日,具体方法参看北京大学研究生招生网();特别提醒如下: 1)报考类别:(类别错误不予录取) a)高等教育学、教育学原理、教育经济与管理(不含高级教育行政管理方向)、教 育技术学四个专业: 非定向; b)教育领导与管理专业(.)、教育经济与管理高级教育行政管理方向: 定向; 2)导师姓名:不需填写; 3)英语水平:优先填写时限和成绩均合格的英语水平信息; 4)专业志愿:仅接受一个专业一个方向的报考信息,多报无效; . 提交初审材料: 1)材料形式:纸质版 2)截止时间:年月日前(需寄达,逾期不予受理)
一、选择题 1. 下列说法中不正确的是:( C ) (A) 生成的新鲜液面都有表面张力 (B) 平面液体没有附加压力 (C) 弯曲液面的表面张力的方向指向曲率中心 (D) 弯曲液面的附加压力指向曲率中心 2. 水在临界温度时的表面Gibbs自由能: ( C ) (A)(A) 大于零 (B) 小于零 (C) 等于零 (D) 无法确定 3. 一个 U 型管的两臂直径不同,一端为 1×10-3 m,另一端为 3×10-3 m,水的表 面张力为 0.072 N·m-1。如用这个 U 型管装上水来测量压力,将引入的误差为: ( B ) (A) 72 Pa (B) 192 Pa (C) 96 Pa (D) 288 Pa 4. 低压下,气体 A 在表面均匀的催化剂上进行催化转化反应, 其机理为: A(g) + K A K ─→ B(g) + K 第一步是快平衡, 第二步是速控步, 则该反应表观为几级? ( B ) (A) 零级 (B) 一级 (C) 二级 (D) 无级数 5 . 表面过程中ΔG(表面)= -W'的充要条件除了等温等压外,还有:( D ) A,不做其它功; B,热力学可逆; C,组成不变; D,是B和C。 6. 物质表面张力的值与:( C ) A,温度无关; B,压力无关; C,表面大小无关; D,另一相物质无关。 7. 以P平、P凸、P凹分别表示平面、凸面、凹面液体上的饱和蒸汽压,三者关系为:( B ) A,P平>P凹>P凸; B,P凸>P平>P凹; C,P凸>P凹>P平; D,三者相同。 8. 常见亚稳态现象都与表面性质有关,下面说法正确的是:( D ) A,过饱和蒸气是由于小液滴的蒸气压小于大液滴的蒸气压所致; B,过热液体形成原因是新相种子——小气泡的附加压力太小; C,饱和溶液陈化、晶粒长大,因为小晶粒溶解度比大晶粒大; D,人工降雨时在大气中撒入化学物质主要的目的是促进凝结中心形成 9. 对亲水性固体表面,其相应接触角θ是:( B ) A,θ>90°; B,θ<90°; C,θ=180°; D,θ可为任意角 1O. Langmuir吸附理论中说法符合基本假定得是:( A ) A,固体表面均匀、各处吸附能力相同;B,吸附分子可以是单层或多层分子层;C,被吸附 分子间有作用、相互影响;D,吸附和解吸附之间很难建立动态平衡。 11. Langmuir吸附形式之一:θ=bp/(1+bp),它不适用于:( C ) A,化学吸附;B,单分子层吸附;C,多种分子同时被强吸附;D,固体对稀溶液中溶质的吸 附。 12. 表面活性物质的实质性作用是:( B ) A,乳化作用;B,降低表面张力;C,加溶作用;D,降低物质的溶解性 13. 一定体积的水,当聚成一个大水球或分散成许多水滴时,同温度下,两种状态相 比,:以下性质保持不变的 ( B ) (A) 表面能 (B) 表面张力 (C) 比表面
表面2A 一、选择题 1. 在催化剂表面上进行的双分子气相反应, 其机理为: A +K AK B +K BK AK +BK ─→C +D +2K 若催化剂表面是均匀的, 表面反应为控制步骤, 且A、B的吸附皆弱, 则反应表现为几级? ( ) (A) 零级(B) 一级 (C) 二级(D) 无数级 2. 298 K时,蒸气苯在石墨上的吸附,符合Langmuir 吸附等温式,在40 Pa 时,覆盖度θ= 0.05,当θ= 1/2 时,苯气体的平衡压力为:( ) (A) 400 Pa (B) 760 Pa (C) 1 000 Pa (D) 200 Pa 3. 在等温等压条件下,将1 mol水的表面积增加10 倍,作功为W,水的Gibbs自由能变化为?G,此时W与?G的关系为:(?U = Q - W) ( ) (A) ?G = -W(B) ?G = W (C) ?G < -W(D) 不能确定 4. 同一固体, 大块颗粒和粉状颗粒, 其溶解度哪个大? ( ) (A) 大块颗粒大 (B) 粉状颗粒大
(C) 一样大(D) 无法比较 5. 有一露于空气中的球形液膜,直径为2×10-3 m,表面张力为0.072 N·m-1,液膜的附加压力为() (A)36 Pa (B) 72 Pa (C) 144 Pa (D) 288 Pa 6. 单组分气-液平衡体系,在孤立条件下,界面A 发生了d A > 0 的微小变化, 体系相应的熵变d S变化为:( ) (A) d S > 0 (B) d S = 0 (C) d S < 0 (D) 不能确定 7. 在下图的毛细管内装入普通不润湿性液体,当将毛细管右端用冰块冷却时,管内液体将:( ) (A) 向左移动(B) 向右移动 (C) 不移动(D) 左右来回移动 8. 在农药中通常都要加入一定量的表面活性物质, 如烷基苯磺酸盐, 其主要目的是:( ) (A) 增加农药的杀虫药性 (B) 提高农药对植物表面的润湿能力 (C)防止农药挥发 (D) 消除药液的泡沫 9. 对于亲水性固体表面,其表面张力间的关系是:( ) (A) γ固-水> γ固-空气(B) γ固-水< γ固-空气
北京中医药大学《无机化学》考试辅导试题及答案 用离子-电子法配平并完成下列反应 答:+ + 2I-= 2Fe2+ + I2 -+ 3SO32-+H2O = 2MnO2 + 3SO42-+ 2OH— + + Zn = Cu+ Zn2+ -+3S2-+14H+ =2Cr3++3S +7 H2O -+ 5SO32-+ 6H+= 2Mn2+ + 5SO42-+3 H2O — + SO32-+ 2OH—= 2MnO42—+ SO42-+ H2O 简答题 1. 一种钠盐A,在A的水溶液中加入稀盐酸产生刺激性气体B。A的水溶液在酸性中能使KMnO4溶液腿色,得到无色溶液C。若在A的水溶液中通入Cl2得溶液D,在D中加入AgNO3溶液产生白色沉淀E,若在E中加入NH3水,震荡后得到无色溶液F。指出A、B、C、D、E、F各为何物。 答:A、Na2SO3B、SO2C、Mn2+ D、Cl- E、AgCl F、[Ag(NH)2]+ 2.根据配合物的价键理论,指出下列配离子中,中心离子和配体的配位情况(即画出中心离子杂化后价电子排布、指出杂化轨道类型及空间构型)。 (1)[FeF6]3-μ= . (2)[Fe(CN)6]3-μ= . 答:(1)Fe3+ 3d53d轨道有5个单电子sp3d2杂化八面体 (2)Fe3+ 3d53d轨道有1个单电子d2sp3杂化八面体 3.有四种试剂:Na2SO4、Na2SO3、Na2S2O3、Na2S,它们的标签已脱落,请设计只加一种试剂的简便方法鉴别它们,并写出有关配平的离子反应方程式。 答:加稀HCl (略) 4.根据配合物的价键理论,确定下列配离子是内轨型还是外轨型,说明理由。 (1) [Fe(H2O)6]3-(Fe3+3d 5)μ= . (2) [Mn(CN)6] 4-(Mn2+3d 5)μ= . 答:(1)μ= 则n=5 Fe3+ 3d53d轨道有5个单电子sp3d2杂化八面体 (2)μ= 则n=1 Fe3+ 3d53d轨道有1个单电子d2sp3杂化八面体 5.现有一种含结晶水的淡绿色晶体A,将其配成溶液,若加入BaCl2溶液,则产生不溶于酸的白色沉淀B,若加入NaOH溶液,则生成白色胶状沉淀C并很快变成红棕色沉淀D,再加入盐酸,此红棕色沉淀又溶解,滴入硫氰化钾溶液显深红色溶液E。指出A、B、C、D、E各为何物。 答:A、Na2SO3B、SO2C、Mn2+ D、Cl- E、AgCl F、[Ag(NH)2]+
无机化学习题参考答案(II) 第一章 1.4.解: (1)H 2O 2 2C (2)S 2O 32 3v C (3)N 2O (N N O 方式) v C ∞ (4)Hg 2Cl 2 h D ∞ (5)H 2C=C=CH 2 2d D (6)UOF 4 C 5v (7)BF 4 d T (8)SClF 5 4v C (9)反-Pt(NH 3)2Cl 2 2h D (10)PtCl 3(C 2H 4) 2v C 1.B(CH 3)3和BCl 3相比,哪一个的Lewis 酸性强,为什么? 一般来说,CH 3为推电子基团,Cl 为吸电子基团,因此的Lewis 酸性强。 (BCl 3易水解;B(CH 3)3不溶于水,在空气中易燃) 2.BH 3和BF 3都可和(CH 3)2NPF 2生成加合物,在一种加合物中,B 原子和N 相连,另一种则和P 相连,绘出两种结构式,并说明形成两种结构的原因。 P F F H 3C CH 3 N P F F H 3C CH 3 N B B H 3F 3 (该题可参考史启桢等翻译的"无机化学",作者Shriver 等,由高教社出版, 其中关于热力学酸度参数的部分,p.190-191; 或者该书的英文原版第5章的相关内容) 3. 无水AlCl 3可作为傅-克烷基化反应的催化剂, 而吸水后则失效, 原因何在? 配位饱和(6配位),失去Lewis 酸性 4. 吸水后失效 的AlCl 3有什么方法可以脱水? 因为Al 3+是典型的硬酸,与氧的亲合力很强,因此实验室不能在HCl ,NH 4Cl ,SOCl 2等气氛下加热脱水。(只能加强热生成 Al 2O 3后,用高温下用加C 和Cl 2用还原氯化法制备,这就不是脱水方法了)。 第二章
北京大学关于博士研究生培养工作的若干规定 (2007年7月修订) 根据《中华人民共和国学位条例》、《中华人民共和国学位条例暂行实施办法》及国家教育部有关文件的精神,结合我校具体情况,特制定本规定。各学科专业根据本规定,结合本学科专业的实际情况,制定本学科专业的培养方案、博士研究生个人培养计划,努力做好博士研究生的培养和管理工作。 一、培养目标 1.能较好地掌握马列主义、毛泽东思想和邓小平理论,拥护党的基本路线,热爱祖国,遵纪守法,品德良好,学风严谨,具有较强的事业心和献身精神,积极为社会主义现代化建设事业服务。 2.在本门学科掌握坚实宽广的基础理论和系统深入的专门知识,同时要掌握一定的相关学科知识;具有独立从事科学研究工作的能力,在科学或专门技术上做出创造性的成果。 3.身体健康。 二、学习年限 硕士起点的博士研究生的基本学习年限为4年;直接攻读博士学位的研究生(简称直博生)、硕士—博士连续培养的研究生(简称硕博连读生)的基本学习年限为5年。博士研究生最长学习年限为8年。硕博连读生从其硕士研究生入学年月起计算在校学习最长年限。基本年限由各学位分委会确定,列入培养方案,报研究生院培养办公室备案。 博士研究生可以提前毕业或延长学习年限。提前毕业或延长学习年限应按规定办理相关手续。 三、培养方式 在博士研究生培养过程中,应合理安排课程学习、社会实践、科学研究、学术交流等各个环节,应着重培养博士研究生的优良学风、探索精神、独立从事科学研究的能力和创新能力。 博士研究生的培养实行导师负责和集体培养相结合的办法。对每位博士研究生都必须成立博士研究生指导小组。博士研究生指导小组,应由该生的导师为组长,另有3—5名本专业、相关学科专业的专家组成。 博士研究生导师应全面关心和指导研究生的成长。指导小组成员协助导师,主要做好以下几方面工作:①制定博士研究生培养计划,并督促检查其实施;②对博士研究生进行政治思想、学风、品德等方面的教育;③指导和检查博士研究生的课程学习、科学研究和学位论文工作。 培养博士研究生的过程中,在保证基本要求的前提下,导师和指导小组可采取灵活多样、
物理化学表面现象练习题 一、判断题: 1.只有在比表面很大时才能明显地看到表面现象,所以系统表面增大是表面张力产生的原因。 2.对大多数系统来讲,当温度升高时,表面张力下降。 3.比表面吉布斯函数是指恒温、恒压下,当组成不变时可逆地增大单位表面积时,系统所增加的吉布斯函数,表面张力则是指表面单位长度上存在的使表面张紧的力。 所以比表面吉布斯函数与表面张力是两个毫无联系的概念。 4.恒温、恒压下,凡能使系统表面吉布斯函数降低的过程都是自发过程。 5.过饱和蒸气之所以可能存在,是因新生成的微小液滴具有很低的表面吉布斯自由能。6.液体在毛细管内上升或下降决定于该液体的表面张力的大小。 7.单分子层吸附只能是化学吸附,多分子层吸附只能是物理吸附。 8.产生物理吸附的力是范德华力,作用较弱,因而吸附速度慢,不易达到平衡。 9.在吉布斯吸附等温式中,Γ为溶质的吸附量,它随溶质(表面活性物质)的加入量的增加而增加,并且当溶质达饱和时,Γ达到极大值。。 10.由于溶质在溶液的表面产生吸附,所以溶质在溶液表面的浓度大于它在溶液内部的浓度。 11.表面活性物质是指那些加入到溶液中,可以降低溶液表面张力的物质。 二、单选题: 1.下列叙述不正确的是: (A) 比表面自由能的物理意义是,在定温定压下,可逆地增加单位表面积引起系 统吉布斯自由能的增量; (B) 表面张力的物理意义是,在相表面的切面上,垂直作用于表面上任意单位长 度切线的表面紧缩力; (C) 比表面自由能与表面张力量纲相同,单位不同; (D) 比表面自由能单位为J·m-2,表面张力单位为N·m-1时,两者数值不同。 2.在液面上,某一小面积S周围表面对S有表面张力,下列叙述不正确的是: (A) 表面张力与液面垂直; (B) 表面张力与S的周边垂直; (C) 表面张力沿周边与表面相切; (D) 表面张力的合力在凸液面指向液体内部(曲面球心),在凹液面指向液体外部。 3.同一体系,比表面自由能和表面张力都用σ表示,它们: (A) 物理意义相同,数值相同;(B) 量纲和单位完全相同; (C) 物理意义相同,单位不同;(D) 物理意义不同,单位不同。 4.一个玻璃毛细管分别插入25℃和75℃的水中,则毛细管中的水在两不同温度水中上升的高度: (A) 相同;(B) 无法确定; (C) 25℃水中高于75℃水中;(D) 75℃水中高于25℃水中。 5.纯水的表面张力是指恒温恒压下水与哪类相接触时的界面张力: (A) 饱和水蒸气;(B) 饱和了水蒸气的空气; (C) 空气;(D) 含有水蒸气的空气。 6.水的相图中s、l、g分别表示固、液、气三态,
第五章 化学平衡 在某恒定的温度和压力下,取的A(g)进行如下化学反应 若 ,试证明,当反应进度 时,系统的吉布斯函数G 值为最小,这时A, B 间达化学平衡。 已知四氧化二氮的分解反应 在 K 时,1?754=-mol kJ .G Δθ m r 。试判断在此温度及下列条件下,反应进行的方向。 (1) N 2O 4(100 kPa), NO 2(1000 kPa); (2) N 2O 4(1000 kPa), NO 2(100 kPa);
(3) N 2O 4(300 kPa), NO 2(200 kPa); 解:由J p 进行判断 14720=15 298×314810×754=3 .)...exp()RT G Δexp(K θ m r --= 1000 K 时,反应 的1?39719=-mol kJ .G Δθ m r 。现有与碳反应的气体混合物,其组成为体积分数 ,,。试问: (1)T = 1000 K ,p = 100 kPa 时,m r G Δ等于多少,甲烷能否形成 (2)在1000 K 下,压力需增加到若干,上述合成甲烷的反应才可能进行。 已知同一温度,两反应方程及其标准平衡常数如下: 求下列反应的 K 。 解:所给反应 = (2)-(1),因此 θ m r θ.m r θm r G ΔG ΔG Δ1 2=,-
θ θθ θ θ θ 1 2 1 2 ) ln ( ln ln K K K K RT K RT K RT = - - - = - 已知同一温度,两反应方程及其标准平衡常数如下: 求下列反应的。 解:所给反应= 2×(2)-(1),因此 θ m r θ . m r θ m r G Δ G Δ G Δ 1 2 2 = , - θ θ θ θ θ θ 1 2 2 1 2 ) ( ) ln ( ln 2 ln K K K K RT K RT K RT = - - - = - 注:平衡组成的计算关键是物料衡算。 在一个抽空的恒容容器中引入氯和二氧化硫,若它们之间没有发生反应,则在K时的分压分别为kPa和kPa。将容器保持在K,经一定时间后,总压力减少至kPa,且维持不变。求下列反应的K θ。 解:反应各组分物料衡算如下 因此, 使一定量摩尔比为1:3的氮、氢混合气体在1174 K,3 MPa下通过铁催化剂以合成氨。设反应达到平衡。出来的气体混合物缓缓地通入20 cm3盐酸吸收氨。用气量计测得剩余气体的体积相当于K,kPa的干燥气体(不含水蒸气)dm3。原盐酸溶液20 cm3需用浓度为mmol·dm-3的氢氧化钾溶液18.72 cm3滴定至终点。气体通过后只需用同样浓度的氢氧化钾溶液15.17 cm3。求1174 K时,下列反应的。