
《化学平衡的移动》教案
一、教学目的要求:
1、使学生理解浓度,压强和温度等条件对化学平衡的影响
2、使学生理解化学平衡的移动.
二、本节重难点:
重点:浓度,压强和温度等条件对化学平衡的影响
难点:平衡移动原理的应用?
课时安排:1课时
教学过程:
导言:
我们研究化学平衡的目的,不是要保持一个化学平衡不变?而是要研究如何利用外界条
件的改变,去破坏化学平衡?使之向我们所希望的方向转变,去建立新的化学平衡
化学平衡的移动:可逆反应中,旧化学平衡的破坏,新化学平衡的建立的过程就叫做化学平衡的移动?
(一)浓度对化学平衡的影响:
做实验:实验1、2
实验证明:
加入硝酸溶液变橙色,加入NaOh溶液变黄色。
说明加入硝酸溶液化学平衡向正反应的方向移动了,加入NaO溶液化学平衡向正反应的
方向移动。
无数实验证明:增大任何一种反应物的浓度,都可以使化学平衡向正反应方向移动。
增大任何一种生成物的浓度,都可以使化学平衡向逆反应方向移动。
减小任何一种反应物的浓度,都可以使化学平衡向逆反应方向移动。
减小任何一种生成物的浓度,都可以使化学平衡向正反应方向移动。
(二)压强对化学平衡的影响:
处于平衡状态的反应混合物里,无论是反应物,还是生成物,只要有气态物质存在,
强的改变,就有可能使化学平衡移动。
女口:高温高压
N23H22NH3
3
2 2
催化剂
反应中,1体积氮气和3体积的氢气反应,生成了2体积的氨气。反应后,气体总体积减少了!
可知,对这种气体总体积减少的反应,增大压强,平衡向正反应方向移动。即:增大压强,平衡
向体积缩小的方向移动;减小压强,平衡向体积增大的方向移动。
气体总体积不变化,改变压强,化学平衡不移动!
女'CO -日2。9)= co? - H2反应前后,气体物质总体积不变。改变压强,平衡不移动!
(三)温度对化学平衡的影响:
在吸热或放热的可逆反应中,反应混合物达平衡后,改变温度,也会使化学平衡移动
在可逆反应中,正反应如果放热,则,逆反应必定吸热!反之亦然
做实验:P51页实验
由实验可知:
升高温度,(混合气体颜色加深,)平衡向吸热反应的方向移动?
降低温度,(混合气体颜色变浅,)平衡向放热反应的方向移动
(四)催化剂对化学平衡的影响:
催化剂能同等程度的增加正反应速率和逆反应速率,即,催化剂不能改变达到化学平衡
状态的反应混合物的组成?即:催化剂不能使化学平衡移动!但催化剂可以改变达到化学平衡所需要的时间?
平衡移动原理(即勒夏特列原理)
如果改变影响平衡的一个条件,平衡就像削弱这种改变的方向移动
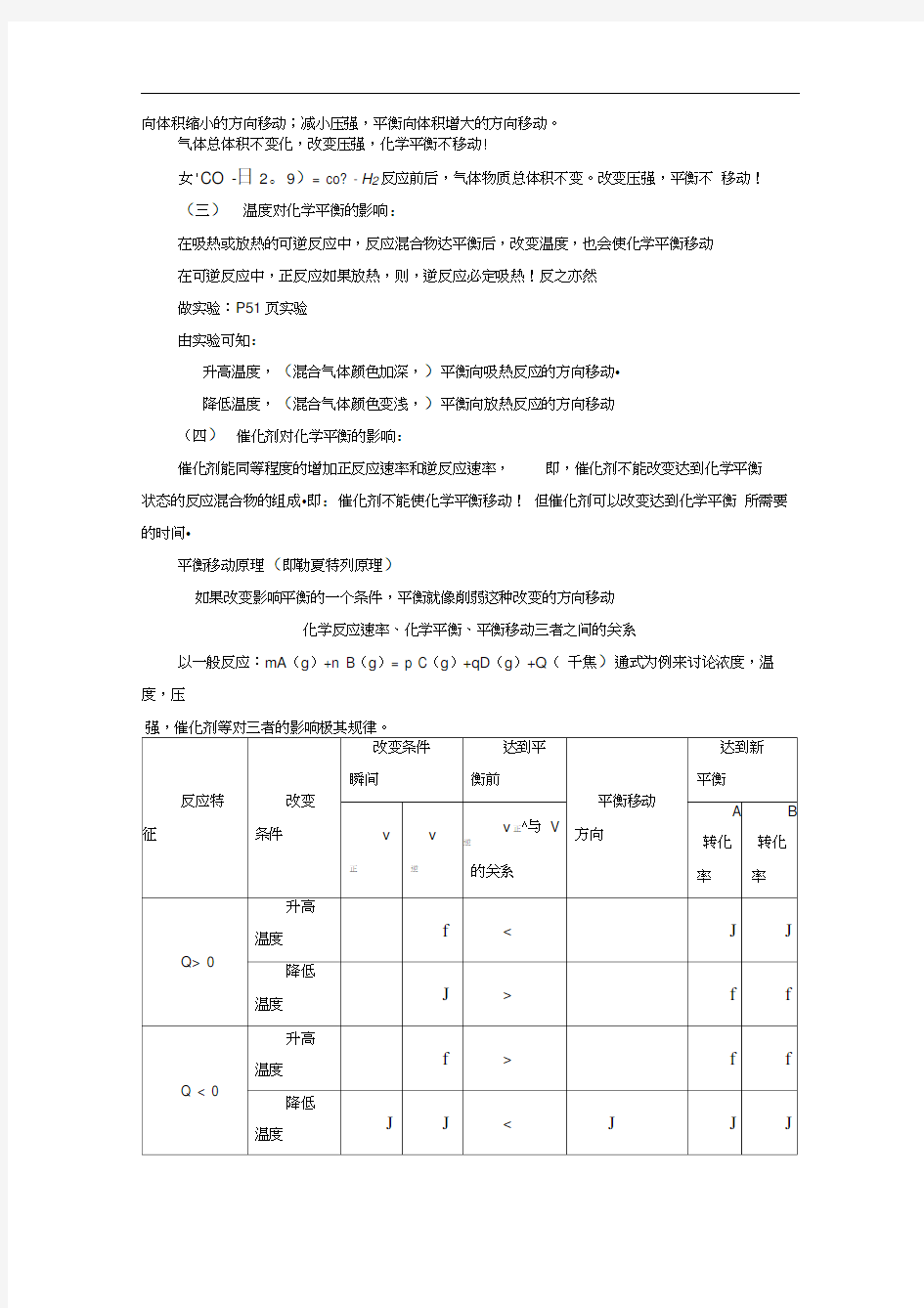
化学反应速率、化学平衡、平衡移动三者之间的关系
以一般反应:mA(g)+n B(g)= p C(g)+qD(g)+Q(千焦)通式为例来讨论浓度,温度,压