
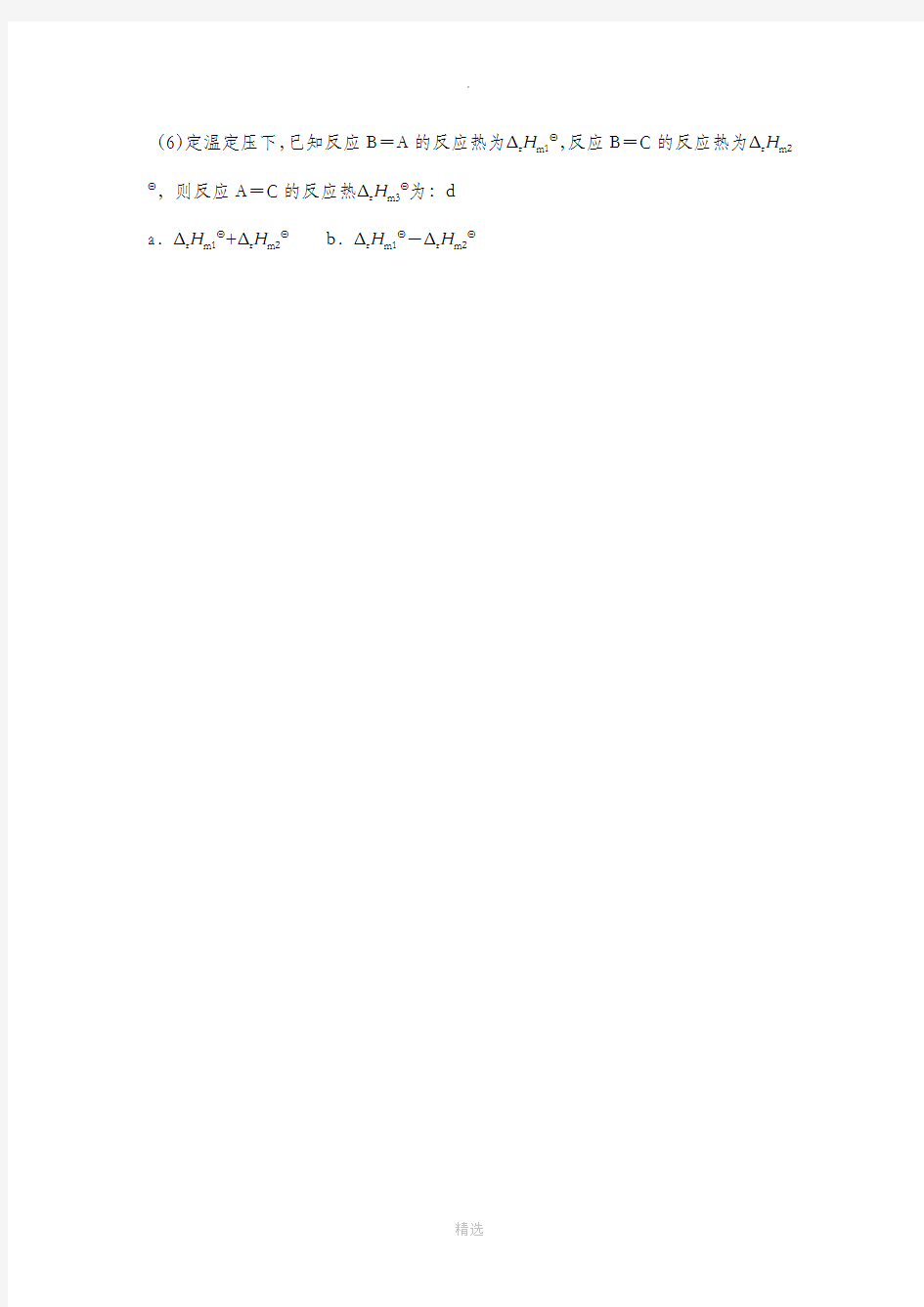
《无学化学》复习题答案
一、是非题:请在各题括号中,用“√”、“×”分别表示题文中叙述是否正确。(√) 1. 电子云是描述核外某空间电子出现的几率密度的概念。
(√)2. 同种原子之间的化学键的键长越短,其键能越大,化学键也越稳定。(√)3.系统经历一个循环,无论多少步骤,只要回到初始状态,其热力学能和焓的变化量均为零。
(√)4. AgCl在NaCl溶液中的溶解度比在纯水中的溶解度小。
(×)5. 原子轨道的形状由量子数m决定,轨道的空间伸展方向由l决定。
二、选择题
(1)某元素原子基态的电子构型为1s22s22p63s23p5,它在周期表中的位置是:a a.p区ⅦA族b.s区ⅡA族c.ds区ⅡB族d.p区Ⅵ族
(2)下列物质中,哪个是非极性分子:b
a.H2O b.CO2c.HCl d.NH3
(3)极性共价化合物的实例是:b
a.KCl b.HCl c.CCl4d.BF3
(4)下列物质凝固时可以形成原子晶体的是:c
a. O2
b. Pt,
c. SiO2
d. KCl
(5)在298K,100kPa下,反应2H2(g)+O2(g)=2H2O(1) Δr H mΘ= -572 kJ·mol-1则H2O(l)的Δf H mΘ为:d
a.572 kJ·mol-1b.-572 kJ·mol-1c.286 kJ·mol-1d.-286 kJ·mol-1
(6)定温定压下,已知反应B=A的反应热为Δr H m1Θ,反应B=C的反应热为Δr H m2Θ,则反应A=C的反应热Δr H m3Θ为:d
a.Δr H m1Θ+Δr H m2Θb.Δr H m1Θ-Δr H m2Θ
c .Δr H m1Θ+2Δr H m2Θ
d .Δr H m2Θ-Δr H m1Θ
(7)已知HF (g )的标准生成热Δf H m Θ= -565 kJ ·mol -1,则反应H 2(g)+F 2(g)=2HF(g)的Δr H m Θ为:d
a .565 kJ ·mol -1
b .-565 kJ ·mol -1
c .1130 kJ ·mol -1
d .-1130 kJ ·mol -1
(8)在氨水溶液中加入固体NH 4Cl 后,氨水的离解度:d
a .没变化
b .微有上升
c .剧烈上升
d .下降
(9)N 的氢化物(NH 3)的熔点都比它同族中其他氢化物的熔点高得多,这主要由于NH 3:c
a .分子量最小
b .取向力最
c .存在氢键
d .诱导力强
(10)在一定条件下,一可逆反应其正反应的平衡常数与逆反应的平衡常数关系是:c
a .它们总是相等
b .它们的和等于1
c .它们的积等于1
d .它们没有关系
(11)下列反应及其平衡常数H 2 (g)+S(s)=H 2S(g) K 1Θ;(g)SO (g)O S(s)22=+ K 2Θ,则反应S(g)H (g )O (g )SO (g )H 2222+=+的平衡常数K Θ是:d
a. K 1Θ+K 2Θ b .K 1Θ- K 2Θ c .K 1Θ×K 2Θ. d .K 1Θ÷K 2Θ
(12)在298K 时石墨的标准摩尔生成焓Δf H m Θ为:c
a .大于零
b .小于零
c .等于零
d .无法确定
(13)不合理的一套量子数(n ,l ,m ,m s )是:b
a .4,0,0,21+
b .4,0,-1,2
1-
c .4,3,+3,21-
d .4,2,0,21+
(14)向HAc 溶液中,加入少许固体物质,使HAc 离解度减小的是:b
a .NaCl
b .NaA
c c .FeCl 3
d .KCN
(15)
NH溶于水后,分子间产生的作用力有:d
3
a.取向力和色散力b.取向力和诱导力
c.诱导力和色散力d.取向力、色散力、诱导力及氢键(16)25℃时,Mg(OH)2的K spΘ为1.2×10-11,在0.01mol · L-1的NaOH溶液中的溶解度为:c
a.1.2×10-9 mol · L-1b.2.4×10-9 mol · L-1
c.1.2×10-7 mol · L-1d.1.7×10-5 mol · L-1
(17)已知EΘ(Fe3+/Fe2+) =0.770V,EΘ(Cu2+/Cu)=0.340V,则反应
2Fe3+(1mol·L-1)+Cu=2Fe2+(1mol·L-1) + Cu2+(1mol·L-1)可以:b a.呈平衡状态b.自发正向进行c.自发逆向进行d.前三者都错(18)已知Fe3++e = Fe2+,EΘ= 0.770V,测定一个Fe3+/Fe2+电极电势E= 0.750 V,则溶液中必定是:d
a.c(Fe3+)<1 b.c( Fe2+)<1 c.c( Fe2+)/ c(Fe3+)<1 d.c(Fe3+)/ c( Fe2+)<1(19)角量子数l描述核外电子运动状态的:c
a.电子能量高低;b.电子自旋方向;c电子云形状;d电子云的空间伸展方向;(20)以下各组物质可做缓冲对的是:a
a.HCOOH—HCOONa b.HCl一NaCl
c.HAc—H2SO4d.NaOH—NH3·H2O
三、填空题
1. 写出具有下列指定量子数的原子轨道符号:
A. n=4,l=1____4p________
B. n=5,l=2 ______5d______
2.写出下列原子在基态时的电子排布
(1). Mn: 1s22s22p63s23p63d54s2; (2). Fe___1s22s22p63s23p63d64s2;
3. 等性sp2、sp3杂化轨道的夹角分别为__120_____._109.5____.
4. 在定温定压下已知反应A=3B的反应热为Δr H m1Θ,反应3A=C的反应热为
Δr H m2Θ,则反应9B=C的反应热Δr H m3Θ为(Δr H m2Θ- 3Δr H m1Θ)。
5. CaO(s)+ CO2(g)= CaCO3(s)的平衡常数表达式为(KΘ=1/P CO2 )。
6. 25℃时Ag2CrO4的溶解度为( 6.1 ×10-4)。(K spΘ(Ag2CrO4)=9.0×10-10)。
7. 已知: Zn 2+ + 2e - E Θ(Zn 2+/Zn )
= -0.762 8V, 那么
21Zn 2+ + e - 2
1Zn E Θ(Zn 2+/Zn ) = (-0.762 8V )由此可知,标准电极电势E Θ由( 物质的电势 )决定,与电极反应中(计量系数)无关。
8. 某元素电子构型为[Ar]3d54s2,此元素位于( 4 )周期,( 7 )族。
9. 命名下列配合物:a. [Ni(en)2]Cl2( 二氯化二-乙二胺合镍(II)) b. Na3[AlF6] ( 六氟合氯酸钠)
五、简答题
1、用四个量子数描述基态C原子外层p轨道上2个电子的运动状态?
2. BF3分子构型是平面三角形,而NF3分子构型是三角锥形,试用杂化轨道理论
解释.
3. CH4、H2O、NH3中心原子杂化态皆是sp3,其键角大小是否相同?为什么?其空
间构型各为何?
2、化学Ag++Fe2+=Fe3++Ag在原电池中发生,试写出原电池符号和电极反应。
六、计算题
1. 对于A(s)+B2+(aq)=A2+(aq)+B(s)反应,已知A2+的初始浓度为零,B2+的初始浓度为0.06 mol·L-1,平衡时B2+的浓度为0.02 mol·L-1,计算上述反应25℃时的KΘ。
解:0.04/0.02=2
2. 浓度均为0.01mol·L-1的Cl—和CrO42-的混合溶液中,逐滴加入AgNO3溶液,何种离子先沉淀?当第二种离子沉淀时先沉淀离子的浓度是多少?(K spΘ(AgCl)=2×10-10,K spΘ(Ag2CrO4)=1×10-12)
解:AgCl先沉淀
[Cl-]=2×10-5
3.
①. Cu(NH 3)42+/Cu 在标准状态下的2+[Cu ]浓度可由[Cu(NH 3)4]2+的解离求算:
[Cu(NH 3)4]2+
Cu 2++ 4NH 3 ])NH (Cu []NH ][Cu [])NH (Cu [2434
32243θ不稳+++=K
标准状态下,[Cu(NH 3)42+]=[NH 3]=1.0 mol ·L -1,
14243θ不稳210
8.4])NH (Cu []Cu [-++?==K E [Cu(NH 3)42+/Cu]的电极电势可以根据能斯特方程式求出: E ?[Cu(NH 3)42+/Cu ] = E ?(Cu 2+/Cu ) + 20592.0lg [Cu 2+] E ?[Cu(NH 3)42+/Cu ] = E ?(Cu 2+/Cu ) + 2
0592.0lg K 不稳?[Cu(NH 3)4]2+ E ?[Cu(NH 3)42+/Cu ] = 0.34 + V 05.0)108.4lg(20592.014-=?-
②. 在1.0 mol ·L -1的NH 3水溶液中,OH - 离子浓度可以根据弱电解质电离平衡求出:
NH 3 + H 2O NH 4+ + OH -
c /K b ?≥500 (1分)
-θ5-133OH K (NH ) (NH ) 1.7910 1.00.0042mol L c -=??=b []=
O 2/OH - 在1.0 mol ·L -1的NH 3水溶液中的电极电势也可以根据能斯特方程式求出:
O
2 + 2H 2O + 4e - 4OH -
4222]
OH [)]([lg 40.0592)/OH (O )/OH (O ---+=O p E E 40.059210.401lg 0.4010.1400.541V 40.0042
=+=+= ③. 比较①和②的结果发现,E (O 2/OH -)=0.541V ,比E ?[Cu(NH 3)42+/Cu ]=-0.05V 要大,说明在1.0 mol ·L -1 NH 3水中,分压为100kPa 的氧气能够氧化金属铜Cu 。所以在通氧的条件下Cu 能溶于1.0 mol ·L -1 NH 3水中。
第二章 热化学
填空题:
1、热是 能量传递 的一种形式,系统吸热,Q > 0;系统放热,Q < 0;定压下气体所做的体积功W = -p ex (V 2-V 1) ;气体膨胀时,体积功W < 0。若NaOH 溶液与HCl 溶液正好中和时,系统的焓变r H Θ=a kJ ·mol -1,则其热力学能的变化rU Θ= a kJ ·mol -1。这是一个 均(单) 相反应。
2、反应进度ζ的单位是 mol ;反应计量式中反应物B 的计量数υB < 0。
生成物的υB> 0。
3、由石墨制取金刚石的焓变r H mΘ> 0,燃烧相同质量的石墨和金刚石,石墨燃烧放出的热量更多。
4、己知298K时下列热化学方程式:
第一章气体、液体和溶液的性质 1. 敞口烧瓶在7℃所盛的气体,必须加热到什么温度,才能使1/3气体逸出烧瓶? 2. 已知一气筒在27℃,30.0atm时,含480g的氧气。若此筒被加热到100℃,然后启开阀门(温度保持在100℃),一直到气体压力降到1.00atm时,共放出多少克氧气? 3. 在30℃时,把8.0gCO2、6.0gO2和未知量的N2放入10dm3的容器中,总压力达800 mmHg。试求: (1) 容器中气体的总摩尔数为多少?(2) 每种气体的摩尔分数为多少? (3) 每种气体的分压为多少?(4) 容器中氮气为多少克? 4. CO和CO2的混合密度为1.82g?dm-3(在STP下)。问CO的重量百分数为多少? 5. 已知某混合气体组成为:20份氦气,20份氮气,50份一氧化氮,50份二氧化氮。问:在0℃,760mmHg下200dm3此混合气体中,氮气为多少克? 6. S2F10的沸点为29℃,问:在此温度和1atm下,该气体的密度为多少? 7. 体积为8.2dm3的长颈瓶中,含有4.0g氢气,0.50mol氧气和分压为2atm 的氩气。这时的温度为127℃。问: (1) 此长颈瓶中混合气体的混合密度为多少? (2) 此长颈瓶内的总压多大? (3) 氢的摩尔分数为多少? (4) 假设在长颈瓶中点火花,使之发生如下反应,直到反应完全: 2H2(g) + O2(g) =2H2O(g) 当温度仍然保持在127℃时,此长颈瓶中的总压又为多大? 8. 在通常的条件下,二氧化氮实际上是二氧化氮和四氧化二氮的两种混合气体。在45℃,总压为1atm时,混合气体的密度为2.56g?dm-3。计算: (1) 这两种气体的分压。(2) 这两种气体的重量百分比。 9. 在1.00atm和100℃时,混合300cm3H2和100 cm3O2,并使之反应。反应后温度和压力回到原来的状态。问此时混合气体的体积为多少毫升?若反应完成后把温度降低到27℃,压力仍为1.00atm,则混合气体的体积为多少毫升? (已知27℃时水的饱和蒸汽压为26.7mmHg) 10. 当0.75mol的“A4”固体与2mol的气态O2在一密闭的容器中加热,若反应物完全消耗仅能生成一种化合物,已知当温度降回到初温时,容器内所施的压力等于原来的一半,从这些数据,你对反应生成物如何下结论? 11. 有两个容器A和B,各装有氧气和氮气。在25℃时: 容器A:O2 体积500 cm3,压力1atm。 容器B:N2 体积500 cm3,压力0.5atm。 现将A和B容器相连,让气体互相混合,计算: (1) 混合后的总压。(2) 每一种气体的分压。
无机化学实验报告 【实验名称】实验八:醋酸解离常数的测定及稀释法配置准确浓度溶液的方法【班级】【日期】 【姓名】【学号】 一、实验目的 1. 了解醋酸解离常数的测定方法。 2. 掌握稀释法配置准确浓度溶液的方法。 3. 学会pH计的使用方法。 二、实验原理 1.稀释法配制准确浓度的溶液 稀释后溶液的浓度可由稀释定律c1V1 = c2V2求出。式中c1为稀释前溶液的浓度;c2为稀释后溶液的浓度;V1、V2分别为所取被稀释溶液的体积和稀释后溶液的体积。 根据有效数字运算规则,若c1只有二位有效数字,则得到的c2最多只有二位有效数字。同理,若c1是具有四位有效数字的准确浓度,若所取的体积V1或所配溶液的体积V2中有一个不准(即不具有四位有效数字),则所配溶液的浓度也不准确。为得到四位有效数字的c2,则c1、V1及V2必须要有四位有效数字。 为此必须有一个准确浓度的标准溶液。并且标准溶液的体积V1必须用移液管吸取,稀释溶液的体积必须用容量瓶来确定。 2.醋酸解离常数的测定 醋酸HAc是一元弱酸,在溶液中存在下列平衡 HAc === H+ + Ac- 其标准平衡常数称解离常数Kθa,为: [c (H3O+)/cθ][c(Ac-)/ cθ] Kθa HAc(aq) = —————————————(3-10) [c(HAc)/ cθ] 用pH计测出不同浓度HAc溶液的pH,则: c(H+) = c(Ac-) c平(HAc) = c初(HAc) - c(H+) ≈c初(HAc) 代入上式则可计算出Kθa HAc。 由pH计测出的pH,计算出的c(H+)只有二位有效数字,计算出的Kθa HAc 最多也只有二位有效数字。要得到有二位有效数字的Kθa,要求c初(HAc)至少也有二位有效数字。 三、仪器和药品 1.仪器 DELTA320酸度计;烧杯(100mL)3个;10mL吸量管(1支);100mL容量瓶(2个);10mL量筒;100mL量筒(或量杯)各1个;洗耳球(1个)。 2.药品 HAc(约0.2mol·L-1),准确浓度见试剂瓶;pH=4.00缓冲溶液;铬酸洗液。
《无机化学》试题 学号: 姓名: 座号: 系别: 年级: 专业: 总分合计人: 复核人: 一、单项选择题 (在每小题列出的四个选项中只有一个选项是符合题目要求的,请选出正确选项并在“答题卡”的相应位置上涂黑。多涂、少涂、错误均无分。每小题1分,共40分) 1、对于Zn 2+ /Zn 电对,增大Zn 2+ 的浓度,则其标准电极电势将 ( ) A 增大 B 减小 C 不变 D 无法判断 2 、 Cu 2 + 离子的外层电子构型为 ( ) A 8e B 18e 型 C 18+2e D 9~17e 型 3、设氨水的解离平衡常数为θb K 。浓度为m mol ·L -1 的氨水溶液,若将其用水稀释一倍,则溶液中OH -的浓度(mol ·L -1 )为 ( ) A m 21 B θb K m ?2 1 C 2/m K b ?θ D 2m
4、已知θ K(Ag3PO4) = 1.4×10-16,其溶解度为 sp ( ) A 1.1×10-4mol?L-1; B 4.8×10-5mol?L-1; C 1.2×10-8mol?L-1; D 8.3×10-5mol?L-1 5、下列各组物质,能自发发生反应的是() A Cu、Cu2+; B Cr2O72-、Cr3+; C MnO2、Mn2+; D SnCl4、Sn 6、3d轨道的磁量子数可能是() A 1,2,3 B 0,1,2 C 0,±1 D 0, ±1, ±2 7、下列各分子中,以sp3不等性杂化轨道成键的是() A BeCl2 B PCl3 C BF3 D SiH4 8、熔化下列晶体时,只需克服色散力的是() A HF B Ag C KF D CO2 9.已知V E A/θ:Cr2O72- +1.36 Cr3+ -0.41 Cr2+ -0.86 Cr,则判断发生歧化反应的是() A 都不能 B Cr2O72- C Cr3+ D Cr2+ 10.下列各物质中,熔点最高的是() A K2O B MgO C CaO D Na2O
第六章化学键理论 本章总目标: 1:掌握离子键、共价键和金属键的基本特征以及它们的区别; 2:了解物质的性质与分子结构和键参数的关系; 3:重点掌握路易斯理论、价电子对互斥理论、杂化轨道理论以及分子轨道理论。 4:熟悉几种分子间作用力。 各小节目标: 第一节:离子键理论 1:掌握离子键的形成、性质和强度,学会从离子的电荷、电子构型和半径三个方面案例讨论离子的特征。 2:了解离子晶体的特征及几种简单离子晶体的晶体结构,初步学习从离子的电荷、电子构象和半径三个方面来分析离子晶体的空间构型。 第二节:共价键理论 1;掌握路易斯理论。 2:理解共价键的形成和本质。掌握价键理论的三个基本要点和共价键的类型。3:理解并掌握价层电子对互斥理论要点并学会用此理论来判断共价分子的结构,并会用杂化轨道理论和分子轨道理论来解释分子的构型。 第三节:金属键理论 了解金属键的能带理论和三种常见的金属晶格。 第四节:分子间作用力 1:了解分子极性的判断和分子间作用力(范德华力)以及氢键这种次级键的形成原因。 2;初步掌握离子极化作用及其强度影响因素以及此作用对化合物结构及性质的影响。 习题 一选择题 1.下列化合物含有极性共价键的是()(《无机化学例题与习题》吉大版) A.KClO 3 B.Na 2 O 2 C. Na 2 O D.KI 2.下列分子或离子中键能最大的是()
A. O 2 B.O 2 - C. O 2 2+ D. O 2 2- 3. 下列化合物共价性最强的是()(《无机化学例题与习题》吉大版) A.LiI B.CsI C. BeI 2 D.MgI 2 4.极化能力最强的离子应具有的特性是() A.离子电荷高,离子半径大 B.离子电荷高,离子半径小 C.离子电荷低,离子半径小 D.离子电荷低,离子半径大 5. 下列化合物中,键的极性最弱的是()(《无机化学例题与习题》吉大版) A.FeCl 3 B.AlCl 3 C. SiCl 4 D.PCl 5 6.对下列各组稳定性大小判断正确的是() A.O 2+>O 2 2- B. O 2 ->O 2 C. NO+>NO D. OF->OF 7. 下列化合物中,含有非极性共价键的离子化合物是()(《无机化学例题与习题》吉大版) A.H 2O 2 B.NaCO 3 C. Na 2 O 2 D.KO 3 8.下列各对物质中,是等电子体的为() A.O 22-和O 3 B. C和B+ C. He和Li D. N 2 和CO 9. 中心原子采取sp2杂化的分子是()(《无机化学例题与习题》吉大版) A.NH 3 B.BCl 3 C. PCl 3 D.H 2 O 10.下列分子中含有两个不同键长的是() A .CO 2 B.SO 3 C. SF 4 D.XeF 4 11. 下列分子或离子中,不含有孤电子对的是()(《无机化学例题与习题》吉大版) A. H 2O B. H 3 O+ C. NH 3 D. NH 4 + 12.氨比甲烷易溶于水,其原因是() A.相对分子质量的差别 B.密度的差别 C. 氢键 D.熔点的差别 13. 下列分子属于极性分子的是()(《无机化学例题与习题》吉大版) A. CCl 4 B.CH 3 OCH 3 C. BCl 3 D. PCl 5 14.下列哪一种物质只需克服色散力就能使之沸腾( ) A.HCl B.CH 3Cl https://www.doczj.com/doc/ba4482529.html,l 4 D.NH 3 15. 下列分子中,中心原子采取等性杂化的是()(《无机化学例题与习题》吉大版)
(√) 1. 电子云是描述核外某空间电子出现的几率密度的概念。 (√)2. 同种原子之间的化学键的键长越短,其键能越大,化学键也越稳定。 (√)3.系统经历一个循环,无论多少步骤,只要回到初始状态,其热力学能和焓的变化量均为零。(√)4. AgCl在NaCl溶液中的溶解度比在纯水中的溶解度小。 (×)5. 原子轨道的形状由量子数m决定,轨道的空间伸展方向由l决定。 (1)某元素原子基态的电子构型为1s22s22p63s23p5,它在周期表中的位置是:a a.p区ⅦA族 b.s区ⅡA族 c.ds区ⅡB族 d.p区Ⅵ族 (2)下列物质中,哪个是非极性分子:b a.H2O b.CO2 c.HCl d.NH3 (3)极性共价化合物的实例是:b a.KCl b.HCl c.CCl4 d.BF3 (4)下列物质凝固时可以形成原子晶体的是:c a. O2 b. Pt, c. SiO2 d. KCl (5)在298K,100kPa下,反应 2H2(g)+O2(g)=2H2O(1) Δr H mΘ= -572 kJ·mol-1 则H2O(l)的Δf H mΘ为:d a.572 kJ·mol-1 b.-572 kJ·mol-1 c.286 kJ·mol-1 d.-286 kJ·mol-1 (6)定温定压下,已知反应B=A的反应热为Δr H m1Θ,反应B=C的反应热为Δr H m2Θ,则反应A=C的反应热Δr H m3Θ为:d a.Δr H m1Θ+Δr H m2Θ b.Δr H m1Θ-Δr H m2Θ c.Δr H m1Θ+2Δr H m2Θ d.Δr H m2Θ-Δr H m1Θ (7)已知HF(g)的标准生成热Δf H mΘ= -565 kJ·mol-1,则反应H2(g)+F2(g)=2HF(g)的Δr H mΘ为:d a.565 kJ·mol-1 b.-565 kJ·mol-1 c.1130 kJ·mol-1 d.-1130 kJ·mol-1 (8)在氨水溶液中加入固体NH4Cl后,氨水的离解度:d a.没变化 b.微有上升 c.剧烈上升 d.下降 (9)N的氢化物(NH3)的熔点都比它同族中其他氢化物的熔点高得多,这主要由于NH3:c
(√ ) 1. 电子云是描述核外某空间电子出现的几率密度的概念。(√)2. 同种原子之间的化学键的键长越短,其键能越大,化学键也越稳定。 (√)3.系统经历一个循环,无论多少步骤,只要回到初始状态,其热力学能和焓的变化量均为零。 (√)4. AgCl在NaCl溶液中的溶解度比在纯水中的溶解度小。(×)5. 原子轨道的形状由量子数m决定,轨道的空间伸展方向由l决定。 (1)某元素原子基态的电子构型为1s22s22p63s23p5,它在周期表中的位置是:a a.p区ⅦA族 b.s区ⅡA族 c.ds区ⅡB族 d.p区Ⅵ族 (2)下列物质中,哪个是非极性分子:b a.H2O b.CO2 c.HCl d.NH3 (3)极性共价化合物的实例是:b a.KCl b.HCl c.CCl4 d.BF3
(4)下列物质凝固时可以形成原子晶体的是:c a. O2 b. Pt, c. SiO2 d. KCl (5)在298K,100kPa下,反应 2H2(g)+O2(g)=2H2O(1) Δr H mΘ= -572 kJ·mol-1 则H2O(l)的Δf H mΘ为:d a.572 kJ·mol-1 b.-572 kJ·mol-1 c.286 kJ·mol-1 d.-286 kJ·mol-1 (6)定温定压下,已知反应B=A的反应热为Δr H m1Θ,反应B=C的反应热为Δr H m2Θ,则反应A=C的反应热Δr H m3Θ为:d a.Δr H m1Θ+Δr H m2Θ b.Δr H m1Θ-Δr H m2Θ c.Δr H m1Θ+2Δr H m2Θ d.Δr H m2Θ-Δr H m1Θ(7)已知HF(g)的标准生成热Δf H mΘ= -565 kJ·mol-1,则反应H2(g)+F2(g)=2HF(g)的Δr H mΘ为:d a.565 kJ·mol-1 b.-565 kJ·mol-1 c.1130 kJ·mol-1 d.-1130 kJ·mol-1 (8)在氨水溶液中加入固体NH4Cl后,氨水的离解度:d
北京科技大学 2012年硕士学位研究生入学考试试题=============================================================================================================试题编号:833 试题名称:无机化学(共8 页) 适用专业:化学、应用化学 说明:所有答案必须写在答题纸上,做在试题或草稿纸上无效。 ============================================================================================================= 一、选择题(共28小题, 每小题2分, 共56分) 1、下列分子中偶极矩最大的是..................................... ()。 (A) HCl;(B) HI;(C) HBr;(D) HF。 2、下列对氧族元素性质的叙述中正确的是.........()。 (A) 氧族元素与其它元素化合时,均可呈现+2,+4,+6 或-1,-2 等氧化值; (B) 氧族元素电负性从氧到钋依次增大; (C) 氧族元素的电负性从氧到钋依次减小; (D) 氧族元素都是非金属元素。 3、下列各族元素中,金属的化学活泼性随原子序数增加而减弱的是........................................................................................()。 (A) ⅠA;(B)ⅡA ;(C)ⅢA ;(D)ⅠB 。 4、关于配合物形成体的配位数,下列叙述中正确的是…........................................................................................................................()。 (A) 配位体半径愈大,配位数愈大; (B) 形成体的电荷数愈多,配位数愈大 (C) 中心原子( 或离子) 半径愈大,配位数愈大; (D) 由单齿( 单基) 配体形成的配合物,则配体总数就是形成体的配位数。 5、将50.0 mL 0.100 mol·L-1(NH4)2SO4溶液,加入到50.0 mL 0.200 -5 )溶液中,得到的缓冲溶 mol·L-1 NH 液pH 值是............................................................................................. ()。 (A) 8.70;(B) 9.56;(C) 9.26;(D) 9.00。 6、已知反应 C 2H2 (g) + 5 O2(g) → 2CO2 (g) + H2O (l) ?r H(1) = -1301.0 kJ·mol-1, 2 C(s) + O 2(g) → CO2 (g) ?r H(2) = -393.5 kJ·mol-1,
目录 绪论 实验1 仪器的认领和洗涤 实验2 灯的使用玻璃管的简单加工 实验3 称量练习——台秤和分析天平的使用 实验4 CO 相对分子质量的测定 2 实验5 硫酸铜结晶水的测定 实验6 溶液的配制 实验7 酸碱滴定 实验8 HAC电离度和电离常数的测定 实验9 水的净化——离子交换法 溶度积的测定 实验10 PbI 2 实验11 由海盐制试剂级NaCl 实验12 化学反应速率和活化能——数据的表达和处理 ——溶解、蒸发、结晶和固液分离 实验13 转化法制备KNO 3 实验14 碱式碳酸铜的制备——设计实验 实验15 氧化还原反应和氧化还原平衡 实验16 硫酸亚铁铵的制备——设计实验 实验17 P区非金属元素(一)(卤素、氧、硫) 实验18 P区非金属元素(二)(氮族、硅、硼) 实验19 常见非金属阴离子的分离与鉴定 实验20 硫代硫酸钠的制备 实验21 主族金属(碱金属、碱土金属、铝、锡、铅、锑、铋) 实验22 ds区金属(铜、银、锌、镉、汞) 实验23 常见阳离子的分离与鉴定(一) 实验24 第一过渡系元素(一)(钛、钒、铬、锰) 实验25 第一过渡系元素(二)(铁、钴、镍) 实验26 磺基水杨酸合铁(III)配合物的组成及其稳定常数的测定实验27 一种钴(III)配合物的制备 实验28 高锰酸钾的制备——固体碱熔氧化法 实验29 醋酸铬(II)水合物的制备——易被氧化的化合物的制备
实验30 从烂版液回收硫酸铜——设计实验(本科) 实验31 生物体中几种元素的定性鉴定(专科) 实验32 离子鉴定和未知物的鉴别——设计实验 绪论 一、为什么要学习无机实验课? 化学是一门实验科学,学习化学,离不开实验。 1、传授知识和技术; 2、训练科学方法和思维; 3、培养科学精神和品德 二、怎样学好无机实验? 1、预习——P2; 2、实验; 3、实验报告。 三遵守实验室规则。 一、注意实验室安全,学会自我保护。 二、对学生的要求。 1)关于预习报告:正规笔记本,不定期检查,评定平时成绩。两次没有者本学期成绩 评为不及格; 2)准时进入实验室,保持安静,穿好实验服; 3)每人都必须完成实验作业,及时如实地记录,凡有实验测定数据的都必须填好原始 数据表,我签字并贴在实验报告上。 保持实验台整洁有序,实验结束后清扫自己实验台及水池。 实验结束后给我看实验记录或产品,允许后再离开。每次实验当80%左右学生做完后,最好点评一次,当天问题当天解决。 4)做好值日,整理实验室,做好“三关”(关水、断电、关窗); 请假及纪律; 5)及时洗涤仪器,遵守仪器损坏赔偿制度; 6)及时交实验报告,杜绝抄袭; 7)成绩=平时成绩*60%+考试成绩*40%。
大学无机化学第六章试 题及答案 Document serial number【NL89WT-NY98YT-NC8CB-NNUUT-NUT108】
第六章化学键理论 本章总目标: 1:掌握离子键、共价键和金属键的基本特征以及它们的区别; 2:了解物质的性质与分子结构和键参数的关系; 3:重点掌握路易斯理论、价电子对互斥理论、杂化轨道理论以及分子轨道理论。 4:熟悉几种分子间作用力。 各小节目标: 第一节:离子键理论 1:掌握离子键的形成、性质和强度,学会从离子的电荷、电子构型和半径三个方面案例讨论离子的特征。 2:了解离子晶体的特征及几种简单离子晶体的晶体结构,初步学习从离子的电荷、电子构象和半径三个方面来分析离子晶体的空间构型。 第二节:共价键理论 1;掌握路易斯理论。 2:理解共价键的形成和本质。掌握价键理论的三个基本要点和共价键的类型。3:理解并掌握价层电子对互斥理论要点并学会用此理论来判断共价分子的结构,并会用杂化轨道理论和分子轨道理论来解释分子的构型。 第三节:金属键理论 了解金属键的能带理论和三种常见的金属晶格。 第四节:分子间作用力 1:了解分子极性的判断和分子间作用力(范德华力)以及氢键这种次级键的形成原因。 2;初步掌握离子极化作用及其强度影响因素以及此作用对化合物结构及性质的影响。 习题 一选择题 1.下列化合物含有极性共价键的是()(《无机化学例题与习题》吉大版) 2 C. Na 2 O 2.下列分子或离子中键能最大的是()
A. O 2 C. O 2 2+ D. O 2 2- 3. 下列化合物共价性最强的是()(《无机化学例题与习题》吉大版) C. BeI 2 4.极化能力最强的离子应具有的特性是() A.离子电荷高,离子半径大 B.离子电荷高,离子半径小 C.离子电荷低,离子半径小 D.离子电荷低,离子半径大 5. 下列化合物中,键的极性最弱的是()(《无机化学例题与习题》吉大版) 3 C. SiCl 4 6.对下列各组稳定性大小判断正确的是() +>O 22- B. O 2 ->O 2 C. NO+>NO D. OF->OF 7. 下列化合物中,含有非极性共价键的离子化合物是()(《无机化学例题与习题》吉大版) 3 C. Na 2 O 2 8.下列各对物质中,是等电子体的为() 和O 3 B. C和B+ C. He和Li D. N 2 和CO 9. 中心原子采取sp2杂化的分子是()(《无机化学例题与习题》吉大版) 3 C. PCl 3 10.下列分子中含有两个不同键长的是() A .CO 2 3 C. SF 4 11. 下列分子或离子中,不含有孤电子对的是()(《无机化学例题与习题》吉大版) A. H 2O B. H 3 O+ C. NH 3 D. NH 4 + 12.氨比甲烷易溶于水,其原因是() A.相对分子质量的差别 B.密度的差别 C. 氢键 D.熔点的差别 13. 下列分子属于极性分子的是()(《无机化学例题与习题》吉大版) A. CCl 43 C. BCl 3 D. PCl 5 14.下列哪一种物质只需克服色散力就能使之沸腾( ) 15. 下列分子中,中心原子采取等性杂化的是()(《无机化学例题与习题》吉大版)
一、是非判断题: 1.粗氯化钠必须用称量纸称量。(非) 2.溶解粗氯化钠时,加入的20ml蒸馏水需要很精确。(非) 3.用玻璃棒搅拌溶解氯化钠时,玻璃棒不应该碰撞烧杯内壁。(是) 4.可以把粗氯化钠溶液配制成饱和溶液。(非) 5.粗氯化钠溶液中含有不溶性杂质和可溶性杂质,必须先将不溶性杂质过滤除去。(是) 6.可以用无毒的CaCl2代替毒性很大的BaCl2除SO42- 。( 非) 7.BaSO4刚沉淀完全就应该立刻过滤。(非) 8.待过滤的溶液都应该冷却至室温再过滤。(非) 9.除去SO42-、Mg2+、Ca2+、K+离子的先后顺序可以倒置过来。(非) 10.氯化钠溶液在蒸发结晶过程中可以不搅拌,直到蒸干为止。(非) 实验五硫酸铝的制备 一、是非判断题: 1. NH4HCO3的作用是为了调节溶液pH值,以便生成Al(OH)3沉淀。( 是) 2. Al2(SO4)3的结晶水合物只有Al2(SO4)3·18H2O一种。( 非) 3. 在生成Al(OH)3 的过程中要加热煮沸并不断搅拌。( 是) 4. 硫酸铝加热至赤热分解成SO3和Al2O3。( 是) 5. 停止减压过滤时,操作不当会导致自来水溢入吸滤瓶内。( 是) 二、选择填空题: 1.在Al3+溶液中加入茜素的氨溶液,生成( A )色沉淀。 A.红色B.白色C.蓝色D.黑色 2.Al2(SO4)3易与碱金属M I(除Li以外)的硫酸盐结合成(B )。 A.配合物B.矾C.混合物 3.在蒸发皿中制备硫酸铝晶体时,加热浓缩至溶液体积为原来的(A )左右,在空气中缓慢冷却结晶。A.1/2 B.1/3 C.2/3 D.2/5 4.硫酸铝可作净水剂,是因为与水作用所得的(B )具有很强的吸附性能。 A.结晶水合物B.氢氧化铝C.Al2(SO4)3胶体 5.下面Al3+形成的配合物中,哪一个是错误的。(D) A.[AlF6]3- B.[Al(C2O4)3]3- C.[Al(EDTA)]- D.[AlBr6]3-
2004-2005年度第二学期 无机化学中段考试卷 一、选择题 ( 共15题 30分 ) 1. 2 分 (7459) 对于H2O2和N2H4,下列叙述正确的是…………………………………………() (A) 都是二元弱酸(B) 都是二元弱碱 (C) 都具有氧化性和还原性(D) 都可与氧气作用 2. 2 分 (4333) 下列含氧酸中属于三元酸的是…………………………………………………() (A) H3BO3 (B) H3PO2(C) H3PO3(D) H3AsO4 3. 2 分 (1305) 下列各对含氧酸盐热稳定性的大小顺序,正确的是……………………………() (A) BaCO3 > K2CO3(B) CaCO3 < CdCO3 (C) BeCO3 > MgCO3(D) Na2SO3 > NaHSO3 4. 2 分 (1478) 铝在空气中燃烧时,生成…………………………………………………………() (A) 单一化合物Al2O3 (B) Al2O3和Al2N3 (C) 单一化合物Al2N3 (D) Al2O3和AlN 5. 2 分 (7396) 下列含氧酸根中,属于环状结构的是…………………………………………() (A) (B) (C) (D) 6. 2 分 (1349) 下列化合物与水反应放出 HCl 的是……………………………………………() (A) CCl4(B) NCl3(C) POCl3(D) Cl2O7 7. 2 分 (1482) InCl2为逆磁性化合物,其中In的化合价为……………………………………() (A) +1 (B) +2 (C) +3 (D) +1和+3 8. 2 分 (7475) 鉴别Sn4+和Sn2+离子,应加的试剂为……………………………………………() (A) 盐酸 (B) 硝酸(C) 硫酸钠 (D) 硫化钠(过量)
北京科技大学成人教育学院 2007—2008学年第二学期 《无机化学》试题B卷 一、填空题:(每空1分,共30分) 1、频率越高,活化分子数,反应。 2、H2(g)+I2(g)=2HI(g),Kθ=50.3(713k).某状态下,p氢气=p碘=5.379×105pa,p碘化氢=62.59×105pa.则自发进行的方向是______________,原因是________________。 2、2NH3(g)=N2(g)+3H2(g).298k,△rHθ m =+92.22kj·mol-1, △rSθ m =+198.53j·mol-1·k-1,则标准状态下,NH3(g)自发分解的温度是_________________。 3、系统命名[CoCl(NH3)3(H2O)2]Cl2 为,三羟基.水.乙二胺合铬(Ⅲ)的化学式 为。 4、已知基元反应2NO2=2NO+O2,则其速率方式为 v= ,反应级数为。 5、当J
第五章 原子结构和元素周期表 本章总目标: 1:了解核外电子运动的特殊性,会看波函数和电子云的图形 2:能够运用轨道填充顺序图,按照核外电子排布原理,写出若干元素的电子构型。 3:掌握各类元素电子构型的特征 4:了解电离势,电负性等概念的意义和它们与原子结构的关系。 各小节目标: 第一节:近代原子结构理论的确立 学会讨论氢原子的玻尔行星模型213.6E eV n = 。 第二节:微观粒子运动的特殊性 1:掌握微观粒子具有波粒二象性(h h P mv λ= =)。 2:学习运用不确定原理(2h x P m π???≥ )。 第三节:核外电子运动状态的描述 1:初步理解量子力学对核外电子运动状态的描述方法——处于定态的核外电子在核外空间的概率密度分布(即电子云)。 2:掌握描述核外电子的运动状态——能层、能级、轨道和自旋以及4个量子数。 3:掌握核外电子可能状态数的推算。 第四节:核外电子的排布 1:了解影响轨道能量的因素及多电子原子的能级图。 2;掌握核外电子排布的三个原则: ○ 1能量最低原则——多电子原子在基态时,核外电子尽可能分布到能量最低的院子轨道。 ○ 2Pauli 原则——在同一原子中没有四个量子数完全相同的电子,或者说是在同一个原子中没有运动状态完全相同的电子。 ○3Hund 原则——电子分布到能量简并的原子轨道时,优先以自旋相同的方式
分别占据不同的轨道。 3:学会利用电子排布的三原则进行 第五节:元素周期表 认识元素的周期、元素的族和元素的分区,会看元素周期表。 第六节:元素基本性质的周期性 掌握元素基本性质的四个概念及周期性变化 1:原子半径——○1从左向右,随着核电荷的增加,原子核对外层电子的吸引力也增加,使原子半径逐渐减小;○2随着核外电子数的增加,电子间的相互斥力也增强,使得原子半径增加。但是,由于增加的电子不足以完全屏蔽增加的核电荷,因此从左向右有效核电荷逐渐增加,原子半径逐渐减小。 2:电离能——从左向右随着核电荷数的增多和原子半径的减小,原子核对外层电子的引力增大,电离能呈递增趋势。 3:电子亲和能——在同一周期中,从左至右电子亲和能基本呈增加趋势,同主族,从上到下电子亲和能呈减小的趋势。 4:电负性——在同一周期中,从左至右随着元素的非金属性逐渐增强而电负性增强,在同一主族中从上至下随着元素的金属性依次增强而电负性递减。 习题 一选择题 1.3d电子的径向函数分布图有()(《无机化学例题与习题》吉大版) A.1个峰 B.2个峰 C. 3个峰 D. 4个峰 2.波函数一定,则原子核外电子在空间的运动状态就确定,但仍不能确定的是() A.电子的能量 B.电子在空间各处出现的几率密度 C.电子距原子核的平均距离 D.电子的运动轨迹 3.在下列轨道上的电子,在xy平面上的电子云密度为零的是()(《无机化学例题与习题》吉大版) A .3s B .3p x C . 3p z D .3d z2 4.下列各组量子数中,合理的一组是() A .n=3,l=1,m l=+1,m s= +1/2 B .n=4,l=5,m l= -1,m s= +1/2 C .n=3,l=3,m l=+1,m s= -1/2
《无机化学》试题 学号:姓名:座号: 系别:年级:专业: 总分合计人:复核人: 一、单项选择题 (在每小题列出的四个选项中只有一个选项是 符合题目要求的,请选出正确选项并在“答题卡” 的相应位置上涂黑。多涂、少涂、错误均无分。 每小题1分,共40分) 1、对于Zn2+/Zn电对,增大Zn2+的浓度,则其标准电极电势将() A 增大 B 减小 C 不变 D 无法判断 2、Cu2+离子的外层电子构型为() A 8e B 18e型 C 18+2e D 9~17e型 3、设氨水的解离平衡常数为 K。浓度为m mol·L-1的氨水溶液, b 若将其用水稀释一倍,则溶液中OH-的浓度(mol·L-1)为()
A m 21 B θb K m ?2 1 C 2/m K b ?θ D 2m 4、已知θsp K (Ag 3PO 4) = 1.4× 10-16,其溶解度为 ( ) A 1.1×10-4mol?L -1; B 4.8×10-5mol?L -1; C 1.2×10-8mol?L -1; D 8.3×10-5mol ?L -1 5、下列各组物质,能自发发生反应的是 ( ) A Cu 、Cu 2+; B Cr 2O 72-、Cr 3+; C MnO 2、Mn 2+; D SnCl 4、Sn 6 、 3d 轨 道 的 磁 量 子 数 可 能 是 ( ) A 1,2,3 B 0,1,2 C 0,±1 D 0, ±1, ±2 7、下列各分子中,以sp 3不等性杂化轨道成键的是 ( ) A BeCl 2 B PCl 3 C BF 3 D SiH 4 8、熔化下列晶体时,只需克服色散力的是 ( ) A HF B Ag C KF D CO 2 9.已知V E A /θ:Cr 2O 72- +1.36 Cr 3+ -0.41 Cr 2+ -0.86 Cr ,则判断发 生歧化反应的是 ( ) A 都不能 B Cr 2O 72- C Cr 3+ D Cr 2+ 10. 下 列 各 物 质 中 ,熔 点 最 高 的 是
大学无机化学试题集及答案 第一章气体、液体和溶液的性质 1. 敞口烧瓶在7℃所盛的气体,必须加热到什么温度,才能使1/3气体逸出烧瓶? 2. 已知一气筒在27℃,30.0atm时,含480g的氧气。若此筒被加热到100℃,然后启开 阀门(温度保持在100℃),一直到气体压力降到 1.00atm时,共放出多少克氧气? 3. 在30℃时,把8.0gCO2、6.0gO2和未知量的N2放入10dm3的容器中,总压力达800 mmHg。试求: (1) 容器中气体的总摩尔数为多少?(2) 每种气体的摩尔分数为多少? (3) 每种气体的分压为多少?(4) 容器中氮气为多少克? 4. CO和CO2的混合密度为 1.82g dm-3(在STP下)。问CO的重量百分数为多少? 5. 已知某混合气体组成为:20份氦气,20份氮气,50份一氧化氮,50份二氧化氮。问:在0℃,760mmHg下200dm3此混合气体中,氮气为多少克? 6. S2F10的沸点为29℃,问:在此温度和1atm下,该气体的密度为多少? 7. 体积为8.2dm3的长颈瓶中,含有 4.0g氢气,0.50mol氧气和分压为2atm 的氩气。这 时的温度为127℃。问: (1) 此长颈瓶中混合气体的混合密度为多少? (2) 此长颈瓶内的总压多大? (3) 氢的摩尔分数为多少? (4) 假设在长颈瓶中点火花,使之发生如下反应,直到反应完全: 2H2(g) + O2(g) =2H2O(g) 当温度仍然保持在127℃时,此长颈瓶中的总压又为多大? 8. 在通常的条件下,二氧化氮实际上是二氧化氮和四氧化二氮的两种混合气体。在45℃,总压为1atm时,混合气体的密度为 2.56g dm-3。计算: (1) 这两种气体的分压。(2) 这两种气体的重量百分比。 9. 在1.00atm和100℃时,混合300cm3H2和100 cm3O2,并使之反应。反应后温度和压力 回到原来的状态。问此时混合气体的体积为多少毫升?若反应完成后把温度降低到27℃,压力仍为 1.00atm,则混合气体的体积为多少毫升? (已知27℃时水的饱和蒸汽压为26.7mmHg) 10. 当0.75mol的“A4”固体与2mol的气态O2在一密闭的容器中加热,若反应物完全消 耗仅能生成一种化合物,已知当温度降回到初温时,容器内所施的压力等于原来的一半,从这些数据,你对反应生成物如何下结论? 11. 有两个容器A和B,各装有氧气和氮气。在25℃时: 容器A:O2 体积500 cm3,压力1atm。
实验习题 p区非金属元素(卤素、氧、硫) 1.氯能从含碘离子的溶液中取代碘,碘又能从氯酸钾溶液中取代氯,这两个反应有无矛盾?为什么? 答:这两个反应无矛盾。因为氯的氧化性强于碘,而碘的氧化性又强于氯酸钾。 2.根据实验结果比较: ①S2O82-与MnO4-氧化性的强弱;②S2O32-与I-还原性的强弱。 答:因为S2O82-可以将Mn2+氧化为MnO4-,所以S2O82-的氧化性强于MnO4-,S2O32-能将I2还原为I-,S2O32-和还原性强于I-。 3.硫代硫酸钠溶液与硝酸银溶液反应时,为何有时为硫化银沉淀,有时又为[Ag(S2O3)2]3-配离子? 答:这与溶液的浓度和酸碱性有关,当酸性强时,会生成硫化银沉淀,而在中性条件下就会生成[Ag(S2O3)2]3-配离子。 4.如何区别: ①次氯酸钠和氯酸钠; ②三种酸性气体:氯化氢、二氧化硫、硫化氢; ③硫酸钠、亚硫酸钠、硫代硫酸钠、硫化钠。 答:①分别取少量两种固体,放入试管中,然后分别往试管中加入适量水,使固体全部溶解,再分别向两支试管中滴入两滴品红溶液,使品红溶液褪色的试管中放入的固体为次氯酸钠,剩下的一种为氯酸钠。 ②将三种气体分别通入品红溶液中,使品红褪色的是二氧化硫,然后将 剩余的两种气体分别通入盛有KMnO4溶液的试管中,产生淡蓝色沉淀的是H2S,剩下的一种气体是氯化氢。 ③分别取四种溶液放入四支试管中,然后向四支试管中分别加入适量等量 的H2SO4溶液,有刺激性气味气体产生的是亚硫酸钠,产生臭鸡蛋气味气体是的硫化钠,既有刺激性气味气体产生,又有黄色沉淀产生的是硫代硫酸钠,无明显现象的是硫酸钠。 5.设计一张硫的各种氧化态转化关系图。
《无机化学》试题 学号:姓名: 座号: : 复核人: 一、单项选择题 (在每小题列出得四个选项中只有一个选项就 是符合题目要求得,请选出正确选项并在“答题 卡”得相应位置上涂黑。多涂、少涂、错误均无分. 每小题1分,共40分) 1、对于Zn2+/Zn电对,增大Zn2+得浓度,则其标准电极电势将() A 增大B减小 C 不变D无法判断 2、Cu2+离子得外层电子构型为() A8 B 18型C18+2 D 9~17型 3、设氨水得解离平衡常数为。浓度为mol·L-1得氨水溶液,若将其用水稀释一倍,则溶液中OH-得浓度(mol·L-1)为() AB C D 2 4、已知(Ag3PO4)=1、4×10-16,其溶解度为
( ) A1、1×10-4mol?L-1; B 4、8×10—5mol?L-1; C1、2×10-8mol?L—1; D8、3×10-5mol?L-1 5、下列各组物质,能自发发生反应得就是() ACu、Cu2+;B Cr2O72—、Cr3+; CMnO2、Mn2+;D SnCl4、Sn 6、3d轨道得磁量子数可能就是() A 1,2,3 B 0,1,2C0,±1 D 0,±1,±2 7、下列各分子中,以sp3不等性杂化轨道成键得就是() ABeCl2BPCl3 C BF3 D SiH4 8、熔化下列晶体时,只需克服色散力得就是( ) AHF BAg CKF D CO2 9、已知:Cr2O72— +1、36 Cr3+ -0、41Cr2+—0、86 Cr,则判断发生歧化反应得就是()
A 都不能 B Cr2O72- C Cr3+ D Cr2+ 10、下列各物质中,熔点最高得就是( ) A K2O B MgO C CaO DNa2O 11稀溶液依数性得本质就是() A、渗透压B、沸点升高C、蒸汽压下降D、凝固点降低 12要降低反应得活化能,可以采取得手段就是() A、升高温度 B、降低温度 C、移去产物 D、使用催化剂 13如果一个反应得吉布斯自由能变为零,则反应( ) A、能自发进行B、就是吸热反应C、就是放热反应D、处于平衡状态 14、反应A+ BC,焓变小于零,若温度升高10℃,其结果就是() A、对反应没有影响B、使平衡常数增大一倍C、不改变反应速率D、使平衡常数减小
无机化学实验报告 【实验名称】实验七:水的总硬度及电导率的测定 【班级】 【日期】 【姓名】 【学号】 一、实验目的 ① 了解硬水,软水及去离子水的概念。 ② 学会化学法(配位滴定法)和电导率法两种检验水质的方法。 ③ 学习电导率仪和微量滴定管的操作和使用。 二、 实验原理 1、配位滴定法测定水的总硬度 (1)实验原理 Ca 2+、Mg 2+是生活用水中主要的杂质离子,他们以碳酸氢盐、氯化物、硫酸盐、硝酸盐等形式溶于水中,水中还有微量的Fe 3+、Al 3+等,由于Ca 2+、Mg 2+远比其他几种离子含量高,所以通常用Ca 2+、Mg 2+的总量来计算水的总硬度。 水质的分类 法,即在pH=10的碱性缓冲溶液中,用酸性铬兰K-萘酚绿B 混合指示剂(简称K-B 指示剂),以EDTA (Na 2H 2Y )标准溶液直接滴定水中的Ca 2+、Mg 2+。滴定反应表示如下。 ○ 1滴定前: Ca 2+、Mg 2+与酸性铬蓝K 形成红色螯合物,在萘酚绿B 的衬托下,溶液呈紫红色 K-B + M (Ca 2+、Mg 2+ ) 10 =======pH M -K-B (蓝绿) (紫红) ○ 2滴定开始至化学计量点以前: EDTA 与游离的Ca 2+、Mg 2+配位 H 2Y 2- + Ca 2+ ==== CaY 2- +2H + H 2Y 2- + Mg 2+ ==== MgY 2- +2H + ○ 3化学计量点时: EDTA 与酸性铬兰K 的Ca 2+、Mg 2+螯合物反应,溶液由紫红色变为蓝绿色 H 2Y 2- + M-K-B ==== MgY 2- + K-B + 2H + (紫红色) (蓝绿) 水样中存在微量的杂质离子Fe 3+、Al 3+,可用三乙醇胺进行掩蔽。