
??
∈ ??1 ?10023?? ??? ?0.02 – 2.50 mg/L NH
- N Test tN Tube TM?
3
?? ???∈? ∈??∈?
1 ??Clin. Chim. Acta, 14, 403 (1966).
?? ?
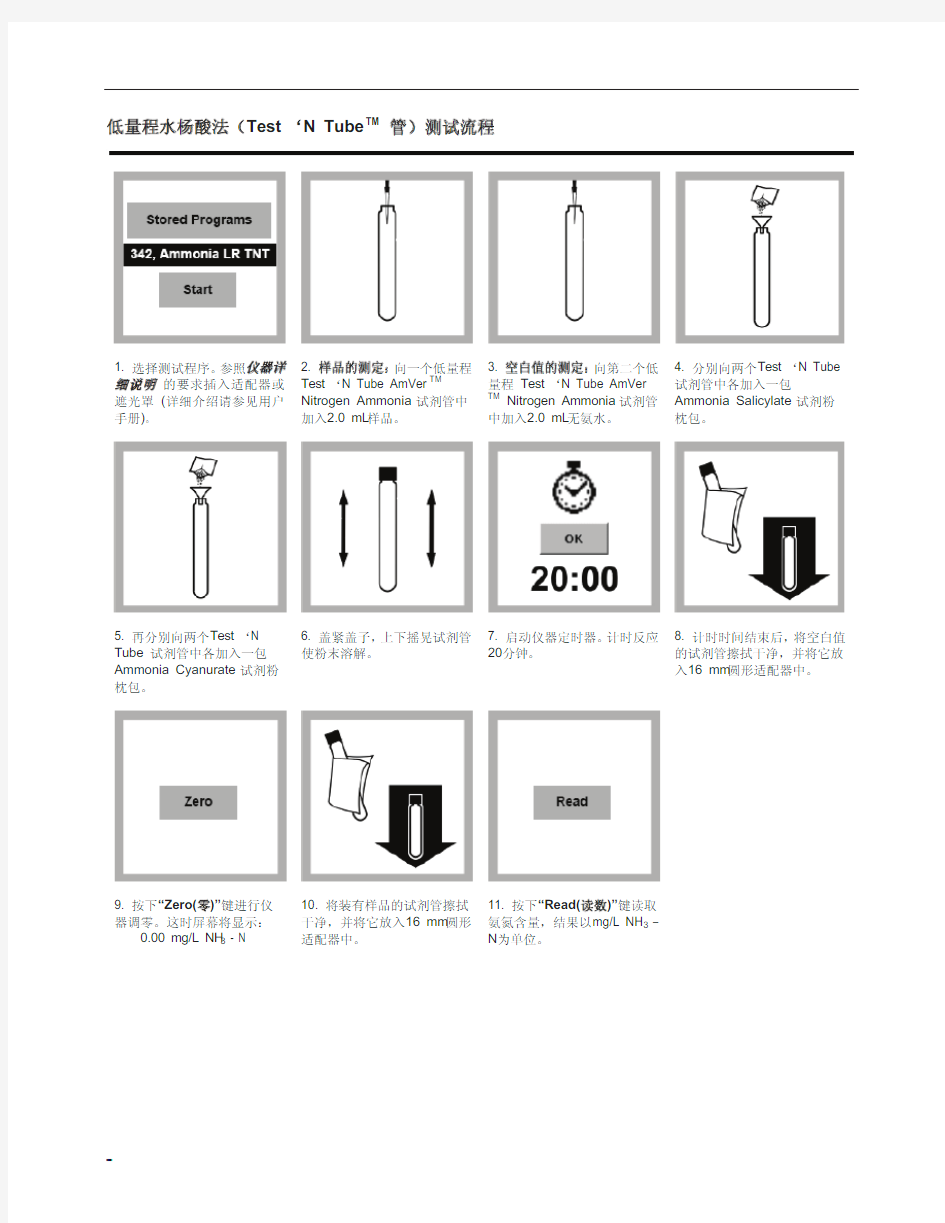
???∈ ???Test tN Tube TM ??????
1. ? ??? ? ?? ??? ??? ?? ? ? (????? ?? )?
2. ? ?? ?
????? Test tN Tube AmVer TM
Nitrogen Ammonia ? ?Ё 2.0 mL ? ? 3. ぎ? ?? ? ?????? Test tN Tube AmVer
TM
Nitrogen Ammonia ? ?Ё 2.0 mL ?∈?
4. ??Test tN Tube
? ?Ё ?
Ammonia Salicylate ? ? ?
5. ??Test tN Tube ? ?Ё ? Ammonia Cyanurate ? ? ?
6. ??? ??? ? ??? ⒊??
7. ? ?? 20
??
8. ? ?? ? ぎ? ?? ? ? 16 mm ?? Ё?
9. ?“Zero(?)”???? ???? ??
0.00 mg/L NH 3 - N 10. ? ? ?? ? ? 16 mm ?? Ё? 11. ?“Read(? )”?? ?? ??? ?mg/L NH 3 – N ? ??
??
? ???? ?
? ?? ??????? ??? ? ?? ??
? Ё?? ? ?? ? ∈?Ё? ?? 0.3 mg/L Cl 2 1?0.1 N ?????⒊????? 1 ∈??? ??
?? ??? ?? ???????? ? ?pH ? ?2 ?2??? ?
? ??4 ? ( 39 ? )? ???? ?
? ? ? 28 ?
?? ?? ? ?? ??
?? ?? ??5.0 N?? ?⒊?Ё ? ? ? ? ?pH ? ?7.0?
? ? ?? ? ???? ?
? ? ?
?( ?)
? ? ??? ?? ?
??Voulette ?
?? ? ?? ?50 mg/L NH 3 – N
??
TenSette??? ? ?
? ?ㄦ?25 mL???
1. ? ??? ? ? ? ????( ??)? ? Ё?* ?? ? ? ? ? ??
? ?? ? ? 乊ッ???? ?? ? ?? ?
4. ? ?50 mg/L NH3 – N???Voulette ? ?? ? ?
5. ?TenSette??? ?? ?? ? ??? ?ㄦЁ????25 mL ? 唤???TenSette???
??? ?ㄦЁ?? 0.1 mL?0.2 mL 0.3 mL? ???? ?
6. ?0.1 mL? ? ? ??????∈ ???Test tN Tube TM???????? ?? ? ?????
“Read(? )”??? ??? ? ??? ?
7. ????? ? “Graph( ?)”? ? ? ?? ? ? ??? ? ? ?
“Ideal Line(? ? )”? ? ? ?100% ??“? ? ”П?? ???? ?? ?? ?100%? ??
⒊??
? ? ??? ? ???? ?? ? ?
??? ?? ? ?
?? ⒊??? ?1.0 mg/L
tN Tube TM???????????
1. ?? ?1.0 mg/L??? ⒊?? ? ??????∈ ???Test
⒊?? ??
???
?? ???? ? ????????∈ ?? ? 5-? ∈ ??? ?? ?? ? ?????5-? ∈ ???? ?????? ???? 咘????? Ё?⒊? ?????? ???655 nm? ? ?? ??
?? ?
??
∈ ?? ?10031催? ??? ?0.4 – 50.0 mg/L NH
- N Test tN Tube TM?
3
?? ???∈? ∈??∈?
?? ?
催??∈ ???Test tN Tube TM ??????
1. ? ??? ? ?? ??? ??? ?? ? ? (????? ?? )?
2. ? ?? ? ??催?? Test tN Tube AmVer TM
Nitrogen Ammonia ? ?Ё 0.1 mL ? ? 3. ぎ? ?? ? ????
?? Test tN Tube AmVer
TM
Nitrogen Ammonia ? ?Ё 0.1 mL ?∈? 4. ?? ??5 mL ?
Test t
N Tube ? ?Ё ? Ammonia Salicylate ? ? ?
5. ??Test tN Tube ? ?Ё ? Ammonia Cyanurate ? ? ?
6. ??? ??? ? ??? ⒊??
7. ? ?? 20 ??
8.
? ?? ? ぎ? ?? ? ? 16 mm ?? Ё?
9. ?“Zero(?)”???? ???? ??
0.0 mg/L NH 3 - N 10. ? ? ?? ? ? 16 mm ?? Ё? 11. ?“Read(? )”?? ?? ??? ?mg/L NH 3 – N ? ??
??
? ???? ?
? ?? ??????? ??? ? ?? ??
? Ё?? ? ?? ? ∈?Ё? ?? 0.3 mg/L Cl 2 1?0.1 N ?????⒊????? 1 ∈??? ??
?? ??? ?? ???????? ? ?pH ? ?2 ?2??? ?
? ??4 ? ( 39 ? )? ???? ?
? ? ? 28 ?
?? ?? ? ?? ??
?? ?? ??5.0 N?? ?⒊?Ё ? ? ? ? ?pH ? ?7.0?
? ? ?? ? ???? ?
? ? ?
?( ?)
? ? ??? ?? ?
??Voulette ?
?? ? ?? ?150 mg/L NH 3 – N
??
TenSette??? ? ?
? ?ㄦ?25 mL???
1. ? ??? ? ? ? ????( ??)? ? Ё?* ?? ? ? ? ? ??
? ?? ? ? 乊ッ???? ?? ? ?? ?
4. ? ?150 mg/L NH3 – N???Voulette ? ?? ? ?
5. ?TenSette??? ?? ?? ? ??? ?ㄦЁ????25 mL ? 唤???TenSette???
??? ?ㄦЁ?? 0.2 mL?0.4 mL 0.6 mL? ???? ?
6. ?0.2 mL? ? ? ???催??∈ ???Test tN Tube TM???????? ?? ? ?????
“Read(? )”??? ??? ? ??? ?
7. ????? ? “Graph( ?)”? ? ? ?? ? ? ??? ? ? ?
“Ideal Line(? ? )”? ? ? ?100% ??“? ? ”П?? ???? ?? ?? ?100%? ??
⒊??
? ? ??? ? ???? ?? ? ?
??? ?? ? ?
?? ⒊??? ?100 mg/L
? ∈
???A??50 mL
????A??20 mL
1. ?? ?? ? ?40.0 mg/L??? ⒊??
a. ? 20.0 mL? ?100 mg/L??? ⒊?? 50 mL? ??Ё?
b. ? ? ∈?? ??? ??? ?
2. ?? ?40.0 mg/L??? ⒊?? ? ???催??∈ ???Test tN Tube TM??????????
⒊?? ??
???
?? ???? ? ????????∈ ?? ? 5-? ∈ ??? ?? ?? ? ?????5-? ∈ ???? ?????? ???? 咘????? Ё?⒊? ?????? ???655 nm? ? ?? ??
?? ?
??
∈ ??1 ?8155??? ?0.01 – 0.50 mg/L NH
- N ?
3
?? ???∈? ∈??∈?
1 ??Clin. Chim. Acta, 14, 403 (1966).
?? ?
∈ ???? ?????
1. ? ??? ? ?? ??? ??? ?? (????? ?? )?
2. ? ?? ? 10 mL ? ?????Ё?
3. ぎ? ?? ? 10 mL ? ∈ ??????Ё?
4. ????Ё ?
Ammonia Salicylate ? ? ?
5. ????? ??? ?? ⒊??
6. ? ?? 3 ??
7. ? ?? ? ????Ё ?
Ammonia Cyanurate ? ? ?
8. ????? ?
?? ?? ⒊??
9. ? ?? 15 ??
? Ё? ??? ? ⒊? ??? 10. ? ?? ? ぎ? ???? ? ?? Ё? 11. ?“Zero(?)”???? ???? ??
0.00 mg/L NH 3 - N
12. ? ? ???? ? ?? Ё? ?“Read(? )”?? ?? ??? ? mg/L NH 3 - N ? ??
??
? ???? ?
? ?? ??????? ??? ? ?? ??
? Ё?? ? ?? ? ∈?Ё? ?? 0.3 mg/L Cl 2 1?0.1 N ?????⒊????? 1 ∈??? ??
?? ??? ?? ????????(? ∈Ё 2 mL???) ? ?pH ? ?2 ?2??? ?
? ????4 ? ( 39 ? )? ???? ?? ? ? 28 ?
?? ?? ? ?? ?? ?5.0 N?? ?⒊?Ё ? ? ? ? ?pH ? ?7.0?
? ? ?? ? ???? ?
? ? ?
?( ?)
? ? ??? ?? ?
?? ⒊??? ?10 mg/L NH 3 – N
TenSette??? ? ?
? ?ㄦ?25 mL???
1. ? ??? ? ? ? ????( ??)? ? Ё?
* ?? ? ? ? ? ??
3. “OK( )”??? ?? ?? ?? ???咬? ? “EDIT(??? )”? ? ??咬? ? ?? ??
? ?? ? ? 乊ッ???? ?? ? ?? ?
4. ? ?10 mg/L NH3 – N??? ⒊??
5. ?TenSette??? ?? ?? ? ??? ?ㄦЁ????25 mL ? 唤???TenSette???
??? ?ㄦЁ?? 0.2 mL?0.4 mL 0.6 mL? ???? ?
6. ?0.2 mL? ? ? ???∈ ???? ??????? ?? ? ????? “Read(? )”???
??? ? ??? ?
7. ????? ? “Graph( ?)”? ? ? ?? ? ? ??? ? ? ?
“Ideal Line(? ? )”? ? ? ?100% ??“? ? ”П?? ???? ?? ?? ?100%? ??
⒊??
? ? ??? ? ???? ?? ? ?
??? ?? ? ?
?? ⒊??? ?10 mg/L
??Voulette ?
?? ? ?? ?50 mg/L NH3 – N
? ∈
???A??100 mL
????A??4 mL
TenSette??? ? ? ???? ?0.1 ? 1.0 mL
1. ?? ?? ? ?0.40 mg/L??? ⒊??
a. ? 4.00 mL? ?10 mg/L??? ⒊?? 100 mL? ??Ё?
b. ? ? ∈?? ??? ??? ?
a. ?TenSette??? ? 0.8 mL? ?50 mg/L NH3 – N???Voulette ? ?? ? ? 100 mL? ??Ё?
b. ? ? ∈?? ??? ??? ?
2. ?? ?0.40 mg/L??? ⒊?? ? ???∈ ???? ?????????
⒊?? ??
???
?? ???? ? ????????∈ ?? ? 5-? ∈ ??? ?? ?? ? ?????5-? ∈ ???? ?????? ???? 咘????? Ё?⒊? ?????? ???655 nm? ? ?? ??
?? ?
??
USEPA1 ??? ?2 ?8038??? ?0.02 – 2.50 mg/L NH
- N
3
?? ???∈? ∈??∈? ∈??∈???佣乘 ??USEPA? ? ∈ ?(???佣乘 ?)?? ? ???佣? ?
1 USEPA? ? ∈?? ?(???佣)?
2 ??Standard Methods for the Examination of Water and Wastewater 4500 - NH
B & C.
3
?? ?
??? ? ????
1. ? ??? ? ?? ??? ??? ?? (????? ?? )?
2. ? ?? ? 25 mL ? ??? ?ㄦЁ????25 mL ? 唤?
3. ぎ? ?? ? 25 mL ? ∈ ???? ?ㄦ
Ё????25 mL
? 唤? 4. ??? ?ㄦЁ
3?Mineral Stabilizer ? ⒊????? ? ??ㄦ
??? ?
5. ??? ?ㄦЁ 3?Polyvinyl Alcohol Dispersing ? ⒊????? ? ??ㄦ ??? ?
6. ??? ?ㄦЁ
1.0 mL ??? ???? ? ??ㄦ ??? ?
7. ? ??
1 ??
8. ? ?? ? ???ㄦЁ?⒊? ?????Ё????10 mL ? 唤?
9. ぎ? ???? ? ?? Ё? 10. ?“Zero(?)”???? ???? ??
0.00 mg/L NH 3 - N
11. ? ? ???? ? ?? Ё?
12. ?“Read(? )”?? ?? ??? ? mg/L NH 3 - N ? ??
??
? ???? ?
? ?? ??????? ?
? Ё?? ? ?? ? ∈?Ё? ?? 0.3 mg/L Cl2 1?0.1 N ?????⒊?* ???? 1 ∈??? ??
?? ??? ?? ????????(? ∈Ё 2 mL???) ? ?pH ? ?2 ?2??? ?
? ????4 ? ( 39 ? )? ???? ?? ? ? 28 ?
?? ?? ? ?? ?? ?5.0 N?? ?⒊?* Ё ? ? ? ? ?pH ? ?7.0?
? ? ?? ? ???? ?
? ? ?
?( ?)
? ? ??? ?? ?
??Voulette ?
?? ? ?? ?50 mg/L NH 3 – N
??
TenSette??? ? ?
? ?ㄦ?25 mL???
1. ? ??? ? ? ? ????( ??)? ? Ё?
? ?? ? ? 乊ッ???? ?? ? ?? ?
4. ? ?50 mg/L NH3 – N???Voulette ? ?? ? ?
5. ?TenSette??? ?? ?? ? ??? ?ㄦЁ????25 mL ? 唤???TenSette???
??? ?ㄦЁ?? 0.1 mL?0.2 mL 0.3 mL? ???? ?
* ?? ? ? ? ? ??
6. ?0.1 mL? ? ? ?????? ??????? ?? ? ????? “Read(? )”??? ??
? ? ??? ?
7. ????? ? “Graph( ?)”? ? ? ?? ? ? ??? ? ? ?
“Ideal Line(? ? )”? ? ? ?100% ??“? ? ”П?? ???? ?? ?? ?100%? ??
⒊??
? ? ??? ? ???? ?? ? ?
??? ?? ? ?
??Voulette ?
?? ? ?? ?1 mg/L NH 3 – N
1. ?? ?1 mg/L??? ⒊?? ? ? ?????? ??????????
⒊?? ??
?佣
1. ? 250 mL? ??250 mL?? ?Ё? ?? ??400 mL?? Ё? ????? ? ??mg/L Cl2
1?? ?0.1 N??????⒊????? ? ??乘 ??
2. 25 mL??? ⒊??? ??1 N??? ? pH ? ?9.5 ??pH???? ?pH ?
3. ??佣?? ? ??佣??? ??⒊? ?佣?? ?? ?
4. ??ㄦ? 25 mL ? ∈? ??250 mL?? ?Ё? ? Boric Acid ? ?? ? ? ?? ?佣??
????? ? ? 催????? ッ?? ⒊?Ё?
5. ? ? ??5?? ? ??10?? ? ∈? ? ∈?? Ё ? ????
6. ? 150 mL?佣? ? ? ? ?? ??佣??? ?? ????佣? ? ? ?佣???????
? ?150 mL?佣?( ?? ?175 mL)?
7. ?1 N??? ?⒊? ?佣??pH ? ?7 ??pH????佣??pH ?
8. ?佣? ??250 mL? ??Ё?? ? ∈ ?? ?? ?? ???? ? ∈ ? ?? ? ?
? ? ?????? ??????????
???
?Ё??????〇 (Mineral Stabilizer) ? Ё??? ??? ?? ??Э?? (Polyvinyl Alcohol Dispersing Agent) ??? ?? ?????? Ё ?? ?咘???? ? Ё??? ??? ????? ???425 nm? ? ?? ??
?? ?
水质氨氮的测定 氨氮(NH3-N)以游离氨(NH3)或铵盐(NH4+)形式存在于水中,两者的组成比取决于水的pH值和水温。当pH值偏高时,游离氨的比例较高。反之,则铵盐的比例高,水温则相反。 氨氮的测定方法主要有纳氏比色法、气相分子吸收法、苯酚——次氯酸盐(或水杨酸——次氯酸盐)比色法和电极法等。本节将主要介绍纳氏比色法和蒸馏——酸滴定法。 当水样带色或浑浊以及含有其他一些干扰物质,影响氨氮的测定。为此,在分析时需作适当的预处理。对较清洁的水,可采用絮凝沉淀法(加适量的硫酸锌于水样中,并加氢氧化钠使成碱性,生成氢氧化锌沉淀,再经过滤除去颜色和浑浊);对污染严重的水或工业废水,则用蒸馏法消除干扰(调节水样的pH值使在6.0-7.4的范围,加入适量氧化镁使成微碱性,蒸馏释放出的氨被吸收于硫酸或硼酸溶液中。采用纳氏比色法或酸滴定法时,以硼酸溶液为吸收液;采用水杨酸——次氯酸盐比色法时,则以硫酸溶液为吸收液)。 本实验的主要目的: 1 掌握水样预处理的方法; 2 掌握氨氮的测定原理及测定方法的选择 3 掌握分光光度计的使用方法,学习标准系列的配制和标准曲线的制作 一、纳氏试剂光度法(A1) 1 实验原理 碘化汞和碘化钾与氨反应生成淡红棕色胶态化合物,此颜色在较宽的波长内具强烈吸收。通常测量用410~425nm范围。 2 实验仪器 2.1 分光光度计 2.2 pH计 2.3 20mm比色皿 2.4 50mL比色管 1本方法与GB7479-87等效。
3 实验试剂 3.1 纳氏试剂:可任择以下两种方法中的一种配制。 3.1.1 称取20g碘化钾溶于约100ml水中,边搅拌边分次少量加入二氯化汞结晶粉末(约10g),至出现朱红色沉淀不易溶解时,改为滴加饱和二氯化汞溶液,并充分搅拌,当出现微量朱红色沉淀不易溶解时,停止滴加二氯化汞溶液。 另称取60g氢氧化钾溶于水,并稀释至250ml,充分冷却至室温后,将上述溶液在搅拌下,徐徐注入氢氧化钾溶液中,用水稀释至400ml,混匀。静置过夜。将上清液移入聚乙烯瓶中,密塞保存待用。 3.1.2 称取16g氢氧化钠,溶于50ml水中,充分冷却至室温。 另称取7g碘化钾和10g碘化汞溶于水,然后将此溶液在搅拌下徐徐注入氢氧化钠溶液中,用水稀释至100ml,贮于聚乙烯瓶中,密塞保存待用。 3.2 酒石酸钾钠溶液:称取50g酒石酸钾钠(KNaC4H4O6·4H2O)溶于100ml水中,加热煮沸以去除氨,放冷,定容100ml。 3.3 铵标准贮备溶液:称取3.819g经100℃干燥过的优级纯氯化铵(NH4Cl)溶于水中,移入1000ml容量瓶中,稀释至标线。此溶液每毫升含1.00mg氨氮。 3.4 铵标准使用液:移取5.00ml铵标准贮备液(3.3)于500ml容量瓶中,用水稀释至标线。此溶液每毫升含0.010mg氨氮。 4 实验步骤 4.1 标准曲线的制作 4.1.1 吸取0、0.50、1.00、3.00、 5.00、7.00和10.00ml铵标准使用液(3.4)于50ml 比色管中,加水至标线,加1.0ml酒石酸钾钠溶液(3.2),摇匀。加1.5ml纳氏试剂(3.1.1或3.1.2),混匀。放置10min后,在波长420nm出,用光程20mm比色皿,以水为参比,测量吸光度。 4.1.2 由测得的吸光度减去空白的吸光度后,得到校正吸光度,以氨氮含量(mg)对校正吸光度的统计回归标准曲线。 4.2 水样的测定 4.2.1 分取适量经絮凝沉淀预处理后的水样(使氨氮含量不超过0.1mg),加入50ml 比色管中,稀释至标线,加1.0ml酒石酸钾钠溶液。以下同标准曲线的制作(4.1)。 4.2.2 分取适量经蒸馏预处理后的馏出液,加入50ml比色管中,加一定量1mol/L氢
氨氮在线分析仪使用说明书简介
使用安全说明 一、总则 请在开机运行前认真阅读本手册,并严格按照本手册说明进行操作,尤其注意所有有关危险和谨慎问题的说明,请不要擅自维修、拆装仪器上任意组件,否则可能会导致对操作人员的严重伤害和对仪器的严重损伤。 二、触电与灼伤预防 1、维护或修理前务必断开电源; 2、按照地方或国家规则进行电力连接; 3、尽可能使用接地故障断路器; 4、在连接操作条件下将操作单元接地,接地电阻≤10Ω。 5、化学药品危险预防。 本设备所需的部分化学药品为有毒有腐蚀性物质,在处理这些药品时,请参照本手册试剂章节中的相关内容,采取一定的预防措施。 不正确的使用仪器或其部件以及/或其附件会导致人身伤害、仪器损坏或污染。 因此一定要确保正确使用仪器和/或其部件以及/或其附件。 仪器是专门为了测量经过处理的水溶液中的NH3-N而设计的(废水、过程水和地表水)。
目录 使用安全说明 (2) 一、总则 (2) 二、触电与灼伤预防 (2) 第一章、技术参数 (4) 第二章、概述 (5) 一、基本原理 (5) 二、产品特点 (5) 三、系统描述 (5)
第一章、技术参数 仪器尺寸图:
第二章、概述 一、基本原理 本仪器采用纳式试剂比色法来测量水体中的以游离态的氨或铵离子存在的氨氮。 水样中游离态的氨或铵离子与纳式试剂反应生成淡红棕色络合物,该络合物的浓度与氨氮的量成正比,在波长420nm下测量。 二、产品特点 1、全新的计量系统 ▲ 光学定量试样/试剂,从本质上提高了定量精度。 ▲ 法国OEM 进样阀岛,最大可能的减少了死体积对定量精度的影响。 2、校正清洗功能 ▲ 仪器可以自动实现用热硫酸清洗管道,无需用户干预,避免测量误差。 3、完善的系统自我维护功能 ▲ 仪器在出现故障时,具有自我检查和维护功能,确保人身安全和设备安全。 ▲ 当发生液体泄漏的时,设备自带的湿度传感器会发生报警,并自动锁定.。 ▲ 所有故障信息都在HMI显示终端处予以记录,用户可以查询,对设备运行状况了如指掌。 4、远程升级功能 ▲ 仪表具备远程升级功能,可以通过ETHERNET口、GPRS口等实现对设备的远程维护和监控。 5、软件升级功能 ▲ 仪表具备完善的联网功能,可以实现和ETHERNET等广域网的互联互通。 大屏幕触摸屏显示终端 ▲ 仪表采用的是640*480带触摸的TFT显示终端,显示信息更加丰富,操作更加简单 6、强大的对外接口功能 ▲ 仪表对外接口丰富,现场使用的各种接口(如ETHERNET/4-20mA输入、输出/RS485/开关量输入、输出等)都具备 ▲ 仪表的良好的可扩展性,使得可以按用户需求增加设备的功能。 三、系统描述 1、内部结构图
水质氨氮检测方法及操作步骤 氨氮 氨氮(NH3-N)以游离氨(NH3)或铵盐(NH4+)形式存在于水中,两者的组成比取决于水的pH值。当pH值偏高时,游离氨的比例较高。反之,则铵盐的比例为高。 水中氨氮的来源主要为生活污水中含氮有机物受微生物作用的分解产物,某些工业废水,如焦化废水和合成氨化肥厂废水等,以及农田排水。此外,在无氧环境中,水中存在的亚硝酸盐亦可受微生物作用,还原为氨。在有氧环境中,水中氨亦可转变为亚硝酸盐、甚至继续转变为硝酸盐。 测定水中各种形态的氮化合物,有助于评价水体被污染和“自净”状况。 氨氮含量较高时,对鱼类则可呈现毒害作用。 1.方法的选择 氨氮检测方法,通常有纳氏比色法、苯酚-次氯酸盐(或水酸-次氯酸盐)比色法和电极法等。纳氏试剂比色法具操作简便、灵敏等特点,水中钙、镁和铁等金属离子、硫化物、醛和酮类、颜色,以及浑浊等干扰测定,需做相应的预处理,苯酚-次氯酸盐比色法具灵敏、稳定等优点,干扰情况和消除方法同纳氏试剂比色法。电极法通常不需要对水样进行预处理和具测量围宽等优点。氨氮含量较高时,尚可采用蒸馏﹣酸滴定法。 2.水样的保存 水样采集在聚乙烯瓶或玻璃瓶,并应尽快分析,必要时可加硫酸将水样酸化至pH<2,于2—5℃下存放。酸化样品应注意防止吸收空气中的氮而遭致污染。 预处理 水样带色或浑浊以及含其它一些干扰物质,影响氨氮的测定。为此,在分析时需做适当的预处理。对较清洁的水,可采用絮凝沉淀法,对污染严重的水或工业废水,则以蒸馏法使之消除干扰。 (一)絮凝沉淀法 概述 加适量的硫酸锌于水样中,并加氢氧化钠使呈碱性,生成氢氧化锌沉淀,再经过滤去除颜色和浑浊等。 仪器 100ml具塞量筒或比色管。 试剂
氨氮是指水中以游离氨(NH3)和铵离子(NH4)形式存在的氮。动物性有机物的含氮量一般较植物性有机物为高。同时,人畜粪便中含氮有机物很不稳定,容易分解成氨。因此,水中氨氮含量增高时指以氨或铵离子形式存在的化合氨。 氨氮主要来源于人和动物的排泄物,生活污水中平均含氮量每人每年可达2.5~4.5公斤。 雨水径流以及农用化肥的流失也是氮的重要来源。 另外,氨氮还来自化工、冶金、石油化工、油漆颜料、煤气、炼焦、鞣革、化肥等工业废水中。 当氨溶于水时,其中一部分氨与水反应生成铵离子,一部分形成水合氨,也称非离子氨。 非离子氨是引起水生生物毒害的主要因子,而氨离子相对基本无毒。国家标准Ⅲ类地面水,非离子氨的浓度≤0.02毫克/升。 氨氮是水体中的营养素,可导致水富营养化现象产生,是水体中的主要耗氧污染物,对鱼类及某些水生生物有毒害。 纳氏试剂比色法 1 原理 碘化汞和碘化钾的碱性溶液与氨反映生成淡红棕色胶态化合物,其色 度与氨氮含量成正比,通常可在波长410~425nm范围内测其吸光度,计算其含量. 本法最低检出浓度为0.025mg/L(光度法),测定上限为2mg/L.采用目视比色法,最低检出浓度为0.02mg/L.水样做适当的预处理后,本法可用于地 面水,地下水,工业废水和生活污水中氨氮的测定. 2 仪器 2.1 带氮球的定氮蒸馏装置:500mL凯氏烧瓶,氮球,直形冷凝管和导管. 2.2 分光光度计 2.3 pH计 3 试剂 配制试剂用水均应为无氨水 3.1 无氨水可选用下列方法之一进行制备:
3.1.1 蒸馏法:每升蒸馏水中加0.1mL硫酸,在全玻璃蒸馏器中重蒸馏,弃去50mL初馏液,按取其余馏出液于具塞磨口的玻璃瓶中,密塞保存. 3.1.2 离子交换法:使蒸馏水通过强酸型阳离子交换树脂柱. 3.2 1mol/L盐酸溶液. 3.3 1mol/L氢氧化纳溶液. 3.4 轻质氧化镁(MgO):将氧化镁在500℃下加热,以出去碳酸盐. 3.5 0.05%溴百里酚蓝指示液:pH6.0~7.6. 3.6 防沫剂,如石蜡碎片. 3.7 吸收液: 3.7.1 硼酸溶液:称取20g硼酸溶于水,稀释至1L. 3.7.2 0.01mol/L硫酸溶液. 3.8 纳氏试剂:可选择下列方法之一制备: 3.8.1 称取20g碘化钾溶于约100mL水中,边搅拌边分次少量加入二氯化汞(HgCl2)结晶粉末(约10g),至出现朱红色沉淀不易溶解时,改写滴加饱和二氯化汞溶液,并充分搅拌,当出现微量朱红色沉淀不再溶解时,停止滴加二氯化汞溶液. 另称取60g氢氧化钾溶于水,并稀释至250mL,冷却至室温后,将上述溶液徐徐注入氢氧化钾溶液中,用水稀释至400mL,混匀.静置过夜将上清液移入聚乙烯瓶中,密塞保存. 3.8.2 称取16g氢氧化纳,溶于50mL水中,充分冷却至室温. 另称取7g碘化钾和碘化汞(HgI2)溶于水,然后将此溶液在搅拌下徐徐注入氢氧化纳溶液中,用水稀释至100mL,贮于聚乙烯瓶中,密塞保存. 3.9 酒石酸钾纳溶液:称取50g酒石酸钾纳KNaC4H4O6·4H2O)溶于100mL水中,加热煮沸以除去氨,放冷,定容至100Ml. 3.10 铵标准贮备溶液:称取3.819g经100℃干燥过的优级纯氯化铵(NH4Cl)溶于水中,移入1000mL容量瓶中,稀释至标线.此溶液每毫升含 1.00mg氨氮. 3.11 铵标准使用溶液:移取5.00mL铵标准贮备液于500mL容量瓶中,用水稀释至标线.此溶液每毫升含0.010mg氨氮. 4 测定步骤 4.1 水样预处理:取250mL水样(如氨氮含量较高,可取适量并加水至250mL,使氨氮含量不超过2.5mg),移入凯氏烧瓶中,家数滴溴百里酚蓝指示液,用氢氧化纳溶液或演算溶液调节至pH7左右.加入0.25g轻质氧化镁和数粒玻璃珠,立即连接氮球和冷凝管,导 管下端插入吸收液液面下.加热蒸馏,至馏出液达200mL时,停止蒸馏,定容至250mL. 采用酸滴定法或纳氏比色法时,以50mL硼酸溶液为吸收液;采用水杨酸-次氯酸盐比色法时,改用50mL0.01mol/L硫酸溶液为吸收液.
氨氮的测定方法 氨氮的测定方法,通常有纳氏比色法、苯酚—次氯酸盐(或水杨酸—次氯酸盐)比色法和电极法等。纳氏比色法具有操作简便、灵敏等特点,但钙、镁、铁等金属离子、硫化物、醛、酮类,以及水中色度和混浊等干扰测定,需要相应的预处理。以下是纳氏试剂比色法的测定方法。 一、纳氏试剂比色法的原理 碘化钾和碘化汞的碱性溶液与氨反应生成淡红棕色胶态化和物,其色度与氨氮含量成正比,通常可在 410-425nm 范围内测其吸光度,计算其含量。 本法最低检出浓度为 0.025mg/L(光度法),测定上限为 2 mg/L。采用目视比色法,最低检出浓度为 0.02mg/L。水样作适当的预处理后,本法可适用于地面水、地下水、工业废水和生活污水。 二、仪器 1、带氮球的定氮蒸馏装置:500 mL 凯氏烧瓶、氮球、直形冷凝管。 2、分光光度计 3、 PH 计 三、试剂 做次实验配制试剂均应用无氨水配制。 1、无氨水。配制可选用以下任意一种方法制备: (1)蒸馏法:每升蒸馏水中加 0.1mL 硫酸,在全玻璃蒸馏器中重蒸馏,弃去 50mL 初馏液,接取其余馏出液于具塞磨口的玻璃瓶中,密塞保存。 (2)离子交换法:使蒸馏水通过强酸性阳离子交换树脂柱。 2、1mol/L 的盐酸溶液 3、1mol/L 的氢氧化钠溶液 4、轻质氧化镁:将氧化镁在 500℃下加热,以除去碳酸盐。
5、0.05%溴百里酚蓝指示计(PH6.0-7.6)。 6、防沫剂:如石蜡碎片 7、吸收剂:①硼酸溶液:称取 20g 硼酸溶于水,稀释至 1L。② 0.01mol/L 硫酸溶液。 8、纳氏试剂。可选用下列方法之一制备: (1)称取 20g 碘化钾溶于约 25mL 水中,边搅拌边分次加入少量的二氯化汞(HgCl 2)结晶粉末(约 10g),至出现朱红色不易降解时,改为滴加饱和二氯化汞溶液,并充分搅拌,当出现微量朱红色沉淀不再溶解时,停止滴加氯化汞溶液。 另称取 60g 氢氧化钾溶于水,并稀释至 250mL,冷却至室温后,将上述溶液徐徐注入氢氧化钾溶液中,用水稀释至 400mL,混匀。静置过夜,将上清液移入聚乙烯瓶中,密塞保存。 (2)称取 16g 氢氧化钠,溶于 50mL 水中,充分冷却至室温。另称取 7g 碘化钾和碘化汞溶于水,然后将次溶液在搅拌下徐徐注入氢氧化钠溶液中,用水稀释至 100mL,贮于聚乙烯瓶中,密塞保存。 9、酒石酸钾钠溶液:称取 50g 酒石酸钾钠(KNaC 4H 4 O 6 .4H 2 O)溶于100mL 水中,加热煮 沸以除去氨,放冷,定容至 100mL。 10、铵标准贮备溶液:称取 3.819g 经 100℃干燥过的氯化氨(NH 4 Cl)溶于水中,移入 1000mL 容量瓶中,稀释至标线。从溶液每毫升含1.00mg 氨氮。 11、铵标准使用溶液:移取5.00 mL 铵标准贮备溶液于500mL 容量瓶中,用水稀释至标线。此溶液每毫升含0.01mg 氨氮。 四、测定步骤 1、水样预处理:取 250mL 水样(如氨氮含量较高,可取适量并加水至 250mL,使氨氮含量不超过 2.5mg),移入凯氏烧瓶中,加数滴溴百里酚蓝指示液,用氢氧化钠溶液或盐酸溶液调节至 PH 为 7 左右。加入 0.25g 轻质氧化镁和数粒玻璃珠,立即连接氮球和冷凝管,导管下端插入吸收液液面下。加热蒸馏,至馏出液达 200mL 时,停止蒸馏。定容至 250mL。 采用酸滴定法或纳氏比色法时,以 50mL 硼酸溶液为吸收剂;采用水扬酸—次氯酸盐比色法时,改用 50mL0.01mol/L 硫酸溶液为吸收剂。 2、标准曲线的绘制:吸取 0、0.50、1.00、3.00、5.00、7.00 和10.00mL 铵标准使用
氨氮的测定纳氏试剂分光光度法 目次 前言............................................................................................................................... ..................III 1适用范围............................................................................................................................... .. (1) 2方法原理............................................................................................................................... .. (1) 3干扰及消除............................................................................................................................... . (1) 4试剂和材料............................................................................................................................... . (1) 5仪器和设备............................................................................................................................... . (3) 6样品............................................................................................................................... . (3) 7分析步骤............................................................................................................................... .. (4) 8结果计算............................................................................................................................... .. (4) 9准确度和精密度 (5) 10质量保证和质量控制 (5)
水质氨氮检测方法及操作步骤
水质氨氮检测方法及操作步骤 氨氮 氨氮(NH3-N)以游离氨(NH3)或铵盐(NH4+)形式存在于水中,两者的组成比取决于水的pH值。当pH值偏高时,游离氨的比例较高。反之,则铵盐的比例为高。 水中氨氮的来源主要为生活污水中含氮有机物受微生物作用的分解产物,某些工业废水,如焦化废水和合成氨化肥厂废水等,以及农田排水。另外,在无氧环境中,水中存在的亚硝酸盐亦可受微生物作用,还原为氨。在有氧环境中,水中氨亦可转变为亚硝酸盐、甚至继续转变为硝酸盐。 测定水中各种形态的氮化合物,有助于评价水体被污染和“自净”状况。 氨氮含量较高时,对鱼类则可呈现毒害作用。 1.方法的选择 氨氮检测方法,一般有纳氏比色法、苯酚-次氯酸盐(或水杨酸-次氯酸盐)比色法和电极法等。纳氏试剂比色法具操作简便、灵敏等特点,水中钙、镁和铁等金属离子、硫化物、醛和酮类、颜色,以及浑浊等干扰测定,需做相应的预处理,苯酚-次氯酸盐比色法具灵敏、稳定等优点,干扰情况和消除方法同纳氏试剂比色
法。电极法一般不需要对水样进行预处理和具测量范围宽等优点。氨氮含量较高时,尚可采用蒸馏﹣酸滴定法。 2.水样的保存 水样采集在聚乙烯瓶或玻璃瓶内,并应尽快分析,必要时可加硫酸将水样酸化至pH<2,于2—5℃下存放。酸化样品应注意防止吸收空气中的氮而遭致污染。 预处理 水样带色或浑浊以及含其它一些干扰物质,影响氨氮的测定。为此,在分析时需做适当的预处理。对较清洁的水,可采用絮凝沉淀法,对污染严重的水或工业废水,则以蒸馏法使之消除干扰。 (一)絮凝沉淀法 概述 加适量的硫酸锌于水样中,并加氢氧化钠使呈碱性,生成氢氧化锌沉淀,再经过滤去除颜色和浑浊等。 仪器 100ml具塞量筒或比色管。 试剂
精心整理 1.范围 1.1 本方法规定了用纳氏试剂分光光度法测定水中的氨氮。 1.2 本方法适用于地下水、地表水、生活污水和工业废水中氨氮的测定。 1.3 当水样体积为50mL,使用20mm比色皿时,本方法检出限为0.025mg/L,测定下限为0.10mg/L, 测定上限为2.0mg/L(均以N计)。 2.参考标准 水质氨氮的测定纳氏试剂分光光度法HJ535-2009 3.职责 4. 5. 5.1 5.2 6.试剂 6.1制备6.1 6.1.2蒸馏法:在1000mL的蒸馏水中,加0.1mL硫酸(ρ=1.84g/mL),在全玻璃蒸馏器中重蒸 馏,弃去前50mL馏出液,然后将约800mL馏出液收集在带有磨口玻璃塞的玻璃瓶内。每升 馏出液加10g强酸性阳离子交换树脂(氢型)。 6.2 盐酸,ρ(HCl)=1.18g/mL。 6.3 硫酸,ρ(H2SO4)=1.84g/mL。 6.4 无水乙醇 6.5 轻质氧化镁(MgO):不含碳酸盐,在500℃下加热氧化镁,以除去碳酸盐。
6.6 氢氧化钠(NaOH) 6.7 可溶性淀粉 6.8 碘化钾(KI) 6.9 碘化汞(HgI) 6.10 氢氧化钾(KOH) 6.11 二氯化汞(HgCl2) 6.12 纳氏试剂 ?碘化汞–碘化钾–氢氧化钠(HgI2-KI-NaOH)溶液: (6.8) 氢氧化? 6.13 6.14 6.15 6.16 。6.17 硫酸锌(ZnSO4·7H2O) 6.18 硫酸锌溶液,ρ=100g/L,称取10.0g硫酸锌(6.17)溶于水中,稀释至100mL。 6.19 氢氧化钠溶液,ρ=250g/L。称取25g氢氧化钠(6.6)溶于水中,稀释至100mL。 6.20 氢氧化钠溶液,c(NaOH)=1mol/L。称取4g氢氧化钠(6.6)溶于水中,稀释至100mL。 6.21 盐酸溶液,c(HCl)=1mol/L。用吸量管吸取8.5mL盐酸(6.2)于100mL容量瓶中,用水稀释 至标线。 6.22 硼酸(H3BO3)
水质分析中氨氮测定的标准方法 氨氮 氨氮(NH3-N)以游离氨(NH3)或铵盐(NH4+)形式存在于水中,两者的组成比取决于水的pH值。当pH值偏高时,游离氨的比例较高。反之,则铵盐的比例为高。 水中氨氮的来源主要为生活污水中含氮有机物受微生物作用的分解产物,某些工业废水,如焦化废水和合成氨化肥厂废水等,以及农田排水。此外,在无氧环境中,水中存在的亚硝酸盐亦可受微生物作用,还原为氨。在有氧环境中,水中氨亦可转变为亚硝酸盐、甚至继续转变为硝酸盐。 测定水中各种形态的氮化合物,有助于评价水体被污染和“自净”状况。 氨氮含量较高时,对鱼类则可呈现毒害作用。 测定方法一:纳氏试剂光度法(GB7479--87) 1.方法原理 碘化汞和碘化钾的碱性溶液与氨反应生成淡红棕色胶态化合物,此颜色在较宽的波长范围内具强烈吸收。通常测量用波长在410—425nm范围。 2.干扰及消除 脂肪胺、芳香胺、醛类、丙酮、醇类和有机氯胺类等有机化合物,以及铁、锰、镁、硫等无机离子,因产生异色或浑浊而引起干扰,水中颜色和浑浊亦影响比色。为此,须经絮凝沉淀过滤或蒸馏预处理,易挥发的还原性干扰物质,还可在酸性条件下加热除去。对金属离子的干扰,可加入适量的掩蔽剂加以消除。 3.方法适用范围 本法最低检出浓度为0.025molL(光度法),测定上限为2mgL。采用目视比色法,最低检出浓度为0.02mgL。水样作适当的预处理后,本法可适用于地表水、地下水、工业废水和生活污水。 仪器 (1)分光光度计:UV-2800(UNICO) (2)pH计。
试剂 配制试剂用水应为无氨水。 1.纳氏试剂 可选择下列一种方法制备。 (1)称取20g碘化钾溶于约25ml水中,边搅拌边分次少量加入二氯化汞(HgCI2)结晶粉末(约10g),至出现朱红色沉淀不易溶解时,改为滴加饱和二氯化汞溶液,并充分搅拌,当出现微量朱红色沉淀不再溶解时,停止滴加二氯化汞溶液。 另称取60g氢氧化钾溶于水,并稀释至250ml,冷却至室温后,将上述溶液在边搅拌下,徐徐注入氢氧化钾溶液中,用水稀释至400ml,混匀。静置过夜,将上清液移入聚乙烯瓶中,密塞保存。 (2)称取16g氢氧化钠,溶于50ml充分冷却至室温。 另称取7g碘化钾和10g碘化汞(HgI2)溶于水,然后将此溶液在搅拌下徐徐注入氢氧化钠溶液中,用水稀释至100ml,贮于聚乙烯瓶中,密塞保存。 2.酒石酸钾钠溶液 称取50g酒石酸钾钠(KnaC4H4O6·4H2O)溶于100ml水中,加热煮沸以除去氨,放冷,定容至100ml。 3.铵标准贮备溶液 称取3.819g经100℃干燥过的氯化铵(NH4Cl)溶于水中,稀释至标线。此溶液每毫升含1.00mg氨氮。 4.铵标准使用溶液 移取5.00ml铵标准贮备液于500ml容量瓶中,用水稀释至标线。此溶液每毫升含0.010mg 氨氮。 步骤 1.校准曲线的绘制 吸取0、0.50、1.00、3.00、5.00、7.00、和10.0ml铵标准使用液于50ml比色管中,加水至标线。加1.0ml酒石酸钾钠溶液,混匀。加1.5ml纳氏试剂,混匀。放置10min后,在波长4250nm处,用光程20mm比色皿,以水作参比,测量吸光度。
氨氮 氮是有好几个指标:氨氮,总氮,硝酸盐氮,亚硝酸盐氮,凯式氮等 氨氮比较简便准确,精密度尚可的就是纳氏试剂比色法,不过一般根据水样浑浊程度,确定采用哪种预处理方法,一般较浑浊的用蒸馏法预处理,较清洁的用絮凝沉降预处理。预处理过的水样,测定氨氮一般用纳氏试剂法测定,含量高点也可以用滴定法。都是国标。 氨氮(NH3-N)以游离氨(NH3)或铵盐(NH4+)形式存在于水中,两者的组成比取决于水的pH值。当pH值偏高时,游离氨的比例较高。反之,则铵盐的比例为高。 水中氨氮的来源主要为生活污水中含氮有机物受微生物作用的分解产物,某些工业废水,如焦化废水和合成氨化肥厂废水等,以及农田排水。此外,在无氧环境中,水中存在的亚硝酸盐亦可受微生物作用,还原为氨。在有氧环境中,水中氨亦可转变为亚硝酸盐、甚至继续转变为硝酸盐。 测定水中各种形态的氮化合物,有助于评价水体被污染和“自净”状况。 氨氮含量较高时,对鱼类则可呈现毒害作用。 1.方法的选择 氨氮的测定方法,通常有纳氏比色法、苯酚-次氯酸盐(或水杨酸-次氯酸盐)比色法和电极法等。纳氏试剂比色法具操作简便、灵敏等特点,水中钙、镁和铁等金属离子、硫化物、醛和酮类、颜色,以及浑浊等干扰测定,需做相应的预处理,苯酚-次氯酸盐比色法具灵敏、稳定等优点,干扰情况和消除方法同纳氏试剂比色法。电极法
通常不需要对水样进行预处理和具测量范围宽等优点。氨氮含量较高时,尚可采用蒸馏﹣酸滴定法。 2.水样的保存 水样采集在聚乙烯瓶或玻璃瓶内,并应尽快分析,必要时可加硫酸将水样酸化至pH<2,于2—5℃下存放。酸化样品应注意防止吸收空气中的氮而遭致污染。 预处理 水样带色或浑浊以及含其它一些干扰物质,影响氨氮的测定。为此,在分析时需做适当的预处理。对较清洁的水,可采用絮凝沉淀法,对污染严重的水或工业废水,则以蒸馏法使之消除干扰。 (一)絮凝沉淀法 概述 加适量的硫酸锌于水样中,并加氢氧化钠使呈碱性,生成氢氧化锌沉淀,再经过滤去除颜色和浑浊等。 仪器 100ml具塞量筒或比色管。 试剂 (1)10%(m/V)硫酸锌溶液:称取10g硫酸锌溶于水,稀释至100ml。(2)25%氢氧化钠溶液:称取25g氢氧化钠溶于水,稀释至100ml,贮于聚乙烯瓶中。
1. 范围 1.1 本方法规定了用纳氏试剂分光光度法测定水中的氨氮。 1.2 本方法适用于地下水、地表水、生活污水和工业废水中氨氮的测定。 1.3 当水样体积为50mL,使用20mm比色皿时,本方法检出限为0.025mg/L,测定下限为 0.10mg/L,测定上限为2.0mg/L(均以N计)。 2. 参考标准 水质氨氮的测定纳氏试剂分光光度法HJ 535-2009 3. 职责 检测技术人员按本作业指导书对水样中氨氮进行分析检测。 4. 方法原理 以游离态的氨或铵离子等形式存在的氨氮与纳氏试剂反应生成淡红棕色络合物,该络合物的吸光度与氨氮含量成正比,于波长420nm处测量吸光度。 5. 干扰及消除 5.1 水样中含有悬浮物、余氯、钙镁离子等金属离子、硫化物和有机物时会产生干扰,含 有此类物质时要作适当处理,以消除对测定的影响。 5.2 若样品中存在余氯,可加入适量的硫代硫酸钠溶液去除,用淀粉–碘化钾试纸检验余氯 是否除尽。在显色时加入适量的酒石酸钾钠溶液,可消除钙镁等金属离子的干扰。若水样浑浊或有颜色时可用预蒸馏法或絮凝沉淀法处理。 6. 试剂 除非另有说明,分析时所用试剂均为符合国家标准的分析纯化学试剂,实验用水为按6.1制备的水,使用经过检定的容量器皿和量器。 6.1 无氨水,在无氨环境中用纯水器法制备。用市售纯水器直接制备。或采用下述方法之 一制备: 6.1.1 离子交换法:蒸馏水通过强酸性阳离子交换树脂(氢型)柱,将流出液收集在带有 磨口玻璃塞的玻璃瓶内。每升流出液加10g同样的树脂,以利于保存。 6.1.2 蒸馏法:在1000mL的蒸馏水中,加0.1mL硫酸(ρ=1.84g/mL),在全玻璃蒸馏器 中重蒸馏,弃去前50mL馏出液,然后将约800mL馏出液收集在带有磨口玻璃塞的 玻璃瓶内。每升馏出液加10g强酸性阳离子交换树脂(氢型)。 6.2 盐酸,ρ(HCl)=1.18g/mL。 6.3 硫酸,ρ(H2SO4)=1.84g/mL。 6.4 无水乙醇 6.5 轻质氧化镁(MgO):不含碳酸盐,在500 ℃下加热氧化镁,以除去碳酸盐。 6.6 氢氧化钠(NaOH)
ODM系列产品-水质自动分析仪器氨氮(水杨酸比色法)自动分析仪产品说明书
目录 第一章安全预防措施特别声明 (1) 1.1 总则 (1) 1.2 触电与灼伤预防 (1) 1.3 化学药品危险预防 (1) 第二章技术规格 (2) 第三章系统概述 (3) 3.1 应用 (3) 3.2 系统描述 (3) 3.3 电气器件 (3) 3.4 基本原理 (3) 3.5 检测步骤 (4) 第四章拆箱和安装 (5) 4.1 拆箱 (5) 4.2 安装 (5) 4.2.2 监测子站房室内要求 (6) 4.2.3 安装 (6) 第五章试剂 (10) 5.1 零点标准溶液 (10) 5.2 氨氮标准溶液 (10) 5.3 试剂A溶液 (11) 5.4 试剂B溶液 (11) 5.5 试剂C溶液 (12) 5.6 试剂的使用与保存 (13) 5.7 稳定性和反应性 (13) 5.8 试剂的放置 (13) 5.9 废液处理 (13) 第六章仪器操作 (14) 6.1 仪器初始化 (14) 6.2 校准 (14) 6.3清洗 (14) 6.4 测量 (14) 6.5 触摸屏介绍 (15) 6.5.1 数据设置方法 (15) 6.5.2 指令输入与生效显示 (15) 6.5.3 屏幕操作 (15) 第七章故障维修 (25) 第八章日常维护 (27)
第一章安全预防措施特别声明 1.1 总则 请在开机运行前认真阅读本手册,并严格按照本手册说明进行操作,尤其注意所有有关危险和谨慎问题的说明,请不要擅自维修、拆装仪器上任意组件,否则可能会导致对操作人员的严重伤害和对仪器的严重损伤。 1.2 触电与灼伤预防 1.2.1 维护或修理前务必断开电源; 1.2.2 按照地方或国家规则进行电力连接; 1.2.3 尽可能使用接地故障断路器; 1.2.4 在连接操作条件下将操作单元接地。 1.3 化学药品危险预防 本设备所需的部分化学药品为有毒有腐蚀性物质,在处理这些药品时,请参照本手册试剂章节中的相关内容,采取一定的预防措施。 1.4 标志 注:本产品的性能在不断地改进之中。如有更改,恕不另行通知。
关于环境水质氨氮快速检测探索 摘要 :水中氨氮的来源主要为生活污水中含氮有机物受微生物作用的分解产物、某些工业废水 , 如焦化废水和合成氨化肥厂废水、农田排水、养殖水中过剩饲料和鱼、虾大量排泄物的累积及过度施肥等。此外 , 在无氧环境中 , 水中存在的亚硝酸盐亦可受微生物作用 , 还原为氨。在有氧环境中 , 水中氨亦可转变为亚硝酸盐或继续转变为硝酸盐。在水中氨氮主要以游离氨和铵盐两种形式存在。 关键词 :氨氮快速检测 中图分类号 :o657.32 文献标识码 :a 文章编 号 :1672-3791(201206(b-0140-02 目前中国水污染问题已经成为我国经济社会发展的最重要制约因素之一 , 已经引起国家和地方政府的高度重视 , 我国确定了单位 gdp 能耗每年减少 20%的目标 :主要污染物排放 , 包括二氧化硫、化学需氧量总量 5年内要减少 10%的减排目标。水污染在人口范围内的正常生产和生活秩序都造成了人员伤亡 , 而且在财产的巨大和损害人类生存的环境上都存在严重的问题 , 因此“非典”后的环境安全应急响应系统党的建设和国家政府的高度重视。现在需要防范突发性污染事故解决许多问题 , 最紧迫的问题之一是建立应急监测系统 , 一旦污染事故 , 监测可以迅速投入在最短的时间内提供了一个准确的污染这是为了防止污染和应对措施提供了科学依据的传播 , 提高快速应能力。在水体污染防治工作中 , 水质监测工作是污染预警、
持续性污染物监测和治理效果评定的重要手段 , 已受到有关部门的重视。作为连续性监测工具的水质在线监测仪器承担着提供准确监测数据和监测报告的责任 , 在环境监测工作中发挥着越来越重要的作用。根据中国环境保护产业协会环境监测仪器专业委员会发布的《我国环境监测仪器行业 2009年发展综述》 ,2009年 , 废水污染源在线监测设备实现产值约 6.8亿元。废水污染源在线监测市场主要从cod 在线监测仪器安装起步 , 过去十年经历了快速的增长。中国环保产业协会的统计数据表明 ,2008年 , 全国 cod 在线监测系统产值达 68,276万元。 2009年 , 全国cod 在线监测系统产值达 68,000万元。自从 2000年以来 cod 在线监测系统产值的增长情况 :目前全国废水污染源监测系统的市场保有量在 1.8万套以上 , 以每套系统的寿命 5年计算。从中国工控网的统计数据看 , 度过金融危机的影响后 , 废水污染源在线监测仪器的市场仍保持了较快的增长速度 , 到 2010年该细分市场的规模将达 10.68亿元。 1 环境水质氨氮监测技术特点 1.1 形成与传统的实验室方法不同的应急监测和其他物质兼容技术 近年来 , 我们有针对性了很多探索性的工作 , 并从国外的研究已受到启发 , 开始发展中国的国情 , 容易成熟的技术快速检测管在快速和容易掌握和控制作为一种新型的水质检测 , 事实上 , 快速检测方法和方法的动态水质环境监测和应急现场分析。已完成的氰化物、 氟化物、酚、硫化物、溶解氧氨、氯等 50种快速测试管和发展 zzw 现场水质测试仪系的产品。从应用的角度来看 , 技术和产品基本达到了地下水 , 地表水等一个良好的准确度 , 易于使用 , 速度快 , 能够更准确地反映真实的现场水质状况 , 成品整体 , 以满足紧急检查和现场水质测试要求。因为这种方法特别的技术特点 , 在
水杨酸-次氯酸盐法 一、原理: 在碱性介质(pH =11.7)和亚硝基铁氰化钠(硝普钠)存在下,水中的氨、铵离子与水杨酸盐和次氯酸离子反应生成蓝色化合物,在697nm处用分光光度计测量吸光度。 显色反应: ①氨氮与次氯酸盐生成氯胺 ②氯胺与水杨酸反应(硝普钠催化),生成5-氨基水杨酸 ③5-氨基水杨酸生成醌亚胺(硝普钠催化) ④醌亚胺与水杨酸缩合成靛酚蓝(硝普钠催化) 二、测试流程:
三、注意事项: 1、水样保存 ①聚乙烯或者玻璃瓶中,加硫酸酸化至pH<2,在2-5℃可保存7天。 2、水样预处理 ①预蒸馏(水样存在浊度、色度或钙镁氯等离子时):通过弱碱性预蒸馏将水样氨氮分离收集在稀硫酸吸收液中。 3.显色条件 ①显色温度:常温下,1h后可以完全显色。 ②显色时间:显色60mins,在4h内显色稳定。 ③显色pH值:硝普钠-水杨酸体系中,以酒石酸钾钠做掩蔽剂时,显色反应的最佳pH值范围在11.54-11.97。 ④试剂添加顺序:氨氮与次氯酸盐生成的氯胺不稳定、易分解,所以一般最后加入次氯酸钠溶液。但若三种试剂迅速加入时,加入顺序对显色影响不大。
②水杨酸法测试浓度低: 测量下限低,可进行高倍数稀释,有利于减少干扰离子的影响。 ③难去除干扰物质: 含氨基、酰胺、胺等基团的有机物无法除去时,不宜使用这两种光度法,应该使用离子色谱法。 参考标准:HJ 536-2009 质氨氮的测定水杨酸分光光度法 汞-碘化钾溶液制备过程,出现碘化汞不溶时,极可能是因为碘化钾不纯造 成的,推荐使用国药化学试剂。 ②能力验证测试: 目前能力验证测试样品一般为无干扰质控样,无需考虑离子干扰,直接测试。多关注标线配制和显色条件。
1.范围 1.1 本方法规定了用纳氏试剂分光光度法测定水中的氨氮。 1.2 本方法适用于地下水、地表水、生活污水和工业废水中氨氮的测定。 1.3 当水样体积为50mL,使用20mm比色皿时,本方法检出限为L,测定下限为L, 测定上限为L(均以N计)。 2.参考标准 水质氨氮的测定纳氏试剂分光光度法HJ 535-2009 3.职责 检测技术人员按本作业指导书对水样中氨氮进行分析检测。 4.方法原理 以游离态的氨或铵离子等形式存在的氨氮与纳氏试剂反应生成淡红棕色络合物,该络合物的吸光度与氨氮含量成正比,于波长420nm处测量吸光度。 5.干扰及消除 5.1 水样中含有悬浮物、余氯、钙镁离子等金属离子、硫化物和有机物时会产生干扰, 含有此类物质时要作适当处理,以消除对测定的影响。 5.2 若样品中存在余氯,可加入适量的硫代硫酸钠溶液去除,用淀粉–碘化钾试纸检 验余氯是否除尽。在显色时加入适量的酒石酸钾钠溶液,可消除钙镁等金属离子的干扰。若水样浑浊或有颜色时可用预蒸馏法或絮凝沉淀法处理。 6.试剂 除非另有说明,分析时所用试剂均为符合国家标准的分析纯化学试剂,实验用水为按制备的水,使用经过检定的容量器皿和量器。 6.1 无氨水,在无氨环境中用纯水器法制备。用市售纯水器直接制备。或采用下述方 法之一制备: 6.1.1离子交换法:蒸馏水通过强酸性阳离子交换树脂(氢型)柱,将流出液收集 在带有磨口玻璃塞的玻璃瓶内。每升流出液加10g同样的树脂,以利于保存。 6.1.2蒸馏法:在1000mL的蒸馏水中,加硫酸(ρ=mL),在全玻璃蒸馏器中重蒸 馏,弃去前50mL馏出液,然后将约800mL馏出液收集在带有磨口玻璃塞的 玻璃瓶内。每升馏出液加10g强酸性阳离子交换树脂(氢型)。 6.2 盐酸,ρ(HCl)=mL。 6.3 硫酸,ρ(H2SO4)=mL。 6.4 无水乙醇
水样氨氮测定(纳氏试剂光度法) 1 方法原理 纳氏试剂光度法,检出范围:0.025-2mg/L 2 仪器试剂 仪器: 可见分光光度计 50mL具塞玻璃磨口比色管 试剂: 纳氏试剂:称取16gNaOH,溶于50mL水中,充分冷却至室温。另称取7g 碘化钾和10g碘化汞(HgI2)溶于水,然后将此溶液在搅拌下徐徐注入氢氧化钠溶液中,用水稀释至100mL,贮于聚乙烯瓶中保存。(保质1年避光)酒石酸钾钠溶液:称取50酒石酸钾钠(KNaC4H4O6.4H2O)溶于100mL水中,加热煮沸以除去氨,放冷,定溶至100mL。 氨氮标准贮备液,C N=1000mg/L():称取3.819±0.004g氯化铵(NH4Cl,在105℃干燥1h),定容于1000mL水中。(保质半年) 氨氮标准使用液,C N=10mg/L:吸取1mL标准贮备液,定容至100mL,使用前配制。 3 步骤 水样预处理: 10%硫酸锌溶液:称取10g硫酸锌溶于水,稀释至100mL。 25%氢氧化钠溶液:称取巧25g氢氧化钠溶于水,稀释至100mL。贮于聚乙烯瓶中。 加适量的硫酸锌(100mL水样加1mL)于水样中,并加( 0.1-0.2ml )氢氧化钠使呈碱性(pH=10.5),生成氢氧化锌沉淀,再经过滤(或离心)除去颜色和浑浊等。 3.1 校准曲线的绘制 (1)分别吸取0、1、3、5、7、10mL标液于50mL比色管中,定容至标线。170
(2)加1mL酒石酸钾钠溶液。 (3)加1.5mL纳氏试剂,混匀。 (4)显色10分钟。 (5)在可见分光光度计测定。设置波长为:420nm。 3.2 样品测定 (1)分样。取25ml试样放入比色管,定容至50mL。 (2)同3.1中的(2)-(5)操作。 注:校准曲线系列:0、10、30、50、70、100(溶质),样品浓度值等于校准曲线查得值除以水样体积得到。 171
TGH-SN 氨氮在线自动监测仪 用 户 手 册 中绿环保科技股份有限公司
未经版权持有人的事先书面许可,不得以任何形式或者任何手段,无论是电子的还是书面的(其中包括影印),对本手册任何部分进行复制,也不得将其内容传达给第三方。 本公司保留对本用户手册的最终解释权,内容如有变更,恕不另行通知。
目录 第一章安全预防措施特别声明 (2) 1.1 总则 (2) 1.2 触电与灼伤预防 (2) 1.3 化学药品危险预防 (2) 1.4 标志 (2) 第二章技术规格 (3) 第三章系统概述 (4) 3.1 应用 (4) 3.2 系统描述 (4) 3.3 电气器件 (4) 3.4 基本原理 (4) 3.5 检测步骤 (5) 第四章拆箱和安装 (6) 4.1 拆箱 (6) 4.2 安装 (6) 4.2.1 监测子站房建设 (6) 4.2.2 监测子站房室内要求 (7) 4.2.3 安装 (7) 第五章试剂 (11) 5.1 零点标准溶液 (11) 5.2 氨氮标准溶液 (11) 5.3 试剂A溶液 (12) 5.4 试剂B溶液 (12) 5.5 试剂C溶液 (12) 5.6 试剂的使用与保存 (13) 5.7 稳定性和反应性 (13) 5.8 试剂的放置 (13) 5.9 废液处理 (13) 第六章仪器操作 (14) 6.1 仪器初始化 (14) 6.2 校准 (14) 6.3清洗 (14) 6.4 测量 (14) 6.5 触摸屏介绍 (15) 6.5.1 数据设置方法 (15) 6.5.2 指令输入与生效显示 (15) 6.5.3 屏幕操作 (15) 第七章故障维修 (26) 第八章日常维护 (28)