
原电池练习题
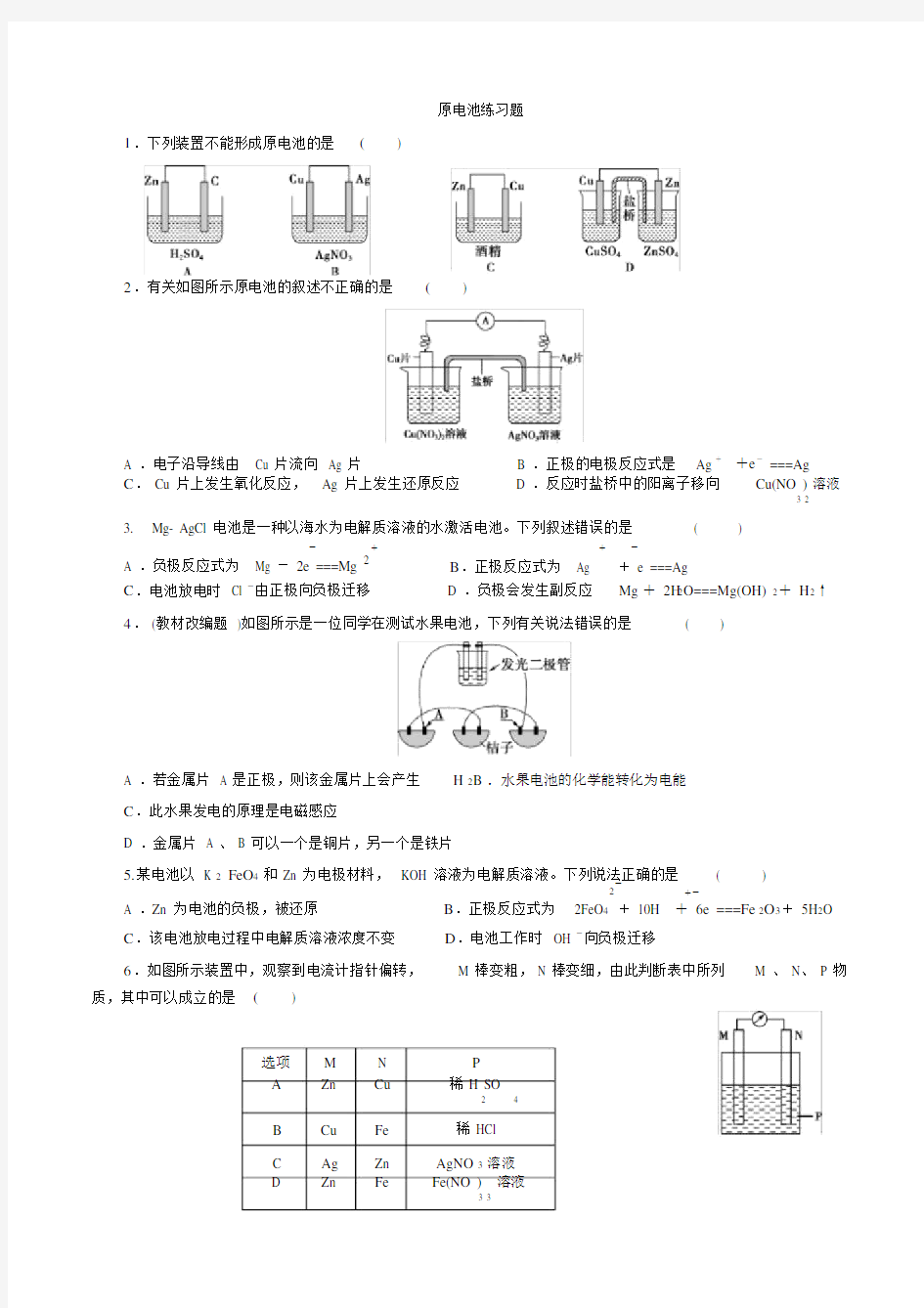
1.下列装置不能形成原电池的是()
2.有关如图所示原电池的叙述不正确的是()
A .电子沿导线由 Cu 片流向 Ag 片
B .正极的电极反应式是Ag ++e- ===Ag C. Cu 片上发生氧化反应,Ag 片上发生还原反应 D .反应时盐桥中的阳离子移向Cu(NO ) 溶液
3 2
3. Mg- AgCl 电池是一种以海水为电解质溶液的水激活电池。下列叙述错误的是( )
-++-
A .负极反应式为 Mg - 2e ===Mg 2 B.正极反应式为 Ag + e ===Ag
C.电池放电时 Cl -由正极向负极迁移 D .负极会发生副反应Mg + 2H2O===Mg(OH) 2+ H 2↑4. (教材改编题 )如图所示是一位同学在测试水果电池,下列有关说法错误的是( )
A .若金属片 A 是正极,则该金属片上会产生H 2
B .水果电池的化学能转化为电能
C.此水果发电的原理是电磁感应
D .金属片 A 、 B 可以一个是铜片,另一个是铁片
5.某电池以 K 2 FeO4和 Zn 为电极材料, KOH 溶液为电解质溶液。下列说法正确的是( )
A .Zn 为电池的负极,被还原
2
-
+-
===Fe2O3+ 5H2O B.正极反应式为 2FeO4+ 10H + 6e
C.该电池放电过程中电解质溶液浓度不变D.电池工作时 OH -向负极迁移
6.如图所示装置中,观察到电流计指针偏转,M 棒变粗, N 棒变细,由此判断表中所列M 、 N、 P 物质,其中可以成立的是()
选项M N P
A Zn Cu 稀 H SO
4
2
B Cu Fe 稀 HCl
C Ag Zn AgNO 3溶液
D Zn Fe Fe(NO ) 溶液
3 3
7.分析下图所示的四个原电池装置,其中结论正确的是 ( )
A .①②中 Mg 作负极,③④中 Fe 作负极
B .②中 Mg 作正极,电极反应式为
-
- + 3H 2↑
6H 2O + 6e ===6OH C .③中 Fe 作负极,电极反应式为
-
2
+
Fe -2e ===Fe D .④中 Cu 作正极,电极反应式为
2H +
+ 2e -
===H 2↑
8. (2017 ·泗洪模拟 )如图是某同学设计的原电池装置,下列叙述中正确的是 ()
A .电极Ⅰ上发生还原反应,作原电池的负极
B .电极Ⅱ的电极反应式为 Cu 2 + -
+ 2e ===Cu C .该原电池的总反应为
2Fe 3+
+ Cu===Cu 2+
+ 2Fe 2
+
D .盐桥中装有含氯化钾的琼脂,其作用是传递电子
9. .M 、 N 、P 、E 四种金属,已知:① M + N 2+
===N + M 2+
;② M 、P 用导线连接放入 NaHSO 4 溶液中,
M 表面有大量气泡逸出;③
N 、 E 用导线连接放入 E 的硫酸盐溶液中,电极反应为
+ - -
E 2 + 2e ===E , N - 2e
===N 2+
。则这四种金属的还原性由强到弱的顺序是
()
A .P > M > N > E
B . E >N > M >P
C . P > N > M > E
D .
E > P > M > N
10.一定量的稀盐酸跟过量锌粉反应时,为了加快反应速率又不影响生成
H 2 的总量,可采取的措施是
()
A .加入少量稀 NaOH 溶液
B .加入少量 CH COONa 固体
3
C .加入少量 NH HSO
4
固体
D .加入少量 CuSO 溶液
4
4
11.(2017 ·封高三调研开 )如图,在盛有稀 H 2SO 4 的烧杯中放入用导线连接的电极 X 、Y ,外电路中电子
流向如图所示,关于该装置的下列说法正确的是
()
A .外电路的电流方向为
X →导线→ Y
B .若两电极分别为铁和碳棒,则 X 为碳棒, Y 为铁
C . X 极上发生的是还原反应,
Y 极上发生的是氧化反应
D .若两电极都是金属,则它们的活动性顺序为 X>Y
12.一次电池 —— 碱性锌锰干电池
负极材料:正极材料:,电极反应式:
,电极反应式:
;
;
总反应:。
13.二次电池 (以铅蓄电池为例)
1.放电时的反应
(1) 负极:(氧化反应 );
(2) 正极:(还原反应 );
(3) 总反应:。
2.充电时的反应
(1) 阴极:(还原反应 ) ;
(2) 阳极:(氧化反应 );
(3) 总反应:。
原电池练习答案
1.解析:选 C。 A 、B 、D 项都具有①活泼性不同的电极;②电解质溶液;③闭合回路;④自发进行的氧
化还原反应,均能构成原电池; C 项中酒精为非电解质,不能构成原电池。
-+
, Ag
2.解析:选 D。该装置是原电池装置,其中 Cu 为负极,失电子发生氧化反应: Cu- 2e ===Cu2
为正极,得电子发生还原反应: Ag ++ e- ===Ag 。原电池中,负极 (Cu) 失去的电子沿导线流向正极(Ag) ,盐桥中的阳离子移向正极,即移向 AgNO 3溶液,综上所述, D 错误。
3.[解析 ] 该电池中Mg 作负极,失去电子发生氧化反应,生成 Mg 2+,A 项正确;正极反应为AgCl + e -===Ag+ Cl -, B 项错误;对原电池来说,阴离子由正极移向负极, C 项正确;在负极, Mg 会发生副反应
Mg + 2H 2O===Mg(OH) 2+H 2↑, D 项正确。
[答案 ] B
4.答案: C
5.解析:选 D 。A . 根据化合价升降判断,Zn 化合价只能升高,故为负极材料,被氧化,不正确; B . KOH 溶液为电解质溶液,则正极电极反应式为2FeO42--+8H2 3 -,错误; C. 该电池放电
+ 6e O===2Fe(OH) + 10OH
过程中电解质溶液浓度减小,错误; D. 电池工作时阴离子OH-向负极迁移,正确。
6.解析: 选 C 。在装置中电流计指针发生偏转
解的一极为负极,增重的一极为正极,所以
M
,说明该装置构成了原电池,根据正负极的判断方法,溶
棒为正极 , N 棒为负极 ,且电解质溶液能析出固体
,则只有
C 项正确。
7.解析: 选 B 。②中 Mg 不与 NaOH
溶液反应 ,而 Al 能和 NaOH 溶液反应失去电子 ,故 Al 是负极; ③
中 Fe 在浓硝酸中易钝化 ,Cu 和浓 HNO 3 反应失去电子作负极 ,A 、C 均错。② 中电池总反应为 2Al + 2NaOH
-
-
-
+ 2H 2O===2NaAlO 2+ 3H 2↑, 负极电极反应式为 2Al + 8OH - 6e ===2AlO 2 +4H 2O ,二者相减得到正极电
极反应式为 6H -
-
+ 3H 2↑, B 正确。 ④ 中 Cu 是正极 ,电极反应式为 -
2O + 6e ===6OH O 2+ 2H 2O + 4e ===4OH
-
,D 错。
8.解析: 选 C 。该原电池的总反应为
2Fe 3+
+Cu===Cu 2+
+ 2Fe 2+
。电极 Ⅰ 上发生还原反应 ,作原电池的
正极 ,反应式为 2Fe 3 +
+ 2e -
===2Fe 2+
,电极 Ⅱ为原电池负极 ,发生氧化反应 ,电极反应式为 Cu - 2e -
===Cu 2
+
。盐桥中装有含氯化钾的琼脂 ,其作用是传递离子。
9.解析: 选 A 。由 ① 知,金属活动性: M > N ; M 、P 用导线连接放入 NaHSO 4 溶液中 , M 表面有大量
气泡逸出 ,说明 M 作原电池的正极
,故金属活动性: P > M ;N 、 E 构成的原电池中 , N 作负极 ,故金属活
动性: N > E 。
10.解析: 选 D 。 A 中加入 NaOH 溶液 ,消耗盐酸 ,反应速率减慢 ,且氢气的生成量会减少 ,错误; B 中加入 CH 3COO -
会结合 H +
,生成醋酸 ,减慢反应速率 ,错误; C 中加入 NH 4HSO 4 固体,增加了 H +
的量 ,
生成的氢气会增多 ,错误; D 中加入少量 CuSO 4 溶液, Zn 置换出少量 Cu 附着在锌表面 ,形成原电池可以 加快反应速率 ,并且没有影响氢气的生成量
,正确。
11.解析: 选 D 。外电路的电子流向为 X → 导线 → Y ,电流方向与其相反; X 极失电子 ,作负极 ,发生的 是氧化反应 , Y 极发生的是还原反应;若两电极分别为铁和碳棒
,则 Y 为碳棒 , X 为铁。
12.负极材料: Zn ,电极反应式: Zn + 2OH -
- 2e -
===Zn(OH) 2; 正极材料: MnO 2,电极反应式: 2MnO 2+ 2H 2O +2e
-
===2MnOOH +2OH -
;
总反应: Zn +2MnO 2+ 2H 2O===2MnOOH + Zn(OH) 2。 13.
1. 放电时的反应
2
-
-
(1)负极: Pb(s)+ SO 4 (aq)- 2e ===PbSO 4(s)( 氧化反应 );
+ (aq)+ SO 2-
- (2)正极: PbO (s)+4H
4 (aq)+ 2e ===PbSO (s)+ 2H O(l)( 还原反应 );
2
4 2
(3)总反应: Pb(s)+PbO 2(s)+ 2H 2 SO 4(aq)===2PbSO 4(s)+ 2H 2O(l) 。 2. 充电时的反应
-
2
-
(1)阴极: PbSO 4(s)+ 2e ===Pb(s)+ SO 4 (aq)( 还原反应 );
(2)阳极: PbSO (s)+ 2H
-
+
2
-
2 O(l) - 2e ===PbO (s)+ 4H
(aq)+ SO (aq)(氧化反应 ) ;
4
2
4 (3)总反应: 2PbSO (s)+ 2H O(l)===Pb(s) + PbO (s)+2H SO (aq)。
4
2
2
2
4