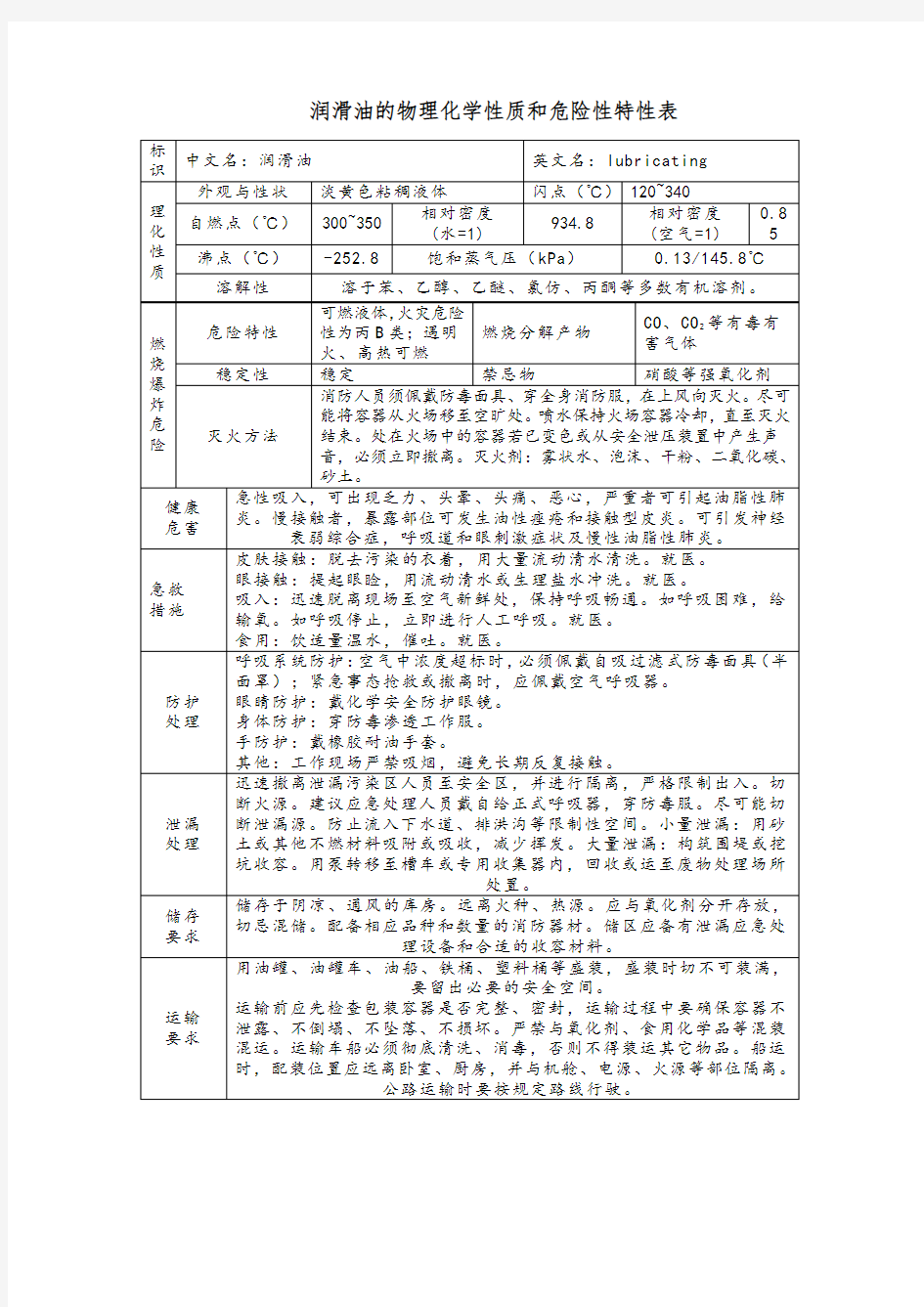
润滑油的物理化学性质和危险性特性表
水的基本物理化学性质 一. 水的物理性质(形态、冰点、沸点): 常温下(0~100℃),水可以出现固、液、气三相变化,利用水的相热转换能量是很方便的。 纯净的水是无色、无味、无臭的透明液体。水在1个大气压时(105Pa),温度 1)在0℃以下为固体,0℃为水的冰点。 2)从0℃-100℃之间为液体(通常情况下水呈液态)。 3)100℃以上为气体(气态水),100℃为水的沸点。 4)水是无色、无臭、无味液体,在浅薄时是清澈透明,深厚时呈蓝绿色。 5)在1atm时,水的凝固点(f.p.)为0℃,沸点(b.p.)为100℃。 6)水在0℃的凝固热为5.99 kJ/mole(或80 cal/g)。 7)水在100℃的汽化热为40.6 kJ/mole(或540 cal/g)。 8)由於水分子间具有氢键,故沸点高、莫耳汽化热大,蒸气压小。 9)沸点: (1)沸点:液体的饱和蒸气压等於液面上大气压之温度,此时液体各点均呈剧烈汽 化现象,且液气相可共存若液面上为1 atm(76 mmHg)时,则该沸点称为「正常沸点」,水的正常沸点为100℃。 (2)若液面的气压加大,则液体需更高的蒸气压才可沸腾;而更高的温度使得更高 的蒸气压,故液体的沸点会上升。液面上蒸气压愈大,液体的沸点会愈高。 (3)反之,若液面上气压变小,则液面的沸点将会下降。 10)水在4℃(精确值为3.98℃)时的体积最小、密度最大,D = 1g/mL。 11)三相点:指在热力学里,可使一种物质三相(气相,液相,固相)共存的一个温度 和压力的数值。举例来说,水的三相点在0.01℃(273.16K)及611.73Pa 出现。 12)临界点(critical point):物理学中因为能量的不同而会有相的改变(例如:冰 →水→水蒸气),相的改变代表界的不同,故当一事物到达相变前一刻时我们称它临 界了,而临界时的值则称为临界点。之温度为临界温度,压力为临界压力。 13)临界温度:加压力使气体液化之最高温度称为临界温度。如水之临界温度为374℃, 若温度高於374℃,则不可能加压使水蒸气液化。 14)临界压力:在临界温度时,加压力使气体液化的最小压力称之。临界压力等於该液 体在临界温度之饱和蒸气压。 二. 水的比热: 把单位质量的水升高1℃所吸收的热量,叫做水的比热容,简称比热,水的比热为4.18xKJ/Kg.K。 在所有的液体中,水的比热容最大。因此水可作为优质的热交换介质,用于冷却、储热、传热等方面。 三. 水的汽化热: 在一定温度下单位质量的水完全变成同温度的气态水(水蒸气)所需的热量,叫做水的汽化热。 水从液态转变为气态的过程叫做汽化,水表面的汽化现象叫做蒸发,蒸发在任何温度下都能进行。 水的汽化热为2257KJ/Kg。一般地:使水在其沸点蒸发所需要的热量五倍于把等量水从1℃加热到100℃所需要的热量。
第二章天然气物理化学性质 学习目标 1、掌握天然气组成及其表示方法; 2、掌握天然气理想气体、实际气体气体状态方程及带压缩因子的状态方程; 3、熟悉天然气的物理性质、热力性质和燃烧性质。 学习指导 天然气的组成; 天然气的容积分数; 天然气的摩尔分数; 天然气组成表示法天然气分子量; 天然气平均密度; 天然气相对密度; 临界参数。 理想气体状态方程; 天然气气体状态方程实际气体状态方程; 带压缩因子的状态方程。 粘度 天然气物理性质 湿度 比热和比热容天然气的物理性质、热力性质和燃烧性质天然气热力性质焓 熵 导热系数 天然气燃烧热值 天然气的燃烧性质天然气的爆炸极限 华白数、燃烧势
内容 一、天然气组成表示法 1.天然气的组成 2.天然气的容积分数:i i i i y n n V V y === ' 天然气的摩尔分数:∑==i i i i n n n n y 3.天然气分子量:∑= i i M y M 4.天然气平均密度:i i i i V y M y ∑∑= /ρ 天然气相对密度:a ρρ/=? 5. 临界参数:∑= ci i c T y T ; ∑= ci i c P y P ; ∑=ci i c y ρρ 适用:各组分的临界压力和临界比容接近(<20%),且任意二组分的临界温度满足0.5< Tci/Tcj <2的条件,否则,可能有很大计算误差。 对比参数:c r P P P /=; c r T T T /=; c r ρρρ/=;或 c r ννν/= 二、天然气气体状态方程 1.理想气体状态方程:pV=mRT=nR M T 2.实际气体状态方程: (1)范德瓦耳方程:(P+a/V 2 )(V-b )=RT (2)R-K 方程:) (5.0b V V T a b V RT P +--= (3)SRK 方程:) (b V V a b V RT P +--= (4)PR 状态方程:) ()(b V b b V V a b V RT P -++--= (5)L-E-E 方程是一个多参数状态方程:()) )((b V b V V bc b V V a b V RT p +-++--= (6)BWRS 方程:3 24 0302000)()(ρρρT d a bRT T E T D T C A RT B RT P --+-+- -+=
甲醇 MSDS 基本信息 中文名:甲醇;木酒精木精;木醇英文名: Methyl alcohol;Methanol 分子式:CH4O 分子量: 32.04 CAS号: 67-56-1 外观与性状:无色澄清液体,有刺激性气味。 主要用途:主要用于制甲醛、香精、染料、医药、火药、防冻剂等。 物理化学性质 熔点: -97.8 沸点: 64.8 相对密度(水=1):0.79 相对密度(空气=1): 1.11 饱和蒸汽压(kPa):13.33/21.2℃ 溶解性:溶于水,可混溶于醇、醚等多数有机溶剂临界温度(℃):240 临界压力(MPa):7.95 燃烧热(kj/mol):727.0 甲醇由甲基和羟基组成的,具有醇所具有的化学性质。[3] 甲醇可以在纯氧中剧烈燃烧,生成水蒸气(I)和二氧化碳(IV)。另外,甲醇也和氟气会产生猛烈的反应。[4] 与水、乙醇、乙醚、苯、酮、卤代烃和许多其他有机溶剂相混溶,遇热、明火或氧化剂易 燃烧。燃烧反应式为: CH3OH + O2 → CO2 + H2O 具有饱和一元醇的通性,由于只有一个碳原子,因此有其特有的反应。例如:① 与氯化钙形成结晶状物质CaCl2·4CH3OH,与氧化钡形成B aO·2CH3OH的分子化合物并溶解于甲醇中;类似的化合物有MgCl2·6CH3OH、CuSO4·2CH3OH、CH3OK·CH3OH、AlCl3·4CH3OH、AlCl3·6CH3OH、AlCl3·10CH3OH等;② 与其他醇不同,由于-CH2OH基与氢结合,氧化时生成的甲酸进一步氧化为CO2;③ 甲醇与氯、溴不易发生反应,但易与其水溶液作用,最初生成二氯甲醚(CH2Cl)2O,因水的作用转变成HCHO与HCl;④ 与碱、石灰一起加热,产生氢气并生成甲酸钠;CH3OH+NaOH→HCOONa+2H2;⑤与锌粉一起蒸馏,发生分解,生成 CO和H2O。[2] 产品用途 1.基本有机原料之一。主要用于制造甲醛、醋酸、氯甲烷、甲胺和硫酸二甲酯等多种 有机产品。也是农药(杀虫剂、杀螨剂)、医药(磺胺类、合霉素等)的原料,合成对苯二甲酸二甲酯、甲基丙烯酸甲酯和丙烯酸甲酯的原料之一。还是重要的溶剂,亦
海底天然气物理化学性质 第一节海底天然气组成表示法 一、海底天然气组成 海底天然气是由多种可燃和不可燃的气体组成的混合气体。以低分子饱和烃类气体为主,并含有少量非烃类气体。在烃类气体中,甲烷(CH 4 )占绝大部分, 乙烷(C 2H 6 )、丙烷(C 3 H 8 )、丁烷(C 4 H 10 )和戊烷(C 5 H 12 )含量不多,庚烷以上 (C 5+)烷烃含量极少。另外,所含的少量非烃类气体一般有氮气(N 2 )、二氧化 碳(CO 2)、氢气(H 2 )、硫化氢(H 2 S)和水汽(H 2 O)以及微量的惰性气体。 由于海底天然气是多种气态组分不同比例的混合物,所以也像石油那样,其物理性质变化很大,它的主要物理性质见下表。 海底天然气中主要成分的物理化学性质 名称分 子 式 相 对 分 子 质 量 密度 /Kg ·m-3 临界 温度 /℃ 临 界 压 力 /MP a 粘度 /KP a ·S 自 燃 点 / ℃ 可燃性 限 /% 热值 /KJ·m-3 (15.6℃, 常压) 气体 常数 / Kg· m· (Kg ·K)-1 低 限 高 限 全 热 值 净 热 值 甲烷CH 4 16. 043 0.71 6 -82. 5 4.6 4 0.01( 气) 6 4 5 5. 15. 372 62 334 94 52.8 4 乙烷C 2 H 6 30. 070 1.34 2 32.2 7 4.8 8 0.009( 气) 5 3 3. 2 12. 45 661 51 602 89 28.2 丙烷C 3 H 8 44. 097 1.96 7 96.8 1 4.2 6 0.125( 10℃) 5 1 2. 37 9.5 937 84 862 48 19.2 3 正丁烷n-C 4 H 10 58. 12 2.59 3 152. 01 3.8 0.174 4 9 1. 86 8.4 1 121 417 108 438 14.5 9 异丁烷i-C 4 H 10 58. 12 2.59 3 134. 98 3.6 5 0.194 1. 8 8.4 4 121 417 108 438 14.5 9 氨He 4.0 03 0.19 7 -267 .9 0.2 3 0.0184 211. 79 氮N 228. 02 1.25 -147 .13 3.3 9 0.017 30.2 6
乙醇32061(3.2类易燃液体) 包装:小开口钢瓶;小开口铝桶;安瓿瓶外普通木箱;螺纹口玻璃瓶、铁盖压口玻璃瓶、塑料瓶或金属桶(罐)外普通木箱。 物质名称:乙醇、酒精英文名称:ethyl alcohol/ ethanol CAS NO: 64-17-5 分子式:C2H6O 分子量:46.07危险货物编号:32061 沸点(℃)78.3比重 (水= 1) 0.79 饱和蒸气压(kPa) 5.33(19℃)熔点 (℃) -114.1 蒸气密度(空气=1)1.59溶解性 与水混溶,可混溶于 醚、氯仿、甘油等多 数有机溶剂。 外观与气味无色液体,有酒香。火灾爆炸危险数据 闪点(℃)12爆炸极限 爆炸上限%(V/V):19.0 爆炸下 限%(V/V):3.3 灭火剂抗溶性泡沫、干粉、二氧化碳、砂土。 灭火方法尽可能将容器从火场移至空旷处。喷水保持火场容器冷却,直至灭火结束。 危险特性本品易燃,具刺激性。其蒸气与空气可形成爆炸性混合物,遇明火、高热能引起燃烧爆炸。与氧化剂接触发生化学反应或引起燃烧。在火场中,受热的容器有爆炸危险。其蒸气比空气重,能在较低处扩散到相当远的地方,遇火源会着火回燃。 反应活性数据 稳定性稳定聚合危险性:不聚合强氧化剂、酸类、酸燃烧(分
禁忌物酐、碱金属、胺类。解)产物二氧化碳健康危害数据 侵入途径吸入√皮 肤 √ 急性中毒LD50:7060 mg/kg(兔经口); 7430 mg/kg(兔经皮) LC50:37620 mg/m3,10小 时(大鼠吸入) 职业接触限值未制定标准 健康危害 本品为中枢神经系统抑制剂。首先引起兴奋,随后抑制。急性中毒:急性中毒多发生于口服。一般可分为兴奋、催眠、麻醉、窒息四阶段。患者进入第三或第四阶段,出现意识丧失、瞳孔扩大、呼吸不规律、休克、心力循环衰竭及呼吸停止。慢性影响:在生产中长期接触高浓度本品可引起鼻、眼、粘膜刺激症状,以及头痛、头晕、疲乏、易激动、震颤、恶心等。皮肤长期接触可引起干燥、脱屑、皲裂和皮炎。 急救措施 皮肤接触:脱去污染的衣着,用流动清水冲洗。眼睛接触:提起眼睑,用流动清水或生理盐水冲洗。就医。吸入:迅速脱离现场至空气新鲜处。就医。食入:饮足量温水,催吐。就医。 储运注意事项 存储于阴凉、通风的库房。远离火种、热源。库温不宜超过30℃。保持容器密封。应与氧化剂、酸类、碱金属、胺类等分开存放,切忌混储。采用防爆型照明、通风设施。禁止使用易产生火花的机械设备和工具。储区应备有泄漏应急处理设备和合适的收容材料。运输时运输车辆应配备相应品种和数量的消防器材及泄漏应急处理设备。夏季最好早晚运输。运输时所用的槽(罐)车应有接地链,槽内可设孔隔板以减少震荡产生静电。严禁与氧化剂、酸类、碱金属、胺类、食用化学品等混装混运。运输途中应防曝晒、雨淋,防高温。装运该物品的车辆排气管必须配备阻火装置,禁止使用易产生火花的机械设备和工具装卸。公路运输时要按规定路线行驶,勿在居民区和人口稠密区停留。 泄漏应急处理
水的物理、化学及物理化学处理方法简介 (一)物理处理方法 利用固体颗粒和悬浮物的物理性质将其从水中分离去除的方法称为物理处理方法。物理处理法的最大优点是简单易行,效果良好,费用较低。 物理处理法的主要处理对象是水中的漂浮物、悬浮物以及颗粒物质。 常用的物理处理法有格栅与筛网、沉淀、气浮等。 (1)格栅与筛网 格栅是用于去除水中较大的漂浮物和悬浮物,以保证后续处理设备正常工作的一种装置。格栅通常有一组或多组平行金属栅条制成的框架组成,倾斜或直立地设立在进水渠道中,以拦截粗大的悬浮物。 筛网用以截阻、去除水中的更细小的悬浮物。筛网一般用薄铁皮钻孔制成,或用金属丝编制而成,孔眼直径为0.5~1.0mm。 在河水的取水工程中,格栅和筛网常设于取水口,用以拦截河水中的大块漂浮物和杂草。在污水处理厂,格栅和筛网常设于最前部的污水泵之前,以拦截大块漂浮物以及较小物体,以保护水泵及管道不受阻塞。 (2)沉淀 沉淀是使水中悬浮物质(主要是可沉固体)在重力作用下下沉,从而与水分离,使水质得到澄清。这种方法简单易行,分离效果良好,是水处理的重要工艺,在每一种水处理过程中几乎都不可缺少。按照水中悬浮颗粒的浓度、性质及其絮凝性能的不同,沉淀现象可分为:自由沉淀、絮凝沉淀、拥挤沉淀、压缩沉淀。 水中颗粒杂质的沉淀,是在专门的沉淀池中进行的。按照沉淀池内水流方向的不同,沉淀池可分为平流式、竖流式、辐流式和斜流式四种。 (3)气浮 气浮法亦称浮选,它是从液体中除去低密度固体物质或液体颗粒的一种方法。通过空气鼓入水中产生的微小气泡与水中的悬浮物黏附在一起,靠气泡的浮力一起上浮到水面而实现固液或液液分离的操作。其处理对象是:靠自然沉降或上浮难以去除的乳化油或相对密度接近于1的微小悬浮颗粒。 浮选过程包括微小气泡的产生、微小气泡与固体或液体颗粒的粘附以及上浮分离等步骤。实现浮选分离必须满足两个条件:一是必须向水中提供足够数量的
编号:SY-AQ-09384 ( 安全管理) 单位:_____________________ 审批:_____________________ 日期:_____________________ WORD文档/ A4打印/ 可编辑 天然气及其组分的物理化学性 质 Physical and chemical properties of natural gas and its components
天然气及其组分的物理化学性质 导语:进行安全管理的目的是预防、消灭事故,防止或消除事故伤害,保护劳动者的安全与健康。在安全管理的四项主要内容中,虽然都是为了达到安全管理的目的,但是对生产因素状态的控制,与安全管理目的关系更直接,显得更为突出。 天然气的主要成分为甲烷,此外还含有乙烷、丙烷、丁烷等烃 类气体,氮、CO2 、H2 S及微量氢、氦、氩等非烃类气体,一般气藏天然气的甲烷含量 在90%以上。油田伴生气中甲烷含量占65%~80%,此外还含有相 当数量的乙烷、丙烷、丁烷等烃类气体。 一、天然气主要组分的物理化学性质 天然气主要组分的物理化学性质见表1-3-1。 表1-3-1天然气主要组分在标准状态下的物理化学性质 名称 分子式 相对分子质量 摩尔体积Vm
/(m3 /kmol) 气体常数R(J/kg·K) 密度ρ/(kg/m3 ) 临界温度Tc /K 临界压力Pc /MPa 高热值Hh /(MJ/m3 ) 高热值Hh /(MJ/kg) 低热值H1 /(MJ/m3
) 甲烷CH4 16.043 22.362 518.75 0.7174 190.58 4.544 39.842 35.906 乙烷 C2 H6 30.07 22.187
初中化学常见物质的物理化学性质 一、初中化学常见物质的颜色 (一)、固体的颜色 1、红色固体:铜,氧化铁 2、绿色固体:碱式碳酸铜 3、蓝色固体:氢氧化铜,硫酸铜晶体 4、紫黑色固体:高锰酸钾 5、淡黄色固体:硫磺 6、银白色固体:银,铁,镁,铝,汞等金属 7、黑色固体:铁粉,木炭,氧化铜,二氧化锰,四氧化三铁,(碳黑,活性炭) 8、红褐色固体:氢氧化铁 9、白色固体:氯化钠,碳酸钠,氢氧化钠,氢氧化钙,碳酸钙,氧化钙,硫酸铜,五氧化二磷,氧 化镁 (二)、液体的颜色 10、蓝色溶液:硫酸铜溶液,氯化铜溶液,硝酸铜溶液 11、浅绿色溶液:硫酸亚铁溶液,氯化亚铁溶液,硝酸亚铁溶液 12、黄色溶液:硫酸铁溶液,氯化铁溶液,硝酸铁溶液 13、紫红色溶液:高锰酸钾溶液 (三)、气体的颜色 14、红棕色气体:二氧化氮15、黄绿色气体:氯气 16、无色气体:氧气,氮气,氢气,二氧化碳,一氧化碳,二氧化硫,氯化氢气体等大多数气体。 二、初中化学溶液的酸碱性 1、显酸性的溶液:酸溶液和某些盐溶液(硫酸氢钠、硫酸氢钾等) 2、显碱性的溶液:碱溶液和某些盐溶液(碳酸钠、碳酸氢钠等) 3、显中性的溶液:水和大多数的盐溶液 三、化学敞口置于空气中质量改变的 (一)质量增加的 1、由于吸水而增加的:氢氧化钠固体,氯化钙,氯化镁,浓硫酸; 2、由于跟水反应而增加的:氧化钙、氧化钡、氧化钾、氧化钠,硫酸铜; 3、由于跟二氧化碳反应而增加的:氢氧化钠,氢氧化钾,氢氧化钡,氢氧化钙; (二)质量减少的1、由于挥发而减少的:浓盐酸,浓硝酸,酒精,汽油,浓氨水 4、由于风化而减少的:碳酸钠晶体。.1.
四、初中化学物质的检验(一)、气体的检验 1、氢气:在玻璃尖嘴点燃气体,罩一干冷小烧杯,观察杯壁是否有水滴,往烧杯中倒入澄清的石灰水,若不变浑浊,则是氢气. 2、氨气:湿润的紫红色石蕊试纸,若试纸变蓝,则是氨气. 3、水蒸气:通过无水硫酸铜,若白色固体变蓝,则含水蒸气. (二)、离子的检验. 1、氢离子:滴加紫色石蕊试液/加入锌粒 2、氢氧根离子:酚酞试液/硫酸铜溶液 3、碳酸根离子:稀盐酸和澄清的石灰水 4、氯离子:硝酸银溶液和稀硝酸,若产生白色沉淀,则是氯离子 5、硫酸根离子:硝酸钡溶液和稀硝酸/先滴加稀盐酸再滴入氯化钡 6、铵根离子:氢氧化钠溶液并加热,把湿润的红色石蕊试纸放在试管口 7、铜离子:滴加氢氧化钠溶液,若产生蓝色沉淀则是铜离子 8、铁离子:滴加氢氧化钠溶液,若产生红褐色沉淀则是铁离子 (三)、相关例题 1、如何检验NaOH是否变质:滴加稀盐酸,若产生气泡则变质 2、检验NaOH中是否含有NaCl:先滴加足量稀硝酸,再滴加AgNO3溶液,若产生白色沉淀,则含有NaCl。 3、检验三瓶试液分别是稀HNO3,稀HCl,稀H2SO4? 向三只试管中分别滴加Ba(NO3)2 溶液,若产生白色沉淀,则是稀H2SO4;再分别滴加AgNO3溶液,若产生白色沉淀则是稀HCl,剩下的是稀HNO3 4、淀粉:加入碘溶液,若变蓝则含淀粉。 5、葡萄糖:加入新制的氢氧化铜,若生成砖红色的氧化亚铜沉淀,就含葡萄糖。。 6、铁的三种氧化物:氧化亚铁,三氧化二铁,四氧化三铁。。 new:实验室制取CO2不能用的三种物质:硝酸,浓硫酸,碳酸钠。 34、三种遇水放热的物质:浓硫酸,氢氧化钠,生石灰。。。 六、初中化学常见混合物的重要成分 1、水煤气:一氧化碳(CO)和氢气(H2) 七、初中化学常见物质俗称 1、硫酸铜晶体(CuSO4 .5H2O):蓝矾,胆矾 2、乙醇(C2H5OH):酒精 3、乙酸(CH3COOH):.2.
WORD 格式可编辑 专业知识 整理分享 乙醇的理化性质及危险特性表 英文名ethylalcohol 分子式:C 2H 6O 分子量:46.07标 识国标编号:32061CAS 号64-17-5 外观与性状无色液体,有酒香。 熔点℃-114.1相对密度(空气=1)1.59 理 沸点℃78.3临界温度℃243.1 化 相对密度(水=1)0.79临界压力MPa6.38 性 饱和蒸汽压℃燃烧热KPa5.33(19)Kj/mol1365.5 质 最小引燃能量无资料mJ 溶解性与水混溶,可混溶于醚、氯仿、甘油等多数有机溶剂。 毒 前苏联车间空气中有害物质的最高容许浓度1000mg/m3接触限值 性前苏联(1977)大气质量标准5.0mg/m3 与 侵入途径吸入、食入、经皮吸收。 危 害 健康危害本品为中枢神经系统抑制剂。首先引起兴奋,随后抑制。 燃烧性易燃闪点℃12燃 引燃温度℃363爆炸极限%上限%:19.0,下限%:3.3烧 爆危险特性其蒸气与空气可形成爆炸性混合物,遇明火、高热能引起燃烧爆炸。 炸燃烧分解产物一氧化碳,二氧化碳聚合危害无资料 危 稳定性稳定禁忌物强氧化剂、酸类、酸酐、碱金 险 属、胺类。 性 灭火方法用流动清水冲洗 储运 储存于阴凉、通风的库房。远离火种、热源。库温不宜超过30℃。保持容器密封。应与氧化剂、酸类、 注意碱金属、胺类等分开存放,切忌混储。采用防爆型照明、通风设施。禁止使用易产生火花的机械设备 事项和工具。 包装分类II 包装标志7包装 包装方法小开口钢桶,塑料瓶或金属桶外木桶 急救 措施 用流动清水冲洗;迅速脱离现场至空气新鲜处。饮足量温水,催吐。 泄露小量泄漏:用砂土或其它不燃材料吸附或吸收。也可以用大量水冲洗,洗水稀释后放入废水系统。大 应急量泄漏:构筑围堤或挖坑收容。用泡沫覆盖,降低蒸气灾害。用防爆泵转移至槽车或专用收集器内, 处理回收或运至废物处理场所处置。 工程 控制 生产过程密闭,全面通风。提供安全淋浴和洗 眼设备。 眼镜 防护 一般不需特殊防护。 呼吸 一般不需要特殊防护,高浓度接触时可佩戴过身体 系统穿防静电工作服。 滤式防毒面具(半面罩)。防护 防护 手防 戴一般作业防护手套。其它工作现场严禁吸烟。 护
超临界水的物理化学性质研究 超临界水的物理化学性质研究 摘要:只要超过了临界,就是在常温常压下水的物理化学性质都有极大变化,并且这些性质还会随着温度与压力的变化而变化,不再像临界内物理化学性质规律变化。同时超过临界后,在平常和非极性物质不互溶也会变成互溶,能够和空气、氧气等进行完全互溶。本文就是研究超临界情形下,水所具备的化学物理性质。 关键词:水超临界物理化学 如今超临界水因具备奇特性质,而被许多领域作为反应介质和溶剂来使用。同时在超临界的状态下,控制温度、压力以及操纵化学反应环境就能够加强反应物与产物溶解度,提升化学反应的转化率及反应速率,也不会产生二次污染。因此在这种情形下,探究超临界水所具备的物理化学性质具有现实意义 一、超临界水的特征 当所处环境的温度与压力到了一定值(374.30C、22.05MPa),高温造成水的密度膨胀与高压造成水蒸气被压缩的密度刚好相同时的水。对于超临界水而言,水的气体与液体没什么确保,两者完全交融到一起,形成一种新的处于高压高温状体流体。对于这种流体主要有如下几个方面的特征 1.具备较强氧化能力,有一些物质还能够进行自然并在水中产生火焰。 2.这种流体能够和油等各种物质混合,具备广泛溶解能力。 3.超临界水能够和氮气、氧气等各种气体按照任意比例进行混合,并产生单一相。 二、超临界水物理化学性质 流体在气体――液体相图上共存曲线终点即为临界点,其标志位固定不变的压力与温度点,在这个点上液相和气相间差别恰好消失,形成了一均相体系。水的临界压力为22.05MPa,临界温度为374.30C。一旦温度与压力超过了临界点,就视为了超临界水,形成了介于液体
LNG的物理化学特性 LLNG 的基本性质的基本性质 1.LNG的物理性质 主要成分:甲烷,临界温度:190.58K在常温下,不能通过加压将其液化,而是经过预处理,脱除重烃、硫化物、二氧化碳和水等杂质后,深冷到-162 O C,实现液化。 主要物理性质如表1-1所示:无色透明41.5~45.3 430~460 约-162°C 0.60~0.70 颜色高热值(MJ/m 3 )液体密度(g/l)(沸点下)沸点/°C (常压)气体相对密度表1-1 4 4 . LNG . LNG 的基本性质的基本性质2. 典型的LNG组成(摩尔分数)/% N 2 CH 4 C 2 H 6 C 3 H 8 I-C 4 H 10 N-C 4 H 10 C 5 H 12 摩尔质量/(kg/mol)泡点温度/ o C 密度/(kg/m 3 ) LNG 的基本性质的基本性质3. LNG的性质特点 温度低在大气压力下,LNG沸点都在-162°C左右。液态与气态密度比大1体积液化天然气的密度大约是1体积气态天然气的600倍,即1体积LNG大致转化为600体积的气体。 可燃性一般环境条件下,天然气和空气混合的云团中,天然气含量在5%~15%(体积)范围内可以引起着火,其最低可燃下限(LEL)为4% LNG 的基本性质
4. LNG的安全特性1)燃烧特性燃烧范围:5%~15%,即体积分数低于5%和高于15%都不会燃烧; 自燃温度:可燃气体与空气混合物,在没有火源的情况下,达到某一温度后,能够自动点燃着火的最低温度称为自燃温度。甲烷性质比较稳定,在大气压力条件下,纯甲烷的平均自燃温度为650°C。以甲烷为主要成分的天然气自燃温度较高,LNG的自燃温度随着组份的变化而变化。 燃烧速度:是火焰在空气-燃气的混合物中的传递速度。天然气的燃烧速度较低,其最高燃烧速度只有0.3m/s。 LNG 的基本性质的基本性质 低温特性隔热保冷:LNG系统的保冷隔热材料应满足导热系数低,密度低,吸湿率和吸水率小,抗冻性强,并在低温下不开裂,耐火性好,无气味,不易霉烂,对人体无害,机械强度高,经久耐用,价格低廉,方便施工等。 蒸发特性:LNG作为沸腾液体储存在绝热储罐中,外界任何传入的热量都会引起一定量液体蒸发成气体,这就是蒸发气(BOG)。标准状况下蒸发气密度是空气60%。当LNG压力降到沸点压力以下时,将有一定量的液体蒸发成为气体,同时液体温度也随之降低到其在该压力下的沸点,这就是LNG闪蒸。由于压力/温度变化引起的LNG蒸发产生的蒸发气处理是液化天然气储存运输中经常遇到的问题。 8 8 一一 . LNG . LNG 的基本性质的基本性质
甲醇水物理化学性质调研报告 一可燃性 甲醇是极易可燃性液体,遇明火、热源即可燃烧,火焰几乎呈无色(稍显极微弱蓝色)。 1.闪点:11℃; 2.甲醇自燃温度:436℃ 3.甲醇空气中甲醇蒸汽含量爆炸上限36.5%,爆炸下限6%; 4.甲醇及甲醇水灭火通常采用干粉或泡沫灭火器,禁止用水灭火。 图1燃烧中的甲醇水图2 干粉灭火器扑灭燃烧中的甲醇水 图3 燃烧中的甲醇图4 干粉灭火器扑灭燃烧中的甲醇 二挥发性 判断挥发性强弱的依据是物质的沸点,沸点越低,挥发性越弱,反之越强。 1.甲醇沸点:64.7℃,凝固点:-97.8℃。 2.甲醇和水不形成共沸物,对于不同浓度甲醇水的沸点不一样,54%的甲醇水沸点为77.7℃,凝固点:-74℃~-54.3℃。 3.汽油是由多种烷烃混合组成,没有沸点只有沸程,一般为30-205℃,也就是说在30℃时,汽油中最低组分就会发生气化,故在炎热的环境中,汽油就会产生较大的气味。 总结: 在30℃以下(即常温以下),甲醇水和汽油的挥发性都较弱,但由于汽
油最低组分沸点低于甲醇沸点,故汽油挥发性大于甲醇挥发性; 在30-77.7℃,随着温度升高,甲醇水和汽油的挥发性越来越大,达到77.7℃时,汽油中低于77.7℃的组分全部挥发,甲醇水可以全部挥发; 高于77.7℃,甲醇水几乎全部气化。 三毒理 甲醇的毒性对人体的神经系统和血液系统影响最大,它经消化道、呼吸道或皮肤摄入都会产生毒性反应,甲醇蒸气能损害人的呼吸道粘膜和视力。急性中毒症状有:头疼、恶心、胃痛、疲倦、视力模糊以至失明,继而呼吸困难,最终导致呼吸中枢麻痹而死亡。慢性中毒反应为:眩晕、昏睡、头痛、耳鸣、视力减退、消化障碍。甲醇摄入量超过4克就会出现中毒反应,误服一小杯超过10克就能造成双目失明,饮入量大造成死亡。致死量为30毫升以上,甲醇在体内不易排出, 会发生蓄积,在体内氧化生成甲醛和甲酸也都有毒性。在甲醇生产工厂,我国有关部门规定,空气中允许甲醇浓度为50mg/m3,在有甲醇气的现场工作须戴防毒面具、工厂废水要处理后才能排放,允许含量小于200mg/L的甲醇。 甲醇的中毒机理是,甲醇经人体代谢产生甲醛和甲酸(俗称蚁酸),然后对人体产生伤害。常见的症状是,先是产生喝醉的感觉,数小时后头痛,恶心,呕吐,以及视线模糊。严重者会失明,乃至丧命。失明的原因:甲醇的代谢产物甲酸累积在眼睛部位,破坏视觉神经细胞。脑神经也会受到破坏,而产生永久性损害。甲酸进入血液后,会使组织酸性越来越强,损害肾脏导致肾衰竭。 甲醇中毒,通常可以用乙醇解毒法。其原理是,甲醇本身无毒,而代谢产物有毒,因此可以通过抑制代谢的方法来解毒。甲醇和乙醇在人体的代谢都是同一种酶,而这种酶和乙醇更具亲和力。因此,甲醇中毒者,可以通过饮用烈性酒(酒精度通常在60度以上)的方式来缓解甲醇代谢,进而使之排出体外。而甲醇已经代谢产生的甲酸,可以通过服用小苏打(碳酸氢钠)的方式来中和。 四中毒症状及措施 身体危害:对中枢神经系统有麻醉作用;对视神经和视网膜有特殊选择作用,引起病变;可致代谢性酸中毒。 急性中毒:短时大量吸入出现轻度眼上呼吸道刺激症状(口服有胃肠道刺激症状);经一段时间潜伏期后出现头痛、头晕、乏力、眩晕、酒醉感、意识朦胧、
天然气及其组分的物理化学性 质(新编版) Safety management is an important part of enterprise production management. The object is the state management and control of all people, objects and environments in production. ( 安全管理 ) 单位:______________________ 姓名:______________________ 日期:______________________ 编号:AQ-SN-0616
天然气及其组分的物理化学性质(新编版) 天然气的主要成分为甲烷,此外还含有乙烷、丙烷、丁烷等烃类气体,氮、CO2 、H2 S及微量氢、氦、氩等非烃类气体,一般气藏天然气的甲烷含量在90%以上。油田伴生气中甲烷含量占65%~80%,此外还含有相当数量的乙烷、丙烷、丁烷等烃类气体。 一、天然气主要组分的物理化学性质 天然气主要组分的物理化学性质见表1-3-1。 表1-3-1天然气主要组分在标准状态下的物理化学性质 名称 分子式
相对分子质量 摩尔体积Vm /(m3 /kmol) 气体常数R(J/kg·K) 密度ρ/(kg/m3 ) 临界温度Tc /K 临界压力Pc /MPa 高热值Hh /(MJ/m3 ) 高热值Hh /(MJ/kg)
低热值H1 /(MJ/m3 ) 甲烷 CH4 16.043 22.362 518.75 0.7174 190.58 4.544 39.842 35.906 乙烷 C2 H6
常用溶剂特性毒性表 液态二氧化硫溶解胺、醚、醇苯酚、有机酸、芳香烃、溴、二硫化碳,多数饱和烃不溶剧毒 甲胺是多数有机物和无机物的优良溶剂,液态甲胺与水、醚、苯、丙酮、低级醇混溶,其盐酸盐易溶于水,不溶于醇、醚、酮、氯仿、乙酸乙酯中等毒性,易燃 二甲胺是有机物和无机物的优良溶剂,溶于水、低级醇、醚、低极性溶剂强烈刺激性 石油醚不溶于水,与丙酮、乙醚、乙酸乙酯、苯、氯仿及甲醇以上高级醇混溶与低级烷相似 乙醚微溶于水,易溶与盐酸.与醇、醚、石油醚、苯、氯仿等多数有机溶剂混溶麻醉性 戊烷与乙醇、乙醚等多数有机溶剂混溶低毒性 二氯甲烷与醇、醚、氯仿、苯、二硫化碳等有机溶剂混溶低毒,麻醉性强 二硫化碳微溶与水,与多种有机溶剂混溶麻醉性,强刺激性 溶剂石油脑与乙醇、丙酮、戊醇混溶较其他石油系溶剂大 丙酮与水、醇、醚、烃混溶低毒,类乙醇,但较大 1,1-二氯乙烷与醇、醚等大多数有机溶剂混溶低毒、局部刺激性
氯仿与乙醇、乙醚、石油醚、卤代烃、四氯化碳、二硫化碳等混溶中等毒性,强麻醉性 甲醇与水、乙醚、醇、酯、卤代烃、苯、酮混溶中等毒性,麻醉性,四氢呋喃优良溶剂,与水混溶,很好的溶解乙醇、乙醚、脂肪烃、芳香烃、氯化烃吸入微毒,经口低毒 己烷甲醇部分溶解,比乙醇高的醇、醚丙酮、氯仿混溶低毒。麻醉性,刺激性 三氟代乙酸与水,乙醇,乙醚,丙酮,苯,四氯化碳,己烷混溶,溶解多种脂肪族,芳香族化合物 1,1,1-三氯乙烷与丙酮、、甲醇、乙醚、苯、四氯化碳等有机溶剂混溶低毒类溶剂 四氯化碳与醇、醚、石油醚、石油脑、冰醋酸、二硫化碳、氯代烃混溶氯代甲烷中,毒性最强 乙酸乙酯与醇、醚、氯仿、丙酮、苯等大多数有机溶剂溶解,能溶解某些金属盐低毒,麻醉性 乙醇与水、乙醚、氯仿、酯、烃类衍生物等有机溶剂混溶微毒类,麻醉性 丁酮与丙酮相似,与醇、醚、苯等大多数有机溶剂混溶低毒,毒性强于丙酮 苯难溶于水,与甘油、乙二醇、乙醇、氯仿、乙醚、四氯化碳、二硫化碳、丙酮、甲苯、二甲苯、冰醋酸、脂肪烃等大多有机物混溶强烈毒性
石油气天然气的组成部分物理化学性质 天然气的组成 天然气是各种碳氢化合物为主的气体混合物。主要成分为甲烷、乙烷、丙烷、异丁烷、正丁烷、戊烷和微量的重碳氢化合物及少量非烃类的气体,如:氮、硫化氢、二氧化碳、氦气等。 天然气可分为气田气、油田气和凝析气田气三种。 气田气主要含甲烷,含量约为80%-98%;乙烷至丁烷烃类的含量一般不大,戊烷以上重烃以及非烃类气体不含或含量甚微。 油田气包括溶解气和气顶气,它的特征是乙烷和丁烷以上的烃类含量一般较高,其组成同分去凝析油以后的凝析气田气相类似。 从凝析气田采出的天然气,除含有大量的甲烷、乙烷外,还含有一定数量的丙烷、丁烷、戊烷及戊烷以上烃类,含有汽油和煤油成分。 天然气还可以分为干气(或贫气)和湿气(或富气)两类。一般来说,天然气中甲烷含量在90%以上时叫干气;甲烷含量低于90%,而乙烷、丙烷等烷烃的含量在10%以上的叫湿气。 若按天然气中含硫量的多少来划分,每立方米天然气中含硫量小于1克的称为净气;每立方米天然气中含硫量大于1克的称为酸气。 一、天然气的组成表示方法 天然气组成有三种表示方法:质量组成、体积组成和摩尔组成。每种组成均可用百分数或小数表示。 1、质量组成 用百分数表示时:gi= ×100 用小数表示时:gi= 2、体积组成 用百分输表示时:Vi= ×100 用小数表示时:Vi= 3、摩尔组成 用百分数表示时:yi= ×100 用小数表示时:yi= 二、表示天然气组成的三种方法可以互相转换 1、如果已知天然气的质量组成,要求换算为体积组成或摩尔组成,则 yi= = 式中Mi:组分i的分子质量 2、如果已知天然气的体积百分数,利用下面方法可换算为质量百分数gi gi= = 天然气的物理化学性质 1、天然气的压力:就是天然气中无规则运动的大量分子之间碰撞力的总和,它表示天然气能量的大小。 2、天然气的温度:表示天然气内分子热运动的剧烈程度。温度的高低取决于天然气内部的热运动状态。 3、天然气的临界温度。对每一种纯的气体都存在着一定的温度,高于此温度时,无论加多大压力也不可能使它由气体变为液体,这个温度称为临界温度,用符号T c表示。临界温度是该气体能以液体状态存在的最高温度。
天然气及其组分的物理化学性质(一) 天然气的主要成分为甲烷,此外还含有乙烷、丙烷、丁烷等烃类气体,氮、CO2、H2S及微量氢、氦、氩等非烃类气体,一般气藏天然气的甲烷含量在90%以上。油田伴生气中甲烷含量占65%~80%,此外还含有相当数量的乙烷、丙烷、丁烷等烃类气体。 一、天然气主要组分的物理化学性质天然气主要组分的物理化学性质见表1-3-1。表1-3-1天然气主要组分在标准状态下的物理化学性质 名称分子式相对分子质量摩尔体积Vm/(m3/kmol)气体常数R(J/kg·K)密度ρ/(kg/m3)临界温度Tc/K临界压力Pc/MPa高热值Hh/(MJ/m3)高热值Hh/(MJ/kg)低热值H1/(MJ/m3)甲烷CH416.04322.362518.750.7174190.584.54439.84235.906乙烷C2H630.0722.187276.641.3553305.424.81670.35155.36764.397丙烷C3H844.09721.936188.652.0102369.824.194101.26651.90893.240正丁烷n-C4H1058.12421.504143.1302.703425.183.747133.88650.376123.649异丁烷i-C4H1058.12421.598143.132.6912408.143.600133.04849.532122.853正戊烷C15H1272.15120.891115.273.453746.9653.325169.37749.438156.733氢H22.01622.427412.67O.089833.251.28012.74549.04210.786氧O231.99922.392259.971.4289154.334.971—141.926—氮N223.01322.403296.951.2507125.973.349——氦
乙醇1. 化学品及企业标识 化学品中文名称:乙醇75% 化学品英文名称:ethyl alcohol75% 主要用途:用于制酒工业、有机合成、消毒以及用作溶剂。 2. 危险性概述 2.1 危险性类别:第 3.2 类中闪点液体。 2.2 侵入途径:吸入、食入。 2.3 健康危害:本品为中枢神经系统抑制剂。首先引起兴奋,随后抑制。过量饮用会中毒。呼吸道刺激。 2.4 环境危害:对环境有害。 2.5 燃爆危险:易燃,其蒸气与空气混合,能形成爆炸性混合物。 3. 成分/组成信息 纯品■混合物□ 主要成分CAS RN 含量(%) 乙醇64-17-5 73.0-75.0 4. 急救措施 4.1 皮肤接触:脱去污染的衣着,用肥皂水和清水彻底冲洗皮肤。如有不适感,就医。 4.2 眼睛接触:提起眼睑,用流动清水或生理盐水冲洗。如有不适感,就医。4.3 吸入:迅速脱离现场至空气新鲜处。就医。 4.4 食入:饮足量温水,催吐。就医。 4.5 急性和迟发效应,主要症状:急性中毒主要见于过量饮酒者,职业中毒者少见。轻度中毒和中毒早期表现为兴奋、欣快、言语增多、颜面潮红或苍白、步态
不稳、轻度动作不协调、判断力障碍、语无伦次、眼球震颤,甚至昏睡。重度中毒可出现昏迷、呼吸表浅或呈潮式呼吸,并可因呼吸麻痹或循环衰竭而死亡。吸入高浓度乙醇蒸气可出现酒醉感、头昏、乏力、兴奋和轻度的眼、上呼吸道粘膜刺激等症状,但一般不引起严重中毒。 慢性中毒长期酗酒者可见面部毛细血管扩张,皮肤营养障碍,慢性胃炎,胃溃疡,肝炎,肝硬化,肝功能衰竭,心肌损害,肌病,多发性神经病等。皮肤长期反复接触乙醇液体,可引起局部干燥、脱屑、皲裂和皮炎。 5. 消防措施 5.1 危险特性:易燃,其蒸气与空气可形成爆炸性混合物,遇明火、高热能引起燃烧爆炸。与氧化剂接触发生化学反应或引起燃烧。在火场中,受热的容器有爆炸危险。蒸气比空气重,沿地面扩散并易积存于低洼处,遇火源会着火回燃。 5.2 有害燃烧产物:一氧化碳。 5.3 灭火方法:用抗溶性泡沫、干粉、二氧化碳、砂土灭火。 5.4 灭火注意事项及措施:消防人员须佩戴防毒面具、穿全身消防服,在上风向灭火。尽可能将容器从火场移至空旷处。喷水保持火场容器冷却,直至灭火结束。 6. 泄漏应急措施 应急处理:消除所有点火源。根据液体流动和蒸气扩散的影响区域划定警戒区,无关人员从侧风、上风向撤离至安全区。建议应急处理人员戴正压自给式呼吸器,穿防静电服。作业时使用的所有设备应接地。禁止接触或跨越泄漏物。尽可能切断泄漏源。防止泄漏物进入水体、下水道、地下室或密闭性空间。小量泄漏:用砂土或其它不燃材料吸收。使用洁净的无火花工具收集吸收材料。大量泄漏:构筑围堤或挖坑收容。用抗溶性泡沫覆盖,减少蒸发。喷水雾能减少蒸发,但不能
分子式:Zn3(PO4)2·2H2O CAS号: 性质:无色斜方结晶或白色微晶粉末。表观密度0.8~1g/cm3。溶于无机酸、氨水、铵盐溶液。不溶于水、乙醇。加热到100℃时失去2个结晶水而成无水物。有潮解性。腐蚀性。由磷酸与氧化锌进行反应,在30℃以下加入晶种进行结晶,经过滤,热水洗涤,粉碎,干燥而制得。用作醇酸、酚醛、环氧树脂等涂料的基料。用于生产无毒防锈颜料和水溶性涂料。还用作氯化橡胶、合成高分子材料的阻燃剂。 分子式Zn3(PO4)2·2H2O CAS号7779-90-0 分子量422.08 性质无色斜方晶系结晶或白色微晶粉末。表观密度0.8~1g/cm3。溶于无机酸、氨水、铵盐溶液;不溶于乙醇;水中几乎不溶,其溶解度随温度上升而减小。加热到100℃时失去2个结晶水而成无水物。有潮解性、腐蚀性。 用途医药, 牙科用粘合剂,也用于防锈漆, 磷光体等。 磷酸锌 一、性状 无色斜方晶系结晶或白色微晶粉末。溶于无机酸,氨水和铵盐溶液;不溶于乙醇;水中几乎不溶,100℃时失去结晶水。有潮解性,腐蚀性。(具有优良的分散性)
磷酸锌(四水) 中文名: 磷酸锌(四水) 英文名: zinc phosphate;tribasic zinc phosphate CAS号: 分子式: 分子量: 密度: 3.03~3.04 熔点: 沸点: 闪点: 粘度: 蒸气压: 折射率: 毒性LD50: 性状: 白色粉末。 溶解情况: 不溶于水,易溶于酸和氨水中。 用途: 用于医药和供钢管的磷酸盐处理等。 制备或来源: 由硫酸锌和磷酸三钠作用而得。 备注: 在105℃以上失去结晶水而成无水物,无水物密度3.998,熔点900℃。 包装及贮运: 生产单位: 类别: 无机盐 - 无色斜方晶系结晶或白色微晶粉末。溶于无机酸、氨水、铵盐溶液;不溶于乙醇;水中几乎不溶,其溶解度随温度上升而减小 。 产品用途Application 用作醇酸、酚醛、环氧树脂等涂料的基料,用于生产无毒 防锈颜料和水溶性涂料,还用作氯化橡胶、高聚物阻燃剂 用作分析试剂用作醇酸、酚醛、环氧树脂等各类涂料的基 料,也用于生产无毒防锈颜料和水溶性涂料。还用于氯化 橡胶,合成高分子材料的阻燃剂。用作医药、牙科用粘合 剂,也用于防锈漆、磷光体等 生产方法Manufacturing_ method 氧化锌法将经稀释的15%磷酸溶液加入反应器中,在搅拌下缓慢加入浓度约20%的氧化锌浆液进行反应生成磷酸锌,温度保持在30℃以下,加入二水磷酸锌晶种,在Ph 值为3的条件下加热至80℃,经过滤、热水洗涤、粉碎、于90℃下干燥,制得二水磷酸锌成品。其