
5.4二组分系统的固?液平衡
5.4.1形成低共熔物的固相不互溶系统
当所考虑平衡不涉及气相而仅涉及固相和液相时,则体系常称为"凝聚相体系" 或"固液体系"0固体和液体的可压缩性甚小,一般除在高压下以外,压力对平衡性质的影响可忽略不计,故可将压力视为恒量。由相律:
/="= C-^+2-n r=2-d> + 2-l = 3-£Z>
因体系最少相数为①=1,故在恒压下二组分体系的最多自由度数 f * =2,仅需用两个独立变量就足以完整地描述体系的状态。由于常用变量为温度和组成,故在二组分固液体系中最常遇到的是T?x (温度?摩尔分数)或T?①(温度?质量分数)图。
二组分固?液体系涉及范围相当广泛,最常遇到的是合金体系、水盐体系、双盐体系和双有机物体系等。在本节中仅考虑液相中可以完全互溶的特殊情况°这类体系在液相中可以互溶,而在固相中溶解度可以有差别。故以其差异分为三类:
(1)固相完全不互溶体系;(2)固相部分互溶体系和(3)固相完全互溶体系。进一步分类可归纳如下:
F
『形成简单低共熔物休系
固相完全不互溶体棗形成化合物体系
彳相合熔点化合物怵系不相合熔点化合物俸系
EM体疾
「没有最1■嚴最高熔点型固相完全互熔体茶最瞬点型
最高熔点型
■1
固相部分互熔体
系,
一低共熔点型、
转熔点型
研究固液体系最常用实验方法为“热分析”法及“溶解度”法。本节先在“形成低共熔物的固相不互溶体系”中介绍这两种实验方法,然后再对各种类型相图作一简介。
(一)水盐体系相图与溶解度法
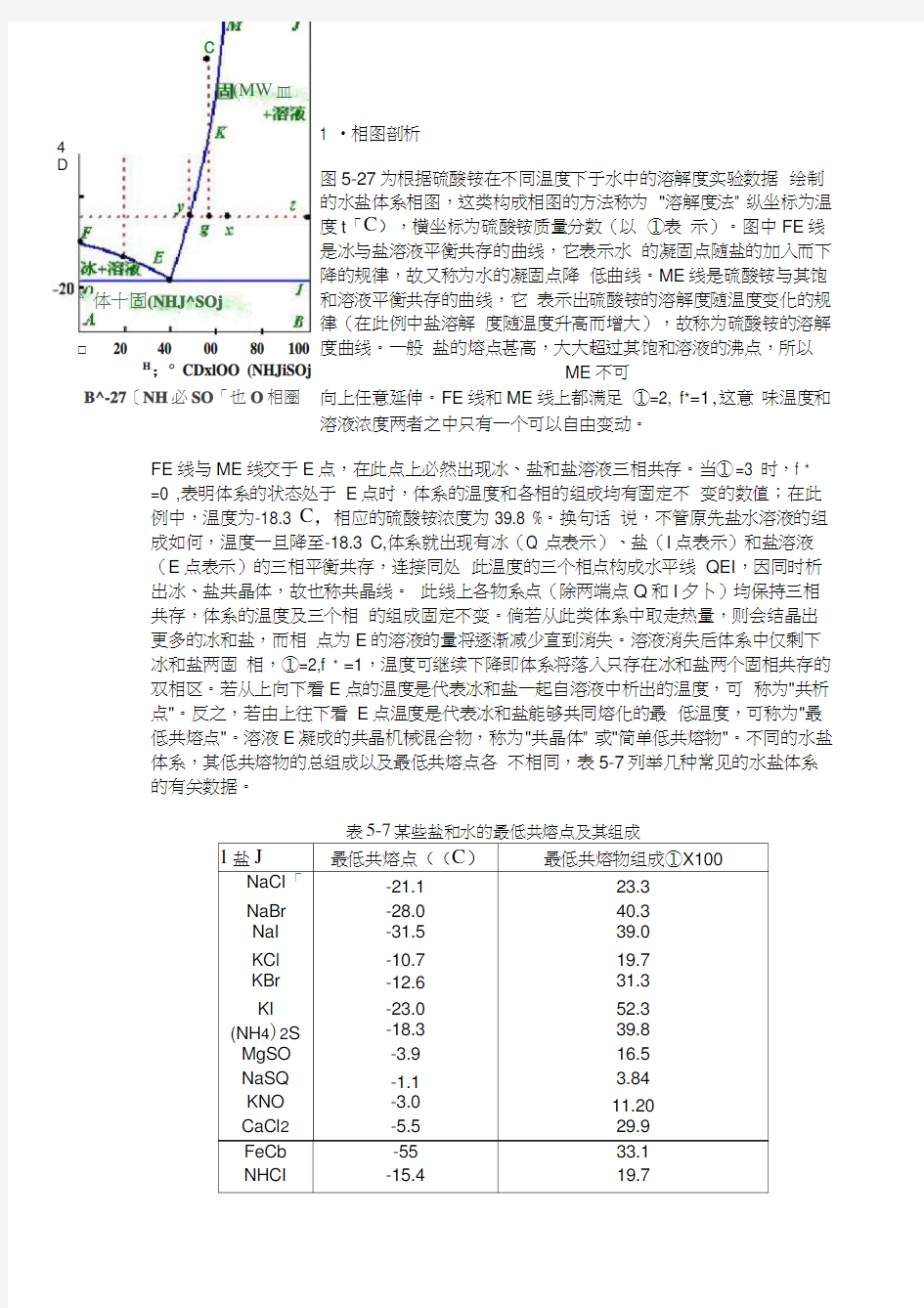
1 ?相图剖析 图5-27为根据硫酸铵在不同温度下于水中的溶解度实验数据 绘制
的水盐体系相图,这类构成相图的方法称为 "溶解度法" 纵坐标为温
度t 「C ),横坐标为硫酸铵质量分数(以 ①表 示)。图中FE 线
是冰与盐溶液平衡共存的曲线,它表示水 的凝固点随盐的加入而下
降的规律,故又称为水的凝固点降 低曲线。ME 线是硫酸铵与其饱
和溶液平衡共存的曲线,它 表示出硫酸铵的溶解度随温度变化的规律(在此例中盐溶解 度随温度升高而增大),故称为硫酸铵的溶解
度曲线。一般 盐的熔点甚高,大大超过其饱和溶液的沸点,所以
ME 不可
向上任意延伸。FE 线和ME 线上都满足 ①=2, f *=1,这意 味温度和
溶液浓度两者之中只有一个可以自由变动。
FE 线与ME 线交于E 点,在此点上必然出现冰、盐和盐溶液三相共存。当①=3 时,f * =0 ,表明体系的状态处于 E 点时,体系的温度和各相的组成均有固定不 变的数值;在此例中,温度为-18.3 C ,相应的硫酸铵浓度为39.8 %。换句话 说,不管原先盐水溶液的组成如何,温度一旦降至-18.3 C,体系就出现有冰(Q 点表示)、盐(I 点表示)和盐溶液(E 点表示)的三相平衡共存,连接同处 此温度的三个相点构成水平线 QEI ,因同时析出冰、盐共晶体,故也称共晶线。 此线上各物系点(除两端点Q 和I 夕卜)均保持三相共存,体系的温度及三个相 的组成固定不变。倘若从此类体系中取走热量,则会结晶出更多的冰和盐,而相 点为E 的溶液的量将逐渐减少直到消失。溶液消失后体系中仅剩下冰和盐两固 相,①=2,f * =1,温度可继续下降即体系将落入只存在冰和盐两个固相共存的 双相区。若从上向下看E 点的温度是代表冰和盐一起自溶液中析出的温度,可 称为"共析点"。反之,若由上往下看 E 点温度是代表冰和盐能够共同熔化的最 低温度,可称为"最低共熔点"。溶液E 凝成的共晶机械混合物,称为"共晶体" 或"简单低共熔物"。不同的水盐体系,其低共熔物的总组成以及最低共熔点各 不相同,表5-7列举几种常见的水盐体系的有关数据。 表某些盐和水的最低共熔点及其组成
1盐J
最低共熔点((C ) 最低共熔物组成①X100 NaCI 「
-21.1 23.3 NaBr
-28.0 40.3 NaI
-31.5 39.0 KCl
-10.7 19.7 KBr
-12.6 31.3 KI
-23.0 52.3 (NH 4)2S
-18.3 39.8 MgSO
-3.9 16.5 NaSQ
-1.1 3.84 KNO
-3.0 11.20 CaCl 2
-5.5 29.9 FeCb
NHCI -55 -15.4 33.1 19.7
c
(MW 皿
K 体十固(NHJ^SOj
4
D □ 20 40 00 80 100 H ;° CDxlOO (NHJiSOj B^-27〔NH 必SO 「也O 相圈
FE线和EM线的上方区域是均匀的液相区,因f*=3-①=3-1=2,故只有同时指定温度和盐溶液浓度两个变量才能确定一个物系点。FQE是冰?盐溶液两相共存
区。MEIJ是盐与饱和盐溶液两相共存区。在受制约的两相区内①=2,f*=1 ,只
能有一个自由度,即液相的组成随温度而变。而QABI为一不受制约的区域,温度及总组成可以任意变动。但因各相组成(纯态)固定,故常选温度为独立变量,即仍f =1 0
为确定两相区内某物系点的两相点,可通过该物系点作水平线(即结线)交于两端点,例如MEIJ区内的物系点g的两个相点就是y和z,y为浓度约44%的饱和盐溶液相,z为固相纯盐,两相质量比应遵守杠杆规则,即
sy
〔例5〕试计算200克含(NH4)SQ 60%的溶液冷至10C时(图5-27中的x 点),各相中各组分的质量?
〔解〕
按图5-27可知
爭=100 - 60 = 40
gy = 60 -44 =16
根据杠杆规则:
叫 X2 200—退40
叫xy 叫 16
从中解出固相(NH4)2SO质量为
三20Z16 *了[克
液相质量为:
w£ =200-57 1=142 9 克
???液相中(NH4)2SQ的质量:
142 9x44% -62 9克
液相中水的质量为:
1429-629?呂0克
2 ?相图的应用
水?盐体系的相图可用于盐的分离和提纯,帮助人们有效地选择用结晶法分离提纯盐类的最佳工艺条件,视具体情况可采取降温、蒸发浓缩或加热等各种不同的方法。例如,欲自80C, 20% (NH02SQ溶液中不能得到纯净的(NH4)2SQ 晶体应采取哪些操作步骤?
此物系点即图5-27中的P点,显然,若单纯降温,则进入FQE冰?液两相区,得到(NH?2SQ晶体。因为继续降温,冰不断析出,溶液的组成往FE线下滑,至E点(-18.3 C)出现三相共存。此时体系的温度及溶液的组成均恒定不变,直至全部液相变为固相为止,最终得到的只能是冰和固体(NH4)2SQ的混合物。由此可见,当溶液的组成落在ME线左边时,用单纯降温的方法是分离不出纯粹的盐。唯一可取的途径是先将此溶液蒸发浓缩,使物系点P沿水平方向移至c点,此时溶液中(NH4)2SQ含量约达50 %,冷却此溶液到K点(约
50C),溶液已成饱和。若再降低温度,无疑将析出(NH”2SQ固体,当温度降至g点(10C),体系中则有组成为y的溶液和纯盐共存。若降至-18.3 C则整个体系又成三相共存状态,析不出纯盐。故最佳方案是先行浓缩而后降温,但温度又不能降至冰?盐共析点,同时,也不必将温度降得太低,因为根据相图分析,10C时体系中固相所占的百分率与0C时所占的百分率相差无几,所以一般以冷却至10?20 r为宜。
根据上述原则,就可以利用相图确定(NH02SQ的纯化条件;如c点代表粗盐的热溶液组成,先滤去杂质,然后降温,由冷至50r即K点时, 便有纯(NH4)2SQ晶体析出,继续降温,结晶不断增加,至i0r时,饱和液浓度相当于y点。
至此,可将晶体与母液分开,并将母液重新加热到H点,再溶入粗(NH4)
2SQ,适当补充些水分,物系点又自H移到C, 然后又过滤、降温、结晶、分离、加热、溶入粗盐……如此使溶液的相点沿HCgyH路程循环多次,从而达到粗盐的提纯精制目的。循环次数多少,视母液中杂质浓缩程度对结晶纯度的影响而定。
水?盐相图具有低共熔点特征,可用来创造科学实验上的低温条件。例如,只要把冰和食盐(NaCl)混合,当有少许冰熔化成水,又有盐溶入,则三相共存,溶液的浓度将向最低共熔物的组成E逼近,同时体系自发地通过
冰的熔化耗热而降低温度直至达到最低共熔点。此后,只要冰和盐存在,且三相共存,则此体系就保持最低共熔点温度(-21.1 r)恒定不变。
(二)合金体系相图与"热分析"原理
现以二组分合金体系为例说明相图的另一种实验方法 "热分 析"的原
理。
对于象锑?铝,铋?镉等合金体系及两种化合物 (如KCI ? AgCI ,
GH ?CHB 3)体系,都可以组成形成低共熔物的固相 互不相溶体系,
以Sb ?Pb 体系为例,其相图如图5-28所示, ME NE 线分别为金属
Sb (即A )和金属Pb (即B )熔 体的凝固点曲线,由其斜率可知,各
自的熔点都随着第二种 组分的增加而降低。由式(4-155):
其中x 指某组分的摩尔数, △ fus H.指纯组分时的溶解焓变,T f*指纯组
分熔点,T f 为某组分当其摩尔分数为 x 时的熔点。
图中E 点是两条熔点曲线的交点,在此点上,固态 Sb 和Pb 以及溶液 三态共存,常称为金属Sb 和Pb 的"最低共熔点"。最低共熔点温度为 246C ,其质量分数为含Pb88%含Sb12%此溶液所析出之固体混合物 称为"共熔合金"(普遍情况下称为"最低共熔物")。显然,MQE 为金属溶 液和固体金属Sb 的两相平衡区。NEI 为溶液和固体金属Pb 的两相平衡 区。水平线QEI 则为纯固体Sb 、纯固体Pb 和组成E 的熔液平衡共存 的三相线,此线下面则是纯Sb 和纯Pb 的两相区。此类相图能提供制备 低熔点合金的方法;如在水银中加入铊(TI ),能使水银凝固点(-38.9 C) 降低,但通过相图可明断最低只能降到-59C,若想进一步降低,贝嚅采 用更多组分的体系。其他如保险丝,焊锡等低熔点合金均可参照这类相图 的实验数据配制。表5-8列出一些二组分简单最低共熔型相图体系中低共 熔物的熔点与组成(摩尔分数)。 组分A
A 的熔点
「C ) 组分B B 的熔点 (C) 低共熔物 低共熔点 (C) 低共熔物组成 (X B X 100)
CHB 3 7.5 GI4 5.5
-26 50 CHC 3 -63 GH 5NH -6
-71 24 苦味酸(NQ)C6H0卜
1 120 三硝基甲苯(TNT)
80 60 64 图亠眈Sb —Pb 体系 ⑷5 ^b xl0° 珂個)
Sb
631 Pb 327 246 88 Cd
321 Bi 271 144 55 KCI
790 AgCl 451 306 69 Si
1412 Al 657 578 89 Be ]1282 Si 1412 J 1090 32
热分析法研究固液平衡体系相图主要是依据体系发生相变时伴随着相变 潜热的吸收或放出,导致体系冷却速度的变化,来研究相变过程的规律。 由实验数据所绘制的温度(T )与时间(t )的曲线,称为“步冷曲线”,由步 冷曲线斜率的变化可提供相的产生、消失、和达成相平衡的信息。下面以 Sb ?Pb 合金体系为例,讨论绘制步冷曲线及由此确定相应的温度?组成 图的方法。
首先配好一定组成的混合物,如含Pb 量0.0 %、40%、60%、88%、95%、 100%等六个样品,加热使其全部熔解,然后让其缓慢地自行冷却,分别 记录每个样品温度随时间变化的数据作出如图 5-29(a )的六条步冷曲线。 其中样品①是纯Sb 属单组分。其步冷曲线可分析如下:由恒压下凝聚体
*
系相律表达式可得f =G ①+2-1=1-①+1=2-①。可见,温度若在凝固点 以上,则 ①=1, f *=1,体系温度可变化而不影响其单相特征,若仅有降 温可得出曲线上部的平滑段。当降温至 Sb 的凝固点(631C )将有固相 析出,固液两相平衡存在
①=2, f *=0,此时温度应维持不变,这就出现 如曲线上所示的平台线段。直到液体全部凝固,体系又变成单一固相,其 自由度f *=1,温度可以变化,冷却过程可用曲线下部的平滑段表示。同 理,曲线⑥为Pb 单组分步冷曲线,形状与曲线①类似,而差别在于其凝 固点较低(327C ),出现平台段较迟。
图Sb —系的图
曲线②为含Pb40%的二组分体系,C=2,由相律,高温时为熔融液相, 温度和组成在一定范围内均可变化而不影响其单相特征。当组成恒定时,
图気珂但)Sb —冷曲线 0)Sb Pb(J3
如曲线的上部平滑线。当温度降至H 点 Sb 达饱
和而析出固体Sb ,出现了固?液 温度仍可不断下
降,而平衡液相含Pb 量逐 增浓度,另固体析出所
放出凝固潜热,可部分抵偿环境吸走 的热,于是冷却速度较前缓慢,出现斜率较小的中间平滑线 Ha,步冷线上拐点(或转折点)H 的出现意味着新相的产生 若继
续降温至最低共熔点温度 T E ,则第二中金属Pb 亦已饱和,将析出 Sb 、Pb 共晶体,
此时三相共存,
温差,但体系通过固相析出量的自动调节维持温度为最低共熔点
不变。故出现平台段aa '(或称停点)。只有当熔液全部凝固后,体系 中仅剩下固体Sb 和Pb ,即包夹着先前析出Sb 晶体的共晶混合物,才 能继续降温,这一过程可用a'点以下的平滑线段表示。曲线③、⑤的形 状与②类似,不同的只是第一拐点温度高低以及平台线段的长短不同, 愈 接近低共熔点组成的同量样品,达低共熔点温度时剩余的熔液量愈多, 析 出低共熔物的时间也愈长,故③的平台线段比②要长,平台段延续的时间 常称为"停顿时间"o 自然,曲线⑤最终可得包夹着先前析出 Pb 晶体的共 晶混合物。
曲线④形状又独具一格。除上下平滑线外,仅在共熔点处出现平台段。而 且都比其它曲线的平台段来得长。其原因是样品组成刚好等于低共熔物的 组成,在降温至T E 时并非哪一种金属固体先行析出,而是两种同时析出, 成为共晶体即两纯组份微晶组成的机械混合物。此时,体系维持温度不 变。
完成不同组成的步冷曲线之后,将各拐点 M H 、K 、E 、F 、N 及同处水平 的三相点(或停点)a 、b 、E 、d ,平行地转移到温度?组成图上,连接M K 、E 即为Sb 的凝固点曲线,连接 N 、F 、E 即为Pb 的凝固点曲线,通 过a 、b 、E 、d 作水平三相线,至此Sb ?Pb 合金相图完成。
应该指出,前述低共熔物组成〔曲线④〕往往事先未能得知,需要由实验 确定;可利用平台段延续时间(停顿时间)与组成的关系,用内插法求得。 如图5-30所示,纵坐标代表停顿时间,横坐标代表 Pb 的质量分数,分 别由M H 、K 点连线及N 、F 点连线交于E 点(88% Pb )就是低共熔物 的组成。顶点 M N 分别代表纯组分Sb 和Pb ,它们不存在三相点,其 步冷曲线在此温度下没有停顿时间,不出现平台段。 05-30 f =3-①=3-3=0 ,表明体系与环境虽有 246C ) CT) tDpjjXlOO
二组分金属相图的绘制 一.实验目的 1.用热分析法(冷却曲线法)测绘Bi —Sn 二组分金属相图。 2.了解固液相图的特点,进一步学习和巩固相律等有关知识。 二.实验原理 表示多相平衡体系组成、温度、压力等变量之间关系的图形称为相图。 较为简单的二组分金属相图主要有三种:一种是液相完全互溶,凝固后,固相也能完全互溶成固熔体的系统,最典型的为Cu —Ni 系统;另一种是液相完全互溶而固相完全不互溶的系统,最典型的是Bi —Cd 系统;还有一种是液相完全互溶,而固相是部分互溶的系统,如本实验研究的Bi —Sn 系统。在低共熔温度下,Bi 在固相Sn 中最大溶解度为21%(质量百分数)。 图1冷却曲线 图2由冷却曲线绘制相图 热分析法(冷却曲线法)是绘制相图的基本方法之一。它是利用金属及合金在加热和冷却过程中发生相变时,潜热的释出或吸收及热容的突变,来得到金属或合金中相转变温度的方法。通常的做法是先将一定已知组成的金属或合金全部熔化,然后让其在一定的环境中自行冷却,画出冷却温度随时间变化的冷却曲线(见图 1)。当金属混合物加热熔化后再冷却时,开始阶段由于无相变发生,体系的温度随时间变化较大,冷却较快(ab 段)。若冷却过程中发生放热凝固,产生固相,将减小温度随时间的变化,使体系的冷却速度减慢(bc 段)。当融熔液继续冷却到某一点时,如c 点,由于此时液相的组成为低共熔物的组成。在最低共熔混 合物完全凝固以前体系温度保持不变,冷却曲线出现平台,(如图cd 段)。当融熔液完全凝固形成两种固态金属后,体系温度又继续下降(de 段)。 由此可知,对组成一定的二组分低共熔混合物系统,可以根据它的冷却曲线得出有固体析出的温度和低共熔点温度。根据一系列组成不同系统的冷却曲线的各转折点,即可画出二组分系统的相图(T - x 或T - w B 图)。不同组成熔液的冷却曲线对应的相图如图2所示。 图3可控升降温电炉前面板 1.电源开关 2.加热量调节旋钮 3、4.电压表 5.实验坩埚摆放区 6.控温传感器插孔 7.控温区电炉8.测试区电炉 9.冷风量调节
二组分简单共熔体系相图的绘制
————————————————————————————————作者: ————————————————————————————————日期:
实验七二组分简单共熔体系相图的绘制 ------Cd~Bi二组分金属相图的绘制1实验目的及要求: 1)应用步冷曲线的方法绘制Cd~Bi二组分体系的相图。 2)了解纯物质和混合物步冷曲线的形状有何不同,其相变点的温度应如何确定。 2 实验原理:… 用几何图形来表示多相平衡体系中有哪些相、各相的成分如何,不同相的相对量是多少,以及它们随浓度、温度、压力等变量变化的关系图,叫相图。 绘制相图的方法很多,其中之一叫热分析法。在定压下把体系从高温逐渐冷却,作温度对时间变化曲线,即步冷曲线。体系若有相变,必然伴随有热效应,即在其步冷曲线中会出现转折点。从步冷曲线有无转折点就可以知道有无相变。测定一系列组成不同样品的步冷曲线,从步冷曲线上找出各相应体系发生相变的温度,就可绘制出被测体系的相图,如图Ⅱ一6一l所示。 纯物质的步冷曲线如①⑤所示,从高温冷却,开始降温很快,口6线的斜率决定于体系的散热程度。冷到A的熔点时,固体A开始析出,体系出现两相平衡(溶液和固体A),此时温度维持不变,步冷曲线出现bc的水平段,直到其中液相全部消失,温度才下降。 混合物步冷曲线(如②、④)与纯物质的步冷曲线(如①、⑤)不同。如②起始温度下降很快(如a′b′段),冷却到b′点的温度时,开始有固体析出,这时体系呈两相,因为液相的成分不断改变,所以其平衡温度也不断改变。由于凝固热的不断放出,其温度下降较慢,曲线的斜率较小(b′c′段)。到了低共熔点温度后,体系出现三相,温度不再改变,步冷曲线又出现水平段c′d′,直到液相完全凝固后,温度又迅速下降。 曲线⑧表示其组成恰为最低共熔混合物的步冷曲线,其图形与纯物相似,但它的水平段是三相平衡。 用步冷曲线绘制相图是以横轴表示混合物的成分,在对应的纵轴标出开始出现相变(即步冷曲线上的转折点)的温度,把这些点连接起来即得相图。 3仪器与药品: 加热电炉1只,热电偶(铜一康铜)1根,不锈纲试管8只,控温测定装置1台,计算机1台,镉(化学纯),铋(化学纯)。 4 实验步骤: 1)配制不同质量百分数的铋、镉混合物各100g(含量分别为0%,15%,25%,40%,55%,75%,90%,100%),分别放在8个不锈纲试管中。 2)用控温测定装置装置,依次测纯镉、纯铋和含镉质量百分数为90%,75%,55%,40%,25%,15%样品的步冷曲线。将样品管放在加热电炉中加热,让样品熔化,同时将热电偶的热端(连玻璃套管)插入样品管中,待样品熔化后,停止加热。用热电偶玻璃套管轻轻搅
实验6 Sn-Bi二组分固液相图的绘制 【实验目的】 1.掌握热分析法绘制二组分固液相图的原理及方法; 2.了解纯物质与混合物步冷曲线的区别并掌握相变点温度的确 定方法; 3.了解简单二组分固液相图的特点; 4.掌握数字控温仪及KWL-80可控升温电炉的使用方法。 【实验原理】 凝聚系统受压力影响很小,因此通常讨论其定压下相平衡图。根据相律,定压下二组分系统f mix=2,最多有温度和组成两个独立变量,其相图为温度-组成图。 凝聚系统相图绘制:常用溶解度法和热分析法。 溶解度法:定温度下,直接测定固-液两相平衡时溶液的浓度,依据测得的温度和溶解度数据绘制成相图,适用于常温下易测定组成的系统,如水盐系统。 热分析法:绘制金属相图最常用的实验方法。原理:测定系统由高温均匀冷却过程中的时间、温度数据,绘制冷却曲线。根据冷却曲线可分析相态变化(若在均匀冷却过程无相变化,系统温度将随时间均匀下降。若系统在均匀冷却过程中有相变化,由于体系产生的相变热与自然冷却时体系放出的热量相抵消,步冷曲线就会出现转折或水平线段,转折点所对应的温度,即为该组成体系的相变温度。)。 简单二组分凝聚系统,其步冷曲线有三种类型。 图 6.1(a)为纯物质的步冷曲线。冷却过程中无相变发生时,系统温度随时间均匀降低,至b点开始有固体析出,建立单组分两相平衡,f=0,温度不变,步冷曲线出现水平段bc,直至液体全部凝固(c点),温度又继续均匀下降。水平段所对应的温度为纯物质凝固点。 图6.1(b)为二组分混合物的冷却曲线。冷却过程中无相变发生
时,系统温度随时间均匀降低,至b 点开始有一种固体析出,随着该固体析出,液相组成不断变化,凝固点逐渐降低,到c 点,两种固体同时析出,固液相组成不变,系统建立三相平衡,此时f=0,温度不随时间变化,步冷曲线出现水平段cd ,当液体全部凝固(d 点),温度又继续均匀下降。水平段cd 所对应的温度为二组分的低共熔点温度。 图6.1(c)为二组分低共熔混合物的步冷曲线。冷却过程中无相变发生时,系统温度随时间均匀降低,至b 点,两种固体按液相组成同时析出,系统建立三相平衡,f=0,温度不随时间变化,步冷曲线出现水平段bc ,当液体全部凝固(c 点),温度又继续均匀下降。 由于冷却过程中常常发生过冷现象,其步冷曲线如图6.1虚线所示。轻微过冷有利于测量相变温度;严重过冷,却会使相变温度难以确定。 以横轴表示混合物的组成,纵轴表示温度,利用步冷曲线所得到的一系列组成和所对应的相变温度数据,就可绘出相图,见图6.2。 6.1 生成简单低共熔混合物的二组分系统 T /K (a) (b) (c) 图 6.2 简单低共熔二组分系统冷却曲线及相
二组分固液系统相图的测定 一、实验目的 1、利用步冷曲线建立二组分铅---锡固液系统相图的方法。 2、介绍PID 温度控制技术和热电阻的使用。 二、实验原理 本实验的目的是通过热分析法获得的数据来构建一个相图,用于表示不同温度、组成下的固相、液相平衡。不同组成的二组分溶液在冷却过程中析出固相的温度可以通过观察温度 – 时间曲线的斜率变化进行检测。当固相析出时,冷却速率会变得比较慢,这可归因于固化过程释放的热量部分抵消了系统向低温环境辐射和传导的热量。 A B B%a b c e f B (c )%I II III I II III B T/K t (a ) (b ) 图8.1 二元简单低共熔物相图(a ) 及其步冷曲线(b ) 图8.1(a )是典型的二元简单低共熔物相图。图中A 、B 表示二个组分的名称,纵轴是物理量温度T ,横轴是组分B 的百分含量B %。在acb 线的上方,系统只有一个相(液相)存在;在ecf 线以下,系统有两个相(固相A 和固相B )存在;在ace 所包围的区域内,一个固相(固体A )和一个液相(A 在B 中的饱和熔化物)共存;在bcf 所包围的区域内,一个固相(固体B )和一个液相(B 在A 中的饱和熔化物)共存。c 点有三相(互不相溶的固
体A 和固体B ,以及A 、B 的饱和熔化物液相)共存,根据相律,在压力确定的情况下,三相共存时系统的自由度为零,即三相共存的温度为一定值,在相图上表现为一条通过c 点的水平线,处于这个平衡状态下的系统温度T c 、系统组成A 、B 和B (c )%均不可改变,T c 和B (c )%构成的这一点称为低共熔点。 热分析法是绘制相图的常用实验方法,将系统加热熔融成一个均匀的液相,然后让系统缓慢冷却,以系统温度对时间作图得到一条曲线,称为步冷曲线或冷却曲线。曲线的转折点表征了某一温度下发生相变的信息,由系统组成和相变点温度可以确定相图上的一个点,多个实验点的合理连接就形成了相图上的相线,并构成若干相区。图1(b )是与相图对应的不同组成系统的步冷曲线。 三、仪器与药品 SWKY-1型数字控温仪、KWL —09可控升降温电炉、Pt-100热电阻温度传感器、配套软件、样品管(南京桑力电子设备厂) 锡(化学纯),铅(化学纯),铋(化学纯),苯甲酸(化学纯) 本实验装置由三部分组成:SWKY-1型数字控温仪、KWL —09可控升降温电炉和数据采集计算机系统(图8.2)。 图8.2 合金相图测定实验装置图 ② ① ③ ④ ⑤
一、实验目的 1.掌握步冷曲线法测绘二组分金属的固液平衡相图的原理和方法。 2、了解固液平衡相图的特点,进一步学习和巩固相律等有关知识。 二、主要实验器材和药品 1、仪器:KWL-II金属相图(步冷曲线)实验装置、微电脑控制器、不锈钢套管、硬质玻璃样品管、托盘天平、坩埚钳 2、试剂:纯锡(AR)、纯铋(AR)、石墨粉、液体石蜡 三、实验原理 压力对凝聚系统影响很小,因此通常讨论其相平衡时不考虑压力的影响,故根据相律,二组分凝聚系统最多有温度和组成两个独立变量,其相图为温度组成图。 、 较为简单的组分金属相图主要有三种:一种是液相完全互溶,凝固后固相也能完全瓦溶成固体混合物的系统最典型的为Cu- Ni系统;另一种是液相完全互溶,而固相完全不互溶的系统,最典型的是Bi- Cd 系统;还有一种是液相完全互溶,而固相是部分互溶的系统,如Pb- Sn 或Bi- Sn系统。 研究凝聚系统相平衡,绘制其相图常采用溶解度法和热分析法。溶解度法是指在确定的温度下,直接测定固液两相平衡时溶液的浓度,然后依据测得的温度和溶解度数据绘制成相图。此法适用于常温F易测定组成的系统,如水盐系统。 热分析法(步冷曲线法)则是观察被研究系统温度变化与相变化的关系,这是绘制金属相图最常用和最基本的实验方法。它是利用金属及合金在加热和冷却过程中发生相变时,潜热的释出或吸收及热容的突变,来得到金属或合金中相转变温度的方法。其原理是将系统加热熔融,然后使其缓慢而均匀地冷却,每隔定时间记录一次温度,物系在冷却过程中温度随时间的变化关系曲线称为步冷曲线(又称为冷却曲线)。根据步冷曲线可以判断体系有无相变的发生。当体系内没有相变时,步冷曲线是连续变化的;当体系内有相变发生时,步冷曲线上将会出现转折点或水平部分。这是因为相变时的热效应使温度随时间的变化率发生了变化。因此,由步冷曲线的斜率变化可以确定体系的相变点温度。测定不同组分的步冷曲线,找出对应的相变温度,即可绘制相图。 图3- 15(b)是具有简单低共熔点的A- B二元系相图,左右图中对应成分点、的步冷曲线。下面对步冷曲线作简单分析。 在固定压力不变的条件下,相律为: f=c-φ+1 (3-6-1) 式中:c为独立组分数;为相数。 》 对于纯组分熔融体系,c=1,q=1。在冷却过程中若无相变化发生,其温度随时间变化关系曲线为平滑曲线。到凝固点时,固液两相平衡,=2,自由度为0,温度不变,出现水平线段。等体系全部凝固后,其冷却情况同纯熔融体系一样,呈一平滑曲线。图3- 15(a)中曲线ave属于这种情况。
5.4二组分系统的固~液平衡 5.4.1形成低共熔物的固相不互溶系统 当所考虑平衡不涉及气相而仅涉及固相和液相时,则体系常称为"凝聚相体系"或"固液体系"。固体和液体的可压缩性甚小,一般除在高压下以外,压力对平衡性质的影响可忽略不计,故可将压力视为恒量。由相律: 因体系最少相数为Φ=1,故在恒压下二组分体系的最多自由度数f *=2,仅需用两个独立变量就足以完整地描述体系的状态。由于常用变量为温度和组成,故在二组分固液体系中最常遇到的是T~x(温度~摩尔分数)或T~ω(温度~质量分数)图。 二组分固~液体系涉及范围相当广泛,最常遇到的是合金体系、水盐体系、双盐体系和双有机物体系等。在本节中仅考虑液相中可以完全互溶的特殊情况。这类体系在液相中可以互溶,而在固相中溶解度可以有差别。故以其差异分为三类:(1)固相完全不互溶体系;(2)固相部分互溶体系和(3)固相完全互溶体系。进一步分类可归纳如下: 研究固液体系最常用实验方法为“热分析”法及“溶解度”法。本节先在“形成低共熔物的固相不互溶体系”中介绍这两种实验方法,然后再对各种类型相图作一简介。 (一)水盐体系相图与溶解度法
1.相图剖析 图5-27为根据硫酸铵在不同温度下于水中的溶解度实验数据 绘制的水盐体系相图,这类构成相图的方法称为"溶解度法"。 纵坐标为温度t(℃),横坐标为硫酸铵质量分数(以ω表 示)。图中FE线是冰与盐溶液平衡共存的曲线,它表示水 的凝固点随盐的加入而下降的规律,故又称为水的凝固点降 低曲线。ME线是硫酸铵与其饱和溶液平衡共存的曲线,它 表示出硫酸铵的溶解度随温度变化的规律(在此例中盐溶解 度随温度升高而增大),故称为硫酸铵的溶解度曲线。一般 盐的熔点甚高,大大超过其饱和溶液的沸点,所以ME不可 向上任意延伸。FE线和ME线上都满足Φ =2,f *=1,这意 味温度和溶液浓度两者之中只有一个可以自由变动。 FE线与ME线交于E点,在此点上必然出现冰、盐和盐溶液三相共存。当Φ=3 时,f *=0 ,表明体系的状态处于E点时,体系的温度和各相的组成均有固定不变的数值;在此例中,温度为 -18.3℃,相应的硫酸铵浓度为 39.8%。换句话说,不管原先盐水溶液的组成如何,温度一旦降至 -18.3℃,体系就出现有冰(Q 点表示)、盐(I点表示)和盐溶液(E点表示)的三相平衡共存,连接同处此温度的三个相点构成水平线QEI,因同时析出冰、盐共晶体,故也称共晶线。此线上各物系点(除两端点Q和I外)均保持三相共存,体系的温度及三个相的组成固定不变。倘若从此类体系中取走热量,则会结晶出更多的冰和盐,而相点为E的溶液的量将逐渐减少直到消失。溶液消失后体系中仅剩下冰和盐两固相,Φ=2,f *=1,温度可继续下降即体系将落入只存在冰和盐两个固相共存的双相区。若从上向下看E点的温度是代表冰和盐一起自溶液中析出的温度,可称为"共析点"。反之,若由上往下看E点温度是代表冰和盐能够共同熔化的最低温度,可称为"最低共熔点"。溶液E凝成的共晶机械混合物,称为"共晶体"或"简单低共熔物"。不同的水盐体系,其低共熔物的总组成以及最低共熔点各不相同,表5-7列举几种常见的水盐体系的有关数据。 表5-7 某些盐和水的最低共熔点及其组成 盐最低共熔点((℃)最低共熔物组成ω x100 NaCl NaBr NaI KCl KBr KI (NH 4) 2 SO 4 MgSO 4 Na 2SO 4 KNO 3 CaCl 2-21.1 -28.0 -31.5 -10.7 -12.6 -23.0 -18.3 -3.9 -1.1 -3.0 -5.5 23.3 40.3 39.0 19.7 31.3 52.3 39.8 16.5 3.84 11.20 29.9
同济大学物理化学实验报告 实验名称:____二组分固液系统相图的测定___姓名:_________李健___________学号:________1251654___________合作者:________靳凯___________院系:______材料科学与工程________专业班级:___材料科学与工程2012级2班___实验日期:________2014/5/6__________
一、摘要: 本实验采用热分析法来绘制铅-锡相图。将系统加热熔融成均匀的液相,然后让系统缓慢冷却,得到时间对温度的步冷曲线,曲线的转折点温度和系统组成可确定相图上的一个点,本实验通过测定十个不同组分系统。 二、关键词: 热分析法、步冷曲线、相变点温度、系统组成、相图 三、内容简介: 本实验测定含锡百分数为0、10%、15%、20%、35%、50%、62%、80%、95%、100%的铅锡混合样品的步冷曲线,读取步冷曲线上的相变点温度,以组成比对相变点温度作图得到相图。 四、实验原理: 二组分固-液相图是描述体系温度与二组分组成之间关系的图形。 若二组分体系的两个组分在固相完全不溶,在液相可完全互溶,一般具有简单低共熔点,其相图具有比较简单的形式。根据相律,对于具有简单低共熔点的二组分体系,其相图可分为三个区域,即液相区、固液共存区和固相区。 绘制相图时,由步冷曲线法可以根据不同组成样品的相变温度(即凝固点)绘制出这三个区域的交界线—液相线,即图1(b)中的T1E和T2E,并找出低共熔点E所处的温度和液相组成。 步冷曲线法又称热分析法,是绘制相图的基本方法之一。它是将某种组成的样品加热至全部熔融,再均速冷却,测定冷却过程中样品的温度–时间关系,即步冷曲线。根据步冷曲线上的温度转折点获得该组成的相变点温度。 (原理图)
南昌大学物理化学实验报告 学生姓名:李江生学号:5802216018 专业班级:安全工程161班实验日期:2018-04-17 实验五二组分凝聚系统相图 一、实验目的 (1)掌握热分析法(步冷曲线法)测绘Bi-Sn二组分凝聚系统相图的原理和方法。 (2)了解简单固液相图的特点、步冷曲线及相图中各曲线代表的物理意义巩固相律等有关知识。 二、实验原理 压力对凝聚系统影响很小,因此通常讨论其相平衡时不考虑压力的影响,故根据相律,二组分凝聚系统最多有温度和组成两个独立变量,其相图为温度-组成图。 热分析法:其原理是将系统加热融化,然后使其缓慢而均匀地冷却,每隔一定时间记录一次温度,绘制温度与时间的关系曲线——步冷曲线。若系统在均匀冷却过程中无相变化,其温度将随时间均匀下降;若系统在均匀冷却过程中有相变化,由于体系产生的相变热与体系放出的热量相抵消,步冷曲线就会出现转折或水平线段,转折点所对应的温度,即为该组成体系的相变温度。 由于冷却过程中常常发生过冷现象,其步冷曲线常如上图中虚线所示,由横轴表示混合物的组成,纵轴表示温度,利用步冷曲线所得到的一系列组成和所对应的相变温度数据,就可以绘出相图,如下图:
简单低共熔混合物二组分系统步冷曲线及相图 三、仪器与药品 步冷曲线测定装置1套(可控升降温电炉1台,数字控温仪1台,控温探头I,测温探头Ⅱ),不锈钢试样管5只,坩埚钳1把,劳保手套1副,Sn、Bi及其合金。 四、实验步骤 1、将数字控温仪温度Ⅰ设定为320℃,按“工作/置数”按钮,切换到工作状态。传感器Ⅰ插入加热炉Ⅰ样品管口内;传感器Ⅱ插入加热炉Ⅱ样品管口内;加热到320℃; 2、将“冷风量调节”旋钮逆时针旋到底,加热使温度降为250℃左右后; 3、适当调节“冷风量调节”旋钮,使温度降温绘制步冷曲线,降温速率控制为6-8℃/min,以便找到曲线拐点; 4、打开金属相图软件,设置绘步冷曲线图坐标; 5、实验结束后,关闭仪器电源,将实验桌面整理干净。 五、数据记录与处理 由以上数据作图得:
实验报告 课程名称: 大学化学实验(P ) 指导老师: 成绩:_______________ 实验名称: 二组分简单共熔系统相图的绘制 实验类型: 物性测试 同组学生姓名: 【实验目的】 1. 用热分析法测绘Zn-Sn 相图。 2. 熟悉热分析法的测量原理 3. 掌握热电偶的制作、标定和测温技术 【实验原理】 本实验采用热分析法中的步冷曲线方法绘制Zn-Sn 系统的固-液平衡相图。将系统加热熔融成一均匀液相,然后使其缓慢冷却,每隔一定时间记录一次温度,表示温度与时间的关系曲线,称为冷却曲线或步冷曲线。当熔融系统在均匀冷却过程中无相变化时,其温度将连续下降,得到一条光滑的冷却曲线,如在冷却过程中发生相变,则因放出相变热,使热损失有所抵偿,冷却曲线就会出现转折点或水平线段。转折点或水平线段对应的温度,即为该组成合金的相变温度。对于简单共熔合金系统,具有下列形状的冷却曲线[图a(a)],由这些冷却曲线,即可绘出合金相图[图a(b)]。 在冷却过程中,常出现过冷现象,步冷曲线在转折处出现起伏[图a(c)]。遇此情况可延长FE 交曲线BD 于点,G 点即为正常的转折点。 用热分析法测绘相图时,被测系统必须时时处于或接近相平衡状态,因此,系统的冷却速度必须足够慢,才能得到较好的结果。 图a 步冷曲线(a )、对应相图(b )及有过冷现象出现的步冷曲线(c ) 【试剂与仪器】 仪器 镍铬-镍硅热电偶1支;UJ-36电位差计1台;小保温瓶1只;盛合金的硬质玻璃管7只;高 温管式电炉2只(加热炉、冷却炉);调压器(2KW )1只; 坩埚钳1把;二元合金相图计算机测试系统1套。 试剂 锡、锌、铋(均为AR );石墨粉。 【实验步骤】 1. 热电偶的制作:取一段长约0.6m 的镍铬丝,用小瓷管穿好,再取两段各长0.5m 的镍硅丝,制作热 电偶(此步骤一般已事先做好)。 2. 配置样品:在7只硬质玻璃管中配制各种不同质量分数的金属混合物:100%Bi ;100%Sn ;100%Zn ; 45%Sn+55%Zn ;75%Sn+25%Zn ;91.2%Sn+8.8%Zn ;95%Sn+5%Zn 。为了防止金属高温氧化,表面放置石墨粉(此步骤由实验室完成)。 3. 安装:安装仪器并接好线路。 4. 加热溶化样品,制作步冷曲线:依次测100%Zn ,100%Bi ,100%Sn ,45%Sn+55%Zn ,
相图 一、是非题 下述各题中的说法是否正确?正确的在题后括号内画“√”,错的画“?”。 1.相是指系统处于平衡时,系统中物理性质及化学性质都均匀的部分。( ) 2.依据相律,纯液体在一定温度下,蒸气压应该是定值。( ) 3.依据相律,恒沸温合物的沸点不随外压的改变而改变。( ) 二、选择题 选择正确答案的编号,填在各题题后的括号内。 1NH4HS(s)和任意量的NH3(g)及H2 S(g)达平衡时有:( )。 (A)C=2,φ=2,f =2;(B) C=1,φ=2,f =1; (C) C=1,φ=3,f =2;(D) C=1,φ=2,f =3。 2已知硫可以有单斜硫,正交硫,液态硫和气态硫四种存在状态。硫的这四种状态____稳定共存。 (A) 能够;(B) 不能够;(C) 不一定。 3硫酸与水可形成H2SO4?H2O(s),H2SO4?2H2O(s),H2SO4?4H2O(s)三种水合物,问在101 325Pa的压力下,能与硫酸水溶液及冰平衡共存的硫酸水合物最多可有多少种?( ) (A) 3种;(B) 2种;(C) 1种;(D) 不可能有硫酸水合物与之平衡共存。 4将固体NH4HCO3(s) 放入真空容器中,恒温到400 K,NH4HCO3按下式分解并达到平衡:NH4HCO3(s) === NH3(g) + H2O(g) + CO2(g) 系统的组分数C和自由度数f为:( ) (A) C=2,f =2;(B) C=2,f =2; (C) C=2,f =0;(D) C=3,f =2。 5某系统存在C(s)、H2O(g)、CO(g)、CO2(g)、H2(g)五种物质,相互建立了下述三个平衡: H 2O(g)+C(s) H2(g) + CO(g) CO 2(g)+H2(g) H2O + CO(g) CO 2(g) + C(s) 2CO(g) 则该系统的独立组分数C为:( )。 (A) 3;(B) 2;(C) 1;(D) 4。 三、计算题 习题1 A,B二组分在液态完全互溶,已知液体B在80?C下蒸气压力为101.325 kPa,汽化焓为30.76 kJ·mol-1。组分A的正常沸点比组分B的正常沸点高10 ?C。在101.325kPa下将8 mol A和2 mol B混合加热到60 ?C产生第一个气泡,其组成为y B=0.4,继续在101.325 kPa下恒压封闭加热到70?C,剩下最后一滴溶液其组成为x B=0.1。将7 mol B和3 mol A气体混合,在101.325 kPa下冷却到65?C产生第一滴液体,其组成为x B=0.9,继续定压封闭冷却到55?C时剩下最后一个气泡,其组成为y B=0.6。 (1) 画出此二组分系统在101.325kPa下的沸点一组成图,并标出各相区; (2) 8 mol B和2 mol A的混合物在101.325 kPa,65 ?C时,
表-1 t/min T/℃ 纯铅锡20% 锡40% 锡61.9% 锡80% 纯锡 0 395.4 395.3 397.5 398.7 399.3 394.5 1 385.3 387.0 396.8 385.3 391.3 384.9 2 374.4 378.5 396.6 375.0 383.5 375.5 3 365.3 369.8 367.3 365.1 375.0 365.7 4 355.2 363. 5 353.8 354. 6 367.8 357.9 5 346.8 356.9 345.0 346.2 359.8 350.0 6 338. 7 348. 8 335.1 336. 9 353.1 341.8 7 329.6 342.1 327.2 329.6 346.7 334.5 8 322.9 335.8 319.5 322.6 339.6 327.6 9 317.8 328.8 311.5 315.4 333.9 320.8 10 311.8 323.2 305.2 309.3 327.3 314.8 11 306.6 316.2 298.6 303.6 321.1 307.2 12 302.2 311.8 293.2 297.3 315.8 302.5 13 298.6 307.2 288.1 292.0 311.0 296.3 14 294.4 302.5 282.1 286.6 306.4 291.2 15 288.7 298.9 276.8 285.0 302.2 286.1 16 283.4 295.3 271.2 275.2 297.4 280.4 17 277.9 291.1 264.8 269.3 293.0 275.5 18 270.6 287.3 259.4 264.4 288.5 271.1 19 264.0 282.3 254.5 257.7 283.3 266.5 20 256.8 277.5 248.9 254.4 278.6 261.7 21 250.8 272.2 244.3 250.2 273.5 257.6 22 245.3 266.2 239.3 245.8 269.3 252.9 23 239.2 261.3 235.1 241.3 265.1 249.2 24 234.5 256.7 231.0 237.4 260.5 245.3 25 230.0 252.0 226.5 233.0 256.6 241.1 26 225.1 247.9 222.7 229.4 252.9 237.6 27 221.0 244.2 219.0 225.9 248.8 233.8 28 217.1 240.3 215.0 221.9 245.3 230.5 29 212.7 236.7 211.5 218.7 241.1 227.2 30 209.1 232.6 208.2 215.4 238.7 223.7 31 205.6 229.2 204.5 211.9 234.9 220.9 32 201.7 225.7 201.5 209.6 231.2 224.5 33 198.1 221.9 198.1 209.4 228.3 230.6 34 194.7 218.7 195.4 208.1 225.3 231.1 35 191.7 215.0 192.9 206.7 222.0 231.1 36 188.7 212.0 190.3 204.9 219.3 230.9
S n-B i二组分固液相图 的绘制 -CAL-FENGHAI-(2020YEAR-YICAI)_JINGBIAN
Sn-Bi 二组分固液相图的绘制 【实验目的】 1. 掌握热分析法绘制二组分固液相图的原理和方法。 2. 了解纯物质与混合物步冷曲线的区别并掌握相变点温度的确定方法。 3. 了解简单二组分固-液相图的特点。 4. 掌握数字控温仪及KWL-80可控升温电炉的使用方法。 【实验原理】 压力对凝聚系统影响很小,因此通常讨论其相平衡时不考虑压力的影响,故根据相律,二组分凝聚系统最多有温度和组成两个独立变量,其相图为温度-组成图。 热分析法:其原理是将系统加热融化,然后使其缓慢而均匀地冷却,每隔一定时间记录一次温度,绘制温度与时间的关系曲线——步冷曲线。若系统在均匀冷却过程中无相变化,其温度将随时间均匀下降;若系统在均匀冷却过程中有相变化,由于体系产生的相变热与体系放出的热量相抵消,步冷曲线就会出现转折或水平线段,转折点所对应的温度,即为该组成体系的相变温度。 由于冷却过程中常常发生过冷现象,其步冷曲线常如上图中虚线所示,由横轴表示混合物的组成,纵轴表示温度,利用步冷曲线所得到的一系列组成和所对应的相变温度数据,就可以绘出相图,如下图: (a )纯物质的步冷曲 (b )二组分混合物的步冷曲线 (c )二组分低共熔混合
【仪器与试剂】 SWKY 数字控温仪1台;KWL-08可控升降温电炉1台;不锈钢样品管1支;炉膛保护筒1个;传感器1支。 纯Bi ;纯Sn ;石灰粉等。 【实验步骤】 1. (配含铋分别为0、20%、40%、70%、80%、100%(质量分数)的铋-锡混合物各100g ,分别装入不锈钢样品管中,再加入少许石墨粉覆盖试样,以防加热过程中试样接触空气而氧化。) 2. 按图2-16连接SWKY 数字控温仪与KWL-08可控升降温电炉,接通电源,将电炉置于 外控状态。 T B t/min W B /% 简单低共熔混合物二组分系统步冷曲线及相图
二组分金属相图的绘制思考题汇总 1.有一失去标签的Pb-Sn合金样品,用什么方法可以确定其组成? 答: 将其熔融、冷却的同时记录温度,作出步冷曲线,根据步冷曲线上拐点或平台的温度,与温度组成图加以对照,可以粗略确定其组成。 2.总质量相同但组成不同的Pb-Sn混合物的步冷曲线,其水平段的长度有什么不同?为什么? 答: (1)混合物中含Sn越多,其步冷曲线水平段长度越长,反之,亦然。 (2)因为Pb 和Sn的熔化热分别为23.0和59.4jg-1,熔化热越大放热越多,随时间增长温度降低的越迟缓,故熔化热越大,样品的步冷曲线水平段长度越长。 3.有一失去标签的Pb-Sn合金样品,用什么方法可以确定其组成? 4.总质量相同但组成不同的Pb-Sn混合物的步冷曲线,其水平段的长度有什么不同?为什么? (查表: Pb 熔点327℃,熔化热23.0jg-1,Sn熔点232℃,熔化热59.4jg-1) 5、何谓热分析法?用热分析法绘制相图时应注意些什么? 热分析法是相图绘制工作中的一种常用的实验方法,按一定比例配制均匀的液相体系,让他们缓慢冷却,以体系温度对时间作图,则为步冷曲线。曲线的转折点表征了某一温度下发生的相变的信息。 6、为什么要控制冷却速度,不能使其迅速冷却? 答:
使温度变化均匀,接近平衡态,必须缓慢降低温度,一般每分钟降低5度。 7、如何防止样品发生氧化变质? 答: 温度不可过高,空气不能过多和样品接触。 8、用相律分析在各条步冷曲线上出现平台的原因。 答: 因为金属熔融系统冷却时,由于金属凝固放热对体系散热发生一个补偿,因而造成冷却曲线上 的斜率发生改变,出现折点。当温度达到了两种金属的最低共熔点,会出现平台。 9、为什么在不同组成融熔液的步冷曲线上,最低共熔点的水平线段长度不同?答: 不同组成,各组成的熔点差值不同,凝固放热对体系散热的补偿时间也不同。 10.样品融熔后为什么要保温一段时间再冷却? 答: 使混合液充分混融,减小测定误差。 11.对于不同成分混合物的步冷曲线,其水平段有什么不同? 答: 纯物质的步冷曲线在其熔点处出现水平段,混合物在共熔温度时出现水平段。而平台长短也不同。 12.作相图还有哪些方法?
Ⅰ、目的要求 1.了解固-液相图的基本特点。 2.用热分析法测绘铅—锡二组分金属相图。 3.学会热电偶的制作、标定。的测温技术 Ⅱ、基本原理 相图是多相(两相及两相以上)体系处于相平衡态时体系的某物理性质(最常见是温度)对体系的某一自变量(如组成)作图所得的图形;图中能反映出相平衡情况(相的数目及性质等),故称为相图。二元或多元的相图常以组成为变量,其物理性质则大多取温度,由于相图能反映出多相平衡体系在不同条件(如自变量不同)下相平衡情况,故研究多相体系的性质以及多相体系平衡的演变(例如,冶金工业钢铁、合金冶炼过程;化学工业原料分离制备过程)等都要用到。 二组分体系的自由度与相的数目有以下关系: 自由度=组分数-相数+2 由于一般物质其固、液两相的摩尔体积相差不大,所以固-液相图手外界压力的影响颇小。这是它与气-液平衡体系的最大差别。 各种体系不同类型相图的解析在物理化学课程中占有重要地位。对相图的制作有很多方法,统称为物理化学分析,而对凝聚相研究(如固-液、固-固相等),最常用的方法是液、固借助相变过程中温度变化而产生的,观察这种热效应的变化情况,以确定一些体系的相态变
化关系,最常用的方法就是热分析及差热分析方法。本实验就是用热分析法绘制二元金属相图。 二组分金属相图是表示两种金属混合体系组成与凝固点关系的图。由于此体系属凝聚体系,一般视为不受压力影响,通常表示为固液平衡时液相组成与温度的关系。若两种金属在固相完全不溶,在液相可完全互溶,其相图具有比较简单的形式。 步冷曲线法是绘制相图的基本方法之一,是通过测定不同组成混合体系的冷却曲线来确定凝固点与溶液组成的关系。通常是将金属混合物或其合金加热全部熔化,然后让其在一定的环境中自行冷却,根据温度与时间的关系来判断有无相变的发生。图1是二元金属体系一种常见的步冷曲线。图2是两组分金属固液相图。图3有过冷现象时的步冷曲线。 当金属混合物加热熔化后冷却时,由于无相变发生,体系的温度随时间变化较大,冷却较快(1~2段)。若冷却过程中发生放热凝固,产生固相,将减小温度随时间的变化,使体系的冷却速度减慢(2~3段)。当融熔液继续冷却到某一点时,如3点,由于此时液相的组成为低共熔物的组成。在最低共熔混合物完全凝固以前体系温度保持不变,步冷曲线出现平台,(如图3~4段)。当融熔液完全凝固形成两种固态金属后,体系温度又继续下降(4~5段)。若图III-5-1中的步冷曲线为图III-5-2中总组成为P的混合体系的冷却曲线,则转折点2 相
实验七二组分简单共熔体系相图的绘制 ------Cd~Bi二组分金属相图的绘制 1 实验目的及要求: 1)应用步冷曲线的方法绘制Cd~Bi二组分体系的相图。 2)了解纯物质和混合物步冷曲线的形状有何不同,其相变点的温度应如何确定。 2 实验原理:… 用几何图形来表示多相平衡体系中有哪些相、各相的成分如何,不同相的相对量是多少,以及它们随浓度、温度、压力等变量变化的关系图,叫相图。 绘制相图的方法很多,其中之一叫热分析法。在定压下把体系从高温逐渐冷却,作温度对时间变化曲线,即步冷曲线。体系若有相变,必然伴随有热效应,即在其步冷曲线中会出现转折点。从步冷曲线有无转折点就可以知道有无相变。测定一系列组成不同样品的步冷曲线,从步冷曲线上找出各相应体系发生相变的温度,就可绘制出被测体系的相图,如图Ⅱ一6一l所示。 纯物质的步冷曲线如①⑤所示,从高温冷却,开始降温很快,口6线的斜率决定于体系的散热程度。冷到A的熔点时,固体A开始析出,体系出现两相平衡(溶液和固体A),此时温度维持不变,步冷曲线出现bc的水平段,直到其中液相全部消失,温度才下降。 混合物步冷曲线(如②、④)与纯物质的步冷曲线(如①、⑤)不同。如②起始温度下降很快(如a′b′段),冷却到b′点的温度时,开始有固体析出,这时体系呈两相,因为液相的成分不断改变,所以其平衡温度也不断改变。由于凝固热的不断放出,其温度下降较慢,曲线的斜率较小(b′c′段)。到了低共熔点温度后,体系出现三相,温度不再改变,步冷曲线又出现水平段c′d′,直到液相完全凝固后,温度又迅速下降。 曲线⑧表示其组成恰为最低共熔混合物的步冷曲线,其图形与纯物相似,但它的水平段是三相平衡。 用步冷曲线绘制相图是以横轴表示混合物的成分,在对应的纵轴标出开始出现相变(即步冷曲线上的转折点)的温度,把这些点连接起来即得相图。 3 仪器与药品: 加热电炉1只,热电偶(铜一康铜)1根,不锈纲试管8只,控温测定装置1台,计算机1台,镉(化学纯),铋(化学纯)。 4 实验步骤: 1)配制不同质量百分数的铋、镉混合物各100g(含量分别为0%,15%,25%,40%,55%,75%,90%,100%),分别放在8个不锈纲试管中。 2)用控温测定装置装置,依次测纯镉、纯铋和含镉质量百分数为90%,75%,55%,40%,25%,15%样品的步冷曲线。将样品管放在加热电炉中加热,让样品熔化,同时将热电偶的热端(连玻璃套管)插入样品管中,待样品熔化后,停止加热。用热电偶玻璃套管轻轻
二组分合金相图的绘制 一、实验目的: 1.通过实验,用热分析法测绘锡-铋二元合金相图。 2.了解热分析法的测量技术与有关测量温度的方法。 二、实验原理: 绘制相图常用的基本方法,其原理是根据系统在均匀冷却过程中,温度随时间变化情况来判断系统中是否发生了相变化。将金属溶解后,使之均匀冷却,每隔一定时间记录一次温度,表示温度与时间关系的曲线称为步冷曲线。若熔融体系在均匀冷却的过程中无相变,得到的是平滑的冷却线,若在冷却的过程中有相变发生,那么因相变热的释放与散失的热量有所抵偿,步冷曲线将出现转折点或水平线段,转折点所对应的温度即为相变温度。 时间(a)纯物质(b)混合物(c)低共熔混合物 图1 典型步冷曲线 对于简单的低共熔二元合金体系,具有图1所示的三种形状的步冷曲线。由这些步冷曲线即可绘出合金相图。如果用记录仪连续记录体系逐步冷却温度,则记录纸上所得的曲线就是步冷曲线。 用热分析法测绘相图时,被测体系必须时时处于或接近相平衡状态,因此体系的冷却速度必须足够慢才能得到较好的结果。 Sn—Bi合金相图还不属简单低共熔类型,当含Sn 81%以上即出现固熔体。 三、实验仪器和药品: 仪器和材料:金属相图实验炉(图2),微电脑温度控制仪,铂电阻,玻璃试管,坩埚,台天平。 药品:纯锡(CR)、纯铋(CR),石墨。
四、实验步骤: 1.配制样品 用感量为0.1g的托盘天平分别配制含铋量为30%、58%、80%的锡铋混合物各100g,另外称纯铋100g、纯锡100g,分别放入五个样品试管中。 2.通电前准备 ①首先接好炉体电源线、控制器电源、铂电阻插头、信号线插头、接地线。 图2 金属相图实验炉接线图 ②将装好药品的样品管插入铂电阻,然后放入炉体。 ③设置控制器拨码开关:由于炉丝在断电后热惯性作用,将会使炉温上冲100℃—160℃(冬天低夏天高)。因此设置拨码开关数值应考虑到这一点。例如:要求样品升温为350℃,夏天设置值为170℃。当炉温加热至170℃时加热灯灭,炉丝断电,由于热惯性使温度上冲至350℃后,实验炉自动开始降温。 ④将炉体黑色旋钮(电压指示旋钮)反时针旋转到底,处于保温状态。3.通电工作 ①通电升温:接通电源,控制器显示室温,加热灯亮,炉体上电压表指示电压值,炉体开始升温。 ②炉体自动断电:当炉内温度(即显示温度)高于设置温度后,加热灯灭,电压表指零,炉内电流切断,停止加热。 ③限温功能:为了防止拨码开关值设置过大而损坏铂电极,软件功能使拨码开关百位数不大于2,即温度最高设置值为299℃(万一拨码开关百位数大于2,程序中也认为是2)这样温度上冲后不会超过铂电阻的极限值500℃。 ④一次加热功能:由于实验中按先升温后降温的顺序进行,所以软件中采取一定的措施使得温度降到低于拨盘值时仍不加热,只有操作人员按复位键或重新通断一次电源,炉体才重新开始加热至拨码开关值。 ⑤中途加热:当炉体升温未达到要求温度时,如果显示温度小于299℃,则可增加拨码开关数值后再按一下复位键,加热继续进行。当显示温度超过299℃时,把黑色旋钮向顺时针旋动(工作人员不能离开),这时炉体继续加热,注意应提前切断炉丝电流(防止热惯性使温度上冲过高),即反时针旋动黑色旋钮至电压指示为零。 ⑥保温功能:由于冬季气温较低,为防止温度下降太快,不易发现拐点平台
二组分凝聚系统相图 一、实验目的 1.熟悉热分析法测绘Sn-Pb二组分凝聚系统相图的原理; 2.掌握热电偶测温的基本原理。 二、实验原理 热分析法是绘制凝聚系统相图的基本方法之一。其原理是根据系统在加热或冷却过程中发生相变所对应的温度来确定系统的状态图。当一个熔融系统均匀冷却时,如无相变化,它的温度将连续均与地下降,在温度-时间图上将得到一条平滑的曲线;如在冷却过程中发生了相变,则令温度下降减缓甚至因新相析出所放出的热量抵消了散失的热量而令温度不变,于是冷却曲线上就会出现转折点或水平线段,而产生水平或转折的温度就是发生相变的温度。 本实验所测定的是具有最低共熔点的固态部分互溶的Sn-Pb系统,实验室测定一系统冷却曲线。如图1(a)中的曲线A为Pb的冷却曲线,熔融的Pb 在高于327℃时,系统中只有液态的Pb,根据相律F=C-P+1可知,单组分系统的自由度为1,故温度可以改变且均匀下降。当逐渐冷却至温度为327℃时,Pb开始凝固,此时系统为两相共存,其自由度为零,即冷却曲线上出现水平线段。当Pb全部凝固后,系统自由度变为1,系统的温度又均匀下降。 图1(a)中曲线E所示的是组成为61.9%Sn的冷却曲线。它和纯金属的冷却曲线很相像,当液体冷却到一定温度时,从液体中同时析出两个固相,三相共存,因此自由度为零,故也出现水平段。此温度是低共熔温度。 对含Sn量在19.5%-97.4%之间的其他样品,冷却曲线比较复杂。本实验中测试的是组分为30%Sn和80%Sn的系统。以30%Sn系统为例,开始均匀冷却,当冷却到图中C点处温度时,开始析出α固溶体,此时自由度为1,温度仍可变化,但由于固相析出而放出相变热,使冷却速度减慢,冷却曲线斜率变小,出现转折点C,随着含有Pb量高的固溶体α的析出,液相中Pb 含量逐渐减少,只有降低温度才能继续析出固体,当温度降到D点处而且液相组成也变成低共熔组成时,另一固溶体β也达到饱和,系统变成三相,自由度为零,冷却曲线上出现水平段,直至液相消失。之后系统只剩下两个相,自由度为1,温度又开始均匀下降。 对Sn含量小于19.5%和含量高于97.5%的样品冷却曲线应该有三个转折点,但本实验热分析方法观测不到。