
浅议气体干燥剂的选择
在化学实验和考试的实验题中,常常涉及某些气体干燥剂的选择。而在教材中有关此内容的介绍是零散的,不系统的。在教学中,就如何正确选择气体干燥剂进行归纳,能快速、准确地进行判断和选择。
一、选择原则:所选的干燥剂不能与被干燥的气体发生反应,且干燥之后不能带入新的气体。
二、气体类别:根据气体的酸碱性,可将常见的气体分为以下三类:
①酸性气体:Cl2、CO2、SO2、NO2、H2S、HX等;
②碱性气体:;NH3
③中性气体:O2、H2、N2、CO、NO、CH4、C2H4、C2H2等。
三、干燥剂类别:与气体分类相似,据其酸碱性,可分为以下三类:
①酸性干燥剂:浓硫酸、五氧化二磷;
②碱性干燥剂:碱石灰、生石灰、固体氢氧化钠
③中性干燥剂:无水氯化钙、无水硫酸铜。
四、干燥剂选择的方法:
①酸性气体一般选用酸性干燥剂或中性干燥剂,不能选用碱性干燥剂。但H2S气体不能用浓硫酸
或无水硫酸铜作干燥剂,因为H2S能与浓硫酸或无水硫酸铜发生反应。
H2S + H2SO4(浓)== S↓+ SO2↑+ 2H2O
H2S +CuSO4 =====CuS↓+ H2SO4
②碱性气体一般选用碱性干燥剂或中性干燥剂,不能选用酸性干燥剂。但NH3气体不能用无水氯
化钙或无水硫酸铜作干燥剂,因为NH3能与无水氯化钙、无水硫酸铜发生反应,生成加合物或
配合物。
8NH3 + CaCl2 ===CaCl2?8NH3
4NH3 + CuSO4 ====Cu(NH3)4SO4
③中性气体一般可任选干燥剂。但H2不能用无水硫酸铜作干燥剂。因为H2能与无水硫酸铜发生
氧化还原反应。
H2 + CuSO4 === Cu + H2SO4
五、记忆方法:
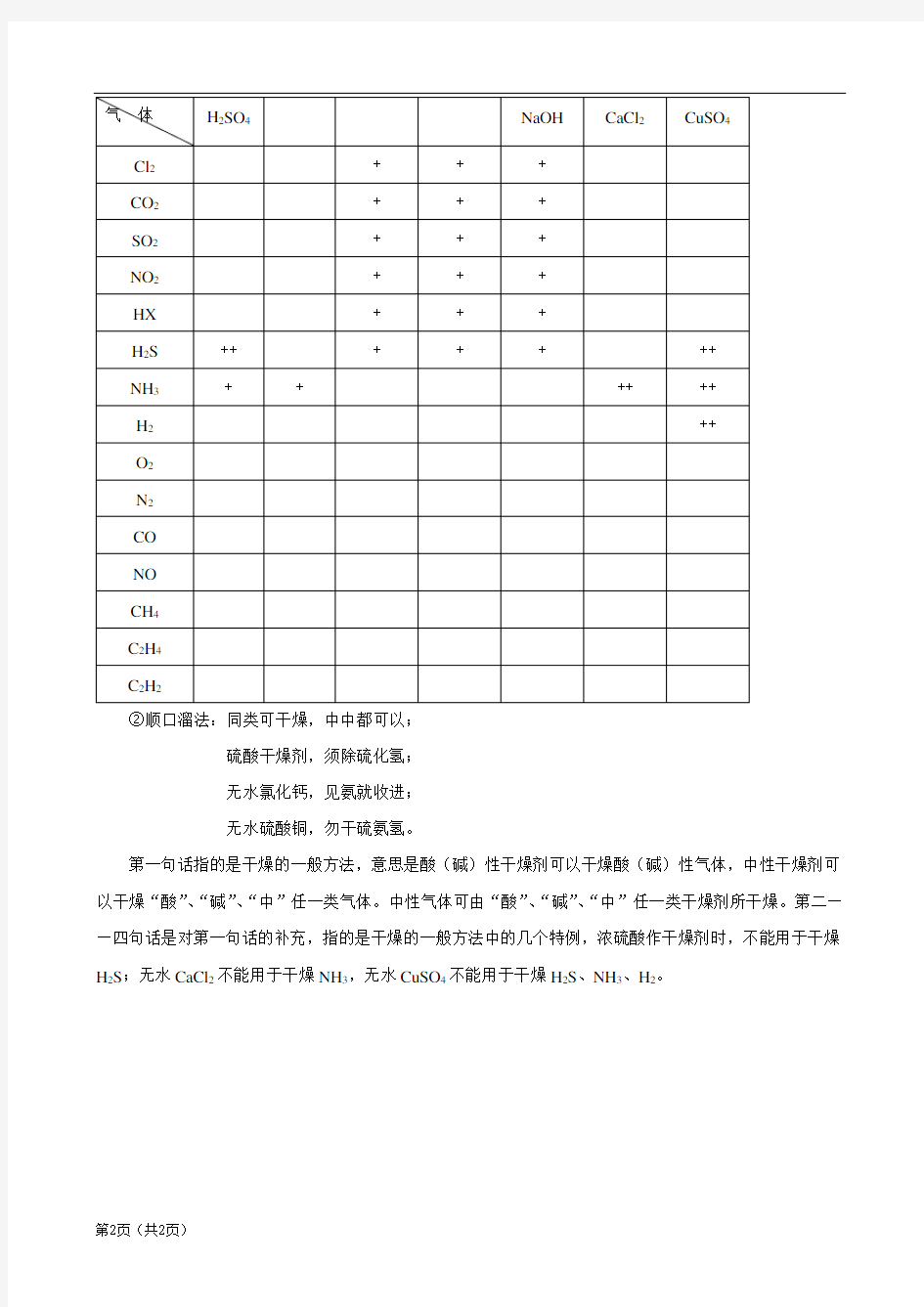
①表格法:综上所述,被干燥气体与干燥剂的选用情况如下表(“+”表示被干燥气体与所选干燥剂能发生反应,不可选用,其中“++”表示上述干燥剂选择方法中的特例,尤其要注意到;空白表示被干燥气体与所选干燥剂不发生反应,可选用。):
干燥剂浓P2O5碱石灰生石灰固体无水无水
气体H2SO4NaOH CaCl2CuSO4 Cl2+ + +
CO2+ + +
SO2+ + +
NO2+ + +
HX+ + +
H2S++ + + + ++
NH3+ + ++ ++
H2++
O2
N2
CO
NO
CH4
C2H4
C2H2
②顺口溜法:同类可干燥,中中都可以;
硫酸干燥剂,须除硫化氢;
无水氯化钙,见氨就收进;
无水硫酸铜,勿干硫氨氢。
第一句话指的是干燥的一般方法,意思是酸(碱)性干燥剂可以干燥酸(碱)性气体,中性干燥剂可以干燥“酸”、“碱”、“中”任一类气体。中性气体可由“酸”、“碱”、“中”任一类干燥剂所干燥。第二——四句话是对第一句话的补充,指的是干燥的一般方法中的几个特例,浓硫酸作干燥剂时,不能用于干燥H2S;无水CaCl2不能用于干燥NH3,无水CuSO4不能用于干燥H2S、NH3、H2。
高中化学干燥剂小结 1、酸性干燥剂:浓硫酸、P2O5、硅胶 1)浓硫酸(强氧化性酸) 2)P2O5(酸性白色粉末)、 3)硅胶(它是半透明,内表面积很大的多孔性固体,有良好的吸附性,对水有强烈的吸附作用。含有钴盐的硅胶叫变色硅胶,没有吸水时呈蓝色,被水饱和后呈粉红色。) 2、碱性干燥剂:碱石灰、CaO、固体NaOH 1)碱石灰(它是白色固体,主要成分CaO和NaOH)、 2)CaO(它是白色固体, 碱性氧化物)、 3)固体NaOH(强碱) 3、中性干燥剂:无水CaCl2、CuSO4 1)无水CaCl2(白色多孔固体)、 2)CuSO4(白色粉末,吸水程度较小,一般用来检验水的存在,吸水后变成蓝色CuSO4·5H20) 二、常见气体的分类 中学阶段常见的气体,按酸碱性也可分为三种: ①酸性气体:CO2、SO2、NO2、Cl2、HCl、H2S、HBr、HI等 ②碱性气体:NH3 ③中性气体:N2、O2、H2、CH4等 三、干燥剂的选择 1、总的原则:(酸碱性要一致且不能发生反应) a、酸性干燥剂不能干燥碱性气体,可以干燥酸性气体及中性气体; b、碱性干燥剂不能干燥酸性气体,可以干燥碱性气体及中性气体; c、中性干燥剂可以干燥各种气体。但这只是从酸碱反应这一角度来考虑, 2、同时还应考虑到规律之外的一些特殊性.如气体与干燥剂之间若发生了氧化还原反应,或生成络合物,加合物等,就不能用这种干燥剂来干燥该气体了。 特殊性: ①不能用浓硫酸干燥H2S, HBr,HI等还原性 ...气体,因为二者会发生氧化还原反应。如 H2S+H2SO4=2H2O+SO2+S↓,H2SO4+HBr= Br2+SO2+2H2O, H2SO4+HI= I2+SO2+2H2O ②不能用无水硫酸铜干燥H2S气体,二者会发生反应:CuSO4+H2S=H2SO4+CuS↓ ③不能用无水硫酸铜干燥NH3,二者可发生反应生成络合物:CuSO4+NH3={Cu(NH3)4}SO4 ④不能用无水CaCl2干燥NH3,二者会发生反应生成一些加合物:CaCl2+8NH3=CaCl2·8NH3
2019年高考化学实验常用的干燥剂 高考化学实验常用的干燥剂 一、高考化学实验常用的干燥剂:干燥剂。根据干燥剂的性质可将干燥剂分为酸性干燥剂、碱性干燥剂和中性干燥剂等。 1、酸性干燥剂 (1)浓硫酸干燥剂。可用浓硫酸干燥中性气体,如氧气、氢气、氮气、一氧化碳及甲烷等;还可以用来干燥非还原性的酸性气体,如二氧化碳、二氧化硫、氯气、氯化氢等。因为浓硫酸是具有氧化性的酸性干燥剂,所以不能用来干燥碱性气体氨气,及还原性气体硫化氢、溴化氢、碘化氢等。浓硫酸作为干燥剂可盛装在洗气瓶中使用。 (2)P2O5干燥剂。可用来干燥中性气体,如氧气、氢气、氮气、一氧化碳、甲烷等;也可用来干燥酸性气体,如二氧化碳、二氧化硫、氯化氢及氯气等。五氧化二磷具有强烈的吸水能力,所以它是中学化学实验室中效果最好的干燥剂。2、碱性干燥剂 (1)碱石灰干燥剂。它是在新制取的CaO粉末中加入NaOH 溶液,充分反应后经干燥制得,其主要成分是氢氧化钙和氢氧化钠。主要用来吸收氨气中的水分、二氧化碳等。碱石灰可盛装在干燥管、干燥塔及干燥器中使用。 (2)CaO干燥剂。可以用来干燥中性气体和碱性气体。可在
干燥管、干燥塔及干燥器中使用。 3、中性干燥剂 CaCl2干燥剂。氯化钙为多孔性固体,有较强的吸水能力。可用来干燥大多数气体,但不能用来干燥氨气,因氯化钙与氨气可形成配合物。 二、催化剂。中学化学实验中用到的催化剂有:二氧化锰、硫酸、铁粉、氧化铝等。 1、二氧化锰催化剂。如,①KClO3分解制取氧气的实验; ②过氧化氢分解实验。 2、硫酸催化剂。如,①乙烯的实验室制取实验;②硝基苯的制取实验;③乙酸乙酯的制取实验;④纤维素硝酸酯的制取实验;⑤乙酸乙酯的水解实验;⑥糖类(包括二糖、淀粉和纤维素)水解实验。 其中①-④的催化剂为浓硫酸,浓硫酸同时还作为脱水剂,⑤⑥的催化剂为稀硫酸,其中⑤也可以用氢氧化钠溶液做催化剂 3、铁催化剂。如溴苯的制取实验(实际上起催化作用的是溴与铁反应后生成的溴化铁)。 4、氧化铝催化剂。如石蜡的催化裂化实验。 三、指示剂 1、酸碱指示剂。常用的酸碱指示剂有石蕊试剂、酚酞试剂和甲基橙试剂。
高中化学常见干燥剂归纳整理 1.高中化学常见的干燥剂有哪些 浓硫酸、五氧化二磷 固体烧碱、石灰和碱石灰(氢氧化钠和氧化钙的混合物)无水氯化钙、无水硫酸镁 无水硫酸铜 2.分类及使用 常用的干燥剂有三类 第一类为酸性干燥剂。有浓硫酸、五氧化二磷、硅胶等; 第二类为碱性干燥剂,有固体烧碱、石灰和碱石灰(氢氧化钠和氧化钙的混合物)等; 第三类是中性干燥剂,如无水氯化钙、无水硫酸镁等。 常用干燥剂的性能和用途如下: 1.浓H 2SO 4:具有强烈的吸水性,常用来除去不与H 2SO 4反应的气体中的水分。例如常作为H 2、O 2、CO 、SO 2、N 2、HCl 、CH 4、CO 2、Cl 2等气体的干燥剂。 2.无水氯化钙:因其价廉、干燥能力强而被广泛应用。干燥速度快,能再生,脱水温度473K 。一般用以填充干燥器和干燥塔,干燥药品和多种气体。不能用来干燥氨、酒精、胺、酰、酮、醛、酯等。
3.无水硫酸镁:有很强的干燥能力,吸水后生成MgSO 4·7H 2O 。吸水作用迅速,效率高,价廉,为一良好干燥剂。常用来干燥有机试剂。 4.固体氢氧化钠和碱石灰:吸水快、效率高、价格便宜,是极佳的干燥剂,但不能用以干燥酸性物质。常用来干燥氢气、氧气和甲烷等气体。 5.变色硅胶:常用来保持仪器、天平的干燥。吸水后变红。失效的硅胶可以经烘干再生后继续使用。可干燥胺、NH 3、 O 2、 N 2等。 6.活性氧化铝(Al 2O 3):吸水量大、干燥速度快,能再生(400 -500K 烘烤)。 7.无水硫酸钠:干燥温度必须控制在30℃以内,干燥性比无水硫酸镁差。 8.硫酸钙:可以干燥H 2 、O 2 、CO 2 、CO 、N 2 、Cl 2、HCl 、H 2S 、 NH 3、 CH4等。 注:无水硫酸铜(CuSO 4)(无水硫酸铜成白色)也具有一定的干燥性,并且吸水后变成蓝色的五水硫酸铜(CuSO 4·5H 2O ),但一般不用来做干燥剂。 3.干燥剂的选择 由上述可知、对一些气体的干燥剂可作如下选择。
高中化学干燥气体以及 除杂 TYYGROUP system office room 【TYYUA16H-TYY-TYYYUA8Q8-
1、根据状态可分为固体干燥剂和液体干燥剂: 2、常见固体干燥剂有:碱石灰、NaOH固体、氧化钙、固体五氧化二磷、无水氯化钙、无水硫酸铜 3、常见液体干燥剂有:浓硫酸2、根据干燥剂的酸碱性可分为酸性干燥剂、中性干燥剂、碱性干燥 剂 4、酸性干燥剂:浓硫酸、浓磷酸、五氧化二磷 5、中性干燥剂:无水氯化钙、无水硫酸铜 6、碱性干燥剂:碱石灰、氧化钙、固体N a O H等 7、使用中应注意的问题: 8、(1)、酸性干燥剂不能干燥碱性气体。如五氧化二磷不能干燥氨气; 9、(2)、碱性干燥剂不能干燥酸性气体:如碱石灰不能干燥氯化氢、硫化氢等; 10、(3)、强氧化性干燥剂不能干燥还原性强的气体:如浓硫酸不能干燥硫化氢、碘化氢、溴化氢; 11、(4)、无水氯化钙不能干燥氨气,发生络合反应生成钙氨络离子 12、无水硫酸铜不能干燥硫化氢,生成硫化铜沉淀,也不能干燥氨气,生成氢氧化铜沉淀,进一步生成铜氨络离子。N2(O2):灼热的铜丝网,洗气
CO2(CO)通过红热的CuO把CO氧化成CO2 CO(CO2)通过NaOH溶液 CO2(HCl)通过NaHCO3溶液 CO2(SO2)通过NaHCO3溶液 SO2(HCl)通过通过NaHSO3溶液 H2S(HCl)通过NaHS溶液 Cl2(HCl)通过饱和食盐水 C(CuO)加入盐酸过滤 Fe2O3(Al2O3)加入过量NaOH溶液,过滤,取固体加热 Al(OH)3 (Fe2O3)加入NaOH溶液取滤液,再通入过量CO2 Al(OH)3 (SiO2)加入NaOH溶液取滤液,再通入CO2(短时间SiO2与NaOH的反应不考虑) Al2O3(SiO2):HCl再用氨水,过滤再加热。 NaHCO3(Na2CO3)继续通入CO2 KNO3(NaCl)利用溶解度差异结晶 CH4(CH2=CH2)通过溴水 溴苯(溴)NaOH溶液,分液 乙醇(水)加入CaO,蒸馏 乙醇(乙酸)蒸馏 乙酸乙酯(乙酸)加入饱和NaHCO3分液乙酸乙酯(乙醇)加水,分液 苯(苯酚)加入NaOH溶液分液 CO2(H2S):CuSO4溶液,洗气 BaSO4(BaCO3):H2SO4,过滤 NaOH(Na2CO3):适量Ba(OH)2,过滤 Na2CO3(NaOH):适量NaHCO3,不需要操作
高中化学常用干燥剂有哪些? 1、浓H2SO4:具有强烈的吸水性,常用来除去不与H2SO4反应的气体中的水分。例如常作为H 2、O2、CO、SO2、N2、HCl、CH4、CO2、Cl2等气体的干燥剂。 2、无水氯化钙:因其价廉、干燥能力强而被广泛应用。干燥速度快,能再生,脱水温度473K。一般用以填充干燥器和干燥塔,干燥药品和多种气体。不能用来干燥氨、酒精、胺、酰、酮、醛、酯等。 3、无水硫酸镁:有很强的干燥能力,吸水后生成MgSO4.7H2O。吸水作用迅速,效率高,价廉,为一良好干燥剂。常用来干燥有机试剂。 4、固体氢氧化钠和碱石灰:吸水快、效率高、价格便宜,是极佳的干燥剂,但不能用以干燥酸性物质。常用来干燥氢气、氧气和甲烷等气体。 5、变色硅胶:常用来保持仪器、天平的干燥。吸水后变红。失效的硅胶可以经烘干再生后继续使用。可干燥胺、NH3、O2、N2等 6、活性氧化铝(Al2O3):吸水量大、干燥速度快,能再生(400 -500K烘烤)。 7、无水硫酸钠:干燥温度必须控制在30℃以内,干燥性比无水硫酸镁差。 8、硫酸钙:可以干燥H2 。O2 。CO2 。CO 、N2 。Cl2、HCl 、H2S、NH3、CH4等 1 实验室中常用的干燥剂及其特性 实验室中常用的干燥剂及其特性 ①无水氯化钙(CaCl2):无定形颗粒状(或块状),价格便宜,吸水能力强,干燥速度较快。吸水后形成含不同结晶水的水合物CaCl2·nH2O(n=1,2,4,6)。最终吸水产物为CaCl2·6H2O (30℃以下),是实验室中常用的干燥剂之一。但是氯化钙能水解成Ca(OH)2 或Ca(OH)Cl ,因此不宜作为酸性物质或酸类的干燥剂。同时氯化钙易与醇类,胺类及某些醛、酮、酯形成分子络合物。如与乙醇生成CaCl2·4C2H5OH、与甲胺生成CaCl2·2CH3NH2,与丙酮生成CaCl2·2(CH3)2CO 等,因此不能作为上述各类有机物的干燥剂。 ②无水硫酸钠(Na2SO4):白色粉末状,吸水后形成带10个结晶水的硫酸钠(Na2SO4·10H2O)。因其吸水容量大,且为中性盐,对酸性或碱性有机物都可适用,价格便宜,因此应用范围较广。但它与水作用较慢,干燥程度不高。当有机物中夹杂有大量水分时,常先用它来作初步干燥,除去大量水分,然后再用干燥效率高的干燥剂干燥。使用前最好先放在蒸发皿中小心烘炒,除去水分,然后再用。
高中化学常见漂白性物质的比较 Na2O2、H2O2、O3、HClO或(Cl2)、浓硫酸、浓硝酸、SO2、活性炭、木炭、和硅胶都有漂白性,但漂白原理及漂白效果是不同的。 Na2O2、H2O2、O3、HClO 、浓硫酸、浓硝酸都具有强氧化性,它们的漂白原理:利用Na2O2、H2O2、O3、HClO、浓硫酸、浓硝酸的强氧化性将有机色素氧化成无色物质,褪色后不能恢复原来的颜色。这几种漂白性物质的漂白为永久性漂白。 SO2的漂白原理:SO2 与有机色素直接化合,形成不稳定的无色物质,褪色后在一定条件下又恢复原来的颜色。SO2的漂白为暂时性漂白。 活性炭、木炭、硅胶的漂白原理:利用的是它们的多孔吸附性漂白,加热后也恢复原来的颜色。活性炭、木炭、硅胶的漂白为物理漂白。活性炭、木炭、硅胶的漂白也是暂时性的。 具有漂白性的物质我们从物理和化学角度可分为两大类:化学漂白和物理漂白。化学漂白又可分为:氧化型漂白和化合型漂白。 其中Cl2、SO2都为气体且都有漂白性,但漂白原理及漂白效果是不同的。Cl2的漂白原理:Cl2溶于水生成的HClO具有强氧化性,将有色物质氧化成无色物质,褪色后不能恢复原来的颜色。SO2的漂白原理:SO2 与有色物质直接结合,形成不稳定的无色物质,褪色后在一定条件下又恢复原来的颜色。 总结: 吸附型漂白:活性炭、氢氧化铝胶体吸附有色物质,起到漂白作用,是物理变化。 强氧化性漂白:氯水、HClO、漂白粉Ca(ClO)2、Na2O2、H2O2、O3、浓硫酸、浓硝酸、NaClO,漂白作用是永久性的。化合型漂白:SO2有漂白作用是因为它溶于水后生成了H2SO3 ,H2SO3 能够和有色有机物(如品红)结合,形成不稳定的无色化合物,无色化合物在一定条件(如加热)下,又可以恢复原来的颜色,这种漂白是暂时性漂白。SO2的漂白作用具有特殊性。 请思考以下几个问题: 一.下列褪色现象是SO2的漂白性吗? (1)SO2使橙色溴水褪色 (2)SO2使紫色KMnO4酸性溶液褪色 (3)SO2使红色酚酞褪色 解析:以上褪色现象都不是SO2的漂白性所致。 (1)、(2)褪色的原因是SO2的还原性。分别发生氧化还原反应 SO2+Br2+2H2O= H2SO4+2HBr 5 SO2+2KMnO4+2H2O=K2SO4+2 MnSO4+ 2H2SO4 (3)褪色的原因是SO2溶于H2O后生成了H2SO3 ,H2SO3 是酸可以使红色酚酞变为无色。 二.氯水和SO2分别使紫色石蕊产生什么现象? 解析:氯水中的HClO先使紫色石蕊变红,而后因为它有强氧化性使红色褪去。 SO2溶于H2O后生成了H2SO3 ,H2SO3 是酸可以使紫色石蕊变为红色。而H2SO3 不具有强氧化性,所以红色不会褪去。 三.SO2和Cl2混合后能否增强漂白效果? 解析:不能。因为SO2和Cl2混合后会发生氧化还原反应 SO2+ Cl2+2 H2O= H2SO4+2HCl
常用干燥剂个作用及原理 干燥剂是指能除去潮湿物质(固态、液态或气态)中水分子的物质。干燥剂根据其干燥原理可分为化学干燥剂和物理干燥剂两类。 一. 化学干燥剂 化学干燥剂是一些能吸收水分并常伴有化学反应的物质。常见的有:、浓、 等。 化学干燥剂的蒸气压比水蒸气的蒸气压要小,结果空气中或潮湿物质中的水蒸气不断凝聚进入干燥剂,并生成结晶水合物或相应的酸或碱。上述物质与水发生反应的方程式为: 碱石灰是另一例化学干燥剂,易吸收水份和,生成, ,既可以用作干燥剂又可以用作的吸收剂。 化学干燥剂的使用原则是,用于干燥气体的干燥剂不能与被干燥的气体发生反应。一般来说,酸性气体如等可以用酸性或中性干燥剂干燥,但不能用碱性干燥剂干燥;碱性气体如等可以用碱性或中性干燥剂干燥,但不能用酸性干燥剂干燥;中性气体如等用酸性、碱性或中性干燥剂干燥都可以;具有还原性的气体如等不能用浓硫酸等氧化性干燥剂干燥。同时,因能与发生氨合反应生成氨合物而不能用无水氯化钙干燥。常见干燥剂与应用如下表所示。 二. 物理干燥剂 能吸收水分但不伴有化学反应的干燥剂称为物理干燥剂。这类干燥剂常见的是硅胶。 硅胶又叫氧化硅胶和硅酸凝胶,化学式可用来表示。它是一种无色透明
或乳白色颗粒,一般约含水3%~7%,吸湿量可达40%。市售商品中常含有,称为变色硅胶。利用它在吸水和脱水中发生的颜色变化来指示硅胶吸湿程度。其过程可用下式表示: 硅胶作为干燥剂,其干燥原理是依靠吸附作用来除去潮湿物质中的水分子,即通过固体表面的质点与各种气体、液体等中的水分子发生相互吸引力而将其吸附在固体物质表面上。这类物质大多有很多的孔隙,有着巨大的表面积。 硅胶可用可溶性硅酸盐与盐酸反应而制得,反应的实际过程很复杂,反应方程式一般可 写为: 硅酸在水里的溶解度不大,但生成后并不立即沉淀,而是硅酸分子之间发生缩合形成硅酸凝胶。将硅酸凝胶充分洗涤除去可溶性盐类后,干燥脱水即成为多孔性固体物质,称为硅胶。 具有吸附作用能作为干燥剂的物理干燥剂,除了硅胶外,还有活性炭、活性氧化铝等。
高中化学常见干燥剂归纳整 理 1。高中化学常见的干燥剂有哪些 浓硫酸、五氧化二磷固体烧碱、石灰和碱石灰(氢氧化钠和氧化钙的混合物)无水氯化钙、无水硫酸镁无水硫酸铜...文档交流仅供参考... 2.分类及使用 常用的干燥剂有三类 第一类为酸性干燥剂。有浓硫酸、五氧化二磷、硅胶等; 第二类为碱性干燥剂,有固体烧碱、石灰和碱石灰(氢氧化钠和氧化钙的混合物)等; 第三类是中性干燥剂,如无水氯化钙、无水硫酸镁等. 常用干燥剂的性能和用途如下: 1.浓H2SO4:具有强烈的吸水性,常用来除去不与H2SO4 反应的气体中的水分.例如常作为H2、O2、CO、SO2、N2、HCl、CH4、CO2、Cl2等气体的干燥剂。...文档交流仅供参考... 2。无水氯化钙:因其价廉、干燥能力强而被广泛应用.干燥速度快,能再生,脱水温度473K.一般用以填充干燥
器和干燥塔,干燥药品和多种气体。不能用来干燥氨、酒精、胺、酰、酮、醛、酯等。...文档交流仅供参考... 3.无水硫酸镁:有很强的干燥能力,吸水后生成MgSO4·7H2O。吸水作用迅速,效率高,价廉,为一良好干燥剂。常用来干燥有机试剂。...文档交流仅供参考... 4.固体氢氧化钠和碱石灰:吸水快、效率高、价格便宜,是极佳的干燥剂,但不能用以干燥酸性物质.常用来干燥氢气、氧气和甲烷等气体。...文档交流仅供参考... 5。变色硅胶:常用来保持仪器、天平的干燥。吸水后变红.失效的硅胶可以经烘干再生后继续使用.可干燥胺、NH3、 O2、N2等。...文档交流仅供参考... 6.活性氧化铝(Al2O3):吸水量大、干燥速度快,能再生(400 -500K烘烤)。 7.无水硫酸钠:干燥温度必须控制在30℃以内,干燥性比无水硫酸镁差。 8.硫酸钙:可以干燥H2、O2、CO2、CO、N2、Cl2、HCl 、H2S、 NH3、CH4等。...文档交流仅供参考... 注:无水硫酸铜(CuSO4)(无水硫酸铜成白色)也具有一定的干燥性,并且吸水后变成蓝色的五水硫酸铜(CuSO4·5H2O),但一般不用来做干燥剂。...文档交流仅供参考... 3。干燥剂的选择 由上述可知、对一些气体的干燥剂可作如下选择。
各类有机物常用干燥剂介绍 1,CaCL2,中性,与水作用产物:CaCL2.nH2O,n=1,2,4,6。适用范围:烃类,卤代烃,烯酮,醚,硝基化合物,中性气体,氯化氢。非适用范围:醇,胺,氨,酚,酯,酸,酰胺和某些醛酮。特点:吸水量大,作用快,效力不高,是良好的初步干燥剂。廉价,含有碱性杂质氢氧化钙。2,硫酸钠中性,与水作用产物:七水和十水硫酸钠。适用范围:醇,酯,醛,酮,酸,酰胺,卤代烃,硝基化合物等不能用氯化钙干燥的物质。吸水特点:吸水量大,作用慢,效力低,是良好的初步干燥剂。 3,硫酸镁中性,与水作用产物:一水和七水硫酸镁。适用范围:醇,酯,醛,酮,酸,酰胺,卤代烃,硝基化合物等不能用氯化钙干燥的物质。特点:较硫酸钠作用快,效力高。 4,硫酸钙中性,与水作用产物:CaSO4.1/2H2O,适用范围:烷,芳香烃,醚,醇,醛,酮。特点:吸水量小,作用快,效力高,可先用吸水量大的干燥剂初步干燥后再用。 5,碳酸钾碱性,与水作用产物:1.5水和2水合物。适用范围:醇,酮,脂,胺和杂环等碱性化合物,非适用范围:酸,酚及其他酸性化合物。 6,硫酸强酸性。与水作用产物:H3OSO4。适用范围:脂肪烃,烷基卤代物。非适用范围:烯,醚,醇及弱碱性化合物。特点:脱水效力高。 7,氢氧化钾,氢氧化钠强碱性。适用于胺,杂环等碱性化合物干燥。非适用于醇,酯,醛酮,酸,酚和酸性化合物干燥。其特点是干燥快速有效。 8,金属钠强碱性。适用于醚,三级胺,烃中的痕量水干燥。对碱土金属或对碱敏感物,醇等不适用。其特点是效力高,作用慢,需经初步干燥后才可再用,干燥后需蒸馏。 9,P2O5,酸性,适用于醚,烃,卤代烃,腈中痕量水分,酸溶液,二硫化碳。不适用于醇,酸,酮,胺,,碱性化合物,氯化氢,氟化氢等的干燥。其特点是吸水效力高,干燥后需蒸馏。10,CaH2,碱性,适用于碱性,中性,弱酸性化合物干燥,不适用于对碱敏感的化合物干燥。其特点是效力高,作用慢,先经初步干燥再用,干燥后需蒸馏。 11,CaO,Bao,碱性,适用于低级醇类,胺。其特点是效力高,作用慢,干燥后需蒸馏。 12,3A,4A分子筛,中性,是物理吸附,适用于各类有机物,不饱和烃气体。其特点是干燥快速高效,经初步干燥后可再用。 13,硅胶,常用于干燥器,不适用于氟化氢干燥。
1、根据状态可分为固体干燥剂和液体干燥剂: 常见固体干燥剂有:碱石灰、NaOH固体、氧化钙、固体五氧化二磷、无水氯化钙、无水硫酸铜 常见液体干燥剂有:浓硫酸2、根据干燥剂的酸碱性可分为酸性干燥剂、中性干燥剂、碱性干燥剂 酸性干燥剂:浓硫酸、浓磷酸、五氧化二磷 中性干燥剂:无水氯化钙、无水硫酸铜 碱性干燥剂:碱石灰、氧化钙、固体NaOH等 使用中应注意的问题: (1)、酸性干燥剂不能干燥碱性气体。如五氧化二磷不能干燥氨气; (2)、碱性干燥剂不能干燥酸性气体:如碱石灰不能干燥氯化氢、硫化氢等; (3)、强氧化性干燥剂不能干燥还原性强的气体:如浓硫酸不能干燥硫化氢、碘化氢、溴化氢; (4)、无水氯化钙不能干燥氨气,发生络合反应生成钙氨络离子 无水硫酸铜不能干燥硫化氢,生成硫化铜沉淀,也不能干燥氨气,生成氢氧化铜沉淀,进一步生成铜氨络离子。 N2(O2):灼热的铜丝网,洗气 CO2(CO)通过红热的CuO把CO氧化成CO2 CO(CO2)通过NaOH溶液 CO2(HCl)通过NaHCO3溶液 CO2(SO2)通过NaHCO3溶液 SO2(HCl)通过通过NaHSO3溶液 H2S(HCl)通过NaHS溶液 Cl2(HCl)通过饱和食盐水 C(CuO)加入盐酸过滤 Fe2O3(Al2O3)加入过量NaOH溶液,过滤,取固体加热 Al(OH)3 (Fe2O3)加入NaOH溶液取滤液,再通入过量CO2 Al(OH)3 (SiO2)加入NaOH溶液取滤液,再通入CO2(短时间SiO2与NaOH的反应不考虑) Al2O3(SiO2):HCl再用氨水,过滤再加热。 NaHCO3(Na2CO3)继续通入CO2
实验室中常用的干燥剂及其特性 1、浓H2SO4:具有强烈的吸水性,常用来除去不与H2SO4反应的气体中的水分。例如常作为H 2、O2、CO、SO2、N2、HCl、CH4、CO2、Cl2等气体的干燥剂。 2、无水氯化钙(CaCl2):无定形颗粒状(或块状),价格便宜,吸水能力强,干燥速度较快,能再生,脱水温度473K。吸水后形成含不同结晶水的水合物CaCl2·nH2O(n=1,2,4,6)。最终吸水产物为CaCl2·6H2O (30℃以下),是实验室中常用的干燥剂之一。但是氯化钙能水解成Ca(OH)2 或Ca(OH)Cl ,因此不宜作为酸性物质或酸类的干燥剂。同时氯化钙易与醇类,胺类及某些醛、酮、酯形成分子络合物。如与乙醇生成CaCl2·4C2H5OH、与甲胺生成CaCl2·2CH3NH2,与丙酮生成CaCl2·2(CH3)2CO 等,因此不能作为上述各类有机物的干燥剂。不能用来干燥氨、酒精、胺、酰、酮、醛、酯等。 3、无水硫酸钠(Na2SO4):白色粉末状,吸水后形成带10个结晶水的硫酸钠 (Na2SO4·10H2O)。因其吸水容量大,且为中性盐,对酸性或碱性有机物都可适用,价格便宜,因此应用范围较广。但它与水作用较慢,干燥程度不高。当有机物中夹杂有大量水分时,常先用它来作初步干燥,除去大量水分,然后再用干燥效率高的干燥剂干燥。使用前最好先放在蒸发皿中小心烘炒,除去水分,然后再用。 4、无水硫酸镁(MgSO4):白色粉末状,吸水容量大,吸水后形成带不同数目结晶水的硫酸镁MgSO4·nH2O (n=1,2,4,5,6,7)。最终吸水产物为MgSO4·7H2O(48℃以下)。由于其吸水较快,且为中性化合物,对各种有机物均不起化学反应,故为常用干燥剂。特别是那些不能用无水氯化钙干燥的有机物常用它来干燥。 5、无水硫酸钙(CaSO4):白色粉末,吸水容量小,吸水后形成2CaSO4·H2O(100℃以下)。虽然硫酸钙为中性盐,不与有机化合物起反应,但因其吸水容量小,没有前述几种干燥剂应用广泛。由于硫酸钙吸水速度快,而且形成的结晶水合物在100℃以下较稳定,所以凡沸点在100℃以下的液体有机物,经无水硫酸钙干燥后,不必过滤就可以直接蒸馏。如甲醇、乙醇、乙醚、丙酮、乙醛、苯等,用无水硫酸钙脱水处理效果良好。 6、无水碳酸钾(K2CO3):白色粉末,是一种碱性干燥剂。其吸水能力中等,能形成带两个结晶水的碳酸钾(K2CO3·2H2O),但是与水作用较慢。适用于干燥醇、酯等中性有机物以及一般的碱性有机物如胺、生物碱等。但不能作为酸类、酚类或其他酸性物质的干燥剂。 7、固体氢氧化钠(NaOH)和氢氧化钾(KOH):白色颗粒状,是强碱性化合物。只适用于干燥碱性有机物如胺类等。因其碱性强,对某些有机物起催化反应,而且易潮解,故应用范围受到限制。不能用于干燥酸类、酚类、酯、酰胺类以及醛酮。 8、五氧化二磷(P2O5):是所有干燥剂中干燥效力最高的干燥剂。 P2O5与水作用非常快,但吸水后表面呈粘浆状,操作不便。且价格较贵。一般是先用其他干燥剂如无水硫酸镁或无水硫酸钠除去大部分水,残留的微量水分再用P2O5干燥。它可
高中化学常用干燥剂 Written by Peter at 2021 in January
高中化学常用干燥剂有哪些? 1、浓H2SO4:具有强烈的吸水性,常用来除去不与H2SO4反应的气体中的水分。例如常作为H 2、O2、CO、SO2、N2、HCl、CH4、CO2、Cl2等气体的干燥剂。 2、无水氯化钙:因其价廉、干燥能力强而被广泛应用。干燥速度快,能再生,脱水温度473K。一般用以填充干燥器和干燥塔,干燥药品和多种气体。不能用来干燥氨、酒精、胺、酰、酮、醛、酯等。 3、无水硫酸镁:有很强的干燥能力,吸水后生成MgSO4.7H2O。吸水作用迅速,效率高,价廉,为一良好干燥剂。常用来干燥有机试剂。 4、固体氢氧化钠和碱石灰:吸水快、效率高、价格便宜,是极佳的干燥剂,但不能用以干燥酸性物质。常用来干燥氢气、氧气和甲烷等气体。 5、变色硅胶:常用来保持仪器、天平的干燥。吸水后变红。失效的硅胶可以经烘干再生后继续使用。可干燥胺、NH3、 O2、 N2等 6、活性氧化铝(Al2O3):吸水量大、干燥速度快,能再生(400 -500K烘烤)。 7、无水硫酸钠:干燥温度必须控制在30℃以内,干燥性比无水硫酸镁差。 8、硫酸钙:可以干燥H2 。O2 。CO2 。CO 、N2 。Cl2、HCl 、H2S、 NH3、CH4等 1 实验室中常用的干燥剂及其特性 实验室中常用的干燥剂及其特性 ①无水氯化钙(CaCl2):无定形颗粒状(或块状),价格便宜,吸水能力强,干燥速度较快。吸水后形成含不同结晶水的水合物CaCl2·nH2O(n= 1,2,4,
6)。最终吸水产物为CaCl2·6H2O (30℃以下),是实验室中常用的干燥剂之一。但是氯化钙能水解成Ca(OH)2 或Ca(OH)Cl ,因此不宜作为酸性物质或酸类的干燥剂。同时氯化钙易与醇类,胺类及某些醛、酮、酯形成分子络合物。如与乙醇生成CaCl2·4C2H5OH、与甲胺生成CaCl2·2CH3NH2,与丙酮生成 CaCl2·2(CH3)2CO等,因此不能作为上述各类有机物的干燥剂。 ②无水硫酸钠(Na2SO4):白色粉末状,吸水后形成带10个结晶水的硫酸钠(Na2SO4·10H2O)。因其吸水容量大,且为中性盐,对酸性或碱性有机物都可适用,价格便宜,因此应用范围较广。但它与水作用较慢,干燥程度不高。当有机物中夹杂有大量水分时,常先用它来作初步干燥,除去大量水分,然后再用干燥效率高的干燥剂干燥。使用前最好先放在蒸发皿中小心烘炒,除去水分,然后再用。 ③无水硫酸镁(MgSO4):白色粉末状,吸水容量大,吸水后形成带不同数目结晶水的硫酸镁MgSO4·nH2O (n=1,2,4,5,6,7)。最终吸水产物为 MgSO4·7H2O(48℃以下)。由于其吸水较快,且为中性化合物,对各种有机物均不起化学反应,故为常用干燥剂。特别是那些不能用无水氯化钙干燥的有机物常用它来干燥。 ④无水硫酸钙(CaSO4):白色粉末,吸水容量小,吸水后形成2CaSO4·H2O (100℃以下)。虽然硫酸钙为中性盐,不与有机化合物起反应,但因其吸水容量小,没有前述几种干燥剂应用广泛。由于硫酸钙吸水速度快,而且形成的结晶水合物在100℃以下较稳定,所以凡沸点在100℃以下的液体有机物,经无水硫酸钙干燥后,不必过滤就可以直接蒸馏。如甲醇、乙醇、乙醚、丙酮、乙醛、苯等,用无水硫酸钙脱水处理效果良好。
一、常用化学仪器及使用方法 (一)能直接加热的仪器 仪器图形与名称主要用途使用方法和注意事项 用于蒸发溶剂或浓缩溶液 可直接加热,但不能骤冷。液体的量不能超过其容积的三分之二。使用坩埚钳取放蒸发皿,加热时用三脚架或铁架台固定。加热后不能直接放到实验桌上,应放在石棉网上,以免烫坏实验桌 常用作反应器,也可收集少量气体 可直接加热,加热时管口不能对着人。放在试管内的液体不超过容积的1/2,加热的不超过1/3。 用于灼烧固体,使其反应(如分解) 可直接加热至高温。灼烧时应放于泥三角上,应用坩埚钳夹取。应避免聚冷。 燃烧少量固体物质可直接用于加热 2.能间接加热(需垫石棉网) 仪器图形和名称主要用途使用方法和注意事项 (分为50、100、250、500、1000ml等规格) 用作配制、浓缩、稀释溶液。 也可用作反应器和给试管水浴加 热等。 加热时应垫石棉网 根据液体体积选用不同规格烧杯 用作在加热条件下进行的反 应器 不能直接加热,应垫石棉网加 热。所装液体的量不应超过其容积1 /2。 用于蒸馏与分馏,也可用作 气体发生器 加热时要垫石棉网 用作接受器 用作反应器,常用于滴定操作 一般放在石棉网上加热。在滴定 操作中液体不易溅出。 3.不能加热的仪器 仪器图形与名称主要用途使用方法及注意事项 用于收集和贮存少量气体上口为平面磨砂,内侧不磨砂, 玻璃片要涂凡士林油,以免漏气, 如果在其中进行燃烧反应且有固体 生成时,应在底部加少量水或细砂。
分装各种试剂,需要避光保存时用棕色瓶。 广口瓶盛放固体 细口瓶盛放液体 瓶口内侧磨砂,且与瓶塞一一对应,切不可盖错。玻璃塞不可盛 放强碱,滴瓶内不可久置强氧化剂等。 制取某些气体的反应器固体+液体 固体为块状,气体溶解性小反应无强热放出,旋转导气管活塞控 制反应进行或停止。 (二)计量仪器 仪器图形与名称 主要用途 使用方法及注意事项 用于粗略量取液体的体积 要根据所要量取的体积数,选择大小合适的规格,以减少误差。不能用作 反应器,不能用作直接在其内配制溶液。 (分为50、100、250、500、1000ml ) 用于准确配制一定物质的 量浓度的溶液 不作反应器,不可加热,瓶塞不可 互换,不宜存放溶液,要在所标记的温 度下使用 用于精确度要求不高的称 量 药品不可直接放在托盘内,左物右 码。若左码右物,则称取质量小于物质 的实际质量。 用于中和滴定(也可 用于其他滴定)实验,也 可准确量取液体体积 酸式滴定管不可以盛装碱性溶液, 强氧化剂(KMnO 4溶液、I 2水等)应放 于酸式滴定管,“零”刻度在上方,精 确到0.01ml 。 胶头滴管 用于吸取或滴加液体,定滴数地加入滴夜。 必须专用,不可一支多用,滴加时不要与其他容器接触。 用于测量温度 加热时不可超过其最大量程,不可 当搅拌器使用,注意测量温度时,水银球的位置。 (三)用作过滤、分离、注入容液仪器 仪器图形与名称 主要用途 使用方法及注意事项 用作过滤或向小口容器中注入液体 过滤时应“一贴二低三靠”
高中所有常见化学方 程式 Revised on November 25, 2020
高中所有化学方程式 一、非金属单质(F2、Cl2、O2、S、N2、P、C、Si) 1、氧化性: F2+H2=2HF F2+Xe(过量)=XeF2 2F2(过量)+Xe=XeF4 nF2+2M=2MFn(表示大部分金属) 2F2+2H2O=4HF+O2 2F2+2NaOH=2NaF+OF2+H2O F2+2NaCl=2NaF+Cl2 F2+2NaBr=2NaF+Br2 F2+2NaI=2NaF+I2 F2+Cl2(等体积)=2ClF 3F2(过量)+Cl2=2ClF3 7F2(过量)+I2=2IF7 Cl2+H2=2HCl 3Cl2+2P=2PCl3 Cl2+PCl3=PCl5 Cl2+2Na=2NaCl 3Cl2+2Fe=2FeCl3 Cl2+2FeCl2=2FeCl3 Cl2+Cu=CuCl2 2Cl2+2NaBr=2NaCl+Br2 Cl2+2NaI=2NaCl+I2 5Cl2+I2+6H2O=2HIO3+10HCl Cl2+Na2S=2NaCl+S Cl2+H2S=2HCl+S Cl2+SO2+2H2O=H2SO4+2HCl Cl2+H2O2=2HCl+O2 2O2+3Fe=Fe3O4 O2+K=KO2 S+H2=H2S 2S+C=CS2 S+Fe=FeS S+2Cu=Cu2S 3S+2Al=Al2S3
S+Zn=ZnS N2+3H2=2NH3 N2+3Mg=Mg3N2 N2+3Ca=Ca3N2 N2+3Ba=Ba3N2 N2+6Na=2Na3N N2+6K=2K3N N2+6Rb=2Rb3N P4+6H2=4PH3 P+3Na=Na3P 2P+3Zn=Zn3P2 2.还原性 S+O2=SO2 S+O2=SO2 S+6HNO3(浓)=H2SO4+6NO2+2H2O 3S+4HNO3(稀)=3SO2+4NO+2H2O N2+O2=2NO 4P+5O2=P4O10(常写成P2O5) 2P+3X2=2PX3(X表示F2、Cl2、Br2) PX3+X2=PX5 P4+20HNO3(浓)=4H3PO4+20NO2+4H2O C+2F2=CF4 C+2Cl2=CCl4 2C+O2(少量)=2CO C+O2(足量)=CO2 C+CO2=2CO C+H2O=CO+H2(生成水煤气) 2C+SiO2=Si+2CO(制得粗硅) Si(粗)+2Cl=SiCl4 (SiCl4+2H2=Si(纯)+4HCl) Si(粉)+O2=SiO2 Si+C=SiC(金刚砂) Si+2NaOH+H2O=Na2SiO3+2H2 3、(碱中)歧化 Cl2+H2O=HCl+HClO (加酸抑制歧化、加碱或光照促进歧化) Cl2+2NaOH=NaCl+NaClO+H2O 2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O
常用干燥剂的性能和用途 1、浓H2SO4:具有强烈的吸水性,常用来除去不与H2SO4反应的气体中的水分。例如常作为H 2、O2、CO、SO2、N2、HCl、CH4、CO2、Cl2等气体的干燥剂。 2、无水氯化钙:因其价廉、干燥能力强而被广泛应用。干燥速度快,能再生,脱水温度473K。一般用以填充干燥器和干燥塔,干燥药品和多种气体。不能用来干燥氨、酒精、胺、酰、酮、醛、酯等。 3、无水硫酸镁:有很强的干燥能力,吸水后生成MgSO4.7H2O。吸水作用迅速,效率高,价廉,为一良好干燥剂。常用来干燥有机试剂。 4、固体氢氧化钠和碱石灰:吸水快、效率高、价格便宜,是极佳的干燥剂,但不能用以干燥酸性物质。党用来干燥氢气、氧气、氨和甲烷等气体。 5、变色硅胶:常用来保持仪器、天平的干燥。吸水后变红。失效的硅胶可以经烘干再生后继续使用。可干燥胺、NH3、O2、N2等。 6、活性氧化铝(Al2O3):吸水量大、干燥速度快,能再生(400 -500K烘烤)。 7、无水硫酸钠:干燥温度必须控制在30℃以内,干燥性比无水硫酸镁差。 8、硫酸钙:可以干燥H2。O2。CO2。CO 、N2。Cl2、HCl 、H2S、NH3、CH4等。 由上述可知、对一些气体的干燥剂可作如下选择。 气体名称常用干燥剂气体名称常用干燥剂 CO 浓H2SO4、CaCl2、P2O5H2S CaCl2 CO2CaCl2、浓H2SO4、P2O5N2浓H2SO4、CaCl2、P2O5 Cl2CaCl2、浓H2SO4NH3CaO、KOH或碱石灰 H2CaCl2、P2O5NO Ca(NO3)2 HBr CaBr2、ZnBr2O3CaCl2 HCl CaCl2、浓H2SO4SO2浓H2SO4、CaCl2、P2O5 HI CaI2 液体适用干燥剂 Drying Agents for Liquids
高中化学知识点“一般”与“特殊”超全总结 高中化学知识点“一般”与“特殊”超全一、基本概念与基本理论 1. 原子的原子核一般是由质子和中子构成的; 但氕的原 子核中无中子。 2. 原子最外层电子数小于或等于2 的一般是金属原子; 但氢、氦原子的最外层电子数分别为1、2,都不是金属元 素。 3. 质子总数与核外电子总数相同的微粒一般是同种微粒但Ne 与HF例外。 4. 离子核外一般都有电子;但氢离子(H+)的核外没有电子。 5. 气体单质一般是由双原子组成的;但稀有气体为单原子,臭氧为三原子组成。 6. 由同种元素组成的物质一般是单质,是纯净物;但O2 与03,白磷与红磷它们是混合物。 7. 由两种或两种以上物质生成一种物质的反应一般是化合反应;但反应物仅一种参加,却属于化合反应。 如:3O2=2O3, 2NO2=N2O4 8. 原子活泼性强,对应单质性质一般较活泼; 但氮原子
活泼,可氮气很稳定。 9. 金属氧化物一般是碱性氧化物;但Mn2O7是酸性氧化物,AI2O3、ZnO是两性氧化物。 10. 非金属氧化物一般是酸性氧化物;但CO、NO不是酸性氧化物。 11. 酸酐一般是非金属氧化物;但HMnO啲酸酐Mn2O7是金属氧化物。 12. 酸酐一般是氧化物;但乙酸酐[(CH3CO)2O] 等例外。 13. 溶于水成酸的氧化物一般是酸酐;但NO2溶于水生成了硝酸,可硝酸的酸酐为N2O5。 14. 一种酸酐对应的酸一般是一种酸;但P2O5 既是偏磷 酸(HPO3)的酸酐,又是磷酸(H3PO4)的酸酐。 15. 无氧酸一般都是非金属元素的氢化物;但氢氰酸(HCN) 例外。 16. 酸的“元数”一般等于酸分子中的氢原子数;但亚磷酸(H3PO3)不是三元酸而是二元酸,次磷酸(H3PO2)不是三元酸而是一元酸,硼酸(H3BO3) 不是三元酸而是一元酸等。 17. 在某非金属元素形成的含氧酸中,该元素化合价越高,对应酸的氧化性一般越强;但次氯酸(HCIO)的氧化性比髙氣酸(HCIO4) 的氧化性强。
实验室常用干燥剂及其使用 除去固体、液体或气体内少量水分的方法称干燥。有机实验中几乎所做的每一步反应都会遇到试剂、溶剂和产品的干燥问题,所以干燥是实验室中最普通但最重要的一项操作。如果试剂和产品不进行干燥或干燥不完全,将直接影响有机反应、定性分析、定量分析、波谱鉴定和物理常数测定的结果。 干燥方法可分为物理方法与化学方法两种。物理方法有吸附(包括离子交换树脂法和分子筛吸附法)、共沸蒸馏、分馏、冷冻、加热和真空干燥等,化学方法按去水作用的方式又可分为两类:一类与水能可逆地结合生成水合物,如氯化钙、硫酸钠等;一类与水会发生剧烈的化学反应,如金属钠、五氧化二磷等。下面按有机物的物理状态介绍各种干燥的方法和实验操作。 1.固体的干燥 (1)晾干:将待干燥的固体放在表面皿上或培养皿中,尽量平铺成一薄层、再用滤纸或培养皿覆盖上,以免灰尘沾污,然后在室温下放置直到干燥为止,这对于低沸点溶剂的除去是既经济又方便的方法。 (2)红外灯干燥:固体中如含有不易挥发的溶剂时,为了加速干燥,常用红外灯干燥。干燥的温度应低于晶体的熔点,干燥时旁边可放一支温度计,以便控制温度。要随时翻动固体,防止结块。但对于常压下易升华或热稳定性差的结晶不能用红外灯干燥。红外灯可用可调变压器来调节温度,使用时温度不要调得过高,严防水滴溅在灯泡上而发生炸裂。 (3)烘箱烘干:实验室内常用带有自动温度控制系统的电热鼓风干燥箱,其使用温度一般为50~300℃,通常使用温度应控制在100~200℃的范围内。烘箱用来干燥无腐蚀、无挥发性、加热不分解的物品。切忌将挥发、易燃、易爆物放在烘箱内烘烤,以免发生危险。 (4)干燥器干燥:普通干燥器一般适用于保存易潮解或升华的样品。但干燥效率不高,所费时间较长。干燥剂通常放在多孔瓷板下面,待干燥的样品用表面皿或培养皿装盛,置于瓷板上面,所用干燥剂由被除去溶剂的性质而定。 1. 变色硅胶是使用较普遍的干燥剂,其制备方法是:将无色硅胶平铺在盘中,在
常见的气体干燥剂有哪些 1、浓H2SO4:具有强烈的吸水性,常用来除去不与H2SO4反应的气体中的水分。例如常作为H 2、O2、CO、SO2、N2、HCl、CH4、CO2、Cl2等气体的干燥剂。 2、无水氯化钙:因其价廉、干燥能力强而被广泛应用。干燥速度快,能再生,脱水温度473K。一般用以填充干燥器和干燥塔,干燥药品和多种气体。不能用来干燥氨、酒精、胺、酰、酮、醛、酯等。 3、无水硫酸镁:有很强的干燥能力,吸水后生成MgSO4.7H2O。吸水作用迅速,效率高,价廉,为一良好干燥剂。常用来干燥有机试剂。 4、固体氢氧化钠和碱石灰:吸水快、效率高、价格便宜,是极佳的干燥剂,但不能用以干燥酸性物质。常用来干燥氢气、氧气和甲烷等气体。 5、变色硅胶:常用来保持仪器、天平的干燥。吸水后变红。失效的硅胶可以经烘干再生后继续使用。可干燥胺、NH3、 O2、 N2等 6、活性氧化铝(Al2O3):吸水量大、干燥速度快,能再生(400 -500K 烘烤)。 7、无水硫酸钠:干燥温度必须控制在30℃以内,干燥性比无水硫酸镁差。 8、硫酸钙:可以干燥H2、O2、CO2、CO 、N2、Cl2、HCl 、H2S、 NH3、CH4等。 实验室中常用的干燥剂及其特性 ①无水氯化钙(CaCl2):无定形颗粒状(或块状),价格便宜,吸水能力强,干燥速度较快。吸水后形成含不同结晶水的水合物CaCl2·nH2O(n
= 1,2,4,6)。最终吸水产物为CaCl2·6H2O (30℃以下),是实验室中常用的干燥剂之一。但是氯化钙能水解成Ca(OH)2或Ca(OH)Cl ,因此不宜作为酸性物质或酸类的干燥剂。同时氯化钙易与醇类,胺类及某些醛、酮、酯形成分子络合物。如与乙醇生成CaCl2·4C2H5OH、与甲胺生成 Ca Cl2·2CH3NH2,与丙酮生成CaCl2·2(CH3)2CO 等,因此不能作为上述各类有机物的干燥剂。上海坪尧贸易有限公司为美国CPI合成润滑油在中国市场的总代理。除专业供应BASF干燥剂外,主要市场有碳氢气体压缩机油,冷冻压缩机油,空气压缩机油,冰箱及冰柜压缩机油,合成设备用油,食品级润滑油,食品级低温导热油,风力发电齿轮箱专用油等。 ②无水硫酸钠(Na2SO4):白色粉末状,吸水后形成带10个结晶水的硫酸钠(Na2SO4·10H2O)。因其吸水容量大,且为中性盐,对酸性或碱性有机物都可适用,价格便宜,因此应用范围较广。但它与水作用较慢,干燥程度不高。当有机物中夹杂有大量水分时,常先用它来作初步干燥,除去大量水分,然后再用干燥效率高的干燥剂干燥。使用前最好先放在蒸发皿中小心烘炒,除去水分,然后再用。上海坪尧贸易有限公司在合成冷冻油的市场主要提供以下的OEM指定用油:如:顿汉布什(Dunham-Bush)、开利Carrier(Carlyle)、格拉索GEA(Grasso)、世纪(Century)、谷轮(Copeland)、恩布拉科(Embraco)、博克(BOCK)、美优乐(Maneurop)、丹佛斯(Danfoss)、麦克维尔(Mcquay)、西亚特(CIAT)、J&E Hall(APV Baker)、特灵(Trane)、莱富康(Refcomp)、富士豪(Frascold)、GRAM、Vilter、布里斯托(Bristol)、克莱门特、Contour。普莱克斯(Praxair)、林德(Linde )、梅塞尔(MESSER)、法液空(Air Liquide) 、 Mycom, Toromont 。