
《反应热的测量与计算》课后练习
1.已知H +
+OH -
===H 2O 生成1 mol H 2O 放出热量57.3 kJ ,下列反应中能放出57.3 kJ 热量的是
( )
A .1 mol 稀H 2SO 4与足量NaOH 溶液反应
B .稀盐酸与氨水反应生成1 mol H 2O
C .稀盐酸与稀Ba(OH)2溶液反应生成1 mol 水
D .稀NaOH 与95%浓硫酸反应生成1 mol 水 2.含有11.2 g KOH 的稀溶液与1 L 0.1 mol·L -1
的H 2SO 4溶液反应,放出11.46 kJ 的热量,表示该反应的中和热的热化学方程式为
( )
A .KOH(aq)+12 H 2SO 4(aq)=== 12 K 2SO 4(aq)+H 2O(l) ΔH =-11.46 kJ·mol -
1
B .2KOH(aq)+H 2SO 4(aq)===K 2SO 4(aq)+2H 2O(l) ΔH =-11.46 kJ·mol -
1 C .2KOH(aq)+H 2SO 4(aq)===K 2SO 4(aq)+2H 2O(l) ΔH =-114.6 kJ·mol -1 D .KOH(aq)+1
2 H 2SO 4(aq)=== 12 K 2SO 4(aq)+H 2O(l) ΔH =-57.
3 kJ·mol -
1
3.将V 1 mL 1.00 mol·L -
1 HCl 溶液和V
2 mL 未知浓度的NaOH 溶液混合均匀后测量并记录溶液温度,实验结果如图所示(实验中始终保持V 1+V 2=50 mL)。下列叙述正确的是( ) A .做该实验时环境温度为22 ℃ B .该实验表明化学能可以转化为热能 C .NaOH 溶液的浓度约为1.00 mol·L -
1 D .该实验表明有水生成的反应都是放热反应 4.已知25 ℃、101 kPa 下,石墨、金刚石燃烧的热化学方程式分别为
C(石墨,s)+O 2(g)===CO 2(g) ΔH =-393.51 kJ·mol -
1① C(金刚石,s)+O 2(g)===CO 2(g) ΔH =-395.41 kJ·mol -1② 据此判断,下列说法正确的是
( )
A .由石墨制备金刚石是吸热反应;石墨的能量比金刚石的低
B .由石墨制备金刚石是吸热反应;石墨的能量比金刚石的高
C .由石墨制备金刚石是放热反应;石墨的能量比金刚石的低
D .由石墨制备金刚石是放热反应;石墨的能量比金刚石的高 5.下列依据热化学方程式得出的结论正确的是 ( )
A .已知2SO 2(g)+O 2(g)
2SO 3(g)为放热反应,则SO 2的能量一定高于SO 3的能量
B .已知C(s ,石墨)===C(s ,金刚石) ΔH >0,则金刚石比石墨稳定
C .已知H +
(aq)+OH -
(aq)===H 2O(l) ΔH =-57.3 kJ·mol -
1,则任何酸碱中和反应的热效应均为57.3 kJ
D.已知2C(s)+2O2(g)===2CO2(g)ΔH1;2C(s)+O2(g)===2CO(g)ΔH2,则ΔH1<ΔH2 6.某实验小组用0.50 mol·L-1 NaOH溶液和0.50 mol·L-1硫酸溶液进行中和热的测定。Ⅰ.配制0.50 mol·L-1 NaOH溶液
(1)若实验中大约要使用245 mL NaOH溶液,至少需要称量NaOH固体________g。
名称托盘天平
(带砝码)
小烧杯坩埚钳玻璃棒药匙量筒
仪器
序号 a b c d e f (2)
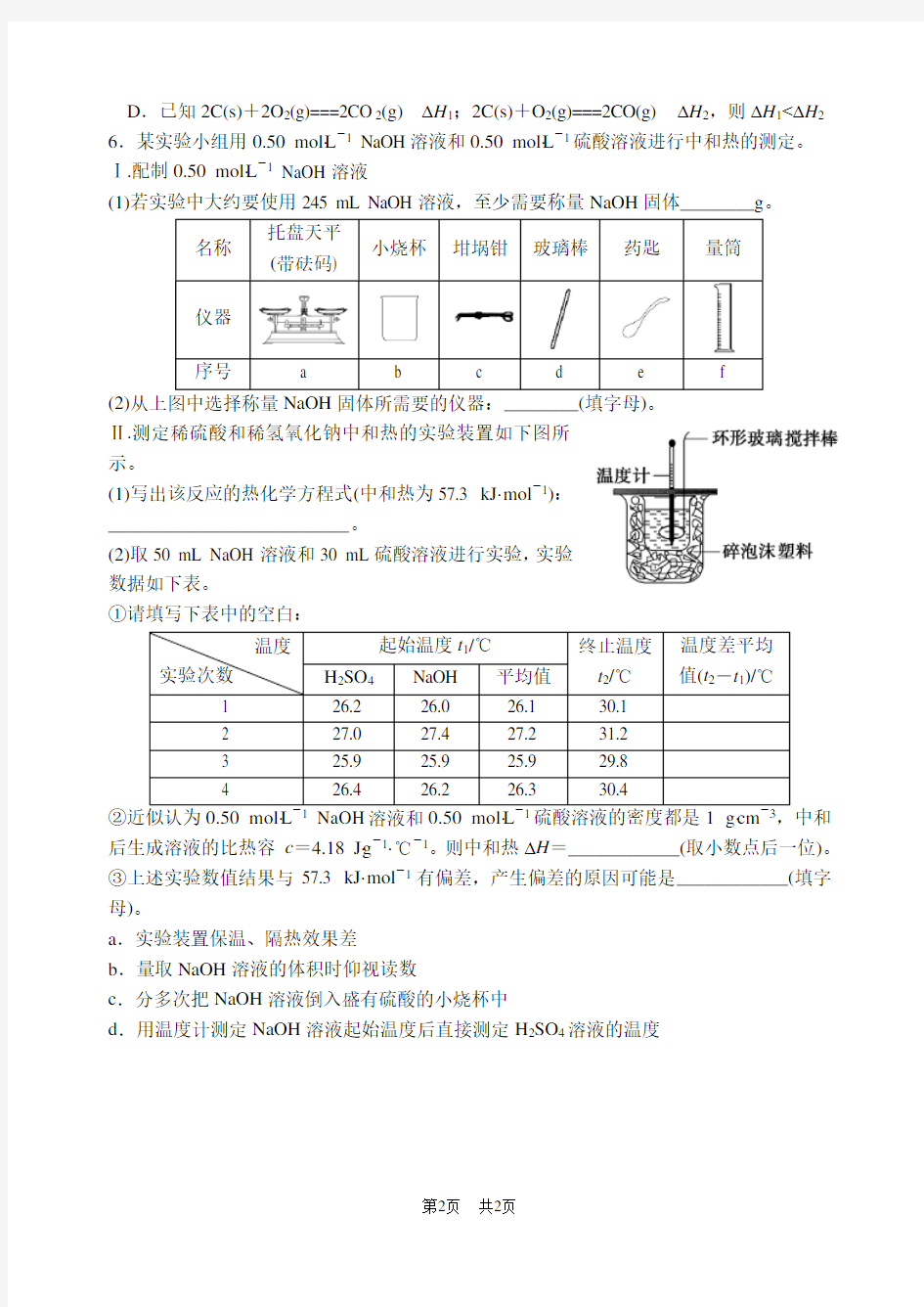
Ⅱ.测定稀硫酸和稀氢氧化钠中和热的实验装置如下图所
示。
(1)写出该反应的热化学方程式(中和热为57.3 kJ·mol-1):
__________________________。
(2)取50 mL NaOH溶液和30 mL硫酸溶液进行实验,实验
数据如下表。
①请填写下表中的空白:
温度实验次数
起始温度t1/℃终止温度
t2/℃
温度差平均
值(t2-t1)/℃H2SO4NaOH 平均值
1 26.
2 26.0 26.1 30.1
2 27.0 27.4 27.2 31.2
3 25.9 25.9 25.9 29.8
4 26.4 26.2 26.3 30.4
后生成溶液的比热容c=4.18 J·g-1·℃-1。则中和热ΔH=____________(取小数点后一位)。
③上述实验数值结果与57.3 kJ·mol-1有偏差,产生偏差的原因可能是____________(填字母)。
a.实验装置保温、隔热效果差
b.量取NaOH溶液的体积时仰视读数
c.分多次把NaOH溶液倒入盛有硫酸的小烧杯中
d.用温度计测定NaOH溶液起始温度后直接测定H2SO4溶液的温度