
体外分析技术
一、概论
体外标记免疫分析是当今先进的超微量检测技术,它的测量值可精确到毫微克(ng)—微微克(pg),甚至达毫微微克级(fg),它的基础是先进的放射性或非放射性标记技术和先进的抗原—抗体结合的免疫技术。它主要被用于检测人体的各种激素和各种肿瘤标志物。是当前的重要检测技术之一。
体外标记免疫分析技术起始于1959年,由美国的Berson和Yalow共同建立了放射免疫分析法(RIA),由于RIA具有灵敏度高、特异性强、重复性好、测量简便、成本低等优点。在生物学和医学中对机体超微量活性物质的分析取得重要突破而获得飞速的发展,故Yalow在1977年获得诺贝尔奖。
但因RIA法必须使用放射性物质,所以在发展中受到一定限制。自70年代起科学家们曾先后研究并建立了多种非放射性物质的标记免疫分析,如酶标记免疫分析(EIA)、时间分辨荧光分析(TRFIA)、酶放大发光分析(CLEIA)、化学放光(CLIA)、电化学发光(ECLRA)等,并且可进行仪器的全自动化测定和全自动的数据分析。
各种测定方法主要是标记技术、标记品的不同而采用的测量方法不同,各具特点和优点,其基本原理还是标记免疫技术,其中最基本的还是放射免疫分析和免疫放射分析。
二、放射免疫分析的基本原理
放射免疫分析法(Radioimmunoassay,RIA)是建立在放射性分析的高度灵敏性与免疫反应高度特异性基础之上的超微量分析技术。通过测定放射性标记抗原—抗体复合物的量来计算出待测抗原(样品)的量。20世纪50年代末Berson和Yalow在研究胰岛素抗体时,首先了建立放射免疫分析法定量测定胰岛素含量,从而开创了生物活性物质微量测定分析的新时代,从此放射免疫分析技术以其灵敏度高、特异性强、重复性好、准确度高等优点而独树一帜。目前应用放射免疫分析技术能测定生物活性物质达300余种,被广泛应用于生物学医学各个领域。
放射免疫分析法的基本原理是竞争性抑制反应。设定限量的特异性抗体(Ab)与一定量的特异性标记抗原(*Ag)在一定条件下发生免疫反应,形成标记抗原—抗体复合物(*AgAb)。如在上述反应体系中加入非标记的抗原(Ag),则非标记抗原和标记抗原与限量抗体间发生了竞争性结合的抑制反应。当反应平衡后,将反应体系中的标记抗原—抗体复合物(B)与游离的标记抗原(F)分离,测定标记抗原-抗体复合物的放射性(每分钟计数cpm),通过计算,求出非标记抗原的量(图1)
Ag + Ab AgAb + Ag
+
*Ag
*Ag+ *AgAb
图1 放射免疫分析法的基本原理
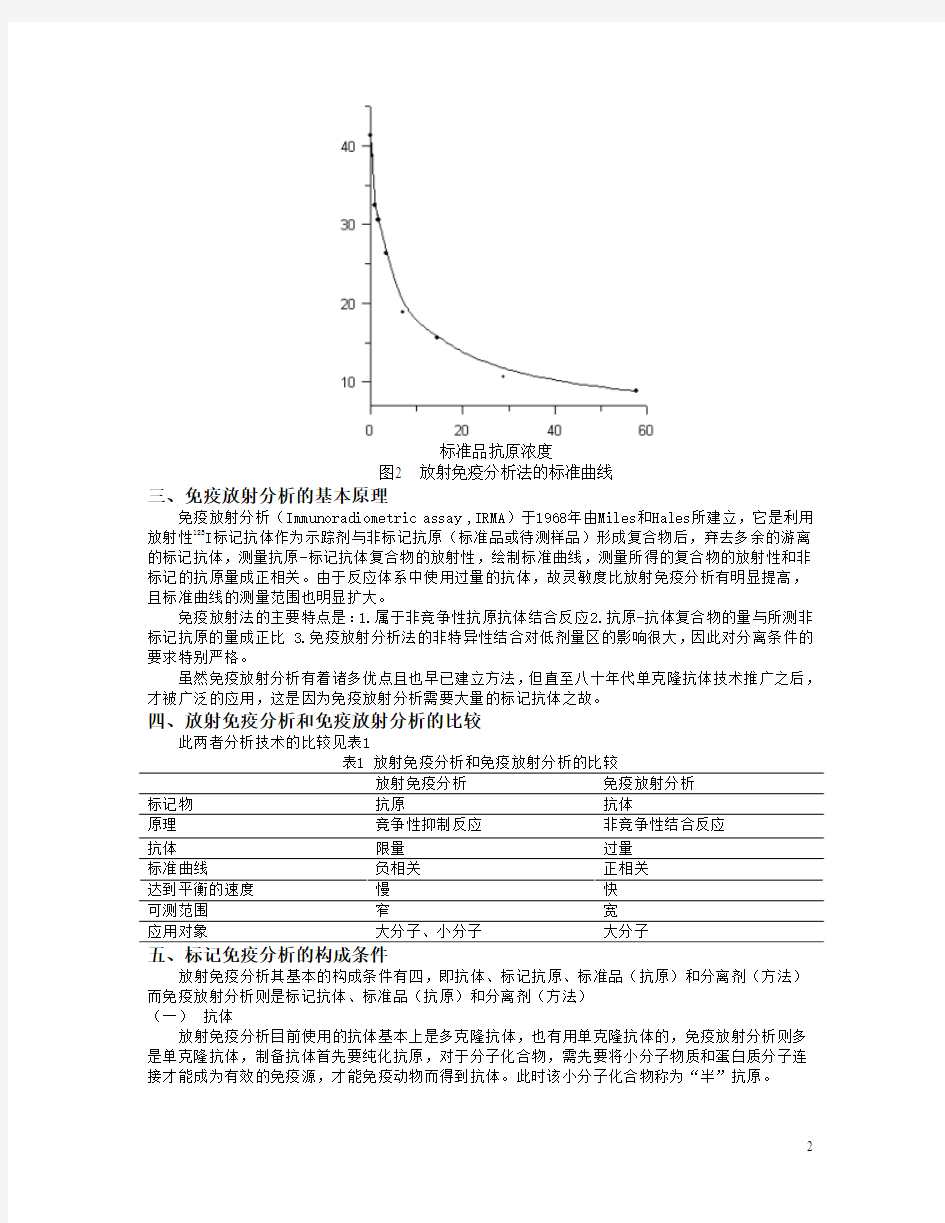
可以看到,在反应体系中由于标记抗原和抗体都是限量的,随着投入的非标记抗原量的增大,标记抗原和抗体的结合量被抑制降低,此即为“竞争性抑制反应”。在实际应用时,用一组不同浓度的标准品抗原,在相同条件下,和标记抗原与抗体发生竞争性反应,随着标准品量的逐步增大,标记抗原-抗体结合率则逐步降低(图2),以标准品抗原浓度作为横坐标,以标记抗原-抗体复合物的结合率(B%)作为纵坐标,绘制标准曲线,测量待测样品的标记抗原-抗体复合物的放射性结合率(B%),即可自标准曲线上查得被测样品相应的含量。
标准品抗原浓度
图2 放射免疫分析法的标准曲线
三、免疫放射分析的基本原理
免疫放射分析(Immunoradiometric assay ,IRMA)于1968年由Miles和Hales所建立,它是利用放射性125I标记抗体作为示踪剂与非标记抗原(标准品或待测样品)形成复合物后,弃去多余的游离的标记抗体,测量抗原-标记抗体复合物的放射性,绘制标准曲线,测量所得的复合物的放射性和非标记的抗原量成正相关。由于反应体系中使用过量的抗体,故灵敏度比放射免疫分析有明显提高,且标准曲线的测量范围也明显扩大。
免疫放射法的主要特点是:1.属于非竞争性抗原抗体结合反应2.抗原-抗体复合物的量与所测非标记抗原的量成正比 3.免疫放射分析法的非特异性结合对低剂量区的影响很大,因此对分离条件的要求特别严格。
虽然免疫放射分析有着诸多优点且也早已建立方法,但直至八十年代单克隆抗体技术推广之后,才被广泛的应用,这是因为免疫放射分析需要大量的标记抗体之故。
四、放射免疫分析和免疫放射分析的比较
此两者分析技术的比较见表1
放射免疫分析其基本的构成条件有四,即抗体、标记抗原、标准品(抗原)和分离剂(方法)而免疫放射分析则是标记抗体、标准品(抗原)和分离剂(方法)
(一)抗体
放射免疫分析目前使用的抗体基本上是多克隆抗体,也有用单克隆抗体的,免疫放射分析则多是单克隆抗体,制备抗体首先要纯化抗原,对于分子化合物,需先要将小分子物质和蛋白质分子连接才能成为有效的免疫源,才能免疫动物而得到抗体。此时该小分子化合物称为“半”抗原。
衡量抗体质量的指标有(1)抗体的亲和力(2)抗体的特异性(3)抗体的滴度。
抗体的亲和力表示抗体和抗原结合的能力,亲和力高,抗原抗体易结合和结合后不易解离。特异性标志抗体和抗原结构类似物不易发生交叉反应。如特异性不高,则抗原类似物也能和抗体结合影响分析结果。滴度是指抗体实际应用时稀释度,滴度越高,所需的抗血清(抗体)量就越少,稀释度通常均在1:1000以上,亲和力高、特异性强的抗体才能建立高灵敏和高特异的标记免疫分析。(二)标记抗原(标记抗体)
放射免疫分析或免疫放射分析,目前使用的大都是125I核素,少数系用的是3H核素。125I标记抗原(抗体)应用γ计数器测量,成本低廉和方法简便。3H测量则要用液体闪烁计数器测量,测量成本较高也比较繁复。对标记抗原或抗标记抗体的主要要求是(1)标记后不改变原有抗原的生物学活性(免疫活性、特异性等)(2)标记的放射性核素的半衰期不能太短,以保证试剂盒的制造,运输和分析过程所需,125I的半衰期为60天,其标记抗原商品流程可达4~8周。3H的半衰期为12.3年,多为生物学或基础医学所用。(3)要求有足够的比活度,以保证放射免疫分析或免疫放射分析的灵敏度。(三)标准品(抗原)
标准品实际上是已知含量并呈梯度浓度的系列标准抗原,做分析的标准曲线之用。其免疫活性必须相同于被测物质且定量要准,是定量分析的凭借和依据。
(四)分离剂
反应达到平衡后,必须将标记抗原-抗体复合物和游离的标记抗原分开,以便分别测量放射性B 或F,游离抗体及非标记抗原无放射性,不干扰测量,由于抗原抗体复合物是大分子,游离抗原是小分子,因而凡能使大分子和小分子物质分离的方法均适用,目前常用的分离方法分为两大类。(1)液相分离技术
抗原抗体在液相环境起反应,常用的分离方法为3种。○1双抗体沉淀法。当抗体和抗原反应结束后,加入抗第一抗体的抗体,称为第二抗体,形成抗原-第一抗体-第二抗体的复合物。通过离心沉淀即可收集和测量。○2聚乙二醇(PEG)沉淀法。PEG能使复合物沉淀○3现常用第二抗体-PEG联合沉淀法,分离效果既快又好。
(2)固相分离技术
固相分离技术是预先将抗体吸附在某种固体支持物上,抗原、抗体的反应就在支持物上进行,反应结束后只需将未结合的游离抗原弃去,测定固体支持物上的放射性即可,现常用固相支持物的材料有聚乙烯、聚苯乙烯等塑料和纤维素,磁性颗粒等。
六、标记免疫分析的质量指标
实验分析总体性能的观察指标是稳定性,在该实际分析试剂材料的有效期内,其各个测量参数和标准曲线形态以及参考样品的测定值均应基本稳定。而对于该实验分析的基本性能指标主要有4点。
(1)精密度:指同一样品重复测定的实际值的离散程度,离散程度越小,实验分析系统的精密度就越高。
(2)灵敏度:指实验测定中经统计学处理,能与零剂量相区别的最小量,在实际工作中还需注意其有效测定范围。
(3)特异性:实验分析对被测物的特异性决定于所用抗体的特异性
(4)准确度:准确度是指样品的测定值偏离真值的程度。由于实际样品的真值是未知的,常用的估计准确度的方法是测定实际样品加标准品的回收率。
综前所述,标记免疫分析体系中最重点的是抗体的质量和标记抗原的质和量。
七、标记免疫分析的质量控制
鉴于标记免疫分析是一种超微量的定量分析技术,因此必须要加以质量控制,以保证检测结果的可靠性。质量控制就是对分析工作的误差进行经常性的检查,将误差控制在可接受的范围内。如有质量异常,则及时采取对策,以校正、改进之。标记免疫的质量控制,包括实验室内部质量控制和实验室间的质量评估两大方面。
(一)内部质量控制
实验室误差分为两大类:随机误差及系统误差。前者出现纯属随机现象,如测定体系中各个样品的加样,分离,测量等步骤的差异引起复管误差过大。后者的出现则是由于整批实验发生了某系统变化,使很多样品受到类似的影响,例如标准品浓度不准或失活,抗体的效价降低等等,而导致
整批样品测定值的偏高或偏低。随机误差是不可避免的,要求批内误差变异系数<5%,批间的变异系数<10%。而系统误差则可以校正而避免。内部质控就是要通过严格操作规程来进行控制,亦可通过同批检测的参考血清来观察。
(二)实验室间的质量评估
这种实验室间的质量评估由地区性或全国性机构就一些项目对个实验室的结果进行比较,得到共同性或个别性的性息,提供行政主管部门,生产厂家和各实验室参考。
八、各种非放射标记免疫分析技术
放射免疫分析法和免疫放射分析法,经数十年来的应用和发展,是相当成熟的技术,具有方便、稳定、成本低、实用价值大等优点。对医学研究和临床诊断起了极大的推动作用。但是由于存在放射性污染和难以实现自动化操作,很多学者早已在研究建立各种非放射性标记免疫分析和实现快速的自动化操作。近年来,已完成了多项非放射性标记免疫分析的自动化技术,优点是○1无放射性污染○2自动化操作减少了随机误差○3灵敏度更高○4测定快捷,报告及时,尤其适宜大批样本的测定。从免疫分析的角度来看,其原理是相同的,只是标记物是非放射性的,其最后的信号不是射线,而是其他物理形式,探测技术(仪器)各有不同。目前常用的为下类四种非放射性标记免疫分析技术(一)化学发光免疫分析(Chemiluminescence Immunoassay, CLEIA)
化学发光免疫分析是用能产生化学发光的化合物代替放射性标记物,最常用的发光化合物是异鲁米那或吖啶酯,他们在碱性条件下遇到过氧化物便发生单光子发射,这种方法不需要外源性激发光源,避免了本底光和杂散光的干扰,大大提高了信噪比,因此有很高的灵敏度,但这种方法的发光时间集中在加入过氧化物或碱的短时间内,测量时间极短,必须严格掌握。
(二)酶放大化学发光免疫分析 (Chemiluminescence Enzyme Immunoassay, CLEIA) 本法标记物是碱性磷酸酶标记的抗体,经过夹心法免疫反应(和IRMA相似)复合物带有酶标记,加入底物金刚烷,在碱性磷酸酶作用下底物断裂,同时发射光子,由于酶反应持续一段时间,发射光子的过程明显比上述单纯化学发光长,而且在一段时间内维持稳定,所以本法的稳定性较高。(三)电化学发光免疫分析(Electorchemluminescence Immunoassay ECLI)电化学发光反应的底物三联吡啶钌被作为标记物制成标记的抗原或抗体,测定模式分两个步骤,以双抗夹心法测定抗原为例,先由三联吡啶钌标记的抗体,吸附在磁性微球上的固相抗体与受检样本在试管中反应,反应后进入反应室,由三丙胺缓冲液冲洗去除多余的游离的标记抗体,反应室电极下磁铁含有磁性微球的夹心物和固相抗体被吸附在电极表面发生化学发光反应,通过光电信号测定而反映样品中抗原含量。
此法较为敏感而稳定,为测试技术中一项新技术。
(四)时间分辨荧光免疫分析(Time-resolved Fluorescence Immunoassay, TR-RIA)本法的免疫反应原理和放射免疫分析相同,唯标记物为非放射性而能产生荧光的镧系元素[铕(Eu)铽(Tb)钐(Sm)镝(Dy)]。这些镧系元素的螯合物可以与抗原或抗体结合,在紫外线激发下可产生一段时间的荧光,采取延迟时间测定镧系元素的荧光,可以完全排除本底的干扰,所以称为时间分辨荧光免疫分析。
本法的特点是灵敏度高,特异性强,重复性好,人为误差小,且与上述诸法最大不同点是上述诸法的自动化均为非兼容性,只能应用本机指定的试剂盒,而时间分辨荧光免疫分析自动仪为兼容性,可使用其他厂商的各种时间分辨荧光分析试剂盒,故有良好的发展前进。
九、放射免疫分析与非放射性标记免疫分析法的比较
放射免疫分析历经了40年的研究和应用,其特异性、灵敏度、精密度和准确性均达到较高的技术指标。在此基础上发展起来的非放射性免疫标记分析具有放射免疫分析相似的优点,而且又排除了放射性污染等缺点,弥补了不能自动化分析的不足,因而深受医技人员的青睐。但目前各种非放射性标记免疫自动化分析,多应用于样本量较大的各项常规测定,对于各种特殊项目的测定和科研项目的新建,仍然有赖于放射免疫分析。放射免疫分析和非放射标记分析的技术性能比较见表2.
体外标记免疫分析技术应用范围十分广泛。包括蛋白质、激素、药物、肿瘤标志物、病毒抗原等的测定。其临床上常用的检测项目及主要应用可见教科书P59-P60.其中最主要的是各种激素和肿瘤标志物。
激素的作用很重要但血中含量极微,在放射免疫分析建立以前,激素的测定很难实现,而现在大多数激素项目都已可常规测定,,诸如脑垂体-甲状腺轴,脑垂体-生殖腺轴,脑垂体-肾上腺轴的各项激素测定都已普及至区级医疗机构,难以检测的胃肠道激素也已被测定和做详尽的研究。而目前最被关注的各种肿瘤标志物测定,已被列入于体格检查的保健项目。
十一、肿瘤标志物的测定
凡可以特异于癌细胞产生的物质都被归类为肿瘤标志物。其主要分类可有癌胚抗原类、糖类抗原类、肿瘤相关抗原类、同功酶类、宿主反应标志物类、激素和其他类,其中目前最常用的是癌胚抗原类的AFP、CEA、各种糖类抗原和前列腺特异性抗原等。
肿瘤标志物测定的应用有四:1.辅助临床诊断 2.观察治疗反应 3.检测复发、转移和预后 4。肿瘤高发地区普查。当前国际上的应用,则以观察治疗反应和监控复发、转移为主。
肿瘤标志物有广谱和针对性较强的区别,详见表3
由某些良性病变所引起,也屡发现不明原因的假性升高(经长期随访而证实)对此必须注意并结合其他检查综合分析之。
(朱翠英)