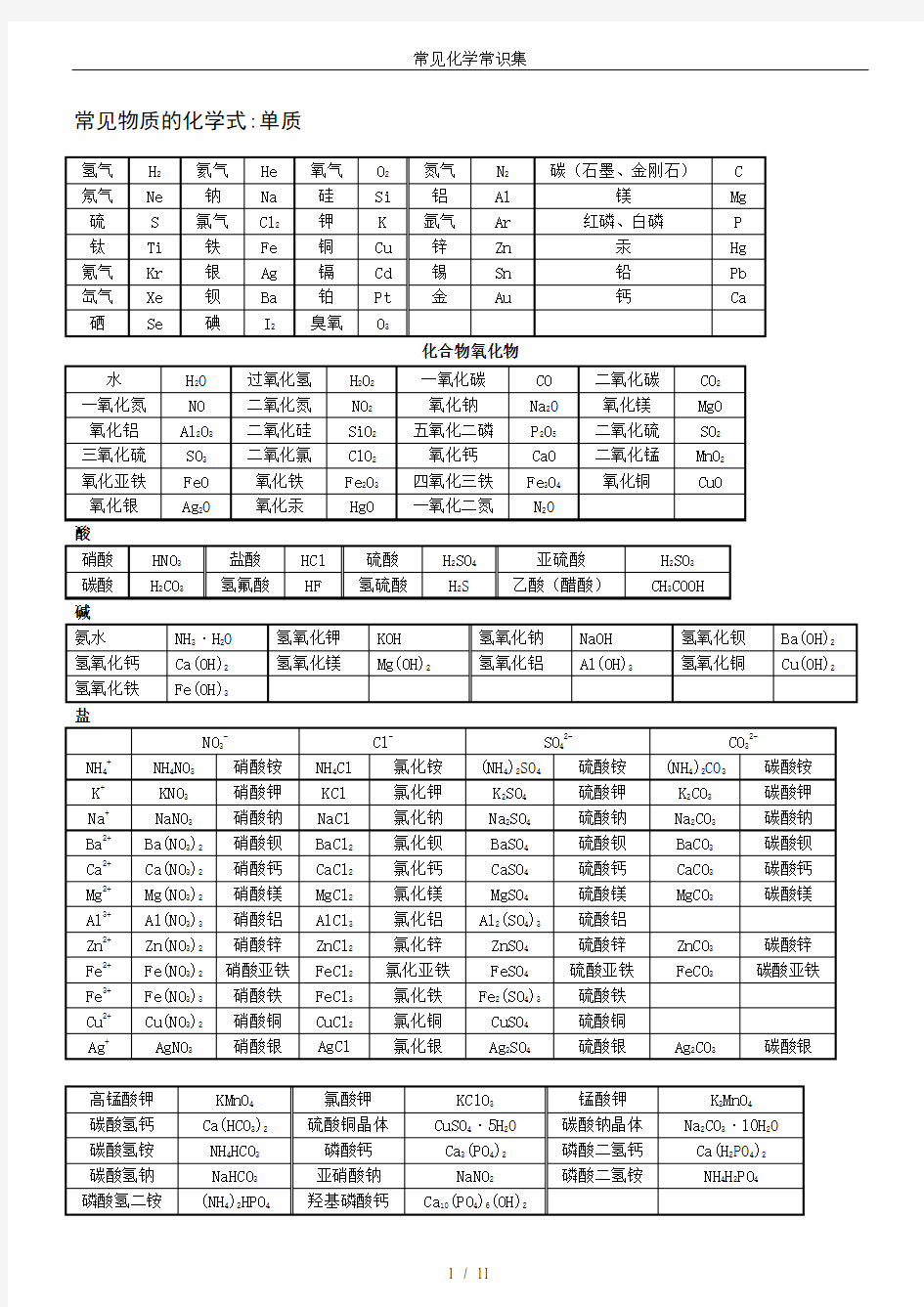

常见物质的化学式:单质
化合物氧化物
酸
盐
有机物
其他:氨气NH3
常见物质的俗名
常见的化学方程式
说明:用楷体标示的内容不是重点。
化合反应
●红磷在空气中燃烧,产生白烟:4P+5O22P2O5
白磷自燃:4P+5O2=2P2O5
●木炭充分燃烧:C+O2CO2
●木炭不充分燃烧:2C+O22CO
●硫在空气(氧气)中燃烧:S+O2SO2
●铁丝在氧气中燃烧:3Fe+2O2Fe3O4
●铝在氧气中燃烧:4Al+3O22Al2O3
铝不易生锈的原因:4Al+3O2=2Al2O3
●镁在空气中燃烧:2Mg+O22MgO
●铜在空气中加热:2Cu+O22CuO
●氢气在氧气中燃烧:2H2+O22H2O
●将CO2变成CO:C+CO22CO
●二氧化碳溶于水形成碳酸:CO2+H2O=H2CO3
●用生石灰制取熟石灰:CaO+H2O=Ca(OH)2
●一氧化碳燃烧:2CO+O22CO2
●向澄清的石灰水中通入过量的二氧化碳,变浑浊的石灰水又变澄清:CaCO3+CO2+H2O=Ca(HCO3)2●氢气在氯气中燃烧:H2+Cl22HCl
钠在氯气中燃烧:2Na+Cl22NaCl
镁在氮气中燃烧:3Mg+N2Mg3N2(注意氮元素的化合价)
上面三个化学方程式给我们的启示是:燃烧不一定有氧气参与。
分解反应
●汞在空气中加热:2Hg+O22HgO
●氧化汞加强热:2HgO2Hg+O2↑
●分解过氧化氢制取氧气(实验室制取氧气的反应原理之一):2H2O22H2O+O2↑
加热高锰酸钾制取氧气(实验室制取氧气的反应原理之一):2KMnO4K2MnO4+MnO2+O2↑
加热氯酸钾制取氧气(实验室制取氧气的反应原理之一):2KClO32KCl+3O2↑
分解过氧化氢制取氧气符合绿色化学的观念,是三种方案中最安全、最节约资源的一种。
●电解水生成氢气和氧气:2H2O2H2↑+O2↑
●工业制取生石灰和CO2的反应原理:CaCO3CaO+CO2↑
●干粉灭火器的反应原理(碳酸氢钠受热分解):2NaHCO3Na2CO3+H2O+CO2↑
●碱式碳酸铜受热分解:Cu2(OH)2CO32CuO+H2O+CO2↑
●过氧化氢溶液不稳定,发生分解:2H2O2=2H2O+O2↑
●碳酸不稳定,分解成水和二氧化碳:H2CO3=H2O+CO2↑
●碳铵(碳酸氢铵)“消失”并发出刺激性气味:NH4HCO3=NH3↑+CO2↑+H2O
●石笋、钟乳石的形成过程:CaCO3+CO2+H2O=Ca(HCO3)2 Ca(HCO3)2=CaCO3↓+CO2↑+H2O
置换反应
●氢气还原氧化铜:H2+CuO Cu+H2O
●木炭还原氧化铜:C+2CuO2Cu+CO2↑
●木炭还原氧化铁:3C+2Fe2O34Fe+3CO2↑
●水煤气的形成:C+H2O H2+CO(注意没有气体生成符号↑)
●实验室制取氢气的反应原理:Zn+H2SO4=ZnSO4+H2↑
●金属与稀盐酸的反应
?2X+2HCl=2X Cl+H2↑(X是+1价的金属,包括K、Na)
?X+2HCl=X Cl2+H2↑(X是+2价的金属,包括Ca、Mg、Zn、Fe)
?2Al+6HCl=2AlCl3+3H2↑
●金属与稀硫酸的反应
?2X+H2SO4=X2SO4+H2↑(X是+1价的金属,包括K、Na)
?X+H2SO4=X SO4+H2↑(X是+2价的金属,包括Ca、Mg、Zn、Fe)
?2Al+3H2SO4=Al2(SO4)3+3H2↑
●金属与盐溶液的反应
?镁
◆3Mg+2AlCl3=3MgCl2+2Al
3Mg+Al2(SO4)3=3MgSO4+2Al
3Mg+2Al(NO3)3=3Mg(NO3)2+2Al
◆Mg+X Cl2=MgCl2+X(X是+2价的金属,包括Zn、Fe、Cu)
◆Mg+X SO4=MgSO4+X(X是+2价的金属,包括Zn、Fe、Cu)
◆Mg+X(NO3)2=Mg(NO3)2+X(X是+2价的金属,包括Zn、Fe、Cu)
◆Mg+2AgNO3=Mg(NO3)2+2Ag
?铝
◆2Al+3X Cl2=2AlCl3+3X(X是+2价的金属,包括Zn、Fe、Cu)
◆2Al+3X SO4=Al2(SO4)3+3X(X是+2价的金属,包括Zn、Fe、Cu)
◆2Al+3X(NO3)2=2Al(NO3)3+3X(X是+2价的金属,包括Zn、Fe、Cu)
◆Al+3AgNO3=Al(NO3)3+3Ag
?锌
◆Zn+X Cl2=ZnCl2+X(X是+2价的金属,包括Fe、Cu)
◆Zn+X SO4=ZnSO4+X(X是+2价的金属,包括Fe、Cu)
◆Zn+X(NO3)2=Zn(NO3)2+X(X是+2价的金属,包括Fe、Cu)
◆Zn+2AgNO3=Zn(NO3)2+2Ag
?铁
◆Fe+CuCl2=FeCl2+Cu
◆Fe+CuSO4=FeSO4+Cu
◆Fe+Cu(NO3)3=Fe(NO3)3+Cu
◆Fe+2AgNO3=Fe(NO3)2+2Ag
?铜:Cu+2AgNO3=Cu(NO3)2+2Ag
?K、Ca、Na不遵循这样的置换反应,它们与盐溶液反应时,会先和水反应生成对应的碱,然后再和盐溶
液反应。如:2Na+2H2O=2NaOH+H2↑NaOH+CuSO4=Na2SO4+Cu(OH)2↓
●镁在二氧化碳中燃烧:2Mg+CO22MgO+C
●水蒸气与铁在高温的条件下反应:3Fe+4H2O Fe3O4+4H2(注意没有气体生成符号↑)
复分解反应
●NaOH溶液与稀盐酸反应:NaOH+HCl=NaCl+H2O
●NaOH溶液与稀硫酸反应:2NaOH+H2SO4=Na2SO4+2H2O
●Ba(OH)2溶液与稀硫酸反应:Ba(OH)2+H2SO4=BaSO4↓+2H2O
●用胃舒平(氢氧化铝)中和过多的胃酸:Al(OH)3+3HCl=AlCl3+3H2O
●用氢氧化镁中和过多的胃酸:Mg(OH)2+2HCl=MgCl2+2H2O
●用熟石灰中和含有硫酸的污水:Ca(OH)2+H2SO4=CaSO4+2H2O
●稀盐酸除铁锈:Fe2O3+6HCl=2FeCl3+3H2O
●稀硫酸除铁锈:Fe2O3+3H2SO4=Fe2(SO4)3+3H2O
●稀盐酸与氧化铜反应:CuO+2HCl=CuCl2+H2O
●稀硫酸与氧化铜反应(制取CuSO4):CuO+H2SO4=CuSO4+H2O
●提示:CaO、Na2O、K2O、BaO可以直接和酸反应。
●实验室制取CO2的反应原理:CaCO3+2HCl=CaCl2+H2O+CO2↑
●盐酸与水垢中的主要成分发生反应:CaCO3+2HCl=CaCl2+H2O+CO2↑
●实验室不用大理石和稀硫酸制取CO2的原因:CaCO3+H2SO4=CaSO4+H2O+CO2↑
●泡沫灭火器的反应原理:Na2CO3+2HCl=2NaCl+H2O+CO2↑
●误食碳酸钡后发生中毒的原因:BaCO3+2HCl=BaCl2+H2O+CO2↑
●用小苏打治疗胃酸过多:NaHCO3+HCl=NaCl+H2O+CO2↑
●硝酸银溶液与稀盐酸反应:AgNO3+HCl=HNO3+AgCl↓
●钡盐与稀硫酸反应:
Ba(NO3)2+H2SO4=2HNO3+BaSO4↓BaCl2+H2SO4=2HCl+BaSO4↓BaCO3+H2SO4=BaSO4↓+H2O+CO2↑
●硫酸和碱式碳酸铜反应:Cu2(OH)2CO3+2H2SO4=2CuSO4+2H2O+CO2↑
●工业制取烧碱:Ca(OH)2+Na2CO3=2NaOH+CaCO3↓
●氯化铵与氢氧化钠溶液反应:NH4Cl+NaOH=NaCl+NH3↑+H2O
●硫酸铵与氢氧化钠溶液反应:(NH4)2SO4+2NaOH=Na2SO4+2NH3↑+2H2O
●将熟石灰与氯化铵两种固体一起研磨,闻到刺激性气味:2NH4Cl+Ca(OH)2=CaCl2+2NH3↑+2H2O
●将熟石灰与硫酸铵两种固体一起研磨,闻到刺激性气味:(NH4)2SO4+Ca(OH)2=CaSO4+2NH3↑+2H2O
●生成蓝色沉淀的反应:CuSO4+2NaOH=Cu(OH)2↓+Na2SO4(参加反应的碱只能是四大强碱)
●生成红褐色沉淀的反应:FeCl3+3NaOH=Fe(OH)3↓+3NaCl(参加反应的碱只能是四大强碱)
●生成白色沉淀的反应:MgCl2+2NaOH=Mg(OH)2↓+2NaCl(生成物只能是弱碱)
●生成白色沉淀的反应:MgSO4+Ba(OH)2=Mg(OH)2↓+BaSO4↓(硫酸盐与氢氧化钡反应)
●生成蓝白沉淀的反应:CuSO4+Ba(OH)2=Cu(OH)2↓+BaSO4↓
●生成红白沉淀的反应:Fe2(SO4)3+3Ba(OH)2=2Fe(OH)3↓+3BaSO4↓
●配制波尔多液时发生的反应:CuSO4+Ca(OH)2=CaSO4+Cu(OH)2↓
●误食BaCO3或BaCl2发生中毒之后,要服用泻盐(MgSO4)解毒:BaCl2+MgSO4=MgCl2+BaSO4↓
●其他常见的反应:
?NaCl+AgNO3=NaNO3+AgCl↓
?CaCl2+Na2CO3=2NaCl+CaCO3↓(CaCl2可以换成Ca(NO3)2,Na2CO3可以换成K2CO3)
?BaCl2+Na2CO3=2NaCl+BaCO3↓(BaCl2可以换成Ba(NO3)2,Na2CO3可以换成K2CO3)
?BaCl2+Na2SO4=2NaCl+BaSO4↓(BaCl2可以换成Ba(NO3)2,Na2SO4可以换成K2SO4)
●证明NaOH变质的三种方法:
?Na2CO3+2HCl=2NaCl+H2O+CO2↑
?Na2CO3+Ca(OH)2=2NaOH+CaCO3↓
?Na2CO3+CaCl2=2NaCl+CaCO3↓
Na2CO3+Ca(NO3)2=2NaNO3+CaCO3↓
●证明NaOH部分变质(先用下面的方法除去Na2CO3,然后向溶液中滴加酚酞,如果溶液变红说明NaOH部分变
质):
?Na2CO3+CaCl2=2NaCl+CaCO3↓
?Na2CO3+Ca(NO3)2=2NaNO3+CaCO3↓
●证明Ca(OH)2变质的方法:CaCO3+2HCl=CaCl2+H2O+CO2↑
●证明Ca(OH)2部分变质的方法(取两份相同的样品,分别按以下方法做)
?证明Ca(OH)2变质:CaCO3+2HCl=CaCl2+H2O+CO2↑
?证明还有Ca(OH)2存在:Ca(OH)2+2NH4Cl=CaCl2+2H2O+2NH3↑
●证明CaO部分变质的方法(取三份相同的样品,分别按以下方法做):
?证明CaO仍然存在:CaO+H2O=Ca(OH)2
?证明CaCO3的存在:CaCO3+2HCl=CaCl2+H2O+CO2↑
?证明Ca(OH)2的存在:Ca(OH)2+2NH4Cl=CaCl2+2H2O+2NH3↑
非基本类型
●一氧化碳还原氧化铜(检验一氧化碳的反应原理):CO+CuO Cu+CO2
●一氧化碳还原氧化铁(用赤铁矿炼铁、高炉炼铁的反应原理):3CO+Fe2O 32Fe+3CO2
●一氧化碳还原氧化亚铁:CO+FeO Fe+CO2
●一氧化碳还原四氧化三铁(用磁铁矿炼铁):4CO+Fe3O 43Fe+4CO2
●黑火药点燃爆炸:S+2KNO3+3C K2S+N2↑+3CO2↑
●甲烷充分燃烧:CH4+2O 2CO2+2H2O
●甲烷不充分燃烧:2CH4+3O 22CO+4H2O
●乙醇充分燃烧:C2H5OH+3O 22CO2+3H2O
●乙醇不充分燃烧:C2H5OH+2O 22CO+3H2O
●二氧化碳使澄清的石灰水变浑浊(Ca(OH)2固体变质的原因):Ca(OH)2+CO2=CaCO3↓+H2O
●用NaOH溶液吸收CO2(NaOH固体变质的原因):2NaOH+CO2=Na2CO3+H2O
●用NaOH溶液吸收SO2:2NaOH+SO2=Na2SO3+H2O
●NaOH溶液与SO3反应:2NaOH+SO3=Na2SO4+H2O
●葡萄糖的缓慢氧化:C6H12O6+6O 26CO2+6H2O
2CO
2SO
22P
2
2Fe
22Al
22MgO
22CuO
22HgO
22CO
2Hg+O
2
2H
2
Cu+H
2Cu+CO
Cu+CO
32Fe+3CO
描述实验现象时要注意不能说出生成物的名称,但可以根据生成物的化学性质来描述生成物。
常见物质的颜色、气味
固体
●红色:红磷P、铜Cu、氧化铁Fe2O3、氧化汞HgO
●红褐色:氢氧化铁Fe(OH)3
●黄色:金Au、硫S
●绿色:碱式碳酸铜Cu2(OH)2CO3
●紫黑色:高锰酸钾晶体KMnO4
●淡蓝色:固态氧O2
●蓝色:氢氧化铜Cu(OH)2、硫酸铜晶体CuSO4·5H2O
●银白色:大多数金属(铁Fe、银Ag、铝Al、锌Zn、镁Mg……)
●黑色:木炭C、铁粉Fe、氧化铜CuO、二氧化锰MnO2、四氧化三铁Fe3O4、氧化亚铁FeO等
●深灰色:石墨C
●灰白色:大多数磷肥
●无色:金刚石C、干冰CO2、冰H2O
●白色:除了上述固体之外,我们学过的其他固体、固体粉末或晶体基本上都是白色的。
●有刺激性气味的固体:碳酸氢铵NH4HCO3
液体
●淡蓝色:液态氧O2
●蓝色:含有Cu2+的溶液
●浅绿色:含有Fe2+的溶液
●黄色:含有Fe3+的溶液
●银白色:汞Hg
●我们学过的大多数液体都是无色的。
●有特殊气味的液体:乙醇C2H5OH
●有刺激性气味的液体:醋酸CH3COOH
气体
●红棕色气体:二氧化氮NO2
●有毒的气体:一氧化碳CO、氯化氢HCl、氨气NH3、二氧化硫SO2、二氧化氮NO2等
●有刺激性气味的气体:氯化氢HCl、氨气NH3、二氧化硫SO2、二氧化氮NO2等
●我们学过的大多数气体都是无色无味的。
●计入空气污染指数的项目:二氧化硫SO2、一氧化碳CO、二氧化氮NO2、可吸入颗粒物和臭氧O3等
●能产生温室效应的气体:二氧化碳O2、臭氧O3、甲烷CH4、氟氯代烷等
多功能瓶
下面是多功能瓶的常见用途:
一、洗气瓶(图①)
多功能瓶作为洗气瓶来使用时,气体要从长导管进入,从短导管中出去。洗气瓶一般用来检验气体(如二氧化碳)、干燥气体(如混有水蒸气的气体)、吸收气体(如二氧化硫)或除去气体中的杂质(如HCl气体等)
●检验气体:检验二氧化碳的试剂是澄清的石灰水。
●干燥气体:试剂一般是浓硫酸。需要注意的是,浓硫酸不能干燥NH3等碱性气体。
●吸收气体或除去气体中的杂质:
①对于SO2、CO2等气体,可以使用NaOH溶液吸收(最好不用Ca(OH)2溶液,因为Ca(OH)2微溶于水)
②对于混在CO2中的HCl气体,不可以使用NaOH溶液吸收,但可以使用NaHCO3溶液来吸收。
③ Cl2可以用NaOH溶液吸收。
二、向上排空气取气瓶(图②)
使用条件:收集的气体的密度大于空气密度(组成气体的分子的相对分子质量大于29),并且气体不与空气中的成分反应。
规则:长管进,短管出。
常见实例:O2、CO2、Cl2、NO2
利用多功能瓶收集有毒或者有污染气体,可以方便地进行尾气处理,以免气体逸出污染空气。
如Cl2可以用②装置收集,再用①装置进行尾气处理。
三、向下排空气取气瓶
使用条件:收集的气体的密度小于空气密度(组成气体的分子的相对分子质量小于29),并且气体不与空气中的成分反应。
规则:短管进,长管出。
常见实例:H2、NH3
四、排水集气瓶
使用条件:①气体不溶或难溶于水;②气体不与水反应;(③对于部分气体来说,密度与空气密度接近,无法用排空气法收集。)
规则:短管进,长管出。
常见实例:O2、H2、NO
五、排水量气瓶
使用条件:同“四”
规则:短管进,长管出。
如果忽略导管内的水,量筒内水的体积就是进入集气瓶中气体的体积。
除杂
●除杂的原则:① 主要成分的质量不能减少(可以增多);② 除杂时不能引进新的杂质。
●除去CuO中的C:在氧气流中灼烧(C+O2CO2)。
●除去CO中的CO2:使混合气体通过澄清的石灰水或氢氧化钠溶液
(Ca(OH)2+CO2=CaCO3↓+H2O和2NaOH+CO2=Na2CO3+H2O)。
●除去CO2中的CO:使混合气体通过灼热的氧化铜(CO+CuO Cu+CO2)。
●除去CaO中的CaCO3:高温煅烧(CaCO3CaO+CO2↑)
【注意】不能加稀盐酸,因为CaO能与稀盐酸中的水反应生成Ca(OH)2。
●除去大理石中的杂质:
① 高温煅烧大理石或石灰石(CaCO3CaO+CO2↑);
② 将反应后的固体放入足量的水中,使其充分溶解,过滤(CaO+H2O=Ca(OH)2);
③ 通入过量的二氧化碳(Ca(OH)2+CO2=CaCO3↓+H2O);
④ 过滤。
【注意】如果杂质很难用一般方法除去,可以将主要成分从混合物中分离出来,然后通过反应再变回来。●除去Cu中少量的Fe:
物理方法——用磁铁反复吸引。
化学方法——滴加稀盐酸或稀硫酸,然后过滤。
【注意】不能加硫酸铜溶液,否则容易导致除杂不彻底。
●除去FeSO4溶液中的CuSO4:①加入铁粉(铁丝);②过滤。
●除去可溶物中的不溶物:①溶解;②过滤;③蒸发结晶。
●除去不溶物中的可溶物:①溶解;②过滤。
●将两种可溶物分离:见“溶液”单元的冷却热饱和溶液法和蒸发溶剂结晶法。
●在溶液中,杂质有盐的时候,可以考虑把盐变成水、气体沉淀。
鉴定
●氧气的鉴定方法:把一根带火星的木条伸入集气瓶中,如果带火星的木条复燃,证明是氧气。
●氢气:点燃,气体会发出淡蓝色火焰。如果气体较纯,气体将会安静地燃烧,并发出“噗”声;如果气体不
纯,会发出尖锐爆鸣声。
●二氧化碳:把气体通入澄清的石灰水中,如果澄清的石灰水变浑浊,就证明收集的气体是CO2。
●三大可燃性气体的鉴定:点燃,通过无水硫酸铜CuSO4,再通过澄清的石灰水(顺序不能颠倒!)
H2:生成物能使无水硫酸铜变蓝,但不能使澄清石灰水变浑浊。
CO:生成物不能使无水硫酸铜变蓝,但能使澄清的石灰水变浑浊。
CH4:生成物既能使无水硫酸铜变蓝,又能使澄清石灰水变浑浊。
【注意】不可以根据气体燃烧时的火焰颜色来鉴别气体。
●水的鉴定:如果液体能使无水硫酸铜变蓝,说明液体中含有水。
●碳酸根的鉴定:加盐酸,然后将产生的气体通入澄清石灰水。如果澄清的石灰水变浑浊,说明有碳酸根离子。
●鉴定CaO是否含CaCO3也加盐酸。
●鉴定Cl-:先加入AgNO3溶液,再加入稀硝酸。如果有沉淀生成,说明含有Cl-。
●鉴定SO42-:先加入Ba(NO3)2溶液,再加入稀硝酸。如果有沉淀生成,说明含有SO42-。
●鉴定CO32-:加入稀盐酸,将产生的气体通入澄清的石灰水中,如果澄清的石灰水变浑浊,说明含有CO32-。
●鉴定HCO3-:同上。
●鉴定Cu2+:加入NaOH溶液,如果有蓝色沉淀,说明含有Cu2+。
●鉴定Fe3+:加入NaOH溶液,如果有红褐色沉淀,说明含有Fe3+。
●鉴定H+:
① 借助石蕊或pH试纸。如果石蕊变红或用pH试纸测出的pH值小于7,说明含有H+。
② 加入碳酸盐(如CaCO3),将产生的气体通入澄清的石灰水中,如果澄清的石灰水变浑浊,说明含有H+。
③ 加入活泼金属,如果金属表面产生气泡,并且产生一种可燃性气体(点燃之后安静燃烧,发出淡蓝色火
焰。如果气体不纯,会发出尖锐的爆鸣声),说明含有H+。
④ 加入Fe2O3(铁锈),如果铁锈逐渐溶解消失,溶液由无色变成黄色,说明含有H+。
⑤ 加入弱碱,如果弱碱逐渐溶解消失(如果加入Fe(OH)2、Fe(OH)3、Cu(OH)2,溶液的颜色还会发生变化),
说明含有H+。
●鉴定OH-:
① 借助石蕊、酚酞或pH试纸。如果石蕊变蓝、酚酞变红或用pH试纸测出的pH值大于7,说明含有OH-。
② 加入CuSO4,如果出现蓝色沉淀,说明含有OH-。
③ 加入Fe2(SO4)3,如果出现红褐色沉淀,说明含有OH-。
④ 可以参考“碱的通性”中的第四条,使溶液中有气体或沉淀生成。
●鉴定水:通过白色的硫酸铜,如果硫酸铜变蓝,说明有水(CuSO4 + 5H2O = CuSO4·5H2O)
如果要鉴定多种物质,必须把鉴定水放在第一步。如果除水,必须放在最后一步。
●鉴定二氧化碳:通入澄清的石灰水中,如果澄清的石灰水变浑浊,说明气体是CO2。
●鉴定一氧化碳:通过灼热的氧化铜,如果黑色粉末逐渐变成红色,并且产生的气体能使澄清的石灰水变浑浊,
说明气体是CO。
●鉴定NH4+:以氯化铵(NH4Cl)为例,
方法一 NH4Cl + NaOH = NaCl + NH3↑+ H2O;
方法二把NH4Cl和Ca(OH)2混在一起研磨。
如果闻到刺激性的氨味,或者能使红色的石蕊试纸变蓝,说明是铵态氮肥。
●蛋白质的鉴定:点燃,如果有烧焦羽毛的气味,就说明有蛋白质。
●鉴别聚乙烯塑料和聚氯烯塑料(聚氯烯塑料袋有毒,不能装食品):
点燃后闻气味,有刺激性气味的为聚氯烯塑料。
●鉴别羊毛线和合成纤维线:
物理方法:用力拉,易断的为羊毛线,不易断的为合成纤维线;
化学方法:点燃,产生焦羽毛气味,不易结球的为羊毛线;无气味,易结球的为合成纤维线。
区分与鉴定的区别在于,鉴定是要确定一种物质,而区分只需把物质分辨开。区分的要求是无论用什么试剂,采取什么方法,现象必须明显。