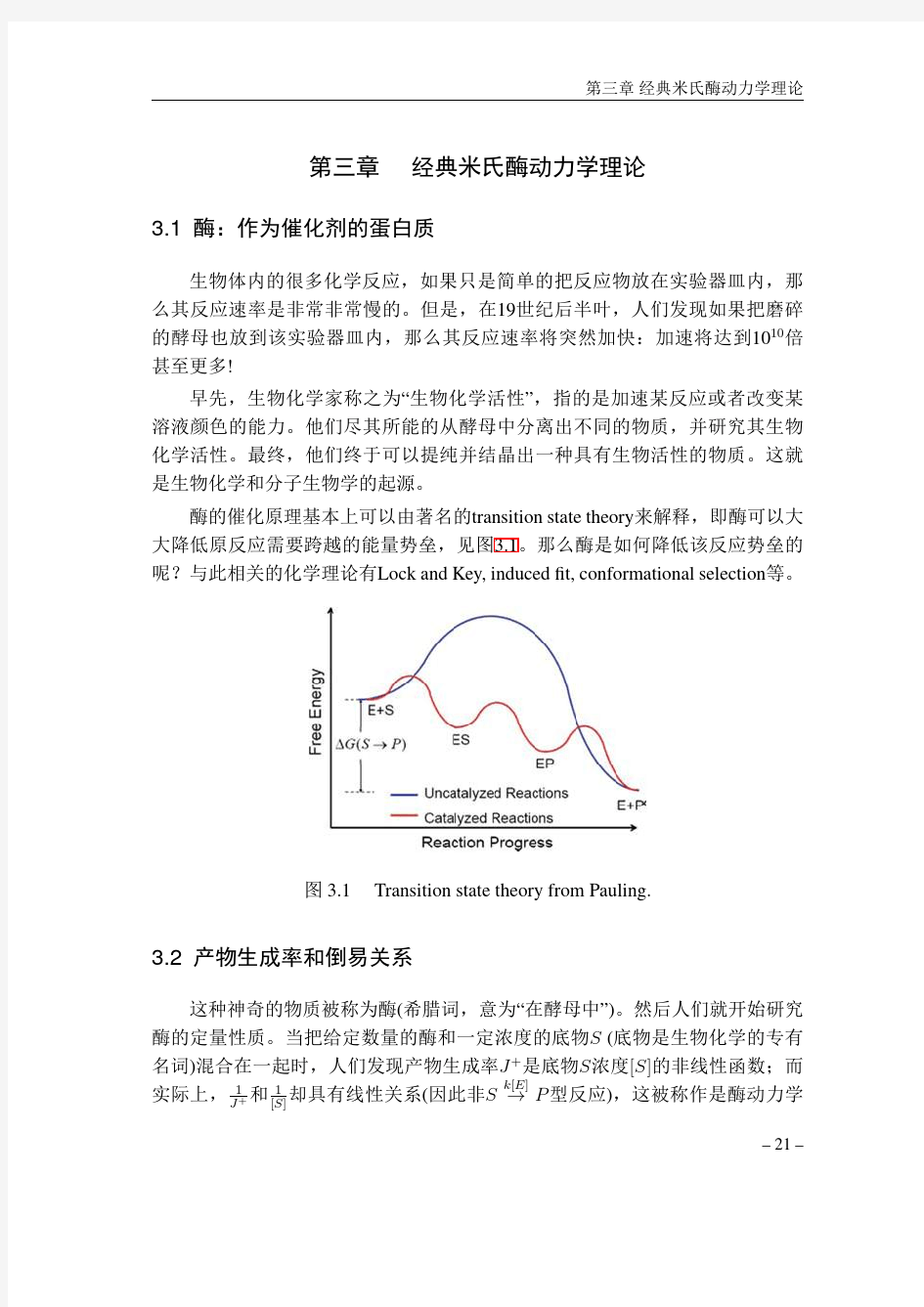

酶动力学综合实验 实验(一)——碱性磷酸酶Km值的测定 【目的要求】 1.了解底物浓度对酶促反应速度的影响 2.了解米氏方程、Km值的物理意义及双倒数作图求Km值的方法。 【实验原理】 1、碱性磷酸酶: 碱性磷酸酶是广泛分布于人体各脏器器官中,其中以肝脏为最多。其次为肾脏、骨骼、肠和胎盘等组织。但它不是单一的酶,而是一组同功酶。本实验用的碱性磷酸酶是从大肠杆菌中提取的。 2、米氏方程: Michaelis-Menten 在研究底物浓度与酶促反应速度的定量关系时,导出了酶促反应动力学的基本公式,即: 错误!未找到引用源。(1) 式中:v表示酶促反应速度, 错误!未找到引用源。表示酶促反应最大速度, [S]表示底物浓度, 错误!未找到引用源。表示米氏常数。 3、错误!未找到引用源。值的测定主要采用图解法,有以下四种: ①双曲线作图法(图1-1,a) 根据公式(1),以v对[s]作图,此时1/2错误!未找到引用源。时的底物浓度[s]值即为Km值,以克分子浓度(M)表示。这种方法实际上很少采用,因为在实验条件下的底物浓度很难使酶达到饱和。实测错误!未找到引用源。一个近似值,因而1/2错误!未找到引用源。不精确。此外由于v对[S]的关系呈双曲线,实验数据要求较多,且不易绘制。 ②Lineweaver- Burk作图法双倒数作图法(图1-1,b) 实际工作中,常将米氏方程(式(1))作数学变换,使之成为直线形式,测定要方便、精确得多。其中之一即取(1)式的倒数,变换为Lineweaver- Burk方程式:错误!未找到引用源。(2) 以错误!未找到引用源。对错误!未找到引用源。作图,即为y=ax+b形式。此时斜率为错误!未找到引用源。,纵截距为错误!未找到引用源。。把直线外推与横轴相交,其截距相交,其截距即为—错误!未找到引用源。。 ③Hofstee作图法(略) 把(2)式等号两边乘以错误!未找到引用源。,得: 错误!未找到引用源。(3) 以v对错误!未找到引用源。作图,这时斜率为错误!未找到引用源。,纵截距
血流动力监测各指标及临床意义 血流动力学监测的每个参数都有他的临床意义,怎样结合其它参数或临床等等都是我们应该掌握和经常思考的,而且只有在临床中不断运用、思考才能真正理解这些参数。本文介绍了直接测量所得指标:上肢动脉血压、心率、中心静脉压、右心房压、右心室压、肺动脉压、肺毛细血管嵌顿压、心输出量。由直接测量指标所派生的指标:心脏排血指数、心脏搏出量、肺血管阻力、心室做功指数和PICCO参数:血管外肺水、胸血容量。介绍了临床应用于判断左心功能、疾病的鉴别、心功能状态的治疗原则、指导疾病的治疗等。供大家参考。 1、主要监测指标 1.1直接测量所得指标 1.1.1上肢动脉血压(AP) 正常值:收缩压1 2.0~18.7kPa(90~140mmHg),舒压8.0~12.0kPa(60~90mmHg)。心排量、全身血管阻力、大动脉壁弹性、循环容量及血液粘度等均可影响动脉血压。一般用袖带血压计测量。在休克或体循环直视心脏手术时,应以桡动脉穿刺直接测量为准[1]。血压是反应心排量水平和保证器官有效灌注的基础,过高时增大左室后负荷和心肌耗氧,过低不能保证重要器官有效灌注。当MAP低于75mmHg 时,心肌供血曲线变陡下降,因此,MAP75~80mmHg,是保证心肌供血大致正常的最低限度[2]。对原有高血压病人,合理的MAP应略高于此。 1.1.2心率(HR)正常值:60~100次/min。反映心泵对代改变、应激反应、容量改变、心功能改变的代偿能力。心率适当加快有助于心输出量的增加,<50次/min或>160次/min,心输出量会明显下降[3]。 1.1.3中心静脉压(CVP)正常值:0.49~1.18kPa(5~12cmH20)。体循环血容量改变、右心室射血功能异常或静脉回流障碍均可使CVP发生变化,胸腔、腹腔压变化亦可影响
酶促反应动力学实验报告 杨恩原 实验目的: 1.观察底物浓度对酶促反应速度的影响 2.观察抑制剂对酶促反应速度的影响 3.掌握用双倒数作图法测定碱性磷酸酶的Km值 实验原理: 一、底物浓度对酶促反应速度的影响 在温度、pH及酶浓度恒定的条件下,底物浓度对酶的催化作用有很大的影响。在一般情况下,当底物浓度很低时,酶促反应的速度(v)随底物浓度[S]的增加而迅速增加,但当底物浓度继续增加时,反应速度的增加率就比较小,当底物浓度增加到某种程度时反应速度达到一个极限值(即最大速度Vmax)。底物浓度和反应速度的这种关系可用米氏方程式来表示(Michaelis-Menten方程)即: 式中Vmax为最大反应速度,Km为米氏常数,[S]为底物浓度 当v=Vmax/2时,则Km=[S],Km是酶的特征性常数,测定Km是研究酶的一种重要方法。但是在一般情况下,根据实验结果绘制成的是直角双曲线,难以准确求得Km和Vmax。若将米氏方程变形为双倒数方程(Lineweaver-Burk方程),则此方程为直角方程,即: 以1/V和1/[S]分别为横坐标和纵坐标。将各点连线,在横轴截距为-1/Km,据此可算出Km值。
本实验以碱性磷酸酶为例,测定不同浓度底物时的酶活性,再根据1/v和1/[S]的倒数作图,计算出其Km值。 二、抑制剂对酶促反映的影响 凡能降低酶的活性,甚至使酶完全丧失活性的物质,成为酶的抑制剂。酶的特异性抑制剂大致上分为可逆性和不可逆性两类。可逆性抑制又可分为竞争性抑制和非竞争性抑制等。竞争性抑制剂的作用特点是使该酶的Km值增大,但对酶促反映的最大速度Vmax值无影响。非竞争性抑制剂的作用特点是不影响[S]与酶的结合,故其Km值不变,然而却能降低其最大速度Vmax。本实验选取Na2HPO4作为碱性磷酸酶的抑制物,确定其抑制作用属于哪种类型。 实验步骤: 实验一:底物浓度对酶促反应速度的影响 管号 试剂 1.取试管9支,将L基质液稀释成下列不同浓度:
第3章酶催化反应动力学 (2学时) 主要内容: 3.1 酶催化反应速度 3.2 底物浓度对酶促反应速度的影响 3.3 抑制剂对酶促反应速度的影响 3.4 其它因素对酶促反应速度的影响 ?酶催化反应动力学也称酶促反应动力学(kinetics of enzyme-catalyzed reactions),是研究酶促反应速度以及影响此速度的各种因素的科学。在研究酶的结构与功能的关系以及酶的作用机制时,需要酶促反应动力学提供相关的实验证据;为了找到最有利的反应条件从而提高酶催化反应的效率以及了解酶在代谢过程中的作用和某些药物的作用机制等,也需要我们掌握酶促反应动力学的相关规律。因此,对于酶促反应动力学的研究既有重要的理论意义又具有相当的实践价值。 酶的动力学研究包括哪些内容? ?酶促反应动力学以化学动力学为基础,通过对酶促反应速度的测定来讨论诸如底物浓度、抑制剂、温度、pH和激活剂等因素对酶促反应速度的影响。 ?温度、pH及激活剂都会对酶促反应速度产生十分重要的影响,酶促反应不但需要最适温度和最适pH,还要选择合适的激活剂。而且在研究酶促反应速度以及测定酶的活力时,都应选择相关酶的最适反应条件。 3.1酶催化反应速度 ?如果我们以产物生成量(或底物减少量)来对反应时间作图,便可以得到如图3-1所示的曲线图。 该曲线的斜率表示单位时间内产物生成量的变化,因此曲线上任何一点的斜率就是相应横坐标上时间点的反应速度。从图中的曲线可以看出在反应开始的一段时间内斜率几乎不变,然而随着反应时间的延长,曲线逐渐变平坦,相应的斜率也渐渐减小,反应速度逐渐降低,显然这时测得的反应速度不能代表真实的酶活力。 ?引起酶促反应速度随反应时间延长而降低的原因很多,如底物浓度的降低、产物浓度增加从而加速了逆反应的进行、产物对酶的抑制或激活作用以及随着反应时间的延长引起酶本身部分分子失活等等。因此在测定酶活力时,应测定酶促反应的初速度,从而避免上述各种复杂因素对反应速度的影响。由于反应初速度与酶量呈线性关系,因此可以用测定反应初速度的方法来测
“蛋白酶凝乳特性研究” 1.实验目的 通过研究胃蛋白酶、木瓜蛋白酶作用于脱脂乳的最适凝乳温度、最适pH值、以及金属离子对酶凝乳效果的影响,使学生掌握酶学研究的基本方法,从而掌握生物化工研究的一些基本理论和主要思路,为科研开发打下必要的基础。 2.实验原理 胃蛋白酶、木瓜蛋白酶等具有很强的蛋白质催化特性,又具有良好的凝乳特性。因脱脂乳含大量酪蛋白,木瓜蛋白酶的凝乳特性主要表现为随机切割精氨酶-苯丙氨酸的肽键,达到破坏蛋白质稳定的效果,进而发生凝乳。奶酪的生产以前主要利用牛凝乳酶达到凝乳效果,但牛凝乳酶主要是从小牛的第四胃中提取得来,其来源受到极大的限制,通过研究蛋白酶、木瓜蛋白酶的凝乳特性并对其进行优化,一定程度地缓解凝乳酶来源的紧缺状态。 3.实验材料、仪器和试剂 3.1实验材料优质脱脂乳 3.2实验药品和器皿
3.3试剂 (1)配制浓度为100g/L的脱脂乳1000ml,混匀后待用。(5组) (2)配制浓度为10g/L的木瓜蛋白酶液和浓度为2g/L胃蛋白酶溶液各500ml,混匀后待用。(5组) (3)配制0.1mol/L NaOH和0.1mol/L的HCl溶液各1000ml,用于调节溶液pH 值。(5组) 4.操作步骤 4.1木瓜蛋白酶(胃蛋白酶)凝乳活力的测定 取 5mL100g.L-1的脱脂乳,在65℃下保温5min,加入0.5mL10g.L-1的木瓜蛋白酶液(或胃蛋白酶液),迅速混合均匀,准确记录从加入酶液到乳液凝固的时间(s)。把40min凝固1mL100g.L-1的脱脂乳的酶量定义为一个索氏单位(Soxhletunit),并以相对活性(RU)表示各因素的影响效果。SU=(2400/T)×(5 / 0.5)。式中:T为凝乳时间(s) RU(%)=(各因素下SU / 最大SU)×100 4.2酶的最适凝乳温度的测定:分别在55,60,65,70, 75℃下测定酶凝乳活性。 4.3酶的热稳定性:酶液分别在55 ,60,65,70,75℃下处理10,30,60min后, 测定酶的凝乳活性。(上述温度对凝乳特性研究,可根据实际情况,缩小两个水平间的差距) 4.4 pH对酶凝乳效果的影响:用0.1mol/LHCl和0.1mol/L NaOH将100g/L的 脱脂乳的pH调到6.0,6.5,7,7.5,8在65℃下测定酶的凝乳活性。 4.5 酶对pH的稳定性:用0.1mol/L HCl和0.1moL/LNaOH将酶液调到pH为 4.0, 5.0, 6.0, 7.0, 8.0,室温下(约25℃)放置1h后,再将酶液pH调到6.0, 在65℃下测定酶的凝乳活性。(上述pH对凝乳特性研究,可根据实际情况,缩小两个水平间的差距) 4.6 NaCl对酶活的影响:在酶液中添加0.2,0.5,0.8,1.1,1.5 (%)浓度的NaCl 溶液,分别测定酶的凝乳活性。 4.7 Ca2+、Mg2+、K+对酶凝乳效果的影响:在乳液中添加CaCl 2,MgCl 2 、KCl使其 含量分别为0.2,0.5,0.8, 1.1,1.4 (%),然后测定酶的凝乳活性。(上述离子对凝乳特性研究,可根据实际情况,缩小两个水平间的差距)
酶促反应动力学实验报告 14301050154 杨恩原 实验目的: 1.观察底物浓度对酶促反应速度的影响 2.观察抑制剂对酶促反应速度的影响 3.掌握用双倒数作图法测定碱性磷酸酶的Km值 实验原理: 一、底物浓度对酶促反应速度的影响 在温度、pH及酶浓度恒定的条件下,底物浓度对酶的催化作用有很大的影响。在一般情况下,当底物浓度很低时,酶促反应的速度(v)随底物浓度[S]的增加而迅速增加,但当底物浓度继续增加时,反应速度的增加率就比较小,当底物浓度增加到某种程度时反应速度达到一个极限值(即最大速度Vmax)。底物浓度和反应速度的这种关系可用米氏方程式来表示(Michaelis-Menten方程)即: 式中Vmax为最大反应速度,Km为米氏常数,[S]为底物浓度 当v=Vmax/2时,则Km=[S],Km是酶的特征性常数,测定Km是研究酶的一种重要方法。但是在一般情况下,根据实验结果绘制成的是直角双曲线,难以准确求得Km和Vmax。若将米氏方程变形为双倒数方程(Lineweaver-Burk方程),则此方程为直角方程,即: 以1/V和1/[S]分别为横坐标和纵坐标。将各点连线,在横轴截距为-1/Km,据此可算出Km值。 本实验以碱性磷酸酶为例,测定不同浓度底物时的酶活性,再根据1/v和1/[S]的倒数作图,计算出其Km值。 二、抑制剂对酶促反映的影响
凡能降低酶的活性,甚至使酶完全丧失活性的物质,成为酶的抑制剂。酶的特异性抑制剂大致上分为可逆性和不可逆性两类。可逆性抑制又可分为竞争性抑制和非竞争性抑制等。竞争性抑制剂的作用特点是使该酶的Km 值增大,但对酶促反映的最大速度Vmax 值无影响。非竞争性抑制剂的作用特点是不影响[S]与酶的结合,故其Km 值不变,然而却能降低其最大速度Vmax 。本实验选取Na 2HPO 4作为碱性磷酸酶的抑制物,确定其抑制作用属于哪种类型。 实验步骤: 实验一:底物浓度对酶促反应速度的影响 1. 取试管9支,将0.01mol/L 基质液稀释成下列不同浓度: 2. 另取9支试管编号,做酶促反应: 3. 混匀,37 ℃水浴保温5分钟左右。 4. 加入酶液后立即计时,各管混匀后在37 ℃准确保温15分钟。 5. 保温结束,立即加入0.5mol/L NaOH 1.0 ml 以中止反应。各管分别加入0.3% 4-氨基安替 比林1.0 ml 及0.5% 铁氰化钾 2.0 ml 。 试剂 管号 试剂 管号
酶促反应动力学实验 Document serial number【UU89WT-UU98YT-UU8CB-UUUT-UUT108】
实验 酶促反应动力学 ————蔗糖酶米氏 常数的测 【目的要求】 1.了解酶促动力学研究的范围。 2.以蔗糖酶为例,掌握测定米氏常数(Km) 【实验原理】 在酶促反应中,当反应体系的温度、pH 和酶浓度恒定时,反应初速度(v)则随底物 浓度[S]的增加而加速,最后达到极限,称为最大反应速度(v)。Michaelis 和Menten 根据反应速度与底物浓度的这种关系,推导出如下方程: ] [] [S k S V v m += 此式称为米氏方程,式中Km 称为米氏常数,按此方程,可用作图法求出Km 。方法有: 1.以v[S]作图 由米氏方程可知,v=V /2时,Km =[S]即米氏常数值等于反应速度达到最大反应速度一半时所需底物浓度。因此,可测定一系列不同底物浓度的反应速度v,以v 对[S]作图。当v =V /2时,其相应底物浓度即为Km 。 2.以1/v 对1/[S]作图 取米氏方程的倒数式:
V S V k v m 1][11+?= 以1/v 对1/[S]作图可得一直线,其斜率为Km /V ,截距为1/V 。若将直线延长与横轴相交,则该交点在数值上等于—l /Km 。 本实验以蔗糖为底物.利用一定量蔗糖酶水解不同浓度蔗糖所形成的产物(葡萄糖和果糖)的量来计算蔗糖酶的Km 值。葡萄糖和果糖能与3,5—二硝基水杨酸试剂反应,生成桔红色化合物,可于520nm 处比色测定之。 【试验材料】 1.试剂 (1)标准葡萄糖溶液:准确称取100mg 葡萄糖溶于少量饱和的苯甲酸溶液%),再转移到100ml 容量瓶中,用饱和苯甲酸溶液稀释到刻度,混匀,即得浓度为1mg /m1的标准葡萄糖溶液。冰箱贮藏可长期保存; (2)的L 醋酸缓冲液:取lmol/L 醋酸钠溶液43m1及lmol /L 醋酸溶液57m1,稀释至1000m1即得;
酶动力学综合实验 实验(一)一一碱性磷酸酶Km直的测定 【目的要求】 i. 了解底物浓度对酶促反应速度的影响 2?了解米氏方程、Km值的物理意义及双倒数作图求Km值的方法。 【实验原理】 1、碱性磷酸酶: 碱性磷酸酶是广泛分布于人体各脏器器官中,其中以肝脏为最多。其次为肾脏、骨骼、肠和胎盘等组织。但它不是单一的酶,而是一组同功酶。本实验用的碱性磷酸酶是从大肠杆菌中提取的。 2、米氏方程: Michaelis-Menten在研究底物浓度与酶促反应速度的定量关系时,导出了酶促反 应动力学的基本公式,即: 式中:v表示酶促反应速度, 車表示酶促反应最大速度, [S]表示底物浓 度,表示米氏常 数。 3、?值的测定主要采用图解法,有以下四种: ①双曲线作图法(图1-1, a) 根据公式(1),以v对[s]作图,此时1/2%肚时的底物浓度[s]值即为Km值,以克分子浓度(M)表示。这种方法实际上很少采用,因为在实验条件下的底物浓度很难使酶达到饱和。实测—个近似值,因而1/2 一不精确。此外由于v对[S]的关系呈双曲线,实验数据要求较多,且不易绘制。 ②Lin eweaver- Burk作图法双倒数作图法(图1-1,b) 实际工作中,常将米氏方程(式(1))作数学变换,使之成为直线形式,测定要方便、精确得多。其中之一即取(1)式的倒数,变换为Lin eweaver- Burk方程式:
以対…作图,即为y=ax+b 形式。此时斜率为丄,纵截距为 丄。把直线外推与 u [jj % 横轴相交,其截距相交,其截距即为一 ③ Hofstee 作图法(略) Vmax 卩址1丄1 〒-心冏+1 以V 对 作图,这时斜率为 ,纵截距为二,横截距为 ④ Han as 作图法(略) 把(2)式等号两边乘以[S],得: 本实验主要以双倒数法,即 Li neweaver- Burk 作图法来测定碱性磷酸酶 Km 值。 具体原理如下: 本实验以碱性磷酸酶为例,用磷酸苯二钠为其作用物,碱性磷酸酶能分解磷酸苯 二钠产生酚和磷酸,在适宜条件下(PH10.0,和60C ),准确反应13分钟。在 碱性条件下酚可与酚试剂生成蓝色化合物,以波长 620nm 比色。在一定条件下 色泽深浅与光密度成正比。反应式如下: max 把(2)式等号两边乘以 ,得: ,纵截距为 --------------
酶促反应动力学实验
————————————————————————————————作者: ————————————————————————————————日期:
酶动力学综合实验 实验(一)——碱性磷酸酶Km值的测定 【目的要求】 1.了解底物浓度对酶促反应速度的影响 2.了解米氏方程、Km值的物理意义及双倒数作图求Km值的方法。 【实验原理】 1、碱性磷酸酶: 碱性磷酸酶是广泛分布于人体各脏器器官中,其中以肝脏为最多。其次为肾脏、骨骼、肠和胎盘等组织。但它不是单一的酶,而是一组同功酶。本实验用的碱性磷酸酶是从大肠杆菌中提取的。 2、米氏方程: Michaelis-Menten在研究底物浓度与酶促反应速度的定量关系时,导出了酶促反应动力学的基本公式,即: (1) 式中:v表示酶促反应速度, 表示酶促反应最大速度, [S]表示底物浓度, 表示米氏常数。 3、值的测定主要采用图解法,有以下四种: ①双曲线作图法(图1-1,a) 根据公式(1),以v对[s]作图,此时1/2时的底物浓度[s]值即为Km值,以克分子浓度(M)表示。这种方法实际上很少采用,因为在实验条件下的底物浓度很难使酶达到饱和。实测一个近似值,因而1/2不精确。此外由于v对[S]的关系呈双曲线,实验数据要求较多,且不易绘制。 ②Lineweaver- Burk作图法双倒数作图法(图1-1,b) 实际工作中,常将米氏方程(式(1))作数学变换,使之成为直线形式,测定要方便、精确得多。其中之一即取(1)式的倒数,变换为Lineweaver- Burk方程式: (2)
以对作图,即为y=ax+b形式。此时斜率为,纵截距为。把直线外推与横轴相交,其截距相交,其截距即为—。 ③Hofstee作图法(略) 把(2)式等号两边乘以,得: (3) 以v对作图,这时斜率为,纵截距为,横截距为。 ④Hanas作图法(略) 把(2)式等号两边乘以[S],得: (4) 以对[s]作图,这时斜率为,纵截距为。 (a)(b) 本实验主要以双倒数法,即Lineweaver-Burk作图法来测定碱性磷酸酶Km值。具体原理如下: 本实验以碱性磷酸酶为例,用磷酸苯二钠为其作用物,碱性磷酸酶能分解磷酸苯二钠产生酚和磷酸,在适宜条件下(PH10.0,和60℃),准确反应13分钟。在碱性条件下酚可与酚试剂生成蓝色化合物,以波长620nm比色。在一定条件下色泽深浅与光密度成正比。反应式如下:
酶动力学——米氏动力学原理 摘要: 酶是蛋白质分子,通常操纵其他分子- 的酶的底物。这些目标分子结合到酶的活性部位,并转化为产品,通过一个已知的酵素作用机制的一系列步骤。这些机制可以分为单基和多基体的机制。对酶动力学研究,只能绑定一个基板,如磷酸丙糖异构酶,旨在衡量亲和力与该酶结合本衬底和周转率。当酶结合多个基板,如二氢叶酸还原酶,酶动力学还可以显示的顺序,并结合这些基板在哪些产品发布顺序。例如,结合的酶底物和释放一个多种产品的蛋白酶,它劈开成两个多肽底物蛋白产品之一。如DNA连接一个核苷酸的DNA聚合酶。虽然这些机制往往是一系列复杂的步骤,通常就是一个速率决定步骤,确定整体动力学。这个速率决定步骤可能是一种化学反应或酶的构象变化或基板。并非所有的生物催化剂的酶是蛋白质;如核糖体RNA的核酶和基催化剂是必不可少的许多细胞功能,如RNA的剪接和翻译。核酶和酶之间的主要区别是,RNA的核苷酸组成的催化剂,而酶的氨基酸组成。核酶也履行了反应较有限,但他们的反应机制和动力学进行分析,可以以同样的方法分类。 关键词:周转率酶动力学米氏方程进度曲线
一般原则 反应发生率增加为底物浓度的增加,而在由一种酶催化反应衬底非常高浓度饱和使用完全相同的反应物,并产生完全一样的反应相同的产品。像其他催化剂,酶不改变基材和产品之间的平衡位置。但是,酶催化反应动力学研究显示饱和。对于给定的酶浓度和底物浓度较低时,反应速率与底物浓度的增加而呈线性,酶分子在很大程度上是免费的催化反应,增加底物浓度增加速率是指该酶和底物分子彼此相遇。但是,在相对较高的底物浓度,反应速度渐近接近理论最大值;酶的活性部位几乎所有被占领的,反应速度是由内在的酶周转率决定。 两个最重要的一种酶的动力学性质是如何迅速成为一个特定酶底物饱和,最大速度,可以实现的。了解这些特性意味着什么可以做的一种酶,能在细胞中的酶将展示如何应对这些条件的变化。 酶活性测定 进度曲线的酶反应。在初始利率期斜率为反应初始速率如米氏方程描述的,酶浓度变化是实验室检测程序,测量酶反应速率。由于酶的反应,他们不消耗催化,酶检测通常遵循的任何底物或产物的浓度变化来测量反应速率。有多种方法测量。分光实验观察之间的产物和反应物的光吸收变化;辐射实验涉及注册或放射性来衡量产品的数量随着时间的推移作出释放。光度法检测是最方便,因为它们允许的反应速度要连续测量。虽然辐射检测要求拆除和样本,他们通常是非常
实验 酶促反应动力学 ————蔗糖酶米氏常数的测 【目的要求】 1.了解酶促动力学研究的范围。 2.以蔗糖酶为例,掌握测定米氏常数(Km) 【实验原理】 在酶促反应中,当反应体系的温度、pH 和酶浓度恒定时,反应初速度(v)则随底物 浓度[S]的增加而加速,最后达到极限,称为最大反应速度(v)。Michaelis 和Menten 根据反应速度与底物浓度的这种关系,推导出如下方程: ] [] [S k S V v m += 此式称为米氏方程,式中Km 称为米氏常数,按此方程,可用作图法求出Km 。方法有: 1.以v[S]作图 由米氏方程可知,v=V /2时,Km =[S]即米氏常数值等于反应速度达到最大反应速度一半时所需底物浓度。因此,可测定一系列不同底物浓度的反应速度v,以v 对[S]作图。当v =V /2时,其相应底物浓度即为Km 。 2.以1/v 对1/[S]作图 取米氏方程的倒数式: V S V k v m 1][11+?= 以1/v 对1/[S]作图可得一直线,其斜率为Km /V ,截距为1/V 。若将直线延长与横轴相交,则该交点在数值上等于—l /Km 。 本实验以蔗糖为底物.利用一定量蔗糖酶水解不同浓度蔗糖所形成的产物(葡萄糖和果糖)的量来计算蔗糖酶的Km 值。葡萄糖和果糖能与3,5—二硝基水杨酸试剂反应,生成桔红色化合物,可于520nm 处比色测定之。 【试验材料】 1.试剂 (1)标准葡萄糖溶液:准确称取100mg 葡萄糖溶于少量饱和的苯甲酸溶液%),再转移到100ml
容量瓶中,用饱和苯甲酸溶液稀释到刻度,混匀,即得浓度为1mg/m1的标准葡萄糖溶液。冰箱贮藏可长期保存; (2)的L醋酸缓冲液:取lmol/L醋酸钠溶液43m1及lmol/L醋酸溶液57m1,稀释至1000m1即得; (3)的10%蔗糖溶液:准确取l0g蔗糖溶于少量的/L醋酸缓冲液,转移到100ml容量瓶中,用同样缓冲液稀释到刻度备用; (4)3,5—二硝基水杨酸试剂:溶液I:%NaOH溶液300m1,1%3,5一二硝基水杨酸溶液880m1及酒石酸钾钠(KNaC4O6·4H20)255g三者一起混合均匀。 溶液Ⅱ:取结晶酚10g及lo%NaOH溶液22m1,加蒸馏水稀释成100ml,混匀。 溶液Ⅲ:取溶于64ml溶液n中。 将溶液皿和溶液I混合,激烈振摇混匀,即得3,5—二硝基水杨酸溶液,放置一周后备用。 (5)酵母蔗糖酶溶液:称取鲜酵母l0g于研钵中,加少量细砂及10一15ml蒸馏水研磨。磨细后置冰箱中,过滤,滤液加2—3倍体积冷丙酮,搅拌均匀后离心,沉淀用丙酮洗两次,真空干燥得固体粉末状酶,再溶于100ml蒸馏水,即得酶溶液。若有不溶物可用离心法除去。该酶液活力以6—12单位为佳。蔗糖酶活力单位的定义为:在一定条件下反应5min,每产生lmg葡萄糖所需要的酶量。备用。 2.器材 (1)100m1三角烧瓶2只; (2)研钵1只; (3)50m1及100m1容量瓶各1只; (4)离心机1台(4000rpm); (5)糖管8支; (6)恒温水浴1台; (7)吸量管:×2支; (8)秒表1只; (9)72l型分光光度计1台。 【实验方法】 1.标准曲线的绘制 取干净糖管6支,如下表所示添加试剂。 调零点,于520nm处测定吸光度。以葡萄糖含量为横坐标,以吸光度为纵坐标作图。2.根据活力选择酶浓度 将10%蔗糖溶液稀释成的%的溶液,取此溶液5m1于试管中,共加两管。 将两管同时置于25℃水浴中保温5min,然后向管中加入蔗糖酶溶液,立即混匀, 同时用秒表计时,准确反应5min后,立即加入LNaOH溶液终止酶反应。另 一管先加入溶液,再加入蔗糖酶溶液(此为对照管)。 取干净糖管3支,第l、2管分别加入上述反应液各及水各,第3管加蒸馏水,然后各