
1.催化剂的定义是:催化剂是一种能够改变一个化学反应的反应速度,却不改变化学反应热力学平衡位置,本身在化学反应中不被明显地消耗的化学物质。
2.催化作用是指催化剂对化学反应所产生的效应。
3.催化剂的基本特征:
1)催化剂只能加速热力学上可以进行的反应,而不能加速热力学上无法进行的反应。
2)催化剂只能加速反应趋于平衡,不能改变平衡的位置(平衡常数)。
3)催化剂对反应具有选择性;
4)催化剂的寿命。
4.工业催化剂一般有哪些组分组成?各组分具有什么功能?
①活性组分:提供改变反应历程的组分,多为金属、氧化物、酸碱
②载体组分:提供高的比表面积、孔结构、活性组分的分散剂、粘合剂、或支撑体。多数为硅
和铝的氧化物
③助催化剂组分:催化剂的辅助组分,本身没有活性或者活性很低,用于活性组分或载体改性。
5.载体的功能主要体现在哪几个方面?(分散作用、稳定作用、支撑作用,传热和稀释作用、助催化作用)
①提供适宜的比表面和孔结构
②维持催化的形状和机械强度
③改善催化剂热传导性
④提高催化剂中活性组分分散度
⑤提供附加活性中心
⑥活性组分和载体的溢流现象和强相互作用
6.催化剂的反应性能是评价催化剂好坏的主要指标,它包括催化剂的活性、选择性和稳定。
7.多相催化反应过程中,从反应物到产物一般经历哪些步骤
包括五个连续的步骤。
(1)反应物分子从气流中向催化剂表面和孔内扩散;
(2)反应物分子在催化剂表面上吸附;
(3)被吸附的反应物分子在催化剂表面上相互作用或与气相分子作用进行化学反应;(4)反应产物自催化剂表面脱附;
(5)反应产物离开催化剂表面向催化剂周围的介质扩散。
8.当气体与固体表面接触时,固体表面上气体的浓度高于气相主体浓度的现象称为吸附现象。
9.几种等温吸附
等温吸附平衡过程用数学模型方法来描述可得到等温方程,其中包括:Langmuir(朗格缪尔)等温方程,Freundlich(弗郎得力希)等温方程,T}MKI}IH(焦姆金)等温方程及BET(Brunauer, Emmett 及Teller)等温方程等。
朗格缪尔等温方程和弗郎得力希等温方程既可用于物理吸附,又可用于化学吸附;
焦姆金等温方程只适用于化学吸附;
BET等温方程用于多层物理吸附。
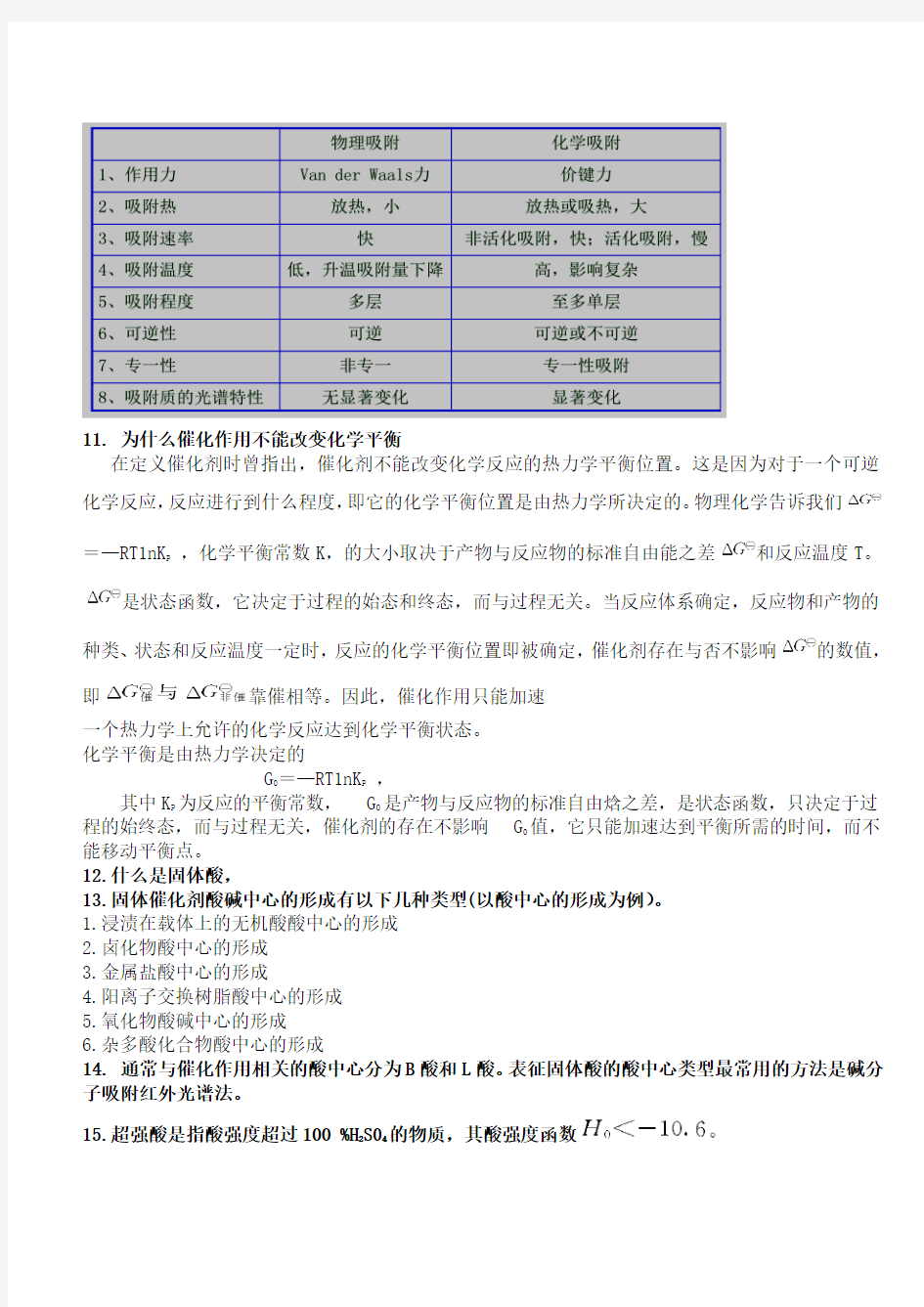
10.物理吸附与化学吸附的区别
11. 为什么催化作用不能改变化学平衡
在定义催化剂时曾指出,催化剂不能改变化学反应的热力学平衡位置。这是因为对于一个可逆化学反应,反应进行到什么程度,即它的化学平衡位置是由热力学所决定的。物理化学告诉我们
=—RT1nK
P
,化学平衡常数K,的大小取决于产物与反应物的标准自由能之差和反应温度T。
是状态函数,它决定于过程的始态和终态,而与过程无关。当反应体系确定,反应物和产物的种类、状态和反应温度一定时,反应的化学平衡位置即被确定,催化剂存在与否不影响的数值,即靠催相等。因此,催化作用只能加速
一个热力学上允许的化学反应达到化学平衡状态。
化学平衡是由热力学决定的
G
0=—RT1nK
P
,
其中K
P 为反应的平衡常数, G
是产物与反应物的标准自由焓之差,是状态函数,只决定于过
程的始终态,而与过程无关,催化剂的存在不影响 G
值,它只能加速达到平衡所需的时间,而不能移动平衡点。
12.什么是固体酸,
13.固体催化剂酸碱中心的形成有以下几种类型(以酸中心的形成为例)。
1.浸渍在载体上的无机酸酸中心的形成
2.卤化物酸中心的形成
3.金属盐酸中心的形成
4.阳离子交换树脂酸中心的形成
5.氧化物酸碱中心的形成
6.杂多酸化合物酸中心的形成
14. 通常与催化作用相关的酸中心分为B酸和L酸。表征固体酸的酸中心类型最常用的方法是碱分子吸附红外光谱法。
15.超强酸是指酸强度超过100 %H
2S0
4
的物质,其酸强度函数
16.沸石分子筛是一种水合结晶硅铝酸盐,其化学组成表示如下:
式中 M—金属阳离子或有机阳离子
n—金属阳离子的价数
m—Si02摩尔数,数值上等于Si02和A1203的摩尔比,又简称硅铝比
P—H2O的摩尔数。
17. 分子筛择形催化有哪几种形式?
1.反应物择形催化(当反应混合物中某些能反应的分子因太大而不能扩散进入催化剂孔腔内,只有那些直径小于内孔径的分子才能进入内孔,在催化活性部分进行反应。)2.产物的择形催化(当产物混合物中某些分子太大,难于从分子筛催化剂的内孔窗口扩散出来, 就形成了产物的择形选择性。)
3.过渡态限制的选择性(有些反应,其反应物分子和产物分子都不受催化剂窗口孔径扩散的限制,只是由于需要内孔或笼腔有较大的空间,才能形成相应的过渡态,不然就受到限制使该反应无法进行;相反,有些反应只需要较小空间的过渡态就不受这种限制,这就构成了限制过渡态的择形催化。)
4.分子交通控制的择形催化(在具有两种不同形状和大小和孔道分子筛中,反应物分子可以很容易地通过一种孔道进入到催化剂的活性部位,进行催化反应,而产物分子则从另一孔道扩散出去,尽可能地减少逆扩散,从而增加反应速率。这种分子交通控制的催化反应,是一种特殊形式的择形选择性,称分子交通控制择形催化。)
18. 为什么金属催化剂主要是过渡金属?
金属催化剂的元素是d区元素,即过渡金属(工B,V工B,V亚B和V皿族元素)。这些元素的外层电子排布的共同特点是最外层或次外层均未被电子填满,具有只含一个d电子的d轨道,即能级中含有未成对的电子,在物理性质中表现出具有强的顺磁性或铁磁性;在化学吸附过程中,这些d 电子可与被吸附物中的s电子或P电子配对,发生化学吸附,生成表面中间物种,使被吸附分子活化。另外,过渡金属作为固体催化剂通常是以金属晶体形式存在的,金属晶体表面裸露着的原子可为化学吸附的分子提供很多吸附中心。
19.试说明金属催化剂的特性?
(1)金属催化剂通常是以金属晶体的形式存在,而且具有多种晶体结构,由此也为化学吸附提供多种吸附中心。(2)由于这些中心相互靠近,有利于被吸附物种相互作用而进行反应。(3)由于吸附中心的多样性,也就造成竞争反应的同时发生,降低了金属催化剂的选择性。(4)对双原子分子,容易进行解离吸附,从而进行各类反应。
20.试说明金属与载体间的相互作用?
相互作用为三种类型:一是金属颗粒和载体的接触位置处在界面部位处,则分散了的金属可保持阳离子的性质;二是分散了的金属原子熔于氧化物载体的晶格结构中或与载体形成混合氧化物;三是金属颗粒表面被来自载体氧化物涂释。正是由于金属-载体的相互作用,结果使得电子流体在二者之间转移,出现电荷的位移。金属与载体之间的相互作用,使得催化过程发生了变化。
21.溢流现象:被吸附的活性物种从一个相向另一个相转移,另一个相是不能直接吸附生成该物种的相。
22.根据合金的体相性质和表面组成可将合金分为3类:(1>机械混合(2)化合物合金(3)固溶体
23.表面富集由如下两因素:
①合金中表面自由能较低(升华热较低)的组分容易在表面富集。因为表面自由能的很小差别就会造成很大的表面富集。
②合金表相组成与接触的气体性质有关,与气体有较高吸附热的组分容易在表面富集。
24.催化剂传统的制造方法(沉淀法、浸溃法、热分解法、熔融法、还原法)
一体化催化剂:沉淀法,Sol-gel法,微乳液法,熔融法,混合法
负载型催化剂:浸渍法,离子交换法,沉积沉淀法
25.沉淀影响因素:
(1)浓度,
晶形沉淀应在稀溶液中进行(稀溶液中更有利于晶核长大),过饱和度不太大时(S= 1.5-2.0)可得到完整结晶,过饱和度较大时,结晶速率很快,易产生错位和晶格缺陷,但也易包藏杂质、晶粒较小,沉淀剂应在搅拌下均匀缓慢加入,以免局部过浓。非晶形沉淀应在较浓溶液中进行,沉淀剂应在搅拌下迅速加入
(2)温度,
晶核生成速率、长大速率存在极大值(晶核生成速率最大时的温度比晶核长大速率最大时的温度低得多),低温有利于晶核生成,不利于晶核长大,一般得到细小颗粒,晶形沉淀应在较热溶液中进行,并且热溶液中沉淀吸附杂质少、沉淀时间短(一般70-80 oC)
(3)pH值,
同一物质在不同pH值下沉淀可能得到不同的晶形,多组分金属盐的共沉淀,pH值的变化会引起先后沉淀,(故而为了保证沉淀颗粒的均一性、均匀性,pH值必须保持相对稳定。)
(4)加料方式,
顺加法:沉淀剂加入到金属盐溶液中,逆加法:金属盐溶液加入到沉淀剂中,并加法:金属盐溶液和沉淀剂按比例同时并流加到沉淀槽中
(5)搅拌强度
沉淀时搅拌是必需的。搅拌强度大,液体分布均匀,但沉淀粒子可能被搅拌浆打碎;搅拌强度小,液体不能混合均匀。对于晶形沉淀:沉淀剂应在搅拌下均匀缓慢加入,以免局部过浓,对于非晶形沉淀:沉淀剂应在搅拌下迅速加入
沉淀的后处理过程:老化-过滤-洗涤-干燥-焙烧-成型-活化
26.浸渍法分类:(1)过量浸渍法:将载体浸渍在过量溶液中,溶液体积大于载体可吸附的液体体积,一段时间后除去过剩的液体,干燥、焙烧、活化。(2)等体积浸渍法:预先测定载体吸入溶液的能力,然后加入正好使载体完全浸渍所需的溶液量(实际采用喷雾法——把配好的溶液喷洒在不断翻动的载体上,达到浸渍的目的。(3)多次浸渍法:将浸渍、干燥和焙烧反复进行多次。(4)浸渍沉淀法:使载体先浸渍在含有活性组分的溶液中一段时间后,再加入沉淀剂进行沉淀。(5)蒸气浸渍法:借助浸渍化合物的挥发性,以蒸气相的形式将其负载于载体上。
浸渍法的影响因素:浸渍时间,浸渍浓度(低浓度浸渍溶液和较长浸渍时间有利于活性组分在载体孔内均匀分布),27. 催化剂的预处理(活化)
(1)氧化物或盐类加氢还原成金属催化剂;(2)氧化物硫化制备硫化物催化剂;
(3)择形催化剂的预积碳处理、外表面覆盖、孔口收缩预处理(化学气象沉积(CVD)
积碳失活的催化剂可通过烧焦使催化剂再生。在烧焦前通常用惰性气体或水蒸气吹扫催化剂。将吸附的有机物解吸吹出。结焦催化剂再生过程最主要的是把碳燃烧转化为C02或CO时所放出的热量及时移出床层,避免床层飞温而引起的催化剂烧结。
通常将失活过程划分为三种类型:(1化剂积炭等堵塞失活,属于物理的;(2)催化剂中毒失活,属于化学的;(3)催化的热失活和燃烧失活;属于热学的。
28.d带空穴与磁化率
d带空穴是指d能带中未充填电子的空能级。
d带中较密集的能级间距允许电子保持不成对,饱和磁矩在数值上等于d能带中的未配对电子数。金属的磁化率决定于未配对电子数,金属的磁化率可以表示d带空穴的大小。
29. 金属的价键理论
认为过渡金属原子以杂化轨道相结合,杂化轨道通常为s、p、d等原子轨道的线性组合,称之为spd 或dsp杂化。杂化轨道中d原子轨道所占的百分数称为d特性百分数,表以符号d%它是价键理论用以关联金属催化活性和其它物性的一个特性参数。金属的d%越大,相应在的d能带中的电子填充的越多,d空穴越小。
d特性%-金属原子的d电子参加dsp成键轨道的程度
30.合成氨工业催化剂工业用合成氨催化剂的主要组成是什么?说明主催化剂和各助催化剂的作用。
工业上使用的合成氨催化剂以Fe30}为主催化剂,A1203, K20 , Ca0和Mg0等为助催化剂。合成氨催化剂通常是用天然磁铁矿和少量助剂在电熔炉里熔融,在室温下冷却制备的。
氨的合成为放热可逆反应:
操作温度通常为400^5000C,压力为15^-30MPa
各种助催化剂的作用及其最佳含量:
工业用合成氨催化剂的主要组成是:Fe30} , A1203 , K20 , Ca0 , MgC)和Si02等。Fe30、是主催化剂,它还原后生成a-Fe,它可以化学吸附N2,使N:活化加氢生成NH3 ;
A1203为结构型助催化剂,它可与Fe302,K20生成FeA1204,K2A1204等高熔点且难还原的组分,隔开了a-Fe微晶,阻止a-Fe的重结晶,稳定了晶格,增加比表面积;此外,A120:还可与K20生成铝酸钾,将表面游离K20束缚住,不致使K20产生KOH覆盖a-Fe表面而降低催化剂活性;
K20为电子型助催化剂,它可使a-Fe的电子输出功降低,从而提高催化剂活性;
Ca0和Mg0能使A1203与磁铁矿熔融温度降低,粘滞性变小,有利于A1203在熔融物中均匀分布;
Si0:可改善催化剂物理结构,使K十分布更均匀或调节表面K十的百分含量。
总的说来,助催化剂的各种成分是互相联系,互相制约的,它们通过对a-Fe微晶大小及其分布、a-Fe电子逸出功的改变等使催化剂活性、稳定性达到最佳值。
1.催化重整主要是加工直馏石脑油、加氢裂化石脑油和加氢改质后的石脑油,也可加工热加工石脑油(经加氢处理后的焦化石脑油和减粘裂化石脑油)、乙烯裂解汽油的抽余油和加氢后的催化裂化汽油馏分等。催化重整过程的主要目的是生产高辛烷值汽油或芳烃。
2. 固定床半再生重整工艺特点是运转中的催化剂活性缓慢下降,为保持产品的辛烷值或芳烃产率,则必须不断提高反应温度,既要不断提高反应苛刻度直至催化剂进行再生。该工艺反应系统比较简单,运转、操作、维护方便,投资省。但装置开工率较低,近年来,随着双(多)金属催化剂的活性和选择性的改进,催化剂能在苛刻条件下长周期运行,该工艺的优势得以发挥。
连续重整分为重叠式移动床连续重整工艺和并列式连续重整工艺,连续重整工艺的特点是:反应压力低、操作苛刻度高,芳烃转化率高、液收高,生成油辛烷值高,氢产率高。
总之,由于半再生式催化重整和连续再生式催化重整的操作方式不同,对催化剂的要求也不同,一般半再生式催化重整催化剂要求具有更好的稳定性、更低的积炭速率,而连续重整催化剂要求具有良好的低压反应性能、抗积炭性能和再生性能、金属抗烧结性能、金属再分散性能、适当的
堆积密度、良好的机械性能等。
48.合成氨的主催化剂是什么?助催化剂是什么?为什么要选用多组元催化剂?助催化剂的作用是什么?
51.为什么金属催化剂主要是过渡金属元素?过渡金属作为催化剂有什么特点?
14.工业用合成氨催化剂的主要组成是什么?说明主催化剂和各助催化剂的作用。
14. 工业用合成氨催化剂的主要组成是:Fe30} , A1203 , K20 , Ca0 , MgC)和Si02等。Fe30、是主催化剂,它还原后生成a-Fe,它可以化学吸附N2,使N:活化加氢生成NH3 ; A1203为结构型助
催化剂,它可与Fe302,K20生成FeA1
204,K2A1
2
04等高熔点且难还原的组分,隔开了a-Fe微晶,阻
止a-Fe的重结晶,稳定了晶格,增加比表面积;此外,A120:还可与K20生成铝酸钾,将表面游离K20束缚住,不致使K20产生KOH覆盖a-Fe表面而降低催化剂活性;K20为电子型助催化剂,它可使a-Fe的电子输出功降低,从而提高催化剂活性;Ca0和Mg0能使A1203与磁铁矿熔融温度降低,粘滞性变小,有利于A1203在熔融物中均匀分布;Si0:可改善催化剂物理结构,使K十分布更均匀或调节表面K十的百分含量。
27.给你一种固体酸,你将采用哪些表征方法来说明这种固体酸的酸性质?
27.固体酸的性质包括三层涵意:酸中心性质,即B酸或L酸,酸中心的强度和酸中心的数量(酸量),酸浓度的测定,可用非水溶液正丁胺滴定法确定(表酸中心密度),结合不同Hammett指示剂可测定不同酸中心强度和酸强度分布;通过红外光谱法测定吸附毗陡的酸碱键的振动频率,可确定B 酸中心及L酸中心,在红外光谱上1540 cm‘峰是吡啶在B酸中心的特征峰,1450 cm‘是L酸中心上的特征峰,1490cm‘是两种酸中心的总和峰。
用NH:吸附程序升温脱附方法也可以测定固体酸表面的酸强度和酸浓度。
32.写出分子筛的化学组成通式。分子筛作为催化剂,对反应选择性主要与它的什么因素有关?而稳定性又主要与它的什么因素有关?
32.分子筛的化学组成通式:MZ从) " Ai203 " mSi02 " pH20,式中n为金属阳离子的价数,M为金属离子或有机阳离子,二表示Si0 2摩尔数,P表示H20摩尔数。
分子筛作为催化剂,对反应选择性影响较大的是分子筛的类型。因为不同类型的分子筛孔径不同,对反应物、产物及过渡态都有选择性。不同类型分子筛硅铝比不同,表面酸性质不同,对其选择性有影响;再者,不同阳离子交换后,既会影响表面酸性质又会影响孔径大小,故对选择性有影响。对稳定性影响较大的主要因素是分子筛的硅铝比和阳离子类型。硅铝比越高,耐酸、耐热、耐水热稳定性越高;耐高温的阳离子取代钠离子也会提高耐热和水热稳定性,如稀土离子,可大大改善催化剂水热稳定性。此外,孔结构也会影响选择性,如A型、Y型具有超笼和M型具有一维孔道都会影响积碳,从而使催化剂易失活。
1、简述催化作用的定义与特征。 定义:1981年,根据IUPAC于提出的定义,催化剂是一种物质,它能够加速反应的速率而不改变该反应的标准Gibbs自由焓变化。这种物质起的作用称为催化作用。 四个基本特征:(1)催化剂只能加速热力学上可以进行的反应,不能加速热力学上无法进行的反应;(2)催化剂只能加速反应趋于平衡,而不能改变平衡的位置(平衡常数);(3)催化剂对反应具有选择性;(4)催化剂存在一定的寿命. 2、催化剂组成及其功能。 组成:一般包括三种成分:①活性组分、②助催化剂;③载体 (1)活性组分或称主催化剂;对催化剂的活性起着主要作用。它是催化剂设计的第一步,没有它,催化反应几乎不发生。其类别主要有三:即导体、半导体和绝缘体。 (2)载体;①最重要的功能是分散活性组分、作为活性组分的基底,使活性组分保持大的表面积。②降低对毒物的敏感性;③载体为Cat.提供一定的孔隙结构;④改进催化剂的机械强度,及抵抗条件的应力能力⑤有些载体具有双功能性。 (3)助催化剂:本身没有活性或活性很小,但在加入催化剂后(一般小于催化剂总量的10%)能使催化剂具有所期望的活性、选择性或稳定性。其作用是:①帮助载体,控制载体的稳定性,控制不希望有的活性,②帮助活性组分,可能是结构的或电子的,③助抗中毒 3、简述化学工业对催化剂的一般要求。 化学工业要求催化剂具有较高的活性,良好的选择性、抗毒害性、热稳定性、环境友好性和合理的价格。 1、活性:反映催化剂的效能高低的重要性能指标。即反应催化剂改变化学反应速度能力的高低。 表示方法: 1)比活性或比速率。用在某指定条件下(T,P)一定量催化剂上的反应速率来衡量。 2)转化率Xa=已反应的反应物量/起始的反应物量 注明:指定条件下(T,P),相同的反应空时或空速 空速:在流动体系中,物料的流速(单位时间的体积或质量)除以催化剂的体积或质量。S-1或者h-1 3)温度 相同的反应转化率、压力、空时或空速 2、选择性:反映催化剂抑制副反应能力大小的性能指标。 3、寿命:催化剂从开始使用至活性下降到不能再用所经历的时间。 寿命试验:在正常条件下连续运转1000h以上。 4、稳定性:即催化剂在使用条件下的化学稳定性,对热的稳定性、耐压、耐磨和耐冲击等的稳定性。 5、环境友好和自然界相容性::社会发展对催化反应过程要求适应循环经济,催化剂不仅具有高转化率和高选择性,还要具有无毒无害,对环境友好,反应尽量遵循“原子经济性”,反应剩余物与自然相容。 6:价格合理。 4、多相催化的基本步骤。 ⑴反应物分子从气流中向催化剂表面和孔内扩散。⑵反应物分子在催化剂内表面上吸附。⑶
工业催化试卷及答案 Document number【SA80SAB-SAA9SYT-SAATC-SA6UT-SA18】
一、单项选择题(每小题 1 分,共 10 分) 1.为催化剂提供有效的表面和适宜孔结构的是() A.活性组分B.载体 C.助剂 D.助催化剂 2.BET等温式属于五种吸附等温线中的类型() A.I B.II C.III D.IV 3.能给出质子的称为() A.B酸 B.B碱 C.L酸 D.L碱 4.工业上氧化乙烯制环氧乙烷的催化剂是() A.Cu/γ-Al 2O 3 B.Ag/α-Al 2 O 3 C.Ag/γ-Al 2O 3 D.Ni/γ-Al 2 O 3 5.所有金属催化剂几乎都是过渡金属,主要是因为它们______()A.易失去电子 B.易得到电子 C.易强烈吸附反应物D.有着d电子结构 6.X型分子筛最大孔径约为() A. B. C.D. 7.金属在载体上的细微程度用() A.分散度表示 B.单层分布表示 C.粒度表示 D.比表面表示 8.Ziegler-Natta催化属于() A.酸催化 B.金属催化 C.金属氧化物催化 D.络合催化 9.下面属于n型半导体的是() A.ZnO B.NiO C.Cu 2 O D.CuO 10.将燃料的化学能转化为电能的电化学装置称为() A.燃料电池 B.蓄电池 C.发电机 D.燃烧反应器 二、填空题(每空 1 分,共 10 分) 11.一种良好的工业实用催化剂,应该具有三方面的要求,即活性、选择性和稳定性。 12.能给出电子对的固体称为L碱。13.对固体表面酸的描述包括酸的类型、酸强度和酸量。 14.吸附的逆过程称为脱附。 15.在分子筛结构中,相邻的四面体由氧桥联结成环。 16.研究金属化学键的理论有能带理论、价键理论和配位场理论。 17.Cu的加入使Ni的d带空穴变少。 18.金属氧化物催化剂中直接承担氧化功能的是晶格氧。 19.三效催化剂中Pt能有效的促进一氧化碳和HC的催化氧化。 20.催化剂的活性随时间的变化分为成熟期、稳定期和衰老期。 三、判断改错,在题后的括号内,正确的打“√”,错误的打“×”并 改正。(每小题 2 分,共 10 分) 21.对于工业催化剂来说,活性越高越好。 (f) 22.有机物的乙酰化要用L酸位催化。( t ) 23.X型和Y型分子筛的结构是一样的。( f ) 24.择形催化是分子筛的主要特征。( t ) 25.金属的禁带宽度很大。( f ) () 四、名词解释(每小题 4 分,共 20 分) 26.催化剂 凡能加速化学反应趋向平衡,而在反应前后其化学组成和数量不发生变化的物质。 27.超强酸 是一种酸性比100%硫酸还强的酸。H。<- 28.结构敏感反应
工业催化复习要点 一、论述题 1、试说明催化剂的稳定性与寿命的区别和联系。 ①催化剂的稳定性是指催化剂的活性和选择性随时间变化的情况;寿命是指在工业生产的条件下,催化剂的活性能够达到装置生产能力和原料消耗定额的允许使用时间。 ②区别:催化剂的稳定性指的是变化情况,而催化剂的寿命指的是时间的长短。 ③联系:催化剂的稳定性直接影响了其寿命,稳定性好的催化剂的寿命长,稳定性不好的寿命短。 2、半导体ZnO在氧气吸附之后电导比未吸附前低,现用ZnO作为CO氧化催化剂,反应时催化剂的电导增加。请问(1)若O2的吸附为控制步骤时,(2)若CO的吸附为控制步骤时,分别提出增加催化剂的活性的措施。 根据半导体能带理论,ZnO是N型半导体,(1)O2的吸附为控制步骤时,O2得电子过程,应添加施主杂质,如Al3+等。(2)CO的吸附为失电子过程,应添加受主杂质如Li+。 3、说说催化剂为什么不能改变平衡的位置。 因为化学平衡是由热力学决定的,DG0=-RTlnkp,其中kp为反应的平衡常数,DG0是产物与反应物的标准自由焓之差,是状态函数,只决定于过程的始态和终态,而与过程无关,催化剂的存在不影响DG0值,它只能加速达到平衡所需要的时间,而不能移动平衡点。 二、简答题 1、什么是d带空穴?它与金属催化剂的化学吸附和催化性能的关系,d带空穴是越多越好吗? d带空穴是指金属的d带中某些能级未被充满,可看做d带中的空穴。 关系:有d带空穴,就能与被吸附的气体分子形成化学吸附键,生成表面中间物种,具有催化性能。D带空穴越多,对反应分子的化学吸附也越强。催化剂的作用在于加速反应物之间的电子转移,这就要求催化剂既具有接受电子的能力,又有给出电子的能力过渡金属的d空穴正是具有这种特性,然而对于一定的反应,要求催化剂具有一定的d空穴,而不是越多越好。因为并不是d带空穴越多,其催化活性就越大。过多可能造成吸附太强,不利于催化反应。 2、催化剂的四个基本特征是什么? ①催化剂只加速热力学上可以进行的反应,而不能加速热力学上无法进行的反应; ②只能改变化学反应的速度,而不能改变化学平衡的位置; ③催化剂参与化学反应: 通过改变反应历程、降低活化能而改变反应速度; ④催化剂对反应的类型、方向及产物的结构具有选择性。一种催化剂只对特定的化学反应起催化作用。 3、载体的功能和作用是什么。 作用:分散作用,稳定化作用,支撑作用,传热和稀释作用,助催化作用。 功能:①提供有效的表面和合适的孔结构②增强催化剂的机械强度; ③改善催化剂的热稳定性;④减少活性组分的含量;⑤提供附加的活性中心; ⑥与活性组分之间的溢流现象和强相互作用 4、物理吸附和化学吸附的特点及两者的本质差别。 物理吸附是表面质点和吸附分子之间的分子力而引起的。具体地是由永久偶极、诱导偶极、色散力等三种范德华引力。物理吸附就好像蒸汽的液化,只是液化发生在固体表面上罢了。分子在发生物理吸附后分子没有发生显著变化。 化学吸附是在催化剂表面质点吸附分子间的化学作用力而引起的,如同化学反应一
工业催化参考试卷――1 一、填空 1. 催化剂只能改变化学反应到达平衡的速率_____________而不改变反应的_ _反应的平衡位置 __________。 2. 多相催化剂通常由_______、_______、_______三部分组成。 3. 评价工业催化剂性能好坏的指标有_______、_______、_______、_______、_______等。 4. 在多相催化反应中有_______、_______、_______三类控制步骤。在连串反应中,控制步骤_______总过程速度。当过程处于_______时,催化剂内表面利用率最高。 5. 固体酸表面存在_______和______两类酸性中心;两者的转化条件是_________________。 6. 催化剂表面能量分布的类型有_______、_______、_______三种形式。 7. Langmuir 吸附等温式用于_______,吸附量与压力的关系是_______。 8. 吸附热表征_______。催化活性与吸附热之间的关系_______。 9. 半导体的附加能级有_______和_______两种,N 型半导体的附加能级是_______能级,它使半导体的E f _______,电导率_______。 10. 络合物催化剂由_______和_______两部分组成。 11. 常用的工业催化剂制备方法有_______、_______、_______等。 12. 造成催化剂失活的原因有_______、_______、_______等。 13. 催化剂上的吸附有_______ 和____________两种类型; H2 的吸附常采用_______ ,烯烃的吸附常采用_________。反应物在催化剂上的吸附态决定了催化反应的 _______。 14. 按照助剂的功能,它可以分为_______、_______两类。 15. d 轨道在四面体配位场中能级分裂为_______、_______两组;当电子成对能P<分裂能Δ 时,电子采取_______排布。 16. 影响过渡金属的催化剂活性的因素有_______、______两方面,组成合金可以调节过渡金属催化剂的_______因素。 17. 分子筛催化剂的特点是_______。常用的分子筛催化剂有_______、_______等。 18. 均相催化的优点是_______、_______;但其缺点是_______、_______等。 19. 选择性的定义是________________________,其计算公式是_______________________。 二、画出[PtCl3(CH2=CH2)]―的空间构型及电子结构图,并指出CH2=CH2 活化的原因。 三、(二选一)1.写出CO+O2→CO2 在P 型半导体催化剂上的反应机理。2.试解释N 型半导体催化剂利于 加氢反应。 n—型半导体: 阳离子过剩,阴离子缺位。 例,ZnO中Zn2+ 离子过剩。 为保持电中性,过剩的离子,拉住一个电子形成eZn2+,在靠近导带附近形成一附加能级。温度升高时,此电子释放出来,成为自由电子,这是ZnO导电的来源。
、单项选择题(每小题 1分,共10 分) 1.为催化剂提供有效的表面和适宜孔结构的是( ) A .活性组分 B .载体 C .助剂 D .助催化剂 2 . BET 等温式属于五种吸附等温线中的类型( ) A . I B . II C . III 3.能给出质子的称为( ) A . B 酸 B . B 碱 C . L 酸 D . L 碱 4.工业上氧化乙烯制环氧乙烷的催化剂是( ) A . Cu/ Y AI 2O 3 B . Ag/ a Al 2O 3 C . Ag/ Y AI 2O 3 D . Ni/ 丫Al 2O 3 5.所有金属催化剂几乎都是过渡金属,主要是因为它们 ___________ () A .易失去电子 B .易得到电子 12 .能给出电子对的固体称为 L 碱。 13 .对固体表面酸的描述包括酸的类型、酸强度和酸量。 14 .吸附的逆过程称为 脱附。 15 .在分子筛结构中,相邻的四面体由氧 _____ 联结成环。 16 .研究金属化学键的理论有 能带理论 、价键理论和配位场理论。 17. Cu 的加入使 Ni 的d 带空穴 变少 。 18 .金属氧化物催化剂中直接承担氧化功能的是 晶格氧 。 19 .三效催化剂中Pt 能有效的促进 一氧化碳 和HC 的催化氧化。 20 .催化剂的活性随时间的变化分为成熟期、稳定期和 衰老期 二、填空题(每空1分,共10分) 11. 一种良好的工业实用催化剂,应该具有三方面的要求,即活性、选择性和稳定性。 26 .催化剂 凡能加速化学反应趋向平衡,而在反应前后其化学组成和数量不发生变化的物质。 C .易强烈吸附反应物 D .有着d 电子结构 6 . X 型分子筛最大孔径约为( ) A . 0.4 nm B . 0.6 nm C . 0.7 nm D . 0.8 nm 7.金属在载体上的细微程度用( ) A .分散度表示 B . 单层分布表示 C .粒度表示 D . 比表面表示 & Ziegler-Natta 催化属于( ) A .酸催化 B . 金属催化 C .金属氧化物催化 D . 络合催化 9.下面属于n 型半导体的是( ) A . ZnO B . NiO 纸 订 装 C . Cu 2O D . CuO 三、判断改错,在题后的括号内,正确的打“V” ,错误的打“x”并 改正。 (每小题2分,共10分) 21 .对于工业催化剂来说,活性越高越好。(f ) 22 .有机物的乙酰化要用 L 酸位催化。(t ) 23 . X 型和Y 型分子筛的结构是一样的。 (f ) 10.将燃料的化学能转化为电能的电化学装置称为( ) A .燃料电池 B .蓄电池 C .发电机 D .燃烧反应器 24 .择形催化是分子筛的主要特征。 (t ) 25 .金属的禁带宽度很大。 (f ) () 四、名词解释(每小题 4分,共20分)
工业催化期末复习题标准化管理处编码[BBX968T-XBB8968-NNJ668-MM9N]
第二章催化作用与催化剂 电子型助催化剂的作用:改变主催化剂的电子结构,促进催化活性及选择性。 金属的催化活性与其表面电子授受能力有关。具有空余成键轨道的金属,对电子有强的吸引力,吸附能力的强弱是与催化活性紧密相联的 在合成氨用的铁催化剂中,由于Fe是过渡元素,有空的d轨道可以接受电子,故在Fe-Al2O3中加入K2O后,后者起电子授体作用,把电子传给Fe,使Fe原子的电子密度增加,提高其活性,K2O是电子型的助催化剂 第三章吸附与多相催化 1简述多相催化反应的步骤 包括五个连续的步骤。 (1)反应物分子从气流中向催化剂表面和孔内扩散; (2)反应物分子在催化剂表面上吸附; (3)被吸附的反应物分子在催化剂表面上相互作用或与气相分子作用进行化学反应; (4)反应产物自催化剂表面脱附; (5)反应产物离开催化剂表面向催化剂周围的介质扩散。 上述步骤中的第(1)和(5)为反应物、产物的扩散过程。属于传质过程。第(2)、(3)、(4)
步均属于在表面进行的化学过程,与催化剂的表面结构、性质和反应条件有关,也叫做化学动力学过程 2外扩散与内扩散的区别 外扩散:反应物分子从流体体相通过吸附在气、固边界层的静止气膜(或液膜)达到颗粒外表面,或者产物分子从颗粒外表面通过静止层进入流体体相的过程,称为外扩散过程。内扩散:反应物分子从颗粒外表面扩散进入到颗粒孔隙内部,或者产物分子从孔隙内部扩散到颗粒外表面的过程,称为内扩散过程。 为充分发挥催化剂作用,应尽量消除扩散过程的影响 外扩散阻力:气固(或液固)边界的静止层。 消除方法:提高空速 内扩散阻力:催化剂颗粒孔隙内径和长度. 消除方法:减小催化剂颗粒大小,增大催化剂孔隙直径 3解离吸附的Langmuir等温式的推导过程 4物理吸附与化学吸附的区别 物理吸附是表面质点和吸附分子之间的分子力而引起的。具体地是由永久偶极、诱导偶极、色散力等三种范德华引力。物理吸附就好像蒸汽的液化,只是液化发生在固体表面上罢了。分子在发生物理吸附后分子没有发生显着变化。
1.什么是催化剂? 根据IUPAC于1981年提出的定义,催化剂)是一种物质,它能够改变反应的速率而不改变该反应的标准Gibbs自由焓变化 2.催化作用的四个基本特征是什么? ⑴催化剂只能加速热力学上可以进行的反应,而不能加速热力学上无法进行的反应; ⑵催化剂只能加速反应趋于平衡,而不能改变平衡的位置(平衡常数),且催化剂可同时加速正逆反应;⑶催化剂对反应具有选择性,当反应有一个以上生成多种产物的方向时,催化剂仅加速其中的一种。⑷催化剂由正常运转到更换所延续时间(寿命)。 3.什么是助催化剂?分为哪几种? 催化剂中加入的另一种或者多种物质,本身不具活性或活性很小的物质,但能改变催化剂的部分性质,如化学组成、离子价态、酸碱性、表面结构、晶粒大小等,从而使催化剂的活性、选择性、抗毒性或稳定性得以改善。结构型和电子型两类 4.请说明理想的催化剂载体应具备的条件。 ⑴具有能适合反应过程的形状和大小;⑵有足够的机械强度,能经受反应过程中机械或热的冲击;有足够的抗拉强度,以抵抗催化剂使用过程中逐渐沉积在细孔里的副反应产物(如积碳)或污物而引起的破裂作用;⑶有足够的比表面,合适的孔结构和吸水率,以便在其表面能均匀地负载活性组分和助催化剂,满足催化反应的需要;⑷有足够的稳定性以抵抗活性组分、反应物及产物的化学侵蚀,并能经受催化剂的再生处理;⑸能耐热,并具有合适的导热系数;⑹不含可使催化剂中毒或副反应增加的物质;⑺原料易得,制备方便,在制备载体以及制备成催化剂时不会造成环境污染;⑻能与活性组分发生有益的化学作用;⑼能阻止催化剂失活 5多相催化反应的一般步骤?物理过程和化学过程分别是哪几步? ⑴反应物分子从气流中向催化剂表面和孔内扩散。⑵反应物分子在催化剂内表面上吸附。⑶吸附的反应物分子在催化剂表面上相互作用或与气相分子作用进行化学反应。 ⑷反应产物自催化剂内表面脱附。⑸反应产物在孔内扩散到反应气流中去 ⑴⑸扩散为物理过程;⑵⑶⑷为化学过程 6物理吸附与化学吸附的特点? 物理吸附是借助分子间力,吸附力弱,吸附热小(8~20kJ/mol),接近于气体的液化热,且是可逆的,无选择性,分子量越大越容易发生,吸附稳定性不高,吸附与解吸速率都很快,可单分子层或多分子层吸附,不需要活化能。
工业催化期末复习题 Revised as of 23 November 2020
第二章催化作用与催化剂 电子型助催化剂的作用:改变主催化剂的电子结构,促进催化活性及选择性。金属的催化活性与其表面电子授受能力有关。具有空余成键轨道的金属,对电子有强的吸引力,吸附能力的强弱是与催化活性紧密相联的 在合成氨用的铁催化剂中,由于Fe是过渡元素,有空的d轨道可以接受电子,故在Fe-Al2O3中加入K2O后,后者起电子授体作用,把电子传给Fe,使Fe原子的电子密度增加,提高其活性,K2O是电子型的助催化剂 第三章吸附与多相催化 1简述多相催化反应的步骤 包括五个连续的步骤。
(1)反应物分子从气流中向催化剂表面和孔内扩散; (2)反应物分子在催化剂表面上吸附; (3)被吸附的反应物分子在催化剂表面上相互作用或与气相分子作用进行化学反应; (4)反应产物自催化剂表面脱附; (5)反应产物离开催化剂表面向催化剂周围的介质扩散。 上述步骤中的第(1)和(5)为反应物、产物的扩散过程。属于传质过程。第(2)、(3)、(4)步均属于在表面进行的化学过程,与催化剂的表面结构、性质和反应条件有关,也叫做化学动力学过程 2外扩散与内扩散的区别 外扩散:反应物分子从流体体相通过吸附在气、固边界层的静止气膜(或液膜)达到颗粒外表面,或者产物分子从颗粒外表面通过静止层进入流体体相的过程,称为外扩散过程。 内扩散:反应物分子从颗粒外表面扩散进入到颗粒孔隙内部,或者产物分子从孔隙内部扩散到颗粒外表面的过程,称为内扩散过程。 为充分发挥催化剂作用,应尽量消除扩散过程的影响 外扩散阻力:气固(或液固)边界的静止层。 消除方法:提高空速 内扩散阻力:催化剂颗粒孔隙内径和长度. 消除方法:减小催化剂颗粒大小,增大催化剂孔隙直径 3解离吸附的Langmuir等温式的推导过程
专科《工业催化》 一、(共50题,共100分) 1. 关于催化剂描述不正确的是 ( ) (2分) A.催化剂量与化学计量方程式无关 B.反应速度通常与催化剂量成正比 C.加速反应但不参加反应者也是催化剂 D.参加反应后催化剂会有变化但很微小 .标准答案:C 2. 工业上用于空气氧化乙烯制环氧乙烷的催化剂中和分别作为( ) (2分) A.主催化剂和助催化剂 B.主催化剂和载体 C.载体和主催化剂 D.助催化剂和主催化剂 .标准答案:B 3. MgO载体是( ) (2分) A.酸性载体 B.两性载体 C.中性载体 D.碱性载体 .标准答案:D 4. 在过渡金属中,下列哪种物质的化学吸附最弱( ) (2分) A.乙烷 B.乙烯 C.乙炔 D.苯 .标准答案:A 5. 孔半径范围在1.5~15nm的孔称为()(2分) A.微孔 B.中间孔 C.中大孔 D.大孔 .标准答案:B 6. 下列催化剂制备方法中,只能制备低含量金属负载型催化剂的是( ) (2分) A.沉淀法 B.机械混合法 C.离子交换法 D.浸渍法 .标准答案:C 7. B.E.T.方程式的导出是基于( ) (2分) A.化学吸附的多分子层理论,用Langmuir的理想表面吸附模型推导出来 B.物理吸附的多分子层理论,用Langmuir的理想表面吸附模型推导出来的 C.物理吸附的单分子层理论,用Langmuir的理想表面吸附模型推导出来的 D.物理吸附的多分子层理论,用Freundlich的非理想表面吸附模型推导出来的 .标准答案:B 8. 两种反应物参加的多相催化反应中( ) (2分) A.两种反应物都必须发生化学吸咐 B.至少一种反应物发生化学吸附 C.至少一种反应物发生物理吸附 D.以上都可以 .标准答案:B 9. 在催化剂的煅烧过程中,下列哪种说法不正确( ) (2分) A.失去化学键合的水或二氧化碳 B.不改变孔径分布 C.形成活性相 D.稳定机械性质 .标准答案:B 10. 助催化剂()(2分) A.本身对某一反应有很好的活性 B.加入的量一般小于催化剂总量的10% C.对载体没有帮助 D.对催化活性组分无影响 .标准答案:B 11. 下列哪种制备方法是控制均匀沉淀的有效方法( ) (2分) A.在金属盐溶液中加NaOH作沉淀剂 B.在金属盐溶液中加尿素作沉淀剂并加热 C.在金属盐溶液中加Na2CO3作沉淀剂 D.在金属盐溶液中加醋酸作沉淀剂 .标准答案:B 12. 在用压汞法测孔结构时( ) (2分) A.样品孔半径越大,所需汞压越大 B.样品孔半径越小,所需汞压越小 C.样品孔半径越大,所需汞压越小 D.样品孔半径与所需汞压无关 .标准答案:C 13. 下列金属催化剂中,加氢反应活性最高的是( ) (2分) A.Pt B.Pd C.Ni D.Cu .标准答案:A 14. 在过渡金属催化加氢催化剂中,一般其“d带空穴”和“d特征百分数”范围在 ( ) (2分) A.0~2,40~50% B.2~4,40~50% C.0~2,80~90% D.2~4,80~90% .标准答案:A
1、论述催化剂是如何加速反应速率的? 催化剂可以改变反应路线,降低反应的活化能,使反应物分子中活化能的百分数增大,反应数率加快 2、催化作用有哪些基本特征? 1) 催化剂只能加速热力学上可以进行的反应,而不能 加速热力学上无法进行的反应。 2) 催化剂只能加速反应趋于平衡,而不能改变平衡的 位置(平衡常数)。 3) 催化剂对反应具有选择性。 4) 催化剂的寿命 3、说明催化剂为什么不能改变平衡反应的平衡位置? 化学平衡是由热力学决定的,DG0=RTlnKP,其中KP为反应的平衡常数,DG0是产物与反应物的标准自由焓之差,是状态函数,只决定于过程的始终态,而与过程无关,催化剂的 存在不影响DG0值,它只能加快达到平衡所需的时间,而不 能移动平衡点 4、具有加氢功能的催化剂往往对脱氢反应也有活性。试给予解释。 根据Kf=K1/K2,催化剂可以以相同的比例加速正、逆反应速率常数。因此,对于可逆反应,能够催化正方向反应的 催化剂,就应该能催化逆方向反应。 5、通常固体催化剂有哪几个部分组成的? 活性组分、助催化剂、载体 6、试说明催化剂稳定性与寿命的区别与联系。 稳定性:是指催化剂的活性和选择性随时间变化的情况。寿命:是指在工业生产条件下,催化剂的活性能够达到装置生产能力和原料消耗定额的允许使用时间。区别:前者指的是变化情况,后者指的是时间长短。联系:催化剂的稳定性直接影响了其寿命,稳定性好的催化剂的寿命长,稳定 性不好的则短。 7、多相催化反应通常包括哪个连续的步骤? (1)反应物分子从气流中向催化剂表面和孔内扩散;(2)反应物分子在催化剂内表面上吸附;(3)吸附的反应物分子在催化剂表面上相互作用或与气相分子作用进行化 学反应;(4)反应产物自催化剂内表面脱附;(5)反 应产物在孔内扩散并扩散到反应气流中去。 8、试比较物理吸附与化学吸附。 物理吸附是借助分子间力,吸附力弱,吸附热小 (8-20kJ/mol),且是可逆的,无选择性,分子量越大物 理吸附越容易发生。化学吸附化学吸附是借助于化学键力,遵从化学热力学和化学动力学的传统定律,具有选择性特征,化学吸附吸附热大(40-800kJ/mol),一般是不可逆的, 尤其是饱和烃分子的解离吸附。 9、固体表面发生化学吸附的原因是什么? 发生化学吸附的原因,是由于位于固体表面的原子具有 自由价,这些原子的配位数小于固体内原子的配位数,使得每个表面原子受到一种内向的净作用力,将扩散到其附近的 气体分子吸附形成化学键 10、金属表面上甲烷和氢分子的吸附,只能形成解离型 化学吸附,为什么? 因为分子氢、烃分子在吸附之前先必须解离,因为很多 这类分子不能直接与金属的“表面自由价”成键,必须先自身解离,成为有自由价的基团,所以只能形成解离理化学吸附。 11、如何判断一个催化反应是存在内、外扩散的控制? 如果反应物流量的改变对反应物的转化率影响较大,则 存在外扩散控制;如果催化剂的粒径大小的改变对转化率的影响较大,则存在内扩散控制。 12、试叙述固体表面酸中心类型测定方法、以吡啶作 吸附质的IR谱法(1)L酸的红外光谱特征峰:1450cm-1 、1490cm-1 和1610cm -1 (2)B酸的红外光谱特征峰:1540cm-1 13、试叙述固体酸强度测定方法。 (1)胺滴定法:选用一种适合的pKa指示剂(碱),吸附于固体酸表面上,它的颜色将给出该酸的强度(2)气态碱吸附法:当气态碱分子吸附在固体酸位中心时,强酸位 吸附的碱比弱酸位吸附的更牢固,使其脱附也更苦难。当升温排气脱附时,弱吸附的碱将首先排出,故依据不同温度下 排出(脱附)的碱量,可以给出酸强度和酸量。 14、请简要叙述沸石结构的三个层次 第一个结构层次:硅氧四面体和铝氧四面体第二个结构层次:由硅氧四面体或铝氧四面体通过氧桥联结成的环第三个结构层次:氧环通过氧桥相互联结,形成具有三维空间的多面体 15、3A、4A和5A分子筛都是型分子筛吗?它们的孔径大小分别为多少?其结构中的阳离子分别是什么? 是。3A:0.3nm 钾离子;4A:0.4nm 钠离子;5A:0.5nm 钙离子。 16、X型和Y 型分子筛的结构一样吗?它们的区别在哪里?其硅铝比分别是多少? 不一样。区别在于硅铝比不同。X型Si/Al为1-1.5;Y型Si/Al为1.5-3.0。 17、简述分子筛的主要四种催化作用、(1)酸催化;(2)择形催化;(3)双功能催化;(4)催化氧化 18、分子筛择形催化有哪四种不同形式、(1)反应物的择形催化;(2)产物的择形催化;(3)过渡状态限制的择形催化;(4)分子交通控制的择形催化 19、什么类型的分子筛具有催化氧化性能 TS-1 分子筛;ZSM-5 分子筛 20、依形态结构划分,金属催化剂分别有哪五种类型? 1)块状金属催化剂;2)分散或负载型金属催化剂;3)合金催化剂; 4)金属互化物催化剂;5)金属簇状物催化剂 21、简述金属催化剂可以发生的四种反应类型。 1)加氢反应;2)氧化反应;3)重整反应;4)氢醛化反应 22、什么是 d 带空穴?它与金属催化剂的化学吸附和催化性能之间的关系式什么? 金属的 d 带中某些能级未被充满,可看作 d 带中的空穴,称为“d 带空穴”。有 d 带空穴,就能与被吸附的气体分子形成化学吸附键,生成表面中间物种,具有催化性能。 d 带空穴愈多,末配对的 d 电子愈多,对反应分子的化学吸附也愈强。催化剂的作用在于加速反应物之间的电子转移,这就要求催化剂既具有接受电子的能力,又有给出电子的能力。过渡金属的 d 空穴正是具有这种特性,然而对一定的反应,要求催化剂具有一定的 d 空穴,而不是愈多愈好 23、什么是 d 特性百分数?它与金属催化剂的化学吸 附和催化活性有什么关系。 d 特性百分数(d%):杂化轨道中 d 原子轨道所占的百分数。 d%越大化学吸附能力越强。但从活化分子的能量因素考虑,要求化学吸附既不太强,也不要太弱。吸附太强导致不可逆吸附,吸附太弱则不足以活化反应分子,所以要求d%有一定范围 24、为什么金属催剂都是过渡金属? 金属催化剂主要是过渡金属,特别是 VIII 族金属。这与金属的结构、表面化学键有关;过渡金属是很好的加氢、脱氢催化剂,H2 很容易在金属表面吸附,吸附反应不会进行到催化剂的体相;一般金属在反应条件下很容易被氧化到体相,不能作为氧化反应催化剂,但贵金属(Pd,Pt, Ag, Au 等)能抗拒氧化,可作为氧化反应催化剂 25、什么是几何对应理论? 要求催化剂原子和反应物分子结构在几何尺寸上接近的理论称之为几何对应理论, 26、金属催化剂为什么大多数制备成负载型催化剂? 因为金属催化剂尤其是贵金属,价格昂贵,将其分散成微小的颗粒附着在高表面积和大孔隙的的载体上,可以节省用量,增加金属原子暴露于表面的机会。 27、请说明双金属催化剂的主要类型和用途。 第一类,第 VIII 族和 IB 族元素组成的双金属系,如Ni-Cu,Pd-Au 等合金;主要用于烃的氢解,加氢和脱氢等反应;第二类,两种 IB 族元素组成的,如 Ag-Au, Cu-Au 等合金,用于改善部分氧化反应的选择性;第三类,两种 VIII 族元素组成的,如 Pt-Ir, Pt-Fe 等合金,用于增加催化剂活性的稳定性。重整催化剂 Pt-Ir 较之 Pt 的稳定性大大提高,原因: Pt-Ir 形成合金减少表面烧结; Ir 有强的氢解活性,抑制了表面积炭的生成。 28、金属硫化物催化剂的基本用途是什么? 金属硫化物催化剂,如 Mo、W、Ni、Co、Fe 等的金属硫化物具有加氢、异构、氢解等催化活性,用于油品的加氢精制;加氢脱硫(HDS)、加氢脱氮(HDN)、加氢脱金属(HDM)等过
催化科学与技术八大领域: 1.多相催化科学与技术 2.均相催化科学与技术(包括负载络合催化, 均相过程多相化). 3.光、电催化科学与技术(光催化与电极催化过程). 4.酶催化科学与技术(酶的结构与性能,酶改性,酶浓集和固定化, 酶的分离和负载以及仿酶催化). 5.催化分离科学与技术(催化蒸馏,催化膜反应,催化萃取) 6.催化材料科学与技术 7.催化剂制造科学与技术(沉淀法,浸渍法,沉淀沉积法,溶胶凝胶 法,超临界反应法, 等离子体法,生物法制酶等). 8.催化剂性能表征和催化研究方法 ?特征:(1)催化剂只能加速热力学上可以进行的反应. (2)只能加速到达反应平衡的时间,不能改变化学平衡位置. (3)催化剂对反应具有选择性 (4)催化剂活性有一定寿命 ?催化剂组成 ①活性组分:提供改变反应历程的组分,多为金属、氧化物、酸碱 ②载体组分:是或活性组分的分散剂、粘合剂、或支撑体。多数为硅和铝 的氧化物 ③助催化剂组分:催化剂的辅助组分,本身没有活性或者活性很低,用于 改善催化剂的各种性能 ?载体功能: ①提供适宜的比表面和孔结构 ②维持催化的形状和机械强度 ③改善催化剂热传导性 ④提高催化剂中活性组分分散度 ⑤提供附加活性中心 ⑥活性组分和载体的溢流现象和强相互作用 活性组分与载体的溢流现象(Spillover)和强相互作用 所谓溢流现象,是指固体催化剂表面的活性中心(原有的活性中心)经吸附产生出一种离子的或者自由基的活性物种,它们迁移到别的活性中心处(次级活性中心)的现象。它们可以化学吸附诱导出新的活性或进行某种化学反应。如果没有原有活性中心,这种次级活性中心不可能产生出有意义的活性物种,这就是溢流现象。它的发生至少两个必要的条件:(A)溢流物种发生的主源;(B)接受新物种的受体,它是次级活性中心。 ?工业催化剂的要求 1、催化剂的活性: 2、催化剂的选择性: 3、催化剂的稳定性 4、环境相容性 催化剂稳定性
工业催化试卷答案整理 一,催化剂载体的功能?1.提供有效的表面和适宜的孔结构2增强催化剂的机械强度3改善催化剂的传导性4减少活性组分的含量5载体提供附加的活性中心6活性组分与载体之间的溢流现象和强相互作用。 二,工业催化剂的一般要求是什么?1具有高活性和选择性2稳定性好3环境友好和自然界的相容性。 三,络合催化剂有几个关键的基元反应?1配位不饱和与氧化加成反应2穿插反应3,B—氢转移反应4配位体解离和配位体交换反应 四,工业催化剂的制备方法有:沉淀法,浸渍法,混捏法,离子交换法,熔融法等。 常用是沉淀法,浸渍法,混捏法。 五,酶催化的特征为:酶是一种生物催化剂⑴酶具有化学催化的一般特征①不变性,催化剂只能加速催化剂反应的进行,但在反应前后,催化剂本身保持不变②可逆性,催化剂能以相同的效果加速正逆反应的进行,即催化剂只能加速化学平衡的到达,但不能改变化学平衡状态和平衡常数,催化剂只能加速热力学上可以实现的反应③选择性,催化剂能有选择的加速某个反应,从而提高目的产物的收率。⑵酶与一般催化剂比较具有以下特点①催化活性极高,对同一反应酶催化比一般化学催化效率高10~6-10~13倍②极高的催化专一性,酶只能加速一种底物或一些
结构相似的底物的化学反应。③催化反应条件很温和。酶催化可在常温常压和中性PH介质环境下进行。 ㈠催化作用的定义及特征?催化作用:催化剂是一种物质,它能够加速反应的速率而不改变该反应的标准Gibbs自由焓变化。这种作用称为催化作用。涉及催化剂的反应称为催化反应。催化作用的特征:①催化剂只能加速热力学上可以进行的反应,而不能加速热力学上无法进行的反应,②催化剂只能加速反应趋于平衡,而不能改变平衡的位置③催化剂对反应具有选择性④催化剂具有一定的寿命 ㈡催化助剂的种类?催化助剂是催化剂中具有提高催化剂活性、选择性、改善催化剂耐热性、抗毒性、机械强度和寿命等性能的组分。助催化剂本身并无催化活性,但只要在催化剂中添加少量的助催化剂即可显著改善催化剂的性能。 催化助剂有:结构助催化剂,电子助催化剂,晶格缺陷助催化剂,选择性助催化剂,扩散助催化剂等 (三)分子筛催化剂的择形催化特性?1.反应物的择形催化2.产物的择形催化3.过滤状态限制的择形催化4.分子交通控制的择形催化 (四)影响酶催化反应的因素是什么?一、温度对酶促的影响,温度对酶催化作用的影响体现于两个方面1)与一般的化学反应相同,在一定的温度范围内,酶促反应速率随着温度的升高而加快,一般每升高10度,反应速率提高1-2倍2)酶是蛋白质,
1.1、论述催化剂是如何加速反应速率的? 催化剂可使化学反应物在不改变的情况下,经由只需较少活化能的路径来进行化学反应。因而加快了反应速率。 1.2、催化作用有哪些基本特征? 1) 催化剂只能加速热力学上可以进行的反应,而不能加速热力学上无法进行的反应。 2) 催化剂只能加速反应趋于平衡,而不能改变平衡的位置(平衡常数)。 3) 催化剂对反应具有选择性。 4) 实际上催化剂并不能无限期地使用,在长期受热和化学、物理作用下,会发生不可逆的变化,这将导致催化剂活性下降,最终导致催化剂失活。 1.3、说明催化剂为什么不能改变平衡反应的平衡位置? 对于给定的反应,在已知条件下,其催化和非催化过程的-△G r值是相同的,即Kf值是相同的,所以平衡位置没有改变。 另一种答案:化学平衡是由热力学决定的,?G = ? RT ln k p ,其中kp 为反应的平衡常数,?G 是产物与反应物的标准自由焓之差,是状态函数,只决定于过程的始终态,而与过程无关。催化剂的存在不影响?G 值,它只能加速达到平衡所需的时间,而不能移动平衡点。 1.4、具有加氢功能的催化剂往往对脱氢反应也有活性。试给予解释。、具有加氢功能的催化剂往往对脱氢反应也有活性。试给予解释。根据Kf= ,催化剂可以以相同的比例加速正、逆反应的速率常数。因此,对于可逆反应,能够催化正方向反应的催化剂,就应该能催化逆方向反应。 2.1、通常固体催化剂有哪几个部分组成的?通常估计催化剂由活性组分、载体和助催化剂三个部分组成。 (1)载体:载体是催化剂活性组分的分散剂、黏合物或支撑体,是负载活性组分的骨架。(2)助催化剂:本身没有活性或者活性很小,但加入到催化剂中后,可以改变催化剂的化学组成、化学结构、离子价态、酸碱性、晶格结构、表面结构、孔结构、分散状态、机械强度等,从而提高催化剂的活性、选择性、稳定性和寿命。 2.2、在甲烷催化氧化偶联反应研究中,如果反应物进料为甲烷和氧气,反应产物经气相色谱分析结果mol % 、在甲烷催化氧化偶联反应研究中,如果反应物进料为甲烷和氧气,反应产物经气相色谱分析结果组成如下:组成如下:CH4 20%、C2H4 30%、C2H6 20% 、CO2 20% 、CO 10% 。不考虑反应过程中的积碳问、、试计算()甲烷的转化率;(2)题。试计算(1)甲烷的转化率;)乙烯的选择性。(乙烯的选择性。解:设产物以100mol计(1)x(转化率)= 30 × 2 + 20 ×2 + 20 × 1 + 10 ×1 ×100% = 88.67% 20 ×1 + 30 ×2 + 20 ×2 + 20 ×1 + 10 ×1 30 ×2 (2)s(选择性)= ×100% = 46.15% 30 ×2 + 20 ×2 + 20 × 1 + 10 × 1 2.3、试说明催化剂稳定性与寿命的区别与联系。、试说明催化剂稳定性与寿命的区别与联系。稳定性:是指催化剂的活性和选择性随时间变化的情况。寿命:是指在工业生产条件下,催化剂的活性能够达到装置生产能力和原料消耗定额的允许使用时间。区别:前者指的是变化情况,后者指的是时间长短。联系:催化剂的稳定性直接影响了其寿命,稳定性好的催化剂的寿命长,稳定性不好的则短。 3.1、多相催化反应通常包括哪个连续的步骤?、多相催化反应通常包括哪个连续的步骤?(1)反应物分子从气流中向催化剂表面和孔内扩散;(2)反应物分子在催化剂内表面上吸附;(3)吸附的反应物分子在催化剂表面上相互作用或与气相分子作用进行化学反应;(4)反应产物自催化剂内表面脱附;(5)反应产物在孔内扩散并扩散到反应气流
1什么是催化剂?催化剂作用的特征是什么? 催化剂定义:凡能加速化学反应趋向平衡,而在反应前后其化学组成和数量不发生变化的物质。 特征①不能改变化学平衡②通过改变化学反应历程而改变反应速度③对加速化学反应具有选 择性 2工业催化剂的基本指标是什么?工业催化剂的性能要求有哪些? 基本指标:活性、选择性、寿命、经济性。 性能要求: 活性、选择性、生产能力、稳定性、寿命、机械强度、导热性能、形貌和粒度、 再生性。 3什么是催化剂的稳定性?什么是催化剂的寿命? 催化剂的稳定性是指催化剂在使用条件下具有稳定活性的时间。 催化剂的寿命是指从开始使用到活性下降到生产不能再用时所经历的时间。 4什么是催化剂失活?导致催化剂失活的主要原因有哪些? 定义:在恒定反应条件下进行的催化反应的转化率随时间增长而下降的的现象叫催化剂失活。 原因:中毒、生焦、烧结、活性组分流失 5如何计算催化剂的活性(转化率 X 、转换数TON 转换频率TOF ? ( P 12) 反应速率表示法、反应速率常数表示法、转化率表示法。 转化率X:反应物A 的总量/流经催化床层进料中反应物 A 的总量 转换数TON 催化剂上每个活性位通过催化循环使总反应发生的次数 转换频率TOF 每个活性位每秒时间内完成的催化循环的次数 6固体催化剂的组成有几部分?说明合成氨催化剂各部分的作用?说明 各部分的作用? 组成:活性组分(主催化剂和共催化剂)、载体、助催化剂。 各部分作用:Fe 为活性组分;AI2O3为载体;K20为助催化剂。 Pt 活性组分,Sn 助催化剂,AI2O3酸功能性载体。 7. 固体催化剂载体的作用是什么?常用的载体有哪几种? 作用:分散作用、稳定化作用、支撑作用、传热和稀释作用、助催化作用。 常用载体:低比表面(刚玉、碳化硅、浮石、硅藻土、石棉、耐火砖);高比表面(氧化铝、 SiO2/Al2O3、铁矶土、白土、氧化镁、硅胶、活性炭)。 8. 多相催化反应的步骤有哪些?(课本 P 14) 外扩散-内扩散-化学吸附-表面反应-脱附-内扩散-外扩散 I 物理过程 9、什么是扩散控制、动力学控制?提高宏观反应速率措施? 扩散控制:最慢步骤是物理过程--扩散 动力学控制:最慢步骤是化学过程--吸附、脱附、表面反应 措施:外扩散控制:提高气流速率。 内扩散控制:扩大孔径,减少颗粒直径。 动力学控制:则提高温度,改变催化剂活性组份。 如何消除内、外扩散的影响? 外扩散:按比例同时改变空速及床层填充高度;控制合适的反应温度。 内扩散:选择的催化剂的颗粒及颗粒孔径要大小合适。 Pt-Sn/AI 2Q 催化剂 7 化学过程 物理过程
1.1、论述催化剂是如何加速反应速率的?催化剂可使化学反应物在不改变的情况下,经由只需较少活化能的路径来进行化学反应。 因而加快了反应速率。 1.2、催化作用有哪些基本特征? 1)催化剂只能加速热力学上可以进行的反应,而不能加速热力学上无法进行的反应。 2)催化剂只能加速反应趋于平衡,而不能改变平衡的位置(平衡常数)。 3)催化剂对反应具有选择性。 4)实际上催化剂并不能无限期地使用,在长期受热和化学、物理作用下,会发生不可逆的变化,这将导致催化剂活性下降,最终导致催化剂失活。 1.3、说明催化剂为什么不能改变平衡反应的平衡位置? 对于给定的反应,在已知条件下,其催化和非催化过程的-△ G r值是相同的,即Kf值是相同的,所以平衡位置没有改变。 另一种答案:化学平衡是由热力学决定的,?G = ? RT ln k p ,其中kp 为反应的平衡常 数,?G 是产物与反应物的标准自由焓之差,是状态函数,只决定于过程的始终态,而与过程无关。催化剂的存在不影响?G 值,它只能加速达到平衡所需的时间,而不能移动平衡点。 1.4、具有加氢功能的催化剂往往对脱氢反应也有活性。试给予解释。、具有加氢功能的催 化剂往往对脱氢反应也有活性。试给予解释。根据Kf= , 催化剂可以以相同的比例加速正、逆反应的速率常数。因此,对于可逆反应,能够催化正方向反应的催化剂,就应该能催化 逆方向反应。 2.1、通常固体催化剂有哪几个部分组成的?通常估计催化剂由活性组分、载体和助催化剂三个部分组成。 (1)载体:载体是催化剂活性组分的分散剂、黏合物或支撑体,是负载活性组分的骨架。(2)助催化剂:本身没有活性或者活性很小,但加入到催化剂中后,可以改变催化剂的化学组成、化学结构、离子价态、酸碱性、晶格结构、表面结构、孔结构、分散状态、机械强度等,从而提高催化剂的活性、选择性、稳定性和寿命。 2.2、在甲烷催化氧化偶联反应研究中,如果反应物进料为甲烷和氧气,反应产物经气相色谱分析结果mol % 、在甲烷催化氧化偶联反应研究中,如果反应物进料为甲烷和氧气,反应产物经气相色谱分析结果组成如下:组成如下:CH4 20%、C2H4 30%、C2H6 20% 、CO2 20% 、CO 10% 。不考虑反应过程中的积碳问、、试计算()甲烷的转化率;(2)题。试计算(1)甲烷的转化率;)乙烯的选择性。(乙烯的选择性。解:设产物以100mol 计(1)x(转化率)=30 X 2 + 20 X 2 + 20 X 1 + 10 X 1 X 100% =88.67% 20 X 1 + 30 X 2 + 20 X 2 + 20 X 1 + 10 X 1 30 X 2 (2)s (选择性)= X 100% = 46.15% 30 X 2 + 20 X 2 + 20 X 1 + 10 X 1 2.3、试说明催化剂稳定性与寿命的区别与联系。、试说明催化剂稳定性与寿命的区别与联系。稳定性:是指催化剂的活性和选择性随时间变化的情况。寿命:是指在工业生产条件下,催化剂的活性能够达到装置生产能力和原料消耗定额的允许使用时间。区别:前者指的是变化情况,后者指的是时间长短。联系:催化剂的稳定性直接影响了其寿命,稳定性好的催化剂的寿命长,稳定性不好的则短。 3.1、多相催化反应通常包括哪个连续的步骤?、多相催化反应通常包括哪个连续的步骤? ( 1 )反应物分子从气流中向催化剂表面和孔内扩散;(2)反应物分子在催化剂内表面 上吸附;(3)吸附的反应物分子在催化剂表面上相互作用或与气相分子作用进行化学反 应;(4)反应产物自催化剂内表面脱附;(5)反应产物在孔内扩散并扩散到反应气流 中去。 3.2、试比较物理吸附与化学吸附。、试比较物理吸附与化学吸附。物理吸附是借助分子 间力,吸附力弱,吸附热小(8-20kJ/mol ),且是可逆的,无选择性,分子量越大物理吸附越容易发生。化学吸附化学吸附是借助于化学键力,遵从化学热力学和化学动力学的传统定律,具有选