
醋酸盐氢氧化物*CdS 8.0×10-27 **AgAc 1.94×10-3*AgOH 2.0×10-8*CoS(α-型) 4.0×10-21卤化物*Al(OH)
3
(无定形) 1.3×10-33*CoS(β-型) 2.0×10-25
*AgBr 5.0×10-13*Be(OH)
2(无定形) 1.6×10-22*Cu
2
S 2.5×10-48
*AgCl 1.8×10-10*Ca(OH)
2
5.5×10-6*CuS
6.3×10-36
*AgI 8.3×10-17*Cd(OH)
2
5.27×10-15*FeS
6.3×10-18
BaF
21.84×10-7**Co(OH)
2
(粉红色) 1.09×10-15*HgS(黑色) 1.6×10-52
*CaF
25.3×10-9**Co(OH)
2
(蓝色) 5.92×10-15*HgS(红色)4×10-53
*CuBr 5.3×10-9*Co(OH)
3
1.6×10-44*MnS(晶形)
2.5×10-13
*CuCl 1.2×10-6*Cr(OH)
2
2×10-16**NiS 1.07×10-21
*CuI 1.1×10-12*Cr(OH)
3
6.3×10-31*PbS 8.0×10-28
*Hg
2Cl
2
1.3×10-18*Cu(OH)
2
2.2×10-20*SnS 1×10-25
*Hg
2I
2
4.5×10-29*Fe(OH)
2
8.0×10-16**SnS
2
2×10-27
HgI
22.9×10-29*Fe(OH)
3
4×10-38**ZnS 2.93×10-25
PbBr
26.60×10-6*Mg(OH)
2
1.8×10-11磷酸盐
*PbCl
21.6×10-5*Mn(OH)
2
1.9×10-13*Ag
3
PO
4
1.4×10-16
PbF
23.3×10-8*Ni(OH)
2
(新制备) 2.0×10-15*AlPO
4
6.3×10-19
*PbI
27.1×10-9*Pb(OH)
2
1.2×10-15*CaHPO
4
1×10-7
SrF
2
4.33×10-9*Sn(OH)
2
1.4×10-28*Ca
3
(PO
4
)
2
2.0×10-29
碳酸盐*Sr(OH)
2
9×10-4**Cd
3
(PO
4
)
2
2.53×10-33
Ag
2CO
3
8.45×10-12*Zn(OH)
2
1.2×10-17Cu
3
(PO
4
)
2
1.40×10-37
*BaCO
35.1×10-9草酸盐FePO
4
·2H
2
O 9.91×10-16
CaCO
33.36×10-9Ag
2
C
2
O
4
5.4×10-12*MgNH
4
PO
4
2.5×10-13
CdCO
31.0×10-12*BaC
2
O
4
1.6×10-7Mg
3
(PO
4
)
2
1.04×10-24
*CuCO
31.4×10-10*CaC
2
O
4
·H
2
O 4×10-9*Pb
3
(PO
4
)
2
8.0×10-43
FeCO
33.13×10-11CuC
2
O
4
4.43×10-10*Zn
3
(PO
4
)
2
9.0×10-33
Hg
2CO
3
3.6×10-17*FeC
2
O
4
·2H
2
O 3.2×10-7其它盐
MgCO
36.82×10-6Hg
2
C
2
O
4
1.75×10-13*[Ag+][Ag(CN)
2
-] 7.2×10-11
MnCO
32.24×10-11MgC
2
O
4
·2H
2
O 4.83×10-6*Ag
4
[Fe(CN)
6
] 1.6×10-41
NiCO
31.42×10-7MnC
2
O
4
·2H
2
O 1.70×10-7*Cu
2
[Fe(CN)
6
] 1.3×10-16
*PbCO
37.4×10-14**PbC
2
O
4
8.51×10-10AgSCN 1.03×10-12
SrCO
35.6×10-10*SrC
2
O
4
·H
2
O 1.6×10-7CuSCN 4.8×10-15
ZnCO
3
1.46×10-10ZnC
2
O
4
·2H
2
O 1.38×10-9*AgBrO
3
5.3×10-5
铬酸盐硫酸盐*AgIO
3
3.0×10-8
Ag
2CrO
4
1.12×10-12*Ag
2
SO
4
1.4×10-5Cu(IO
3
)
2
·H
2
O 7.4×10-8
*Ag
2Cr
2
O
7
2.0×10-7*BaSO
4
1.1×10-10**KHC
4
H
4
O
6
(酒石酸氢3×10-4
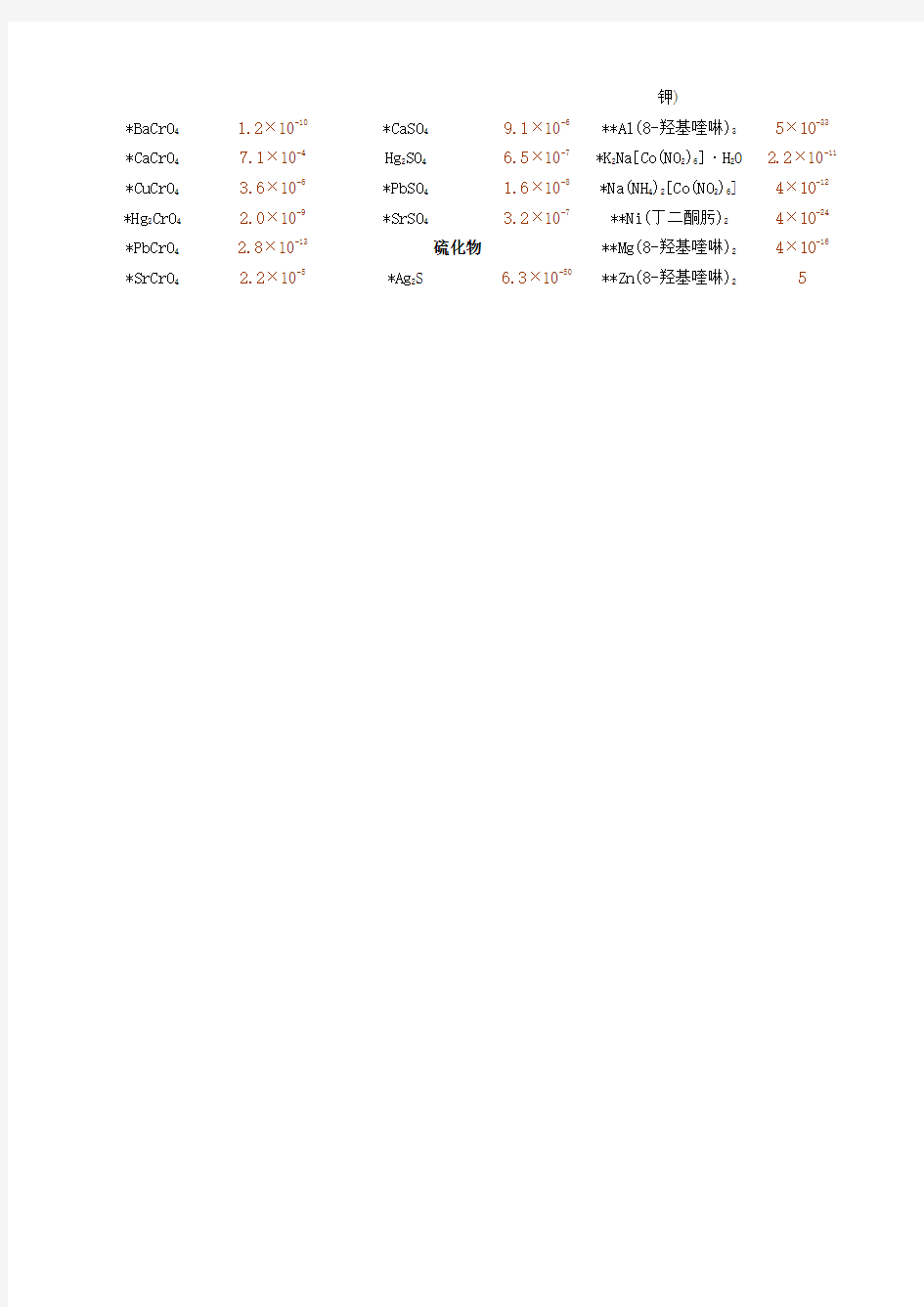
钾)
*BaCrO
41.2×10-10*CaSO
4
9.1×10-6**Al(8-羟基喹啉)
3
5×10-33
*CaCrO
47.1×10-4Hg
2
SO
4
6.5×10-7*K
2
Na[Co(NO
2
)
6
]·H
2
O 2.2×10-11
*CuCrO
43.6×10-6*PbSO
4
1.6×10-8*Na(NH
4
)
2
[Co(NO
2
)
6
] 4×10-12
*Hg
2CrO
4
2.0×10-9*SrSO
4
3.2×10-7**Ni(丁二酮肟)
2
4×10-24
*PbCrO
42.8×10-13硫化物**Mg(8-羟基喹啉)
2
4×10-16
*SrCrO
42.2×10-5*Ag
2
S 6.3×10-50**Zn(8-羟基喹啉)
2
5
化学溶解性表 图例 溶:该物质可溶于水 难:难溶于水(溶解度小于0.01g,几乎可以看成不溶,但实际溶解了极少量,绝对不溶于水的物质几乎没有) 微:微溶于水 挥:易挥发或易分解 —:该物质不存在或遇水发生水解
常见沉淀 白色:BaSO4 BaCO3 CaCO3 AgCl Ag2CO3 Mg(OH)2 Fe(OH)2 Al(OH)3 CuCO3 ZnCO3 MnCO3 Zn(OH)2 蓝色:Cu(OH)2 浅黄色:AgBr 红褐色:Fe(OH)3 溶解性口诀 溶解性口诀一 钾钠铵盐溶水快,① 硫酸盐除去钡银铅钙。② 氯化物不溶氯化银, 硝酸盐溶液都透明。③ 氢氧根多溶一个钡④ 口诀中未有皆下沉。⑤ 注:①钾钠铵盐都溶于水; ②硫酸盐中只有硫酸钡、硫酸铅不溶(硫酸钙硫酸银微溶也是沉淀); ③硝酸盐都溶于水; ④碱性物质中除了钾离子钠离子铵离子锂离子还有钡离子也可溶 ⑤口诀中没有涉及的盐类都不溶于水; 溶解性口诀二 钾、钠、铵盐、硝酸盐; 氯化物除银、亚汞; 硫酸盐除钡和铅; 碳酸、磷酸盐,只溶钾、钠、铵。 说明,以上四句歌谣概括了8类相加在水中溶解与不溶的情况。 溶解性口诀三 钾钠铵硝皆可溶、盐酸盐不溶银亚汞; 硫酸盐不溶钡和铅、碳磷酸盐多不溶。 多数酸溶碱少溶、只有钾钠铵钡溶 溶解性口诀四 钾、钠、硝酸溶,(钾盐、钠盐和硝酸盐都溶于水。) 盐酸除银(亚)汞,(盐酸盐里除氯化银和氯化亚汞外都溶。) 再说硫酸盐,不容有钡、铅,(硫酸盐中不溶的是硫酸钡和硫酸铅。) 其余几类盐,(碳酸盐、亚硫酸盐、磷酸盐、硅酸盐和硫化物) 只溶钾、钠、铵,(只有相应的钾盐、钠盐和铵盐可溶) 最后说碱类,钾、钠、铵和钡。(氢氧化钾、氢氧化钠、氢氧化钡和氨水可溶) 另有几种微溶物,可单独记住。 溶解性口诀五(适合初中化学课本后面的附录) 钾钠铵盐硝酸盐① 氢氧根多钡离子② 硫酸盐除钡钙银③ 碳酸溶氢钾钠铵④ 生成沉淀氯化银⑤ 溶解性口诀六(初学记忆) 不是沉淀物……我们初中的口诀是 钾【化合物】、钠【化合物】、铵【铵根】、硝【硝酸盐】都可溶 氯化物里银不溶 硫酸盐里钡不溶 注:①钾盐、钠盐、铵盐、硝酸盐都溶于水 ②除了以上四种,氢氧根和钡离子结合时也溶于水 ③硫酸根除了和钡离子、钙离子、银离子结合时不溶于水,其他都溶 ④碳酸根除了和氢离子、钾离子、钠离子和铵离子结合时溶于水,其他都不溶 ⑤氯离子只有和银离子结合时不溶于水
溶液浓度和溶解度的换算 (师大附中高级教师王际定老师撰写) 学习误区: 溶液溶解度和溶解度之间的换算,关键是要掌握溶解度的概念,根据溶解度的概念找出溶质、溶剂和溶液三者间量的关系,如果要计算溶液的物质的量浓度,则必须用上密度。还要注意溶解度是对饱和溶液而言,溶液的浓度则与此无关。 学习点拔: 溶解度是指在一定温度下在100克溶剂中达到饱和溶液所能溶解的溶质的克数。这个概念有四个要点:温度一定,溶液是饱和溶液,溶剂(一般是水)是100克,溶解溶质的克数,这个概念本身告诉了我们溶质、溶剂、溶液三者间量的关系,也告诉了溶液的质量百分比浓度,例如物质A在t℃时的溶解度为xg,则t℃时的饱和溶液中有溶剂(水)100g,溶质Axg,溶液为(100+x)g,质量百分比深度为[x/(100+x)]×100%=质量百分比浓度。如果要求A在t℃时饱和溶液的物质的量浓度,则把溶质除以A的摩尔质量得到物质的量,把(100+x)g除以密度得到溶液的体积(mL),再根据溶液的物质的量概念(或公式)去计算。 例1硝酸钾在60℃时的溶解度为110g,求60℃时饱和硝酸钾溶液中溶质的质量分数。 分析:根据溶解度的概念60℃时饱和硝酸钾溶液中每含100g水,必有110g硝酸钾溶质,则溶液为:(100+110)g,然后根据溶液浓度的计算方法去计算。 解:硝酸钾的质量分数=[110/(100+110)]×100%≈52.4% 答:60℃时饱和硝酸钾溶液中硝酸钾的质量分数为52.4%
例220℃时的饱和食盐水的食盐质量分数为26.5%,试计算20℃时食盐的溶解度。 分析:已知20℃时饱和食盐水中溶质的质量分数,即知道食盐水中溶质和溶液的质量关系,因为溶液是由溶剂和溶质组成,从而可求出溶质与溶剂的质量关系,即可求出溶解度。 解:设溶解度为x,则有: [x/(100+x)]×100%=26.5%x≈36(g) 或假设溶液为100g,则溶质为26.5g,溶剂为73.5g,溶解度为: [26.5g/(100g-26.5g)]×100g≈36g 例3某物质的式量为M,取V1ml该物质质量分数为a%的溶液,加Vml水后溶质的质量分数为b%,试求: (1)若原溶液为饱和溶液时,求该温度下,该物质的溶解度。 (2)原溶液铁物质的量浓度 分析:①已知深度为a%,若为饱和溶液,则溶解度可按公式求得。 解:设溶解度为x [xg/(x+100)g]=a/100x=100a/(100-a) 溶解度为[100a/(100-a)]g/100gH2O (1)已知原溶液的体积为V1ml,求物质的量浓度C,关键是求出V1ml溶液中
溶解度与溶度积 联系:溶度积与溶解度均可表示难溶电解质的溶解性,两者之间可以相互换算。区别:溶度积是一个标准平衡常数,只与温度有关。而溶解度不仅与温度有关,还与系统的组成、 pH 值的改变及配合物的生成等因素有关。 在溶度积的计算中,离子浓度必须是物质的量的浓度,其单位为 而溶解度的单位有 g/100g 水, g·L-1, mol·L-1。计算时一般要先将难溶电解质的溶解度 S 的单位换算为 mol·L-1。对于难溶物质饱和溶液浓度极稀,可作近似处理: (xg/100gH2O)×10/M mol ·L-1。 几种类型的难溶物质溶度积、溶解度比较 物质类型难溶物质溶度积 Ksp 溶解度 /mol ·L-1 换算公式 AB AgCl 1.77 ×10-10 1.33 ×10-5 Ksp =S2 BaSO4 1.08 ×10-10 1.04 ×10-5 Ksp =S2 AB 2 CaF2 3.45 ×10-11 2.05 ×10-4 Ksp =4S3 A 2 B Ag 2CrO4 1.12 ×10-12 6.54 ×10-5 Ksp =4S3 对于同种类型化合物而言,Ksp , S 。 但对于不同种类型化合物之间,不能根据Ksp 来比较 S 的大小。 mol·L -1;
例 1、25℃时, AgCl 的溶解度为 1.92 ×10-3g ·L -1,求同温度下 AgCl 的溶度积。 例 2、25℃时,已知 Ksp(Ag 2 4 -12 4) -1 。 ×10 ,求同温度下 S(Ag 2 · CrO )=1.1 CrO /g L 例 3、查表知 PbI 2 的 Ksp 为 1.4 ×10-8,估计其溶解度 S(单位以 g ·L -1 计)。 溶度积规则 在难溶电解质溶液中,有关离子浓度幂的乘积称为浓度积,用符号 Q C 表 示 ,它表示任一条件下离子浓度幂的乘积。 Q C 和 Ksp 的表达形式类似,但其 含义不同。 Ksp 表示难溶电解质的饱和溶液中离子浓度幂的乘积, 仅是 Q C 的一 个特例。 对某一溶液,当 (1)Q C = Ksp ,表示溶液是饱和的。 这时溶液中的沉淀与溶解达到动态平衡, 既无沉淀析出又无沉淀溶解。 (2)Q C < Ksp ,表示溶液是不饱和的。溶液无沉淀析出, 若加入难溶电解质,则会继续溶解。 (3)Q C > Ksp ,表示溶液处于过饱和状态。有沉淀析出。 以上的关系称溶度积规则 (溶度积原理 ),是平衡移动规律总结,也是判断沉淀生成和溶解的依据。 当判断两种溶液混合后能否生成沉淀时,可按下列步骤进行: (1)先计算出混合后与沉淀有关的离子浓度; (2) 计算出浓度积 Qc ; (3) 将 Qc 与 Ksp 进行比较,判断沉淀能否生成。 溶度积规则的应用 (1)判断是否有沉淀生成 原则上只要 Qc >Ksp 便应该有沉淀产生,但是只有当溶液中含约 10-5g ·L -1 固体时,人眼才能观察到混浊现象, 故实际观察到有沉淀产生所需的离子浓度往往要比理论计算稍高些。 (2)判断沉淀的完全程度 没有一种沉淀反应是绝对完全的,通常认为溶液中某离子的浓度小于 -5 -1
1.锕、氨、铵 物质化学式0℃10℃20℃30℃40℃50℃60℃70℃80℃90℃100℃氢氧化锕Ac(OH)3 0.0022 氨NH3 88.5 70 56 44.5 34 36.5 20 15 11 8 7 叠氮化氨NH2N2 16 25.3 37.1 苯甲酸氨NH4C7H5O2 20 碳酸氢氨NH4CO3 11.9 16.1 21.7 28.4 36.6 59.2 109 170 354 溴化氨NH4Br 60.6 68.1 76.4 83.2 91.2 108 125 135 145 碳酸氨(NH4)2CO3100 氯酸氨NH4ClO328.7 氯化氨NH4Cl 29.4 33.2 37.2 41.4 45.8 50.4 55.3 60.2 65.6 71.2 77.3 氯铂酸铵(NH4)2PtCl60.289 0.374 0.499 0.637 0.815 1.44 2.16 2.61 3.36 铬酸铵(NH4)2CrO425 29.2 34 39.3 45.3 59 76.1 重铬酸铵(NH4)2Cr2O718.2 25.5 35.6 46.5 58.5 86 115 156 砷酸二氢铵NH4H2AsO433.7 48.7 63.8 83 107 122 磷酸二氢铵NH4H2PO422.7 39.5 37.4 46.4 56.7 82.5 118 173 氟硅酸铵(NH4)2SiF6 18.6 甲酸铵NH4HCO2 102 143 204 311 533 磷酸一氢铵(NH4)2HPO4 42.9 62.9 68.9 75.1 81.8 97.2 碳酸氢铵NH4HSO4 100 酒石酸氢铵NH4HC4H4O6 1.88 2.7 碘酸铵NH4IO3 2.6 碘化铵NH4I 155 163 172 182 191 209 229 250 硝酸铵NH4NO3 118 150 192 242 297 421 580 740 871 高碘酸铵(NH4)5IO6 2.7 草酸铵(NH4)2C2O4 2.2 3.21 4.45 6.09 8.18 14 22.4 27.9 34.7 高氯酸铵NH4ClO4 12 16.4 21.7 37.7 34.6 49.9 68.9 高锰酸铵NH4MnO4 0.8 磷酸铵(NH4)3PO4 26.1 硒酸铵(NH4)2SeO4 96 105 115 126 143 192 硫酸铵(NH4)2SO4 70.6 73 75.4 78 81 88 95 103 亚硫酸铵(NH4)2SO3 47.9 54 60.8 68.8 78.4 104 114 150 153 酒石酸铵(NH4)2C4H4O6 45 55 63 70.5 76.5 86.9 硫氰酸铵NH4SCN 120 144 170 208 234 346 硫代硫酸铵(NH4)2S2O3 2.15 钒酸铵NH4VO3 0.48 0.84 1.32 2.42
溶度积与溶解度的关系 关键词:溶度积,溶解度 难溶电解质的溶度积及溶解度的数值均可衡量物质的溶解能力。因此,二者之间必然有着密切的联系,即在一定条件下,二者之间可以相互换算。根据溶度积公式所表示的关系,假设难溶电解质为A m B n,在一定温度下其溶解度为S,根据沉淀-溶解平衡: B n(s)mA n+ + nB m? A [A n+]═ m S,[B m?]═ n S 则K sp(A m B n)═ [A n+]m[B m?]n ═ (m S)m(n S)n ═ m m n n S m+n(8-2)溶解度习惯上常用100g溶剂中所能溶解溶质的质量[单位:g/(100g)]表示。在利用上述公式进行计算时,需将溶解度的单位转化为物质的量浓度单位(即:mol/L)。由于难溶电解质的溶解度很小,溶液很稀,可以认为饱和溶液的密度近似等于纯水的密度,由此可使计算简化。 【例题8-1】已知298K时,氯化银的溶度积为1.8×10?10,Ag2CrO4的溶度积为1.12×10?12,试通过计算比较两者溶解度的大小。 解(1)设氯化银的溶解度为S1 根据沉淀-溶解平衡反应式: AgCl(s)Ag++Cl? 平衡浓度(mol/L)S1S1 K sp(AgCl)═ [Ag+][Cl?]═ S12 S1 ═10 ?═ 1.34×10?5(mol/L) 8.1- 10 (2)同理,设铬酸银的溶解度为S2 Ag CrO4(s)2Ag++ CrO42- 平衡浓度(mol/L)2S2 S2 K sp(Ag2CrO4)═[Ag+]2 [CrO42-]═(2S2)2S2═4S23 S2 6.54×10?5(mol/L)>S1 在上例中,铬酸银的溶度积比氯化银的小,但溶解度却比碳酸钙的大。可见对于不同类型(例如氯化银为AB型,铬酸银为AB2型)的难溶电解质,溶度积小的,溶解度却不一定小。因而不能由溶度积直接比较其溶解能力的大小,而必须计算出其溶解度才能够比较。对于相同类型的难溶物,则可以由溶度积直接比较其溶解能力的大小。
醋酸盐氢氧化物*CdS 8.0×10-27 **AgAc 1.94×10-3*AgOH 2.0×10-8*CoS(α-型) 4.0×10-21卤化物*Al(OH) 3 (无定形) 1.3×10-33*CoS(β-型) 2.0×10-25 *AgBr 5.0×10-13*Be(OH) 2(无定形) 1.6×10-22*Cu 2 S 2.5×10-48 *AgCl 1.8×10-10*Ca(OH) 2 5.5×10-6*CuS 6.3×10-36 *AgI 8.3×10-17*Cd(OH) 2 5.27×10-15*FeS 6.3×10-18 BaF 21.84×10-7**Co(OH) 2 (粉红色) 1.09×10-15*HgS(黑色) 1.6×10-52 *CaF 25.3×10-9**Co(OH) 2 (蓝色) 5.92×10-15*HgS(红色)4×10-53 *CuBr 5.3×10-9*Co(OH) 3 1.6×10-44*MnS(晶形) 2.5×10-13 *CuCl 1.2×10-6*Cr(OH) 2 2×10-16**NiS 1.07×10-21 *CuI 1.1×10-12*Cr(OH) 3 6.3×10-31*PbS 8.0×10-28 *Hg 2Cl 2 1.3×10-18*Cu(OH) 2 2.2×10-20*SnS 1×10-25 *Hg 2I 2 4.5×10-29*Fe(OH) 2 8.0×10-16**SnS 2 2×10-27 HgI 22.9×10-29*Fe(OH) 3 4×10-38**ZnS 2.93×10-25 PbBr 26.60×10-6*Mg(OH) 2 1.8×10-11磷酸盐 *PbCl 21.6×10-5*Mn(OH) 2 1.9×10-13*Ag 3 PO 4 1.4×10-16 PbF 23.3×10-8*Ni(OH) 2 (新制备) 2.0×10-15*AlPO 4 6.3×10-19 *PbI 27.1×10-9*Pb(OH) 2 1.2×10-15*CaHPO 4 1×10-7 SrF 2 4.33×10-9*Sn(OH) 2 1.4×10-28*Ca 3 (PO 4 ) 2 2.0×10-29 碳酸盐*Sr(OH) 2 9×10-4**Cd 3 (PO 4 ) 2 2.53×10-33 Ag 2CO 3 8.45×10-12*Zn(OH) 2 1.2×10-17Cu 3 (PO 4 ) 2 1.40×10-37 *BaCO 35.1×10-9草酸盐FePO 4 ·2H 2 O 9.91×10-16 CaCO 33.36×10-9Ag 2 C 2 O 4 5.4×10-12*MgNH 4 PO 4 2.5×10-13 CdCO 31.0×10-12*BaC 2 O 4 1.6×10-7Mg 3 (PO 4 ) 2 1.04×10-24 *CuCO 31.4×10-10*CaC 2 O 4 ·H 2 O 4×10-9*Pb 3 (PO 4 ) 2 8.0×10-43 FeCO 33.13×10-11CuC 2 O 4 4.43×10-10*Zn 3 (PO 4 ) 2 9.0×10-33 Hg 2CO 3 3.6×10-17*FeC 2 O 4 ·2H 2 O 3.2×10-7其它盐 MgCO 36.82×10-6Hg 2 C 2 O 4 1.75×10-13*[Ag+][Ag(CN) 2 -] 7.2×10-11 MnCO 32.24×10-11MgC 2 O 4 ·2H 2 O 4.83×10-6*Ag 4 [Fe(CN) 6 ] 1.6×10-41 NiCO 31.42×10-7MnC 2 O 4 ·2H 2 O 1.70×10-7*Cu 2 [Fe(CN) 6 ] 1.3×10-16 *PbCO 37.4×10-14**PbC 2 O 4 8.51×10-10AgSCN 1.03×10-12 SrCO 35.6×10-10*SrC 2 O 4 ·H 2 O 1.6×10-7CuSCN 4.8×10-15 ZnCO 3 1.46×10-10ZnC 2 O 4 ·2H 2 O 1.38×10-9*AgBrO 3 5.3×10-5 铬酸盐硫酸盐*AgIO 3 3.0×10-8 Ag 2CrO 4 1.12×10-12*Ag 2 SO 4 1.4×10-5Cu(IO 3 ) 2 ·H 2 O 7.4×10-8 *Ag 2Cr 2 O 7 2.0×10-7*BaSO 4 1.1×10-10**KHC 4 H 4 O 6 (酒石酸氢3×10-4
物质的溶解度与温度有什么关系?与溶解度曲线有关吗? 初中化学有关溶解度与温度的关系只需明白4点 1:大部分固体溶解度随温度的上升而上升,如氯化氨,硝酸钾 2:少部分固体溶解度随温度的上升而基本不变,如氯化钠 3:少部分固体溶解度随温度的上升而下降,如含结晶水的氢氧化钙,醋酸钙 4:气体溶解度随温度的上升而下降,随压强增大而增大 既然在一定温度下,溶质在一定量的溶剂里的溶解量是有限度的,科学上是如何表述和量度这种溶解限度呢?好,那么我们就先来看一下溶解性的概念。 溶解性 通过实验的验证,在相同条件下(温度相同),同一种物质在不同的溶剂里,溶解的能力是各不相同的。我们通常把一种物质溶解在另一种物质里的能力叫做溶解性。溶解性的大小跟溶剂和溶质的本性有关。所以在描述一种物质的溶解性时,必须指明溶剂。 物质的溶解性的大小可以用四个等级来表示:易溶、可溶、微溶、难溶(不溶),很显然,这是一种比较粗略的对物质溶解能力的定性表述。 溶解度 1.固体的溶解度 从溶解性的概念,我们知道了它只是一种比较粗略的对物质溶解能力的定性表述。也许会有同学问:能不能准确的把物质的溶解能力定量地表示出来呢?答案是肯定的。这就是我们本节课所要学的溶解度的概念。 溶解度:在一定温度下,某固态物质在100g溶剂中达到饱和状态时所溶解的质量,叫做这种物质在这种溶剂中的溶解度。在这里要注意:如果没有指明溶剂,通常所说的溶解度就是物质在水里的溶解度。 用纵坐标表示溶解度,横坐标表示温度,根据物质在不同温度时溶解度数据,可以画出溶解度随温度变化的曲线,叫做溶解度曲线(Solubility curve) 大部分固体物质的溶解度随着温度升高而显著增大,如硝酸钾、硫酸铜等。有少数固体物质的溶解度受温度的影响很小,如食盐。此外,有极少数固体物质的溶解度随温度升高而减小,如硫酸锂、氢氧化钙等。 2.气体的溶解度
沉淀的溶解度及其影响因素 在利用沉淀反应进行重量分析时,要求沉淀反应进行完全,一般可根据沉淀溶解度的大小来衡量。通常,在重量分析中要求被测组分在溶液中的残留量在 1g 以内,即小于分析天平的称量允许误差。但是,很多沉淀不能满足这个条件。例如,在1 000 mL水中,BaSO4的溶解度为 3 g, 故沉淀的溶解损失是重量分析法误差的重要来源之一。因此,在重量分析中,必须了解各种影响沉淀溶解度的因素。 一、沉淀的溶解度 当水中存在1: 1型难溶化合物MA时,MA溶解并达到饱和状态后,有下列平衡关系: MA (固)MA (水)M+ + A- 式中MA (固) 表示固态的MA,MA (液) 表示溶液中的MA,在一定温度下它的活度积是一常数,即: a (M+)×a (A-) == (7—1) 式中a (M+)和a (A-)是M+和A-两种离子的活度,活度与浓度的关系是: a (M+) = (M+) ×ceq(M+);a (A—) = ( A—) ×ceq (A—)(7—2) 式中(M+)和( A—)是两种离子的活度系数,它们与溶液中离子强度有关。将式( 7 - 2 )代入 (7 – 1 )得 (M+) ceq(M+)·( A-) ceq(A-) = (7—3) 故= ceq(M+)·ceq(A—) = (7—4) 称为微溶化合物的溶度积常数,简称溶度积。 在纯水中MA的溶解度很小,则
ceq(M+) = ceq(A—) = so(7—5) ceq(M+)·ceq(A—) = so2 =(7—6) 上二式中的so是在很稀的溶液内,没有其他离子存在时MA的溶解度,由so所得溶度积非常接近于活度积。一般溶度积表中所列的是在很稀的溶液中没有其他离子存在时的数值。实际上溶解度是随其他离子存 在的情况不同而变化的。因此溶度积只在一定条件下才是一个常数。如果溶液中的离子浓度变化不太大,溶度积数值在数量级上一般不发生改变。所以在稀溶液中,仍常用离子浓度乘积来研究沉淀的情况。如果溶液中的电解质浓度较大(例如以后将讨论的盐效应对沉淀溶解度的影响),就必须用式 (7 - 3) 来考虑沉淀的情况。 对于其他类型沉淀如MmAn的溶解度公式,根据质量作用定律可推导为: = [ceq (M n+)]m·[ceq (A m-)]n =((7—7)= = = (7—8)在一定温度下,难溶电解质在纯水中都有其一定的溶度积,其数值的大小是由难溶电解质本身的性质所决定的。外界条件变化,例如酸度的变化、配位剂的存在等,都将使金属离子浓度或沉淀剂浓度发生变化,因而影响沉淀的溶解度和溶度积。这和配位滴定中,外界条件变化引起金属离子或配位剂浓度变化,因而影响稳定常数的情况相似。 二、影响沉淀溶解度的因素 影响沉淀溶解度的因素很多,如同离子效应、盐效应、酸效应及配位效应等。此外,温度、溶剂、沉淀的颗粒大小和结构,也对溶解度有影响,分别讨论如下。
一些溶剂的溶度参数[单位(cal/cm^3)^1/2] 季戊烷 6.3 四氢萘9.5 异丁烯 6.7 四氢呋喃9.5 环己烷7.2 醋酸甲酯9.6 正己烷7.3 卡必醇9.6 正庚烷7.4 二乙醚7.4 氯甲烷9.7 正辛烷7.6 二氯甲烷9.7 甲基环己烷7.8 丙酮9.8 异丁酸乙酯7.9 1,2-二氯乙烷9.8 二异丙基甲酮8.0 环己酮9.9 戊基醋酸甲酯8.0 乙二醇单乙醚9.9 松节油8.1 二氧六环9.9 环己烷8.2 二硫化碳10.0 2,2-二氯丙烷8.2 正辛醇10.3 醋酸异丁酯8.3 醋酸戊酯8.3 醋酸异戊酯8.3 丁腈10.5 甲基异丁基甲酮8.4 正己醇10.7 醋酸丁酯8.5 二戊烯8.5 异丁醇10.8 醋酸戊酯8.5 吡啶10.9 二甲基乙酰胺11.1 甲基异丙基甲酮8.5 硝基乙烷11.1 四氯化碳8.6 正丁醇11.4 环己醇11.4 哌啶8.7 异丙醇11.5 二甲苯8.8 正丙醇11.9 二甲醚8.8 二甲基甲酰胺12.1 乙酸12.6 硝基甲烷12.7 甲苯8.9 二甲亚砜12.9 乙二醇单丁醚8.9 乙醇12.9 1,2二氯丙烷9.0 甲酚13.3 异丙叉丙酮9.0 甲酸13.5 醋酸乙酯9.1 甲醇14.5 四氢呋喃9.2 二丙酮醇9.2 苯9.2 苯酚14.5 甲乙酮9.2 乙二醇16.3 氯仿9.3 甘油16.5 三氯乙烯9.3 水23.4 氯苯9.5
溶剂对聚合物溶解能力的判定 (一)“极性相近”原则 极性大的溶质溶于极性大的溶剂;极性小的溶质溶于极性小的溶剂,溶质和溶剂的极性越相近,二者越易溶。 例如:未硫化的天然橡胶是非极性的,可溶于气油、苯、甲苯等非极性溶剂中;聚乙烯醇是 极性的,可溶于水和乙醇中。 (二)“内聚能密度(CED)或溶度参数相近”原则 δ越接近,溶解过程越容易。 1、非极性的非晶态聚合物与非极性溶剂混合 聚合物与溶剂的ε或δ相近,易相互溶解; 2、非极性的结晶聚合物在非极性溶剂中的互溶性 必须在接近Tm温度,才能使用溶度参数相近原则。 例如:聚苯乙烯δ=8.9,可溶于甲苯(δ=8.9)、苯(δ=9.2)、甲乙酮(δ=9.2)、乙酸乙酯(δ=9.2)、氯仿(δ=9.2)、四氢呋喃(δ=9.2),但不溶于乙醇(δ=12.92和甲醇(δ=14.5)中以及脂肪烃(溶 度参数较低)。 混合溶剂的溶度参数δ的计算: δ混=δ1Φ1+δ2Φ2 例如:丁苯橡胶(δ=8.10),戊烷(δ1=7.08)和乙酸乙酯(δ2=9.20) 用49.5%所戊烷与50.5%的乙酸乙酯组成混合溶剂 δ混为8.10,可作为丁苯橡胶的良溶剂。 但是当聚合物与溶剂之间有氢键形成时,用溶度参数预测结果很不准确,这是因为氢键对溶 解度影响很大,此时需要三维溶度参数的概念。
溶解度表 溶解度表以化学品中特征元素的拼音顺序排列。所有数据都为1atm下的数据,单位为g/100cm3。 锕、氨、铵 物质化学式0°C 10°C 20°C 30°C 40°C 50°C 60°C 70°C 80°C 90°C 100°C 氢氧化锕(III) Ac(OH)3 0.0022 氨NH3 88.5 70 56 44.5 34 26.5 20 15 11 8 7 叠氮化铵NH4N3 16 25.3 37.1 苯甲酸铵NH4C7H5O2 20 碳酸氢铵NH4HCO3 11.9 16.1 21.7 28.4 36.6 59.2 109 170 354 溴化铵NH4Br 60.6 68.1 76.4 83.2 91.2 108 125 135 145 碳酸铵(NH4)2CO3 100 氯酸铵NH4ClO3 28.7 氯化铵NH4Cl 29.4 33.2 37.2 41.4 45.8 50.4 55.3 60.2 65.6 71.2 77.3 氯铂酸铵(NH4)2PtCl6 0.289 0.374 0.499 0.637 0.815 1.44 2.16 2.61 3.36 铬酸铵(NH4)2CrO4 25 29.2 34 39.3 45.3 59 76.1 重铬酸铵(NH4)2Cr2O7 18.2 25.5 35.6 46.5 58.5 86 115 156 砷酸二氢铵NH4H2AsO4 33.7 48.7 63.8 83 107 122 磷酸二氢铵NH4H2PO4 22.7 39.5 37.4 46.4 56.7 82.5 118 173 氟硅酸铵(NH4)2SiF6 18.6 甲酸铵NH4HCO2 102 143 204 311 533