
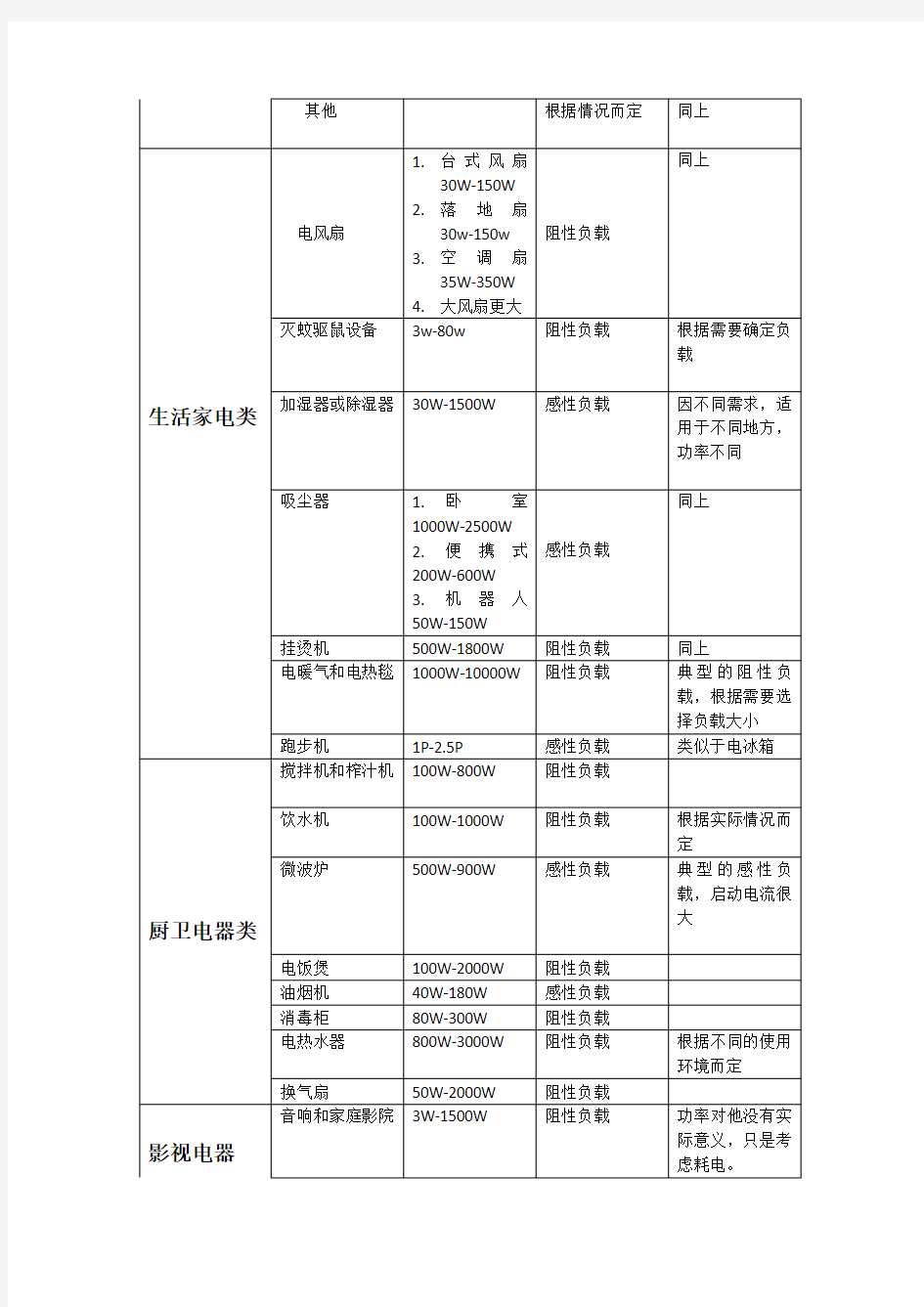
常用电器负载性质分类
阻性负载:
通俗一点讲,电阻类元件进行工作的纯阻性负载称为“阻性负载”。阻性负载的特点是,电流和电压同步变化,相位差为“零度”,工作时会产生热量(焦耳热),常见的阻性负载有电炉、电热杯、电热毯、饮水机、白炽灯等,还有电吹风中用于加热(吹热风)的部分也是阻性负载,事实上,几乎所有依靠加热来工作的电器都是阻性电器,阻性负载的最大危险就在于发热并有可能引发火灾,安装用电识别器最重要的目的也在于防止由于阻性电器发热酿成火灾。
容性负载:
一般把带电容参数的负载,即符合电压滞后电流特性的负载称为容性负载。容性负载的特点是,电压的变化落后于电流的变化,完美的容性负载相位差为“负90度”,是不会产生任何热量的。
感性负载:
通常情况下,一般把带电感参数的负载,即符合电压超前电流特性的负载,称为感性负载。通俗地说,即应用电磁感应原理制作的大功率电器产品,如电动机、压缩机、继电器、日光灯等等。这类产品在启动时需要一个比维持正常运转所需电流大得多(大约在3-7倍)的启动电流。例如,一台在正常运转时耗电150瓦左右的电冰箱,其启动功率可高达1000瓦以上。此外,由于感性负载在接通电源或者断开电源的一瞬间,会产生反电动势电压,这种电压的峰值远远大于车载交流供电器所能承受的电压值,很容易引起车用逆变器的瞬时超载,影响逆变器的使用寿命。因此,这类电器对供电
体分析。
讲稿几点错误:
——蓄电池放电深度, 一般为0.5-0.8
1.β
A
β
电池温度系数,一般为1.0~1.2
B ——
蓄电池放电深度, 一般为0.5-0.8 改为:β
B ——
——电池温度系数,一般为1.0~1.2
β
A
2.H——负载日使用时间
改为:H——峰值日照时间(h为负载使用时间)销售部刘威
2012.8.17
兰州交通大学博文学院教案 课题: 第一章土的物理性质及工程分类 一、教学目的:1.了解土的生成和工程力学性质及其变化规律; 2.掌握土的物理性质指标的测定方法和指标间的相互转换; 3.熟悉土的抗渗性与工程分类。 二、教学重点:土的组成、土的物理性质指标、物理状态指标。 三、教学难点:指标间的相互转换及应用。 四、教学时数: 6 学时。 五、习题:
第一章土的物理性质及工程分类 一、土的生成与特性 1.土的生成 工程领域土的概念:土是指覆盖在地表的没有胶结和弱胶结的颗粒堆积物,土与岩石的区分仅在于颗粒胶结的强弱,土和石没有明显区分。 土的生成:岩石在各种风化作用下形成的固体矿物、流体水、气体混合物。 不同风化形成不同性质的土,有下列三种: (1)物理风化:只改变颗粒大小,不改变矿物成分。由物理风化生成土为粗粒土(如块碎石、砾石、砂土),为无粘性土。 (2)化学风化:矿物发生改变,生成新成分—次生矿物。由化学风化生成土为细粒土,具有粘结力(粘土和粘质粉土),为粘性土。 (3)生物风化:动植物与人类活动对岩体的破坏。矿物成分没有变化。 2.土的结构和构造 (1)土的结构 定义:土颗粒间的相互排列和联结形式称为土的结构。 1)种类: ●单粒结构:每一个颗粒在自重作用下单独下沉并达到稳态。 ●蜂窝结构:单个下沉,碰到已下沉的土颗粒,因土粒间分子引力大于重力不再下沉,形成大孔隙蜂窝状结构。 ●絮状结构:微粒极细的粘土颗粒在水中长期悬浮,相互碰撞吸引形成小链环状土集粒。小链之间相互吸引,形成大链环,称絮状结构。 图1.1 土的结构 3)工程性质: 密实的单粒结构工程性质最好,蜂窝结构与絮状结构如被扰动破坏天然结构,则强度低、压缩性高,不可用做天然地基。
四、无黏性土的物理性质 无黏性土主要是指砂土和碎石土,其工程性质与其密实度密切相关。密实度越大,土的强度越大。因此,密实度是反映无黏性土工程性质的主要指标。 评判无黏性土的密实度有以下方法:1、根据相对密实度 Dr (大小位于0~1 之间)判别: 密实( 1 ≥Dr≥0 . 67 );中密( 0 . 67≥Dr≥0 . 33 );松散( 0 . 33 ≥ Dr ≥0 )。该法适用于透水性好的无黏性土,如纯砂、纯砾。 2、根据天然孔隙比e判别: e越小,土越密实。一般,e< 0 . 6 时属密实,e> 1 . 0 时属疏松。该法适用于砂土,但不能考虑矿物成分、级配等对密实度的影响。 3、根据原位标准贯入试验判别: 密( N > 30 )、中密( 15 ≤N≤ 30 )、稍密( 10≤N≤15 )、松散( N≤10 ) 原位标准贯入试验:在土层钻孔中,利用重63.5kg的锤击贯入器,根据每贯入30cm所
需锤击数来判断土的性质,估算土层强度的一种动力触探试验。 4、根据野外方法鉴别(针对碎石类土) 肉眼观察、挖、钻等。 五、黏性土的物理性质 黏性土的特性主要是由于黏粒与水之间的相互作用产生,因此含水量是决定因素。黏性土的含水量对其物理状态和工程性质有重要影响。 液限(ωL, Liqud Limit ):土由可塑状态变到流动状态的界限含水量;土处于可塑状态的最大含水量,稍大即流态; 塑限(ωP, Plastic Limit ):土由半固态变为可塑状态的界限含水量;土处于可塑状态的最小含水量,稍小即半固态; 缩限(ωS , Shrinkage Limit ):土由固态变为半固态的界限含水量;土处于半固态的最小含水量,稍小即为固态。 塑性指数IP ―表示土处于可塑状态的含水量变化范围。 IP 越大,土处于可塑状态的含水量范围也越大。
物质的组成、性质和分类: (一)掌握基本概念 1.分子 分子是能够独立存在并保持物质化学性质的一种微粒。 (1)分子同原子、离子一样是构成物质的基本微粒. (2)按组成分子的原子个数可分为: 单原子分子如:He、Ne、Ar、Kr… 双原子分子如:O2、H2、HCl、NO… 多原子分子如:H2O、P4、C6H12O6… 2.原子 原子是化学变化中的最小微粒。确切地说,在化学反应中原子核不变,只有核外电子发生变化。 (1)原子是组成某些物质(如金刚石、晶体硅、二氧化硅等原子晶体)和分子的基本微粒。 (2)原子是由原子核(中子、质子)和核外电子构成的。 3.离子 离子是指带电荷的原子或原子团。 (1)离子可分为: 阳离子:Li+、Na+、H+、NH4+… 阴离子:Cl–、O2–、OH–、SO42–… (2)存在离子的物质: ①离子化合物中:NaCl、CaCl2、Na2SO4… ②电解质溶液中:盐酸、NaOH溶液…
③金属晶体中:钠、铁、钾、铜… 4.元素 元素是具有相同核电荷数(即质子数)的同—类原子的总称。 (1)元素与物质、分子、原子的区别与联系:物质是由元素组成的(宏观看);物质是由分子、原子或离子构成的(微观看)。 (2)某些元素可以形成不同的单质(性质、结构不同)—同素异形体。 (3)各种元素在地壳中的质量分数各不相同,占前五位的依次是:O、Si、Al、Fe、Ca。 5.同位素 是指同一元素不同核素之间互称同位素,即具有相同质子数,不同中子数的同一类原子互称同位素。如H有三种同位素:11H、21H、31H(氕、氘、氚)。 6.核素 核素是具有特定质量数、原子序数和核能态,而且其寿命足以被观察的一类原子。 (1)同种元素、可以有若干种不同的核素—同位素。 (2)同一种元素的各种核素尽管中子数不同,但它们的质子数和电子数相同。核外电子排布相同,因而它们的化学性质几乎是相同的。 7.原子团 原子团是指多个原子结合成的集体,在许多反应中,原子团作为一个集体参加反应。原子团有几下几种类型:根(如SO42-、OHˉ、CH3COOˉ等)、官能团(有机物分子中能反映物质特殊性质的原子团,如—OH、—NO2、—COOH等)、游离基(又称自由基、具有不成价电子的原子团,如甲基游离基·CH3)。 8.基 化合物中具有特殊性质的一部分原子或原子团,或化合物分子中去掉某些原子或原子团后剩下的原子团。 (1)有机物的官能团是决定物质主要性质的基,如醇的羟基(—OH)和羧酸的羧基(—COOH)。 (2)甲烷(CH4)分子去掉一个氢原子后剩余部分(·CH3)含有未成对的价
专题13 圆的基本性质 考纲要求: 1.理解圆、弧、弦、圆心角、圆周角的概念;了解等圆、等弧的概念. 2.了解弧、弦、圆心角的关系;理解圆周角与圆心角及其所对弧的关系. 3.能利用圆的有关概念、垂径定理、圆周角定理及其推论解决有关简单问题. 基础知识回顾: 知识点一:圆的有关概念 1.与圆有关的概念和性质(1)圆:平面上到定点的距离等于定长的所有点组成的图形.如图所示的 圆记做⊙O. (2)弦与直径:连接圆上任意两点的线段叫做弦,过圆心的弦叫做直径,直径是圆内最长的弦. (3)弧:圆上任意两点间的部分叫做弧,小于半圆的弧叫做劣弧,大于半圆的弧叫做优弧. (4)圆心角:顶点在圆心的角叫做圆心角. (5)圆周角:顶点在圆上,并且两边都与圆还有一个交点的角叫做圆周角. (6)弦心距:圆心到弦的距离. 知识点二:垂径定理及其推论 2.垂径定理及其推论定理垂直于弦的直径平分这条弦,并且平分弦所对的两条弧. 推论 (1)平分弦(不是直径)的直径垂直于弦,并且平分弦所对的两条弧; (2)弦的垂直平分线经过圆心,并且平分弦所对的两条弧. 延伸 根据圆的对称性,如图所示,在以下五条结论中:
① 弧AC=弧AD; ②弧BC=弧BD ; ③CE=DE; ④AB ⊥CD;⑤AB 是直径. 只要满足其中两个,另外三个结论一定成立,即推二知三. 知识点三 :圆心角、弧、弦的关系 3.圆心角、 弧、弦 的关 系 定理 在同圆或等圆中,相等的圆心角所对的弧相等,所对的弦相等. 推论 在同圆或等圆中,如果两个圆心角、两条弧、两条弦中有一组量相等,那么它们所对应的其余各组量都分别相等. 知识点四 :圆周角定理及其推论 4.圆周 角定 理及其推论 (1)定理:一条弧所对的圆周角等于它所对的圆心角的一半. 如图a ,∠A= 12∠O. 图a 图b 图c ( 2 )推论: ① 在同圆或等圆中,同弧或等弧所对的圆周角相等.如图b ,∠A=∠C. ② 直径所对的圆周角是直角.如图c ,∠C=90°. 圆内接四边形的对角互补.如图a ,∠A+∠C=180°,∠ABC+∠ADC=180°. 应用举例: 招数一、垂径定理及其推论 【例1】13的O 中,弦AB 与CD 交于点E ,75DEB ∠=?,6AB =,1AE =,则CD 的长是( )
高中化学:物质的组成、性质和分类知识点 考点1 物质的组成 1.元素——宏观概念,说明物质的宏观组成。 元素是质子数相同的一类原子的统称。质子数相同的微粒不一定是同一种元素,因为微粒的含义要比原子广泛。 2.分子、原子、离子——微观概念,说明物质的微观构成。 (1)分子是保持物质化学性质的一种微粒。(单原子分子、双原子分子、多原子分子) (2)原子是化学变化中的最小微粒。(不是构成物质的最小微粒) (3)离子是带电的原子或原子团。(基:中性原子团) 3.核素——具有一定数目的质子和一定数目的中子的一种原子 同位素——具有相同质子数和不同中子数的原子互称为同位素 同素异形体——同种元素形成的结构不同的单质 特别提醒: 1.离子与基团: 2.同位素与同素异形体: [知识规律] 物质到底是由分子、原子还是离子构成?这与物质所属的晶体类型有关。如金刚石(C)、晶体Si都属原子晶体,其晶体中只有原子;NaCl、KClO3属离子晶体,其晶体中只有阴阳离子;单质S、P4属分子晶体,它们是由原子形成分子,进而构成晶体的。具体地: (1)由分子构成的物质(分子晶体): ①非金属单质:如H2、X2、O2、O3、N2、P4、S、C60、稀有气体等 ②非金属氢化物:如HX、H2O、NH3、H2S等 ③酸酐:如SO2、CO2、SO3、P2O5、N2O5 等 ④酸类:如HClO4、HClO、H2SO4、H3PO4、H2SiO3等 ⑤有机物:如烃类、烃的衍生物、糖类、氨基酸等 ⑥其它:如NO、N2O4、Al2Cl6等 (2)由原子直接构成的物质(原子晶体):稀有气体、金刚石、晶体硅、二氧化硅、碳化硅、石墨(混合型晶体)等; (3)由阴阳离子构成的物质(离子晶体):绝大多数盐、强碱、低价金属氧化物。 (4)由阳离子和自由电子构成的物质(金属晶体):金属单质、合金
第六章 圆的有关性质 本章进步目标 ★★★★☆☆ Level 4 通过对本节课的学习,你能够: 1.对圆的有关概念及垂径定理达到【初级运用】级别; 2.对弧、弦、圆心角关系达到【初级运用】级别; 3.对圆周角定理达到【初级运用】级别。 VISIBLE PROGRESS SYSTEM 进步可视化教学体系 73 VISIBLE PROGRESS SYSTEM
74 VISIBLE PROGRESS SYSTEM
第一关圆的有关概念及垂径定理 ★★★★☆☆Level 4 本关进步目标 ★★☆☆☆☆你能够掌握圆有关的概念及性质; ★★★★☆☆你能够理解垂径定理,会根据垂径定理解决运用问题。 75 VISIBLE PROGRESS SYSTEM
76 VISIBLE PROGRESS SYSTEM 学习重点:掌握与圆有关的概念以及性质. 1.(1)弦是直径( ) (2)半圆是弧( ) (3)过圆心的线段是直径( ) (4)过圆心的直线是直径( ) (5)半圆是最长的弧( ) (6)直径是最长的弦( ) (7)圆心相同,半径相等的两个圆是同心圆( ) (8)半径相等的两个圆是等圆( ) (9)等弧就是拉直以后长度相等的弧( ) 2.下列说法正确的是( ) A .长度相等的弧是等弧 B .优弧大于劣弧 C .直径是一个圆中最长的弦 D .同圆或等圆中的弦一定相等 圆的有关概念【初级理解】 知道与圆有关的概念 会识别并区分相关概念 关卡1-1 圆的有关概念 过关指南 Tips 笔记 ★★☆☆☆☆ 初级理解 例题
77 VISIBLE PROGRESS SYSTEM 下列命题正确的有( ) ①半径是弦;②直径是最长的弦;③在同一平面内,到定点距离等于定长的点都在同一个圆上。 A .0个 B .1个 C .2个 D .3个. 下列说法中正确的序号是_________________. ①直径相等的两个圆是等圆;②长度相等的两条弧是等弧;③圆中最长的弦是通过圆心的弦;④一条弦把圆分成两条弧,这两条弧不可能是等弧. 下列说法正确的是( ) A .弦是圆上两点间的部分 B .弧比弦大 C .劣弧比半圆小 D ..弧是半圆 过关练习 错题记录 Exercise 2 错题记录 Exercise 1 错题记录 Exercise 3
第一章土的物理性质及工程分类 一、思考题 1、土是由哪几部分组成的? 2、建筑地基土分哪几类?各类土的工程性质如何? 3、土的颗粒级配是通过土的颗粒分析试验测定的,常用的方法有哪些?如何判断土的级配情况? 4、土的试验指标有几个?它们是如何测定的?其他指标如何换算? 5、粘性土的含水率对土的工程性质影响很大,为什么?如何确定粘性土的状态? 6、无粘性土的密实度对其工程性质有重要影响,反映无粘性土密实度的指标有哪些? 二、选择题 1、土的三项基本物理性质指标是() A、孔隙比、天然含水率和饱和度 B、孔隙比、相对密度和密度 C、天然重度、天然含水率和相对密度 D、相对密度、饱和度和密度 2、砂土和碎石土的主要结构形式是() A、单粒结构 B、蜂窝结构 C、絮状结构 D、层状结构 3、对粘性土性质影响最大的是土中的( ) A、强结合水 B、弱结合水 C、自由水 D、毛细水 4、无粘性土的相对密实度愈小,土愈() A、密实 B、松散 C、居中 D、难确定 5、土的不均匀系数C u 越大,表示土的级配() A、土粒大小不均匀,级配不良 B、土粒大小均匀,级配良好 C、土粒大小不均匀,级配良好 6、若某砂土的天然孔隙比与其能达到的最大孔隙比相等,则该土() A、处于最疏松状态 B、处于中等密实状态 C、处于最密实状态 D、无法确定其状态 7、无粘性土的分类是按() A、颗粒级配 B、矿物成分 C、液性指数 D、塑性指数 8、下列哪个物理性质指标可直接通过土工试验测定() A、孔隙比 e B、孔隙率 n C、饱和度S r D、土粒比重 d s 9、在击实试验中,下面说法正确的是() A、土的干密度随着含水率的增加而增加 B、土的干密度随着含水率的增加而减少 C、土的干密度在某一含水率下达到最大值,其它含水率对应干密度都较小 10、土粒级配曲线越平缓,说明()
《专题一物质的组成、性质和分类化学用语》〉 【专题要点】 物质的组成、性质和分类、化学用语是化学最基础的主干知识,是对物质及其变化的本质特征的反映。它们涉及的化学概念、物质的分类方法和它们相互转化的方式,是中学化学最基本的知识,也是学生从化学视觉观察和思考问题的必备知识,同时也是高考的重点内容。复习本考点是应深刻理解化学概念的内涵和外延,掌握不同概念间的区别和联系,掌握物质的分类方法及物质间相互转化的方式和转化条件;要理解各个化学用语的的实际含义,掌握反应的条件与本质,正确、科学、规范的进行运用。本考点在高考中的题型主要以选择题为主,常常结合元素化合物来进行考查。从09年和08年高考考题来看高考题除了直接考查基本概念外,还考查以物质组成和分类的概念为出发点,以反映高新科技和人们普遍关注的社会问题为切入点,逐步向环保、高科技、生产等方面渗透发展。除此之外我们还可以看出来元素、物质的组成与分类、化学用语,以成为高考的一个热点,而且融入其他专题进行考查。 【考纲要求】 1.理解分子、原子、离子、元素等概念的涵义,初步了解原子团的定义。 2.理解物理变化与化学变化的区别和联系 3.理解混合物和纯净物、单质和化合物、金属和非金属的概念 4.了解同素异形体的概念,注意其与同位素、同系物、同分异构体等的区别。 5.理解酸、碱、盐、氧化物的概念及其相互联系。 6. 熟记并正确书写常见元素的名称、符号、离子符号 7. 熟悉常见元素的化合价。能根据化合价正确书写化学式(分子式),或根据化学式判断化合价。 8. 了解原子结构示意图、分子式、结构式和结构简式的表示方法 9. 掌握溶液、悬浊液、乳浊液、胶体的概念,区别及鉴别它们的方法; 10.掌握胶体的本质特征及性质; 【教法指引】 复习此专题时要做到―准确‖、―系统‖、―灵活‖,可以从三点入手: 1.以高考的热点、考点、难点为依据,合理设置复习内容和练习题,熟练掌握解题思路、注 重方法、技巧,不求面面俱到,但求在某些考点的深度和广度的挖掘上有所突破 2.加强区别相似概念的异同,理顺不同概念间的联系,进而形成连贯的知识系统。
物质的组成、性质和分类 最新考纲 考向分析考点一物质的组成和分类 Z 真题感悟 hen ti gan wu (课前) 1.(2017·北京·6)古丝绸之路贸易中的下列商品,主要成分属于无机物的是(A) A.瓷器B.丝绸C.茶叶D.中草药 属于有机物,B项错误;茶叶的主要成分为茶多酚(属于酚类)、生物碱、氨基酸、有机酸等,属于有机物,C项错误;中草药成分复杂,通常含有糖类、氨基酸、蛋白质、油脂、维生素、有机酸、生物碱等,其主要成分属于有机物,D项错误。 2.(2018·江苏·6)下列有关物质性质的叙述一定不正确的是(A) A.向FeCl2溶液中滴加NH4SCN溶液,溶液显红色 B.KAl(SO4)2·12H2O溶于水可形成Al(OH)3胶体 C.NH4Cl与Ca(OH)2混合加热可生成NH3 D.Cu与FeCl3溶液反应可生成CuCl2 [解析]A错:Fe3+遇SCN-溶液显红色。 3.(2018·江苏·3)下列有关物质性质与用途具有对应关系的是(D) A.NaHCO3受热易分解,可用于制胃酸中和剂 B.SiO2熔点高硬度大,可用于制光导纤维
C.Al2O3是两性氧化物,可用作耐高温材料 D.CaO能与水反应,可用作食品干燥剂 [解析]D对:CaO无毒,能与水反应生成Ca(OH)2,常用作食品干燥剂。A错:NaHCO3能与胃酸中的盐酸反应,可用于中和胃酸,但与NaHCO3受热易分解无关。B错:SiO2制光导纤维是利用了SiO2可以对光进行折射和全反射,与其熔点和硬度无关。C错:Al2O3的熔点很高,可用作耐高温材料,与Al2O3的两性无关。 4.(2016·全国Ⅱ·26)联氨(又称肼,N2H4,无色液体)是一种应用广泛的化工原料,可用作火箭燃料。回答下列问题: (1)联氨分子的电子式为,其中氮的化合价为_-2__。 (2)实验室中可用次氯酸钠溶液与氨反应制备联氨,反应的化学方程式为2NH3+NaClO===N2H4+NaCl+H2O。 [解析](1)N2H4中原子间以共价键结合,其电子式为。N2H4中H为+1价,由各元素化合价代数和为0,可确定N为-2价。(2)反应中NaClO和NH3分别作氧化剂和还原剂,根据得失电子守恒和原子守恒可写出并配平相应的化学方程式。 R 弱点突破 uo dian tu po (课堂) 知能补漏 1.警惕物质组成、分类中的“四大误区” (1)误认为由同种元素组成的物质一定是纯净物。 ①某物质可能由一种元素的不同单质混合而成。如O2、O3组成的混合气体就是混合物。 ②分子式相同的化合物可能存在同分异构体。如C4H10的结构有两种,正丁烷和异丁烷,二者组成混合物。 (2)误认为能电离出H+的物质一定是酸。如NaHSO4是一种盐。 (3)误认为酸性氧化物一定是非金属氧化物。如Mn2O7是金属氧化物但属于酸性氧化物,而且非金属氧化物也不一定属于酸性氧化物,如CO、NO为不成盐氧化物等。 (4)误认为金属氧化物一定是碱性氧化物。如Al2O3属于两性氧化物,Na2O2属于过氧化物。 2.拓展延伸 高中化学涉及的基本概念比较多,可设题的角度还有: (1)反应类型:四大基本反应类型、氧化还原反应等。 (2)物质概念:电解质和非电解质,强电解质和弱电解质,溶液、胶体和浊液,酸性氧
《圆的基本性质复习课》教案 潮阳区华阳初级中学陈朝鸿 复习目标 1、使学生理解圆及其有关概念,圆的性质; 2、使学生掌握垂径定理及推论的应用;掌握圆心角、弧、弦、弦心距的关系;理解圆周角定理及其推论,圆内接四边形的性质定理; 3、使学生理解圆的对称性(轴对称和中心对称); 复习重点 1、垂径定理及推论; 2、圆心角、弧、弦、弦心距之间的关系; 3、圆周角的定理及其推论; 4、与性质相关的计算。 复习难点 1、垂径定理及推论; 2、圆心角与圆周角之间的关系以及圆周角的相关性质; 3、圆心角、弧、弦、弦心距之间的关系。 4、与性质相关的综合计算 目标分析 新课程标准的总体目标,即:知识与技能,过程与方法,情感、态度与价值观三位一体的目标,它们对人的成长、素养的形成与发展都具有十分重要的作用。过程与方法和情感、态度与价值观的发展离不开知识与技能的学习,同时,知识与技能的学习培养必须要以有利于其他目标的实现为前提。 教学过程 教学环节教师活动学生活动设计意图 (一)课前反馈用多媒体小试卷的形式: 展示自主学习案习题:1.在一个平面内,线段OA绕的一个端 点O旋转一周,所形成的图形叫做圆,固定的叫做, 线段叫做。 2.连接圆上任意两点的线段叫;经过圆心的弦叫 ; 圆上任意两点间的部分叫 ;大于半圆的弧叫 ;小于 半圆的弧叫。 3.外接圆的圆心是三角形三条垂直平分线的交点,叫三角形的外 心,锐角三角形的外心在三角形的,钝角三角形的外心在 三角形的,直角三角形的外心在三角形。 4. 圆是一个特殊的图形,它既是一个对称图形,又是一个对 称图形。 5.垂径定理:垂直于弦的直径平分这条弦,并且平分弦所对的两 条弧; 6.推论:(1)平分弦(非直径)的直径垂直于弦,并且平分弦所 对的弧;(2)弦的垂直平分线经过圆心,并且平分弦所对的弧; (3)平分弦所对的一条弧的直径,垂直平分弦,并且平分弦所对 的另一条弧;(4)圆的两条平行弦所夹的弧相等。 参与习 题的解 答。 使学生 对所学的 圆的性质 有一个较 系统的回 顾。
第二章 化学物质及其变化 物质的组成、性质和分类 一、物质的组成 1.元素、物质及微粒间的关系 (1)宏观上物质是由元素组成的,微观上物质是由______、______或______构成的。 (宏观组成只讲种类不讲个数,微观组成既讲种类又讲个数) (2)元素:具有______________的一类原子的总称。 (3)元素与物质的关系 元素――→组成? ?? 单质: 的纯净物。化合物: 的纯净物。 (4)元素在物质中的存在形态 ①游离态:元素以________形式存在的状态。 ②化合态:元素以________形式存在的状态。 (5)元素、物质及微粒间的关系如右图所示: 二、物质的分类 1.简单分类法概述:分类是学习和研究化学物质及其变化的一种常用科学方法。 2.分类法:常用的两种是_______ ___法和____________法。 3.物质的分类: 注意:由同种元素组成的物质不一定是纯净物,如氧气和臭氧的混合气体,金刚石和石墨的混合物。 4.无机化合物的树状分类
三、分散系、胶体 1.分散系 (1)概念:__________________________________________所得到的体系。 (2)分类: 分类标准:根据对分散系进行分类,共有三种类型(见下图):根据分类标准在数轴上填写分散系名称。 2.胶体
(1)定义:分散质粒子直径介于____________之间的分散系。 (2)分类:按分散剂划分??? ① :如AgI 胶体② :如烟水晶③ :如烟、雾、云 按分散系颗粒的情况划分: (3) 胶体的性质 ①丁达尔效应:用一束光通过盛有Fe(OH)3胶体的烧杯时,在与光束垂直的方向上 进行观察,可以看到__________________,这个现象称作____________,这是由于胶体微粒对可见光的散射而形成的。丁达尔效应可用于区别________和________。 ②电泳:在________的作用下,胶体微粒作________移动,这种现象称为电泳,电 泳现象说明________带电荷。利用电泳可进行工厂除尘。 ③聚沉:胶体形成沉淀析出的现象称为聚沉:三角洲的形成、明矾净水、盐卤点豆 腐都是胶体聚沉现象。胶体聚沉的条件有:a.____________;b.__________;c._________ __________。 (4) Fe(OH)3胶体的制备 向沸水中逐滴加入____________,继续煮沸至液体呈____________,停止加热,即制得Fe(OH)3胶体,化学方程式为__________ ___________________。 (5)由于胶粒半径较大不能透过半透膜,而离子、小分子半径较小可透过半透膜, 可以用 渗析的方法对胶体进行提纯 四、三类分散系的比较 五、物质的性质和变化
1.(重庆市名校联盟2014届高三联合考试化学试卷)化学与生活、生产、航天、航海等诸多领域相关。下列有关上述领域的描述不正确的是() A. 在太空舱可以实现过滤和分液的实验操作 B. 在海轮外壳上镶入铜块,可加速船体的腐蚀速率 C. 我国首艘航母“辽宁舰” 上用于舰载机降落的拦阻索是特种钢缆,属于金属材料 D. 石英光导纤维,在遇到强碱时可能发生“断路” 难易度:容易 答案: A 2.解读:在太空舱里没有地球引力,处于失重状态,在失重状态下不能实现过滤和分液的实验操作,A项错误;Cu与Fe构成原电池时,Fe的活泼性比Cu强,Fe作负极被腐蚀,所以在海轮外壳上镶入铜块,可加速船体的腐蚀速率,B项正确;特种钢缆是铁的合金,属于金属材料,C项正确;石英的主要成分是二氧化硅,二氧化硅能与强碱反应生成硅酸盐和水,所以石英光导纤维,在遇到强碱时可能发生“断路” ,D(天津市蓟县第二中学2014届 高三第一次模拟考试化学试卷)下列对生产、生活有关化学问题的分析正确的是() A. 医疗上进行胃部造影前,患者服用的“钡餐” 是BaCO3等不溶于水的物质 B. 铝合金的大量使用归功于人们能用焦炭等还原剂从氧化铝中获取铝 C. 明矾净水是利用了Al3+的水解性和氧化性 D. 液氯罐中的液氯泄漏时,可将其移入水塘中,并向水塘中加入生石灰 难易度:容易 答案:D 解读:碳酸钡与胃酸中的盐酸反应生成的可溶性氯化钡有剧毒,所以碳酸钡不能用作钡餐,A项错误;铝的冶炼应用电解氧化铝法,不能用热还原法,B项错误;明矾净水是利用了Al3+的水解生成的氢氧化铝胶体的吸附性净水,C项错误;生石灰和水反应生成氢氧化钙,氯气有毒,氯气和氢氧化钙反应生成无毒的氯化钙、次氯酸钙和水,从而降低氯气的毒性,D项正确。
物质的组成、分类、变化和性质 双基训练 *1. 下列物质中,有固定的熔、沸点的是( )。【1】(方括号中所示数字为完成该题所需的大致时间,单位分。下同。 (A)碘酒 (B)花生油 (C)油酸 (D)福尔马林 *2. 下列物质中,不含结晶水的是( )。【1】 (A)芒硝 (B)大理石 (C)明矾 (D)生石膏 *3. 下列物质由固定元素组成的是( )。【1】 (A)空气 (B)石蜡(C)氨水(D)二氧化氮气体 *4. 下列各组俗称表示同一种物质的是( )。(1999年上海市高考试题)【1】 (A)苏打、小苏打 (B)胆矾、绿矾 (C)三硝酸甘油酯、硝化甘油 (D)纯碱、烧碱 **5. 下列选项中,说明乙醇作为燃料的优点的是( )。(2002年上海市高考理科综合试题) 【1】 ①燃烧时发生氧化反应②充分燃烧时产物不污染环境③乙醇是一种再生能源④燃烧时放出大量热量 (A)①②③ (B)①②④ (C)①③④ (D)②③④ **6. 航天飞机用铝粉与高氯酸铵(NH 4ClO 4)的混合物为固体燃料,点燃时铝粉氧化放热引发高氯酸铵反应,其化学方程式可表示为:2NH 4ClO 4 = N 2↑+4H 2O+Cl 2↑+2O 2↑+Q ,下列对此反应的叙述中,错误的是( )。(2002年上海市高考理科综合试题)【1】 (A)上述反应属于分解反应 (B)上述反应瞬间产生大量高温气体,推动航天飞机飞行 (C)反应从能量变化上说,主要是化学能转变为热能和动能 (D)在反应中,高氯酸铵只起氧化剂作用 **7. 1999年度诺贝尔化学奖授予了开创“飞秒(10-15s)化学”新领域的科学家,使运用激光光谱技术观测化学反应时分子中原子运动成为可能。你认为该技术不能观察到的是( )。 【1】 (A)原子中原子核的内部结构 (B)化学反应中原子的运动 (C)化学反应中生成物分子的形成 (D)化学反应中反应物分子的分解 **8. 上海环保部门为了使城市生活垃圾得到合理利用,近年来逐步实施了生活垃圾分类投放的办法。其中塑料袋、废纸、旧橡胶制品等属于( )。(2003年上海市高考试题)【1】 (A)无机物 (B)有机物 (C)盐类 (D)非金属单质 纵向应用 ***1. 某元素氧化物的相对分子质量为a ,其相同价态硫酸盐的相对分子质量为b ,则该元素的化合价数值不可能是( )。【2】 (A)20a b - (B)40b a - (C)20b a - (D)80 b a - ***2. 1995年12月8日,在克拉玛依特大火灾中有288名中小学生葬身火海,灾难震惊国人。为此,专家呼吁:每个人都应懂得防火知识,学会如何逃生。当高层楼房下层起火,火热凶猛无法扑灭时,下列逃生措施中正确的是( )。【1】 ①沿楼梯迅速下楼 ②用湿毛巾堵住口鼻 ③匍匐前进,寻找安全出口 ④封闭房门 ⑤迅速转移到阳台,用绳索下坠 ⑥跳楼 (A)①②③④ (B)②③④⑤ (C)③④⑤⑥ (D)①②④⑤
第一讲物质的组成、性质和分类 1.了解分子、原子、离子和原子团等概念的含义。 2.理解物理变化与化学变化的区别与联系。 3.理解混合物和纯净物、单质和化合物、金属 和非金属的概念。 4.理解酸、碱、盐、氧化物的概念及其相互联 系。 5.了解胶体是一种常见的分散系,了解溶液和 胶体的区别。 2016,卷甲 13T(A); 2015,卷Ⅰ 7T ;2015,卷Ⅱ 7T ; 2014,卷Ⅱ 7T 物质的组成与分类 [学生用书P27] [知识梳理] 一、元素、微粒及物质间的关系 1.宏观上物质是由元素组成的,微观上物质是由分子、原子或离子构成的。2.元素:具有相同核电荷数(即质子数)的一类原子的总称。3.元素与物质的关系 元素A――→ 组成 单质:只由一种元素组成的纯净物化合物:由多种元素组成的纯净物 4.元素在物质中的存在形态 (1)游离态:元素以单质形式存在的状态。(2)化合态:元素以化合物形式存在的状态。5.混合物和纯净物
(1)纯净物:由同种单质或化合物组成的物质。 (2)混合物:由几种不同的单质或化合物组成的物质。 6.同素异形体 (1)同种元素形成的不同单质叫同素异形体。同素异形体的形成有两种方式:①原子个数不同,如O2和O3;②原子排列方式不同,如金刚石和石墨。 (2)同素异形体之间的性质差异主要体现在物理性质上,同素异形体之间的转化属于化学变化,但不属于氧化还原反应。 7.元素、微粒及物质间的关系图 二、物质的分类 1.交叉分类法——从不同角度对物质进行分类(如图为氧化物的分类) 2.树状分类法——按不同层次对物质进行逐级分类,各层之间属于包含关系。 [自我检测] 1.判断下列说法是否正确,若不正确,说出理由。 (1)元素在自然界中的存在形式有原子、分子或离子。 (2)在化学变化中,分子可以再分,离子和原子不可以再分。
土层的工程分类及性质 一、土的工程分类 在建筑施工中,按照开挖的难易程度,土可分为八类:一类土(松软土)、二类土(普通土)、三类土(坚土)、四类土(砂砾坚土)、五类土(软石)、六类土(次坚石)、七类土(坚石)、八类土(特坚石)。一至四类为土,五至八类为岩石。 二、土的工程性质 1、土的密度 (1)土的天然密度土在天然状态下单位体积的质量,称为土的天然密度。 (2)土的干密度单位体积中土的固体颗粒的质量称为土的干密度。注:土的干密度越大,表示土越密实。工程上把土的干密度作为评定土体密实程度的标准,以控制基坑底压实及填土工程的压实质量。 2、土的含水量 土的含水量是土中水的质量与固体颗粒质量之比,以百分数表示。注:土的干湿程度用含水量表示。5%以下称干土、5%—30%称潮湿土、30%以上称湿土。含水量越大,土就越湿,对施工越不利。 3、土的可松性 自然状态下的土经开挖后,其体积因松散而增大,以后虽经回填压实,其体积仍不能恢复原状,这种性质称为土的可松性。土的可松性程度用可松性系数表示。
4、土的渗透性 土的渗透性指水流通过土中孔隙的难易程度,水在单位时间内穿透土层的能力称为渗透系数,用表示,单位为。注:土的渗透性大小取决于不同的土质。地下水的流动以及在土中的渗透速度都与土的渗透性有关。 下面来介绍一下,岩石风化。一般情况下,岩体的风化程度呈现出由表及里逐渐减弱的规律。但由于岩体中岩性并不均一,且有断裂存在,所以岩体风化的情况并不一定完全符合一般规律。岩体风化厚度一般为数米至数十米,沿断裂破碎带和易风化岩层,可形成风化较剧的岩层。断层交会处还可形成风化囊。在这两种情况下深度可超过百米。岩体风化分为:①物理风化,如气温变化使岩石胀缩导致破裂等;②化学风化,如低价铁的黄铁矿在水参与下变为高价铁的褐铁矿;③生物风化,如植物根系可使岩石的裂隙扩张等。岩体风化的速度和程度取决于岩石的性质和结构、地质构造、气候条件、地形条件、人类活动的影响等。 另外,按照岩石分化程度不同可以分为:1、未风化:岩质新鲜偶见风化痕迹。2、微风化:结构基本未变,仅节理面有渲染或略有变色,有少量风化裂隙。3、中风化:结构部分破坏,沿节理面有次生矿物,有风化裂隙发育,岩体被切割成岩块。用镐难挖,干钻不易钻进。4、强风化:结构大部分破坏,矿物成分显著变化,风化裂隙发育,岩体破碎,用镐可挖,干钻不易钻进。5、全风化:结构基本破坏,但尚可辨认,有残余结构强度,可用镐挖,干钻可钻进。6、残积土:组织结构全部破坏,已成土状,锹镐易开挖,干钻易钻进,具可塑。
中考复习专题一:物质的组成、构成和分类 1、理解元素的涵义,知道元素的性质与原子最外层电子数的关系,描述元素与原子的区别。 2、知道物质的简单分类,能据此区分一些常见物质。 3、正确描述分子、原子、离子概念的含义、区别与联系。 4、准确描述原子构成,认识常见原子的原子结构示意图。 【探索导航】 要求:(1)浏览教材并填写下面知识网络 (2)想一想,对于基础知识你还有那些不明白的地方? 元素 元素分类及在自然界存在状态 据元素原子结构和化学性质,元素可分为金属元素、 和 。 元素在地壳中含量(按质量分数的由大到小)依次为: 物质的简单分类 (1)纯净物和混合物的区别与联系 (2)单质和化合物的区别 单质 单质 单 质 物 物 混合物 物质 氧化物 酸 碱 盐 氧化物 氧化物 无机化合物 有机化合物CH 4 C 2H 5OH CH 3OH CH 3COOH
4 ①每个质子相对原子质量约等于1 质子
质子②每个质子带一个单位的电荷。 ③决定种类。 原子核中子 原 子①质量约等于(或)质量的1/1836。 ②每个电子带一个单位的电荷。 ③核外电子分层排布, 最外层电子数决定。 1、具有相同核电荷数(质子数)的微粒一定是同种元素吗?请举例说明。 2、同种元素组成的物质一定是单质吗?不同种元素组成的物质一定是化合物吗? 3、原子的最外层电子数是1或2的元素都是金属元素吗?8的微粒一定是稀有气体元素的原子吗? 4、分子能否保持物质的所有性质? 只有分子保持物质的化学性质吗? 5、分子一定比原子大吗? 所有物质都是由分子构成的吗? 6、任何原子的原子核都是由质子和中子构成的吗?怎样理解原子的质量主要集中在原子核上? 1,现有C、H、O、Na、Cu、S六种元素,从中选出相关元素组成下列类别物质的化学式:(每一类各写两例) ⑴单质_____________ ⑵酸_____________ ⑶碱_____________ ⑷盐_____________ ⑸氧化物____________⑹有机物_____________ 2、构成氧气的分子和构成液氧的分子具有( ) A、相同的性质 B、不同的性质 C、相同化学性质 D、不同化学性质 3、钾的相对原子质量较氩的相对原子质量小1,而核电荷数大1,由此可推断,一 个钾原子和一个氩原子所含中子数的关系是( ) A、钾的中子数比氩的中子数少1个 B、钾的中子数比氩的中子数少2个 C、钾的中子数等于氩的中子数 D、钾的中子数比氩的中子数多1个 4、下列关于物质组成的说法中正确的是( ) A、任何纯净物都是由一种元素组成的 B、一种元素只能组成一种单质 C、任何一种化合物都是由不同种元素组成的 D、任何物质都是由分子构成 5、20XX年,我国成功发射了“神舟六号”载人飞船,实现了多人多天的太空飞行,发射神舟号的火箭中的燃料是偏二甲基肼[(CH3)2N-NH2]],氧化剂N2O4,发射时反应可写为 (CH3)2N-(NH)2+2N2O4点燃 3N2↑+2CO2↑+4H2O↑,下列说法不正确的是:() A、偏二甲基肼中原子个数比为C:H:N=1:4:1 B、参加反应的物质中只含有 C、H、N、O四种元素 C、在宇宙中(失重条件下)比地球还难做过滤实验
第章 化学物质及其变化 第一节 物质的组成、分类和性质 (对应学生用书第14页) [考纲知识整合] 1.物质的组成 (1)构成粒子 (2)元素与物质的关系
元素组成,??? 单质:只由一种元素组成的纯净物。 化合物:由多种元素组成的纯净物。 (3)元素在物质中的存在形态 ①游离态:元素以单质形式存在的状态。 ②化合态:元素以化合物形式存在的状态。 提醒:同种元素形成的不同单质互称同素异形体,他们之间的转化为化学变化;它们混合后形成混合物。如O 2与O 3,金刚石与石墨等。 2.物质的分类 (1)分类方法 ①交叉分类法——从不同角度对物质进行分类。 ②树状分类法——按不同层次对物质进行逐级分类,各层之间属于包含关系。 请把下列物质的序号填写到下图的括号中 ①硫黄 ②HClO ③苛性钠 ④铜 ⑤小苏打 ⑥氧化钠 ⑦Fe(OH)3胶体 ⑧NaCl 溶液 (2)几类物质的概念 ①纯净物:由同种单质或化合物组成的物质。 ②混合物:由几种不同单质或化合物组成的物质。 ③氧化物:由两种元素组成其中一种为氧元素的化合物。 ④酸:电离出的阳离子全部是H +的化合物。 ⑤碱:电离出的阴离子全部是OH -的化合物。
⑥盐:金属阳离子或铵根离子与酸根阴离子构成的化合物。 [高考命题点突破] 命题点1物质的组成和构成粒子 1.下列说法正确的是________(填序号)。 (1)构成物质的粒子一定是原子或分子 (2)物质发生化学反应时,分子可以变化但原子不可变化 (3)同一种元素可能有多种不同原子,同一种原子也可能形成不同的离子 (4)只由一种分子构成的物质一定为纯净物,组成混合物的物质可能只有一种 元素 (5)只由一种元素的阳离子与另一种元素的阴离子构成的物质一定为纯净物 (6)CuSO4·5H2O中含有CuSO4和H2O,故CuSO4·5H2O为混合物 (7)任何化合物均由原子构成 (8)OH-和—OH属于相同的原子团 (9)NH+4、OH-、H3O+的电子数和质子数均相同 (10)O2与O3形成的混合气体为纯净物,O2与O3的转化为化学变化 (11)正丁烷与异丁烷的分子式均为C4H10,但二者的混合气体为混合物 【答案】(2)(3)(4)(11) [易错防范]误认为由相同元素组成的物质一定是纯净物 (1)若某物质是由一种元素的单质混合而成,如O2、O3组成的混合气体就是混合物,由12C和13C组成的石墨则是纯净物。 (2)分子式相同的化合物可能存在同分异构体,最简式相同的化合物不一定是同一物质。如C4H10的结构有正丁烷和异丁烷,二者组成混合物。 命题点2物质的分类 2.(2018·铜陵模拟)下列物质中,属于纯净物的是() ①陶瓷②水泥③玻璃④漂白粉⑤胆矾⑥氯水⑦液氯 A.①③⑤B.②④⑥ C.⑤⑦D.⑥⑦ C[①陶瓷的主要成分是SiO2和硅酸盐,属于混合物;②水泥是硅酸三钙、
刘桂花 复习目标 1、理解圆及其有关概念 2.掌握利用垂径定理及推论进行计算和证明的方法 3、理解弧、弦、圆心角的关系,圆周角与圆心角的关系 4、掌握圆的相关计算和证明 重点:圆的基本性质及有关计算 难点:辅助线的做法 教学过程 一、情境示标: (1)情境:由于历年中考考查有关于圆的基本性质的试题总是出现,所以今天我们有必要进行一下这方面知识的复习。 (2)示标:出示目标 1、理解圆及其有关概念 2.掌握垂径定理及推论 3.理解弧、弦、圆心角的关系,圆周角与圆心角的关系 4.掌握圆的相关计算和证明 二、自学指导 完成复习提纲内容 活动一、小组活动 1.组内成员互考概念 2.小组探讨概念重要的或容易出错的地方 3.完成习题训练 4.小组汇报 三、交流讲评 各小组成员抽签选小组后讲解 (一)圆的基本概念: 1.圆的定义:到定点的距离等于定长的点的集合叫做圆. 2.有关概念: (1)弦、直径(圆中最长的弦) (2)弧、半圆、优弧、劣弧、等弧 针对练习1 结合图形,找出⊙O中的弦、弧、优弧、劣弧 若AB是直径,AB=2DE,∠E=20o,则∠AOC的度数是 . 概念辨析:(1)弦是直径 (2)半圆是弧 (3)过圆心的线段是直径;
(4)半圆是最长的弧; (5)直径是最长的弦; (6)等弧就是长度相等的弧 注意-----等弧应同时满足两个条件: 1)两弧的长度相等, 2)两弧的度数相等。 (二)圆的基本性质 1.圆的对称性:1)圆是( )对称图形,任何( )都是它的对称轴.圆有无数条( ) (2)圆是( )对称图形,并且绕( )旋转任何一个角度都能与自身重合,即圆具有旋转( ) 2、垂径定理及其推论 垂径定理:垂直于弦的直径( )弦,并且平分弦所对的( )。 几何语言: 垂径定理推论:平分弦()的直径 ( )于弦,并且平分弦所对 的。 几何语言: 针对练习2 1.半径为4cm的⊙O中,弦AB=4cm, 那么圆心O到弦AB的距离是。 2.半径为2cm的圆中,过半径中点且 垂直于这条半径的弦长是。 3.在⊙O,弦AB=12cm,OC⊥AB, CD=2cm,则⊙0 的半径为 _____ 已知圆O的半径为5cm,弦AB∥弦CD,AB=6cm,CD=8cm, 则AB与CD距离是 cm. 归纳:1常用两条辅助线:( )( ) 2构造一个( )△,3运用两个定理( )( )解决问题 巩固训练 如图,P为⊙O的弦BA延长线上一点,PA=AB=2,PO=5,求⊙O的半径。