AYXL-002-2020
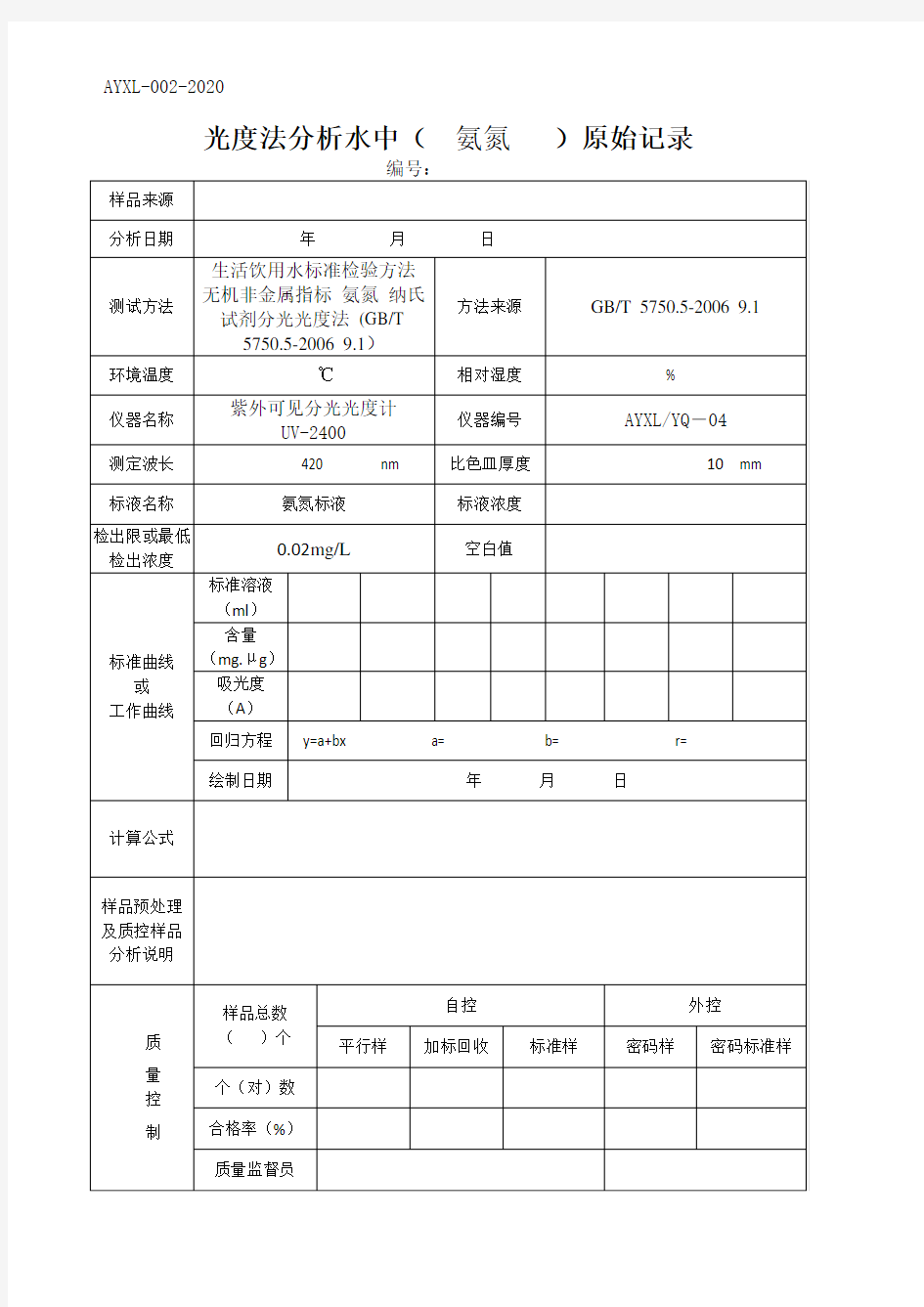
光度法分析水中(氨氮)原始记录
实验序号 4 实验名称水质分析 实验时间2010年4月12 实验室生科院实验楼综合2 一.实验预习 1.实验目的 学习和掌握测定水中溶解氧、浊度、氟化物、铁、氨氮和pH、六价铬、硫化物、钙、亚硝酸盐氮、有效氯(总氯)COD和总磷的方法。 了解这些因素在水环境中的地位及对水生生物的影响。 2.实验原理、实验流程或装置示意图 实验原理: 水是水生生物生活的场所,水体洁净程度如何,各种化学成分含量多少,是我们选用不同用途水源时的主要依据,进行水质分析已成为环境分析化学的一个重要组成部分,也是生态工作不可缺少的手段。 溶解氧的测定: 水中溶解氧的测定一般用碘量法,在水样中加入硫酸锰及碱性碘化钠溶液,生成氢氧化锰沉淀,此时氢氧化锰性质极不稳定,迅速与水中溶解氧化合生成锰酸锰 4MnSO4 + 8NaOH 4Mn(OH)2(肉色沉淀) + 4Na2SO4 2Mn(OH)2 + O22MnO(OH)2(棕黄色或棕色沉淀) 2H2MnO3 + 2Mn(OH)22MnMnO3+ 4H2O 加入浓硫酸使已化合的溶解氧(以MnMnO3的形式存在)与溶液中所加入的碘化钾发生反应而析出碘,溶解氧越多,析出的碘就越多,溶液的颜色也就越深。 4KI + 2H2SO44HI + 2K2SO4 2MnMnO3 + 4H2SO4 + 4HI 4MnSO4 + 2I2 + 6H2O 用移液管取一定量反应完毕的水样,以淀粉作指示剂,用硫代硫酸钠溶液滴定碘含量(碘量与溶解氧量成比例关系),计算出水样溶解氧的含量。 氨氮的测定: 氨与碘化汞钾在碱性溶液中生成黄色络合物,其色度与氨氮含量成正比,在0~L的氨氮范围内近于直线。反应式如下: 2K2(HgI4) + 3KOH + NH3 NH2HgOI (黄棕色沉淀) + 7KI + 2H2O 亚硝酸盐测定: 测定亚硝酸盐氮,通常使用重氮比色法,此法是基于亚硝酸盐和对氨基苯磺酸起重氮化作用,再与α-萘胺起偶合反应,生成紫红色染料,与标准液进行比色。 pH测定: 利用玻璃电极作指示电极,甘汞电极作参比电极,组成一个电池。在此电池中,被测溶液的氢离子随其浓度不同将产生相应的电位差。此电位与溶液的pH值的关系,符合能斯特方程式: E = E0 + log[H+] (25℃) E = E0–pH 式中,E0为常数。 浊度(NTU): 基于不同浊度的被测溶液对电磁辐射有选择性吸收而建立的比浊法。 铁: Fe 2+ +二氮杂菲橙红色络合物 基于在pH3~9的条件下,低价态铁离子与二氮杂菲生成稳定的橙红色络合物,对可见
水质氨氮的测定 氨氮(NH3-N)以游离氨(NH3)或铵盐(NH4+)形式存在于水中,两者的组成比取决于水的pH值和水温。当pH值偏高时,游离氨的比例较高。反之,则铵盐的比例高,水温则相反。 氨氮的测定方法主要有纳氏比色法、气相分子吸收法、苯酚——次氯酸盐(或水杨酸——次氯酸盐)比色法和电极法等。本节将主要介绍纳氏比色法和蒸馏——酸滴定法。 当水样带色或浑浊以及含有其他一些干扰物质,影响氨氮的测定。为此,在分析时需作适当的预处理。对较清洁的水,可采用絮凝沉淀法(加适量的硫酸锌于水样中,并加氢氧化钠使成碱性,生成氢氧化锌沉淀,再经过滤除去颜色和浑浊);对污染严重的水或工业废水,则用蒸馏法消除干扰(调节水样的pH值使在6.0-7.4的范围,加入适量氧化镁使成微碱性,蒸馏释放出的氨被吸收于硫酸或硼酸溶液中。采用纳氏比色法或酸滴定法时,以硼酸溶液为吸收液;采用水杨酸——次氯酸盐比色法时,则以硫酸溶液为吸收液)。 本实验的主要目的: 1 掌握水样预处理的方法; 2 掌握氨氮的测定原理及测定方法的选择 3 掌握分光光度计的使用方法,学习标准系列的配制和标准曲线的制作 一、纳氏试剂光度法(A1) 1 实验原理 碘化汞和碘化钾与氨反应生成淡红棕色胶态化合物,此颜色在较宽的波长内具强烈吸收。通常测量用410~425nm范围。 2 实验仪器 2.1 分光光度计 2.2 pH计 2.3 20mm比色皿 2.4 50mL比色管 1本方法与GB7479-87等效。
3 实验试剂 3.1 纳氏试剂:可任择以下两种方法中的一种配制。 3.1.1 称取20g碘化钾溶于约100ml水中,边搅拌边分次少量加入二氯化汞结晶粉末(约10g),至出现朱红色沉淀不易溶解时,改为滴加饱和二氯化汞溶液,并充分搅拌,当出现微量朱红色沉淀不易溶解时,停止滴加二氯化汞溶液。 另称取60g氢氧化钾溶于水,并稀释至250ml,充分冷却至室温后,将上述溶液在搅拌下,徐徐注入氢氧化钾溶液中,用水稀释至400ml,混匀。静置过夜。将上清液移入聚乙烯瓶中,密塞保存待用。 3.1.2 称取16g氢氧化钠,溶于50ml水中,充分冷却至室温。 另称取7g碘化钾和10g碘化汞溶于水,然后将此溶液在搅拌下徐徐注入氢氧化钠溶液中,用水稀释至100ml,贮于聚乙烯瓶中,密塞保存待用。 3.2 酒石酸钾钠溶液:称取50g酒石酸钾钠(KNaC4H4O6·4H2O)溶于100ml水中,加热煮沸以去除氨,放冷,定容100ml。 3.3 铵标准贮备溶液:称取3.819g经100℃干燥过的优级纯氯化铵(NH4Cl)溶于水中,移入1000ml容量瓶中,稀释至标线。此溶液每毫升含1.00mg氨氮。 3.4 铵标准使用液:移取5.00ml铵标准贮备液(3.3)于500ml容量瓶中,用水稀释至标线。此溶液每毫升含0.010mg氨氮。 4 实验步骤 4.1 标准曲线的制作 4.1.1 吸取0、0.50、1.00、3.00、 5.00、7.00和10.00ml铵标准使用液(3.4)于50ml 比色管中,加水至标线,加1.0ml酒石酸钾钠溶液(3.2),摇匀。加1.5ml纳氏试剂(3.1.1或3.1.2),混匀。放置10min后,在波长420nm出,用光程20mm比色皿,以水为参比,测量吸光度。 4.1.2 由测得的吸光度减去空白的吸光度后,得到校正吸光度,以氨氮含量(mg)对校正吸光度的统计回归标准曲线。 4.2 水样的测定 4.2.1 分取适量经絮凝沉淀预处理后的水样(使氨氮含量不超过0.1mg),加入50ml 比色管中,稀释至标线,加1.0ml酒石酸钾钠溶液。以下同标准曲线的制作(4.1)。 4.2.2 分取适量经蒸馏预处理后的馏出液,加入50ml比色管中,加一定量1mol/L氢
水质氨氮的测定纳氏试剂 分光光度法 The following text is amended on 12 November 2020.
实验三水质氨氮的测定——纳氏试剂分光光度法 仪器和药品: 天平、称量纸、玻璃棒、手套、擦镜纸 可见分光光度计:具20 mm比色皿(6只) 比色管:50mL,40支;25mL,40支 移液管:20mL,5支;10、5、1mL各5支 容量瓶:250、500mL和1000ml 5个;100mL,10个 烧杯:200mL,5个 量筒100ml,5个 聚乙烯瓶、棕色瓶各5个 加热装置 氢氧化钠、碘化钾、碘化汞、酒石酸钾钠、氯化铵 一、目的和意义 水中的氨氮来源于生活污水中含氮有机物受微生物作用分解产物、某些工业废水以及农田排水。水中氨氮含量与人们的生产和生活有密切的关系,如果水中氨氮浓度过高会造成鱼类死亡,水质变臭,无法达到人们正常饮用和使用的标准。 掌握纳氏试剂光度法测定水中氨氮的原理和方法。 二、方法原理 以游离态的氨或铵离子等形式存在的氨氮与纳氏试剂反应生成淡红棕色络合物,该络合物的吸光度与氨氮含量成正比,于波长420 nm处测量吸光度。 水样中含有悬浮物、余氯、钙镁等金属离子、硫化物和有机物时会产生干扰。若样品中存在余氯,可加入适量的硫代硫酸钠溶液去除,用淀粉-碘化钾试纸检验余氯是否除尽。在显色时加入适量的酒石酸钾钠溶液,可消除钙镁等金属离子的干扰。若水样浑浊或有颜色时可用预蒸馏法或絮凝沉淀法处理。 三、溶液配制 1、纳氏试剂【碘化汞-碘化钾-氢氧化钠溶液】 称取 g氢氧化钠,溶于50 ml水中,冷却至室温。称取 g碘化钾和 g碘化汞,溶于水中,然后将此溶液在搅拌下,缓慢加入到上述50 ml氢氧化钠溶液中,用水稀释至100 ml。贮于聚乙烯瓶内,用橡皮塞或聚乙烯盖子盖紧。 2、酒石酸钾钠溶液,ρ=500 g/L。 称取 g酒石酸钾钠(KNaC4H6O6·4H2O)溶于100 ml水中,加热煮沸以驱除氨,充分冷却后稀释至100 ml。 3、氨氮标准溶液氯化铵分子量 氨氮标准贮备溶液,ρN =1000 mg/L。 称取 g氯化铵(优级纯,在100~105℃干燥2 h),溶于水中,移入1000 ml容量瓶中,稀释至标线。
实验三水中氨氮的测定 氨氮的测定方法,通常有纳氏试剂比色法、苯酚-次氯酸盐(或水杨酸-次氯酸盐)比色法和电极法等。纳氏试剂比色法具有操作简便、灵敏等特点,但钙、镁、铁等金属离子、硫化物、醛、酮类,以及水中色度和混浊等干扰测定,需要相应的预处理。苯酚-次氯酸盐比色法具灵敏、稳定等优点,干扰情况和消除方法同纳氏试剂比色法。电极法通常不需要对水样进行预处理和具测量范围宽等优点。氨氮含量较高时,可采用蒸馏-酸滴定法。 一、实验目的和要求 1、掌握氨氮测定最常用的方法-纳氏试剂比色法。 2、复习第二章含氮化合物测定的有关内容。 二、纳氏试剂比色法 (一)原理 碘化汞和碘化钾的碱性溶液与氨反应生成淡红棕色胶态化合物,其色度与氨氮含量成正比,通常可在波长410—425nm范围内测其吸光度,计算其含量。 本法最低检出浓度为0.025mg/L(光度法),测定上限为2mg/L。采用目视比色法,最低检出浓度为0.02mg/L。水样作适当的预处理后,本法可适用于地面水、地下水、工业废水和生活 污水。 (二)仪器 1、带氮球的定氮蒸馏装置:500mL凯氏烧瓶、氮球、直形冷凝管。 2、分光光度计。 3、pH计。
(三)、试剂 配制试剂用水均应为无氨水。 1、无氨水。可选用下列方法之一进行制备: (1)蒸馏法:每升蒸馏水中加0.1mL硫酸,在全玻璃蒸馏器中重蒸馏,弃去50mL初馏液,接取其余馏出液于具塞磨口的玻璃瓶中,密塞保存。 (2)离子交换法:使蒸馏水通过强酸性阳离子交换树脂柱。 2、1mol/L盐酸溶液。 3、1mol/L氢氧化纳溶液。 4、轻质氧化镁(MgO):将氧化镁在500℃下加热,以除去碳酸盐。 5、0.05%溴百里酚蓝指示液(pH6.0—7.6)。 6、防沫剂:如石蜡碎片。 7、吸收液:①硼酸溶液:称取20g硼酸溶于水,稀释至1L。②0.01mol/L 硫酸溶液。 8、纳氏试剂。可选择下列方法之一制备: (1)称取20g碘化钾溶于约25mL水中,边搅拌边分次少量加入二氯化汞(HgCl2)结晶粉末(约10g),至出现朱红色沉淀不易溶解时,改为滴加饱和二氯化汞溶液,并充分搅拌,当出现微量朱红色沉淀不再溶解时,停止滴加氯化汞溶液。 另称取60g氢氧化钾溶于水,并稀释至250mL,冷却至室温后,将上述溶液徐徐注入氢氧化钾溶液中,用水稀释至400mL,混匀。静置过夜,将上清液移入聚乙烯瓶中,密塞保存。 (2)称取16g氢氧化钠,溶于50mL水中,充分冷却至室温。
现场验收检验批检查原始记录
现场验收检验批检查原始记录共页第页 单位(子单位) 名称澧县蓬莱花园6# 检验批名称 土方开挖 检验批编号验收日期年月日编号验收项目验收部位验收情况记录备注 1 标高基础 2 长度、宽度基础 3 表面平整度基础 4 边坡基础符合要求 5 基底土性基础符合要求 6 7 8 9 10 11 12 13 14
人: 注:本表格由质量员在验收现场记录填写。 现场验收检验批检查原始记录共页第页 单位(子单位) 名称澧县蓬莱花园6# 检验批名称 土方回填 检验批编号验收日期年月日编号验收项目验收部位验收情况记录备注 1 标高基础 2 分层压实系数基础符合要求 3 分层厚度及含水量基础符合要求 4 表面平整度基础 5 6 7 8 9 10 11 12
14 人: 注:本表格由质量员在验收现场记录填写。 现场验收检验批检查原始记录共页第页 单位(子单位) 名称澧县蓬莱花园裙楼6# 检验批名称 钢筋加工 检验批编号验收日期年月日编号验收项目验收部位验收情况记录备注 1 受力钢筋的弯钩和 弯折 基础 2 箍筋弯钩形式基础 3 钢筋调直基础 4 受力钢筋顺长度方向 全长的净尺寸 基础 5 箍筋内净尺寸基础6 7 8 9 10
12 13 14 人: 注:本表格由质量员在验收现场记录填写。 现场验收检验批检查原始记录共页第页 单位(子单位) 名称澧县蓬莱花园6# 检验批名称 钢筋安装 检验批编号验收日期年月日编号验收项目验收部位验收情况记录备注 1 受力钢筋和品种、级 别、规格和数量 基础符合要求 2 绑扎钢筋长、宽基础 3 受力钢筋间距基础 4 受力钢筋保护层厚度 基础 基础 5 绑扎箍筋、横向钢筋 间距 基础 6 钢筋弯起点的位置基础7 8
精心整理 1.范围 1.1 本方法规定了用纳氏试剂分光光度法测定水中的氨氮。 1.2 本方法适用于地下水、地表水、生活污水和工业废水中氨氮的测定。 1.3 当水样体积为50mL,使用20mm比色皿时,本方法检出限为0.025mg/L,测定下限为0.10mg/L, 测定上限为2.0mg/L(均以N计)。 2.参考标准 水质氨氮的测定纳氏试剂分光光度法HJ535-2009 3.职责 4. 5. 5.1 5.2 6.试剂 6.1制备6.1 6.1.2蒸馏法:在1000mL的蒸馏水中,加0.1mL硫酸(ρ=1.84g/mL),在全玻璃蒸馏器中重蒸 馏,弃去前50mL馏出液,然后将约800mL馏出液收集在带有磨口玻璃塞的玻璃瓶内。每升 馏出液加10g强酸性阳离子交换树脂(氢型)。 6.2 盐酸,ρ(HCl)=1.18g/mL。 6.3 硫酸,ρ(H2SO4)=1.84g/mL。 6.4 无水乙醇 6.5 轻质氧化镁(MgO):不含碳酸盐,在500℃下加热氧化镁,以除去碳酸盐。
6.6 氢氧化钠(NaOH) 6.7 可溶性淀粉 6.8 碘化钾(KI) 6.9 碘化汞(HgI) 6.10 氢氧化钾(KOH) 6.11 二氯化汞(HgCl2) 6.12 纳氏试剂 ?碘化汞–碘化钾–氢氧化钠(HgI2-KI-NaOH)溶液: (6.8) 氢氧化? 6.13 6.14 6.15 6.16 。6.17 硫酸锌(ZnSO4·7H2O) 6.18 硫酸锌溶液,ρ=100g/L,称取10.0g硫酸锌(6.17)溶于水中,稀释至100mL。 6.19 氢氧化钠溶液,ρ=250g/L。称取25g氢氧化钠(6.6)溶于水中,稀释至100mL。 6.20 氢氧化钠溶液,c(NaOH)=1mol/L。称取4g氢氧化钠(6.6)溶于水中,稀释至100mL。 6.21 盐酸溶液,c(HCl)=1mol/L。用吸量管吸取8.5mL盐酸(6.2)于100mL容量瓶中,用水稀释 至标线。 6.22 硼酸(H3BO3)
文档来源为:从网络收集整理.word版本可编辑.欢迎下载支持. 四、检测表格 (D表) 59文档收集于互联网,已整理,word版本可编辑.
文档来源为:从网络收集整理.word版本可编辑.欢迎下载支持. 检测表格目录 D检001 检测记录表(通用) D检002 检测数据汇总表(通用) D检101 点位偏差测量记录表(全站仪、经纬仪) D检102 高程偏差测量记录表(水准仪) D检103 几何尺寸偏差测量记录表(尺量) D检104 平整度、竖直度、斜度、坡度测量记录表 D检201 压实度检测记录表(环刀法) D检202 压实度检测记录表(灌砂法) D检203 压实度检测记录表(核子密度仪法) D检204 软地基处理检测记录表 D检301 桥头、涵背填筑碾压记录表 D检302 土质边沟(纵坡、断面尺寸、边坡度、边楞直顺度)检测计录表 D检303 浆砌排水沟(断面尺寸、墙面直顺度或坡度、铺砌厚度、垫层厚度)检测记录表D检304 浆砌排水沟(沟底高程、轴线偏位)检测记录表 D检305 涵洞基础检测记录表 D检306 涵洞墙身检测记录表 D检307 管涵检测记录表 D检308 盖板涵检测记录表 D检309 小型预制件检测记录表 D检501 路基、路面(高程、横坡、宽度)检测记录表 D检502 路基、路面弯沉记录表 D检503 路面基层(底基层)施工厚度检测记录表 D检504 路面基层(底基层)强度检测记录表 D检505 水泥混凝土路面纵、横缝直顺度检测记录表 D检506 路面构造深度(手工铺砂法)检测记录表 D检507 路面磨擦系数检测记录表 D检508 路面渗水检测记录表 D检509 平整度检测记录表(平整度仪法) 60文档收集于互联网,已整理,word版本可编辑.
氨氮的测定纳氏试剂分光光度法 目次 前言............................................................................................................................... ..................III 1适用范围............................................................................................................................... .. (1) 2方法原理............................................................................................................................... .. (1) 3干扰及消除............................................................................................................................... . (1) 4试剂和材料............................................................................................................................... . (1) 5仪器和设备............................................................................................................................... . (3) 6样品............................................................................................................................... . (3) 7分析步骤............................................................................................................................... .. (4) 8结果计算............................................................................................................................... .. (4) 9准确度和精密度 (5) 10质量保证和质量控制 (5)
H J水质氨氮测定 The latest revision on November 22, 2020
水质氨氮的测定 1 含义及方法原理 含义 氨氮是指水中以游离氨(NH )和(NH4+)形式存在的氮。动物性的含氮量 3 一般较植物性有机物为高。同时,人畜粪便中含氮有机物很不稳定,容易分解成氨。因此,水中氨氮含量增高时指以氨或铵离子形式存在的化合氨。 方法原理 以游离态的氨或铵离子等形式存在的氨氮与纳氏试剂反应生成淡红棕色络合物,该络合物的吸光度与氨氮含量成正比,于波长420 nm处测量吸光度空气质量标准。 2. 方法名称、标准号及适应范围 方法名称:《水质氨氮的测定纳氏试剂分光光度法》 方法标准号:HJ535 -2009 方法适用范围:本标准适用于地表水、地下水、生活污水和工业废水中氨氮的测定。 3 仪器 可见分光光度计:具20 mm比色皿。 氨氮蒸馏装置:由500 mL凯式烧瓶、氮球、直形冷凝管和导管组成,冷凝管末端可连接一段适当长度的滴管,使出口尖端浸入吸收液液面下。亦可使用500 mL蒸馏烧瓶。 4 试剂 除非另有说明,分析时所用试剂均使用符合国家标准的分析纯化学试剂,实验用水为按制备的水。 无氨水,在无氨环境中用下述方法之一制备。 离子交换法 蒸馏水通过强酸性阳离子交换树脂(氢型)柱,将流出液收集在带有磨口玻璃塞的玻璃瓶内。每升流出液加10 g同样的树脂,以利于保存。 蒸馏法
在1 000 mL的蒸馏水中,加 mL硫酸(ρ= g/mL),在全玻璃蒸馏器中重 蒸馏,弃去前50 mL馏出液,然后将约800 mL馏出液收集在带有磨口玻璃塞的玻璃瓶内。每升馏出液加10 g强酸性阳离子交换树脂(氢型)。 纯水器法 用市售纯水器临用前制备。 轻质氧化镁(MgO) 不含碳酸盐,在500℃下加热氧化镁,以除去碳酸盐。 盐酸,ρ(HCl)= g/mL。 纳氏试剂,可选择下列方法的一种配制。 二氯化汞-碘化钾-氢氧化钾(HgCl 2 -KI-KOH)溶液 称取 g氢氧化钾(KOH),溶于50 mL水中,冷却至室温。 称取 g碘化钾(KI),溶于10 mL水中,在搅拌下,将 g二氯化汞 (HgCl 2 )粉末分多次加入碘化钾溶液中,直到溶液呈深黄色或出现淡红色沉淀溶解缓慢时,充分搅拌混合,并改为滴加二氯化汞饱和溶液,当出现少量朱红色沉淀不再溶解时,停止滴加。 在搅拌下,将冷却的氢氧化钾溶液缓慢地加入到上述二氯化汞和碘化钾的混合液中,并稀释至100 mL,于暗处静置24 h,倾出上清液,贮于聚乙烯瓶内,用橡皮塞或聚乙烯盖子盖紧,存放暗处,可稳定1个月。 碘化汞-碘化钾-氢氧化钠(HgI 2 -KI-NaOH)溶液 称取 g氢氧化钠(NaOH),溶于50 mL水中,冷却至室温。 称取 g碘化钾(KI)和 g碘化汞(HgI 2 ),溶于水中,然后将此溶液在搅拌下,缓慢加入到上述50 mL氢氧化钠溶液中,用水稀释至100 mL。贮于聚乙烯瓶内,用橡皮塞或聚乙烯盖子盖紧,于暗处存放,有效期1年。 酒石酸钾钠溶液,ρ=500 g/L。 称取 g酒石酸钾钠(KNaC 4H 6 O 6 ·4H 2 O)溶于100 mL水中,加热煮沸以驱除 氨,充分冷却后稀释至100 mL。硫代硫酸钠溶液,ρ= g/L。 称取 g硫代硫酸钠(Na 2S 2 O 3 )溶于水中,稀释至1 000 mL。 硫酸锌溶液,ρ=100 g/L。
资料收集于网络,如有侵权请联系网站删除只供学习与交流 只供学习与交流检验原始记录 实验环境:a、温度:℃b、干湿度:% 样品名称:样品编号:产品批号: 样品状态:状态完好,符合检验要求取样数量:执行标准:————————————————————————————————————————————————— 感官测定原始记录 检测依据:GB/T 14454.2 色泽:□正常□异常气味:□正常□异常 形态:□正常□异常滋味:□正常□异常 结论————————————————————————————————————————————————— 干燥失重测定原始记录 检测依据:GB/T 5009.3—2010 序号检验 方法 检验用仪器设 备 测试 温度 称量瓶质 量 称量瓶+ 样品质量 称量瓶+样品 干燥后的质量 检测结果 检测结果 平均值 报出值直接 干燥 法 分析天平、称 量瓶、恒温干 燥箱等 (℃)(g)(g)(g)(%)(%)(%) 1 2 ————————————————————————————————————————————————— 氯化物测定原始记录 检测依据:QB/T 1500—1992 硝酸银标准滴定溶液c[ 0.1 ]/(mol/L) 序号检验 方法 检验用仪器设 备 样品 质量 样品定容 总体积 测定用样 品溶液体 积 标准滴定溶液 消耗量 检测结果 检测结果 平均值 报出值 直接 沉淀 滴定 法 分析天平、酸 式滴定管等 (g)(ml)(ml)(ml)(g/100g) (g/100g ) (g/100 g) 1 2 空 白 mL ————————————————————————————————————————————————— 酸价测定原始记录 检测依据:GB/T 5009.37—2003 氢氧化钾标准滴定溶液c[ 0.050 ]/(mol/L) 序号检验 方法 检验用仪器设备样品质量 标准滴定溶液消 耗量 检测结果 检测结果平 均值 报出值 滴定 法 分析天平、碱式滴定管、 恒温水浴锅等 (g)(ml) (mgKOH/ 100g) (mgKOH/ 100g) (mgK OH/100 g) 1 2 —————————————————————————————————————————————————
1. 范围 1.1 本方法规定了用纳氏试剂分光光度法测定水中的氨氮。 1.2 本方法适用于地下水、地表水、生活污水和工业废水中氨氮的测定。 1.3 当水样体积为50mL,使用20mm比色皿时,本方法检出限为0.025mg/L,测定下限为 0.10mg/L,测定上限为2.0mg/L(均以N计)。 2. 参考标准 水质氨氮的测定纳氏试剂分光光度法HJ 535-2009 3. 职责 检测技术人员按本作业指导书对水样中氨氮进行分析检测。 4. 方法原理 以游离态的氨或铵离子等形式存在的氨氮与纳氏试剂反应生成淡红棕色络合物,该络合物的吸光度与氨氮含量成正比,于波长420nm处测量吸光度。 5. 干扰及消除 5.1 水样中含有悬浮物、余氯、钙镁离子等金属离子、硫化物和有机物时会产生干扰,含 有此类物质时要作适当处理,以消除对测定的影响。 5.2 若样品中存在余氯,可加入适量的硫代硫酸钠溶液去除,用淀粉–碘化钾试纸检验余氯 是否除尽。在显色时加入适量的酒石酸钾钠溶液,可消除钙镁等金属离子的干扰。若水样浑浊或有颜色时可用预蒸馏法或絮凝沉淀法处理。 6. 试剂 除非另有说明,分析时所用试剂均为符合国家标准的分析纯化学试剂,实验用水为按6.1制备的水,使用经过检定的容量器皿和量器。 6.1 无氨水,在无氨环境中用纯水器法制备。用市售纯水器直接制备。或采用下述方法之 一制备: 6.1.1 离子交换法:蒸馏水通过强酸性阳离子交换树脂(氢型)柱,将流出液收集在带有 磨口玻璃塞的玻璃瓶内。每升流出液加10g同样的树脂,以利于保存。 6.1.2 蒸馏法:在1000mL的蒸馏水中,加0.1mL硫酸(ρ=1.84g/mL),在全玻璃蒸馏器 中重蒸馏,弃去前50mL馏出液,然后将约800mL馏出液收集在带有磨口玻璃塞的 玻璃瓶内。每升馏出液加10g强酸性阳离子交换树脂(氢型)。 6.2 盐酸,ρ(HCl)=1.18g/mL。 6.3 硫酸,ρ(H2SO4)=1.84g/mL。 6.4 无水乙醇 6.5 轻质氧化镁(MgO):不含碳酸盐,在500 ℃下加热氧化镁,以除去碳酸盐。 6.6 氢氧化钠(NaOH)
水质氨氮检测方法及操作步骤 氨氮 氨氮(NH3-N)以游离氨(NH3)或铵盐(NH4+)形式存在于水中,两者的组成比取决于水的pH值。当pH值偏高时,游离氨的比例较高。反之,则铵盐的比例为高。 水中氨氮的来源主要为生活污水中含氮有机物受微生物作用的分解产物,某些工业废水,如焦化废水和合成氨化肥厂废水等,以及农田排水。此外,在无氧环境中,水中存在的亚硝酸盐亦可受微生物作用,还原为氨。在有氧环境中,水中氨亦可转变为亚硝酸盐、甚至继续转变为硝酸盐。 测定水中各种形态的氮化合物,有助于评价水体被污染和“自净”状况。 氨氮含量较高时,对鱼类则可呈现毒害作用。 1.方法的选择 氨氮检测方法,通常有纳氏比色法、苯酚-次氯酸盐(或水杨酸-次氯酸盐)比色法和电极法等。纳氏试剂比色法具操作简便、灵敏等特点,水中钙、镁和铁等金属离子、硫化物、醛和酮类、颜色,以及浑浊等干扰测定,需做相应的预处理,苯酚-次氯酸盐比色法具灵敏、稳定等优点,干扰情况和消除方法同纳氏试剂比色法。电极法通常不需要对水样进行预处理和具测量范围宽等优点。氨氮含量较高时,尚可采用蒸馏﹣酸滴定法。 2.水样的保存 水样采集在聚乙烯瓶或玻璃瓶内,并应尽快分析,必要时可加硫酸将水样酸化至pH<2,于2—5℃下存放。酸化样品应注意防止吸收空气中的氮而遭致污染。 预处理 水样带色或浑浊以及含其它一些干扰物质,影响氨氮的测定。为此,在分析时需做适当的预处理。对较清洁的水,可采用絮凝沉淀法,对污染严重的水或工业废水,则以蒸馏法使之消除干扰。 (一)絮凝沉淀法 概述 加适量的硫酸锌于水样中,并加氢氧化钠使呈碱性,生成氢氧化锌沉淀,再经过滤去除颜色和浑浊等。 仪器 100ml具塞量筒或比色管。 试剂
水中氨氮的测定 水中氨氮的测定 作者:胡海鹏等文章来源:《化学教学》2007.7点击数:10905更新时间:2008-1-22 水中氮化合物的多少,可作为水体受到含氮有机物污染程度的指标。反映水体受含氮化合物污染程度的几种形态的氮是氨氮、亚硝酸盐氮、硝酸盐氮、有机氮。测定水中各种形态的氮化合物,有助于评价水体被污染程度和“自净”的程度。水中的氨氮是指以游离氨(或称非离子氨,NH3)和离子氨(NH4+)形式存在的氮。氨氮含量较高时,对鱼类呈现毒害作用,对人体也有不同程度的危害。水中氨氮的来源主要是生活污水中含氮有机物受微生物作用分解的产物、某些工业废水及农田排水等。 大多数中学生对不同形态氮之间的转化的知识认识较为模糊。结合环境化学知识,采用纳氏试剂光度法对水中氨氮进行测定,研究降低水中氨氮含量的方法,可提高学生动脑动手的能力,加强保护环境的意识。本课题案例适用高二年级学习了氮族元素之后,在学生已有知识的基础上实现知识的迁移、拓展和应用。 纳氏试剂光度法的原理是碘化钾和碘化汞的碱性溶液与水中的氨反应生成淡红棕色胶态化合物,该颜色在波长为410-425nm下有强烈的吸收,从而实现水中氨氮的测定。本研究性学习采用目视法对水中的氨氮做粗略的定量,这不仅简单、直观,而且避免引入朗伯-比尔定律的新知识,毕竟这不是中学生所必须掌握的。 纳氏试剂光度法测量水中氨氮 1、方法原理纳氏试剂分光光度法HgI和KI的碱性溶液与氨反应生成淡红棕色胶态化合物,此颜色在较宽的波长范围内具强烈吸收。通常测量用波长在410-425nm范围。本法最低检出浓度为0.025mg·L-1(光度法),测定上限为2mg·L-1。采用目视比色法,最低检出浓度为0.02mg·L-1。水样作适当的预处理后,本法可适用于地面水、地下水、工业废水和生活污水。 2、方法的适用范围本法最低检出浓度为0.025mg·L-1(光度法),测定上限为2mg·L-1。 3、试验仪器与试剂仪器:500mL凯氏烧瓶、氮球、直形冷凝管、分光光度计、pH计试剂:无氨水、1mol·L-1盐酸溶液、1mol·L-1氢氧化纳溶液、纳氏试剂、酒石酸钾钠溶液试剂的配制:1)纳氏试剂:可选择下列一种方法制备①称取20g碘化钾溶于约100mL水中,边搅拌边分次少量加入二氯化汞(HgCl2)结晶粉末(约10g),至出现朱红色沉淀不易溶解时,改为滴加饱和二氯化汞溶液,并充分搅拌,当出现微量朱红色沉淀不易溶解时,停止滴加二氯化汞溶液。②另称取60g氢氧化钾溶于水,并稀释至250mL,充分冷却至室温后,将上述溶液在搅拌下,徐徐注入氢氧化钾溶液中,用水 稀释至400mL,混匀。静置过夜。将上清液移入聚乙烯瓶中,密塞保存。2)酒石酸钾钠溶液:称取50g酒石酸钾钠(KNaC4H4O6.4H2O)溶于100mL水中,加热煮沸
水质氨氮的测定方法纳氏试剂分光光度法 1.含义 本测定方法适用于地表水、地下水、生活污水和工业废水中氨氮的测定。 当水样体积为 50 ml,使用 20 mm 比色皿时,本方法的检出限为 0.025 mg/L,测定下限为 0.10 mg/L,测定上限为 2.0 mg/L(均以 N 计)。 2.方法原理 以游离态的氨或铵离子等形式存在的氨氮与纳氏试剂反应生成淡红棕色络合物,该络合物的吸光度与氨氮含量成正比,于波长 420 nm 处测量吸光度。 3.检测依据 水质氨氮的测定纳氏试剂分光光度法HJ 535-2009 4.检测程序 4.1 试剂和材料 除非另有说明,分析时所用试剂均使用符合国家标准的分析纯化学试剂,实验用水为按4:1 制备的水。 4.1.1无氨水,在无氨环境中用下述方法之一制备。 (1)离子交换法 蒸馏水通过强酸性阳离子交换树脂(氢型)柱,将流出液收集在带有磨口玻璃塞的玻璃瓶。每升流出液加 10 g 同样的树脂,以利于保存。 (2)蒸馏法 在1 000 ml 的蒸馏水中,加 0.1 ml 硫酸(ρ=1.84 g/ml),在全玻璃蒸馏器中重蒸馏,弃去前 50 ml 馏出液,然后将约 800 ml 馏出液收集在带有磨口玻璃塞的玻璃瓶。每升馏出液加 10 g 强酸性阳离子交换树脂(氢型)。 (3)纯水器法 用市售纯水器临用前制备。 4.1.2轻质氧化镁(MgO) 不含碳酸盐,在 500℃下加热氧化镁,以除去碳酸盐。 4.1.3盐酸,ρ(HCl)=1.18 g/ml。 4.1.4纳氏试剂,可选择下列方法的一种配制。
(1)二氯化汞-碘化钾-氢氧化钾(HgCl2-KI-KOH)溶液 称取 15.0 g 氢氧化钾(KOH),溶于 50 ml 水中,冷却至室温。称取 5.0 g 碘化钾(KI),溶于 10 ml 水中,在搅拌下,将 2.50 g 二氯化汞(HgCl2)粉末分多次加入碘化钾溶液中,直到溶液呈深黄色或出现淡红色沉淀溶解缓慢时,充分搅拌混合,并改为滴加二氯化汞饱和溶液,当出现少量朱红色沉淀不再溶解时,停止滴加。在搅拌下,将冷却的氢氧化钾溶液缓慢地加入到上述二氯化汞和碘化钾的混合液中,并稀释至 100 ml,于暗处静置 24 h,倾出上清液,贮于聚乙烯瓶,用橡皮塞或聚乙烯盖子盖紧,存放暗处,可稳定 1 个月。 (2)碘化汞-碘化钾-氢氧化钠(HgI2-KI-NaOH)溶液 称取 16.0 g 氢氧化钠(NaOH),溶于 50 ml 水中,冷却至室温。 称取 7.0 g 碘化钾(KI)和 10.0 g 碘化汞(HgI2),溶于水中,然后将此溶液在搅拌下,缓慢加入到上述 50 ml 氢氧化钠溶液中,用水稀释至 100 ml。贮于聚乙烯瓶,用橡皮塞或聚乙烯盖子盖紧,于暗处存放,有效期 1 年。 4.1.5酒石酸钾钠溶液,ρ=500 g/L。 称取 50.0 g 酒石酸钾钠(KNaC4H6O6·4H2O)溶于 100 ml 水中,加热煮沸以驱除氨,充分冷却后稀释至 100 ml。 4.1.6硫代硫酸钠溶液,ρ=3.5 g/L。 称取 3.5 g 硫代硫酸钠(Na2S2O3)溶于水中,稀释至 1 000 ml。 4.1.7硫酸锌溶液,ρ=100 g/L。 称取 10.0 g 硫酸锌(ZnSO4·7H2O)溶于水中,稀释至 100 ml。 4.1.8氢氧化钠溶液,ρ=250 g/L。 称取 25 g 氢氧化钠溶于水中,稀释至 100 ml。 4.1.9氢氧化钠溶液,c(NaOH)=1 mol/L。 称取 4 g 氢氧化钠溶于水中,稀释至 100 ml。 4.1.10盐酸溶液,c(HCl)=1 mol/L。 量取 8.5 ml 盐酸(4.3)于适量水中用水稀释至 100 ml。 4.1.11硼酸(H3BO3)溶液,ρ=20 g/L。 称取 20 g 硼酸溶于水,稀释至 1 L。 4.1.12溴百里酚蓝指示剂(bromthymol blue),ρ=0.5 g/L。 称取 0.05 g 溴百里酚蓝溶于 50 ml 水中,加入 10 ml 无水乙醇,用水稀释至 100 ml。 4.1.13淀粉-碘化钾试纸
原始记录书写要求
1. 记录表格使用炭素,蓝黑墨水填写或计算机打印(必须保证记录的原始性),字体 要书写工整,不得使用圆珠笔、铅笔或纯蓝墨水填写;分析结果报告单要求必须打印。所有打印的记录不能手工改错,如果改错,须重新打印。 2. 每项监测任务的所有质量记录和技术记录表格,均应使用同一个编号,即本次监测任务的唯一性标识。 3. 手写的记录表格如有空格,则划斜线和加盖“以下空白”印章:打印的记录表格如有空格,不得手划斜线,在最后一个监测分析数据下方如有空格,应在紧邻下一空格内加盖“以下空白”印章或手填“以下空白。” 4. 记录表格整体框架和要素原则上不得变动,但可根据需要适当调整列宽、行高, 也可进行个别相邻格的合并或拆分等。如使用者认为整体框架和要素确需变动或修改,应按照有关程序规定进行。 5. 原始记录填写应在一格中的下半部,不得涂改、刀刮。如需修改,应在错误处划一斜线(应能看清原记录数据),并加盖本人私章,并在此格上部书写正确的数据, 每页原始记录改错地方不应超过三个。 6. 所有落款应签姓名不得盖章,签姓名用全称,签名字体工整、消晰、整齐原始记录单“分析人”一栏,未持证人员不能单独签名,应将姓名签在持证人员之后:分析人员只有 1 人时,该分析人员不得在校核或审核处签名。 7. 原始记录中相对偏差取一位有效数字或整数,修约规则为只入不舍,加标回收率取整数。 8. 原始记录和分析结果报告单中,当测试结果低于方法检出限或最低检出浓度时, 应填报为“未检出”,并在记录中注明方法检出限或最低检出浓度。容量及重量分析项日,如化学需氧量、生化需氧量、高锰酸盐指数、悬浮物、氯化物、石油类,全盐量。矿化度、溶解性总固体等低于检测下限时,以<L”的形式填报L”为检测下限值。 9. 气相色谱,液相(离子)色谱,GC-MS色质联用仪、原子荧光仪、测汞仪测试气态、固态样品原始记录可参照相应水质测试原始记录填写。 10. 质控措施在任务通知单中下达,应具体到每个监测因子:采样原始记录单和分析 项目原始记录中“质控措施”一栏填写实际质控情况。检测项目分析工作结束后,应填报质控结果统计表,质量负责人应在任务通知单及质控结果统计表上签字,目的是对质量负责。 11. 无组织排放分析结果报告单“备注”一栏应注明上风向、下风向点位序号、风向、风速、气温、气压、天气情况等因素。 12. 各仪器设备填写使用、维护或维修记录应使用专用表格。 13. 仪器设备使用记录封面唯一性标识编号同仪器设备使用记录表编号。 14. 原始记录、报告单及检测报告中必须采用法定计量单位,诸如mg/标干m3 mg/Nm3”等非法定计量单位一律换成法定计量单位,写出mg/m3”。 15. 检测结果在0.1—1000(不含1000)之内的,不能用科学计数法表示,如540不能写成5.40X102,直接报540即可。 16. 采样记录应填写有关的现场参数。项目名称应该按国家有关标准的名称规范书写,如氰化物不能写成氰,除pH、PM10、TSP三个项目可以用符号外,其他项目一律用文字书写。
样品编号:XL2019— 检测项目:色度 检验依据:GB/T5750.4-2006《生活饮用水标准检验方法》感官性状和物理指标1.1铂—钴标准比色法 (一)检测步骤: (1)本批次均取透明的水样于比色管中,如水样色度过高,可取水样,加纯水稀释后比色,将结果乘以稀释倍数。 (2)另取比色管11支,分别加入铂—钴标准溶液0,0.50, 1.00, 1.50, 2.00, 2.50, 3.00, 3.50, 4.00, 4.50及5.00mL ,加纯水至刻度,摇匀,即配制成色度为0,5,10,15,20,25,30,35,40,45及50度的标准色列,可长期使用。 (3)将水样与铂—钴标准色列比较。如水样与标准色列的色调不一致,即为异色。 (4)标准系列: 铂-钴标准液0 0.50 1.00 1.50 2.00 2.50 3.00 3.50 4.00 4.50 5.00 色度 0 5 10 15 20 25 30 35 40 45 50 (5)本批次检测结果(度):报告结果为中位数 样品编号 比色结果1 比色结果2 比色结果3 报告结果 样品编号 比色结果1 比色结果2 比色结果3 报告结果 检测者:检测日期:年月日 校核者:校核日期:年月日
样品编号:XL2019— 检测项目:浑浊度 检验依据:GB/T5750.4-2006《生活饮用水标准检验方法》感官性状和物理指标2.2目视比浊法—福尔马肼标准 (一)检测步骤: A、浑浊度10度以上的水样 (1)本批次均取浑浊度250度的标准液(吸取含250mg硅藻土的悬浮液,置于1000mL容量瓶中,加纯水至刻度,振摇混匀即得)0,10,20,30,40,50,60,70,80,90及100mL,置于250mL 容量瓶中,加纯水稀释至刻度,振摇混匀后移入成套的250mL具塞玻璃瓶中,即得浑浊度为0,10,20,30,40,50,60,70,80,90及100度的标准液。每瓶中加入1g氯化汞以防菌类生长。将瓶塞塞紧以免水份蒸发。 (2)将振摇均匀的水样盛入成套的250mL具塞玻璃瓶中。 (3)将水样与浑浊度标准液都摇匀,同时从瓶侧观察同一目标(如报纸铅字或划有黑线的白纸等),根据目标清晰程度,选出与水样所产生的视觉效果相近的标准液,读得水样的浑浊度。水样的浑浊度超过100度时,可用纯水稀释后测定。 B、浑浊度10度以下的水样 (1)本批次均取 mL比色管11支,分别加入浑浊度为100度的标准溶液(吸取浑浊度为250度的标准液100mL,置于250mL容量瓶中,加纯水稀释至刻度,振摇混匀,即得浑浊度为100度的标准液)0, 1.0, 2.0, 3.0, 4.0, 5.0, 6.0, 7.0, 8.0, 9.0及10.0mL,各加纯水稀释至100mL,混匀,即得浑浊度0,1,2,3,4,5,6,7,8,9,10度的标准液。 (2)取100mL水样,置于同样规格的比色管中,与浑浊度标准液同时振摇均匀,并进行比较,比较时由上往下垂直观察。 (二)本批次检测结果(度):报告结果为中位数 样品编号 比色结果1 比色结果2 比色结果3 报告结果 样品编号 比色结果1 比色结果2 比色结果3 报告结果 检测者:检测日期:年月日 校核者:校核日期:年月日
水质原始记录-CAL-FENGHAI.-(YICAI)-Company One1
水质检验原始记录 样品编号:HS2017— 检测项目:色度 检验依据:GB/《生活饮用水标准检验方法》感官性状和物理指标铂—钴标准比色法 (一)检测步骤: (1)本批次均取透明的水样于比色管中,如水样色度过高,可取水样,加纯水稀释后比色,将结果乘以稀释倍数。 (2)另取比色管11支,分别加入铂—钴标准溶液0,, , , , , , , , 及,加纯水至刻度,摇匀,即配制成色度为0,5,10,15,20,25,30,35,40,45及50度的标准色列,可长期使用。 (3)将水样与铂—钴标准色列比较。如水样与标准色列的色调不一致,即为异色。 (4)标准系列: 铂-钴标准液0 色度 0 5 10 15 20 25 30 35 40 45 50
检测者:检测日期:年月日 校核者:校核日期:年月日 水质检验原始记录 样品编号:HS2017— 检测项目:浑浊度 检验依据:GB/《生活饮用水标准检验方法》感官性状和物理指标目视比浊法—福尔马肼标准 (一)检测步骤: A、浑浊度10度以上的水样 (1)本批次均取浑浊度250度的标准液(吸取含250mg硅藻土的悬浮液,置于1000mL容量瓶中,加纯水至刻度,振摇混匀即得)0,10,20,30,40,50,60,70,80,90及100mL,置于250mL容量瓶中,加纯水稀释至刻度,振摇混匀后移入成套的250mL具塞玻璃瓶中,即得浑浊度为0,10,20,30,40,50,60,70,80,90及100度的标准液。每瓶中加入1g氯化汞以防菌类生长。将瓶塞塞紧以免水份蒸发。 (2)将振摇均匀的水样盛入成套的250mL具塞玻璃瓶中。 (3)将水样与浑浊度标准液都摇匀,同时从瓶侧观察同一目标(如报纸铅字或划有黑线的白纸等),根据目标清晰程度,选出与水样所产生的视觉效果相近的标准液,读得水样的浑浊度。水样的浑浊度超过100度时,可用纯水稀释后测定。 B、浑浊度10度以下的水样 (1)本批次均取 mL比色管11支,分别加入浑浊度为100度的标准溶液(吸取浑浊度为250度的标准液100mL,置于250mL容量瓶中,加纯水稀释至刻度,振摇混匀,即得浑浊度为100度的标准液)0, , , , , , , , , 及,各加纯水稀释至100mL,混匀,即得浑浊度0,1,2,3,4,5,6,7,8,9,10度的标准液。 (2)取100mL水样,置于同样规格的比色管中,与浑浊度标准液同时振摇均匀,并进行比较,比较时由上往下垂直观察。