
实验八工业纯碱中总碱度测定
一、实验目的
1. 了解基准物质碳酸钠及硼砂的分子式和化学性质;
2.掌握HCl标准溶液的配制和标定过程
3.掌握强酸滴定二元弱碱的滴定过程,突跃范围及指示剂选择。
4.掌握定量转移操作的基本特点。
二、实验原理
工业纯碱的主要成分为碳酸钠,商品名为苏打,其中可能还含有少量NaCl,Na2SO4,NaOH及NaHCO3。常以HCl标准溶液为滴定剂测定总碱度来衡量产皮的质量。滴定反应为
Na2CO3 + 2HCl = 2NaCl + H2CO3
H2CO3=CO2↑+H2O
反应产物H2CO3易形成过饱和溶液并分解为CO2逸出。化学计量点时溶液pH 为3.8至3.9,可选用甲基橙为指示剂,用HCl标准溶液滴定,溶液由黄色转变为橙色即为终点。试样中NaHCO3同时被中和。
由于试样易吸收水分和CO2,应在270~300℃将试样烘干2h,以除去吸附水并使NaHCO3全部转化为Na2CO3,工业纯碱的总碱度通常以w(Na2CO3)或w(Na2O)表示,由于试样均匀性较差,应称取较多试样,使其更具代表性。测定的允许误差可适当放宽一点。
三、主要试剂与仪器
1. HCl溶液
2. 无水Na2CO3
3. 0.1%甲基橙指示剂
4. 0.2%甲基红60%的乙醇溶液。
5. 甲基红-溴甲酚绿混合指示剂
6. 硼砂(Na2B4O7·10H2O)
四、实验步骤
1.0.1mol·L-1HCl溶液的标定
(1)用无水Na2CO3基准物质标定用称量瓶准确称取0.08g-0.10g无水Na2CO33份,分别倒入100mL锥形瓶中。称量瓶称样时一定要带盖,以免吸湿然后加入
10-20mL水使之溶解,再加入1-2滴甲基橙指示剂,用待标定的HCl溶液滴定至溶液的黄色恰变为橙色即为终点。计算HCl溶液的浓度。
(2)用硼砂Na2B4O7·10H2O标定准确称取硼砂0.2~0.3g 3份,分别倾入100mL锥形瓶中,加水20mL使之溶解,加入2滴甲基红指示剂,用待标定的HCl溶液滴定至溶液由黄色恰变为浅红色即为终点。根据硼砂的质量和滴定时所消耗的HCl溶液的体积,计算HCl溶液的浓度。
2.总碱度的测定
准确称取试样约1g倾入烧杯中,加少量水使其溶解,必要时可稍加热促进溶解。冷却后,将溶液定量转入100mL容量瓶中,加水稀释至刻度,充分摇匀。平行移取试液10.00mL三份于锥形瓶中,加入1~2滴甲基橙指示剂,用HCl标准溶液滴定溶液由黄色恰变为橙色即为终点。计算试样中Na2O或Na2CO3含量,即为总碱度。测定的各次相对偏差应在±0.5%以内。
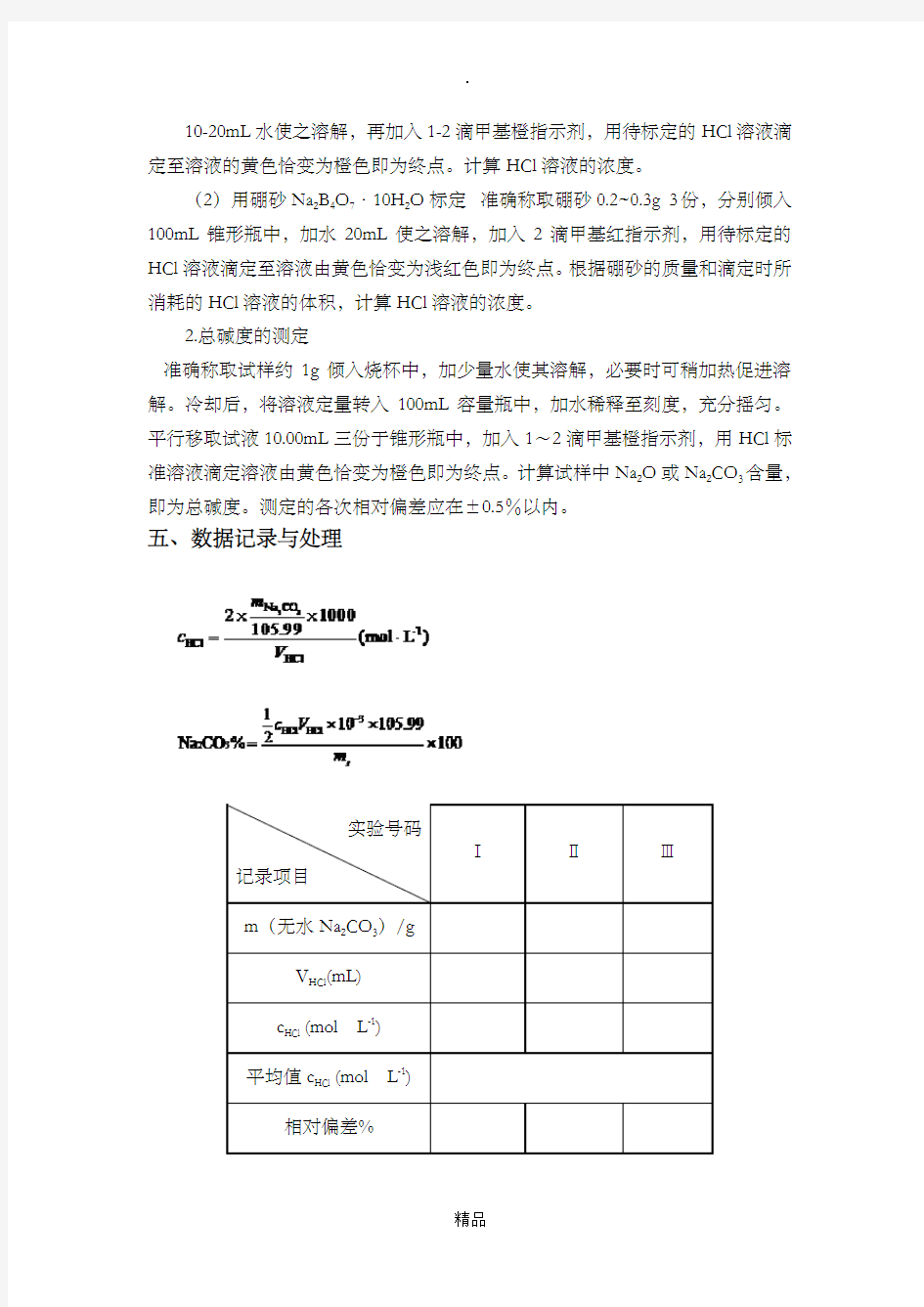
五、数据记录与处理
实验号码
记录项目ⅠⅡ
Ⅲm(无水Na2CO3)/g
V HCl(mL)
c HCl (mol L-1)
平均值c HCl (mol L-1)
相对偏差%
c HCl (mol L-1)
平均值c HCl (mol L-1)
六、注意事项:
1.称量时,一定要减少碳酸钠试剂瓶的开盖时间,防止吸潮。取完试剂后,马上盖好并放入保干器中。
2.煮沸样品时,天然气灯的火量应为能保持溶液沸腾的最小火。加热后的石棉网不能直接放在滴定台上,只能放在铁架台上(铁架台下垫橡皮板)。加热后的锥形瓶可放在实验台上,或直接放入盛有冷却水的塑料盆中冷却。不允许用流动水冷却。煮沸后滴定时,要半滴、半滴地加入滴定剂,否则易过量。
七、思考题:
1.为什么配制0.1mol·L-1HCl溶液1L需要量取浓HCl溶液9mL?写出计算式。
2.无水Na2CO3保存不当,吸收了1%的水分,用此基准物质标定HCl溶液浓度时,对其结果产生何种影响?
3.甲基橙,甲基红及甲基红-溴甲酚绿混合指示剂的变色范围各为多少?混合指示剂优点是什么?
4.标定HCl的两种基准物质Na2CO3和Na2B4O7·10H2O各有那些有缺点?
5.在以HCl溶液滴定时,怎样使用甲基橙及酚酞两种指示剂来判别试样是由NaOH-Na2CO3或Na2CO3-NaHCO3组成的?
如有侵权请联系告知删除,感谢你们的配合!