
第一节氢氧化物沉淀法
除了碱金属和部分碱土金属外,其它金属的氢氧化物大都是难溶的(表12-1)。因此,可用氢氧化物沉淀法去除废水中的重金属离子。沉淀剂为各种碱性药剂,常用的有石灰,碳酸钠、苛性钠、石灰石、白云石等。
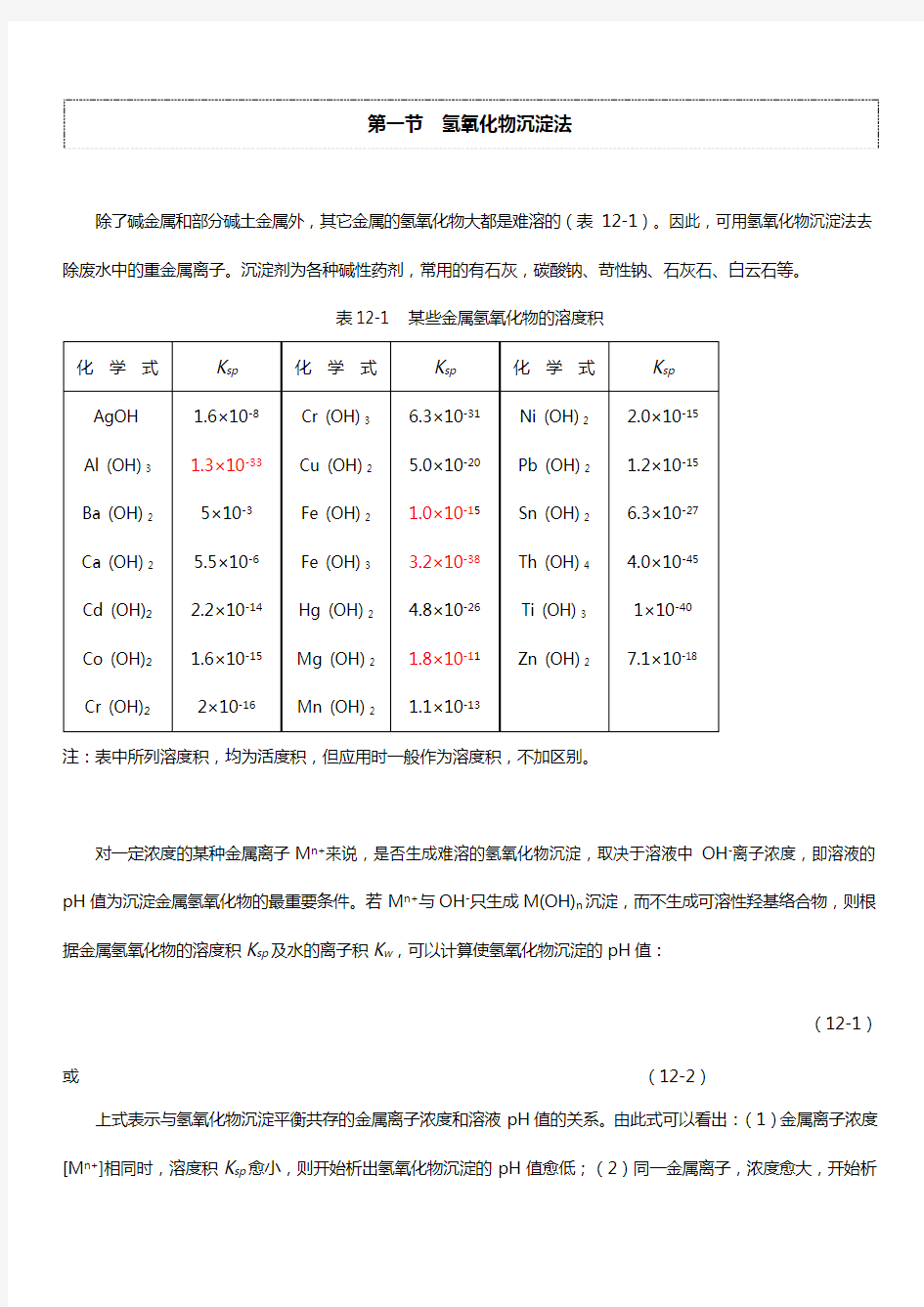
表12-1 某些金属氢氧化物的溶度积
化学式K sp化学式K sp化学式K sp
AgOH Al (OH) 3 Ba (OH) 2 Ca (OH) 2 Cd (OH)2 Co (OH)2 Cr (OH)21.6×10-8
1.3×10-33
5×10-3
5.5×10-6
2.2×10-14
1.6×10-15
2×10-16
Cr (OH) 3
Cu (OH) 2
Fe (OH) 2
Fe (OH) 3
Hg (OH) 2
Mg (OH) 2
Mn (OH) 2
6.3×10-31
5.0×10-20
1.0×10-15
3.2×10-38
4.8×10-26
1.8×10-11
1.1×10-13
Ni (OH) 2
Pb (OH) 2
Sn (OH) 2
Th (OH) 4
Ti (OH) 3
Zn (OH) 2
2.0×10-15
1.2×10-15
6.3×10-27
4.0×10-45
1×10-40
7.1×10-18
注:表中所列溶度积,均为活度积,但应用时一般作为溶度积,不加区别。
对一定浓度的某种金属离子M n+来说,是否生成难溶的氢氧化物沉淀,取决于溶液中OH-离子浓度,即溶液的pH值为沉淀金属氢氧化物的最重要条件。若M n+与OH-只生成M(OH)n沉淀,而不生成可溶性羟基络合物,则根据金属氢氧化物的溶度积K sp及水的离子积K w,可以计算使氢氧化物沉淀的pH值:
(12-1)或(12-2)上式表示与氢氧化物沉淀平衡共存的金属离子浓度和溶液pH值的关系。由此式可以看出:(1)金属离子浓度[M n+]相同时,溶度积K sp愈小,则开始析出氢氧化物沉淀的pH值愈低;(2)同一金属离子,浓度愈大,开始析
出沉淀的pH值愈低。根据各种金属氢氧化物的K sp值,由公式(12-2)可计算出某一pH值时溶液中金属离子的饱和浓度。以pH值为横坐标,以—log[M n+]为纵坐标,即可绘出溶解度对数图(图12-1)。
根据溶解度对数图,可以方便地确定金属离子沉淀的条件。以Cd2+为例,若[Cd2+]=0.1mol/L,则由图上查出,使氢氧化镉开始沉淀出来的pH值应为7.7;若欲使溶液残余Cd2+浓度达10-5mol/L,则沉淀终了的pH值应为9.7。
如果重金属离子和氢氧根离子不仅可以生成氢氧化物沉淀,而且还可以生成各种可溶性的羟基络合物(对于重金属离子,这是十分常见的现象),这时与金属氢氧化物呈平衡的饱和溶液中,不仅有游离的金属离子,而且有配位数不同的各种羟基络合物,它们都参与沉淀-溶解平衡。在此情况下,溶解度对数图就要复杂些。今仍以Cd(II)为例,Cd2+与OH-可形成CdOH+、Cd(OH)2、Cd(OH)3-、Cd(OH)42-等四种可溶性羟基络合物,根据它们的逐级稳定常数和Cd(OH)2的溶度积K sp,可以确定与氢氧化镉沉淀平衡共存的各可溶性羟基络合物浓度与溶液pH值的关系,如图12-2中各实线所示。将同一pH值下各种型态可溶性二价镉Cd(II)s的平衡浓度相加,即得氢氧化镉溶解度与pH值的关系,如图中虚线所示。虚线所包围的区域为氢氧化镉沉淀存在的区域。考虑了羟基络合物的溶解平衡区域图,可以更好地确定沉淀金属氢氧化物的pH值条件。例如,由图12-2可以看出,pH=10~13时,Cd(OH)2(固)的溶解度最小,约等于10-5.2mol/L。因此,用氢氧化物沉淀法去除废水中的Cd(II)时,pH 值常控制在10.5~12.5范围内。其它许多金属离子(如Cr3+、Al3+、Zn2+、Pb2+、Fe2+、Ni2+、Cu2+),在碱性提高时都可明显地生成络合阴离子,而使氢氧化物的溶解度重又增加,这类既溶于酸又溶于碱的氢氧化物,常称为两性氢氧化物。
图12-1 金属氢氧化物的溶解度对数图
图12-2 氢氧化镉溶解平衡区域图
当废水中存在CN-、NH3及Cl-、S2-等配位体时,能与重金属离子结合可溶性络合物,增大金属氢氧化物的溶解度,对沉淀法去除重金属不利,因此要通过预处理将其除去。
采用氢氧化物沉淀法处理重金属废水最常用的沉淀剂是石灰。石灰沉淀法的优点是:去除污染物范围广(不仅可沉淀去除重金属,而且可沉淀去除砷、氟、磷等)、药剂来源广、价格低、操作简便、处理可靠。主要缺点是劳动卫生条件差、管道易结垢堵塞、泥渣体积庞大(含水率高达95~98%)、脱水困难。
废水中往往有多种重金属离子共存。此时,尽管低于理论pH值,有时也会生成氢氧化物沉淀。这是因为在高pH值沉淀的重金属与在低pH值下生成的重金属沉淀物产生共沉现象。例如:含Cd lmg/L的水溶液,将pH值调到11以上也不沉淀,若与10 mg/L的Fe3+共存,则pH值只要达到8以上即可沉淀,并使Cd2+的去除率接近100%。
在有几种重金属离子共存时,由于各自生成的氢氧化物沉淀的最佳pH值条件不同,因此,可进行分步沉淀处理。例如,从锌冶炼厂排出的废水中,往往含锌和镉。该废水处理时,Zn2+在pH=9左右时形成的Zn(OH)2溶解度最低,而Cd2+在pH=10.5~11时沉淀效果最好。然而,由于锌是两性化合物,当pH=10.5~11时,氢氧化锌再次溶解。因而对此种废水,应先加碱性,使pH值等于9左右,沉淀除去氢氧化锌后,再加碱性,将pH值提高到11左右,再沉淀除去氢氧化镉。
化学沉淀是一种晶析现象,结晶的成长速度,决定于结晶核的表面和溶液中沉淀剂浓度与其饱和浓度之差。化学沉淀反应方式可采用单纯沉淀反应和晶种循环反应。晶种循环反应是向反应池中投加良好的沉淀晶种(回流污泥),促使形成良好的结晶沉淀。处理流程见图12-3。图12-3b所示为晶种循环处理法。其特点是除投加沉淀剂外,还从沉淀池回流适当的沉淀污泥,而后混合搅拌反应,经沉淀池浓缩沉淀形成污泥后,其中一部分再次返回反应槽。此法生成的沉淀污泥晶粒大,沉淀快,含水率较低,出水效果好。
沉淀剂
废水出水
沉淀反应沉淀池
污泥
(a)
沉淀剂
废水出水
图12-3 某重金属废水化学沉淀处理流程图
图12-4为国内某有色金属冶炼厂采用石灰沉淀法处理酸性含锌废水的流程。处理废水量约800m3/h,废水中主要污染物为Zn2+和H2SO4,并含有少量Cu2+、Cd2+、Pb2+、等。处理效果见表12-2。处理后的出水外排,而干渣返回冶炼炉重新利用。该工艺采用废水配制石灰乳,并使沉淀池的底泥浆部分回流,这有助于改善泥渣
的沉降性能和过滤性能。
图12-4 某厂石灰沉淀处理含锌废水流程图
表12-2 石灰沉淀法处理效果(除pH外,单位均为mg/L)
项目pH 锌铅铜镉砷
原废水 2.0~6.7 60.64~89.47 3.87~7.78 0.81~3.10 0.78~1.39 0.26~1.15
处理后出水10~11 0.95~3.73 0.39~0.74 0.12~0.27 0.03~0.06 0.021~0.059
其它应用实例如用氢氧化物沉淀法处理含镉废水,一般pH值应为9.5~12.5。当pH=8时,残留浓度为1mg/L;当pH值升至10或11时,残留浓度分别降至0.1和0.00075mg/L;如果采用砂滤或铁盐、铝盐凝聚沉降,则可改进出水水质。对于含铜废水(1~1000mg/L)的处理,pH值为9.0~10.3最好。若采用铁盐共沉淀,效果尤佳,残留浓度为0.15~0.17mg/L。不宜采用石灰处理焦磷酸铜废水,主要原因是pH值要求高(达12),形成大量焦磷酸钙沉渣,使沉渣中铜含量低,回收价值小。对于某含镍100mg/L的废水,投加石灰250mg/L,pH达9.9,出水含镍可降至1.5mg/L。
元素周期律碱金属元素性质总结 I.元素周期律 1.周期表位置IA族(第1纵列),在2、3、4、5、6、7周期上均有分布。元素分别为锂(Li)-3,钠(Na)-11,钾(K)-19,铷(Rb)-37,铯(Cs)-55,钫(Fr)-87。 2.碱金属的氢氧化物都是易溶于水, 苛性最强的碱, 所以把它们被称为为碱金属。 3.碱金属的单质活泼,在自然状态下只以盐类存在,钾、钠是海洋中的常量元素,其余的则属于轻稀有金属元素,在地壳中的含量十分稀少。钫在地壳中极稀少,一般通过核反应制取。 4.保存方法:锂密封于石蜡油中,钠。钾密封于煤油中,其余密封保存,隔绝空气。 II.物理性质 II.1物理性质通性(相似性) 1.碱金属单质皆为具金属光泽的银白色金属(铯略带金黄色),但暴露在空气中会因氧气的氧化作用生成氧化物膜使光泽度下降,呈现灰色。常温下均为固态。 2.碱金属熔沸点均比较低。摩氏硬度小于2,质软。.导电、导热性、延展性都极佳。 3.碱金属单质的密度小于2g/cm3,是典型轻金属,锂、钠、钾能浮在水上。 4.碱金属单质的晶体结构均为体心立方堆积,堆积密度小。 II-2.物理性质递变性 随着周期的递增,卤族元素单质的物理递变性有: 1.金属光泽逐渐增强。 2.熔沸点逐渐降低。 3.密度逐渐增大。钾的密度具有反常减小的现象。 II.3.物理性质特性 1.铯略带有金色光泽,钫根据测定可能为红色,且具有放射性。 2.液态钠可以做核反应堆的传热介质。 3.锂密度比没有小,能浮在煤油中。 4.钾的密度具有反常现象。 钾的密度反常变化的原因:根据公式:ρ=A r/V原子,可知相对原子质量的增大使密度增加,而电子层的增加又使原子体积增大使得密度减小。即单质的密度由相对原子质量和原子体积两个因素决定。对钾来说,核对最外层引力较小,体积增大的效应大于相对原子质量增加产生的影响,结果钾的密度反而比钠小。 II.5焰色反应 1.碱金属离子及其挥发性化合物在无色火焰中燃烧时会显现出独特的颜色,这可以用来鉴定
溶度积的计算 (1)已知溶度积求离子浓度: 例1、已知室温下PbI2的溶度积为7.1×10-9,求在c(I-)=0.1mol·L-1的PbI2饱和溶液中, Pb2+的浓度最大可达到多少? (2)已知溶度积求溶解度: 例2、已知298K 时AgCl 的K sp = 1.8×10-10,求其溶解度S (3)已知溶解度求溶度积 例3、已知AgCl 298 K 时在水中溶解度为1.92×10-4g,计算其K sp。 (4)利用溶度积判断离子共存: 例4、已知298K时,MgCO3的K sp = 6.82×10-6,溶液中c(Mg2+)=0.0001mol·L-1,c(CO32-) = 0.0001mol·L-1,此时Mg2+和CO32-能否共存?
(5)利用溶度积判断沉淀平衡移动方向: 已知:K SP(AgCl)=1.8 ×10-10K SP(AgI)=8.3 ×10-17 往AgCl固体中加入蒸馏水,使其达到溶解平衡, (1)求溶液中c(Ag+)有多大? (2)再向该溶液加入KI,使I-浓度达到0.1mol/L,请判断有没有AgI生成? (6)溶度积与PH: 例5.25℃时,Ksp [Mg(OH)2]= 5.6×10-12, 求Mg(OH)2的饱和溶液中的c(Mg2+)和PH值;若往此饱和溶液中滴入无色酚酞则溶液呈什么颜色? 练习1:在100mL 0.01mol/LKCl 溶液中,加入1mL 0.01mol/L AgNO3溶液,有沉淀(已知AgCl K SP=1.8×10-10)?Ag+沉淀是否完全?(化学上通常认为残留在溶液中的离子浓度小于1×10-5mol/L,沉淀就达完全) 练习2:25℃时Ksp [Fe(OH)2]= 4.9×10-17,Ksp [Al(OH)3]= 1.3×10-33,比较Fe(OH)2、Al(OH)3饱和溶液中溶解度的大小.
高中化学金属氢氧化物的性质总结 总结如下: 白色:NaOH、Mg(OH)2、Al(OH)3 Zn(OH)2、Fe(OH)2、AgOH 红褐色:Fe(OH)3 蓝色:Cu(OH)2 【提问】这些金属氢氧化物对水的溶解性规律是什么?请总结之。 ⅠA和部分ⅡA金属氢氧化物都易溶于水,如NaOH,KOH,Ba(OH)2。Ca(OH)2是微溶性的。 其它的都是难溶性的,如Mg(OH)2、Fe(OH)3、Cu(OH)2 【提问】请分析总结这些氢氧化物的化学性质规律是什么。 可从下面几点去思考,回答。 (1)加热是否分解 (2)与强酸(H+)反应 (3)与强碱(OH-)反应 (4)与氨水反应 (5)是否容易被氧化 (6)是否能被还原 (分析,回答) (1)热稳定性
2AgOH Ag2O+H2O Cu(OH)2 CuO+H2O 2Fe(OH)3 Fe2O3+3H2O 规律:①金属活动顺序“Mg”以前的金属氢氧化物稳定性好,难分解。 ②“AgOH”常温下易分解。 ③“Mg—Hg”的氢氧化物常温下难分解,受热或灼烧易分解。 (2)与强酸(H+)的反应 Mg(OH)2+2H+=Mg2++2H2O Al(OH)3+3H+=Al3++3H2O (3)与强碱(OH-)反应 Al(OH)3+OH-=AlO2-+2H2O 规律:只有两性氢氧化物才能与强碱溶液反应。 (4)与氨水作用 AgOH+2NH3·H2O=Ag(NH3)2OH+2H2O *Cu(OH)2+4NH3·H2O=Cu(NH3)4(OH)2+4H2O * Zn(OH)2+4NH3·H2O=Zn(NH3)4(OH)2+4H2O 规律:易形成氨络合物的金属氢氧化物能与氨水反应。 (5)与氧化剂反应 4Fe(OH)2+O2+2H2O=4Fe(OH)3 规律:低价金属氧化物具有还原性。 【小结】金属氢氧化物所发生的反应,总结起来,主要有:
韩山师范学院化学系化学专业物化实验课实验报告 班级 20011312 学号 23 姓名 高旺珠 同组 评分 实验日期: 2004年9月22日 室温 27.0℃ 气压 101.56×103Pa 教师 难溶金属氢氧化物溶度积的测定 实验目的: 1、掌握pH 自动滴定法测定难溶金属氢氧化物溶度积的原理和方法; 2、学会pH 自动滴定仪测定Ni(OH)2的溶度积。 实验原理: 难溶性金属氢氧化物溶度积符合下式: K SP =a +n M · a n OH - 在定温下 K SP 为常数。根据水的离子积K w =a H +·a OH - 可的得氢离子活度与 K SP 的关 系即溶液pH 与 K SP 的关系。因此若准确地测出形成某金属氢氧化物沉淀时溶液的pH 值和金 属离子的活度或浓度就可以算得 K SP 值。 如图7-1是一个典型的pH 滴定曲线:图中AB 线段为沉淀形成阶段,加入的NaOH 消耗与金属离子结合,故溶液pH 值变化缓慢,滴定曲线几乎呈水平状态。 在沉淀阶段AB 线段间任取一点i ,并确定i 的两个坐标的准确值,就得到该点的pH 值和对应的NaOH 的滴定量,则在实验温度下被测的金属氢氧化物的溶度积: K SP =[Ni 2+ ]i [OH - ]2 i 而[Ni 2+ ]=N NaOH (V B -V i )/2(V +2i N +V i ) [OH -]=10-14 /10 -(pH) j 则 K SP =[N NaOH (V B -V i )/2(V +2i N +V i )]×[10-14/10-(pH)j ]2 P 图7-1 p H滴定曲线
- 97 - 第5期2018年10月No.5 October,2018 具有层状结构的双金属氢氧化物缩写为LDHs ,并且是具有层状晶体结构的类水滑石化合物。 LDHs 的结构通式如下:[M Ⅰ(1-x)M Ⅱx (OH )2]x +(A n -)x/n ·dH 2O ,其中M Ⅰ=Mg 2+、Fe 2+、Co 2+ 等(为低价态阳离子), M Ⅱ=Al 3+、Fe 3+、Ti 4+等(为高价态阳离子),A n -是层间存在 的阴离子,d 代表每摩尔LDHs 结晶水的摩尔数,x 是摩尔比n (M Ⅱ)/[n (M Ⅰ)+n (M Ⅱ)]。 LDHs 的基本构造单元是由金属离子和氧组成的八面体,八面体的中心镶嵌有金属离子,6个顶角均为OH -,并且八面体通过公共边彼此连接以获得二维延伸的单位晶体层。在LDHs 中,M Ⅱ有时会用类似的半径代替M Ⅰ,从而产生永久的正电荷,处于层间的A n -再把永久正电荷平衡[1]。 随着现代双金属氢氧化物科学技术研究的深入,已经观察到LDHs 表现出非常特殊的层状结构以及LDHs 之间的阴离子嵌入和有机物的可插入性。这些性质被广泛地应用到催化方面、环境安全方面、医药健康等方面。1 LDHs的制备方法 关于LDHs 的制备目前有很多研究,基本分为两个方面:首先是由于存在于八面体层板上的阳离子可以进行同晶取代,根据这种性质而制备的;其次是由于存在于层间阴离子可以进行交换,根据这种性质而制备的[3]。LDHs 的常用制备方法包括液相共沉淀法、水热合成法、阴离子交换法和微波晶化法。1.1 共沉淀法制备LDHs 通过共沉淀法制备出的LDHs 材料有很完整的晶体结构,有比较均一的粒度。 在恒pH 的条件下用双滴定的方法制备Mg-Al-LDHs :使用 MgCl 2·5H 2O 和AlCl 3·6H 2O 作为原料,将二者配制成摩尔比为3∶1的混合盐溶液,再加入沉淀剂(特定浓度1 mol/L 的 NaOH 溶液),所以,Mg-Al-LDHs 是通过液相共沉淀的方法制备的。在恒定的pH 下搅拌,并以适当的滴加速率将1 mol/L NaOH 溶液与制备的混合盐溶液缓慢混合以形成沉淀物,老化一段时间后,将其过滤并洗涤。然后,将滤饼密封并在培养箱中加热以获得Mg-Al-LDHs 的固体样品,然后将样品研 磨成粉末以获得Mg-Al-LDHs [4] 。时效晶体对晶体生长和结 晶度具有一定的优势[5] 。 传统共沉淀反应需要等待较长的时间,这就导致了形成晶核的生成时间变长,结果使粒径的大小程度比较分散,并且LDHs 的粒径分布和它的大小对其在各方面的应用影响较 大,因此,Mg-Al-LDHs 纳米粒子可以通过T 形微反应器制备[6]。虽然也是共沉淀法,但该方法可以有效地分离开晶核的生成期和生长期,使得混合盐溶液与沉淀剂在短时间内就可以充分混合,然后使其老化,得到粒径分布较窄的LDHs 。1.2 水热合成法制备LDHs 水热合成法可以制得高纯度、完全晶体生长、分散性好、颗粒均匀的产品。 取特定质量的Ni(NO 3)2·6H 2O 、Fe(NO 3)3·9H 2O 和尿素完全溶解至去离子水中,使其浓度各为15 mmol 、5 mmol 、35 mmol 。再加入浓度为0.25 mmol 的柠檬酸三钠,均匀搅拌后,置于反应釜中,在150 ℃的条件下保温48 h 。保温完成后,将混合物冷却,离心,用水洗涤3次,用无水乙醇清洗1遍,并在室温下干燥,得到Ni-Fe-LDHs 产物[7]。 水热合成法制备的产品性能的影响因素有镍铁比、反应温度、柠檬酸三钠的浓度以及反应时间。镍铁比对于产品的形貌、结晶度、磁性能和吸附性能有很大影响,当镍铁比为2∶1时,产品具有优良的结晶度和磁性能;当镍铁比为3∶1时的产品具有良好的磁性,对某些物质如甲基橙具有良好的吸附性能。如果升高反应温度或者是延长反应时间会使LDHs 的粒径增大。 1.3 离子交换法制备LDHs 该方法是利用LDHs 的阴离子的可交换性与有机物质的可插层性,通过离子交换将阴离子或有机物质引入LDHs 层中以获得所需的LDHs 。离子交换法适用于合成特殊的阴离子LDHs 。 1.3.1 NO 3-LDHs 的制备 将Ni(NO 3)2·6H 2O 和Al(NO 3)3·9H 2O 制成摩尔比为3∶1的混合盐溶液。和特定浓度的1 mol/L 的NaOH 溶液同时滴入烧瓶中,溶液的pH 保持在约8.5。加完后,将混合物在40 ℃的恒温下搅拌24 h 。获得胶体硝酸根离子型双金属氢氧化物(NO 3-LDHs )样品,最后干燥,得到固体样品。1.3.2 Asp-LDHs 的制备 取16 g 制备的NO 3-LDHs 水滑石样品,并将其置于含有100 mL 去离子水的三颈烧瓶中。在40 ℃恒温条件下搅拌5 h 左右,使其溶胀,再取一定量的天冬氨酸(Asp ,Asp 与NO 3-LDHs 的摩尔比是2∶1)溶于100 mL 脱二氧化碳的去离子水中,并加入NaOH 使溶液呈弱碱性。将其缓慢加入NO 3-LDHs 溶液中,在恒温下搅拌24 h 。过滤洗涤后,将滤饼密封并置于 作者简介:钟硕(1998— ),女,河北沧州人,本科;研究方向:制药工程。 双金属氢氧化物的制备及其应用性能的研究进展 钟 硕,刘广涵,姜丽阳,范兰兰,杨 丹 (河北农业大学 理工学院,河北 黄骅 061100) 摘 要:双金属氢氧化物(LDHs )是一类具有双层结构的新型纳米固体材料,具有酸碱、层间阴离子可交换性和催化性能,它 在许多领域具有独特的优势,因此具有广泛的应用。本文研究了双金属氢氧化物的制备及其在医药、催化等领域的应用。关键词:双金属氢氧化物;制备方法;性能现代盐化工 Modern Salt and Chemical Industry
Hexagonal nanosheets from the exfoliation of Ni 2+-Fe 3+LDHs:a route towards layered multifunctional materials ? Gonzalo Abell a n,a Eugenio Coronado,*a Carlos Mart ?-Gastaldo,a Elena Pinilla-Cienfuegos a and Antonio Ribera ab Received 13th May 2010,Accepted 20th June 2010DOI:10.1039/c0jm01447h Here we report the synthesis of a crystalline micrometric-sized hexagonal-shaped Ni 2+-Fe 3+LDH by following a modi?ed homogeneous precipitation method.The exfoliation of the material in formamide leads to stable suspensions of hexagonal nanometric sheets,which have been extensively characterized.Our data con?rm that the intrinsic properties of the bulk material are retained by these segregated nanosheets,thus opening the door for their use in the development of layered multifunctional materials.Exfoliation of layered hydroxides,de?ned as the segregation of these lamellar inorganic solids into single entities through soft chemistry methods,1can be regarded as a versatile synthetic route to prepare stable suspensions of sheets,typically exhibiting homogeneous micrometric lateral size and nanometric thickness.Concerning materials science,these 2D nanosheets offer very interesting features:(a)owing to the nanometric thickness of these layers,they may exhibit new physical properties different from the bulk;(b)compared to other low dimensional nano-materials (0D or 1D),their two-dimensional structure facilitates their processability.In fact,these layers can be re-assembled into highly oriented ?lms by employing Langmuir–Blodgett (LB)or Layer-by-Layer (LbL)techniques;2(c)they can lead to the design of new multifunctional materials combining sophisticated phys-ical properties through the rational choice of the constituting building blocks and the precise control of their arrangement in the solid state.3 Among these layered materials,we were particularly interested in the layered double hydroxides (LDHs)compounds.The struc-ture of these anionic clays is closely related to that of the brucite,Mg(OH)2,with partial substitution of some of the divalent posi-tions with M 3+cations.This fact generates an excess of positive charge in the layers which must be balanced by the presence of anions and water molecules interleaved between the layers according to the formula:[M II 1àx M III x (OH)2](A n à)x/n $yH 2O.In this way,their exfoliation in organic solvents produces steady colloidal suspensions of positively charged nanosheets,4which in the presence of anionic components,can be further re-assembled into sandwich-like layered materials as result of the presence of attractive Coulombic interactions.5In addition,LDHs offer a wide plethora of intrinsic magnetic,optical or catalytic proper-ties,6which ultimately will be retained by the segregated layers and transferred to these layered super-structures.Concerning magne-tism,we recently reported the presence of spontaneous magneti-zation below 15K in Ni 2+-Fe 3+LDHs prepared by the traditional coprecipitation method,as result of the combination of strong antiferromagnetic superexchange interactions between the in-plane ions mediated by the hydroxyl bridge and much weaker dipolar interactions between the layers.7Unfortunately,the synthesis of crystalline Fe 3+-based LDHs with hexagonal morphology in an extendable controlled manner has been elusive so far.More generally,the synthesis of non-Al 3+-based LDHs is very disfavoured mainly due to the speci?c amphoteric behaviour of Al(OH)3.Except for remarkable efforts,8the use of traditional coprecipitation methods,based on the direct combination of the constituting ions in a basic medium,has just led to the isolation of amorphous phases.Although these materials can indirectly enhance its crystallinity after an additional hydrothermal treat-ment,they cannot be effectively exfoliated.9 Here we report how,by following a modi?ed homogeneous precipitation method,whose novelty resides in the use of the chelating agent triethanolamine (TEA;C 6H 15NO 3)as auxiliary reagent,permits the synthesis of a highly crystalline micrometric-sized hexagonal-shaped [Ni 1-x Fe x (OH)2](CO 3)x/2(x ?0.25)LDH.Besides,this material can be readily ion-exchanged with nitrate anions through the so-called ‘‘acid-salt treatment’’,10permitting its quantitative exfoliation in formamide.Regarding the potential magnetic functionality of these Ni 2+Fe 3+-LDH nanosheets,7this work paves the way for their use in the design of advanced multifunctional materials. Experimental Synthesis All chemical reagents,Ni(NO 3)2$6H 2O,Fe(NO 3)3$9H 2O,Al(NO 3)3$9H 2O,NaNO 3,HNO 3,C 6H 15NO 3(triethanolamine,TEA)and CO(NH 2)2(urea)were used as received from commercial suppliers (Sigma-Aldrich and Fluka)without further puri?cation. Synthesis of NiFe-CO 3LDH (1):LDHs were synthesized following a modi?ed homogeneous precipitation method by using urea and TEA as ammonium releasing reagent (ARR)and chelating agent,respectively. a Universidad de Valencia (ICMol),Catedr a tico Jos e Beltr a n n 2,46980Paterna,Spain.E-mail:eugenio.coronado@uv.es;Fax:+34963543273;Tel:+34963544415b Fundaci o n General de la Universidad de Valencia (FGUV),Amadeu de Savoia n 4,46010Valencia,Spain ?Electronic Supplementary Information (ESI)available:Further details concerning the experimental procedure and physical characterization of the materials here reported including X-ray diffraction,SEM images,EDAX metallic analysis,FT-IR and TG/DTA studies.See DOI:10.1039/c0jm01447h/ PAPER https://www.doczj.com/doc/5b17908414.html,/materials |Journal of Materials Chemistry D o w n l o a d e d b y H e F e i U n i v e r s i t y o f T e c h n o l o g y o n 10 J a n u a r y 2012P u b l i s h e d o n 02 A u g u s t 2010 o n h t t p ://p u b s .r s c .o r g | d o i :10.1039/C 0J M 01447H View Online / Journal Homepage / Table of Contents for this issue
第五讲碱金属元素 1.复习重点 碱金属元素的原子结构及物理性质比较,碱金属的化学性质,焰色反应实验的操作步骤; 原子的核外电子排布碱金属元素相似性递变性 2.难点聚焦 (1)碱金属元素单质的化学性质: O、1)相似性:碱金属元素在结构上的相似性,决定了锂、钠、钾、铷、铯在性质上的相似性,碱金属都是强还原剂,性质活泼。具体表现在都能与 2 Cl、水、稀酸溶液反应,生成含R+(R为碱金属)的离子化合物;他们的氧化物对应水化物均是强碱; 2 O 2)递变性:随着原子序数的增加,电子层数递增,原子半径渐大,失电子渐易,还原性渐强,又决定了他们在性质上的递变性。具体表现为:①与 2 H O反应越来越剧烈,③随着核电荷数的增强,其最高价氧化物对应的水化物的碱性增强:反应越来越剧烈,产物越来越复杂,②与 2 CsOH RbOH KOH NaOH LiOH >>>>; (2)实验是如何保存锂、钠、钾:均是活泼的金属,极易氧化变质甚至引起燃烧,它们又都能与水、水溶液、醇溶液等发生反应产生氢气,是易燃易
爆物质,存放它们要保证不与空气、水分接触;又因为它们的密度小,所以锂只能保存在液体石蜡或封存在固体石蜡中,而将钠、钾保存在煤油中; (3)碱金属的制取:金属Li 和Na 主要是用电解熔融氯化物的方法制取;金属K 因为易溶于盐不易分离,且电解时有副反应发生,故一般采用热还原法用Na 从熔融KCl 中把K 置换出来(不是普通的置换,而是采用置换加抽取的方法,属于反应平衡);铷和铯一般也采用活泼金属还原法制取。 (4).焰色反应操作的注意事项有哪些? (1)所用火焰本身的颜色要浅,以免干扰观察. (2)蘸取待测物的金属丝本身在火焰上灼烧时应无颜色,同时熔点要高,不易被氧化.用铂丝效果最好,也可用铁丝、镍丝、钨丝等来代替铂丝.但不能用铜丝,因为它在灼烧时有绿色火焰产生. (3)金属丝在使用前要用稀盐酸将其表面的氧化物洗净,然后在火焰上灼烧至无色,以除去能起焰色反应的少量杂质. (4)观察钾的焰色时,要透过蓝色的钴玻璃片,因为钾中常混有钠的化合物杂质,蓝色钴玻璃可以滤去黄色火焰,以看清钾的紫色火焰. 3. 例题精讲 例1 已知相对原子质量:Li 6.9,Na 23,K 39,Rb 85。今有某碱金属M 及其氧化物2M O 组成的混合物10.8 g ,加足量水充分反应后,溶液经蒸发和干燥得固体16 g ,据此可确定碱金属M 是[ ] A 、Li B 、Na C 、K D 、Rb 解析 设M 的相对原子质量为A ,当设混合物全是碱金属或全是碱金属氧化物时有如下关系: 22222M H O MOH H +=+↑ 222M O H O MOH += 10.8 g →10.8×[(A +17)/A]g 10.8 g →10.8×[2(A +17)/(2A +16)]g 但实际上该混合物中碱金属及其氧化物都存在,则可建立不等式:[10.8(17)/]16[10.8(17)/(8)]A A A A ?+>>?++。 解得:35.3>A >10.7,从碱金属的相对原子质量可知该碱金属只能是钠。 答案 B 例2 为了测定某种碱金属的相对原子质量,有人设计了如图所示的实验装置。该装置(包括足量的水)的总质量为ag 。将质量为bg 的某碱金属单质放入水中,立即塞紧瓶塞,完全反应后再称量此装置的总质量为cg 。
第一节氢氧化物沉淀法 除了碱金属和部分碱土金属外,其它金属的氢氧化物大都是难溶的(表12-1)。因此,可用氢氧化物沉淀法去除废水中的重金属离子。沉淀剂为各种碱性药剂,常用的有石灰,碳酸钠、苛性钠、石灰石、白云石等。 表12-1 某些金属氢氧化物的溶度积 注:表中所列溶度积,均为活度积,但应用时一般作为溶度积,不加区别。 对一定浓度的某种金属离子M n+来说,是否生成难溶的氢氧化物沉淀,取决于溶液中OH-离子浓度,即溶液的pH值为沉淀金属氢氧化物的最重要条件。若M n+与OH-只生成M(OH)n沉淀,而不生成可溶性羟基络合物,则根据金属氢氧化物的溶度积K sp及水的离子积K w,可以计算使氢氧化物沉淀的pH值: (12-1)或(12-2) 上式表示与氢氧化物沉淀平衡共存的金属离子浓度和溶液pH值的关系。由此式可以看出:(1)金属离子浓度[M n+]相同时,溶度积K sp愈小,则开始析出氢氧化物沉淀的pH值愈低;(2)同一金属离子,浓度愈大,开始析
出沉淀的pH值愈低。根据各种金属氢氧化物的K sp值,由公式(12-2)可计算出某一pH值时溶液中金属离子的饱和浓度。以pH值为横坐标,以—log[M n+]为纵坐标,即可绘出溶解度对数图(图12-1)。 根据溶解度对数图,可以方便地确定金属离子沉淀的条件。以Cd2+为例,若[Cd2+]=0.1mol/L,则由图上查出,使氢氧化镉开始沉淀出来的pH值应为7.7;若欲使溶液残余Cd2+浓度达10-5mol/L,则沉淀终了的pH值应为9.7。 如果重金属离子和氢氧根离子不仅可以生成氢氧化物沉淀,而且还可以生成各种可溶性的羟基络合物(对于重金属离子,这是十分常见的现象),这时与金属氢氧化物呈平衡的饱和溶液中,不仅有游离的金属离子,而且有配位数不同的各种羟基络合物,它们都参与沉淀-溶解平衡。在此情况下,溶解度对数图就要复杂些。今仍以Cd(II)为例,Cd2+与OH-可形成CdOH+、Cd(OH)2、Cd(OH)3-、Cd(OH)42-等四种可溶性羟基络合物,根据它们的逐级稳定常数和Cd(OH)2的溶度积K sp,可以确定与氢氧化镉沉淀平衡共存的各可溶性羟基络合物浓度与溶液pH值的关系,如图12-2中各实线所示。将同一pH值下各种型态可溶性二价镉Cd(II)s的平衡浓度相加,即得氢氧化镉溶解度与pH值的关系,如图中虚线所示。虚线所包围的区域为氢氧化镉沉淀存在的区域。考虑了羟基络合物的溶解平衡区域图,可以更好地确定沉淀金属氢氧化物的pH值条件。例如,由图12-2可以看出,pH=10~13时,Cd(OH)2(固)的溶解度最小,约等于10-5.2mol/L。因此,用氢氧化物沉淀法去除废水中的Cd(II)时,pH 值常控制在10.5~12.5范围内。其它许多金属离子(如Cr3+、Al3+、Zn2+、Pb2+、Fe2+、Ni2+、Cu2+),在碱性提高时都可明显地生成络合阴离子,而使氢氧化物的溶解度重又增加,这类既溶于酸又溶于碱的氢氧化物,常称为两性氢氧化物。
溶度积 溶度积定义 对于物质AnBm(s)= n A(aq)+ mB(aq), 溶度积(Ksp)=C(A) C(B)溶度积的应用很广泛。在定性分析中,利用金属硫化物、氢氧化物、碳酸盐等溶度积的差异分离金属离子。若往氯化铅饱和溶液中加入氯化钾时,溶液中Cl浓度增大,C(Pb )C(Cl大于氯化铅的溶度积大,这时将有部分离子发生Pb+2Cl =PbCl2 ↓的反应,将过剩的PbCl2沉淀出来,直至两种离子的浓度幂之积等于氯化铅的溶度积为止。因此,为使溶解度小的物质完全沉淀,需要加入含有共同离子的电解质。 人教版化学选修4化学反应原理第三章沉淀的溶解平衡涉及溶度积的计算溶解度与溶度积的关系 溶解度和溶度积的互相换算: 换算说明:根据溶度积常数关系式,难溶电解质的溶度积和溶解度之间可以互相换算。但在换算时,应注意浓度单位必须采用mol·L;另外,由于难溶电解质的溶解度很小,溶液浓度很小,难溶电解质饱和溶液的密度可近似认为等于水的密度。 1、已知溶度积, 计算溶解度S ( →S ) 例、已知BaSO4在298.15K时的溶度积为1.08×10,求BaSO4在298.15K时的溶解度。解:设BaSO4的溶解度(S)为x mol·L 因BaSO4为难溶强电解质,且Ba、SO4基本上不水解,所以在BaSO4饱和溶液中:BaSO4(s) Ba + SO4离子浓度/(mol·L)x x c(Ba)·c(SO4)= (BaSO4)(c) x·x = 1.08×10 S = x = 1.04×10 则S(BaSO4) = 1.04×10 mol·L (1)AB型难溶强电解质计算结果表明:对于基本上不水解的AB型难溶强电解质,其溶解度(S )在数值上等于其溶度积的平方根。即: S = ×c (2)AB2型难溶强电解质同时可推导出AB2(或A2B)型难溶电解质(如CaF2、Ag2CrO4等)其溶度积和溶解度的关系为: AB2 A+ 2B离子浓度/(mol·L)S 2S c(A)c(B)= (AB2)(c) S×(2S)= 4S= (AB2) 所以:S = ×c 也近似地适用于微弱水解的AB型、A2B(或AB2)型难溶强电解质。如CaSO4、AgCl、AgBr、AgI等,但不适用于易水解的难溶电解质(如ZnS)和难溶弱电解质及在溶液中易以离子对形式存在的难溶电解质。 2、已知溶解度S , 计算溶度积(S → ) 与→S 是可逆过程, 只要列出与S 的关系式, 即能求解。 两者都可以用来表示难溶电解质的溶解性大小。 溶度积是难溶解的固相与溶液中相应离子达到平衡时的离子浓度的乘积,只与温度有关。溶解度不仅与温度有关,还与系统的组成,PH的改变,配合物的生成等因素有关。只有同一类型的难溶电解质才能通过溶度积来比较其溶解度(mol/L)的相对大小。大多数物质实际溶解度S比由Ksp计算得到c要大。 编辑本段溶度积规则
15-16高考化学复习碱金属元素知识点小结碱金属都是银白色的金属(铯略带金色光泽),密度小,熔点和沸点都比较低。以下是碱金属元素知识点小结,请大家掌握。 1.碱金属元素 碱金属包含锂(Li)、钠(Na)、钾(K)、铷(Rb)、铯(Cs)、钫(Fr)六种元素.由于钫是人工放射性元素,中学化学不作介绍. 2.碱金属元素的原子结构 相似性:碱金属元素的原子最外层都只有1个电子,次外层为8个电子(其中Li原子次外层只有2个电子).所以在化学反应中,碱金属元素的原子总是失去最外层的1个电子而显+1价. 递变性:Li、Na、K、Rb、Cs等碱金属元素的原子核外电子层数逐渐增多,原子半径逐渐增大,核对最外层电子的吸引力逐渐减弱,失电子能力逐渐增强,元素的金属性逐渐增强. 3.碱金属的物理性质及其变化规律 (1)颜色:银白色金属(Cs略带金色光泽). (2)硬度:小,且随Li、Na、K、Rb、Cs,金属的硬度逐渐减小.这是由于原子的电子层数逐渐增多,原子半径逐渐增大,原子之间的作用力逐渐减弱所致.碱金属的硬度小,用小刀可切割. (3)碱金属的熔点低.熔点最高的锂为180.5℃,铯的熔点是28.4℃.随着原子序数的增加,单质的熔点逐渐降低. (4)碱金属的密度小.Li、Na、K的密度小于水的密度,且锂的密度小于煤油的密度.随着原子序数的增大,碱金属的密度逐渐增大.但钾的密
度小于钠的密度,出现反常现象.这是由于金属的密度取决于两个方面的作用,一方面是原子质量,另一方面是原子体积,从钠到钾,原子质量增大所起的作用小于原子体积增大的作用,所以钾的密度反而比钠的密度小. 4.碱金属的化学性质 碱金属与钠一样都是活泼的金属,其性质与钠的性质相似.但由于碱金属原子结构的递变性,其金属活泼性有所差异,化合物的性质也有差异. (1)与水反应 相似性:碱金属单质都能与水反应,生成碱和氢气. 2R+2H2O=2ROH+H2(R代表碱金属原子) 递变性:随着原子序数的增大,金属与水反应的剧烈程度增大,生成物的碱性增强. 例如:钠与冷水反应放出热量将钠熔化成小球,而钾与冷水反应时,钾球发红,氢气燃烧,并有轻微爆炸.LiOH是中强碱,CsOH是最强碱. (2)与非金属反应 相似性:碱金属的单质可与大多数非金属单质反应,生成物都是含R+阳离子的离子化合物. 递变性:碱金属与氧气反应时,除锂和常温下缓慢氧化的钠能生成正常的氧化物(R2O)外,其余的碱金属氧化物是复杂氧化物. 4Li+O2=2Li2O 4Na+O2
溶解度与溶度积 联系:溶度积与溶解度均可表示难溶电解质的溶解性,两者之间可以相互换算。区别:溶度积是一个标准平衡常数,只与温度有关。而溶解度不仅与温度有关,还与系统的组成、 pH 值的改变及配合物的生成等因素有关。 在溶度积的计算中,离子浓度必须是物质的量的浓度,其单位为 而溶解度的单位有 g/100g 水, g·L-1, mol·L-1。计算时一般要先将难溶电解质的溶解度 S 的单位换算为 mol·L-1。对于难溶物质饱和溶液浓度极稀,可作近似处理: (xg/100gH2O)×10/M mol ·L-1。 几种类型的难溶物质溶度积、溶解度比较 物质类型难溶物质溶度积 Ksp 溶解度 /mol ·L-1 换算公式 AB AgCl 1.77 ×10-10 1.33 ×10-5 Ksp =S2 BaSO4 1.08 ×10-10 1.04 ×10-5 Ksp =S2 AB 2 CaF2 3.45 ×10-11 2.05 ×10-4 Ksp =4S3 A 2 B Ag 2CrO4 1.12 ×10-12 6.54 ×10-5 Ksp =4S3 对于同种类型化合物而言,Ksp , S 。 但对于不同种类型化合物之间,不能根据Ksp 来比较 S 的大小。 mol·L -1;
例 1、25℃时, AgCl 的溶解度为 1.92 ×10-3g ·L -1,求同温度下 AgCl 的溶度积。 例 2、25℃时,已知 Ksp(Ag 2 4 -12 4) -1 。 ×10 ,求同温度下 S(Ag 2 · CrO )=1.1 CrO /g L 例 3、查表知 PbI 2 的 Ksp 为 1.4 ×10-8,估计其溶解度 S(单位以 g ·L -1 计)。 溶度积规则 在难溶电解质溶液中,有关离子浓度幂的乘积称为浓度积,用符号 Q C 表 示 ,它表示任一条件下离子浓度幂的乘积。 Q C 和 Ksp 的表达形式类似,但其 含义不同。 Ksp 表示难溶电解质的饱和溶液中离子浓度幂的乘积, 仅是 Q C 的一 个特例。 对某一溶液,当 (1)Q C = Ksp ,表示溶液是饱和的。 这时溶液中的沉淀与溶解达到动态平衡, 既无沉淀析出又无沉淀溶解。 (2)Q C < Ksp ,表示溶液是不饱和的。溶液无沉淀析出, 若加入难溶电解质,则会继续溶解。 (3)Q C > Ksp ,表示溶液处于过饱和状态。有沉淀析出。 以上的关系称溶度积规则 (溶度积原理 ),是平衡移动规律总结,也是判断沉淀生成和溶解的依据。 当判断两种溶液混合后能否生成沉淀时,可按下列步骤进行: (1)先计算出混合后与沉淀有关的离子浓度; (2) 计算出浓度积 Qc ; (3) 将 Qc 与 Ksp 进行比较,判断沉淀能否生成。 溶度积规则的应用 (1)判断是否有沉淀生成 原则上只要 Qc >Ksp 便应该有沉淀产生,但是只有当溶液中含约 10-5g ·L -1 固体时,人眼才能观察到混浊现象, 故实际观察到有沉淀产生所需的离子浓度往往要比理论计算稍高些。 (2)判断沉淀的完全程度 没有一种沉淀反应是绝对完全的,通常认为溶液中某离子的浓度小于 -5 -1
高考化学复习碱金属元素知识点总结 碱金属都是银白色的金属(铯略带金色光泽),密度小,熔点和沸点都比较低。以下是碱金属元素知识点,请大家掌握。 1.碱金属元素 碱金属包含锂(Li)、钠(Na)、钾(K)、铷(Rb)、铯(Cs)、钫(Fr)六种元素.由于钫是人工放射性元素,中学化学不作介绍. 2.碱金属元素的原子结构 相似性:碱金属元素的原子最外层都只有1个电子,次外层为8个电子(其中Li原子次外层只有2个电子).所以在化学反应中,碱金属元素的原子总是失去最外层的1个电子而显+1价. 递变性:Li、Na、K、Rb、Cs等碱金属元素的原子核外电子层数逐渐增多,原子半径逐渐增大,核对最外层电子的吸引力逐渐减弱,失电子能力逐渐增强,元素的金属性逐渐增强. 3.碱金属的物理性质及其变化规律 (1)颜色:银白色金属(Cs略带金色光泽). (2)硬度:小,且随Li、Na、K、Rb、Cs,金属的硬度逐渐减小.这是由于原子的电子层数逐渐增多,原子半径逐渐增大,原子之间的作用力逐渐减弱所致.碱金属的硬度小,用小刀可切割. (3)碱金属的熔点低.熔点最高的锂为180.5℃,铯的熔点是28.4℃.随着原子序数的增加,单质的熔点逐渐降低. (4)碱金属的密度小.Li、Na、K的密度小于水的密度,且锂的
密度小于煤油的密度.随着原子序数的增大,碱金属的密度逐渐增大.但钾的密度小于钠的密度,出现反常现象.这是由于金属的密度取决于两个方面的作用,一方面是原子质量,另一方面是原子体积,从钠到钾,原子质量增大所起的作用小于原子体积增大的作用,所以钾的密度反而比钠的密度小. 4.碱金属的化学性质 碱金属与钠一样都是活泼的金属,其性质与钠的性质相似.但由于碱金属原子结构的递变性,其金属活泼性有所差异,化合物的性质也有差异. (1)与水反应 相似性:碱金属单质都能与水反应,生成碱和氢气. 2R+2H2O=2ROH+H2(R代表碱金属原子) 递变性:随着原子序数的增大,金属与水反应的剧烈程度增大,生成物的碱性增强. 例如:钠与冷水反应放出热量将钠熔化成小球,而钾与冷水反应时,钾球发红,氢气燃烧,并有轻微爆炸.LiOH是中强 碱,CsOH是最强碱. (2)与非金属反应 相似性:碱金属的单质可与大多数非金属单质反应,生成物都是含R+阳离子的离子化合物. 递变性:碱金属与氧气反应时,除锂和常温下缓慢氧化的钠能生成正常的氧化物(R2O)外,其余的碱金属氧化物是复杂氧化