
原电池练习题
1.
下列
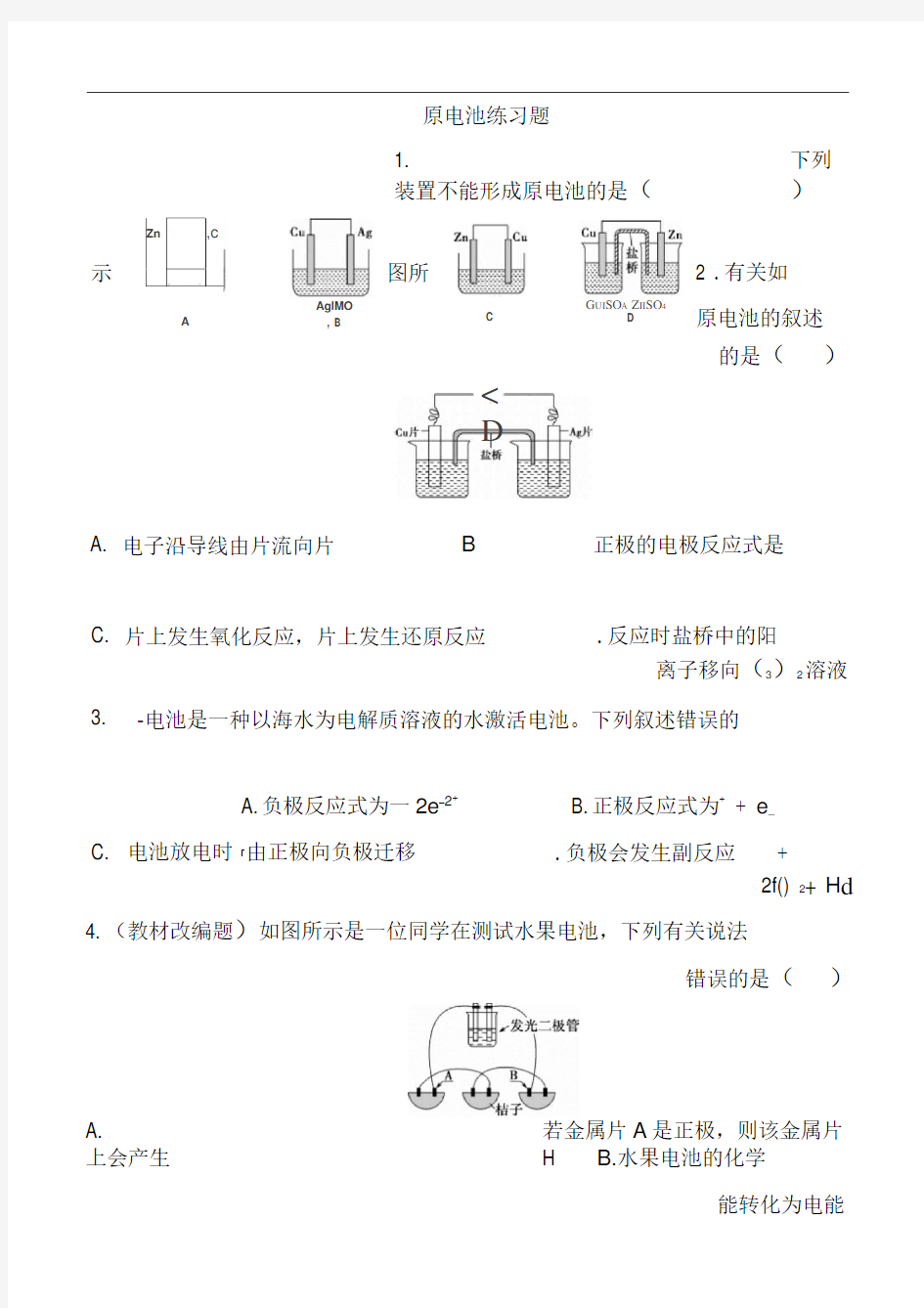
装置不能形成原电池的是(
)
的是(
)
离子移向(3)2溶液
-电池是一种以海水为电解质溶液的水激活电池。下列叙述错误的
2f() 2+ H d
4. (教材改编题)如图所示是一位同学在测试水果电池,下列有关说法
错误的是(
)
A.
若金属片A 是正极,则该金属片上会产生 H B.水果电池的化学
能转化为电能
Zn
,c
-J -
-
~
原电池的叙述 A. 电子沿导线由片流向片
C. 片上发生氧化反应,片上发生还原反应
正极的电极反应式是
.反应时盐桥中的阳
3.
A. 负极反应式为一2e _2+
B. 正极反应式为+
+ e _ C. 电池放电时「由正极向负极迁移
.负极会发生副反应
+ 示
A
AglMO , B
图所
C
2 .有关如
D
G UI SO A Z II SO 4
B C. 此水果发电的原理是电磁感应 D. 金属片A B 可以一个是铜片,另一个是铁片 5. 某电池以K 24和为电极材料,溶液为电解质溶液。下列说法正确的是 ( ) B .正极反应式为2+ 10H + + 6e 2Q + 5H 2O C.该电池放电过程中电解质溶液浓度不变 D .电池工作时「向负极迁 移 6. 如图所示装置中,观察到电流计指针偏转, M 棒变粗,N 棒变细,由 此判断表中所列 M N P 物质,其中可以成立的是( ) M n nN 选项 M N P A 稀H 24 B 稀 C 3溶液 D (3)3溶液 7. 分析下图所示的四个 原电池装置,其中结论正确的是 ( ) A. ①②中作负极,③④中作负极 B. ②中作正极,电极反应式为 6HO+ 6e _ 6_ + 3H4 D.④中作正极,电极反应式为 2H + + 2e — 2T 8. (2017 ?泗洪模拟)如图是某同学设计的原电池装置,下列叙述中正 A.为电池的负极,被还原 C.③中作负极,电极反应式为一 2e 空气 稀H$a N H OH 请液 诳HNOj N H C ]辯 臧 确的是() A .电极I 上发生还原反应,作原电池的负极 B. 电极□的电极反应式为2+ + 2e " C. 该原电池的总反应为 23+ + 2+ + 22+ D. 盐桥中装有含氯化钾的琼脂,其作用是传递电子 9. . M N 、P 、E 四种金属,已知:①X W + M :②M P 用导线连接 放入4溶液中,M 表面有大量气泡逸出;③N E 用导线连接放入E 的硫酸盐 溶液中,电极反应为E 2 + + 2e _ , N-2e —2+ 。则这四种金属的还原性由强到弱 的顺序是( ) A. P > M> N> E B . E > N> M> P C. P > N> E D . E > P > M> N 10 . 一定量的稀盐酸跟过量锌粉反应时,为了加快反应速率又不影响 生成H 2的总量,可米取的措施是( ) A.加入少量稀溶液 B .加入少量3固体 C.加入少量44固体 D .加入少量4溶液 11 . (2017 ?开封高三调研)如图,在盛有稀H 24的烧杯中放入用导线连 接的电极X 、Y 外电路中电子流向如图所示,关于该装置的下 列说法正确的是( ) A. 外电路的电流方向为 X ^导线fY B. 若两电极分别为铁和碳棒,则 X 为碳棒,Y 为铁 C. X 极上发生的是还原反应, Y 极上发生的是 氧化反应 D. 若两电极都是金属,则它们的活动性顺序为 X>Y C1 液 U 稀 M.SO. 12. 一次电池——碱性锌锰干电池 梓粉和KOH 的程合物 -MnO 2 丄金局外壳 13. 二次电池(以铅蓄电池为例) 1.放电时的反应 (1) __________________________________ 负极: (氧化反应); (2) 正极: ___________________________________________ (还原反应 ); (3) ____________________________________________________ 总反 应: ___________________________________________________________ 。 2. 充电时的反应 (1) ______________________________________________________ 阴极: ______________________________________________________ (还原反应); (2) ________________________________________________________ 阳极: __________________________________________________________(氧化反 应); (3) ________________________________________________ 总反应: 。 原电池练习答案 1. 解析:选Co A B 、D 项都具有①活泼性不同的电极;②电解质溶液; ③闭合回路;④自发进行的氧化还原反应,均能构成原电池; C 项中酒精为 非电解质,不能构成原电池。 正极材 ,电极反应式: ; 负极材料: ,电极反应式: 总反应: 2.解析:选D。该装置是原电池装置,其中为负极,失电子发生氧化反应:一 2e_2+,为正极,得电子发生还原反应:+ + e「。原电池中,负极()失去的电子沿导线流向正极() ,盐桥中的阳离子移向正极,即移向3溶液,综上所述, D 错误。 3. [解析]该电池中作 负极,失去电子发生氧化反应,生成2+, A项正 确;正极反应为+ e_ + _?B项错误;对原电池来说,阴离子由正极移向负极, C项正确;在负极,会发生副反应+ 2H()2+ H T, D项正确。 [ 答案] B 4. 答案:C 5. 解析:选D。A. 根据化合价升降判断,化合价只能升高,故为负极材 料,被氧化,不正确;溶液为电解质溶液,则正极电极反应式为2+ 6e-+ 8H22() 3+ 10-,错误; C .该电池放电过程中电解质溶液浓度减小,错误; D. 电池工作时阴离子向负极迁移,正确。6. 解析:选C。在装置中电流计指针发生偏转,说明该装置构成了原电池,根据正负极的判断方法,溶解的一极为负极,增重的一极为正极,所以M棒为正极,N棒为负极,且电解质溶液能析出固体,则只有C项正确。 7. 解析:选B。②中不与溶液反应,而能和溶液反应失去电子,故是负 极;③中在浓硝酸中易钝化,和浓3反应失去电子作负极,A、C均错。②中电池 总反应为2+ 2+ 2HZ + 3H T,负极电极反应式为2+ 8"- 6e" 2+ 4H0, 二者相减得到正极电极反应式为6H0+ 6e-6- + 3H4, B正确。④中是正极,电极反应式为 Q+ 2H b O+ 4e-4-, D错。 8. 解析:选Co该原电池的总反应为23+ + 2 + + 22+。电极I上发生还原反 应,作原电池的正极,反应式为23+ + 2e-22+,电极□为原电池负极,发生氧化反 应,电极反应式为-2e-2 +。盐桥中装有含氯化钾的琼脂,其作用是传递离子。 9. 解析:选A。由①知,金属活动性:M> N; M P用导线连接放入4溶 液中,M表面有大量气泡逸出,说明M作原电池的正极,故金属活动性:P> M; N E构成的原电池中,N作负极,故金属活动性:N> E。10. 解析:选a A中加入溶液,消耗盐酸,反应速率减慢,且氢气的生成量会减少,错误;B中加入3-会结合H+,生成醋酸,减慢反应速率,错误; C中加入44固体,增加了N的量,生成的氢气会增多,错误;D中加入少量 4溶液,置换出少量附着在锌表面,形成原电池可以加快反应速率,并且没有 影响氢气的生成量,正确。 11. 解析:选D。外电路的电子流向为心导线f Y,电流方向与其相反; X极失电子,作负极,发生的是氧化反应,Y极发生的是还原反应;若两电 极分别为铁和碳棒,则Y为碳棒,X为铁。 12. 负极材料:,电极反应式:+ 2_ —2e—() 2; 正极材料:2,电极反应式:22+ 2HO+ 2e—2+ 2—; 总反应:+ 22 + 2H?2 + () 2o 13. 1. 放电时的反应 (1) 负极:(s) + () —2e—4(s)(氧化反应); (2) 正极:2(s) + 4J () + () + 2e—4(s) + 2H0(l)(还原反应); (3) 总反应:(s) + 2(s) + 2H M()2 4(s) + 2HzO(l)。 2. 充电时的反应 (1) 阴极:4(s) + 2e—(s) + ()(还原反应); (2) 阳极:4(s) + 2HbO(l) —2e—2(s) + 4H+() + ()(氧化反应); (3) 总反应:24(S) + 2HO(l)(s) + 2(s) + 2H M()。