元素符号、化学式、离子符号、化合价-练习
- 格式:doc
- 大小:57.50 KB
- 文档页数:2

一、常见元素名称或元素符号1、氢元素氧元素钠元素碳元素氯元素锰元素锌元素钙元素2、Si N Ne AlFe Cu F Mg3、3个氢原子2个氧原子2个碳原子二、常见离子符号3个硫酸根离子硝酸根离子2个碳酸根离子铵根离子4个氢氧根离子3个碳酸氢根离子三、常见单质的书写氦气氯气氖气氮气氢气氧气氩气氟气臭氧碘溴金刚石铜磷石墨四、常见化合物的书写(一)1、水一氧化碳二氧化碳二氧化硫三氧化硫一氧化氮二氧化氮五氧化二磷2、过氧化氢3、氧化铜氧化钙氧化铁氧化铝氧化镁氧化钠四氧化三铁氯化氢4、氯化钠氯化镁氯化钡氯化钙氯化铜氯化铁氯化亚铁五、常见的化合物(二)1、硫酸盐酸硝酸碳酸2、氢氧化钠氢氧化钾氢氧化钡氢氧化铜氢氧化铁氢氧化铝氢氧化钙氢氧化镁3、碳酸钙碳酸钠碳酸钡碳酸氢钠硫酸钠硫酸铜硫酸亚铁硫酸钡硝酸铵硝酸钾硝酸钡硝酸铜六、符号的意义1、“Cl”表示、。
“2Cl”表示;“2Cl2”表示。
2、“Fe”表示3、“H2O”表示4、下列符号的“2”各表示什么意义○1H2○22H○32H2○4H2O○52CO○62O2○7Mg2++2○8MgO○92OH-- 1 -- 2 -化合价(总共7句)1、钾钠氢银+1价2、氟氯溴碘−1价3、钙镁钡锌+2价4、氧是−2铝+35、亚铜+1铜+26、亚铁+2铁+37、莫忘单质是0价常见原子团−1价的有:氢氧根OH−硝酸根NO3−碳酸氢根HCO3−−2价的有:碳酸根CO32−硫酸根SO42−+1价的有:铵根NH4+- 3 -。

化合价与化学式书写练习化合价与化学式书写练1.请默写出前20个元素的名称及符号。
2.请写出下列元素的符号或名称:铁、铜、锌、汞、钙、氦、铝、氧、镁、钠、银。
3.请写出下列常见物质的化学式:氢气、氧气、氮气、氯气、硫、铝箔、碳、红磷、铁丝、五氧化二磷、二氧化碳、二氧化硫、四氧化三铁、水、过氧化氢、二氧化锰、高锰酸钾、锰酸钾、氯酸钾、氯化钾、氯化氢、碳酸钙。
4.请标出下列元素的常见化合价:H、Cl、Na、K、Ag、O、Ca、Mg、Ba、Zn、Al、Si、P、Cu、Hg、OH、NO3、SO4、CO3、NH4.5.练将左竖显正价的元素或原子团与右横显负价的元素或原子团组成的化合物的化学式及名称:HCl、HNO3、H2SO4、Na2CO3、KOH、Ca(OH)2、Mg(OH)2、ZnCl2、AlCl3.6.化合物由不同种的元素组成。
练写出下列物质的化学式。
一)氧化物(氧元素常显-2价):水(H2O)、过氧化氢(H2O2)、二氧化锰(MnO2)、五氧化二磷(P4O10)、二氧化硫(SO2)、二氧化碳(CO2)、一氧化碳(CO)、二氧化氮(NO2)、氧化铁(Fe2O3)、氧化亚铁(FeO)、四氧化三铁(Fe3O4)、氧化铜(CuO)、氧化镁(MgO)、氧化钙(CaO)、氧化铝(Al2O3)。
二)酸:盐酸(HCl)、碳酸(H2CO3)、硫酸(H2SO4)、硝酸(HNO3)。
三)碱:(氢氧根的化合价为-1价):氢氧化钠(NaOH)、氢氧化钙(Ca(OH)2)、氢氧化铝(Al(OH)3)、氢氧化镁(Mg(OH)2)、氢氧化钡(Ba(OH)2)、氢氧化钾(KOH)。
四)盐:1)氯化物(氯元素常显-1价):氯化钠(NaCl)、氯化钙(CaCl2)、氯化铝(AlCl3)。
常见化合物及其离子价1)氯化物(氯离子显价)1.氯化钠 NaCl。
2.氯化钙 CaCl2.3.氯化铝 AlCl3.4.氯化铁FeCl3.5.氯化亚铁 FeCl2.6.氯化铜 CuCl。

一、填空化合价练习(1)在化合物中,氢元素的化合价普通为价,氧元素的化合价普通为价,金属元素在化合物中普通显价,非金属元素在跟金属元素或氢元素化合时,普通显价。
(2)在单质里,元素的化合价为。
(3)在化合物里,元素的正负化合价的代数和为。
二.标出下列物质中各元素的化合价.SiO2MgO SO3CO2K2O AgCl Cu H2NaOH O2三、对于S、H2SO4、H2S、SO2中的硫元素的化合价由高到低的排列是。
四、写出下列物质的化学式.氧化钠硫化钾氯化钙硫化铝氢氧化镁碳酸钙硝酸钠硫酸钡磷酸铵四氯化碳五、写出下列元素或原子团的化合价以及离子符号.六、(1)某三价金属元素R 的相对原子质量为27,则其氧化物的化学式为,其相对分子质量为。
(2)某金属氧化物中,氧元素的质量分数为30%,该金属的相对原子质量为56,则该金属在氧化物中的化合价为,化学式为,相对分子质量为。
七、选择题1.下列物质中,硫元素的化合价相似的一组是()A.SO2 和SO3B.S 和H2SC.H2 S 和H2 SO4D.Na2 SO3 和SO22.某种含硫的化合物中,硫和氧质量比为2:3,则该化合物中硫的化合价可能是()A.-2B. +2C. +4D.+63.下列物质中,氯元素为+5 价的是()A.KClO3B.KClC.KClO4D.Cl24.能对的表达镁离子的是()+2A.MgB.Mg 2+C.Mg +2D.5.下列有关化合价的说法中,对的的是()A.硫元素含有可变的化合价B. 任何物质中,氧元素均显-2 价C. 金属铁能够有-2 价D. 各非金属元素都没有正价6.某元素R 的原子量为23,已知R +的核外电子排布与氖原子相似,则元素R 的原子核内+12 2 8 23 34 4 中子数为( )A. 12B. 11C. 23D. 22 7. 下列各原子团中,含有+6 价元素的是( )A. NO -B. CO 2-C. MnO 2-D. NH +8. 某元素 X 的最外层有 3 个电子,某元素 Y 的最外层有 6 个电子,这两种元素构成的化合物的化学式可能是( )A. X 2Y 3B. XYC. Y 3 X 2D. X 3Y 29. 已知下列各组原子的核电荷数,可形成 AB 2 型化合物的是( )A. 1 和 8B. 6 和 8C. 10 和 16D. 12 和 17 10. 下列物质中氮元素化合价最低的是( ) A. NOB. N 2C. NH 3D. NO 211. 某+3 价金属 A ,它在氧化物中的质量分数为 70%,则 A 的原子量为( )A. 11B. 27C. 56D. 114 12. 钠的原子量为 23,钠原子失去一种电子后发生变化的是( ) A. 电子层数 B. 核电荷数 C. 元素种类 D. 微粒的中子数13. 工业用盐亚硝酸钠( NaNO 2 )误作食盐,会使人中毒死亡, NaNO 2 中 N 的化合价是() A. +2 B. +3 C. +4 D. +514. 下列各组含氮物质中,按氮元素的化合价由低到高的次序排列的是( )A. N 2 、N 2 O 、NH 4 Cl 、NO 2 、HNO 3B. NH 4 Cl 、N 2 、N 2 O 、NO 2 、HNO 3C. HNO 3 、NO 2 、N 2 O 、N 2 、NH 4 ClD. NO 2 、N 2 O 、N 2 、HNO 3 、NH 4 NO 315. 某化合物的化学式为 H m RO n ,则 R 的化合价是( )A. +(2n - m )B. +2(2n - m )C. -(m - 2n )D. +(2n + m ) 16. 对于 Fe 3+ 、Fe 2+ 、Fe 三种微粒的判断,不对的的是()A. 质量几乎相等B. 属于同种元素C. 核外电子数相似D. 核电荷数相似17. 下列各物质中,除氢、氧元素外,第三种元素化合价相等的是()(1) H 2 SO 4 (2) KOH (3) HClO (4) HNO 3 (5) HMnO 4 (6) H 3 PO 4 A. (1)(5) B. (2)(3) C. (4)(6) D. (3)(4)18. 核内质子数相似,核外电子数不同的两种微粒,它们可能是()A.两种不同元素的原子B. 同种元素的原子和离子C. 不同种元素的原子和离子D. 同种元素的两种离子19.把左边和右边的对应关系用直线连结起来。
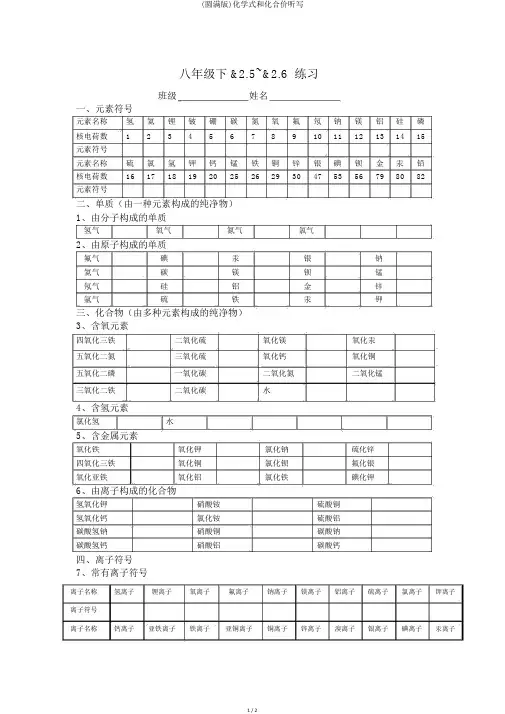
八年级下 &2.5~&2.6 练习班级姓名一、元素符号元素名称氢氦锂铍硼碳氮氧氟氖钠镁铝硅磷核电荷数 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15元素符号元素名称硫氯氩钾钙锰铁铜锌银碘钡金汞铅核电荷数16 17 18 19 20 25 26 29 30 47 53 56 79 80 82元素符号二、单质(由一种元素构成的纯净物)1、由分子构成的单质氢气氧气氮气氯气2、由原子构成的单质氟气碘汞银钠氦气碳镁钡锰氖气硅铝金锌氩气硫铁汞钾三、化合物(由多种元素构成的纯净物)3、含氧元素四氧化三铁二氧化硫氧化镁氧化汞五氧化二氮三氧化硫氧化钙氧化铜五氧化二磷一氧化碳二氧化氮二氧化锰三氧化二铁二氧化碳水4、含氢元素氯化氢水5、含金属元素氧化铁氧化钾氯化钠硫化锌四氧化三铁氧化铜氯化钡氟化银氧化亚铁氧化铝氯化铁碘化钾6、由离子构成的化合物氢氧化钾硝酸铵硫酸铜氢氧化钙氯化铵硫酸铝碳酸氢钠硝酸铜碳酸钠碳酸氢钙硝酸铝碳酸钙四、离子符号7、常有离子符号离子名称氢离子锂离子氧离子氟离子钠离子镁离子铝离子硫离子氯离子钾离子离子符号离子名称钙离子亚铁离子铁离子亚铜离子铜离子锌离子溴离子银离子碘离子汞离子离子符号8、带电的原子团名称氢氧根硫酸根硝酸根碳酸根碳酸氢根铵根离子符号-化合价五、常有化合价金属元素元素符号常有化合价非金属元素元素符号常有化合价钾 氢 钠 氟 银 氧 钙 氯 镁 溴 钡 碘 锌 氮 铝 磷 铜 硫 铁 碳锰硅 六、写出以下符号的意义:O: , 2O:O 2:,2O 2 :O 2--2O H 2OnH 2O+ 22+Mg OMg七、用数字和符号表示:4 个铵根离子 ; 2 个亚铁离子 ;标出氧化铁中 Fe 的化合价2 个氯气分子 ; m 个铜原子; n 个硫酸根离子 ;2 个镁离子4 个铁离子3 个硫酸根离子3 个二氧化硫分子:4 个亚铁离子4 个铁原子八、数字的含义(写出以下符号中数字2 的含义)2H+2++ 22HMgMg O2H O 前面数字 2______下角标数字 2_________2九、请标出带点元素在化合物或原子团中的化合价2-S O 3 2- --2SSSO 2 Na 2SO 3H 2SO 4SO 4C lO 3 N O 3. . . . . . . .. KMnO K 2 MnO F eSO F eCl 3 C a(OH) 2M nO 2M nCl 2M n . 4 . 4 . 4 . . . ..NO NO 2 NH 4NO 3 NaClC12KC lO 3 Fe 2O 3FeSO 4、 CuO.. . . . . . . . .。

“化学用语”(元素符号、化学式、化学方程式)专题练习一.说出下列符号的含义:1.H:2、2H:23、H2:4、2H2:25.H+:6、2H+:27、3Mg2+:二.说出下列符号中数字“2”的含义:1、2S:22、SO2:3、S2-:4、2S2-:5、MgO:6、SO42-:三.用数学或符号表示:1、3个铝原子:2、5个水分子:23、a个氦分子:4、b个铁离子:5、3个硫酸根离子:6、m个碳酸根离子:37、2个亚铁离子:8、氯酸钾中氯的化合价:4四.写出下列物质的化学式:1、氯化钾:2、氯酸钾:3、硫酸铜:4、硫酸锌:5、硫化锌:6、氢氧化钙:7、氯化钠:8、氧化钙:9、碳酸钠:10、硝酸铵:11、硫酸亚铁:12、氢氧化钠:五.用序号回答下列问题:1、写出下列粒子的名.称.、符号..:A:____B:_____C:_____D:____E:______2、以上粒子中,表示原子的是;表示阳离子的有__种,阴离子有__种;电子排布相同的是;五、配平下列化学方程式(反应条件忽略):1、Al + Fe3O4—- Fe + Al2O32、Al + MnO2—Mn + Al2O33、 CO + Fe3O4 —- Fe + CO 24、 C+ Fe3O4 —— Fe + CO 25、 H 2 + WO 3 —— W + H 2O6、 Fe + H 2O —— H 2 + Fe3O47、 FeS 2 + O 2 —— Fe2O3+ SO 28、 MnO 2+ HCl —— MnCl2 + Cl 2 + H 2O9、 Cl 2 + Ca (OH )2 —— CaCl2 + Ca (ClO )2 + H 2O六.(1) 3Cu+8HNO3==3Cu (NO 3)2+2X ↑+4H 2O ,求X 的化学式为 。
(2) R+3O 2==2CO 2+3H 2O 求R 的化学式为 。

精英学校姓名:_______________班级:_______________考号:_______________题号一、选择题二、填空题总分得分一、选择题(每空?分,共?分)1、蒜是常见的调味品之一,大蒜中主要成分大蒜素具有消毒杀菌作用。
大蒜素的化学式为C6H10S3,下列说法不正确的是()A.大蒜素的一个分子由6个碳原子、10个氢原子和3个硫原子构成B.大蒜素中碳、氢、硫三种元素的质量比为6:10:3C.大蒜素由碳、氢、硫三种元素组成D.大蒜素属于化合物2、五氧化二碘(I2O5)可用来测定空气中一氧化碳的含量,I2O5中碘元素的化合价为()A.-5 B.+5 C.+3 D.+23、下列微粒符号中,对“2”含义的理解正确的是:A、2Cu中的“2”表示2个铜元素B、Fe2+中的“2”表示每个亚铁离子带有2个单位的正电荷C、H2S中的“2”表示1个硫化氢分子中含有2个硫原子D、中化学式上方的“2”表示硫元素为-2价4、下列符号中,既表示一个原子,又表示一种元素,还表示一种物质的是(A)NaCl (B)Fe (C)O2(D) H5、1个CO2分子和1个SO2分子中,一样多的是评卷人得分(A)氧分子数(B)氧原子数(C)电子数(D)氧元素的质量分数6、图中○和●分别表示氢原子和氧原子,其中的粒子可用4H表示的是(A)(B)(C)(D)7、脑黄金在医药、食品等行业中应用前景非常广泛,其化学式为C25H51COOH.下列对脑黄金的说法正确的是( )A.该物质中含有80个原子B.脑黄金分子是由碳、氢、氧三种元素组成的C.构成该物质的一个分子是由80个原子构成的D.该物质中碳、氢、氧元素质量比为13︰26︰18、小明的作业有以下表述,其中错误的是A.水是由水分子构成的B.氢氧化钠是由钠离子和氢氧根离子构成的C.铁是由铁原子构成的D.二氧化氮是由一个氮元素和两个氧元素组成的9、世界卫生组织将某氧化物RO2列为A级高效安全灭菌消毒剂,它在食品保鲜、饮用水消毒等方面有着广泛应用。
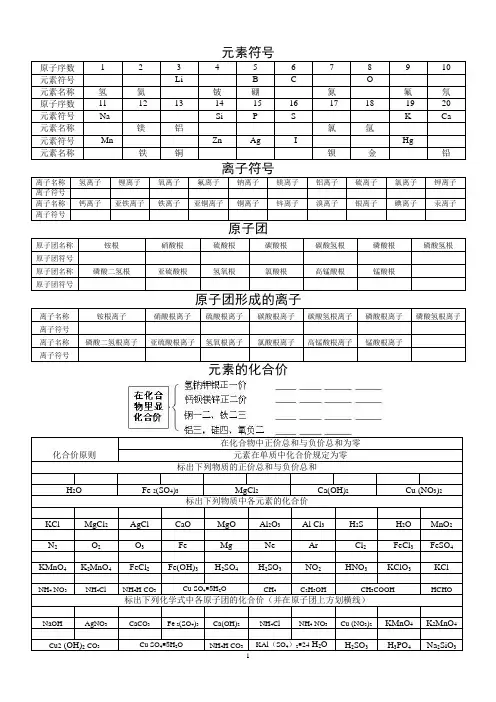
元素符号原子序数 1 2 3 4 5 6 7 8 9 10 元素符号Li B C O元素名称氢氦铍硼氮氟氖原子序数11 12 13 14 15 16 17 18 19 20 元素符号Na Si P S K Ca 元素名称镁铝氯氩元素符号Mn Zn Ag I Hg元素名称铁铜钡金铅离子名称氢离子锂离子氧离子氟离子钠离子镁离子铝离子硫离子氯离子钾离子离子符号离子名称钙离子亚铁离子铁离子亚铜离子铜离子锌离子溴离子银离子碘离子汞离子离子符号原子团名称铵根硝酸根硫酸根碳酸根碳酸氢根磷酸根磷酸氢根原子团符号原子团名称磷酸二氢根亚硫酸根氢氧根氯酸根高锰酸根锰酸根原子团符号离子名称铵根离子硝酸根离子硫酸根离子碳酸根离子碳酸氢根离子磷酸根离子磷酸氢根离子离子符号离子名称磷酸二氢根离子亚硫酸根离子氢氧根离子氯酸根离子高锰酸根离子锰酸根离子离子符号元素的化合价化合价原则在化合物中正价总和与负价总和为零元素在单质中化合价规定为零标出下列物质的正价总和与负价总和H2O Fe 2(SO4)3MgCl2Ca(OH)2Cu (NO3)2标出下列物质中各元素的化合价KCl MgCl2AgCl CaO MgO Al2O3Al Cl3H2S H2O MnO2 N2O2O3Fe Mg Ne Ar Cl2FeCl3FeSO4 KMnO4K2MnO4FeCl2Fe(OH)3H2SO4H2SO3NO2HNO3KClO3KClNH4 NO3NH4Cl NH4H CO3Cu SO4■5H2O CH4C2H5OH CH3COOH HCHO 标出下列化学式中各原子团的化合价(并在原子团上方划横线)NaOH AgNO3CaCO3Fe 2(SO4)3Ca(OH)2NH4Cl NH4 NO3Cu (NO3)2KMnO4K2MnO4 Cu2 (OH)2 CO3Cu SO4■5H2O NH4H CO3KAl(SO4)2■24 H2O H2SO3H3PO4Na2SiO3化学式1:单质的化学式2:化合物的化学式中考类型题1、下列物质中Cl元素化合价最高的是() A. HCl B. HClO C. HClO3 D. HClO42、x、y、z三种元素的化合价分别是+1、+6、-2价,则此三种元素组成化合物的化学式可能为()。

专题一:元素符号、化合价、离子符号、化学式复习测试(一)班级姓名分数一、写出下列元素的符号1---20号元素:氢氦锂铍硼碳氮氧氟氖钠镁铝硅磷硫氯______ 氩钾钙常见元素:锰铁银碘钡汞铅锡铜锌金铂二、写出下列物质的名称:Ca_______, Mg_______,Mn_______,I_______,Na_______,Al_______,Ag_______,Hg_______,Ba_______,Ne_______,Zn_______,He_______,三、写出元素分类及每类元素的特点:练习1:下列选项中的元素都属于非金属元素的是()A.H、S、C B.Ca、F、Cl C.O、Br、Al D.P、K、N练习2:元素中文名称大多数都是使用形声造字法,根据元素名称的汉字可判断金属元素、非金属元素。
下列各组元素属于非金属元素的一组是()A、汞、铁、铝、锕B、氪、铹、镧、碘C、溴、氟、砷、碲D、汞、溴、砹、氡四、用元素符号回答:质子数最少的元素是_______,地壳中含量最多的金属元素是_______。
水中含的元素是____ ___。
氧化物中必含的元素是_____ __,液态金属中所含的元素是_____ __。
符号中都有“C”的元素是___ ____;符号中都有“N”的元素是___ ____。
五、背出常见元素、原子团的化合价:(用符号填写)金属:_______________________________________ ________ 非金属:________________________________________常见原子团化合价:_____________________________________ _________ __________________________________________________(一定要背出!)练习1:标出下列物质中N元素的化合价,请标在N元素的正上方上:① N2;② NO;③ NO2;④ N2O5;⑤ HNO3;⑥ NH4NO3练习2:在下列物质的化学式中原子团下方用短线划出来,并填写原子团的名称及化合价:Fe(OH)3 NH4ClCaCO3 KNO3六、写出下列离子的符号氢离子氧离子氟离子钠离子镁离子铝离子硫离子氯离子钾离子钙离子铁离子亚铁离子铜离子氢氧根离子硫酸根离子硝酸根离子碳酸根离子碳酸氢根离子铵根离子七、写出下列物质的化学式☆1、单质:三原子:臭氧_________双原子:氧气氯气氢气碘溴______ 单原子:稀有气体: 氦气氩气氖气_______金属: 铜银水银锌_________铁_________其他:磷金刚石硫碳_________ 石墨_________☆2、化合物:氧化物:氧化铝水干冰氧化铜三氧化硫过氧化氢二氧化硫氧化钾氧化钙一氧化碳二氧化锰四氧化三铁五氧化二磷氯化物: 氯化铁氯化钠氯化铜氯化银氯化氢氯化镁硫化物: 硫化氢硫化钠_________ 硫化锌_________其他: 氯酸钾碳酸钙锰酸钾高锰酸钾硫酸碳酸铵氢氧化钙氢氧化钾氢氧化铝碳酸钠硫酸钾专题一:元素符号、化合价、离子符号、化学式复习测试(二)班级姓名分数一、填空题:1、元素是具有相同的___ ____(即___ ____)的一类原子的总称。
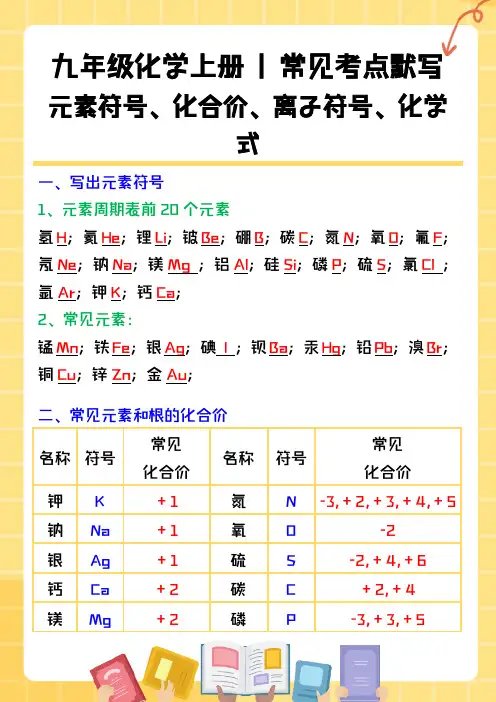
九年级化学上册 | 常见考点默写元素符号、化合价、离子符号、化学式一、写出元素符号1、元素周期表前20个元素氢H;氦He;锂Li;铍Be;硼B;碳C;氮N;氧O;氟F;氖Ne;钠Na;镁Mg;铝Al;硅Si;磷P;硫S;氯Cl;氩Ar;钾K;钙Ca;2、常见元素:锰Mn;铁Fe;银Ag;碘 I ;钡Ba;汞Hg;铅Pb;溴Br;铜Cu;锌Zn;金Au;二、常见元素和根的化合价名称符号常见化合价名称符号常见化合价钾K+1氮N-3,+2,+3,+4,+5 钠Na+1氧O-2银Ag+1硫S-2,+4,+6钙Ca+2碳C+2,+4镁Mg+2磷P-3,+3,+5铜Cu+1,+2锌Zn+2锰Mn +2,+4,+6,+7硅Si+4铝Al+3氢氧根OH--1 氢H+1硫酸根SO42--2氯Cl -1,+1,+5,+7碳酸根CO32--2铁Fe+2,+3铵根NH4++1氟F-1硝酸根NO3--1三、写出下列离子的符号氢离子H-;氧离子O2-;氟离子F-;钠离子Na+;镁离子Mg2+;铝离子Al3+;硫离子S2-;氯离子Cl-;钾离子K+;钙离子Ca2+;铁离子Fe3+;铜离子Cu2+;亚铁离子Fe2+;氢氧根离子OH-;硫酸根离子SO42-;硝酸根离子NO3-;碳酸根离子CO32-;铵根离子NH4+;碳酸氢根离子HCO3-;四、写出下列物质的化学式1、单质三原子:臭氧O3;双原子:氧气O2;氯气Cl2;氢气H2;碘I2;溴Br2;单原子:稀有气体:氦气He;氩气Ar;氖气Ne;金属:铜Cu;银Ag;水银Hg;锌Zn;铁Fe;其他:磷P;金刚石C;硫S;碳C;石墨C;2、化合物氧化物:氧化铝Al2O3;水H2O;干冰CO2;氧化铜CuO;三氧化硫SO3;过氧化氢H2O2;二氧化硫SO2;氧化钾K2O;氧化钙CaO;一氧化碳CO;二氧化锰MnO2;四氧化三铁Fe3O4;五氧化二磷P2O5;氯化物:氯化钠NaCl;氯化铜CuCl2;氯化银AgCl;氯化氢HCl ;氯化镁MgCl2;氯化铁FeCl3;硫化物:硫化氢H2S;硫化钠Na2S;硫化锌ZnS;其他:氯酸钾KClO3;硫酸钾K2SO4;碳酸钙CaCO3;锰酸钾K2MnO4;高锰酸钾KMnO4;硫酸H2SO4;氢氧化钙Ca(OH)2;氢氧化钾KOH;氢氧化铝Al(OH)3;碳酸钠Na2CO3;碳酸铵(NH4)2CO3;。

九年级上册化学期末复习专练元素符号、化合价、离子符号、化学式背写与计算➢背写部分一. 写出元素符号1.元素周期表前20个元素氢氦锂铍硼碳氮氧氟氖钠镁铝硅磷硫氯氩钾钙2.常见元素:锰铁银碘钡汞铅溴铜锌金二. 背出常见元素、原子团的化合价:(用符号填写)常见元素化合价:常见原子团化合价:(一定要靠记忆来背写)练习:1. 标出下列物质中N元素的化合价,请标在N元素的正上方①N.2; ②N.O: ③N.O2: ④N.2O5; ⑤HN.O3⑥N.H4N.O32. NaSO4中S的化合价是KMnO4中Mn的化合价为三、写出下列离子的符号氢离子氧离子氟离子钠离子镁离子铝离子硫离子氯离子钾离子钙离子铁离子铜离子亚铁离子氢氧根离子硫酸根离子硝酸根离子碳酸根离子铵根离子碳酸氢根离子四、写出下列物质的化学式1、单质三原子:臭氧双原子:氧气氯气氢气碘溴单原子:稀有气体:氦气氩气氖气金属:铜银水银锌铁其他:磷金刚石硫碳石墨2、化合物氧化物:氧化铝水干冰氧化铜三氧化硫过氧化氢二氧化硫氧化钾氧化钙一氧化碳二氧化锰四氧化三铁五氧化二磷氯化物:氯化钠氯化铜氯化银氯化氢氯化镁氯化铁硫化物:硫化氢硫化钠硫化锌其他:氯酸钾 硫酸钾 碳酸钙 锰酸钾 高锰酸钾 硫酸 氢氧化钙 氢氧化钾 氢氧化铝 碳酸钠 碳酸铵 综合练习 1、看符号写含义O 5N 3H 2 C Al mC 2、按要求写出下列符号:①氧元素 ②两个氧原子 ③氧气 ④两个氧气分子 ⑤氧离子 ⑥两个氧离子 3、写出下列符号中数字2的意义。
2H Ca 2+ 2SO 3 Cl 2 2H 2O 、2MgO C +2u SO 42-➢ 计算部分一、根据化学式计算相对分子质量或相对分子质量之和1、A12(SO 4)3的相对分子质量=2、下列各相对分子质量的计算中,正确的是( ) A 、2MgO 的相对分子质量之和=2×24+16=64 B 、NO 2的相对分子质量=14×16×2=448C、2N的相对分子质量和=2(14+2)=32D、3O2的相对分子质量和=3×(16×2)=96二、根据化学式计算化合物中各元素的质量比(最简整数比)化合物中各元素的质量比等于各元素的相对原子质量的和之比1:计算硫酸铵【(NH4)2SO4】中各元素的原子个数比及各元素的质量比解:(NH4)2SO4中N、H、S、O原子个数比为:(NH4)2SO4中各元素的质量比:2、在H2SO4中氢、硫、氧三种元素的质量比的计算式正确的是( )A、(1×2):32:(16×4)B、1:32:16C、2:1:4D、(16×4):32:(1×2)三、计算化合物中某元素的质量分数例题:计算碳酸氢铵【NH4HCO3】中氮元素的质量分数。

化学用语专题练习班级________ 姓名____________一、写出下列常见离子的离子符号 1.常见阳离子锌离子 铵根离子2.常见阴离子氯离子 氯酸根离子 硫离子 硫酸根离子 氧离子 氢氧根离子硝酸根离子 碳酸根离子 高锰酸根离子 锰酸根离子二、常见单质化学式氢气氖气镁三、常见化合物化学式 水五氧化二磷氧化铁氯化钾氢氧化钠硫酸钠四、根据下列要求,用元素符号或化学式填空1.空气中含量最多的元素是 ,含量最多的物质是。
2.地壳中含量最多的非金属,金属元素分别是和两种元素组成化的合物是 。
3.相对分子质量最小的物质是 氧化物是 。
4.能支持燃烧气体是 ,能灭火的气体是 。
5.能形成硫酸型酸雨的气体是 SO 2,造成温室效应的主要气体是 。
6.保持水的化学性质的粒子是 。
五、下列化学反应,写出符号表达式1 .过氢化氢分解制氧气:2 .加热高锰酸钾制氧气:3.加热氯酸钾制氧气 4 .电解水: 5. CO 2 与澄清石灰水反应: 6 .铁在氧气中燃烧:7 .镁的燃烧: 8 .磷的燃烧: 六、写出化学符号 1. 2 个氢原子2 个氢离子2 个氢分子2. 2 个氮分子 2 个氨分子 2 个铵根离子 3. 2 个氯离子 2 个氯酸根离子 2 个氯分子4. 2 个钾离子2 个锰酸根离子2 个高锰酸根离子5. 2 个铁离子 2 个亚铁离子七、指出下列符号数字“2”的意义1. 2H2. Mg 2+3. 中②的 2H 2+2M gO的 2过氧化氢氧化镁四氧化三铁氯酸钾氢氧化钙高锰酸钾一氧化碳氧化铜二氧化锰氯化钠氢氧化铜锰酸钾 三氧化硫氧化汞氨气氯化亚铁硫酸铜碳酸二氧化碳氧化钙氧化亚铁氯化钙碳酸钠盐酸 二氧化硫氧化铝甲烷氯化镁碳酸钙硫酸 氮气金刚石铁 镁离子亚铁离子 碘硫粉锌 氧气氩气铝 氯气木炭铜 氦气红磷银钡离子铁离子钠离子钙离子 氢离子 铜离子 钾离子铝离子化学用语专题练习班级________ 姓名 一、写出下列常见离子的离子符号1.常见阳离子 氢离子 Mg 2+ 铵根离子 NH 4+ 2.常见阴离子氢氧根离子OH-3 高锰酸根离子MnO 2 4二、常见单质化学式氮气 Cl 2 金刚石 C 铁 Fe一氧化碳 CO 氧化铜 CuO 二氧化锰 MnO 2 氯化钠 NaCl 氢氧化铜 Cu(OH) 2 锰酸钾 K 2MnO 4四、根据下列要求,用元素符号或化学式填空1.空气中含量最多的元素是 _____N______ ,含量最多的物质是 ____N 2_____。
化合价一、常见元素化合价溶解性表:化合价例题分析:一、根据化学式求元素化合价例1:新型净化剂铁酸钠(N aF e O 24)中铁元素的化合价是( ) A .+2B .+3C .+5D .+6二、由元素在化合物中的质量分数求元素的化合价例2:某金属元素在其氧化物中所占的质量分数为80%,该金属的相对原子质量为64,则该金属元素在其氧化物中的化合价为( ) A .+4B .+3C .+2D .+1三、由元素质量比求元素的化合价例3:硫的某种氧化物中,硫元素与氧元素的质量比为2:3,则该氧化物中硫元素的化合价为( )。
A .+6B .+2C .-2D .+4四、根据化合价确定化学式中某原子或原子团的个数例4:某些乡村用明矾[()]K A l S O H O x 4212⋅来净水,根据元素化合价判断x 为( )。
A .1B .2C .3D .4五、由两种不同物质的相对分子质量求元素的化合价例5:某金属R 氧化物的相对分子质量为M ,对应氯化物的相对分子质量为N ,该金属元素化合价为( )。
A .()/255N M - B .255()/N M - C .()/255MN -D .255()/MN -化学式与化合价练习题1.X 、Y 、Z 三种元素的化合价分别为+1,+4,-2,则这三种元素所组成的化合物的化学式可能为( )A .XYZB .X 4YZ 3C .X 2YZ 3D .X 3YZ 22.下列离子符号书写正确的是 ( ) A.Na 1+ B.OH -1 C.Al 3+ D.SO 42-3.下面是对“2”的含义的解释,其中错误的是( )A.Fe 2+:一个亚铁离子带2个单位正电荷B.Ba(OH)2:氢氧化钡中,钡离子和氢氧根离子的个数比是1:2C.Mg 2+:带2个单位正电荷的镁离子D.2 SO 42-:2个硫酸根离子,每个硫酸根离子带2个单位负电荷4.下列化学式书写正确的是 ( ) A. MgO 2 B. K 2Cl C. ZnCl 3 D. Ca(NO 3)2 5.下列物质中硫元素化合价最低的是( ) A. S B. SO 2 C. H 2SO 4 D. H 2S 6.下列关于化合价的说法正确的是( )A.化合物中,氧元素一定显-2价B.化合物中,非金属元素一定显负价C.氢气中氢元素的化合价为+1价D.化合物中正负化合价的代数和一定为零 7.下列物质的化学式,书写错误的是( )A .氯化亚铁FeCl 2B .氢氧化钠NaOHC .氧化镁MgOD .碳酸钠NaCO 38.有H 、O 、S 、K 四种元素,按指定化合价( H +1、O -2、S -2、K +1)组合,最多可以组成由两种元素组成的化合物的种数是 A .4种 B .5种 C .6种 D .7种9.工业用盐亚硝酸钠(NaNO 2)误作食盐,会使人中毒死亡。
知识点讲解元素€称元盍符号 常见的化合价元盍€称元盍苻号常见的化合价钾-1硅S1 -4NaT碳 C T银Ag-1氮X -3i-4JCaP-J J —?s —5镁近E 磯根SOF ■ —Be碳讓根 co :-~ J 锌Zn硝犠根yo :' 4Cu-L -2氢氧化S OH--1 铁 Ft -乙-Jj谖根-1铝A :-3隣酸根-3猛—2i » —fli-7msCIO' -1 aK -1碳K 氢棍 ncor -1 氯F -1亚硫K 根 SOF ■ ■>Cl■1J —1, -SF猛釀根MaOJ- _ ■> —r S□ ■>高猛讓根 Mn02 - -1 磴s-2J —J —6硫酸S 根HSCL —-1金属元素与非金属元素化合时, 金属元素易失去电子故显正价,非金属元素易得到电子故显负价;元素的化合价是元素的原子在相互形成化合物时表现出来的一种性质,因此,在单质分子里,元素的化合价 为零一些元素在不同化合物中可显不同的化合价化合物中,各元素的化合价代数和为 0 5、利用化合价写化学式:姓名: 时间:讲授内容:化合价教育科目1、练习巩固一、选择题1. 下列含硫物质中,硫元素的化合价为+ 4价的是(A . SB . H 2SC . H 2SO 3D . H 2SO 42. 下列有关化合价的说法中,正确的是( )A .在NaCI 和HCI 里,氯元素均为-1价 C . 一种元素在同一种化合物里,化合价一定相同 3. 下列四种物质①KCI0 3②CI 2③HCI ④HCIO ,氯元素的化合价按由低到高顺序排列的是()A .①②④③B .②③④①C .③②①④ 4. 下列各组物质中,硫元素具有相同化合价的是( )A . Na 2SO 3 和 S03B . SO 2 和 SO 3C . SO 2 和 H 2SO 3M0,如果在其氯化物中金属的化合价与该氧化物中的化合价相等,则 )M 2CI D . M 2CI 3 )A .高锰酸钾(K 2MnO 4)B .氧化镁(MgO 2)C .氯化钾(KCIO 3)D .氯化亚铁(FeCb )7.某化合物化学式为HnMO 2n 已知在该化合物中M 的化合价为+6,则n 值为()A . 1B . 2C . 3D . 68下列物质中氮元素的化合价由低到高的顺序排列一组是( )A . N 2O 3、NH 3、NO 、N 2B . NH 3 N 2 NO N 2O 3C . NH 3、NO 、N 2、N 2O 3D . NO N 2 N 2O 3 NH 39 . X 、丫、Z 三种元素的化合价分别为+1,+4, -2,这三种元素所组成的化合物的化学式可能为 ()A . XYZB . X 4YZ 3C . X 2YZ 3D . X 3YZ 210 .某元素R 的氧化物分子中,R 与O 的原子个数比为2 : 3,则R 的化合价是()A . +2 价B . +3 价C . -2 价D . -3 价 11 .下列物质的化学式,书写错误的是( )A .氯化亚铁FeCI 3B .氢氧化钠NaOHC .氧化镁MgOD .碳酸钠NaCO 312 .某元素氧化物的化学式为 M 2O 3(M 化合价没有变化),则下列化学式中错误的是( )A . MCI 3B . MSO 4C . M 2(SO 4)3D . M (OH )313 .下列说法正确的是()A .元素的化合价数值等于一个原子得失电子的数目 C .铁的化合价为零D .单质铜中铜元素化合价为零,化合物中铜元素化合价为 14 .下列化学式中正确的是( )A . Zn CI 3B . Ca (NO 3)2C . K 2OHD . AICI 215 .某金属元素M 的氯化物的化学式为MCI 3,其氧化物的化学式为()A . MO 2B . M 2OC . MOD . M 2O 316 .某元素的相对原子质量为27,化合价为+3,则其氧化物中含氧的质量分数为( )A . 47 . 1%B . 26 . 5%C . 77 . 1%D . 72%17.下列各个化学变化前后,同种元素的化合价数值变化最大的是( )A . C —CO 2B . KCIO 3— KCIC . KMn O L aMnO 4D . 18 .下列各组物质中氮元素的化合价由低到高的排列顺序是( )A . N 2、NH 3、NO 2B . NH 3、N 2O 5、NO 2C . N 2、N 2O 3、NH 3 19 .酒后驾车是一种非常严重的交通违章行为, 交警常用“司机饮酒检测仪” B .在H2中,氢元素显+1价D .非金属元素在化合物里,一定显负价 D .③②④①5.某金属氧化物的组成为 该金属氯化物的组成为(A . MCIB . MCI 2C . 6 .下列化学式正确的是(B .水中氢气的化合价为零 +1或+2价 NH 3T NHUCI D . NH 3、N 2、N 2O 3检查司机呼出的气体,以判断他是否饮过酒。
答案元素符号原子团及化学式的书写及练习Final revision on November 26, 2020+2Mg_表示镁元素的化合价是正2价+2MgO表示氧化镁中镁元素的化合价是正2价元素符号、原子团及化学式的书写及练习(参考答案)班级_______姓名_______________一、写出各元素的元素符号或名称及部分常见原子团离子的符号。
常见元素化合价口诀:_______(答案略)______________、_________________________________________________________、________________________________________________________、___________________________________________________________、_____________________________常见原子团化合价口诀:________(答案略)________、___________________________________________________________、_____________________________三、理解各种符号或数字的意义:1、写出下列各种符号所表示的意义:“Cu”表示①表示铜元素②表示一个铜原子(表示铜这种物质)“H2O”表示①表示水这种物质②表示水是由氢元素和氧元素组成的③表示一个水分子④表示一个水分子由二个氢原子和一个氧原子构成的。
“5H”表示①表示5个氢原子“2CO2”表示①表示2个二氧化碳分子2、写出下列各种符号或指出符号中的“2”的意义:三个铁原子3Fe五个五氧化二磷分子5P2O5液态氮N2铝离子Al3+氯离子Cl-二个铵根离子2NH4+2Mg_表示2个镁原子Mg2+_表示一个镁离子带2个单位的正电荷SO2_表示一个二氧化硫分子中含有2个氧原子四、熟练书写化学式:(写出下列各种物质的化学式)1、单质:氢气H2氯气Cl2氮气N2氦气He氖气Ne氩气Ar铜Cu锰Mn镁Mg金刚石C固态磷P硫磺S臭氧气体O3 2、化合物:氧化物:一氧化碳CO水H2O二氧化硫SO2氧化镁MgO氧化铁Fe2O3氧化亚铁FeO 氧化铜CuO 氧化铝Al 2O 3氧化锌ZnO 氧化亚铜Cu 2O硫化物:(硫元素显示-2价)硫化镁MgS 硫化锌ZnS 硫化铁Fe 2S 3硫化亚铁FeS 硫化钠Na 2S 氯化物(又称盐酸盐)氯元素显示-1价氯化镁MgCl 2氯化锌ZnCl 2氯化铁FeCl 3氯化亚铁FeCl 2 氯化钠NaCl 氯化铜CuCl 2氯化铵NH 4Cl 氯化氢(盐酸)HCl 氢氧化物(含OH )氢氧化镁Mg(OH)2氢氧化锌Zn(OH)2氢氧化铁Fe(OH)3氢氧化铝Al(OH)3氢氧化钠Na OH 氢氧化铜Cu(OH)2氢氧化钾K OH 氢氧化钡Ba(OH)2硝酸盐(含硝酸根NO 3)硝酸镁Mg(NO 3)2硝酸锌Zn(NO 3)2硝酸铁Fe(NO 3)3硝酸钾K NO 3硝酸钠Na NO 3硝酸铜Cu(NO 3)2硝酸铵NH 4NO 3硝酸银Ag NO 3硝酸钙Ca(NO 3)2硝酸铝Al(NO 3)3硝酸钡Ba(NO 3)2硝酸亚铁Fe(NO 3)2硫酸盐(含SO 4)硫酸镁MgSO 4硫酸锌ZnSO 4硫酸铜CuSO 4硫酸铁Fe 2(SO 4)3 硫酸钠Na 2SO 4硫酸钾K 2SO 4硫酸铵(NH 4)2SO 4硫酸钡BaSO 4 碳酸盐或碳酸氢盐(含CO 3或HCO 3)碳酸镁MgCO 3碳酸锌ZnCO 3碳酸钙CaCO 3碳酸钡BaCO 3碳酸钠Na 2CO 3碳酸钾K 2CO 3碳酸氢钠NaHCO 3碳酸氢铵NH 4HCO 3 酸类(H +与某些阴离子结合而成的化合物)盐酸(氯化氢)HCl 氢硫酸(硫化氢)H 2S 氢氟酸(氟化氢)HF 硫酸H 2SO 4硝酸HNO 3碳酸H 2CO 3亚硫酸H 2SO 3磷酸H 3PO 4 五、其它练习1、写出下列物质化学式中,加点元素的化合价( 已知氧的化合价-2,氢+1)-1-2+5+4+(n+4)00HF .H 2SP ..2O 5H 2C .O 3H n R .O n+2 H 2 Cu2、A 原子和B 原子在形成化合物时,每个A 原子得到2个电子,形成A 离子,每个B 原子失去3个电子,成为B 离子。
元素符号、化学式、离子符号、化合价【练习】一、元素符号练习钾()钠()镁()铝()锌()铁()铜()汞()银()钡()锰()锂()铍()(以上元素都属于元素)碳()硅()磷()硼()氢()氧()氮()氟()氯()溴()碘()(以上元素都属于元素)氦()氖()氩()(以上元素都属于元素)1、2、请写出下列常见原子团并标出化合价:铵根:氢氧根:硫酸根:碳酸根:3、请写出下列离子的符号氢离子氧离子氟离子钠离子镁离子铝离子硫离子氯离子钾离子钙离子铁离子亚铁离子铜离子铵根离子1、单质:氦气氖气氩气金刚石或石墨硫磷氢气氮气氧气氯气溴碘臭氧2、化合物①非金属氧化物一氧化氮一氧化二氮水二氧化碳二氧化氮二氧化硫二氧化硅三氧化硫五氧化二氮五氧化二磷②金属氧化物书写化学式时(要根据化合价)氧化钠氧化钾(以上氧化物中的金属都是价)氧化钙氧化镁氧化钡氧化锌氧化铜氧化亚铁(以上氧化中的金属都是价)氧化铁氧化铝(以上氧化物中的金属都是价)二氧化锰③氯化物(注意化合价)氯化钾氯化钠氯化银氯化氢氯化钙氯化镁氯化钡氯化锌氯化铜氯化亚铁氯化铝氯化铁氯化铵④硫化物硫化氢硫化钠硫化钾硫化铜⑤含有原子团硫酸根的化合物硫酸硫酸钠硫酸镁硫酸钡硫酸锌硫酸铜硫酸亚铁硫酸铝硫酸铁硫酸铵⑥含有原子团硝酸根的化合物硝酸钾硝酸钠硝酸银硝酸铜硝酸铵硝酸钙硝酸钡硝酸铁硝酸铝硝酸⑦含有原子团碳酸根的化合物碳酸钠碳酸钾碳酸铵碳酸钙碳酸⑧含有原子团氢氧根的化合物氢氧化钾氢氧化钠氢氧化钙氢氧化铁⑨含有原子团碳酸氢根的化合物碳酸氢钠碳酸氢钙碳酸氢铵补充:干冰四氯化碳盐酸氯酸钾高锰酸钾锰酸钾练习1、练习:写出下列符号中数字的2意义。
Cl2 2HCa2+ 2SO32H2O +2CuSO42- 2MgO2、标出下列物质中S、Cl、N元素的化合价:①S;② SO2;③ SO3;④Na2SO4①Cl2;② HCl;③HClO;④HClO3 ⑤HClO4①N2;② NO;③ NO2;④ N2O5;⑤ HNO3;⑥ NH4NO33、说出下列符号中2的含义:(1)2O (2)O2—(3)O2 (4)2O2、(5)2O2—、(6)4、使CO2和C质量的氧元素,则CO2和CO的质量比是;若CO2和CO的质量相等,则CO2和CO中的碳元素质量比为。
初三化学(上)(元素符号.化合价.离子符号.化学式温习)姓名一.写出下列元素的符号氢氦锂铍硼碳氮氧氟氖钠镁铝硅磷硫氯______ 氩钾钙罕有元素:锰铁银碘钡汞铅溴铜锌金二.背出罕有元素.原子团的化合价:(用符号填写)_________________________;________________________________________________;________________________________________________;_________________________________________________;________________________罕有原子团化合价:_______________________________________________(必定要背出!)演习:标出下列物资中N元素的化合价,请标在N元素的正上方上:①N2; ②N O;③NO2;④N2O5;⑤ H NO3;⑥NH4NO32.NaHSO4中S的化合价是 , KMnO4中Mn的化合价为 .三.写出下列离子的符号氢离子氧离子氟离子钠离子镁离子铝离子硫离子氯离子钾离子钙离子铁离子亚铁离子铜离子氢氧根离子硫酸根离子硝酸根离子碳酸根离子碳酸氢根离子铵根离子四.写出下列物资的化学式☆1.单质三原子:臭氧_________双原子:氧气氯气氢气碘溴__________单原子:罕见气体: 氦气氩气氖气_______金属: 铜银水银锌_________铁_________其他:磷金刚石硫碳_________ 石墨___________☆2.化合物氧化物:氧化铝水干冰氧化铜三氧化硫过氧化氢二氧化硫氧化钾氧化钙一氧化碳二氧化锰四氧化三铁五氧化二磷氯化物:氯化钠氯化铜氯化银氯化氢氯化镁氯化铁硫酸钾硫化物:硫化氢硫化钠_________ 硫化锌_________其他:氯酸钾碳酸钙锰酸钾高锰酸钾硫酸氢氧化钙氢氧化钾氢氧化铝碳酸钠碳酸铵☆分解演习:1.看符号写寄义:O_________________5N__________________C__________________ mC_______________ Al____________________2.按请求写出下列符号:①氧元素②两个氧原子③氧气④两个氧气分子⑤氧离子⑥两个氧离子3.写出下列符号中数字2的意义.Cl2 2HCa2+2SO32H2O . MgO+2Cu SO42-☆一.依据化学式盘算相对分子质量或相对分子质量之和1.Al2(SO4)3的相对分子质量=_______________________________________2.下列各相对分子质量的盘算中,准确的是 ( )A.2MgO的相对分子质量之和=2×24+16=64B.NO2的相对分子质量=14×16×2=448C.2N2的相对分子质量和=2(14+2)=32D.3O2的相对分子质量和=3×(16×2)=96☆二.依据化学式盘算化合物中各元素的质量比(最简整数比)化合物中各元素的质量比等于各元素的相对原子质量的和之比1:盘算硫酸铵【(NH4)2SO4】中各元素的原子个数等到各元素的质量比解:(NH4)2SO4中N.H.S.O原子个数比为:(NH4)2SO4中各元素的质量比__________________________________2.在H2SO4中氢.硫.氧三种元素的质量比的盘算式准确的是( )A. (1×2):32:(16×4)B.1:32:16C.2:1:4D.(16×4):32:(1×2)☆三.盘算化合物中某元素的质量分数例题:盘算碳酸氢铵【NH4HCO3】中氮元素的质量分数:N解: NH4HCO3中氮元素的质量分数 N%=的子分子质量×100%= 14×100%=17.7%NH4HCO3 791:盘算尿素【CO(NH2)2】中氮元素的质量分数.☆四.化合物与元素之间的质量换算元素的质量=化合物资量×化合物中元素的质量分数1.盘算200Kg尿素【CO(NH2)2】中含氮元素若干Kg?有关化学式的根本盘算类型:以NH4NO3 为例请盘算(写出具体步调)(1)NH4NO3的相对分子质量M= ;(2)先盘算 N.H.O原子个数比为(3)NH4NO3各元素的质量比m N:m H:m O= ;(4)NH4NO3中N元素的质量分数为N%= ;(5)40克NH4NO3含N元素的质量为m N= .3.填补:若干克NH4NO3中含N元素的质量为70克?5.某临盆碳酸氢铵(NH4HCO3)的化肥厂,为谋取好处,打出“本厂临盆的优质碳酸氢铵,属国际开创,含氮量全球最高,达到20.1%”的告白.试经由过程盘算解释该告白的荒诞之处.。
元素符号、化学式、离子符号、化合价【练习】
一、元素符号练习
钾()钙()钠()镁()铝()锌()铁()铜()汞()银()钡()锰()锂()铍()(以上元素都属于元素)
碳()硅()硫()磷()硼()氢()氧()氮()
氟()氯()溴()碘()(以上元素都属于元素)
氦()氖()氩()(以上元素都属于元素)
1、
2、请写出下列常见原子团并标出化合价:
铵根:氢氧根:
硫酸根:碳酸根:
3、请写出下列离子的符号
氢离子氧离子氟离子钠离子镁离子铝离子硫离子氯离子
钾离子钙离子铁离子亚铁离子铜离子铵根离子
1、单质:氦气氖气氩气金刚石或石墨硫磷
氢气氮气氧气氯气溴碘臭氧
2、化合物
①非金属氧化物:一氧化碳一氧化氮一氧化二氮水二氧化碳
二氧化氮二氧化硫二氧化硅三氧化硫五氧化二氮五氧化二磷
②金属氧化物书写化学式时(要根据化合价)
氧化钠氧化钾(以上氧化物中的金属都是价)
氧化钙氧化镁氧化钡氧化锌氧化铜
氧化亚铁(以上氧化中的金属都是价)
氧化铁氧化铝(以上氧化物中的金属都是价)
二氧化锰
③氯化物(注意化合价)
氯化钾氯化钠氯化银氯化氢氯化钙
氯化镁氯化钡氯化锌氯化铜
氯化亚铁氯化铝氯化铁氯化铵
④硫化物
硫化氢硫化钠硫化钾硫化铜
⑤含有原子团硫酸根的化合物
硫酸硫酸钾硫酸钠硫酸镁硫酸钡硫酸锌硫酸铜
硫酸亚铁硫酸铝硫酸铁硫酸铵
⑥含有原子团硝酸根的化合物
硝酸钾硝酸钠硝酸银硝酸铜硝酸铵
硝酸钙硝酸钡硝酸铁硝酸铝硝酸
⑦含有原子团碳酸根的化合物
碳酸钠碳酸钾碳酸铵碳酸钙碳酸
⑧含有原子团氢氧根的化合物
氢氧化钾氢氧化钠氢氧化钙氢氧化铁
⑨含有原子团碳酸氢根的化合物
碳酸氢钠碳酸氢钙碳酸氢铵
补充:干冰四氯化碳盐酸氯酸钾高锰酸钾锰酸钾
练习
1、练习:写出下列符号中数字的2意义。
Cl2 2H
Ca2+ 2SO3
2H2O +2
Cu
SO42- 2MgO
2、标出下列物质中S、Cl、N元素的化合价:
①S;② SO2;③ SO3;④Na2SO4
①Cl2;② HCl;③HClO;④HClO3 ⑤HClO4
①N2;② NO;③ NO2;④ N2O5;⑤ HNO3;⑥ NH4NO3
3、说出下列符号中2的含义:
(1)2O (2)O2—
(3)O2 (4)2O2、
(5)2O2—、
(6)
4、使CO2和CO中含有相同质量的氧元素,则CO2和CO的质量比是;若CO2和CO的质量相等,则CO2和CO中的碳元素质量比为。
5、在一种M的氧化物中,M与氧元素的质量比为7:20,已知M与氧的相对原子质量比为7:8,则氧化物中M元素的化合价为。
6、某物质化学式为H n RO2n-1,相对分子质量为M,则R的化合价为,R的相对原子质量为。
7、元素R有多种氧化物,其中RO中含氧53.33%,那么相对分子质量为76,含氧为63.15%的R的氧化物的化学式是。
8、有12克赤铁矿的样品,经化验测定其中含Fe5.88克,则此赤铁矿中含Fe2O3的质量分数为。
1 元素周期表(默写)
2
3
4
【例】化合物AxBy,A的相对原子质量为a,B的相对原子质量为b。
1、相对分子质量=ax+by;
2、分子中各原子的个数比=x:y;
3、组成物质的各元素的质量比=ax:by
4、物质中某一元素的质量分数;
5、有关混合物中元素质量或元素质量分数
纯度:即混合物中某物质的质量分数
混合物中元素的质量分数=纯度×该元素的质量分数。