
4 水合
H
2
C C
H OH
a. 常用催化剂:H2SO4、H3PO4
b. 符合马氏加成
c. 机理亲电加成
CH3C
CH3
H3
C
CH3
CH32CH
3
C
CH3
2
CH3
-H
CH3C
CH3
OH
CH3
d. 有重排现象
CH3C
CH3
CH
CH3
CH2+H2O
H2SO4
CH3C
OH
CH3
CHCH3
CH3
5 加醇
CH3OH
H SO,H O
(CH3)2C CH2CH3
OCH3
符合马氏加成
+
(CH3)2C CHCH3
6 硼氢化-氧化反应
硼氢化-氧化反应(hydroboration)是美国化学家布郎(H. C. Brown)发展的一类重要反应,在有机合成中有广泛的用途,其中之一就是烯烃间接水合。在1979年获诺贝尔奖。
R CH CH2B2H6
1
2
+(RCH2CH2)3B硼氢化反应
22
OH
(RCH2CH2)3B RCH2CH2OH氧化反应
最终相当于双键上加了一分子水。
①硼烷试剂:
甲硼烷:BH3 BH3·THF或BH3·diglyme 乙硼烷:B2H6
②反应过程:
R CH CH2BH3
+RCH2CH2BH2
RCH2CH2BCH2CH2R
H
R CH CH2+RCH2CH2BH2
R CH CH2+RCH2CH2BCH2CH2R RCH2CH2B(CH2CH2R)2
④顺式加成
B2H6
1
+C C
H2B H
+δ
δ
π络合物
C
H2B
H
四元环过渡态
H2B H
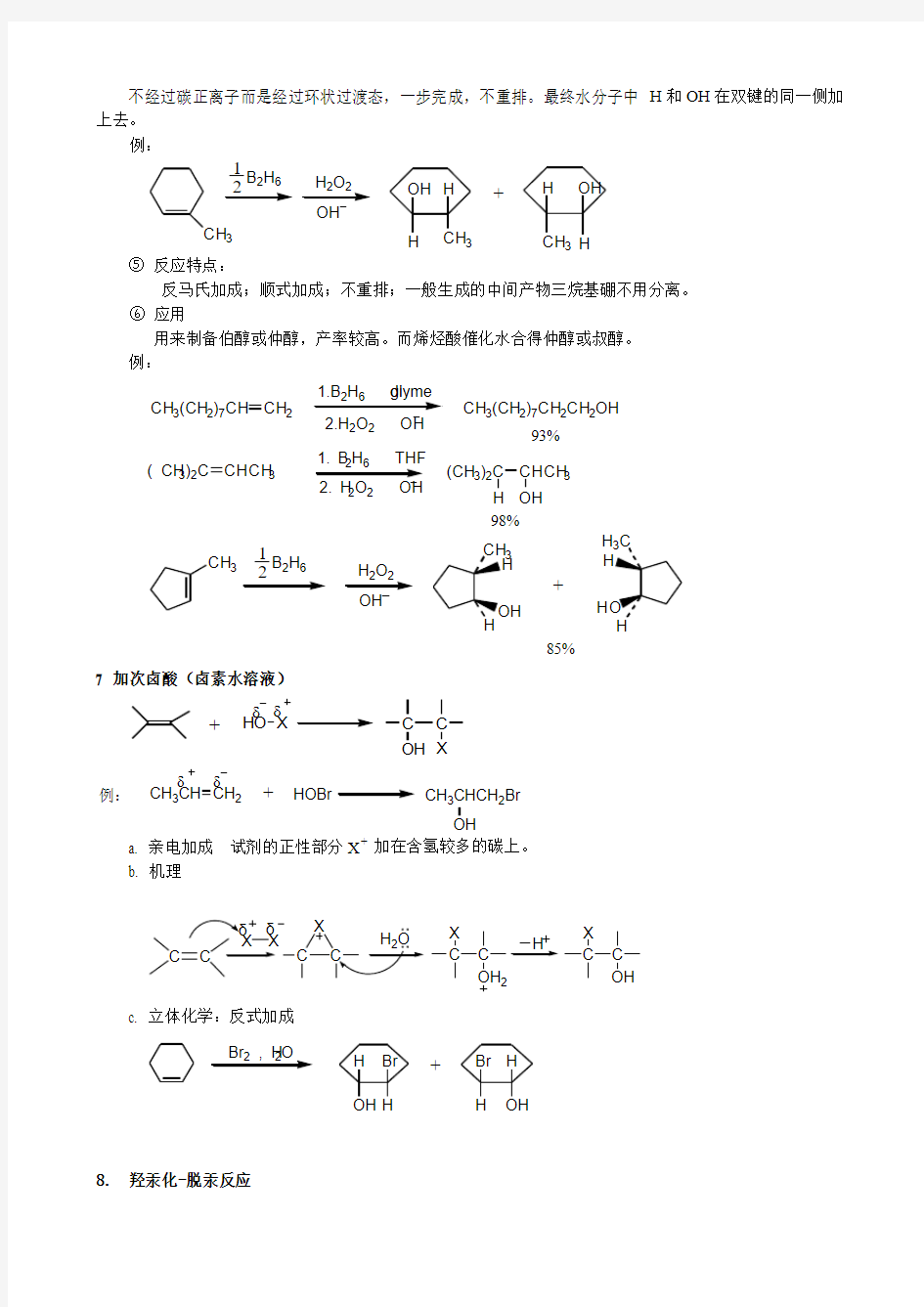
不经过碳正离子而是经过环状过渡态,一步完成,不重排。最终水分子中H和OH在双键的同一侧加上去。
例:
CH3
B2H6
1
222
OH
CH3
OH H
H H
H OH
CH3
+
⑤反应特点:
反马氏加成;顺式加成;不重排;一般生成的中间产物三烷基硼不用分离。
⑥应用
用来制备伯醇或仲醇,产率较高。而烯烃酸催化水合得仲醇或叔醇。
例:
CH3(CH2)7CH CH2
26
2.H2O2 OH
CH3(CH2)7CH2CH2OH
93% ( CH3)2C CHCH326
22
OH
(CH3)2C CHCH3
H OH
98%
CH3B2H6
1
222
OH
3
+
85%
7 加次卤酸(卤素水溶液)
+C C
OH X
HO X
δ
δ
CH3CH CH2HOBr
+CH
3
CHCH2Br
OH
δ
δ
例:
a. 亲电加成试剂的正性部分X+加在含氢较多的碳上。
b. 机理
C C C
OH2
X
H
C C
OH
X
c. 立体化学:反式加成
Br2 , H2O
H
OH
Br
H
+Br
H
H
OH
8. 羟汞化-脱汞反应
脱汞反应的机理尚不清楚。一般认为羟汞化反应机理如下:
NaBH 4
H 2Hg(OAc)2+
+
C
C
OH HgOAc
C
C
OH H
a. 高度专一性。
b. 区域选择性--马氏规则—OH 加在双键位阻大的一端(H 少的一端)。
c. 反式加成产物。 书90页,选讲 9.加氢反应
10.α-H 的活性反应
为什么α-H 易发生取代反应?
①. σ-π超共轭效应,σ键电子离域到π轨道中,使α
-C 上H 的活性增大。
②. 由键裂解能看:
CH 3
CH CH 2
CH 2
CH CH 2
CH 3C CH 2
CH
3
CH CH 烯丙基自由基乙烯型自由基
键裂解能
360KJ/mol
435KJ/mol
稳定性:烯丙基自由基>乙烯型自由基
烯丙基自由基>叔自由基>仲自由基>伯自由基>乙烯型自由基
α-H 溴代试剂:N-溴代丁二酰亚胺,简称NBS
NBS 4
Br
例:CH 3
CH CH 2
4
CH 2CH CH 2
Br
Cl C H 3CH=CH 2+CH 2CH=CH 2Cl
C H 3CH-CH 2
Cl Cl
自由基稳定性:烯丙基氢> 三级氢> 二级氢> 一级氢> 甲烷
11. 氧化反应
烯烃很容易发生氧化反应,随氧化剂和反应条件的不同,氧化产物也不同。氧化反应发生时,首先是碳碳双键中的π键打开;当反应条件强烈时,σ键也可断裂。这些氧化反应在合成和定烯烃分子结构中是很有价值的。
(1)、被高锰酸钾氧化
用碱性冷高锰酸钾稀溶液作氧化剂,反应结果使双键碳原子上各引入一个羟基,生成邻二醇。
CH2=CH2+ KMnO4+ H2O
CH2(OH)CH2(OH) + MnO2+ KOH
立体化学:顺式加成
C
稀、冷KMnO4
C C
O O
Mn
O O
K2C C
1. 稀、冷KMnO4
2. H3 O
H
OH
H
OH
若用酸性高锰酸钾溶液氧化烯烃,则反应迅速发生,此时,不仅π键打开,σ键也可断裂。双键断裂时,由于双键碳原子连接的烃基不同,氧化产物也不同,此反应可用于推断烯烃的结构。
烯烃被热的、浓的高锰酸钾溶液氧化,生成低级的酮或羧酸,端烯生成CO2和H2O。
CH2CO2+H2O
RCH
R C O H
O
R
R
R
C O
C CHCH3
H3C
H3C
1. 热、浓KMnO H3C
C
H3
O+CH3C O H
O
应用:用于合成,也可用于推测结构。
CH3(CH2)10CH CH2CH3(CH2)10C
O
OH
1-十三碳烯月桂酸
84%练习:
CH2=CH2 + KMnO4+ H2SO4------ 2CO2+ MnO2
CH3CH=CH2+ KMnO4+ H2SO4------ CH3COOH + CO2
碱性
CH 3CH=CHCH 3 + KMnO 4 + H 2SO 4 ------ 2CH 3COOH
CH 3C(CH 3)=CHCH 3 + KMnO 4 + H 2SO 4 ------ CH 3COOH +CH 3COCH 3 (2)、臭氧化
CH 3CH 2CH
CH 2
32CH 3CH 2CHO
O CH 2
+① 反应过程
烯烃臭氧化反应分两步:第一步与臭氧加成生成分子臭氧化物,第二步重排成臭氧化物,然后还原水
解成醛酮。臭氧化物不稳定易发生爆炸,因此一般不分离直接水解。
R
CH C
R'R'
3
R
C H
R'
R'O O
分子臭氧化物
重排
O O C O
R H
R'R'
臭氧化物
H 2O
O O C O
R H
R'R'
+C O R
H
C O R'R'
+H 2O 2
+
② 应用
a. 从烯烃制备醛、酮。CH 3CH C(CH 3)2
32CH 3C H
O H 3C C CH 3
O
+
b. 由产物推测烯的结构
CH 3CH 2CH
CH 2
32CH 3CH 2CHO +O CH 2
CH 3CH CHCH 332CH 3CHO +CH 3CHO
CH 3
C CH 2
CH 332C O
CH 3CH 3
+O CH 2
规律:双键碳上有两个氢为甲醛。
双键碳上有一个氢为醛。 双键碳上无氢为酮。
练习推结构:烯烃经臭氧化还原水解后得下列产物,推测原来烯的结构。
CH 3CH 2CHO CH 3CH 2CH
CHCH 2CH 3C O
CH 3CH 3
+
CH 3CHO
CH 3
CHCH 3
CH 3CH 3C(CH 2)4CCH 3
O
O
CH 3
H 3C
臭氧化物在游离状态下很不稳定,容易发生爆炸。在一般情况下,不必从反应溶液中分离出来,可直接加水进行水解,产物为醛或酮,或者为醛酮混合物,另外还有过氧化氢生成。为了避免生成的醛被过氧
化氢继续氧化为羧酸,臭氧化物水解时需在还原剂存在的条件下进行,常用的还原剂为锌粉。不同的烯烃经臭氧化后再在还原剂存在下进行水解,可以得到不同的醛或酮。
(3)、环氧化
烯烃被过氧酸氧化生成环氧乙烷及同系物。
RC
O
OOH
+RC
O
OH
+
H , H2O
O
H
H OH
OH
H
常用的过酸:过氧乙酸、过氧三氟乙酸、过氧苯甲酸、间氯过氧苯甲酸(MCPBA:Mete Chloro Perbenzoic Acid)
CH2CH2
RC
O
OOH
CH2CH2
O
环氧乙烷是生产涤纶的重要原料,工业制备方法:
CH22
O
2
CH2CH2
12. 溴化氢的自由基加成反应及机理
烯烃与溴化氢加成,条件不同得到的产物不同。
CH2CHCH2CH3
HBr
CH3CHCH2CH3
Br
90%
符合马氏加成
BrCH2CH2CH2CH3
95%
反马氏加成
过氧化物效应:由于过氧化物存在,使反应速度加快,生成反马氏加成产物。
CH3CH CH2+HBr ROOR CH3CH2CH2Br
机理:
ROOR2RO
RO+HBr ROH+Br
CH3CH CH2
Br+CH3CHCH2
Br
+CH3CHCH2Br
(主)
CH3CHCH2Br+HBr CH3CH2CH2Br+Br
……
注意:只有HBr有过氧化物效应。HCl,HI没有过氧化物效应。因为HCl中H-Cl键牢固,其中H 不能被自由基夺取而产生氯自由基,所以不能引发自由基反应。H-I键虽弱,容易生成碘自由基,但碘自由基活性较低,很难与碳碳双键加成,不能进行链传递反应。
+HBr CH
2
Br
ROOR
例:
13.邻位效应(选讲)
次序规则是各种取代基按照优先顺序排列的规则
(1)原子:原子序数大的排在前面,同位素质量数大的优先。几种常见原子的优先次序为:I> Br>Cl>S>P>O>N>C>H
(2)饱和基团:如果第一个原子序数相同,则比较第二个原子的原子序数,依次类推。常见的烃基优先次序为:(CH3)3C->(CH3)2CH->CH3CH2->CH3-
(3)不饱和基团:可看作是与两个或三个相同的原子相连。不饱和烃基的优先次序为:
-C CH>-CH=CH2>(CH3)2CH-
次序规则主要应用于烷烃的系统命名和烯烃中几何异构体的命名
烷烃的系统命名:如果在主链上连有几个不同的取代基,则取代基按照“次序规则”一次列出,优先集团后列出。
按照次序规则,烷基的优先次序为:叔丁基>异丁基>异丙基>丁基>丙基>乙基>甲基烯烃中几何异构体的命名:比较双键两端每个碳原子上所连接的两个基团的优先次序,次序较优的两个基团在双键同侧的定义为Z构型,即同侧、顺。反之则为E构型,即异侧、反。
二烯烃的分类 含两个碳碳双键的烃类化合物。通式为CnH(2n-2),属于不饱和烃。 根据分子中两个双键的相对位置可以分为: (1)累积二烯烃。分子中两个双键连在同一个碳原子上。 (2)孤立二烯烃。分子中两个双键被一个以上的单键所隔开。 (3)共轭二烯烃。分子中两个双键被一个单键所隔开。 累积二烯烃数目很少。孤立二烯烃与一般烯烃性质相似。共轭二烯烃最为重要,具有某些不同于普通烯烃的性质。例如分子较稳定;能发生1,4-加成;比普通烯烃容易聚合。共轭二烯烃在合成橡胶上十分重要,例如:1,3-丁二烯自身聚合成顺丁橡胶;与苯乙烯共聚得丁苯橡胶;与丙烯腈共聚得丁腈橡胶。 共轭二烯烃是二烯烃的一类,分子中含有两个相隔一个单键的双键(一般为碳碳双键)。最简单的共轭二烯烃是1,3-丁二烯。共轭二烯烃相对于累积二烯烃来说,更加稳定。[1] 中文名 共轭二烯烃 两个双键被一个单键隔开,即含有—C=C—C=C—体系的二烯烃。 例如1,3-丁二烯(CH2=CH-CH=CH2)。 共轭二烯烃中共轭体系的存在,使其具有特殊的原子间相互影响——共轭效应。 与孤立二烯相比,键长发生平均化,分子折射率增加,内能降低。 除和一般烯烃一样发生加成反应外,特点是能起1,4-加成之类的反应,也容易聚合。 如1,3-丁二烯(CH2=CH-CH=CH2)聚合生成-[-CH2-CH=CH-CH2-]n- 反应:⒈1,2-加成 1,4-加成极性试剂有利于1,4-加成;低温有利于1,2-加成,高温有利于1,4-加成 ⒉电环化反应?直链共轭多烯烃可发生分子内反应,π键断裂,?双键两端碳原子以σ键相连,形成一个环状分子。电环化反应的显着特点是高度的立体专一性,即在一定条件下(光或热)生成特定构型的产物。 ⒊双烯合成(Diels-Alder反应)具有供电基团的双烯体和具有吸电基团的亲双烯体反应时有利于反应的进行。由于双烯合成的产物是固体,此反应可用来鉴别共轭二烯烃。 ⒋聚合反应?通过聚合反应,生成相对分子质量高
项目总结 1. DMTO项目设计思路 图1 DMTO项目设计思路图 如图 1 所示,乙烯和丙烯等低碳烯烃是现代化学工业的重要基础原料,是衡量一个国家综合国力的重要指标,制备乙烯和丙烯的传统方法是采用石油裂解工艺,但石油储量有限,且近年来石油价格更是持续攀升,通过石油裂解生产低碳烯烃的传统方法已不再受青睐,所以世界各国开始致力于非石油路线制乙烯和丙烯类低碳烯烃的开发。其中,以煤或天然气为原料经甲醇制备低碳烯烃的MTO 或MTP工艺由于污染小,产品收率高而备受重视。 其中,MTO工艺可适当调节乙烯、丙烯产量,适应市场变化,且装置操作简单,易控制,安全性好;此外,我国大连化学物理研究所自主研发的DMTO工艺已实现了万吨级工业化试验,处于世界领先地位;结合我国多煤少气的国情,我们采用了以煤为原料经甲醇制备低碳烯烃的DMTO工艺。 依此思路,经过详细论证,我们为中煤化工集团设计了180万吨/年甲醇年产60万吨烯烃项目,本项目包含一套烯烃合成装置、一套烯烃预分离装置、一套烯烃精馏装置和一套制冷装置。
2. DMTO项目工段解读 2.1 合成工段 ①内置水平筛板的多层阶梯式取热流化床反应器 ★层间换热管快速取出热量,保持反应器在等温条件下发生反应。 ★筛板上反应物与处于流化态的催化剂颗粒接触充分,温度、浓度分布均匀。★多层筛板减少返混,使反应生成物能及时移出反应器以减少副反应的发生,提高目的产物的产率。 ★多层筛板严格控制催化剂在反应器中的停留时间,保证催化剂的高活性。 ②再生系统,能量回收利用 ★充分回收燃烧热,生产蒸汽 2.2预分离工段 ①四段压缩,经济可行 ★流程简单,设备费用低,投资省。 ②两段碱洗,提高利用率 ★混合气中CO2含量较少,仅占0.87%,采用两段碱洗法脱除混合气中的中CO2,提高了碱液利用率。 ③吸附-再生两床工艺,干燥脱水 ★以3A分子筛为脱水的吸附剂,采用吸附-再生两床工艺实现干燥脱水。 2.3精馏工段 ①前脱丙烷精馏方案,节省成本与能耗 ★脱丙烷塔置于压缩机三、四段间,先除去C4以上烃,减少了进入脱甲烷塔的物料量,节省了深冷冷耗和压缩功功耗。 ② Aspen Split软件,论证最优塔序 ★利用Aspen split软件对精馏序列进行模拟和优化,依次得到各塔在一定温度
综述聚丙烯热降解行为 摘要: 关键词: 1.性能 聚丙烯,英文名称:Polypropylene,日文名称:ポリプロピレン分子式:C3H6nCAS简称:PP由丙烯聚合而制得的一种热塑性树脂。按甲基排列位置分为等规聚丙烯(isotaeticPolyProlene)、无规聚丙烯(atacticPolyPropylene)和间规聚丙烯(syndiotaticPolyPropylene)三种。 聚丙烯( PP) 是一种性能优良的热塑性合成树脂, 具有比重小、无毒、易加 工、抗冲击强度高、抗扰曲性以及电绝缘性好等优点, 在工业建设、汽车工业、 家用电器、电子、包装及建材家具等方面具有广泛的应用[1]。由于pp链上含有 α氢及大量不稳定的叔碳原子, 所以热氧化是PP最主要的致老化破坏的因素。对 PP热降解的研究对延长其使用寿命、再生利用、加速降解、保护环境等均具有十 分重要的意义[2]。 2 聚丙烯的分类如下 (1)按聚丙烯分子链上甲基的排布情况分,可以把聚丙烯分成等规、间规及无规三大类。等规聚丙烯的甲基都排布在分子链的一侧,整个分子的规整性最高,所以结晶度高,机械物理性能高,是聚丙烯的主要成型树脂;间规聚丙烯分子链中的甲基,分别有秩序排布于两侧,等规性比等规PP差,结晶度也低,随之性能也不如等规PP;无规PP分子中的甲基混乱地排布,无规律性可言。因此也就不能结晶,因为结晶的首要条件是分子空间排布的规整性要高。无规聚丙烯是黏稠状半固体物质,是生产聚丙烯树脂过程中一定会产生的副产品。过去不需费用,直接可从石化厂中运来,现在发现无规PP有不少用途:无规PP经过冷却、二辊挤压去除水分后,可用于热熔胶添加剂,和包装材料、各种包装材料的添加剂使用,还可提高主黏结树脂的相容性及黏结力,是热熔材料的有用增黏剂。 (2)聚丙烯同其他聚合物一样,有均聚丙烯和共聚丙烯之分,均聚丙烯有其固有的优点,也有其固有的缺点,为改善均聚丙烯的某些缺点,采用共聚改性的方法,在丙烯聚合时很普遍,最为广泛使用的共聚单体是乙烯,乙烯均聚物的特点是柔软性好,耐低温性好,可耐-70℃以下的温度;而丙烯均聚物的最大缺点是耐低温性差,不能使用在0℃以下的场合。在低温下易发脆,冲击强度尤其是低温冲击强度低,低温下受冲击易产生裂纹,二者共聚合生成嵌段共聚丙烯(blockPP)就可以提高PP的低温冲击强度,提高PP的耐低温性。 3聚丙烯催化剂新进展 3.1Z-N催化剂
教学要求及教学内容提纲 1.掌握烯烃的结构特征、通式和命名 2.理解烯烃的同分异构现象 3.了解烯烃的物理、化学性质 重点与难点: 重点: 1.烯烃的结构特征:π键的形成和特点;顺反异构的构型标记及次序规则 2.烯烃的化学性质 难点: 烯烃的结构特征 教学实施手段: 讲授、讨论、提问、讲评 推荐参考书及预复习任务: 参考书 参考书:《药用有机化学》郭扬主编,第一版,中国医药科技出版社 复习总结新课重点、难点内容 1.烯烃的定义 2.烯烃的分类 3.烯烃的异构现象:构造异构(碳链异构,位置异构);立体异构(顺反异构) 4.烯烃的性质:加成、氧化、聚合反应 教学过程
【引言】: 复习上节课的内容; 由烷烃的结构、命名、性质导入新课,并引入不饱和烃的概念。 【教师】: 如果烃分子中只有单键,则叫做饱和烃,饱和链烃称为烷烃,烷就是“完”全的意思,分子内只有单键且成链状。 如果各键没有被氢原子占满,富余的键会和其他碳原子组成双键或三键,就是不饱和烃。 不饱和烃中有双键的叫“烯”,是氢原子“稀”少的意思;有三键的为“炔”,是氢原子“缺”乏的意思。除此之外还有芳香烃,例如“苯”。不饱和烃的双键和三键不太牢固,比较容易断裂,容易发生化学反应。 {分类见教材25页} 【板书】:第一节 烯烃 【教师】: 烯烃是指分子中含有碳碳双键C=C 键的不饱和烃,根据含有碳碳双键的数目又可分为单烯烃、二烯烃和多烯烃。如果不加说明,通常所说的烯烃是指含有一个碳碳双键的单烯烃。 在单烯烃分子中,含有一个碳碳双键,所以它比相同碳数的烷烃少两个氢原子,单烯烃的通式为CnH2n 。 【板书】:(一):烯烃的结构 【教师】: 最简单的烯烃是乙烯。医药上,乙烯与氧的化合物可以作为麻醉剂。 以乙烯为例,介绍烯烃的结构特征。 H H H C C 双键基团是烯烃分子中的官能团,具有反应活性。 双键的表示方法:双键一般用两条短线来表示,如:C=C , 【教师】: 现代物理方法研究表明:乙烯分子中的碳碳双键的键能为610kJ.mol -1 ,键长为134pm , 而乙烷分子中碳碳单键的键能为345kJ.mol -1 ,键长为154pm 。比较可知,双键并不是单键的简单的加合。 【教师】:乙烯分子中,两个碳原子和四个氢原子都在一个平面上,即乙烯分子为平面分子。 【板书】:展示乙烯的分子结构{PPT 有动态版}
烃类化合物 同系物: 结构相似,在分子组成上相差一个或多个CH2原子团的物质互称为同系物。 同系物特点:通式相同,结构相似,化学性质相似;物理性质一般随碳原子数目的增加而呈规律性变化(如熔沸点逐渐升高);在分子组成上相差一个或多个CH2原子团。 同分异构体: 化学上,同分异构体是一种有相同化学式,有同样的化学键而有不同的原子排列的化合物。简单地说,化合物具有相同分子式,但具有不同结构的现象,叫做同分异构现象;具有相同分子式而结构不同的化合物互为同分异构体。很多同分异构体有相似的性质。 烃类化合物 烃类化合物是碳、氧与氢原子所构成的化合物,主要又分为醇(alcohols)、醛(aldehydes)、酯(esters)、酮(ketones)与酚(phenols)。 常见的烃类 常见的烃有甲烷(沼气),丙烷和丁烷(打火机油),异辛烷,石蜡 烃的主要来源: 天然气:甲烷(主要)、乙烷、丙烷、丁烷 石油:各种烃的混合物:汽油、煤油、柴油、润滑油、石蜡、沥青 煤:芳香烃等 主要烃类 一.烷烃 分子中的碳,以碳、碳单键相结合,其他的键都为氢原子所饱和的烃 化学式规律:当碳原子数为n时,氢原子数为2n+2 烷烃的通式为CnH2n+2 烷烃的物理性质 1.物质状态:在室温和一个大气压下,C1-C4是气体,C5-C16是液体,C17以上是固体。
2.沸点:正烷烃的沸点是随着分子量的增加而有规律升高。液体沸点的高低决定了分子间引力的大小,分子间引力愈大,使之沸腾就必须提供更多的能量,所以沸点就愈高。而分子间引力的大小取决了分子结构。 3.熔点:正烷烃的熔点,同系列C1-C3不那么规则,但C4以上的是随着碳原子数的增加而升高。不过,其中偶数的升高多一些,以至含奇数和含偶数的碳原子的烷烃各构成一条熔点曲线,偶数在上,奇数在下。 烷烃的化学性质 1、共价键都为σ键,键能大; C-H 390~435KJ/mol C-C 345.6KJ/mol 2、分子中的共价键不易极化。 (电负性差别小 C:2.5, H:2.2) 烷烃的化学性质稳定(特别是正烷烃)。在一般条件(常温、常压)下,与大多数试剂如强酸、强碱、强氧化剂、强还原剂及金属钠等都不起反应,或反应速度极慢。 命名: 找出最长的碳链当主链,依碳数命名主链,前十个以天干(甲、乙、丙、丁、戊、己、庚、辛、壬、癸)代表碳数,碳数多于十个时,以中文数字命名,如:十一烷。 从最近的取代基位置编号:1.2.3...(使取代基的位置数字越小越好)。以数字代表取代基的位置。数字与中文数字之间以“-”隔开。 有多个取代基时,以取代基数字最小且最长的碳链当主链,并依甲基、乙基、丙基的顺序列出所有取代基。 有两个以上的取代基相同时,在取代基前面加入中文数字:一、二、三...,如:二甲基,其位置以, 隔开,一起列于取代基前面。 注:1.若有两个不同的支链,且分别处于距主链两端相同的位置,则应从较简单的支链那段开始编号。 2.若有两个相同的支链,且分别处于距主链两端相同的位置,但中间还有支链则编号是应遵循支链位号之和最小的原则。 3.选取主链时,若存在两个等长的碳链时应选取支链数最多的碳链作为主链。 反应类型 1、氧化还原反应 氧化反应——有机物分子中引入氧原子或去掉氢原子的反应。
烯烃部实习报告 篇一:烯烃厂认识实习报告实习报告 东南大学化学化工学院 认识实习报告 姓名:李贺 学号:19112211 实习地点:扬子化工烯烃厂 20XX年8月 目录 一、实习目的 二、认识实习内容 1、安全教育 2、丁二烯装置介绍 3、丁二烯生产装置参观 4、中控室参观 三、认识实习的体会与收获 一、实习目的 认识实习是本专业重要的一个实践环节,安排在学习专业基础课过程中进行。通过这个环节培养同学们理论联系实际的能力,可起到承前启后的作用,有利于专业基础课的学习,从而引发学生对后续专业课学习的兴趣。
同学们下到工厂、车间,对企业的生产、安全、设备管理情况作一概况性的了解;对丁二烯装置及包装车间等典型石油化工生产装置的工艺原理及简单工艺流程有一初步认识和了解,对装置中的通用设备如塔、换热器、泵、压缩机等的工艺作用、结构特征有所了解,对专用设备有一定的认识;并对产品包装过程等后处理过程有所了解。通过实习使学生对本专业有个初步的感性认识。 二、认识实习内容 1、安全教育时间:6月30日(星期一)上午 地点:扬子石化烯烃厂会议室 活动内容:安全教育 指导老师绘声绘色的给我们上了一节关于认识实习期间的安全教育,主要有以下几个方面: 1.在实习期间,学生必须提高安全防范意识,提高自我保护能力。注意自身的人身和财物安全,防止各种事故的发生,对生产实习中有关安全问题的复杂性要有充分的思想准备。 2.着装方面,实习期间必须穿工人工作时工作服(尤指一线工人穿戴的长袖),头戴安全帽。 3.注意饮食卫生和饮食安全,由于实习期间天气炎热,所以自己带着饮用水,防止中暑。 4.凡实习的学生应严格遵守实习纪律及实习单位的保卫、安全操作规程、保密制度。特别要注意安全,杜绝各类
我国煤(甲醇)制烯烃项目情况 序号项目名称建设规模(万吨/年)总投资(亿元)项目进展 1神华宁煤宁东MTP项目521852010年10月投产2大唐公司多伦MTP项目461802010年11月投产3中原石化SMTO项目20152011年10月投产4宁波禾元DMTO项目60582013年2月投产5惠生南京MTO项目30202013年9月投产6联想集团滕州DMTO项目4035预计2014年投产7陕煤化蒲城DMTO项目682782014年投产 8中煤榆林DMTO项目682262014年投产 9延长石油靖边DMTO项目602332014年投产10神华包头DMTO项目601702010年8月投产11青海盐湖公司(格尔木)100158预计2014年投产12宁夏宝丰集团(宁东)60142预计2014年投产13神华宁东二套MTP项目506预计2015年投产14神华乌鲁木齐DMTO68245预计2015年投产15神华榆林DMTO项目60110预计2015年投产
16山东恒通3063预计2015年投产17山西焦化(洪洞县)6086预计2015年投产18久泰能源(准格尔)6083预计2015年投产19甘肃华亭煤业集团2025预计2015年投产20中煤蒙大(纳林河)60104预计2015年投产21江苏盛虹(连云港)120235正在设计 22兴兴新能源(嘉兴)60120在建 23同煤集团(大同)60101在建 24中电投/Total(内蒙)80254已发路条 25黑龙江龙泰公司60157已发路条 26中石化贵州织金60167已发路条,报批27神华/陶氏(榆林)1201200已发路条,完成环评28河南煤业中石化,鹤壁60173已发路条 29中天合创(内蒙图克)127416已发路条 30中安联合(安徽淮南)60209已发路条 31平凉华泓DMTO项目70243已发路条 32神华呼伦贝尔DMTO项目68前期工作 33盘江煤电(贵州)60284前期工作 34国电准东(新疆)60209前期工作
第三节乙烯烯烃 【知识讲解】一、乙烯的分子结构(与乙烷比较) 乙烯乙烷分子式C2H4C2H6 电子式 结构式 结构简式CH2=CH2CH3CH3 C原子间键C=C(双键)C-C(单键)键角120°109°28' 键长 1.33×10-10m 1.54×10-10m 键能615KJ/mol(一个键易断)348KJ/mol 分子内各原子相对位置各原子均在同一平面不在一个平面加成反应不能能 取代反应能较难 二、乙烯的实验室制法 1、试剂:乙醇(酒精)和浓硫酸按体积比1:3混合 2、反应原理 3、气体发生装置:的装置(与制Cl2相似) 4、集气方法:排水集气法 5、几个应该注意的问题 ① 浓硫酸的作用催化和脱水 ② 碎瓷片的作用防止液体剧烈跳动(防止煮沸)。
③ 反应温度应控制在170℃,若温度过低(140℃)将发生副反应,而生成乙醚;若温度过高,则乙醇易被浓H2SO4氧化。为了控制温度,应将温度计的水银球插在液面下。以准确测定反应液体的温度。 ④ 反应后液体易变黑,且有刺激性气味气体产生。这是由于浓硫酸的强氧化性将乙醇氧化生成C和CO2,且硫酸被还原成SO2所致。其反应方程式可表示为: 若要净化乙烯,可将其通过NaOH溶液除去SO2、CO2。 三、乙烯的性质 通常情况下,乙烯是无色,稍有气味的气体,密度与空气相近,难溶于水。乙烯化学性较活泼,易发生如下反应: 1、加成反应:有机物分子里不饱和碳原子跟其它原子或原子团直接结合生成别的物质的反应。 ① 与卤素加成:CH2=CH2+Br2→CH2Br-CH2Br(使溴水褪色,可用于检验乙烯或除去乙烯) ② 与氢气加成: ③ 与卤化氢HX加成:(可用于制氯乙烷) ④ 与水加成:(可用于工业上制酒精) 2、氧化反应 ① 燃烧:(火焰明亮有黑烟) ② 可与强氧化剂反应:使酸性KMnO4溶液褪色(可用于检验乙烯) 3、加聚反应:(可用于制聚乙烯塑料)加聚反应是指不饱和单体通过加成反应互相结合成高分子化合物的反应。 四、烯烃:含有碳碳双键的一类链烃 1、烯烃的结构特点是具有碳碳双键。烯烃的通式为C n H2n(n≥2)。
第二册第五章烃 一、知识要点与规律 1.有机物 (1).有机物通常是指含碳元素的化合物。但象CO、CO2 、H2CO3和HCN及其盐等少数物质,虽然含有碳元素,但其性质与无机物很相似,故一般归于无机物。 (2).有机物种类繁多达上千万种(无机物只有十几万种),其重要原因是: ①.碳原子有4个价电子,能与其它原子形成4个共价键。 ②.碳原子之间的结合方式可以有多种(单键、双键、三键),碳原子之间可成链可成环,碳链的长度可以不同,碳环的大小可以不同。 ③.有机物普遍存在同分异构现象。 (3).有机物的性质:对于大多数有机物,有如下性质 ①难溶于水,易溶与汽油、苯等有机溶剂(相似相溶); ②多为非电解质,不易导电(非极性分子); ③多数熔沸点较低(分子晶体); ④大多易燃烧、易分解(多由C、H组成,故易于燃烧;碳链越长越易于断裂分解); ⑤有机反应复杂、速率慢,多需催化剂(分子反应一般慢于离子反应;有机分子中共价键多,反应中可以断裂的部位多,故副反应多)。 (4)重要的有机原理 ①价键数原理:碳四键,氮三键,氧二键,氢一键。 ②同系列原理:同系列中的各不同有机物均具有十分相似的化学性质。这是学习有机化学的主要方法。 ③官能团原理:分子结构决定化学性质在有机化学中的体现是-官能团决定化学性质。学习有机化学从某种意义上说就是学习官能团。这一原理是进行有机物性质、结构推理的主要依据。 2.烃的概念和分类 (1).概念:仅由碳氢两种元素组成的有机物,叫碳氢化合物,简称烃。
3.同系物和同分异构体概念比较 4. 烃的同系物的含碳量比较 烷烃(C n H 2n+2):C%=12n/(14n+2)=12/(14+2/n); n=1时,C %=75%;n →∞时,C%→85.7%; 烯烃(C n H 2n ):C%=12n/14n =85.7%; 炔烃(C n H 2n-2):C%=12n/(14n –2)=12/(14–2/n); n=2时,C %=92.3%;n →∞时,C%→85.7%; 苯及其同系物(C n H 2n -6):C%=12n/(14n –6)=12/(14–6/n); n=6时,C %=92.3%;n → ∞时,C%→85.7%; 5.烃的物理性质递变规律 一般随碳原子数的增多,沸点升高,液态时密度增大。碳原子数为1~4时为气态。不溶于水,密度比水小。 对于同分异构体,支链越多,熔沸点越低。如:正戊烷>异戊烷>新戊烷。 6.烃中五种共价键的比较 7.烃的结构特点和化学性质 75% 87.5% 92.3% 烷烃 烯烃 的 同系物 甲烷 乙炔和苯 %
烯烃产品项目 初步方案 规划设计/投资方案/产业运营
摘要 该烯烃产品项目计划总投资5485.58万元,其中:固定资产投资4778.11万元,占项目总投资的87.10%;流动资金707.47万元,占项目总投资的12.90%。 达产年营业收入5793.00万元,总成本费用4527.55万元,税金及附加88.55万元,利润总额1265.45万元,利税总额1528.54万元,税后净利润949.09万元,达产年纳税总额579.45万元;达产年投资利润率 23.07%,投资利税率27.86%,投资回报率17.30%,全部投资回收期7.28年,提供就业职位87个。 充分依托项目承办单位现有的资源或社会公共设施,以降低投资,加快项目建设进度,采取切实可行的措施节约用水。贯彻主体工程与环境保护、劳动安全和工业卫生、消防工程“同时设计、同时建设、同时投产”的总体规划与建设要求。 我国“富煤、贫油、少气”的资源禀赋特点使我国石油以及天然气进口依存度较高。石化行业烯烃生产受制于石油进口依赖,导致国内烯烃生产量低于需求量,国内烯烃供需缺口明显,烯烃进口依存度较高。大力发展煤制烯烃等煤制化学品,对保障我国产业经济自主性、安全性有重要意义。 报告主要内容:项目总论、背景和必要性研究、产业分析、项目建设内容分析、项目选址评价、项目土建工程、工艺方案说明、环保和清洁生
产说明、企业卫生、风险评估、节能评估、项目进度方案、投资情况说明、项目经济收益分析、项目评价等。
烯烃产品项目初步方案目录 第一章项目总论 第二章背景和必要性研究第三章项目建设内容分析第四章项目选址评价 第五章项目土建工程 第六章工艺方案说明 第七章环保和清洁生产说明第八章企业卫生 第九章风险评估 第十章节能评估 第十一章项目进度方案 第十二章投资情况说明 第十三章项目经济收益分析第十四章项目招投标方案 第十五章项目评价
降烯烃类助剂 烯烃在发动机内燃烧容易形成积碳,从而影响发动机燃烧效率、增加污染物排放等影响排放问题。GB17930-2006《车用汽油》规定,烯烃含量,%/体积比:不大于35。 为了降低汽油的烯烃含量,采取措施使已经生成的汽油馏分继续进行反应,通过汽油的深度反应,实现汽油中烯烃组分的有效转化;反应温度的提高将会加剧热裂化反应在裂化反应中的份量,进一步恶化高价产品的选择性,同时降低氢转移反应的能力,不利于汽油烯烃含量的降低。 工艺上目前能做的,提催化剂活性、提剂油比,采用相对较低反应温度,使用降烯烃催化剂。 催化裂化工艺是我国重质油轻质化加工过程中的主要技术手段,我国成品汽油中的80%来自催化裂化,重整汽油、烷基化汽油等其他调合组分所占的比例很少,而催化裂化汽油中的烯烃含量较高,达到40%以上,而这种局面在短期内难以改变。 对于催化裂化过程,开发具有高活性和选择性的催化剂及助剂,是改变催化产物分布和性质的主要手段。在催化反应过程中,氢转移反应能够显著降低汽油中的烯烃含量,氢转移反应为双分子反应,则催化剂设计思路应提供更多发生双分子反应的条件,加强选择性氢转移反应,并抑制深度氢转移反应的发生,实现低生焦的选择性氢转移反应,并提供有效的正碳离子链传递终止能力,最终实现以正碳离子的β-断裂为主的单分子裂化反应和以氢转移及芳构化等有利于提升管产物分布的催化理想反应的双分子反应的合理匹配。 中国石化石油化工科学研究院(RIPP)通过分子筛改性技术,精细调节分子筛的酸改质,根据反应对分子筛性能的要求,对Y型分子筛和ZRP分子筛进行改性,成功开发了GOR系列降烯烃催化剂[6]。兰州石化公司在研究催化反应中烯烃的生成和转化规律的基础上,以改善氢转移活性及选择性为研制开发降烯烃催化剂和助剂的技术关键,研发了LBO系列降烯烃催化剂[7]。此外,我国还开发了如DODC、LHO-1、CDC等汽油降烯烃催化剂。在FCC 汽油降烯烃助剂方面,有LAP系列降烯烃催化裂化助剂、LBO-A高辛烷值型降烯烃助剂以及LGO-A 降烯烃助剂。这些汽油降烯烃催化剂和助剂均得到了不同程度的
烯烃加成反应 一、催化加氢反应 烯烃与氢作用生成烷烃的反应称为加氢反应,又称氢化反应。 加氢反应的活性能很大,即使在加热条件下也难发生,而在催化剂的作用下反应能顺利进行,故称催化加氢。 在有机化学中,加氢反应又称还原反应。 这个反应有如下特点: 1.转化率接近100%,产物容易纯化,(实验室中常用来合成小量的烷烃;烯烃能定量吸收氢,用这个反应测定分子中双键的数目)。 2.加氢反应的催化剂多数是过渡金属,常把这些催化剂粉浸渍在活性碳和氢氧化铝颗粒上;不同催化剂,反应条件不一样,有的常压就能反应,有的需在压力下进行。工业上常用多孔的骨架镍(又称Raney镍)为催化剂。 3.加氢反应难易与烯烃的结构有关。一般情况下,双键碳原子上取代基多的烯烃不容易进行加成反应。 4.一般情况下,加氢反应产物以顺式产物为主,因此称顺式加氢。下例反应顺式加氢产物比例为81.8%,而反式产物为18.2%。产物顺反比例受催化剂、溶剂、反应温度等影响。 5.催化剂的作用是改变反应途径,降低反应活化能。一般认为加氢反应是H2和烯烃同时吸附到催化剂表面上,催化剂促进H2的σ键断裂,形成两上M-H σ键,再与配位在金属表面的烯烃反应。 6.加氢反应在工业上有重要应用。石油加工得到的粗汽油常用加氢的方法除去烯烃,得到加氢汽油,提高油品的质量。又如,常将不饱和脂肪酸酯氢化制备人工黄油,提高食用价值。 7.加氢反应是放热反应,反应热称氢化焓,不同结构的烯烃氢化焓有差异。 例1. 反应物:
ΔHr/KJmol-1126.6 119.5 115.3 例二. 反应物: ΔHr/KJmol-1126.6 119.1 112.4 各种甲基丁烯热力学能比较: 每组的产物相同,吸收H2一样多,氢化焓反映了烯烃的含能量 由此得出直链烯烃热力学能(E)-2-丁烯 <(Z)-2-丁烯 < 1-丁烯 烯烃的热稳定性的一般规律: RCH=CHR' >RCH=CH2 > CH2=CH2 R2C=CR2 > R2C=CHR > R2C=CH2 > RHC=CH2 二、加卤素反应: 烯烃容易与卤素发生反应,是制备邻二卤代烷的主要方法,丙烯通入液溴中即生成1,2一二溴丙烷: 1.这个反应在室温下就能迅速反应,实验室用它鉴别烯烃的存在,(溴的四氯化碳溶液是红棕色,溴消耗后变成无色)。 2.不同的卤素反应活性规律: 氟反应激烈,不易控制;碘是可逆反应,平衡偏向烯烃边;常用的卤素是Cl2和Br2,且反应活性Cl2>Br2。 3.烯烃与溴反应得到的是反式加成产物:
本章重难点专题突破 1 各类烃的结构与性质归纳解读 键含有加成反应 后者为铁粉。②苯不能使酸性高锰酸钾溶液褪色,但苯的同系物一般能被氧化而使酸性高锰酸钾溶液褪色。 溴水、溴的四氯化碳溶液、光照、催化剂等)对反应的影响。 2 烃类燃烧规律集锦 1.烃完全燃烧前后气体体积变化规律 烃完全燃烧的通式:C x H y +(x +y 4)O 2――→点燃x CO 2+y 2 H 2O (1)燃烧后温度高于100 ℃,即水为气态 ΔV =V 后-V 前=y 4 -1 ①y =4时,ΔV =0,体积不变②y >4时,ΔV >0,体积增大③y <4时,ΔV <0,体积减小 (2)燃烧后温度低于100 ℃时,即水为液态
ΔV=V前-V后=1+y 4,总体积减小 [特别提示]烃完全燃烧时,无论水是气态还是液态,燃烧前后气体体积变化都只与烃分子中的氢原子数有关,而与烃分子中碳原子数无关。 2.烃完全燃烧时耗氧量规律 (1)等物质的量的烃(C x H y)完全燃烧时,其耗氧量的大小取决于(x+y 4)的值,其值越大,耗氧 量越多。 (2)等质量的烃完全燃烧,其耗氧量大小取决于该烃分子中氢的质量分数,其值越大,耗氧量越多。相同碳原子数的烃类,碳的质量分数越大,耗氧量越多。 (3)最简式相同的烃,不论它们以何种比例混合,只要总质量一定,完全燃烧时所消耗的氧气为定值。 (4) 3 (1)2 (2)碳的质量分数相同的烃,只要总质量一定,以任意比混合,完全燃烧后,产生的CO2的量总是一个定值。 4.燃烧时火焰亮度与含碳量的关系比较规律 (1)含碳量越高,燃烧现象越明显,表现为火焰越明亮,黑烟越浓。如C2H2、苯、甲苯等燃烧时火焰明亮,并伴有大量浓烟;而含碳量越低,燃烧现象越不明显,无黑烟,如甲烷;对于C2H4及单烯烃的燃烧则是火焰较明亮,并伴有少量黑烟。 (2)含碳原子较少的各类烃,燃烧时的现象是不同的,烷烃无黑烟产生,烯烃有少量黑烟产生,炔烃及芳香烃有浓黑烟产生。应用燃烧来鉴别简单的烷烃、烯烃和炔烃是一种简单而有效的方法。 3、确定混合烃组成的四种方法 1.平均相对分子质量法 假设混合烃的平均相对分子质量为M,则必含相对分子质量比M小或相等(由同分异构体组成的混合气体)的烃。如M<26(烷、炔相混),则混合烃中一定有CH4,或M<28(烷、 烯相混),则混合烃中一定有CH4,等等。 2.平均分子组成法 假设混合烃的平均分子式为C x H y,根据其平均分子组成情况有以下规律:若1 石化烯烃厂爆炸事故文件管理序列号:[K8UY-K9IO69-O6M243-OL889-F88688] 某石化烯烃厂“2.23”爆炸事故事故经过 2002年2月23日1时,某石化烯烃厂聚乙烯车间新生产线零点班接班,零点班值班班长身体有病,但未向车间领导请假,擅自让聚合班长代理值班班长。 接班时生产正常。 6时40分,当班人员发现聚乙烯新、老生产线反应速度下降。6时50分,老生产线悬浮液接收罐高压联锁停车,新生产线聚合反应速度继续下降,聚合班长立即向车间副主任报告,车间副主任让聚合班长向调度报告并询问是否乙烯原料出现问题,调度说正在检查原因。聚合班长等人一边等候调度指令,一边调整反应并开始减少投料量。 7时20分左右,车间副主任向聚合班长询问现场情况。此时,新生产线悬浮液接收罐压力迅速上升,达到联锁动作值,新生产线联锁停车。聚合班长立即让3名操作工去现场关手阀。7时25分,3人到达现场,发现悬浮液接收罐泄漏,立即向车间主控室报告,聚合班长听后立刻奔向现场,当其离开主控室不足1分钟时,现场发生爆炸。事故造成8人死亡,1人重伤,18人轻伤。 事故原因 1.直接原因:聚乙烯新线聚合釜反应不正常,未聚合的乙烯单体进入悬浮液接收罐11305X中挥发,系统压力升高。由于安装在11305X上下管道上的两个DN200的玻璃视镜是伪劣产品,因而发生破裂,致使大量的乙烯气体瞬间喷出,弥漫整个厂房空间,从厂房上部窗户溢出的乙烯气体被设置在该处的引风机吸风口吸入沸腾干燥器内,与聚乙烯粉末、热空气形成的爆炸混合物,达到爆炸浓度,被聚乙烯粉末沸腾过程中产生的静电火花引爆,发生爆炸。 2.其他原因: (1)采购环节存在严重问题 事故发生的直接原因是新线悬浮液接收罐连接在管线上的视镜破裂造成的。视镜设计的公称压力为2.5兆帕,实际在0.5兆帕时就发生破裂。事故调查表明,在视镜采购环节上存在许多问题。视镜的生产厂家采购单上是北京某阀门厂,实际上该厂根本不生产视镜,而是该厂的业务员(事故后已逃逸)从温州某个经销点购买的,该视镜是由上海郊区一个小厂生产的,该厂根本没有检验手段,无法鉴定其产品是否合格。更为 烯烃产品项目 合作方案 规划设计/投资分析/实施方案 烯烃产品项目合作方案 我国“富煤、贫油、少气”的资源禀赋特点使我国石油以及天然气进口依存度较高。石化行业烯烃生产受制于石油进口依赖,导致国内烯烃生产量低于需求量,国内烯烃供需缺口明显,烯烃进口依存度较高。大力发展煤制烯烃等煤制化学品,对保障我国产业经济自主性、安全性有重要意义。 该烯烃产品项目计划总投资7868.92万元,其中:固定资产投资5984.53万元,占项目总投资的76.05%;流动资金1884.39万元,占项目总投资的23.95%。 达产年营业收入16311.00万元,总成本费用12688.71万元,税金及附加148.91万元,利润总额3622.29万元,利税总额4270.83万元,税后净利润2716.72万元,达产年纳税总额1554.11万元;达产年投资利润率46.03%,投资利税率54.27%,投资回报率34.52%,全部投资回收期4.40年,提供就业职位281个。 报告根据项目实际情况,提出项目组织、建设管理、竣工验收、经营管理等初步方案;结合项目特点提出合理的总体及分年度实施进度计划。 ...... 烯烃产品项目合作方案目录 第一章申报单位及项目概况 一、项目申报单位概况 二、项目概况 第二章发展规划、产业政策和行业准入分析 一、发展规划分析 二、产业政策分析 三、行业准入分析 第三章资源开发及综合利用分析 一、资源开发方案。 二、资源利用方案 三、资源节约措施 第四章节能方案分析 一、用能标准和节能规范。 二、能耗状况和能耗指标分析 三、节能措施和节能效果分析 第五章建设用地、征地拆迁及移民安置分析 一、项目选址及用地方案 高一化学 HX-13-01-022 《烯烃》导学案 审核人:高一化学组 编写时间:5月31日 班级: 组别: 层次: 姓名: 【学习目标】1.初步掌握单烯烃分子的组成和结构。 2.了解共轭二烯烃1,2加成反应和1,4加成反应规律。 【学法指导】1.学会判断烷烃与烯烃的方法。 2.通过乙烯性质的科学探究学习,提高分析问题的能力。 【知识链接】乙烯的分子式、电子式、结构式、空间构型、键角,乙烯的化学性质。 【问题设计】 〔基础梳理〕【选修5P 29—30】 一.烯烃【C 级】 [核心整合] 1.符合烯烃通式的烃一定是烯烃吗?【C 级】 2.丙烯的分子式为 ,结构简式为 ,结构式为 ,分子中所有原子 (是,否)在同一平面,在同一平面的原子最多有 个。【B 级】 二.烯烃的物理性质【C 级】 三.烯烃的化学性质【B 级】 [核心整合] 3.等质量的乙烯和丙烯完全燃烧,消耗氧气的质量之比是多少?为什么?【C级】 【当堂检测】 1、室温下1体积气态烃和一定量的氧气混合并充分燃烧, 再冷却至室温, 气体体积比反应前缩小了3体积, 则该气态烃是( ) A.丙烷B.丙烯C.丁烷D.丁烯 2、下列各组中的二种物质以等物质的量混合, 其碳元素的质量分数比乙稀高的是( ) A.甲烷和丙稀B.乙烷和丁稀 C.乙稀和丙稀D.1, 3—丁二稀和环丙烷 3、有二种烯烃和(—R表示烷基), 它们混合后进行加聚反应, 产物中不可能含有下列结构: ( ) ①② ③④ A.②B.③④C.②④D.④ 4、关于烷烃和烯烃的下列说法, 正确的是( ) A.烷烃的通式是C n H2n+2, 符合这个通式的烃为烷烃 B.烯烃的通式是C n H2n, 符合这个通式的烃一定是烯烃 C.烯烃和二烯烃都能与溴水反应, 都能与酸性高锰酸钾溶液 D.烯烃和二烯烃属于同系物 5、某烯烃CH2=CH-C(CH3)3的名称叫“3,3-二甲基-1-丁烯”。该烯烃跟氢气加氢后所得到的 产物的名称( ) A.2,2-二甲基丁烷 B. 3,3-二甲基丁烷 C. 1,1,1-三甲基丙烷 D. 1,1-二甲基丁烷 1。概述 齐鲁72万吨/年乙烯改造工程中大部分的管道、设备需要绝热,根据设计要求绝热施工根据不同的介质温度分别采用高温矿物纤维、硅酸铝纤维、泡沫玻璃、硬质聚氨酯泡沫塑料等材料。防腐涂料种类也较多(无机富锌漆、8000C有机硅耐热漆、)。由于装置要在不停产情况下进行施工,或在相邻生产装置区附近进行施工,而装置一般属易燃易爆场所,因而对施工的质量、安全和文明施工要求较高.为了优质、高效地完成防腐绝热工程的施工,特编制本方案,以指导和规范现场防腐绝热施工。 2.编制依据 2.1《工业设备及管道绝热工程施工及验收规范》GBJ126-89 2。2《炼油、化工施工安全规程》SHJ505-87 2。3《热力设备及管道保温》标准图(86R-411-1) 2。4《涂装前钢材表面预处理规范》SY/T0407-97 2。5《设备及管道隔热设计施工规定》A—SH1—89 2。6SEI提供的其他资料 3.施工准备 3。1施工前施工人员应熟悉图纸及有关技术说明。 3。2钢结构防腐施工应在安装全部完成,办完工序交接手续后进行。防腐前应检查焊接工作是否完成,以上工作全部完成后方可进行防腐施工. 3。3保温施工应在管道的安装工作全部完成,强度试验及气密试验合格,办完工序交接手续后进行。保温前应检查防腐工作是否完成,焊接、管托等是否补刷完油漆,然后进行保温前共检。 3.4根据图纸要求对保温的管线进行挂牌标记(要求写明管线号、保温材料、保温厚度、涂漆种类)。 3.5现场配备必要的预制加工机具和现场施工机具。 3.6对到货的防腐涂料及保温材料,应认真检查其质量、几何尺寸,并及时向主管部门报验;检查复验其性能合格后,按材质、规格分类存放,并要求按规定下垫上盖,做好防雨、放火措施,堆放高度不宜超过2米。 3.7保温铁皮的预制场地应搭设防雨棚,地面应铺设工作平台。 4.防腐工程 4.1防腐涂料 4.1。1防腐涂料应有出厂合格证和质量证明书,具体数据应符合规范要求. 4.1。2桶装成品涂料打开后,如发现有结块现象,供应部门应按规范要求进行有关项目的复验。4。2防腐层施工的一般规定 4。2.1所有防腐涂料的底漆、面漆、稀释剂应根据设计说明或产品说明书配套使用。不同厂家、不同型号的防腐涂料不宜掺和使用. 4。2.2施工环境温度宜为5~300C,相对湿度不宜大于85%。 4.2.3不应在风沙、雨、雪天进行室外涂漆. 4。2。4防腐涂料品种的选用和涂层层数、厚度应符合设计要求。 4。2。5钢结构和工艺管道如在焊接处理、强度试验和严密性试验合格前进行涂刷,应将全部焊缝预留,待试验合格后,按涂层要求补刷。 4.2。6防腐涂料和稀释剂在贮存、施工及干燥过程中,不得与酸、碱及水接触,并应防尘、防爆晒,严禁烟火。对于有毒有害的涂料在施工过程中,需用轴流风机通风,防止作业人员中毒。 4.2.7钢结构表面处理的等级应达到二级;管道表面处理应达到St3级.4.2。8钢结构及管道的 降低催化汽油烯烃的措施 何声强 (中国石化安庆分公司炼油一部催化装置,安徽安庆246001) 摘要催化裂化装置汽油烯烃含量与原料油性质、催化剂性质、反应温度、剂油比、反应时间等 因素有关,通过采用新工艺,使用降烯烃催化剂,优化原料油性质等措施,可有效降低催化汽油烯 烃含量。 关键词催化汽油烯烃措施 烯烃主要来自催化裂化汽油,是不饱和烃类化合物,具有比较好的抗爆性。但烯烃的稳定性较差,容易堵塞发动机喷嘴,在发动机进气阀及燃烧室中生成沉积物,一方面影响汽油的充分燃烧,加剧汽车尾气的排放污染,另一方面,挥发性较强的烯烃,容易蒸发排放入大气,加速对流层臭氧的生成,形成光化学烟雾。由于我国车用汽油以催化裂化汽油为主,其中烯烃含量较高,达40%~50%,加工石蜡基原料的装置,烯烃含量更高,达60%以上,因此降低催化裂化汽油烯烃含量是解决车用汽油烯烃含量高的关键。 由于催化裂化装置汽油烯烃含量与原料油性质、催化剂性质、反应温度、剂油比、反应时间等因素有关,因此,解决汽油烯烃含量高的问题也应当从这些角度出发。本文将对汽油烯烃含量高的原因进行分析,并提出解决措施。 1原因分析 1.1原料油性质 一般认为,催化裂化主要是正碳离子反应,汽油中烯烃主要来自于原料油中烷烃的裂化。直链烷烃裂化一次生成一个烯烃和一个正碳离子,正碳离子二次裂化又生成一个烯烃和一个正碳离子。烷烃分子越大,裂化次数越多,汽油中烯烃含量越高;环烷烃开环裂化生成两个小分子烯烃,但环烷烃也能够氢转移缩合芳构化。因此,原料中链烷烃含量高,链烷烃分子大时,汽油中烯烃含量较高。实验数据表明1:氢含量高、K值大的原料油,裂化转化率高,汽油产率高,汽油中烯烃含量也较高。 1.2催化剂活性 一般来说,随着分子筛含量增高,氢转移活性也相应增加,因此,产品中的烯烃含量相对减少。实验数据表明2:在相同的反应条件下随着催化剂平衡活性的提高,汽油中烯烃含量逐渐下降,当平衡剂的微反活性从50提高到60.8时,汽油烯烃由67.46%下降至55.33%。 1.3反应温度 催化裂化过程中主要发生热裂化和催化裂化反应,催化反应主要有裂化、氢转移、异构化、芳构化等,裂化和芳构化反应是吸热反应,裂化反应生成烯烃,芳构化反应消耗烯烃;氢转移和异构化反应是放热反应,消耗烯烃。提高反应温度,有利于裂化反应和芳构化反应,不利于氢转移反应和异构化反应。此外,随反应温度的提高,热烈化反应速度提高的幅度大于催化裂化反应速度提高的幅度,不利于汽油 《烃》总结 一、烃的分类及结构和性质 要求掌握本章所涉及的化学方程式 三、专题总结 (一)烃类反应6种类型 1、取代反应——一上一下,取而代之 对象:饱和烃、苯和苯的同系物; 卤素要求是纯净的卤素单质 如:甲烷和氯气的取代反应(方程式、实验现象、产物的物性、取代的有关计算)苯和苯的同系物:卤化、硝化、磺化(方程式、实验设计、产物的物性、除杂)2、加成反应——断一拉二,只上不下 对象:不饱和烃(烯烃、炔烃和苯及苯的同系物) 烯与H2、X2、HX、H2O的加成。炔与H2、X2、HX 的加成; 苯与H2、Cl2的加成。马氏加成。 掌握单烯烃的单一加聚和混合加聚,掌握由加聚产物反推单体。 4、氧化反应 点燃:所有烃都可以燃烧。充分燃烧意即O2适量或过量。产物为CO2和H2O。 掌握所涉及的计算:差量法、极限法、平均值法、十字交叉法、守恒法 被酸性KMnO4溶液氧化:烯、炔、苯的同系物 5、还原反应——不饱和烃加氢 6、分解反应 甲烷分解成C和H2;烷烃的裂化 (二)常见经验规律 1、气态烃燃烧前后总物质的量的变化 C x H y+(x+y/4)O2——XCO2 + y/2 H2O(气) 当y=4时,反应前后气体总物质的量不变 当y>4时,n前<n后 当y<4时,n前>n后(只有C2H2) 如:125℃,1L某气态烃在9L氧气中充分燃烧后的混合气体体积为10L,则该烃可能是:CH4、C2H4、C3H4 2、·质量相同的不同烃,燃烧耗氧量由y/x决定或H%决定,比值越大,耗氧量越大。 生成CO2、H2O的量分别由C%、H%决定。 因此最简式相同的有机物(各元素百分比相同),不管以任何比例混合,只要混合物总的质量一定,各元素的质量就相同,完全燃烧后生成的CO2和H2O及消耗O2的总量就一定。 ·物质的量相同的不同烃,燃烧耗氧量由x+y/4决定,生成CO2、H2O的量分别由x、y决定。 如:C3H8、C3H6、C4H6、C7H8四种物质分析。 3、烃中含碳量的高低 烷烃<烯烃<炔烃、苯及其同系物 烷烃中碳数越多,碳的质量分数越大(<6/7);烯烃中碳的质量分数为一定值(6/7);炔烃、苯的同系物中碳数越多,碳的质量分数越小(>6/7)。 4、烃类物质熔沸点、密度规律:随分子量(碳原子个数)增大而升高。碳数相等的情况下,支链越多, 沸点越低。 5、“根”、“基”、“原子团”的区别 (三)区别一组概念: 同系物、同分异构体(书写、判断数目)、同位素、同素异形体 如:液氯、氯气、P4、P、D、T、CH4、C3H8、1—丁烯、2—甲基丁烯 属于同系物的是CH4、C3H8; 属于同分异构体的是1—丁烯、2—甲基丁烯; 属于同素异形体的是P4、P; 属于同位素的是D、T; 属于同一种物质的是液氯、氯气。 (四)命名: 烷烃、烯烃、炔烃类的命名。石化烯烃厂爆炸事故
烯烃产品项目合作方案
烯烃
【精品】烯烃厂保温方案
降低催化汽油烯烃的措施
烃类知识点