
第23卷,第4期光 谱 实 验 室Vol.23,No.4 2006年7月Chinese J ournal of Sp ectrosco p y L aboratory July,2006测定总氮时影响空白吸光值的因素
董纪珍 宋莹 李建坡 丁致英
(北京城市排水集团有限责任公司水质检测中心 北京市 100022)
摘 要 针对G B11894—89测定污水中总氮空白值偏高的情况,分析了碱性过硫酸钾本身以及纯度的影响、消解量、消解温度和时间、去离子水纯度、玻璃器皿的洁净度、碱性过硫酸钾存储时间、环境因素等影响因素,找出了实验出现问题的原因,并进行了校正。
关键词 总氮,空白,过硫酸钾,紫外可见分光光度法。
中图分类号:O657.32 文献标识码:B 文章编号:1004-8138(2006)04-0791-06
1 前言
总氮是指水体中有机氮和无机氮(NH3—N+NO-3—N+NO-2—N)含量的总和,水体中氮含量的增加会造成生物和微生物类的大量繁殖,消耗水中的溶解氧,使水体质量恶化。水中含氮、磷量较高时,会使浮游生物大量繁殖,出现富营养化状态。因此,总氮是控制水质质量的重要指标之一。
在国家标准中建议采用碱性过硫酸钾氧化-紫外分光光度法(GB11894-89,以下简称《方法》)测定总氮[1],在实际操作中,由于受到某些因素的影响,往往会遇到实验空白值偏高,难以控制,致使测定准确度和精密度差,直接影响测定结果。现对这些影响因素作一些探讨,以供大家参考。2 测定原理
在60℃以上水溶液中,过硫酸钾可分解产生硫酸氢钾和原子态氧。硫酸氢钾在溶液中离解而产生氢离子,故在氢氧化钠的碱性介质中可促使分解过程趋于完全。在120—124℃条件下,原子态的氧使水样中含氮化合物的氮转化为硝酸盐。其方程式为:
K2S2O8+H2O2KHSO4+1/2O2↑
KHSO4K++HSO-4
HSO-4H++SO2-4
分解出的原子态氧在120—124℃条件下,可使水样中含氮化合物的氮元素转化为硝酸盐。并且在此过程中有机物同时被氧化分解。可用紫外分光光度法于波长220nm和275nm处,分别测出吸光度A220及A275,按式(1)求出校正吸光度A。
A=A220-2A275(1)按A的值查校准曲线并计算总氮(以NO-3—N计)含量。
3 实验部分
3.1 试剂和仪器
3.1.1 试剂
水:去离子水;
联系人,电话:(010)87743414;E-mail:jz hdong1978@https://www.doczj.com/doc/4913298692.html,;djz@https://www.doczj.com/doc/4913298692.html,
作者简介:董纪珍(1978—),女,湖北省京山县人,硕士,现主要从事环境科研、环境监测和实验室管理工作。
收稿日期:2006-03-21;接受日期:2006-04-14
碱性过硫酸钾溶液:称取40g 过硫酸钾(K 2S 2O 8),另称取15g 氢氧化钠(NaOH ),溶于水中,稀释至1000m L,溶液存放在聚乙烯瓶内,最长可贮存一周。
盐酸溶液(1+9)。3.1.2 主要仪器和设备
8500紫外可见分光光度计(上海天美科技有限公司)及10m m 石英比色皿。
医用蒸气灭菌器(上海市申安医疗器械厂,压力为1.1—1.4kg /cm 2),锅内温度相当于120—124℃。
Easypureii UV/U F 超纯水器(美国Barnstead 公司)。
具塞玻璃磨口比色管,25mL 。
所用玻璃器皿用盐酸(1+9)浸泡,清洗后再用去离子水冲洗3次以上; 所有试剂均使用符合国家标准或专业标准的分析纯试剂。3.2 实验方法
用适量水样置于25m L 的具塞玻璃磨口比色管,去离子水定容至10m L 刻度,加入5mL 碱性过硫酸钾溶液,塞紧磨口塞,摇匀,用布及绳等扎紧瓶塞,以防弹出。将比色管置于医用手提蒸气灭菌器中,加热,使压力表指针到1.1—1.4kg /cm 2,此时温度达120—124℃后开始计时。保持此温度加热45min 。冷却、开阀放气,移去外盖,取出比色管,冷至室温。加盐酸(1+9)1m L,用去离子水稀释至25m L 标线,混匀。移取部分溶液至石英比色皿中,在紫外分光光度计上,以去离子水作参比,分别在波长为220nm 与275nm 处测定吸光度,并按式(1)计算出校正吸光度A 。
4 结果和讨论
4.1 碱性过硫酸钾本身的影响
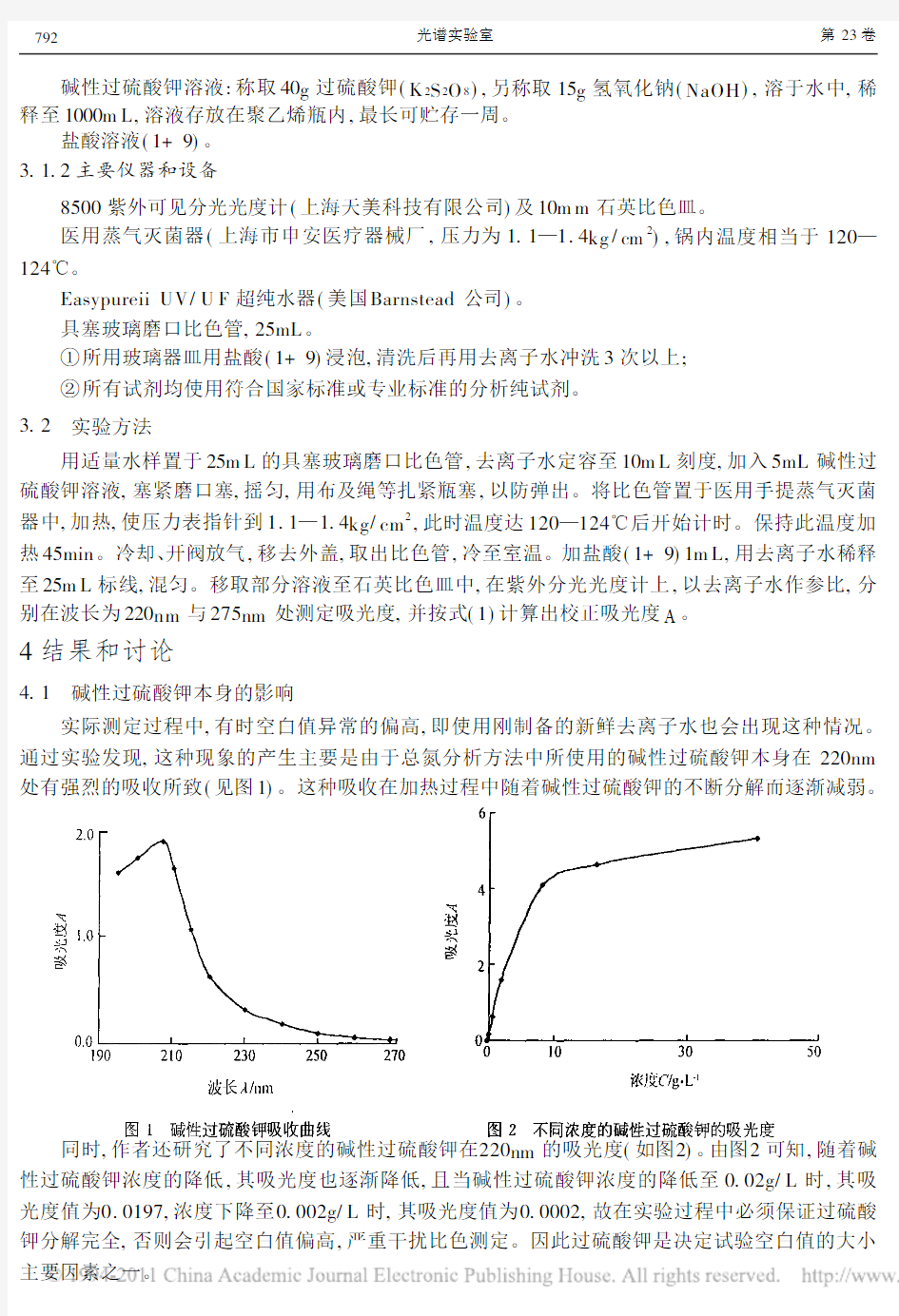
实际测定过程中,有时空白值异常的偏高,即使用刚制备的新鲜去离子水也会出现这种情况。通过实验发现,这种现象的产生主要是由于总氮分析方法中所使用的碱性过硫酸钾本身在220nm 处有强烈的吸收所致(见图1)
。这种吸收在加热过程中随着碱性过硫酸钾的不断分解而逐渐减弱。
同时,作者还研究了不同浓度的碱性过硫酸钾在220nm 的吸光度(如图2)。由图2可知,随着碱性过硫酸钾浓度的降低,其吸光度也逐渐降低,且当碱性过硫酸钾浓度的降低至0.02g/L 时,其吸光度值为0.0197,浓度下降至0.002g/L 时,其吸光度值为0.0002,故在实验过程中必须保证过硫酸钾分解完全,否则会引起空白值偏高,严重干扰比色测定。因此过硫酸钾是决定试验空白值的大小主要因素之一。
792
光谱实验室第23卷
4.2 消解温度和时间对空白的影响
方法[1]和文献[2]规定消解温度控制在120—124℃之间,消解时间为30min ,文献[3]对温度进行了详细研究,结果与国标方法吻合。文献[4,5]对消解时间进行了探讨,结果与国标方法不吻合,本文主要对消解时间进行了研究。 为了进一步了解消解时间对测定结果的影响,取碱性过硫
表1 不同消解时间的试验空白值统计表
消解时间(min)303540455060K 2S 2O 8吸光度
0.4595
0.2679
0.1947
0.1320
0.1289
0.1274
酸钾消解后直接进行测定。作者针对消解时间对空白值的影响进行了试验。通过试验发现随着加热时间的延长,过硫酸钾在220nm 处的吸收逐渐降低,其变化情况见表1。
消解过程是过硫酸钾分解产生原子态氧的过程,时间过短均造成过硫酸钾分解不完全而使试验空白值过大。由表1中可知,当消解时间为30min 时,过硫酸钾的吸光度较高,为0.4595,说明过硫酸钾未分解完全,而当消解时间大于45m in 时,试验空白值趋于稳定,可认为其分解完全。因此实验确定消解时间为45min ,由此保证空白试验值最小和试验结果稳定。4.3 过硫酸钾纯度对空白的影响
在分析测试过程中,选用了两种不同质量的过硫酸钾试剂,均按照操作程序在温度120—124℃下消解45m in ,测定空白值的吸光度,试验结果见表2。
表2 不同纯度过硫酸钾空白值表
试剂平行1平行2平行3厂家10.03040.03050.0289厂家2
0.2322
0.2470
0.2390
厂家1的过硫酸钾,纯度较高,空白值较低,氧化性较强;含有杂质或失效的氧化剂表现为空白值偏高,氧化性偏低。从表中可以看到,高纯度的氧化剂空白值为0.03左右,而低纯度的氧化剂空白值为0.24左右,按照操作程序测定过硫酸钾的空白值,当空白值在0.03左右时,可认为氧化剂的纯度达到要求;当空白值偏高时则认为氧化剂纯度偏低。过硫酸钾试剂的质量直接影响总氮测定的结果。实验时应选用分析纯试剂。曾发现某厂的过硫酸钾其总氮空白吸光值高达1以上,且还发现同一厂家不同批号的过硫酸钾试剂的空白值也相差较大。故对不同厂家的不同批号的过硫酸钾试剂均需进行空白检验,才可投入使用。所以,过硫酸钾试剂的质量对测定的空白影响较大,实验前需严格选择合适的厂家的过硫酸钾试剂。4.4 消解量对空白的影响 为了进一步研究碱性过硫酸钾对测定结果的影响,作者还改变碱性过硫酸钾的量进行了空白试验,试验结果见表3。由表3可知,随着碱性过硫酸钾浓度的增高,
表3 不同消解量对空白值的影响
碱性过硫酸钾量
(mL)空白试验值平行1平行2平行3平行4平均值3
0.02110.02160.02180.02400.022150.02980.03040.03050.03050.030310
0.0550
0.0567
0.0568
0.0597
0.0570
其空白值也相应增大。故在样品测定过程中,应在保证消解完全的前提下,选择尽可能少的碱性过硫酸钾。在实验过程中,如果发现样品浓度较低,可以选择较少量的碱性过硫酸钾进行消解,而对于高浓度的样品应先稀释后再消解,尽量避免选择大量碱性过硫酸钾消解,以免引入较大误差。4.5 消解过程对空白的影响
不仅如此,消解过程也会对K 2S 2O 8的分解产生影响。两组空白样一组按常规方法放入医用灭
793
第4期董纪珍等:测定总氮时影响空白吸光值的因素
菌锅,在室温下加热,至120—124℃处消化45m in后,冷却测定,A220nm为0.0302,A275nm为0.0007;另一组先把灭菌锅水煮沸后,再放样品,在120—124℃处消化45min后,迅速放气取出测定,其A220nm 为0.0931,A275nm为0.0028。而后一组样在继续消解一段时间后,A220nm降为0.0310,A275nm为0.0005。两种方法在120—124℃的消解时间相同,但后一种方法升降温时间短,总消化时间也缩短,结果导致了K2S2O8的分解不完全而影响比色测定,因此不宜采用。
4.6 碱性过硫酸钾存储时间对空白的影响
总氮测定的关键在于用碱性过硫酸钾将水样中的非硝酸盐氮氧化生成硝酸盐(NO-3),测定其吸光度,来推算出总氮含量。碱性过硫酸钾起着最关键的作用,如果存放时间过长,也会影响到测定结果(见表4)。
表4 碱性过硫酸钾存放时间对空白吸光度的影响
存放时间d1d3d5d7d9d11
空白吸光度0.02770.02820.02940.03070.04120.0465
由表4看出,碱性过硫酸钾存放3天对结果基本无影响,存放7天以上就会有较大偏差,故碱性过硫酸钾配置好后不能放置超过7天,最好不超过3天。
4.7 试验用玻璃器皿的洁净度对空白的影响
按照分析操作程序,分别使用普通清洗的玻璃器皿、盐酸(1+9)溶液浸泡24h的玻璃器皿进行空白试验值的测定,测定结果列入表5中。
表5 不同玻璃器皿洁净度的空白试验值统计表
器皿处理方法
空白试验值
平行1平行2平行3平行4平均值RSD
普通清洗0.03530.03660.03470.03600.03560.0353盐酸(1+9)浸泡0.02980.03040.03050.03050.03030.0298
由表6可知,试验用玻璃器皿的洁净程度对空白值的也有一定程度的影响。由于含氮化合物转化为硝酸盐氮是在长时间、高温下的消解过程,因此在消解过程中,玻璃壁上难以清洗的有机物及其他物质混入介质中而使空白试验值偏大。而使用酸浸泡过的玻璃器皿,其空白值低于普通清洗过的玻璃器皿的空白值,且精密度比普通清洗好,因此用酸浸泡玻璃器皿是降低空白试验值的手段之一。同时在实验过程中,也发现玻璃器皿清洗干净后,控干后使用可以进一步降低其空白值,可使空白吸光度值低于0.02。
4.8 蒸馏水的纯度对空白的影响
4.8.1 去离子水纯度
国家标准测定方法要求整个总氮分析过程要使用无氨水,其制备方法可采用酸化蒸馏。现用经过阴阳离子交换树脂处理的去离子
表6 用改进方法检测去离子水的纯度方法平行1平行2平行3平行4平均值
标准方法0.03040.03050.02980.03040.0303改进方法0.02800.03040.02720.02930.0302
水进行空白试验和标样测定,空白吸光值在均在0.03附近,测得标样结果与真值相同,表明去离子水已符合实验用水要求,不必另行制备二次蒸馏水。再者,经过阴、阳离子交换树脂制备的去离子水其中的NO-3、NO-2离子也已去除,故此去离子水符合要求。
为了进一步验证去离子水的纯度,可采用以下方法:不加10mL去离子水,而直接取5mL碱性过硫酸钾,消解后加1m L盐酸,再用去离子水定容至25mL,测吸光度值与标准方法测得的空白值794光谱实验室第23卷
相比较即可验证实验室内去离子水的纯度(如表6所示)。标准方法中总氮空白用10mL 去离子水代替水样测定,碱性过硫酸钾可将其中的非硝酸盐氮氧化生成硝酸盐(NO -3)使空白值偏高。由文献[5]可知,铵在220nm 处并无吸收,只有参加氧化反应生成硝酸盐(NO -
3)才会影响空白的测定结果。由表7数据可知,标准方法测得的空白值与改进的方法测得的空白值基本保持一致,说明此去离子水基本不含有氮类化合物(硝酸盐氮除外),满足实验的要求。如果两种方法测得的空白值相差较大,那就说明此去离子水不符合标准,需重新制备或使用无氨水。4.8.2 去离子水存取时间
为了进一步研究去离子水对总氮测定结果的影响,作者分别用隔夜的去离子水和刚制备的去离子水进行空白试验值的测定,试验结果见表7。由表7可知,刚制备的去离子水的吸光度均比隔夜的去离子水低,实验过程中尽量使用刚制备的去离子水。原因可能由于实验室中氨水、硝酸和其他氨盐等试剂易挥发出氨气,重新溶解到去离子水中,经加热氧化后生成硝酸盐(NO -3)使空白值偏高,因此在实验中应选择刚制备的去离子水。
表7 隔夜的去离子水对总氮空白值的影响
去离子水平行1平行2平行3平行4平均值隔夜的去离子水0.03250.03420.03280.03340.0332刚制备的去离子水
0.0303
0.0306
0.0307
0.0301
0.0304
4.9 实验室环境
实验环境对总氮的测定影响很大。环境对样品的污染,主要是由空气中的污染气体和沉降粒子引起的。普通实验室中每立方米空气中含有数百微克的微粒。这些微粒中含有多种化学元素,可引起多种痕量化学元素的污染。在总氮空白测定中,首先要避免项目的交叉污染。凡是能带入氮的水和试剂都不能在实验室使用,不能与用氨水、硝酸以及其他氨盐类试剂的分析项目安排在一个实验室内,因为它们容易挥发进入空气,可能重新溶解在试样中,使测定结果偏高。其次,实验操作时,所用的器皿如蒸汽锅或压力锅、比色管、纱布等均应清洗干净。特别是做完高浓度样品后,影响更大。压力锅和纱布可用去离子水预先多蒸几次,以降低空白值。要选用磨合性好的管子,加热时用纱布扎紧塞子,以防蹦出,加热完后,检查试液的体积是否正常,否则样品报废。
5 结论
由以上讨论可知,为了降低总氮的空白,应采取如下的措施:
(1)严格按照操作规程的消解方法,保证消解温度在120—124℃之间;为了确保过硫酸钾能分解完全,消解时间由《方法》中的30m in 改为45min;同时要严格控制消解过程;
(2)使用分析纯以上的过硫酸钾试剂,且使用新的过硫酸钾试剂前必须进行空白检验;碱性过硫酸钾配置好后不能放置超过7天,最好不超过3天;
(3)使用盐酸(1+9)浸泡的玻璃器皿,使用刚制备的去离子水或者无氨水清洗,使用前控干;
(4)确保能完全消解的前提下,选择较少量的过硫酸钾试剂;
(5)确保实验室环境的干净、整洁;不能与用氨水、硝酸以及其他氨盐类试剂的分析项目安排在一个实验室内;
此外,实验用的器皿、消解时所用的高压灭菌锅、高压灭菌锅的密封性、紫外可见分光光度计的稳定性,比色时所用的石英比色皿的差异都可能影响总氮的测定值。因此,在实际做实验时要注意以上这些影响因素,避免测定值出现偏差,从而影响到总氮空白值,进而影响最终测定结果。
795
第4期董纪珍等:测定总氮时影响空白吸光值的因素
796光谱实验室第23卷
参考文献
[1]中华人民共和国国家标准.水质-总氮的测定-碱性过硫酸钾消解紫外分光光度法[J].GB11894-89.北京:中国标准出版社,
1989.
[2]国家环境保护总局、《水和废水监测分析方法》编委会编.水和废水监测分析方法[M].(第四版).北京:中国环境科学出版社,
2002.254—257.
[3]祁娟娟,梁晓.过硫酸钾氧化-紫外分光光度法测定水中总氮方法的探讨[J].内蒙古环境保护,2000,12(3):30—32.
[4]徐晓春,黄小红,夏羽兰,张海荣.降低总氮测定空白的方法改进[J].甘肃环境研究与监测,2003,16(1):44,51.
[5]张维东,林峰.对提高水质总氮测定结果准确度的探讨[J].山东环境监测,1998,(4):15—16.
Effective Factors upon the Adsorbance of Blank Tests
in the Determination of the Total Nitrogen
D ONG Ji-Zhen S ONG Ying L I Jian-Po D ING Zhi-Ying
(W ater Quality A nalysis Center,Be i j ing Drainage Gr oup Co.L td.,B eij ing100022,P.R.China)
Abstract Due to the hig her adsorbance of blank solution in the determination of the total nitro gen in the sew age by GB11894-1989,the factors,such as purity of o xidant,the quantity of the dig estio n,the purity of distilled w ater,the time and tem peratur e o f the dig estion,the deposited time of o xidation solutio n,ex perimental environment,etc,w er e analy zed and impr oved.
Key words To tal Nitrog en,Blank T est,Po tassium Persulfate,Ultravio let Spectrophotometry.
27 第13卷 第8期 2011 年 8 月 辽宁中医药大学学报 JOURNAL OF LIAONING UNIVERSITY OF TCM Vol. 13 No. 8 Aug .,2011 复方雄蚕蛾胶囊中总多糖和蛋白质含量测定 耿耘,马超英,李子阳,杨超,罗丽勤 (西南交通大学生命科学与工程学院,四川 成都 610031) 收稿日期:2011-05-18 基金项目:四川省科技厅支撑计划资助项目(2008SZ0141);四川省中医药管理局科技专项资助项目(2008-31)作者简介:耿耘(1959-),女,河北石家庄人,教授,硕士,研究方向:中药药理学。 复方雄蚕蛾胶囊是由雄蚕蛾、枸杞子等3味药食两用中药组成的保健食品,临床应用证明其具有补肾壮阳、改善免疫及抗疲劳等功效,主要用于中老年人阳气亏虚、阴精不足或抗病能力下降、易疲劳等症者。为了有效地控制其质量,我们根据该保健食品中药物组成中的有效成分,采用检测该胶囊中多糖和蛋白质的含量来保证质量。多糖含量测定采用苯酚-硫酸法,蛋白质含量测定采用凯氏定氮法。现报道如下。 1 材 料 UV-265型紫外-可见分光光度计(日本岛津公司);微量定氮蒸馏仪一套(深圳三利仪器);复方雄蚕蛾胶囊(由西南交通大学中药研究所提供,规格0.5g/粒,批号080915);D-无水葡萄糖对照品(中国药品生物制品检定所,批号110833200503)。 2 方法与结果2.1 多糖含量测定 2.1.1 对照品溶液的制备 精密称取105℃干燥至恒重的无水葡萄糖对照品25mg,置250mL 量瓶中,加适量水溶解,稀释至刻 度,摇匀,配制成每毫升中含无水葡萄糖0.1mg 的对照品溶液。 2.1.2 标准曲线的制备 精密量取对照品溶液0.2、0.4、0.6、0.8、1.0mL,分别置具塞试管中,加水至2.0mL,各精密加入5%苯酚溶液1mL,摇匀,迅速精密加入硫酸5mL,摇匀,放置10min,置40℃水浴中保温15min,取出后迅速冷却至室温,以相应的试剂为空白。照紫外分光光度法,在490nm 波长处测定吸收度,以吸收度A 为纵坐标,对照品溶液质量浓度C(g ·L -1)为横坐标,得回归方程:Y=0.0141X+0.1642,r =0.9984,结果表明,无水葡萄糖在0.02~0.1g ·L -1范围内,其质量浓度与吸收度线性关系良好。2.1.3 供试品溶液的制备 取6颗胶囊,将其内容物置于三角瓶中,加蒸馏水溶解并稀释至刻度,摇匀超声待糖全溶后,将杂质过滤,滤液置旋转蒸发仪中蒸发,蒸发完全后用无水乙醇溶解超声溶解充分,滤掉杂质,然后将滤液置旋转蒸发仪中蒸发,再用蒸馏水溶解,溶液移至250mL 摘 要:目的:建立复方雄蚕蛾胶囊质量控制的定性定量方法。方法:总多糖含量测定采用苯酚-硫酸显色 法[1],在490nm 波长处测定吸收度,在0.02~0.1g·L -1范围内,其质量浓度与吸光度线性关系良好(r =0.9984);蛋白质含量测定采用凯氏定氮法[2]。结果:复方雄蚕蛾胶囊中总多糖的平均含量为5.9%,蛋白质平均含量为51.3%。结论:该方法操作简便、快速、灵敏度高和重复性好,可以作为复方雄蚕蛾胶囊的质量控制的定性定量方法。 关键词:复方雄蚕蛾胶囊;总多糖;蛋白质;含量测定 中图分类号:R-322 文献标识码:A 文章编号:1673-842X (2011) 08- 0027- 02Determination of Total Polysaccharides Content and Protein Content in Bombycidae Hung Capsule GENG Yun,MA Chao-ying,LI Zi-yang,YANG Chao,LUO Li-qin (College of Life Science and Engineering of Southwest Jiaotong University,Chengdu 610031,Sichuan,China) Abstract: Objective :To study the quality standard of bombycidae hung capsule. Method :The contents of Total Polysaccharides were determined by phenol-sulfuric method [1] ,the detection wavelength was 490nm,from 0.02~0.1g ·L -1,The Linear Relationship was good between Concentrations and Absorbency of Total Polysaccharides(r =0.9984);The content of Protein were determined by Micro - Kjeldahl method [2]. Result :The average contents of Total Polysaccharides was determined 5.9%,the average content of Proteinin was determined 51.3%,from Bombycidae hung Capsule. Conclusion :The above method for the quantification was proved to have the advantages of simple operation, rapidity, high sensitivity and fine repetition, and it should be helpful for monitoring the quality control methods of Bombycidae hung Capsule. Key words:bombycidae hung capsule;total polysaccharides;protein;determination
蛋白质含量测定方法的比较及肽含量的测定 (一)蛋白质测定方法的比较(原理、优缺点)蛋白质含量测定法,目前包括定氮法、双缩脲法、福林酚法(Lowry 法)和紫 外吸收法、考马斯亮蓝法。其中考马斯亮蓝和福林酚法灵敏度最高,比紫外吸收法灵敏10~20 倍,比双缩脲法灵敏100倍以上。定氮法较复杂,但准确,往往以定氮法测定的蛋白质作为其他方法的标准蛋白质。在选择方法时应该考虑:(1)实验测定要求的灵敏度和精确度;(2)蛋白质的性质;(3)溶液中存在的干扰物质;(4)测定花费时间。蛋白质含量测定法,目前包括定氮法、双缩脲法、福林酚法(Lowry 法)和紫外吸收法、考马斯亮蓝法。其中考马斯亮蓝和福林酚法灵敏度最高,比紫外吸收法灵敏10~20 倍,比双缩脲法灵敏100倍以上。定氮法较复杂,但准确,往往以定氮法测定的蛋白质作为其他方法的标准蛋白质。在选择方法时应该考虑:(1)实验测定要求的灵敏度和精确度;(2)蛋白质的性质;(3)溶液中存在的干扰物质;(4)测定花费时间。 1 微量凯氏定氮法(GB 5009.5-2010) 1.1原理样品与浓硫酸共热。含氮有机物即分解产生氨(消化),氨又与硫酸作用,变成硫酸氨。经强碱碱化使之分解放出氨,借蒸汽将氨蒸至酸液中,根据此酸液被中和的程度可计算得样品之氮含量。 1.2操作方法样品经前处理、炭化、消化、蒸馏、滴定等主要步骤 1.3特点准确度较高,适用于0.2~ I.Omg氮,误差为土2%;操作复杂费时,整个过程需要耗时8~10h,试剂消耗量大。,测得结果为总氮含量,包括蛋白氮和非蛋白氮含 量;适用范围广,几乎所有样品均可用此方法。 2双缩脲比色法
食品中蛋白质含量测定(凯氏定氮法) 一、目的与要求 1、学习凯氏定氮法测定蛋白质的原理。 2、掌握凯氏定氮法的操作技术,包括样品的消化处理、蒸馏、滴定及蛋白质含量计算等。 二、实验原理 蛋白质是含氮的化合物。食品与浓硫酸和催化剂共同加热消化,使蛋白质分解,产生的氨与硫酸结合生成硫酸铵,留在消化液中,然后加碱蒸馏使氨游离,用硼酸吸收后,再用盐酸标准溶液滴定,根据酸的消耗量来乘以蛋白质换算系数,即得蛋白质含量。 因为食品中除蛋白质外,还含有其它含氮物质,所以此蛋白质称为粗蛋白。 三、仪器与试剂 硫酸铜(CuSO4·5H20)硫酸钾硫酸(密度为L)硼酸溶液(20g/L) 氢氧化钠溶液(400g/L)L盐酸标准滴定溶液。 混合指示试剂:%甲基红乙溶液液1份,与%溴甲酚绿乙醇溶液5份临用时混合。 微量定氮蒸馏装置:如图3-所示。 图3-微量凯氏定氮装置 1、电炉; 2、水蒸气发生器(2L平底烧瓶); 3、螺旋夹a; 4、小漏斗及棒状玻璃塞(样品入口处); 5、反应室; 6、反应室外层; 7、橡皮管及螺旋夹b;8、冷凝管;9、蒸馏液接收瓶。 四、实验步骤 1、样品消化 称取样品约(±),移入干燥的100mL凯氏烧瓶中,加入硫酸铜和6g硫酸钾,稍摇匀后瓶口放一小漏斗,加入20mL浓硫酸,将瓶以450角斜支于有小孔的石棉网上,使用万用电炉,在通风橱中加热消化,开始时用低温加热,待内容物全部炭化,泡沫停止后,再升高温度保持微沸,消化至液体呈蓝绿色澄清透明后,继续加热,取下放冷,小心加20mL水,放冷后,无损地转移到100mL容量瓶中,加水定容至刻度,混匀备用,即为消化液。 试剂空白实验:取与样品消化相同的硫酸铜、硫酸钾、浓硫酸,按以上同样方法进行消化,冷却,加水定容至100mL,得试剂空白消化液。 2、定氮装置的检查与洗涤
蛋白质各种定量方法的优缺点的比较 1.蛋白质的常规检测方法 1.1 凯氏(Kjeldahl)定氮法 一种最经典的蛋白质检测方法。 原理:样品中含氮有机化合物与浓硫酸在催化剂作用下共热消化,含氮有机物分解产生氨,氨又与硫酸作用变成硫酸铵。然后加碱蒸馏放出氨,氨用过量的硼酸溶液吸收,再用盐酸标准溶液滴定求出总氮量换算为蛋白质含量。 优点:范围广泛、测定结果准确、重现性好 缺点:操作复杂费时、试剂消耗量大 1.2 双缩脲法 常用于需要快速但并不需要十分精确的蛋白质检测。 原理:双缩脲(NH3CONHCONH3)是3 分子的脲经180℃左右加热,放出1分子氨后得到的产物。在强碱性溶液中,双缩脲与硫酸铜形成紫色络合物(肽键中的氮原子和铜离子配价结合),称为双缩脲反应。紫色络合物颜色的深浅与蛋白质浓度成正比,因此可用来测定蛋白质含量。 测定范围:1~10mg(有的文献记载为1~20mg) 优点:较快速,干扰物质少,不同蛋白质产生的颜色深浅相近 缺点:①灵敏度差; ②三羟甲基氨基甲烷、一些氨基酸和EDTA等会干扰该反应。 1.3 Folin-酚试剂法 原理:Folin-酚法的原理与双缩脲法大体相同,利用蛋白质中的肽键与铜结合产生双缩脲反应。 同时也由于Folin-酚试剂中的磷钼酸-磷钨酸试剂被蛋白质中的酪氨酸和苯丙氨酸残基还原,产生深蓝色的钼蓝和钨蓝的混合物。在一定的条件下,蓝色深度与蛋白的量成正比,由此可测定蛋白质的含量。 测定范围:20~250ug 优点:灵敏度高,对水溶性蛋白质含量的测定很有效 缺点:①费时,要精确控制操作时间; ②Folin -酚法试剂的配制比较繁琐,且酚类和柠檬酸、硫酸铵、Tris缓冲液、甘氨酸、 糖类、甘油、还原剂(二硫代苏糖醇、巯基乙醇)、EDTA和脲素均会干扰反应。
FSPTWPJY003 酱油 氨基酸态氮的测定 中和滴定法 F_SP _TWP_JY _003 酱油—氨基酸态氮的测定—中和滴定法 1 范围 本方法采用滴定法测定酱油中氨基酸态氮的含量。 本方法适用于各种类型酱油中氨基酸态氮含量的测定。以g/100mL 报告其结果,测定值保留两位小数。 2 原理 利用氨基酸的两性作用,加入甲醛以固定氨基的碱性,使羧基显示出酸性,用氢氧化钠标准溶液滴定后定量,以酸度计测定终点。 3 试剂 3.1 甲醛溶液,体积百分数为37~40。 3.2 氢氧化钠标准溶液,c (NaOH)=0.1mol/L 3.2.1 配制 将氢氧化钠配成饱和溶液,注入塑料瓶(或桶)中,封闭放置至溶液清亮,使用前虹吸上层清液。量取5mL 氢氧化钠饱和溶液,注入1000mL 不含二氧化碳的水中,混匀。 3.2.2 标定 称取0.6g 于105~110℃烘至恒量的基准邻苯二甲酸氢钾,精确至0.0001g 。溶于50mL 不含二氧化碳的水中,加入2滴酚酞指示剂溶液,以新制备的氢氧化钠标准溶液滴定至溶液呈微红色为其终点。同时做空白试验。 3.2.3 计算 按下式计算氢氧化钠标准溶液的浓度: C =2042 .0)(1×?V V m 式中:C —氢氧化钠标准溶液浓度,mol/L ; m —基准邻苯二甲酸氢钾的质量,g ; V —滴定时所消耗氢氧化钠溶液的体积,mL ; V 1 —空白试验消耗氢氧化钠溶液的体积,mL ; 0.2042—与1.00mL 氢氧化钠标准溶液[c (NaOH)=1.000mol/L]相当的,以克表示的 邻苯二甲酸氢钾的质量。 3.3 氢氧化钠标准滴定溶液,c (NaOH)=0.05mol/L 将配制的0.1mol/L 氢氧化钠标准溶液准确稀释一倍。 4 仪器 4.1 分析天平,感量0.1mg 。 4.2 酸度计,附磁力搅拌器; 4.3 碱式滴定管,25mL 。 5 操作步骤 5.1 仪器校准 按仪器使用说明书校正pH 计,并注意校正温度使其与测定时保持一致。 将玻璃电极和甘汞电极事先用pH 9.22标准缓冲溶液校准。 5.2 样品的测定 吸取酱油样品5.0mL 置于100mL 容量瓶中,加水至刻度,混匀后吸取20.0mL ,置于200mL 烧杯中,加水60mL ,插入玻璃电极和甘汞电极,开动磁力搅拌器,用氢氧化钠标准滴定溶液
蛋白质的测定方法比较 一、分光光度法 1、测定原理: 食品中的蛋白质在催化加热条件下被分解,分解产生的氨与硫酸结合生成硫酸铵,在pH 4.8 的乙酸钠-乙酸缓冲溶液中与乙酰丙酮和甲醛反应生成黄色的3,5-二乙酰-2,6-二甲基-1,4-二氢化吡啶化合物。在波长400 nm 下测定吸光度值,与标准系列比较定量,结果乘以换算系数,即为蛋白质含量。 2、测定步骤: ①试样消解:称取经粉碎混匀过40目筛的固体试样0.1g~0.5g(精确0.001g)、半固体试样0.2g~1g(精确至0.001g)或液体试样1g~5g(精确0.001g),移入干燥的100 mL 或250 mL 定氮瓶中,加入0.1 g硫酸铜、1 g 硫酸钾及5 mL 硫酸,摇匀后于瓶口放一小漏斗,将定氮瓶以45°角斜支于有小孔的石棉网上。缓慢加热,待内容物全部炭化,泡沫完全停止后,加强火力,并保持瓶内液体微沸,至液体呈蓝绿色澄清透明后,再继续加热半小时。取下放冷,慢慢加入20 mL 水,放冷后移入50 mL 或100 mL容量瓶中,并用少量水洗定氮瓶,洗液并入容量瓶中,再加水至刻度,混匀备用。按同一方法做试剂空白试验。 ②试样溶液的制备:吸取2.00 mL~5.00 mL 试样或试剂空白消化液于50 mL 或100 mL 容量瓶内,加1 滴~2 滴对硝基苯酚指示剂溶液,摇匀后滴加氢氧化钠溶液中和至黄色,再滴加乙酸溶液至溶液无色,用水稀释至刻度,混匀。 ③标准曲线的绘制:吸取0.00 mL、0.05 mL、0.10 mL、0.20 mL、0.40 mL、0.60 mL、0.80 mL 和1.00 mL 氨氮标准使用溶液(相当于0.00μg、5.00μg、10.0μg 、20.0μg、40.0μg、60.0μg、80.0μg 和100.0μg 氮),分别置于10 mL 比色管中。加4.0 mL 乙酸钠-乙酸缓冲溶液及4.0 mL 显色剂,加水稀释至刻度,混匀。置于100 ℃水浴中加热15 min。取出用水冷却至室温后,移入1 cm 比色杯内,以零管为参比,于波长400 nm 处测量吸光度值,根据标准各点吸光度值绘制标准曲线或计算线性回归方程。 ④试样测定:吸取0.50 mL~2.00 mL(约相当于氮<100μg)试样溶液和同量的试剂空白溶液,分别于10 mL 比色管中。以下按上述中“加4 mL 乙酸钠-乙酸
凯氏定氮法测定粗纤维素中蛋白质含量 1、原理 蛋白质是含氮的有机化合物。蛋白质与硫酸和催化剂一同加热消化,使蛋白质分解,分解的氨与硫酸结合生成硫酸铵。然后碱化蒸馏使氨游离,用硼酸吸收后再以硫酸或盐酸标准溶液滴定,根据酸的消耗量乘以换算系数,蛋白质含量。 2、试剂 所有试剂均用不含氨的蒸馏水配制。 2.1 硫酸铜。 2.2 硫酸钾。 2.3 硫酸。 2.4 2%硼酸溶液。 2.5 混合指示液:1份0.1%甲基红乙醇溶液与5份0.1%溴甲酚绿乙醇溶液临用时混合。也可用2份0.1%甲基红乙醇溶液与1份0.1%次甲基蓝乙醇溶液临用时混合。 2.6 30%氢氧化钠溶液。 2.7 0.025mol/L硫酸标准溶液或0.05mol/L盐酸标准溶液。 3、仪器 安全管导管汽水分离管样品入口塞子冷凝管吸收瓶隔热液套反应管蒸汽发生瓶 如图1所示:
图1 3、操作步骤 3.1样品处理:精密称取0.2-2.0g固体样品或2-5g半固体样品或吸取10-20ml液体样品(约相当氮30-40mg),移入干燥的100ml或500ml定氮瓶中,加入0.2g硫酸铜,6g硫酸钾及20毫升硫酸,稍摇匀后于瓶口放一小漏斗,将瓶以45度角斜支于有小孔的石棉网上,小火加热,待内容物全部炭化,泡沫完全停止后,加强火力,并保持瓶内液体微沸,至液体呈蓝绿色澄清透明后,再继续加热0.5小时。取下放冷,小心加20ml水,放冷后,移入100ml 容量瓶中,并用少量水洗定氮瓶,洗液并入容量瓶中,再加水至刻度,混匀备用。取与处理样品相同量的硫酸铜、硫酸钾、浓硫酸同一方法做试剂空白试验。但是此法比较危险,不易在实验室演示,现在大多数实验室有消煮仪一次可以进行多个(一次可以消煮16个样品)样品处理,并有通风橱进行通风,温度可以自己设定,更加安全和可操作性,因此逐步成为主要的凯氏定氮法的首选处理方法。 一般消解温度都设在240度及240度以上,如果想快速消解可以适当提高温度甚至可以用最大温度进行消解。 3.2、按图装好定氮装置,于水蒸气发生器内装水约2/3处加甲基红指示剂数滴及数毫升硫酸,以保持水呈酸性,加入数粒玻璃珠以防暴沸,用调压器控制,加热煮沸水蒸气发生瓶内的水。 3.3、向接收瓶内加入10ml 2%硼酸溶液及混合指示剂1滴,并使冷凝管的下端插入液面下,吸取10.0ml样品消化液由小玻璃杯流入反应室,并以10ml水洗涤小烧杯使流入反应室内,塞紧小玻璃杯的棒状玻璃塞。将10ml 40%氢氧化钠溶液倒入小玻璃杯,提起玻璃塞使其缓慢流入反应室,不能立即将玻璃盖塞紧,这样易使玻璃塞粘在进样口,应先用蒸馏水冲洗然后再盖,并加水于小玻璃杯以防漏气。夹紧螺旋夹,开始蒸馏,蒸气通入反应室使氨通过冷凝管而进入接收瓶内,蒸馏5min。移动接收瓶,使冷凝管下端离开液皿,再蒸馏1min,然后用少量水冲洗冷凝管下端外部。取下接收瓶,以0.05N硫酸或0.05N盐酸标准溶液定至灰色或蓝紫色为终点。 同时吸取10.0ml试剂空白消化液按3操作。 4、计算 X =((V1-V2)*N*0.014)/( m*(10/100)) *F*100%
一、硫酸苯酚法测多糖含量 1、试剂配制 ①浓硫酸:分析纯,95.5% ②80%苯酚:80克苯酚(分析纯重蒸馏试剂)加20克水使之溶解,可置冰箱中避光长期储存。6%苯酚:临用前以80%苯酚配制。(每次测定均需现配) ③5%苯酚:取苯酚100 g,加铝片0. 1 g和碳酸钠0. 05 g,常压蒸馏,收集182℃馏分。称取 该馏分(100%苯酚)5 g,置100 ml容量瓶中,加蒸馏水至刻度,摇匀后,置棕色试剂瓶中, 冰箱中冷藏储存备用。 ④标准葡聚糖(Dextran,瑞典Pharmacia)或分析纯葡萄糖。准确称取20m g经105℃干 燥至恒重的葡萄糖标准品于500ml容量瓶中,蒸馏水溶解定容。 2、制作标准曲线 准确称取标准葡聚糖(或葡萄糖)20mg于500ml容量瓶中,加水至刻度,分别吸取0.2、0.3、0.4、0.5、0.6、0.7、0.8及0.9ml,各以蒸馏水补至1.0ml,然后加入6%(5%,9%)苯 酚0.5ml及浓硫酸5.0ml,摇匀冷却,室温放置20min以后于490nm测光密度,以2.0ml水按同 样显色操作为空白,横坐标为多糖微克数,纵坐标为光密度值,得标准曲线。 1 2 3 4 5 6 7 8 0 标准葡萄糖溶液(mL)0.2 0.3 0.4 0.5 0.6 0.7 0.8 0.9 0 蒸馏水(mL)0.8 0.7 0.6 0.5 0.4 0.3 0.2 0.1 1.0 6%苯酚(mL)0.5 0.5 0.5 0.5 0.5 0.5 0.5 0.5 0.5 浓硫酸(mL) 2.5 2.5 2.5 2.5 2.5 2.5 2.5 2.5 2.5 3 注意事项 (1)此法简单、快速、灵敏、重复性好,对每种糖仅制作一条标准曲线,颜色持久。(2)制作标准线宜用相应的标准多糖,如用葡萄糖,应以校正系数0.9校正μg数。
酱油中氨基酸态氮含量的测定 摘要:本次实验用甲醛值法来测定酱油中氨基酸态氮的含量,甲醛值法滴定的终点容易判断。 关键词:酱油氨基酸态氮空白实验 前言:酱油是中国传统的调味品。主要由大豆、小麦、食盐经过制油、发酵等程序酿制而成的,色泽红褐色,有独特酱香,滋味鲜美。酱油的鲜味和营养价值取决于氨基酸态氮含量的高低,一般来说氨基酸态氮越高,酱油的等级就越高,也就是说品质越好。按照我国酿造酱油的标准,配制酱油每100ml中氨基酸态氮含量应≥0.4g 实验目的:1.掌握氨基酸态氮的测定原理2.了解酸碱滴定法在食品分析中的应用和学会判断有色溶液终点确定的方法 实验原理:氨基酸有氨基及羧基两种基团,具有酸碱两性,他们相互作用形成中性的内盐。加入甲醛溶液,氨基与甲醛作用,碱性消失,使羧基的酸性显现出来,用氢氧化钠标准溶液进行中和滴定,根据滴定用的氢氧化钠标准溶液的体积可计算出氨基酸态氮的含量。甲醛与氨基酸的反应如下: 实验仪器和药品:酸度计,电磁搅拌器,100ml容量瓶,5ml、20ml移液管,10ml 酸式滴定管,100ml量筒,100ml烧杯,250ml烧杯,NaOH固体(A.R.),邻苯二甲酸氢钾(A.R.),酚酞指示剂,分析天平,洗耳球,500ml橡胶或软木塞细口试剂瓶,250ml
锥形瓶(3个),50ml碱式滴定管,铁架台,酒精灯,石棉网,滴定管,温度计,玻璃棒,甲醛溶液w=36%,标准缓冲溶液(pH=6.86和pH=9.18),酱油,蒸馏水 1.0.05mol/LNaOH溶液的粗配:用天平迅速称量约0.6g固体NaOH放到烧杯中,用适量的新制的蒸馏水溶解稀释至300ml,盛于带橡胶塞或软木塞的试剂瓶中。 2.NaOH溶液的标定:用直接称量法准确称取邻苯二甲酸氢钾1.0~1.1g(称准至0.1mg)于洁净的250ml烧杯中,加入20~30ml蒸馏水,温热使之溶解,冷却至室温,定量转移定容于100ml容量瓶中,用移液管移取20ml于250ml锥形瓶中,加酚酞指示剂2滴,用NaOH溶液滴定至溶液呈现粉红色,30s内不褪色为终点,平行滴定3次。 酸度计的准备:酸度计先开机预热30分钟,将开关拨至PH位置,按“温度”键,调到室温,30分钟后,将电极插入PH=6.86的缓冲溶液中,调“定位”,用蒸馏水清洗并用纸吸干,再将电极插入PH=9.18的溶液中,调“斜率”,用蒸馏水清洗并吸干实验操作步骤:1. 准确吸取酱油5.0ml置于100ml容量瓶中,加水至刻度,摇匀后吸取20.0ml置于100ml烧杯中,加水60ml,插入酸度计,开动磁力搅拌器,用配好的NaOH标准溶液滴定酸度计指示pH=8.2,记录消耗氢氧化钠标准溶液的体积V(ml)2. 向上述溶液中准确加入甲醛溶液10.0ml,摇匀,继续用NaOH标准溶液滴定至pH=9.2,记录消耗氢氧化钠标准溶液的体积(ml),供计算氨基酸态氮含量用。3. 试剂空白试验:取蒸馏水80ml置于另一200ml洁净烧杯中,先用的氢氧化钠标准溶液滴定至pH=8.2,再加入10.0ml甲醛溶液,继续用NaOH标准溶液滴定酸度计指示pH=9.2,第二次所用的氢氧化钠标准溶液的体积V0为测定氨基酸态氮的试剂空白试验。 结果与计算: (V-V0)C×0.014×V2 X= ×100 1000×V3×V1 V——测定用的样品稀释液加入甲醛后消耗氢氧化钠标准溶液的体积,ml; V1——样品稀释液取用量,ml
蛋白质含量测定主要有五种方法,分别是凯式定氮法、双缩脲法、紫外吸收法、酚试剂法和考马斯亮蓝法。这五种方法各有特点,优缺点明确。 凯氏定氮法 蛋白质是含氮的化合物。食品与浓硫酸和催化剂共同加热消化,使蛋白质分解,产生的氨与硫酸结合生成硫酸铵,留在消化液中,然后加碱蒸馏使氨游离,用硼酸吸收后,再用盐酸标准溶液滴定,根据酸的消耗量来乘以蛋白质换算系数,即得蛋白质含量。因为食品中除蛋白质外,还含有其它含氮物质,所以此蛋白质称为粗蛋白。 优点:重现性好,是目前分析有机化合物含氮量常用的方法,是一种蛋白质测定的经典方法, ,测试结果准确。 缺点:操作比较繁复,费时,试剂消耗量大。且此法测定的蛋白质含量实际上包括了核酸,生物碱,含氮类脂,卟啉,含氮色素等非蛋白质含氮化合物。双缩脲定氮法 双缩脲(NH3CONHCONH3)是两个分子脲经180℃左右加热,放出一个分子氨后得到的产物。在强碱性溶液中,双缩脲与CuSO4形成紫色络合物,称为双缩脲反应。凡具有两个酰胺基或两个直接连接的肽键,或能过一个中间碳原子相连的肽键,这类化合物都有双缩脲反应。紫色络合物颜色的深浅与蛋白质浓度成正比,而与蛋白质分子量及氨基酸成分无关,故可用来测定蛋白质含量。测定范围为1~10mg蛋白质。干扰这一测定的物质主要有:硫酸铵、Tris缓冲液和某些氨基酸等。 优点:较快速,不同的蛋白质产生颜色的深浅相近,以及干扰物质少。主要的缺点是灵敏度差。因此双缩脲法常用于需要快速,但并不需要十分精确的蛋
白质测定。 缺点:不太灵敏;不同蛋白质显色相似。 紫外吸收定氮法 双缩脲法是传统的分光光度法测定蛋白质的方法,当含有两个或者两个以上肽键的物质和碱性的硫酸铜反应时,形成紫色的络合物,这个颜色产物是肽键中的氮原子和铜离子配价结合的结果。蛋白质分子中,酪氨酸、苯丙氨酸和色氨酸残基的苯环含有共轭双键,使蛋白质具有吸收紫外光的性质。形成颜色产物的量取决于蛋白质的浓度。实际测定时,必须预先用标准蛋白质溶液制作一个标准校正曲线,通常用牛血清白蛋白水溶液做蛋白质标准溶液。不同浓度的标准蛋白质溶液加入双缩脲试剂后,反应生成的颜色产物用紫外-可见分光光度计在540nm 波长下测定吸光度,以双缩脲试剂加缓冲或水作空白对照。然后将测得的值分别对蛋白浓度(mg/ ml) 作图,得标准曲线。未知蛋白样品用双缩脲试剂做同样处理,根据测得吸光度值在标准曲线上直接查得未知蛋白质样品中得蛋白质浓度。 优点:对各种蛋白质呈色基本相同;特异性和准确度好,精密度好;呈色稳定性好,试剂单一,方法简便。快速,不消耗样品,测定后仍能回收使用。 缺点:准确度较差,干扰物质多,在用标准曲线法测定蛋白质含量时,对那些与标准蛋白质中酪氨酸和色氨酸含量差异大的蛋白质,有一定的误差。故该法适于用测定与标准蛋白质氨基酸组成相似的蛋白质。若样品中含有嘌呤、嘧啶及核酸等吸收紫外光的物质,会出现较大的干扰。核酸的干扰可以通过查校正表,再进行计算的方法,加以适当的校正。但是因为不同的蛋白质和核酸的紫外吸收是不相同的,虽然经过校正,测定的结果还是存在一定的误差。此外,进行紫外
凯氏定氮法测定蛋白质的原理及其消化、蒸馏 以凯氏定氮法测定氮含量换算蛋白质的方法,是国际上通用的标准方法,操作简单,测定结果重复性和重现性都很好,广泛用于各种食品、谷物、饲料等样品的蛋白质含量测定。此法又分为常量、半微量、微量法三种。国家标准规定为半微量凯氏定氮法。其测定原理相同,主要区别在于常量法的样品及试剂用量较微量法多。而微量法则具有实验规模小,实验费用低的优点。但微量法的准确度和精密度比常量法要差一些。凯氏定氮法整个测定过程分为消解、蒸馏、滴定三步。凯式定氮法包括消化炉和蒸馏装置,它们的结合能够让实验尽可能的简单。 要使测定结果有更好的正确度、准确度和精准度,认真细致掌握测定的每个步骤、各个细节及相应的注意事项,就显得尤为重要。 实验过程操作 1、主要试剂的配制 40%氢氧化钠:化学纯400g氢氧化钠溶于1000ml无氨蒸馏水中。 2%硼酸:分析纯20g硼酸溶于1000ml无氨蒸馏水中。
0.05mol/L盐酸:分析纯4.2ml盐酸定容至1000ml,通过无水碳酸钠标定。 混合指示剂:把溶解于95%乙醇的0.l%溴甲酚绿溶液5份和溶于95%乙醇的0.l% 甲基红溶液1份混合而成. 2、实验过程注意事项 (1)样品应是均匀的。固体样品应预先研细混匀,液体样品应振摇或搅拌均匀。 固体样品一般取样范围为0.20g~2.00g;半固体试样一般取样范围为 2.00g~5.00g;液体样品取样10.0mL~25.0mL(约相当氮30mg~40mg)。若检测液体样品,结果以g/100mL表示。 样品应是均匀的。固体样品应预先研细混匀,液体样品应振摇或搅拌均匀。 (2)样品放入定氮瓶内时,不要沾附颈上。万一沾附可用少量水冲下,以免被检样消化不完全,结果偏低,或者用滤纸包裹好一起投入消化,滤纸影响通过空白扣除。消化时应注意旋转凯氏烧瓶,将附在瓶壁上的碳粒冲下,对样品彻底消化。若样品不易消化至澄清透明,可将凯氏烧瓶中溶液冷却,加入数滴过氧化氢后,再继续加热消化至完全。 (3)消化时,不要用强火。若样品含糖高或含脂及较多时,注意控制加热温度,以免大量泡沫喷出凯氏烧瓶,造成样品
第九章多糖的测定 第一节淀粉的测定 ●一、测定淀粉含量对于决定用途具有重要意义: ●1、淀粉是供给人体热量的主要来源。 ●2、淀粉在食品中的作用是作为增稠剂、胶体生成剂、保潮剂、乳化剂、粘合剂等。 ●二、淀粉的测定方法: ●(一)淀粉的物理检验法:淀粉因其品种不同,淀粉的大小和形状也不同。用显微 镜分析法可鉴别不同品种的淀粉。 ●(二)淀粉含量的测定方法: ●1、酶水解法: ●(1)概念:淀粉用麦芽淀粉酶水解成二糖,再用酸将二糖水解为单糖,然后测定由 水解所得到的单糖。(还原糖) ●(2)常用于液化的淀粉酶是麦芽淀粉酶。它是?—淀粉酶和?—淀粉酶的混合物。 ●(3)酸直接水解法:淀粉的测定方法也可采用酸直接水解法,但酸水解法不仅是淀 粉水解,而且也能分解半纤维素,结果产生了具有还原力的木糖、阿拉伯糖等单糖,使淀粉测定所得的结果较实际含量偏高。 ●(4)酶水解法的优点:在一定条件下,用?—淀粉酶处理样品,则能使淀粉与半纤 维素等某些多糖分开来。因为?—淀粉酶具有严格的选择性,它只使淀粉液化变成低分子糊精和可溶性糖分,而对半纤维素不起作用。在用?—淀粉酶液化淀粉除去半纤维素等不溶性残留物后,再用酸水解使生成葡萄糖,所得结果比较准确。这种酶水解作用,叫作选择性水解。 ●(5)酶水解法测定淀粉的具体步骤: ●a:样品的处理:将磨碎样品置漏斗中,用乙醚50ml分数次洗涤,除去脂肪,再用10% 乙醇洗去可溶性糖分,先5次。 ●b:酶水解:将滤纸上残留物用水移至烧杯内,水浴加热直到淀粉糊化。冷却至60℃, 加麦芽汁20ml在60℃保温1小时,再重复加热冷却,保温冷却过滤,将滤液定容250ml。 ●c:酸水解,吸取滤液加入1:4硫酸,放在120—130℃油浴中保持沸腾5—6min用 40%NaOH 滴定至碱性。 ●d:用非林氏试剂测定葡萄糖含量,同时做空白试验。 ●e:计算:淀粉=[(A-B)*0.9*100]/[W*(50/250)*(V/100)*100] A:样品中淀粉相当于还原糖重量(mg) B:空白相当于还原糖的重量0.9:还原糖换算为淀粉因数 V/100:样液酸解后稀释100ml取Vml W:样品重量(g) 第二节纤维的测定 ●植物性食品内含有粗纤维,它集中存在于谷类的麸、糠、果蔬的表皮及其纤维样组 织之中。从现代营养学的观点来看,我们膳食中每天需要摄入一定数量的纤维(称为膳食纤维),它可防止包括阑尾炎、心脏病和结肠癌等多种疾病,所以,深入了解膳食纤维的特性及其分析方法更具有迫切的现实意义。此外,粗纤维的含量是果蔬制品的一项质量指标,借此可以鉴定果蔬的鲜嫩度。例如:青豌豆按其鲜嫩程度分为三级,其粗纤维含量分别为:一级1.8%左右,二级2.2%左右,三级2.5%左右。 ●一、概念: ●粗纤维:指动物饲料中那些对稀酸、稀碱难溶的,家畜(特别是反刍动物)不容易
前言 中国的酱油在国际上享有极高的声誊。三千多年前,我们的祖先就会酿造酱油了。最早的酱油是用牛、羊、鹿和鱼虾肉等动物性蛋白质酿制的,后来才逐渐改用豆类和谷物的植物性蛋白质酿制酱油用豆、麦、麸皮酿造的液体调味品。色泽红褐色,有独特酱香,滋味鲜美,有助于促进食欲。是中国的传统调味品。酿造酱油又可分为生抽和老抽:生抽——以优质黄豆和面粉为原料,经发酵成熟后提取而成。“色泽淡雅,酯香、酱香浓郁,味道鲜美。老抽——是在生抽中加入焦糖,经过特别工艺制成的浓色酱油,适用于红烧肉、烧卤食品及烹调深色菜肴。色泽浓郁,具有醋香和酱香。此次试验主要测定普通酱油、生抽、老抽中氨基酸态氮的含量。氨基态氮是酱油的营养指标,是酿造酱油中大都蛋白水解率高低的特征性指标,是酱油的质量指标,是酱油中氨基酸含量的特征指标,含量越高酱油的鲜味越强,质量越好。配制酱油(SB 10336-2000)每100ml 中氨基酸态氮含量应≥0.4g 【本任务应掌握知识点及技能】 【实验目的】 ⒈学习及掌握电位滴定法测氨基酸态氮的基本原理及操作要点。 ⒉会电位滴定法的基本操作技能。 【实验原理】 氨基酸含有羧基和氨基,利用氨基酸的两性作用,加入甲醛固定氨基的碱性,使羧基显示出酸性,用氢氧化钠标准溶液滴定后进行测量,以酸度计测定终点。此反应的化学方程式为: COOHRCHCNH OH NHCH RCH HCOH COOH NH RCH )()(22=+
O H OH NHCH RCH NaOH COOH OH NHCH RCH 222)()(+=+ PH=7.0是溶液中游离氢离子与氢氧化钠标准溶液完全反应后的PH 值,即有效酸度 PH=8.2是溶液中除有效酸度以外的物质与氢氧化钠标准溶液完全反应后的PH 值,即总酸 PH=9.2是溶液中氨基态氮中的羧基与氢氧化钠标准溶液完全反应后的PH 值 本实验用的是PH 为8.2和9.2数据。由于酱油还含有总酸度,即使不测定总酸度,也有将总酸中和。用PH=8.2时氢氧化钠消耗的体积与PH=9.2时氢氧化钠消耗的体积 的差计算出样品中氨基态氮含量。 【仪器和试剂】 1.仪器 酸度计PHS-3C 型、磁力搅拌器JB-1A 、碱式滴定管(50ml )、容量瓶(250ml ) 2.试剂 0.04515mol/L 氢氧化钠标准溶液、(1+1)甲醛溶液 【实验步骤】 氢氧化钠溶液的配制:称取0.5014g 氢氧化钠试剂溶解,稀释后定容于250ml 容量瓶中。 氢氧化钠溶液的标定:称取邻苯二甲酸氢钾2.5530g ,溶解,稀释后定容于250ml 容量瓶中。首先用25ml 移液管移取氢氧化钠溶液放入锥形瓶中,加入三滴酚酞指示剂,用邻苯二甲酸氢钾溶液滴定氢氧化钠溶液,溶液由红变为无色为滴定终点,计录用去邻苯二甲酸氢钾的体积,重复三次。 准确吸取酱油5.0ml 置于100ml 容量瓶中,加水至刻度,混匀后吸取20.0ml ,置于200ml 烧杯中,加水60ml ,插入酸度计复合电极,开动磁力搅拌器,用0.04515mol/L 氢氧化钠标准溶液滴定至酸度计指示PH=8.2,记录氢氧化钠标准溶液的体积(按总酸计算公式,可以算出酱油的总酸含量)。 向上述溶液中,准确加入(1+1)甲醛溶液20ml ,混匀。继续用0.04514mol/L 氢氧化钠标准溶液滴定至PH=9.2,计入用去氢氧化钠标准溶液的体积,供计算氨基酸态氮含量用。 试剂空白试验:取水80 ml ,先用0.04514mol/L 氢氧化钠标准溶液滴定至PH=8.2(记录用去氢氧化钠标准溶液的体积,此为测总酸的试剂空白试验)。再加入20ml 甲醛溶液,继续用0.04514mol/L 氢氧化钠标准溶液滴定至酸度计指示PH=9.2。第二次所用氢氧化钠标准溶液的体积为测定氨基酸态氮的试剂空白试验。 2.结果计算 ()100100 50141.03 21????-=V C V V ρ 式中 ρ—样品中氨基酸态氮的含量,g/100 ml; V 1—测定用的样品稀释液加入甲醛后消耗氢氧化钠 标准溶液的体积,
几种蛋白质含量测定方法的比较 【摘要】:蛋白质含量测定方法,是生物化学研究中最常用、最基本的分析之一。目前常 用的方法有凯氏定氮法、双缩脲法(Biuret)、紫外吸收法、考马斯亮蓝法(Bradford),Folin —酚试剂法(Lowry)杜马斯燃烧法。其中Bradford 法灵敏度颇高,比紫外吸收法灵敏10~20 倍,比Biuret法灵敏100 倍以上。凯氏定氮法虽然比较复杂,但较准确,往往以定氮法测定的蛋白质作为其他方法的标准蛋白质。过去Folin—酚试剂法法是应用最广泛的一种方法,由于其试剂乙的配制较为困难(现在已可以在本公司订购),近年来逐渐被考马斯亮兰法所取代。测定农产品中全氮的凯氏定氮法在许多国家已被杜马斯然烧定氮法所代替,杜马斯燃烧法是基于在高温下(大约 900 ℃),通过控制进氧量、氧化消解样品的原理而进行氮测定的。这6种方法并不能在任何条件下适用于任何形式的蛋白质,每种方法都有其优缺点,在选择方法时应考虑:⑴实验对测定所要求的灵敏度和精确度;⑵蛋白质的性质;⑶溶液中存在的干扰物质;⑷测定所要花费的时间 【关键词】:凯氏定氮法双缩脲法紫外吸收法考马斯亮蓝法 Folin—酚试剂法杜马斯燃烧法 一、凯氏定氮法 1.1原理 凯氏定氮法测定蛋白质分为样品消化、蒸馏、吸收和滴定4 个过程。其原理是样品中含氮有机化合物与浓硫酸在催化剂作用下共热消化,含氮有机物分解产生氨,氨又与硫酸作用,变成硫酸铵。然后加碱蒸馏放出氨, 氨用过量的硼酸溶液吸收,再用盐酸标准溶液滴定求出总氮量换算为蛋白质含量。 1.2特点 凯氏定氮法是目前分析有机化合物含氮量常用的方法,是测定试样中总有机氮最准确和最简单的方法之一,被国际国内作为法定的标准检验方法。凯氏定氮法样品的最佳消化条件为硫酸铜2.50 g, 硫酸钾0.10 g,浓硫酸4.00 mL;硫酸铜的用量为影响消化时间的主要因素,硫酸钾和浓硫酸用量为第二和第三主要因素;用此最佳条件做实验, 消化时间仅为12 min;与其他硫酸铜、硫酸钾、浓硫酸用量方法对比,该法所需消化时间最短,试剂用量减少,可降低实验成本,也降低了对环境的污染。 凯氏定氮法适用范围广泛,测定结果准确,重现性好,但操作复杂费时,试剂消耗量大。若采用模块式消化炉代替传统的消化装置, 可同时测定几份样品,节省时间,提高了工作效率,适用于批量蛋白质的测定,具有准确、快速、简便、低耗、稳定的优点。 二、双缩脲法(Biuret ) 2.1原理 双缩脲(NH3CONHCONH3)是两个分子脲经180 ℃左右加热,放出1 个分子氨后得到的产物。在强碱性溶液中,双缩脲与CuSO4 形成紫色络合物,称为双缩脲反应。凡具有两个酰胺基或两个直接连接的肽键,或能够以1 个中间碳原子相连的肽键,这类化合物都有双缩脲反应。紫色络合物颜色的深浅与蛋白质浓度成正比,而与蛋白质分子量及氨基酸成分无关,故可用来测定蛋白质含量。
实验七考马斯亮蓝G250法测定的蛋白质含量 一、试验目的 1. 学习分光光度计的原理及操作 2.学习利用染色方法提高蛋白质消光系数,以提高分光光度法检测灵敏度 二、基本原理 1. 根据物质的吸收光谱进行定性或定量分析的方法称为吸收光谱法或分光 光度法。该法所用的仪器称为分光光度计或吸收光谱仪。该法所使用的光谱范围包括可见光和紫外光,即包括波长在200 - 800 nm之间的光。 2.分光光度计灵敏度高,测定速度快,应用范围广,其中的紫外/可见分光 光度技术更是生物化学研究工作中必不可少的基本手段之一。 3.紫外区可分为紫外(近紫外)和真空紫外(远紫外)。由于吸收池(又称样 品池、比色杯等)和光学元件以及氧气能吸收小于190nm波长的光,因此常规紫外测定集中在近紫外区,即200nm-400nm。可见光区为400nm -800nm。 4.考马斯亮蓝G250法 原理:考马斯亮蓝G250与蛋白质结合后,其最大吸收波长从465nm改变为595nm,该蛋白-染料复合物吸光系数很高,所以检测灵敏度很高,可以测定1μg /mL的蛋白质,染料和蛋白结合只需要2分钟,颜色在1小时内稳定。 操作简便,快速,是常用的蛋白含量测定方法之一。去污剂,粘多糖等严重干扰该方法的测定 三、试剂 1. 标准蛋白质溶液:0.5mg/ml牛血清白蛋白溶液 2. 考马斯亮蓝G250蛋白染色剂: 四、操作步骤 1.标准曲线的绘制: 取6只试管,分别加入浓度为0,0.1,0.2,0.3,0.4,0.5mg/ml的标准蛋白质溶液0.1ml,然后加入5ml考马斯亮蓝试剂,震荡混匀,2分钟后于595nm 测定吸光值,以蛋白质浓度为横坐标,光吸收值为纵坐标绘制标准曲线。 2.样品测定: 样品液0.1mL , 然后加入5ml考马斯亮蓝试剂,震荡混匀,2分钟后于595nm 测定吸光值。从标准曲线中查出相应的浓度。 五、试验结果
氨基酸态氮的测定 1概述 2氨基酸态氮的测定 一、概述 蛋白质可以被酶、酸或碱水解,其水解的最终产物为氨基酸。氨基酸是构成蛋白质的最基本物质,虽然从各种天然源中分离得到的氨基酸已达175种以上,但是构成蛋白质的氨基酸主要是其中的20种,而在构成的氨基酸中,亮氨酸、异亮氨酸、赖氨酸、苯丙氨算、蛋氨酸、苏氨酸、色氨酸和缬氨酸等8种氨基酸在人体中不能合成,必须依靠食品供给,故被称为必需氨基酸,它们对人体有着极其重要的生理功能,常会因其在体内缺乏而导致患病或通过补充而增强了新陈代谢作用。 随着食品科学的发展和营养知识的普及,食物蛋白质中必需氨基酸含量的高低及氨基酸的构成,愈来愈得到人们的重视。为提高蛋白质的生理效价而进行食品氨基酸互补和强化的理论,对食品加工工艺的改革,对保健食品的开发及合理配膳等工作都具有积极的指导作用。因此,食品及其原料中氨基酸的分离、鉴定和定量也就具有极其重要的意义。 二、氨基酸态氮的测定 (1)双指示剂甲醛滴定法:原理、试剂、测定方法、结果计算 (2)电位滴定法:原理、试剂、仪器、测定方法、结果计算 1、双指示甲醛滴定法 (1)原理 氨基酸具有酸性的-COOH基和碱性的-NH2基。它们相互租用而使氨基酸成为中性的内盐。当加入甲醛溶液时,-NH2基与甲醛结合,从而使其碱性消失。这样就可以用强碱标准溶液来滴定-COOH基,并用间接的方法测定氨基酸的总量。 (2)方法特点及应用 此法简单易行、快速方便,与亚硝酸氮气容量法分析结果相近。在发酵工业中常用此法测定发酵液中氨基酸含量的变化,以了解可被微生物利用的氮源的量及利用情况,并以此作为控制发酵生产的指标之一。普氨酸与甲醛作用时产生不稳定的化合物,使结果偏高;溶液中若有存在也可与甲醛反应,往往使结果高。 (3)试剂 ①40%中性甲醛溶液:以百里酚酞作指示剂, 用氢氧化钠将40%甲醛中和至淡蓝色。 ②0.1%百里酚酞乙醇溶液 ③0.1%中性红50%乙醇溶液 ④0.1%mol/L氢氧化钠标准溶液 (4)操作步骤 1)含氨基酸溶液20-30mg→250ml锥形瓶中→中性红指示剂2-3滴,滴0.01mol/lNAOH 滴定终点(红→琥珀色) 2)含氨基酸溶液20-30mg→250ml锥形瓶中→百里红酚酞3滴/中性甲醛20ml→摇匀,滴0.01mol/lNAOH滴定终点(淡蓝色) 3)分别记录两次消耗碱液的用量 (5)结果计算