
第三章红外吸收光谱分析
3.1概述
3.1.1红外吸收光谱的基本原理
红外吸收光谱法又称为分子振动转动光谱,属于分子光谱的范畴,是有机物结构分析的重要方法之一。当一定频率的红外光照射分子时,若分子中某个基团的振动频率和红外辐射的频率一致,两者产生共振,光的能量通过分子偶极矩的变化传递给分子,该基团就吸收了这个频率的红外光,产生振动能级跃迁;如果红外辐射的频率和分子中各基团的振动能级不一致,该频率的红外光将不被吸收。如果用频率连续变化的红外光照射某试样,分子将吸收某些频率的辐射,引起对应区域辐射强度的减弱,用仪器以吸收曲线的形式记录下来,就得到该试样的红外吸收光谱,稀溶液谱带的吸光度遵守Lambert-Beer定律。
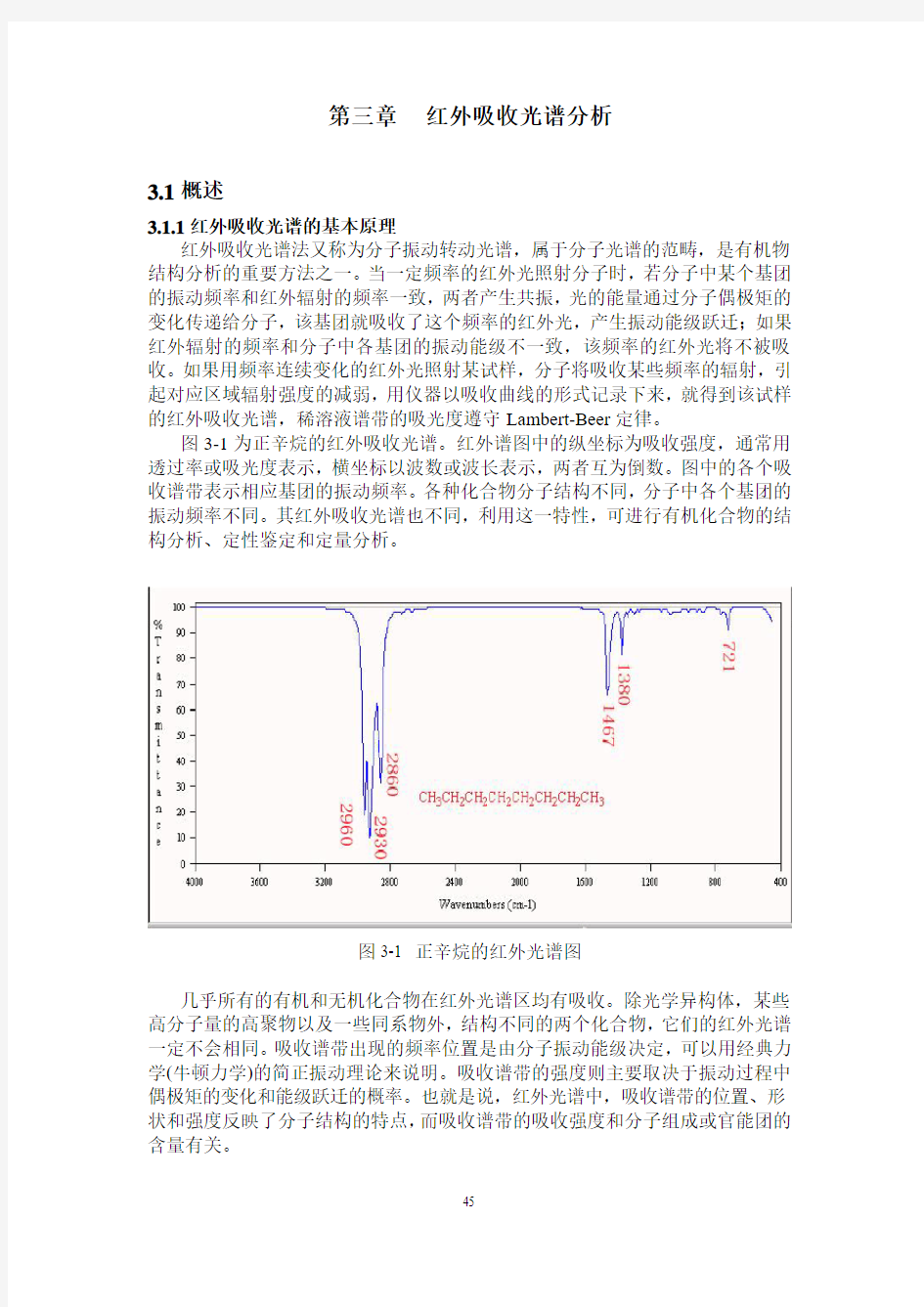
图3-1为正辛烷的红外吸收光谱。红外谱图中的纵坐标为吸收强度,通常用透过率或吸光度表示,横坐标以波数或波长表示,两者互为倒数。图中的各个吸收谱带表示相应基团的振动频率。各种化合物分子结构不同,分子中各个基团的振动频率不同。其红外吸收光谱也不同,利用这一特性,可进行有机化合物的结构分析、定性鉴定和定量分析。
图3-1 正辛烷的红外光谱图
几乎所有的有机和无机化合物在红外光谱区均有吸收。除光学异构体,某些高分子量的高聚物以及一些同系物外,结构不同的两个化合物,它们的红外光谱一定不会相同。吸收谱带出现的频率位置是由分子振动能级决定,可以用经典力学(牛顿力学)的简正振动理论来说明。吸收谱带的强度则主要取决于振动过程中偶极矩的变化和能级跃迁的概率。也就是说,红外光谱中,吸收谱带的位置、形状和强度反映了分子结构的特点,而吸收谱带的吸收强度和分子组成或官能团的含量有关。
因此,红外吸收光谱在化学领域中的应用,大体上可分为两个方面,即分子结构的基础研究和用于化学组成的分析。
首先,红外光谱可以研究分子的结构和化学键。利用红外光谱法测定分子的键长和键角,以此推断出分子的立体构型;利用红外光谱法测定分子的力常数和分子对称性等,根据所得的力常数就可以知道化学键的强弱;由简正频率来计算热力学函数等等。
其次,红外光谱可对物质的化学组成进行分析,这是它最广泛和最重要的应用。用红外光谱法可以根据光谱中吸收谱带的位置、形状和强度来推断未知物结构,依照特征吸收谱带的强度来测定官能团和混合物中各组分的含量。
总之,红外吸收光谱法是物质结构研究、定性鉴定和定量分析中不可缺少的工具,在诸多科学研究领域发挥着重要作用。
3.1.2 红外吸收光谱法的特点
红外吸收光谱反映的是物质的分子结构,属于分子光谱的范畴,与其他仪器分析法相比较,红外光谱法有如下特点:
(1)红外光谱是依据样品在红外光区吸收谱带的位置、强度、形状、个数,并参照谱带与溶剂、聚集态温度、浓度等的关系求化学键的力常数、键长和键角,推测分子的空间构型,判断分子中某种官能团的存在与否,以及各官能团的连接次序,从而确定化合物结构。
(2)红外光谱适用范围广,几乎所有的有机和无机化合物在红外光谱区均有吸收。无论是纯净物,还是混合物都可以进行分析,并且对任何状态的样品,如气体、液体、可研细的固体或薄膜物质等都适用,对不透光样品还可采用反射技术等等,测定方便,制样简单。
(3)红外光谱特征性高。由于红外光谱信息多,可以对不同结构的化合物给出特征性的谱图,从“指纹区”就可以确定化合物的异同。对于一些同分异构体、几何异构体和互变异构体也可以鉴定。
(4)分析时间短。一般红外光谱做一个样可在10~30min内完成,傅里叶变换技术的采用更是为快速分析、在线分析和化学动力学研究提供了重要手段。
(5) 红外光谱所需样品用量少,一次用样量约1~5mg,有时甚至可以低到几十微克,而且不破坏样品,可以回收。
3.1.3 红外光谱法的应用
根据仪器及应用不同,习惯上又将红外光区分为近红外光区、中红外光区、和远红外光区三个区域。
近红外光区的波长范围为12800~4000cm-1(0.78~2.5μm),该光区的吸收谱带主要是由低能电子跃迁、含氢原子团(如O-H、N-H、C-H)伸缩振动的倍频及组合频吸收产生的,可用来研究稀土和其他过渡金属离子的化合物,并适用于水、醇、某些高分子化合物以及含氢原子团化合物的定量分析,测量准确度及精密度与紫外、可见吸收光谱相当。
中红外光区波长范围为4000~200cm-1(2.5~50μm),绝大多数有机化合物和无机离子的基频吸收带都出现在中红外光区。由于基频振动是分子中吸收最强的振动,所以该区最适于进行化合物的定性和定量分析。随着傅里叶变换技术的出现,该光谱区也开始用于表面的显微分析,通过衰减全反射、漫反射以及光声测定法等对固体试样进行分析。
由于中红外光谱仪最为成熟、简单,而且已经积累了该区大量的标准谱图数据,因此它是应用最为广泛的光谱区。通常所说的红外光谱就是指中红外区的光谱。
远红外光区波长范围为200~10cm-1(50~1000μm),气体分子中的纯转动跃迁、振动-转动跃迁、液体和固体中重原子的伸缩振动、骨架振动以及晶体中的晶格振动都在此区。由于低频骨架振动能灵敏地反映出结构的变化,所以对异构体的研究特别方便。此外,由于参与金属-配位体振动的原子质量比较大或由于振动力常数比较低,使金属原子与无机及有机配体之间的伸缩振动和弯曲振动的吸收出现在<200cm-1的波长范围,故该区特别适合研究无机化合物,提供晶格能及半导体材料的跃迁能量;还能用于金属有机化合物(包括配合物)、氢键、吸附现象的研究。但此区能量弱,应用受到了极大的限制。然而随着傅里叶变换仪器的出现,这个区域的研究又变得活跃起来。
3.2 红外吸收光谱仪
3.2.1 色散型红外光谱仪
色散型红外光谱仪的基本结构和工作原理如图3-2所示,主要由光源、单色器、检测器、放大器和记录仪等部件组成。
图3-2 色散型光学零位平衡式红外光谱仪示意图
作为红外光谱仪的光源,要求能发射出稳定的高强度的连续红外光,中红外区通常使用能斯特灯和硅碳棒。能斯特灯是由氧化锆、氧化钇和氧化钍等粉末按一定比例混合压制成棒状,并在高温下烧结而成。能斯特灯在室温下是非导体,加热到700℃以上才成为导体,因此.需由一个辅助加热器预热,当能斯特灯被点燃后,辅助加热器停止加热。该灯的优点是发出的光强度高,使用寿命较长,可达2000h。缺点是性脆易碎,且在光源线路上还需加一限制电流的稳流装置。硅碳棒是由硅碳砂压制成型后经高温烧结而成,在室温下是一导体,工作前不需预热,工作温度为1000℃左右,成品坚固耐用,寿命比能斯特灯长,缺点是电极接触部分需用水冷却。
单色器是由色散元件(光栅或棱镜)、入射与出射狭缝以及准直反射镜等组成。其功能是将连续光色散为一组波长单一的单色光,然后将单色光按波长大小依次由出射狭缝射出。红外光谱仪中目前大多采用闪耀光栅,在进行光谱级次分离时
采用滤光片或棱镜。大部分的红外光学材料易吸湿(KRS-5除外),因此,红外光谱仪放置和使用环境应保持干燥。
红外光谱仪常用真空热电偶、高莱槽或测辐射热计等作检测器。检测器受到红外光照射时,将产生的热效应转变为十分微弱的电信号经放大器放大后,带动伺服马达工作,记录红外吸收光谱,记录方式有光学零位式和比例记录式两类。这些检测器具有对红外辐射接受灵敏度高,响应快,热容量小等特点。
3.2.2 傅里叶变换红外光谱仪
傅里叶变换红外光谱仪(FTIR)是20世纪70年代出现的新—代红外光谱测量技术和仪器。它没有色散元件,主要由光学检测系统和数据处理系统组成。
取代色散元件的是FTIR的光学检测系统,由光源、主干涉仪、激光干涉仪、检测器和各种红外反射镜组成,其中主干涉仪是FTIR的核心部分,最常用的是迈克尔逊干涉仪,包括分束器、定镜、动镜和动镜驱动结构,其结构和工作原理如图3-3所示。
1.动镜驱动机构;
2.动镜;
3.顶镜;
4. 分束器;
5. 光源;
6.激光检测器;
7.红外检测器
迈克逊干涉仪的作用是获得样品干涉图,激光干涉仪的作用是实现干涉图的
等间隔取样、动镜速度和移动距离的监控和采样初始位置的确定。样品干涉图经计算机进行傅里叶变换而得到红外光谱图。
在FI'IR中常用的检测器有通用型的热释电检测器,如TGS(硫酸三甘肽)、DTGS(氘代TGS)、LATGS(L-丙氨酸TGS)、DLATGS(氘代LATGS)),高灵敏的光电导检测器,如MCT(汞镉碲)、锑化铟,和氦冷式热辐射计等。
计算机通过接口与光学测量系统电路相连,把检测器得到的信号经放大器、滤波器等处理,然后送到计算机接口,再经处理后送到计算机数据处理系统,计算结果输出给显示器或打印机。另外,由键盘输入仪器控制指令,对干涉仪动镜等光学系统进行自动控制。
傅里叶变换红外光谱仪不用狭缝机构和分光系统,消除了狭缝对光谱能量的限制,使光能的利用率大大提高。使仪器具有测量时间短、高通量、高信噪比、高分辨的特性。与色散型仪器的扫描不同,傅里叶红外光谱仪能同时测量记录全波段光谱信息,使得在任何测量时间内都能够获得辐射源的所有频率的全部信息。
傅里叶变换红外光谱仪价格贵,环境要求高,但是它具有分辨率高,波数准确度高,扫描时间短,灵敏度高,测量范围宽、极低的杂散光等特点,使得它可用于快速化学反应的追踪、研究瞬间的变化,同时又特别适合与各种仪器联机,如与色谱仪联用的GC- FTIR,与超临界色谱联用的SFC- FTIR,与热重联用的FTIR-TGA,因而发展迅速,并逐步取代色散型红外光谱仪。
3.3 操作要领
下面以美国热电公司Nexus470 FTIR为例介绍FTIR仪器的操作要领。
1. 开机:打开仪器光学台(主机)的电源开关;打开计算机的电源开关,双击OMNIC图标.打开OMNIC应用软件。
2. 检查光谱仪的工作状态在OMNIC窗口的Bench Status(光学台状态)指示显示绿色“√”,即为正常。
3. 设定光谱收集参数:在Collect命令下单击Experiment Setup,弹出如下菜单,按实验要求设置包括采集的波数范围、扫描次数、光谱分辨率、显示所收集数据的形式等参数,
也可以在实验设置下拉列表框中选择已有的实验方法。
实验设置下拉列表框
采集背景按钮
采集样品按钮
4. 采集试样的光谱图,按软件的提示,在确认光路中没有试样时,采集背景的干涉图;将制好的试样插入光路,采集试样的干涉图。计算机将自动进行傅里叶变换和背景扣除处理,最后给出扣除背景后的试样红外光谱图。
5. 光谱处理:对试样光谱图进行基线校正、平滑和标峰等处理。
6. 从试样架上移走试样。
7. 结果的处理:建立或选取摸板,按要求填入谱图和其他必要信息,而后以
报告的形式打印出来,或加入笔记本中保存。
采集谱图工具
谱图处理工具
谱库工具
报告工具
选择工具 区间工具 坐标工具 峰高工具 峰面积工具 标峰工具
8. 复原并关闭仪器和辅助设施。
3.4 红外吸收光谱分析的制样技术
要获得—张高质量的红外光谱图,除仪器本身因素之外,还必须对不同状态和性质的试样,采用相应的制备方法,以适应不同的分析目的和测试仪器。
选择制样方法时,首先要考虑样品的聚集态和物化性质。纯度不高的样品,建议进行提纯处理。含有水分和溶剂的样品要先进行干燥处理。不稳定样品要避免使用压片法。制样过程中,要避免空气中的水分、二氧化碳和其他污染物的混入。
图3-4 2米光程气体池
3.4.1 气体试样
气体试样一般是在气体池内进行测定。气体池长度和光程可以选择。气体池的两端粘合有透红外光的盐基窗片,窗片的材质一般是氯化钠或溴化钾。进样时,先将池体抽成真空,然后导入测试气体至所需压力,即可进行测量。
3.4.2 液体试样
液体试样可采用液膜法或溶液法进行测定。
液膜法是将试样直接滴放在可拆池的一块盐片上,在盖上另一块盐片之前,放上适当厚度的间隔片,借助池架的螺丝拧紧两盐片。此法不适于定量分析和低沸点试样的测试。如果试样吸收很强。不必放置间隔片;高挥发性样品可用密闭固定池进行测定。
溶液法是将液体(或固体)试样溶在适当的红外溶剂中,然后注入固定池中进行测定。该法特别适于定量分析。此外,它还能用于红外吸收很强,用液膜法不能得到满意谱图的液体试样的定性分析。
在使用溶液法时,必须特别注意红外溶剂的选择。除了对试样有一定的溶解度外,要求溶剂不侵蚀窗片,不与试样起反应,对试样没有强烈的溶剂化效应,在所测光谱范围内没有强烈吸收。分子简单的非极性溶剂如四氯化碳和二硫化碳最为适用,极性较强的氯仿,因其溶解能力较强也广为应用。四氯化碳在1300cm-1以上吸收较小,而二硫化碳在1300cm-1以下几乎没有吸收,为得到完整的红外光谱图,可以并行使用这两种溶剂,或使用溶剂补偿法避免干扰。
、
1.前框;
2.后框;
3. 溴化钾;
4. 垫圈;
5.间隔片;
6.螺帽
图3-5 可拆卸液体池和固定液体池的示意图
3.4.3 固体试样
固体试样的制备,除前面介绍的溶液法外,还有糊状法、压片法、薄膜法、反射法等,其中尤以糊状法、压片法和薄膜法最为常用。
糊状法又称Nujol法。该法是将研细的试佯粉末分散在与其折射率相近的液体介质(即糊剂)中进行测定。最常用的分散剂是石蜡油,但它不适于用来研究结构与其相似的饱和烃,此时可采用六氯丁二烯代替石蜡油。操作时,用干净的玛瑙研钵将3~4mg固体试样研细,滴两滴石蜡油后继续研磨,用不锈钢刀刮到盐片上,压上另一块盐片,放在可拆液体池的池架上,测定光谱图。
压片法是把固体试样分散在碱金属卤化物,如溴化钾和氯化钠等中,压成透明薄片后进行测定,操作时,取约0.5~2mg固体试样于玛瑙研钵中,在红外灯下研磨成细粉,加约100mg干燥的溴化钾再一起研磨至2μm以下,然后移入压模的底模片上,小心放入顶模,并用顶模施压旋动使粉末分布均匀铺平,将装配好的模具放在油压机下,抽真空预排气2min,用压把加压至7×103Pa左右,维
持5min。放气泄压后,取出模具,用顶样器顶出锭片,得一透明圆形锭片。
图3-6 压片机和压片模具
薄膜法主要用于高分子化合物的测定,通常将试样热压成膜,或将试样溶解在沸点低易挥发的溶剂中,然后倒在平板上,待溶剂挥发后成膜,此法常因溶剂未除尽而干扰图谱,或因熔融试样时温度过高,使试样分解。对于不溶、难熔又难粉碎的样品,可用机械切片成膜。
图3-7 薄膜制样器
反射法主要用于那些不溶解、不熔融且又难粉碎、以及深色和不透明表面涂层等样品的分析,一般是在专用的测定附件和反射晶体上完成的。
在红外光区,使用的光学部件和吸收池的材质多为氯化钠或溴化钾等晶体,不能受潮。操作时应注意不要用手直接接触盐片表面,不要对着盐片呼吸,同时避免与吸潮液体或溶剂接触。各种池体使用完毕后用四氯化碳等容易挥发的溶剂
清洗,干燥后放入干燥器内保存。
3.5 红外光谱附件和联机技术
3.5.1常用附件
用于红外光谱仪的附件很多,而且应用也十分广泛。衰减全反射(ATR)、漫反射(DIR)、镜反射(MR) (包括掠角反射)、光声附件(PAS)和各种液体池及气体池等附件用于不同状态(固、液、气)、各种形状和类型样品的分析。红外偏振器、振动圆二色(VCD)和振动线性二色(VLD)等附件用于分子取向及构型和构象的研究。近红外和中红外光导纤维及其探头、高温高压红外原位池可对样品进行在线和原位测量。高压金刚石砧型池、变温光谱附件(低温、高温)等可用于极端条件下物质性质变化的研究。
衰减全反射ATR又称为内反射光谱,由于一次反射能量变化比较小,所以现在均采用多次衰减全反射技术。ATR附件适合各类样品材料的表面分析,而且具有无需制样、样品用量小且不破坏样品的特点。
图3-8 红外全衰减反射工作示意图
漫反射光谱又称为粉末反射法,照射到粉末样品上的光首先在其表面反射,一部分直接进入检测器,另一部分进入样品内部多次透射、散射后再从表面射出,后者称为扩散反射光。DIR法就是利用扩散散射光获取红外光谱的方法。与压片法相比,DIR法由于测定的是多次透过样品的光,因此两者的光谱强度比不同,压片法中的弱峰有时会增强。在利用DIR法进行定量分析时要进行Kubelka-Munk变换,一般仪器软件可以自动进行。漫反射光谱用于粉末样品以及表面涂层等分析。
傅里叶变换红外光声光谱仪(PASIR)采用光声池、前置放大器代替傅里叶变换红外光谱仪的检测器,样品置于光声池中测定。红外光声光谱法主要用于强吸收、高分散的样品(如深色催化剂、煤样等),橡胶、高聚物等难以制样的样品,和不允许加工处理的样品的分析。
欧米采样器是美国热电公司推出的通用型单次反射水平全衰减反射制样附件,几乎可以应用到所有种类的样品,所以也称之为“万能采样器”。与其他具有平板型制样表面ATR(衰减全反射)附件相比,采用了晶体与样品的“点对点”接触方式和压力柱装置的欧米采样器大大提高了光谱质量。晶体的材料和形状使得欧米采样器成为一个非常不错的红外附件。液体池更加拓宽了欧米采样器的用途。“池”的设计具有小容积并且容易清洗的特点。
0I
变频
红外
b l βl l g μg l s
μ样品支撑台厚 光吸收长度 样品厚
气体热扩散长 气体层厚 样品热扩散长
图3-9 PASIR 工作示意图
3.5.2 红外光谱仪的联用技术
为适应微量样品、混合物和化合物分解过程的分析测试,发展了红外显微镜、
不同色谱仪和热重分析仪等与红外光谱仪的联用技术。
气相色谱是除毛细管电泳外分离效果最好的方法,红外光谱是分子结构测定
的有力手段,两者的结合可以有效地进行复杂体系中各个组分的分离和鉴定。如
图3-10所示,气相色谱红外光谱联用仪最关键的部位是GC 和FTIR 的接口,接
口多采用被称为“光管”的、与色谱流出气体相适应的流通型气体吸收小池。光
管一方面不断接收GC 馏分;一方面FTIR 同步跟踪扫描以检测光管中GC 每个
色谱流出峰;采集到的数据经过计算机处理可以获得与GC —MS 类似的重建色
谱图,进而可以得到色谱图中每一个谱峰的红外光谱图。
图3-10 GC-FTIR 工作示意图
红外显微镜就是将红外光谱仪和显微镜结合起来,由显微镜观察系统、光学
系统和MCT 组成。一般具有透射式和反射式两种工作方式。透射式红外显微镜
用于分析可透过红外光的样品,如厚度小于20μm的薄膜、固体切片和微量液体样品。反射式红外显微镜用于分析样品的表面或样品中的杂物及一些不透光物质。
在分析样品时,来自FTIR光学台的干涉红外光进入红外显微镜后被聚焦照在放在KBr窗片上(或无KBr窗片的固体)的样品上,形成一个直径约几百微米的光斑。透过(或反射)的红外光聚焦到MCT检测器上,得到信号。
MIC-FTIR的测量灵敏度高,检出限可达pg级,空间分辨率为10μm ,适合于样品的微量和微区分析,如工业部门和科研部门的微量样品,司法部门在破案中提取到的极微量犯罪物证,不能破坏样品的特殊分析,如对文物的分析,对某些分析对象表面不同部位或某一微区的分析。多数情况下不需要制样;对非均相的混合物样品,不需要分离,可通过红外显微镜选择混合物中各个单一组分直接测定其红外光谱,真正做到了无损检测。
但是,红外显微镜也有不方便的地方。MCT检测器要用液氮,工作时间受到限制;在分析气体和微量液体时也有一些困难;放样品的窗片及样品表面要很干净,微量的污染物也可能造成误差。
3.6 标准红外光谱图和数据表
常见的标准红外光谱图有萨特勒标准光谱库、Wyandotte-ASTM 红外光谱卡片、Aldrich/Nicolet凝聚相谱图库、Sigma Fourier生物化学谱库、Nicolet蒸气相谱库、Aldrich蒸气相谱库等等。
美国Sadtler研究实验室编印的萨特勒标准光谱集,包括有红外吸收光谱、紫外吸收光谱和核磁共振披谱三种标准谱图集,内容丰富全面,记录原始真实光谱.因此获得广泛应用。其中的标准红外吸收光谱图分为棱镜光谱和光栅光谱两大部分,分别收集10万多种有机化合物的标准谱图。在每张标准光谱图上,都注明化合物的名称、分子式、相对分子质量、熔点、沸点、来源、制样方法以及化合物的结构式等信息。萨特勒红外标准谱图集还附有化合物名称字顺索引、分子式索引、官能团索引、化合物分类索引、商品名索引、谱线索引,可根据需要灵活选用。查阅标准谱图的一般方法是:先从索引查得化合物的光谱号,再按光谱号找到谱图。目前,Sadtler标准光谱已能进行数字化检索。
使用标准谱图时,要注意制样方法、溶剂和仪器类型等信息,应尽可能使测试条件与标准谱图的一致,保证判定的准确度。
国内外许多机构还研制了多种红外检索系统和红外谱图专家系统,这些工具使得红外谱图的解析变得更加快速、准确。
3.3 实验部分
实验3-1 红外吸收光谱的测定
一、实验目的
1.掌握红外吸收光谱分析时各种物态试样的制备方法。
2.熟悉红外光谱仪的工作原理及其使用方法。
3.学习红外吸收光谱解析的基本方法。
二、方法原理
要获得—张高质量的红外光谱图,除仪器本身因素之外,还必须对不同状态和性质的试样,采用相应的制备方法。气体试样—般都采用气体池进行测定;
液体试样可采用液膜法或溶液法测定,分别在可拆卸液体池或固定池内完成;固体试样的制备,有溶液法、粉末法、糊状法、压片法、薄膜法、反射法等,其中尤以糊状法、压片法和薄膜法最为常用。
红外光谱中4000~1350cm-1区域称为基团特征频率区。分子中某些基团或化学键在不同化合物中的振动频率基本固定,总是出现在某一特定范围内,因此,许多有机官能团都有自己的特征吸收谱带,例如CH3(CH2)5CH3,CH3(CH2)5CH=CH2等分子中都有CH3、CH2基团,它们的伸缩振动频率与图3-1正十七烷分子的红外吸收光谱中CH3、CH2基团的伸缩振动频率—样,都出现在3000—2800cm-1范围内,这一区域是C-H伸缩振动的特征频率。但是,当官能团出现在不同物质中时,它们所处的化学环境不同,使振动频率发生一定移动,强度和形状也会有所变化,而这种差别常常反映出分子结构的特点。例如羰基(C=O)的伸缩振动频率在1600~1860 cm-1范围内,当它处于酸酐中时,为1820~1750 cm-1,酯羰基为1750~1725 cm-1,醛羰基为1740~1720 cm-1,酮羰基为1725~1710 cm-1;在酰胺中为1650 cm-1,而乙酰苯中,因与苯环的共轭作用,则为1695~1680 cm-1。因此在基团特征频率区内,根据所掌握的各种基团频率及其位移规律,就可确定有机化合物分子中存在的官能团及其在分子中的相对位置。
红外光谱中1350-650 cm-1区域常称作指纹区。这一区域的振动往往涉及分子中的全部原子,以及各种振动方式,如各种单键的伸缩振动、含氢基团的弯曲振动以及各种振动耦合等,使该区域吸收带变得很复杂,许多谱峰无法归属。化合物结构上的微小差异都会使这一区域的谱峰产生明显差别,许多谱峰无法一一归属,因此,仅仅依靠对红外光谱图的解析常常难以确定有机物的结构,通常还需要借助于标准试样或红外标准谱图。同一物质在相同的测定条件下测得的红外光谱有很好的重复性.如果两张图谱中各吸收峰的位置、形状及其相对吸收强度一致,则两个化合物具有相同的结构。因此,可以通过比对试样与标准物的红外光谱,或比较试样的红外光谱与红外标准谱图,进行定性分析。
因此,红外光谱解析的目的,就是通过对化合物的红外吸收谱带的位置、形状和强度,及其变化规律的研究,指认谱带的归属,从而完成定性鉴定和结构分析工作。解析的一般步骤如下:
1)了解样品的来源:样品的来源和制备方法,可能的物理化学性质和参数等都能提供一定的结构信息。
2)检查谱图质量:注意制样方法对谱图的影响,排除溶剂、水分、二氧化
碳、硅胶和杂质谱带,注意识别各种倍频、组合频等对基频的干扰。
3)观察特征谱带区,同时与其他相关谱带对照,确定官能团的存在。一般来讲,只要对应的特征谱带没有出现,就可以判定该官能团不存在。
4)研究谱带的位移和指纹区等的特征,确定基团连接方式和相对位置,进一步推断可能的结构。
5)与标准谱图或已知物谱图对照:只有谱带的位置、形状、数目和强度一致,才能确定结构完全相同。
三、仪器
1.红外吸收光谱仪
2.红外压片机和压片模具
3.玛瑙研钵
4.快速红外干燥灯
5.热压膜制样器,或不锈钢刮刀、试管、酒精灯和40×40×2mm的聚四氟
乙烯平板
6.溴化钾/氯化钠单晶片
7.试样勺、镊子、玻璃棒、手指套等
四、试剂
1.溴化钾(光谱纯)
2.石蜡油(光谱纯)
3.聚苯乙烯标准膜(厚度3μm)
4.苯甲酸、二苯甲酮、丙酮、乙醛、n-丁醇、p-硝基甲苯、N、N-二甲基甲
酰胺等各类代表性有机化合物和高分子化合物。
五、实验条件
本实验以美国热电公司生产的Nexus 470型傅立叶变换红外吸收光谱仪为例,其他型号仪器需对实验条件作适当调整。
1.测量波数范围:4000~600 cm-1
2.分辨率:4 cm-1
3.扫描次数:16次
4.参比物:空气
六、实验步骤
本实验以美国热电Nexus 470型红外吸收光谱仪为例,其他仪器需对实验条件作相应调整)。
1.开启除湿机,控制室内相对湿度<60%。
2.试样的制备:
1)KBr压片法制备固体试样:取约0.5~2mg固体试样于玛瑙研钵中,在红外灯下研磨成细粉,加入大约100mg干燥的溴化钾再一起研磨
至2μm以下,然后移入压模的底模片上,小心放入顶模,并用顶模
施压旋动使粉末分布均匀铺平,将装配好的模具放在油压机下,抽真
空预排气2min,用压把加压至7×103Pa左右,维持5min。放气泄压
后,取出模具,用顶样器顶出,得一透明圆形锭片。
2)薄膜法制备高聚物固体试样:将聚合物溶解于合适的有机溶剂中,滴两滴该溶液在晶体窗片上,用玻璃棒摊匀,放在红外灯下使溶剂完全
挥发;或者取几粒树脂于小试管内用酒精灯加热软化,用刮刀将软化
物刮涂在聚四氟乙烯平板上,于酒精灯上加热至聚合物重新软化后,
离开热源,立即盖上另一片聚四氟乙烯板,压制薄膜。压板冷却后,
用刮刀小心取下薄膜;
3)糊状法制备固体试样:用干净的玛瑙研钵将3—4mg固体试样研细,滴两滴石蜡油后继续研磨,用玻璃棒或刮刀涂到晶体窗片上,压上另
一块窗片即可。
4)液膜法制备液体试样:在一块晶体窗片上,滴加一滴液体试样,盖上另一块窗片,使两块窗片间形成一定厚度的液膜即可。
3.根据实验条件设定红外光谱仪参数。
4.测定聚苯乙烯标准膜的红外光谱图,以校准仪器的波数。
5.将试样装于相应的试样架或试样卡中,置于光路中测绘红外吸收光谱。
6.测定结束后,取出样品,并进行必要的仪器整理和复原工作,并进行实
验登记。
七、实验记录与结果处理
1.记录实验条件(仪器型号和生产厂家、实验参数、制样方法等等)。
2.在获得的红外吸收光谱图上,标出各特征吸收谱带的频率,并指出各特
征吸收谱带的归属。
八、思考与讨论
1.化合物的红外吸收光谱是怎样产生的?红外吸收光谱图都能提供怎样的
信息?如何进行红外光谱图的解析?
2.红外光谱实验室为什么要求温度和相对湿度维持一定的指标?
实验3-2 间、对二甲苯的红外吸收光谱定量分析——基线法
一、目的要求
1.学习红外吸收光谱定量分析基本原理。
2.掌握基线法定量测定方法。
二、基本原理
红外光谱法定量分析的基础,与其他分光光度定量分析一样,仍是朗伯—比耳定律和吸光度的加合性:
A=κbc (3-1)
但由于制样和测试技术的不同,通常采用基线法测量吸光度,采用标准曲线法完成定量。
基线法如图3-11所示。测绘出红外吸收光谱后,在吸收峰处先画一条与吸收谷相切的直线作基线,然后通过峰顶点作基线的垂线,随即得到分析波数处的吸光度。根据不同的谱带特征,基线有多种取法。若待测峰不受干扰,可选与吸收峰两谷相切的直线为基线;若待测峰受到近旁其它峰的干扰,可选通过一个峰谷的单点水平切线为基线;若待测峰与干扰峰紧靠在一起,但干扰峰的峰谷在浓度改变时变化不大,这时可选取与两侧干扰峰峰谷相切的直线为基线,或者用强干扰峰边沿的外推曲线作为近旁弱分析峰的基线。
图3-11 基线法
三、仪器
1.红外光谱仪
2.固定液体池(0.1mm)
3.微量进样器
4.容量瓶(5mL)
四、试剂
1.邻二甲苯(色谱纯)
2.间二甲苯(色谱纯)
3.对二甲苯(色谱纯)
4.未知试样:含有一定量的间二甲苯和对二甲苯(可由一定比例的已知物
配制)
五、实验条件
本实验以美国热电Nexus 470型傅立叶红外吸收光谱仪为例,其他仪器需作相应调整。
1.测量波数范围:4000~600 cm-1
2.分辨率:4 cm-1
3.扫描次数:16次
4.参比物:空气
六、实验步骤
1.开启除湿机,保持室内相对湿度<60%。
2.标准溶液的测定:分别吸取1.00mL、2.00mL、
3.00mL间二甲苯于三只
5mL容量瓶中,依次加入3.00mL、2.00mL、1.00mL对二甲苯,用邻二
甲苯稀释至刻度,摇匀,依次用液体固定池测绘红外吸收光谱图。
3.吸取未知试样
4.00mL于5mL容量瓶中,用邻二甲苯稀释至刻度,摇匀,
用液体固定池测绘红外吸收光谱图。
4.纯标样谱图的测绘:间二甲苯和对二甲苯纯标样,用液体固定池或液膜
法测绘它们的红外吸收光谱图。
5.进行必要的仪器复原和整理,做好实验登记。
七、实验记录及结果处理
1.记录实验条件。
2.在纯标样红外吸收光谱图上,标出各基团频率峰的波数及其归属,并讨
论这三种同分异构体在红外光谱上的异同点。
3.借助仪器中OMNIC专用软件中的“峰高工具”,在所采集的红外吸收光
谱图上,依照图3-8基线法对邻二甲苯特征吸收峰743cm-1、间二甲苯特
征吸收峰692 cm-1和对二甲苯特征吸收峰792cm-1分别测量各自的吸光度
(以邻二甲苯作内标) 。
值,列表并计算A/A
内标
4.分别作间二甲苯和对二甲苯的A/A内标-c标准曲线,并求出回归方程和相
关系数。在标准曲线上查出试样中间二甲苯和对二甲苯的体积浓度,或
用回归方程计算,再计算原试样中这两种成分的含量。
八、思考题
1.有两个组分的混合试样,都有一个互不干扰的特征吸收峰,欲用溴化钾
压片法制备试样,测定其各自的含量,试提出实验方案。
实验3-3 测定聚硅氧烷中的甲基苯基比
一、目的要求
1. 学习红外吸收光谱定量分析基本原理。
2. 学习用吸光度比例法进行红外光谱定量分析。
二、基本原理
由朗伯-比耳定律A=εbc 可知,要测定样品浓度必须先测定摩尔吸光系数ε
和试样厚度b ,当采用薄膜法、压片法来制备样品时,样品厚度不易精确控制。
这时可采用比例法,即借助比较同一谱图中各分析波数处的吸光度来得到组份之
间的相对含量关系。
设试样只含两个组分,根据朗伯-比耳定律,在所选的两个分析波数处,可
以得到如下的关系:
A 1=ε1b 1c 1, A 2=ε2b 2c 2
(3-2)
由于两个吸光度A 1和A 2系由同一个样片(膜)测得,即b 1=b 2,所以对应于两个组
分的两条分析谱带的吸光度之比为
21221121c c K c c A A ==εε (3-3)
式中,K 为两个组份在各自分析波数处的摩尔吸光系数之比。
配制一系列已知两组分比例的混合物作为标准样品,就可以获得一组相应于
不同c 1/c 2值的A 1/A 2值,以A 1/A 2为纵坐标,浓度比为横坐标作图,画出直线的
斜率即是欲求之K 值。这样就可以用上式来计算未知样品两组份之间的关系,
当然也可以直接由图读出。
对于二元组份,因为c 1+c 2=1,代入3-3式,则有
21221211/,//A A K K c A A K A A c +=+= (3-4)
由此可知,若用比例法来分析二元物质的组成是很方便的。
聚硅氧烷是一种常见的色谱固定相,聚合物中甲基和苯基的数量决定了它的
极性,直接影响对各类物质的分离能力。本实验选2980cm -1和3070cm -1分别为
聚硅氧烷中甲基和苯基的分析波数,以色谱纯聚硅氧烷配制标准系列,采用双波
长比例法测定试样中的甲基苯基比。
三、仪器
1. 红外吸收光谱仪
2. 称量瓶
3. 溴化钾单晶块
4. 窗片抛光器
第四章振动光谱 一、教学目的 理解掌握震动光谱分析的基本理论,掌握红外光谱图的分析处理,了解红外光谱实验技术。 二、重点、难点 重点:震动光谱分析的基本理论,红外光谱图的分析处理。 难点:震动光谱分析的基本理论。 三、教学手段 多媒体教学 四、学时分配 4学时 引言: ●1900~1910年间,科布伦茨(W.W.C。blentz)首先用红外光测量了一些有 机物液体的吸收光谱而建立起一种新的分析方法——红外光谱法。他发现分子中的一定原子群可以吸收特定的频率,这些特定的频率犹如人类的指纹,可以用来辨认分子中特定原子群的存在。 ●它主要可以用作分子结构的基础研究和物质化学组成(物相)的分析(包括定性和 定量)。红外光谱法作分子结构的研究可以测定分子的键长、键角大小,并推断分子的立体构型,或根据所得的力常数,间接得知化学键的强弱,也可以从正则振动频率来计算热力学函数等。 ●不过红外光谱法更多的用途是根据谱的吸收频率的位置和形状来判定本知物,并按 其吸收的强度来测定它们的含量。因此红外光谱法在目前已成为十分方便而有效的分析方法之一。 ●红外光谱法应用得较多的是在有机化学领域,对无机化合物和矿物的红外鉴定开始 较晚。红外光谱法对测定矿物的结构或组分虽不如X射线衍射分析那么成熟,却也有其独特长处。 所谓振动光谱是指物质因受光的作用,引起分子或原子基团的振动,从而产生对光的吸收。如果将透过物质的光辐射用单色器加以色散,使波长授长短依次排列,同时测量在不同波长处的辐射强度,得到的是吸收光谱。如果用的光源是红外光波,即0.78~1000μm,就是红外吸收光谱。如果用的是强单色光,例如激光,产生的是激光拉曼光谱。本章主要介绍红外光谱的原理及其在无机非金属材料中的应用,对拉曼光谱只作简单的介绍。
红外光谱图解析 一、分析红外谱图 (1)首先依据谱图推出化合物碳架类型,根据分子式计算不饱和度。 公式:不饱和度=F+1+(T-O)/2 其中: F:化合价为4价的原子个数(主要是C原子); T:化合价为3价的原子个数(主要是N原子); O:化合价为1价的原子个数(主要是H原子)。 F、T、O分别是英文4,3 1的首字母,这样记起来就不会忘了 举个例子:例如苯(C6H6),不饱和度=6+1+(0-6)/2=4,3个双键加一个环,正好为4个不饱和度。 (2)分析3300~2800cm^-1区域C-H伸缩振动吸收,以3000 cm^-1为界,高于3000cm^-1为不饱和碳C-H伸缩振动吸收,有可能为烯、炔、芳香化合物吗,而低于3000cm^-1一般为饱和C-H伸缩振动吸收。 (3)若在稍高于3000cm^-1有吸收,则应在2250~1450cm^-1频区,分析不饱和碳碳键的伸缩振动吸收特征峰,其中: 炔—2200~2100 cm^-1 烯—1680~1640 cm^-1 芳环—1600、1580、1500、1450 cm^-1 若已确定为烯或芳香化合物,则应进一步解析指纹区,即1000~650cm^-1的频区,以确定取代基个数和位置(顺反,邻、间、对)。 (4)碳骨架类型确定后,再依据其他官能团,如C=O,O-H,C-N 等特征吸收来判定化合物的官能团。 (5)解析时应注意把描述各官能团的相关峰联系起来,以准确判定官能团的存在,如2820、2720和1750~1700cm^-1的三个峰,说明醛基的存在。解析的过程基本就是这样吧,至于制样以及红外谱图软件的使用,一般的有机实验书上都有比较详细的介绍的。 二、记住常见常用的健值 1.烷烃 3000-2850 cm-1C-H伸缩振动 1465-1340 cm-1C-H弯曲振动 一般饱和烃C-H伸缩均在3000 cm-1以下,接近3000 cm-1的频率吸收。 2.烯烃 3100~3010 cm-1烯烃C-H伸缩 1675~1640 cm-1C=C伸缩 烯烃C-H面外弯曲振动(1000~675cm^1)。 3.炔烃 2250~2100 cm-1C≡C伸缩振动 3300 cm-1附近炔烃C-H伸缩振动 4.芳烃 3100~3000 cm-1芳环上C-H伸缩振动 1600~1450 cm-1C=C 骨架振动 880~680 cm-1C-H面外弯曲振动) 芳香化合物重要特征:一般在1600,1580,1500和1450 cm-1可能出现强度不等的4
红外光谱分析概述(上) 1.红外光谱 红外光谱是反映红外辐射强度或其他与之相关性质随波长(波数)变化的谱图。目前,它是一种被广泛应用于研究表征物质的化学组成,在分子层次上的结构及分子间相互作用的有力手段。红外射线发现于1800年,在用普通温度计测量可见光谱的温度效应时,在红光一端的外侧观察到有较强的热效应。后来,实验证实了这是由一种肉眼看不见、波长比红光更长的电磁辐射所造成的,这种电磁辐射被称为红外光。通常将红外辐射的波长范围定为0.8~1000微米,并可粗略地分为三个波段:(1)近红外的波段为0.8~2.5微米,波数为12500~4000厘米-1;(2)中红外的波段为2.5~25微米,波数为4000~400厘米-1;(3)远红外的波段为25~1000微米,波数为400~10厘米,目前,实验上已能测定到2500微米,波数为4厘米-1。相应地有近红外光谱、中红外光谱和远红外光谱。 红外光谱的形式虽然多种多样,从本质上可分为发射光谱和吸收光谱两大类。物体的红外发射光谱是指样品在通过受激或自发辐射的条件下,所发射的红外光的强度随波长(波数)变化的光谱图,红外发射光谱主要决定于物体的温度和化学组成。吸收光谱是指样品对红外辐射的吸收能力随波长(波数)变化的光谱图,在实验上,使红外光与样品发生相互作用,测定红外光与物质相互作用前后光强的变化与波长(波数)之间的关系, 称红外吸收光谱。 2.分子的振动和转动光谱 对于分子体系而言,其振动和转动是量子化的,其能级差所对应的光子的波长落在红外光范围,因此是红外光谱(拉曼光谱)的主要研究对象。研究指出,红外光谱的研究范围不仅仅局限于分子的振动、转动跃迁,某些特殊体系的电子能级跃迁亦可能落在红外光谱波段范围内,例如,超大规模共轭体系的电子跃迁、某些稀土离子的f-f能级跃迁等等。不过目前绝大多数的红外光谱研究工作仍集中于分子的振动能级跃迁上,以最简单的双原子为例,其振动吸收Eν可近似地表示为: 式中h为普朗克常数;ν为振动量子数(取正整数);n0为简谐振动频率。当ν=0时,分子的能量最低,称为基态。处于基态的分子受到频率为n0的红外射线照射时,分子吸收了能量为n0的光量子,跃迁到第一激发态,得到频率为n0的红外吸收带, 它称为分子振动的基频。反之,处于该激发态的分子也可发射频率为n0的红外射线而恢复到基态。n0的数值决定于分子的约化质量μ和力常数κ: κ决定于原子的核间距离、原子的特性和化学键及键级等。 在多原子分子体系中,各原子在平衡位置附近作相对运动。这些振动方式可以被分解为各种简正振动的线性组合,所谓简正振动就是指分子中各原子以同一频率、同一相位在平衡位置附近作简揩振动。含N个原子的非线分子有3N-6个简正振动方式;线性分子有3N-5种简正振动方式。 对于分子的转动而言,往往可以假定分子为刚性转子,则其转动能量Er为: 红外光谱分析概述(中)
第2章红外光谱 通常红外光谱(infrared spectroscopy, IR)就是指波长2~25 μm的吸收光谱(即中红外区),这段波长范围反映出分子中原子间的振动与变角运动。分子在振动的同时还会发生转动运动,虽然分子的转动所涉及的能量变化较小,处在远红外区域,但转动运动影响振动的偶极矩变化,因而在红外光谱区实际所测的谱图就是分子的振动与转动运动的加与表现,因此红外光谱又称为分子振转光谱。 红外光谱可以应用于化合物分子结构的测定、未知物鉴定以及混合物成分分析。 2、1 红外光谱的基本原理 2、1、1 红外吸收光谱 1、当一束具有连续波长的红外光通过物质,物质分子中某个基团的振动频率或转动频率与红外光的频率一样时,分子就吸收能量由原来的基态振(转)动能级跃迁到能量较高的振(转)动能级,分子吸收红外辐射后发生振动与转动能级的跃迁,该处波长的光就被物质吸收。 波谱区近红外光中红外光远红外光 波长/m 0、75~2、5 2、5~50 50~1000 波数/cm-113333~4000 4000~200 200~10 跃迁类型分子振动分子转动 中红外区:绝大多数有机与无机化合物的基频吸收所在,主要就是振动能级的跃迁; 远红外区:分子纯转动能级跃迁及晶体的晶格振动。 3、波数()单位就是cm-1。波长与波数的关系就是: 4、胡克定律: 其中:——折合质量,,单位为kg; ——化学键力常数,与化学键的键能呈正比,单位为N·m-1; ——波数; ——真空中的光速。 (1)因为,红外频率。 (2)与碳原子城建的其她原子,随着其原子质量的增大,折合质量也增大,则红外波数减小。 (3)与氢原子相连的化学键的折合质量都小,红外吸收在高波数区。 (4)弯曲振动比伸缩振动容易,弯曲振动的K均较小,故弯曲振动吸收在低波数区。 5、光谱选律:原子与分子与电磁波作用发生能级跃迁就是要服从一定的规律的,这些规律由量子化学解释。量子化学解得与体系振动量子数(v)相对应的体系能量(E)为: (v = 0, 1, 2, 3…) 简谐振动光谱选律为:,即跃迁必须在相邻震动能级之间进行。
红外光谱分析 序言 二十世纪初叶,Coblentz发表了一百多个有机化合物的红外光谱图,给有机化学家提供了鉴别未知化合物的有力手段。到四十年代红外光谱技术得到了广泛的研究和应用。当今红外光谱仪的分辨率越来越高,检测范围扩展到10000-200cm-1,样品量少至微克级。红外光谱提供的某些信息简捷可靠,检测样品中有无羰基及属于哪一类(酸酐、酯、酮或醛)是其他光谱技术难以替代的。因此,对从事有机化合物为研究对象的化学工作者来说,红外光谱学是必需熟悉和掌握的一门重要光谱知识。 一、基本原理 1、基本知识 光是一种电磁波。可根据电磁波的波长范围分成不同类型的光谱,它们各自反映出物质的不同类型的运动形式。表1列出这些电磁波的波长,其所在区域的光谱名称,以及对应的运动形式。
红外光谱研究的内容涉及的是分子运动,因此称之为分子光谱。 通常红外光谱系指2-25μ之间的吸收光谱,常用的为中红外区4000-650cm-1(2.5-15.4μ)或4000-400cm-1。 这段波长范围反映出分子中原子间的振动和变角振动,分子在振动运动的同时还存在转动运动。在红外光谱区实际所测得的图谱是分子的振动与转动运动的加合表现,即所谓振转光谱。 每一化合物都有其特有的光谱,因此使我们有可能通过红外光谱对化合物作出鉴别。 红外光谱所用的单位波长μ,波数cm-1。光学中的一个基本公式是λυ= C,式中λ为波长,υ为频率,C为光速(3×1010cm/s)。设υ为 波数,其含义是单位长度(1cm)中所含的波的个数,并应具有以下关系:波数(cm-1)=104/波长(μ) 波长和波数都被用于表示红外光谱的吸收位置,即红外光谱图的横坐标。目前倾向于普遍采用波数为单位,而在图谱上方标以对应的波长值。红外光谱图的纵坐标反映的是吸收强度,一般以透过率(T%)表示。 2、红外光谱的几种振动形式 主要的基本可以分为两大类:伸缩振动和弯曲振动。 (1)伸缩振动(υ) 沿着键轴方向伸或缩的振动,存在对称与非对称两种类型。它的吸收频率相对在高波数区。 (2)弯曲振动(δ) 包括面内、面外弯曲振动,变角振动,摇摆振动等。它的吸收频率相对在低波数区。 4000cm-1(高) 400cm-1(低)
常规样品的红外光谱分析 PB07206298龚智良 实验目的 1.初步掌握两种基本样品制备技术及傅立叶变换光谱仪器的简单操作; 2.通过图谱解析及标准谱图的检索,了解由红外光谱鉴定未知物的一般过程。 实验原理 红外光谱:红外光谱是分子的振动转动光谱,也是一种分子吸收光谱。当样品受到频率连续变化的红外光照射时,分子吸收了某些频率的辐射,并由其振动或转动引起的偶极矩的净变化,产生分子振动和转动能级从基态到激发态的跃迁,使相应于这些区域的光透射强度减弱。记录红外光的百分透射比或波长关系曲线,就得到红外光谱。从分子的特征吸收可以鉴定化合物和分子结构,进行定性和定量分析。红外光谱尤其在物质定性分析中应用广泛,它操作简便,分析速度快,样品用量少且不破坏样品,能提供丰富的结构信息,因此红外光谱法往往是物质定性分析中优先考虑的手段。 能产生红外吸收的分子为红外活性分子,如CO?分子;不能产生红外吸收的分子为非红外活性分子,如O?分子。 中红外区为基本振动区:4000-400cm-1研究应用最多。 红外吸收的波数与相应振动的力常数关系密切。双原子分子的基本频率计算公式为 ??=12????? 其中?为约化质量 μ=m??m? m?+m? 对于多原子分子,其振动可以分解为许多简单的基本振动,即简正振动。一般将振动形式分为两类:伸缩振动和变形振动。 各种振动都具有各自的特征吸收。 仪器结构和测试技术 Fourier变换红外光谱仪(FTIR仪):能够同时测定所有频率的信息,得到光强随时间变化的谱图,称时域图,这样可以大大缩短扫描时间。由于不采用传统的色散元件,其分辨率和波数精度都较好。傅立叶变换红外谱仪主要由光源(硅碳棒、高压汞灯)、Michellson干涉仪、检测器、计算机和记录仪组成。测试样品时,由于样品对某些频率的红外光吸收,从而得到不同样品的干涉图。红外光是复合光,检测器接收到的信号是所有频率的干涉图的加合。 对试样的要求:试样应该为纯物质,纯度大于98%,以便于和纯化合物进行比较;样品中不能含游离水;试样的浓度和测试厚度应选择适当,以使大多数吸收峰的透射比处于10%-80%。 制样方法:对于液体样品有液膜法、液体吸收池法;对于固体样品有压片法、糊状法;对于特殊的样品还有薄膜法(包括熔融法和热压成膜法、溶液制膜法);对于气态样品一般都灌注于气体池中进行测试。 除了常规的测试技术外,红外光谱测试还有衰减全发射和偏振红外光谱等特殊的测试技术。 实验步骤、现象及讨论 固体样品制备:使用KBr压片法。用一个玛瑙研钵将少量KBr晶体充分研磨后加入其量5%左右的待测固体样品,混合研磨直至均匀,并使其颗粒大小比所检测的光波长更小(约2μm以下)。在一个具有抛光面的金属模具上方一个圆形纸环,用刮勺将研磨好的粉末移至环中,盖上另一块模具,放入油压机中进行压片。KBr压片形成后,用夹具固定测试。注意样品制备过程中一定要将粉末研得足够细,判断的标准是粉末粘在研钵壁上比较紧。整个操作过程在红外灯下进行,这样可以减少样品制备过程中吸水的量。在制备固体样品之前,要用酒精棉球把刮勺、研钵、研杵擦干净。 液体样品的制备:取一对NaCl窗片,用刮勺沾一滴未知液体在一块窗片上,然后用另外一块窗片覆
1.下列羰基化合物中,C=O伸缩振动频率出现最高的是:() (A)RCOF (B)RCOCl (C)RCOH (D)RCOR 2.在醇类化合物中,O-H伸缩振动频率随溶液C上升,向低波数方向移动的原因是()(A)溶液极性增加(B)诱导效应增加(C)分子间氢键的增加(D)易产生振动偶合 3.一种氯苯的红外谱图在900cm-1~690cm-1间无吸收带,它的可能结构为:() (A)对二氯苯(B)间三氯苯(C)六氯苯(D)四取代氯苯 4.CO2的平动、转动、振动的自由度分别为:() (A)324 (B)234 (C)342 (D)423 5.乙炔分子的平动、转动、振动自由度为() A. 2, 3, 3 B. 3, 2, 8 C. 3, 2, 7 D. 2, 3, 7 6.分子式为C7H11N2OSCl的不饱和度Ω为:() (A)1 (B)2 (C)3 (D)4 7.下面四种气体无红外吸收光谱的为() (A)H2O (B)CO2(C)HCl (D)N2 8. 红外光谱法中的红外吸收带的波长位置与吸收谱带的强度, 可以用来() A. 鉴定未知物的结构组成或确定其化学基团及进行定量分析与纯度鉴定; B. 确定 配位数; C. 研究化学位移; D. 研究溶剂效应. 9. 下列哪种方法是由外层电子跃迁引起的?( ) A. 原子发射光谱和紫外吸收光谱 B. 原子发射光谱和核磁共振谱 C. 红外光谱和Raman光谱 D. 原子光谱和分子光谱 10. 同时具有红外活性和拉曼活性的是:( ) A. O2对称伸缩振动 B.CO2的不对称伸缩振动 C. H2O的弯曲振动 D. CS2的弯曲振动 11. 分子不具有红外活性的者,必须是:( ) A:分子的偶极矩为零B:分子没有振动C:非极性分子D:分子振动时没有偶极矩变化E:双原子分子 12 .试比较以下五个化合物,羰基伸缩振动的红外吸收波数最大者是:( ) A: B: C: D: E: 13.以下五个化合物羰基伸缩振动的红外吸收波数最小的是:( ) A: B: C: D: E:
红外光谱分析概述 1.红外光谱红外光谱是反映红外辐射强度或其他与之相关性质随波长(波数)变化的谱图。目前,它是一种被广泛应用于研究表征物质的化学组成,在分子层次上的结构及分子间相互作用的有力手段。红外射线发现于1800年,在用普通温度计测量可见光谱的温度效应时,在红光一端的外侧观察到有较强的热效应。后来,实验证实了这是由一种肉眼看不见、波长比红光更长的电磁辐射所造成的,这种电磁辐射被称为红外光。通常将红外辐射的波长范围定为0.8~1000微米,并可粗略地分为三个波段:(1)近红外的波段为0.8~2.5微米,波数为12500~4000厘米-1;(2)中红外的波段为2.5~25微米,波数为 (3)远红外的波段为25~1000微米,波数为400~4000~400厘米-1; 10厘米,目前,实验上已能测定到2500微米,波数为4厘米-1。相应地有近红外光谱、中红外光谱和远红外光谱。 红外光谱的形式虽然多种多样,从本质上可分为发射光谱和吸收光谱两大类。物体的红外发射光谱是指样品在通过受激或自发辐射的条件下,所发射的红外光的强度随波长(波数)变化的光谱图,红外发射光谱主要决定于物体的温度和化学组成。吸收光谱是指样品对红外辐射的吸收能力随波长(波数)变化的光谱图,在实验上,使红外光与样品发生相互作用,测定红外光与物质相互作用前后光强的变化与波长(波数)之间的关系, 称红外吸收光谱。 2.分子的振动和转动光谱
对于分子体系而言,其振动和转动是量子化的,其能级差所对应的光子的波长落在红外光范围,因此是红外光谱(拉曼光谱)的主要研究对象。研究指出,红外光谱的研究范围不仅仅局限于分子的振动、转动跃迁,某些特殊体系的电子能级跃迁亦可能落在红外光谱波段范围内,例如,超大规模共轭体系的电子跃迁、某些稀土离子的f-f 能级跃迁等等。不过目前绝大多数的红外光谱研究工作仍集中于分子的振动能级跃迁上,以最简单的双原子为例,其振动吸收Eν可近似地表示为: 式中h为普朗克常数;ν为振动量子数(取正整数);ν0为简谐振动频率。当ν=0时,分子的能量最低,称为基态。处于基态的分子受到频率为ν0的红外射线照射时,分子吸收了能量为ν0的光量子,跃迁到第一激发态,得到频率为ν0的红外吸收带, 它称为分子振动的基频。反之,处于该激发态的分子也可发射频率为ν0的红外射线而恢复到基态。ν0的数值决定于分子的约化质量μ和力常数κ: κ决定于原子的核间距离、原子的特性和化学键及键级等。 在多原子分子体系中,各原子在平衡位置附近作相对运动。这些振动 方式可以被分解为各种简正振动的线性组合,所谓简正振动就是指分子中各原子以同一频率、同一相位在平衡位置附近作简揩振动。含N 个原子的非线分子有3N-6个简正振动方式;线性分子有3N-5种简正振动方式。 对于分子的转动而言,往往可以假定分子为刚性转子,则其转动能量Er为: J=0,1,2,3,…,n
红外光谱分析 二十世纪初叶,Coblentz 发表了一百多个有机化合物的红外光谱图,给有机化学家提供了鉴别未知化合物的有力手段。到四十年代红外光谱技术得到了广泛的研究和应用。当今红外光谱仪的分辨率越来越高,检测范围扩展到10000-200cm-1,样品量少至微克级。红外光谱提供的某些信息简捷可靠,检测样品中有无羰基及属于哪一类(酸酐、酯、酮或醛)是其他光谱技术难以替代的。因此,对从事有机化合物为研究对象的化学工作者来说,红外光谱学是必需熟悉和掌握的一门重要光谱知识。 一、基本原理 1、基本知识 光是一种电磁波。可根据电磁波的波长范围分成不同类型的光谱,它们各自反映出物质的不同类型的运动形式。表1 列出这些电磁波的波长,其所在区域的光谱名称,以及对应的运动形式。 表1 常用的有机光谱及对应的微观运动
红外光谱研究的内容涉及的是分子运动,因此称之为分子光谱。通常红外光谱系指2-25 μ之间的吸收光谱,常用的为中红外区4000-650cm-1(2.5-15.4 μ) 或4000-400cm-1。 这段波长范围反映出分子中原子间的振动和变角振动,分子在振 动运动的同时还存在转动运动。在红外光谱区实际所测得的图谱是分 子的振动与转动运动的加合表现,即所谓振转光谱。 每一化合物都有其特有的光谱,因此使我们有可能通过红外光谱 对化合物作出鉴别。 红外光谱所用的单位波长μ,波数cm-1。光学中的一个基本公式是λυ= C,式中λ为波长,υ为频率,C 为光速(3 ×1010cm/s) 。设υ为波数,其含义是单位长度(1cm) 中所含的波的个数,并应具有以下关系:波数(cm-1) =104/ 波长( μ)波长和波数都被用于表示红外光谱的吸收位置,即红外光谱图的横坐标。目前倾向于普遍采用波数为单位,而在图谱上方标以对应的 波长值。红外光谱图的纵坐标反映的是吸收强度,一般以透过率(T%) 表示。 2、红外光谱的几种振动形式 主要的基本可以分为两大类:伸缩振动和弯曲振动。 (1)伸缩振动( υ) 沿着键轴方向伸或缩的振动,存在对称与非对称两种类型。它的 吸收频率相对在高波数区。 (2)弯曲振动( δ) 包括面内、面外弯曲振动,变角振动,摇摆振动等。它的吸收频率相对在低波数区。 4000cm -1(高) 400cm -1(低) 3、红外光谱吸收峰主要的几种类型 (1)基频峰:伸缩振动,弯曲振动产生的吸收峰均为基频峰。 (2)倍频峰:出现在基频峰波数二倍处。如基频为900cm-1,倍频为
红外光谱谱图质量影响因素汇总 1、扫描次数对红外谱图的影响:傅里叶变换红外光谱仪测量物质的光谱时, 检测器在接受样品光谱信号的同时也接受了噪声信号, 输出的光谱既包括样品的信号也包括噪声信号。 信噪比:与扫描次数的平方成正比。增加扫描次数可以减少噪声、增加谱图的光滑性。 2、扫描速度对红外谱图的影响:扫描速度减慢, 检测器接收能量增加; 反之, 扫描速度加快, 检测器接收能量减小。当测量信号小时( 包括使用某些附件时) 应降低动镜移动速度, 而在需要快速测量时,提高速度。扫描速度降低, 对操作环境要求更高, 因此应选择适当的值。 采用某一动镜移动速度下的背景, 测定不同扫描速度下样品的吸收谱图, 随扫描速度的加快, 谱图基线向上位移。用透射谱图表示时,趋势相反。所以在实验中测量背景的扫描速度与测量样品的扫描速度要一致。 3、分辨率对红外谱图的影响:红外光谱的分辨率等于最大光程差的倒数, 是由干涉仪动镜移动的距离决定的, 确切地说是由光程差计算出来的。分辨率提高可改善峰形, 但达到一定数值后, 再提高分辨率峰形变化不大, 反而噪声增加。分辨率降低可提高光谱的信噪比, 降低水汽吸收峰的影响, 使谱图的光滑性增加。 样品对红外光的吸收与样品的吸光系数有关,如果样品对红光外有很强的吸收, 就需要用较高的分辨率以获得较丰富的光谱信息;如果样品对红光外有较弱的吸收, 就必须降低光谱的分辨率、提高扫描次数以便得到较好的信噪比。 4、数据处理对红外谱图质量的影: (1)平滑处理:红外光谱实验中谱图常常不光滑,影响谱图质量。不光滑的原因除了样品吸潮以外还有环境的潮湿和噪声。平滑是减少来自各方面因素所产生的噪声信号, 但实际是降低了分辨率, 会影响峰位和峰强, 在定量分析时需特别注意。 (2)基线校正:在溴化钾压片制样中由于颗粒研磨得不够细或者不够均匀, 压出的锭片不够透明而出现红外光散射, 所以不管是用透射法测得的红外光谱,还是用反射法测得的光谱, 其光谱基线不可能在零基线上, 使光谱的基线出现漂移和倾斜现象。需要基线校正时,首先判断引起基线变化的原因, 能否进行校正。基线校正后会影响峰面积, 定量分析要慎重。 (3)样品量的控制对谱图的影响:在红外光谱实验中, 固体粉末样品不能直接压片, 必须用稀释剂稀释、研磨后才能压片。稀释剂溴化钾与样品的比例非常重要, 样品太少不行,样品太多则信息太丰富而特征峰不突出, 造成分析困难或吸收峰成平顶。对于白色样品或吸光系数小的样品, 稀释剂溴化钾与样品的比例是100:1; 对于有色样品或吸光系数大的样品稀释剂溴化钾与样品的比例是150:1。 5、影响吸收谱带的因素还有分子外和分子内的因素:如溶剂不同, 振动频率不同, 溶剂的极性不同, 介电常数不同, 引起溶质分子振动频率不同, 因为溶剂的极性会引起溶剂和溶 质的缔合, 从而改变吸收带的频率和强度。氢键的形成使振动频率向低波数移动、谱带加宽和强度增强(分子间氢键可以用稀释的办法消除, 分子内氢键不随溶液的浓度而改变)。 6、影响吸收谱带的其他因素还有:共轭效应、张力效应、诱导效应和振动耦合
有机化合物的红外光谱分析 系别:化学物理系 学号:PB09206108 姓名:倪宇飞
有机化合物的红外光谱分析 一、实验目的 (1)初步掌握两种基本样品制备技术及傅立叶变换红外光谱仪的简单操作。 (2)通过谱图解析及标准谱图的检索,了解由红外光谱鉴定未知物的一般过程。 二、实验原理 (1)原理概述 物质分子中的各种不同基团,在有选择的吸收不同频率的红外辐射后,发生振动能级之间的跃迁,形成各自独特的红外吸收光谱。据此,可对物质进行定性和定量的分析。特别是对化合物结构的分析,应用更为广泛。 (2)对试样的要求 A.试样应该是单一组分的纯物质,纯度应大于98%,便于与纯化合物的标准进行 对照,多组分试样应尽量在测试前预先用分馏、萃取、重结晶、区域熔融和色谱法进行分离提纯; B.试样中不应含有游离水。本身水有红外吸收,会严重干扰样品的谱图,而且会 侵蚀吸收池的盐窗,游离水的吸收为止约为3400cm-1以及1630cm-1; C.试样的浓度和测试厚度应该选择适当,以使光谱图中的大多数吸收峰透射比处 于10%~80%范围内。 (3)制样方法 本次实验中的提供了固体和液体两种未知待测样品,因此有针对性的采用了两种制样方法 A.液膜法 对于沸点较高的的液体,直接将样品滴在两块NaCl盐窗之间,形成没有气泡的毛细厚度液膜,之后用夹具固定,放入仪器的光路中进行测试。本实验中由于液体的流动性较差,故只用一片盐窗即可; B.KBr压片法,将1~2mg固体试样与200mg纯KBr研细混合,研磨至粒径小 于2微米,在油压机上压成透明薄片即可用于测定。 (4)仪器工作原理 傅立叶变换红外光谱仪主要由光源(硅碳棒、高压汞灯)、Michelson干涉仪、检测器、计算机和记录仪组成
红外光谱的吸收
第六章红外吸收光谱法 基本要点: 1. 红外光谱分析基本原理; 2. 红外光谱与有机化合物结构; 3. 各类化合物的特征基团频率; 4. 红外光谱的应用; 5. 红外光谱仪. 学时安排:3学时 第一节概述 分子的振动能量比转动能量大,当发生振动能级跃迁时,不可避免地伴随有转动能级的跃迁,所以无法测量纯粹的振动光谱,而只能得到分子的振动-转动光谱,这种光谱称为红外吸收光谱。 红外吸收光谱也是一种分子吸收光谱。 当样品受到频率连续变化的红外光照射时,分子吸收了某些频率的辐射,并由其振动或转动运动引起偶极矩的净变化,产
生分子振动和转动能级从基态到激发态的跃迁,使相应于这些吸收区域的透射光强度减弱。记录红外光的百分透射比与波数或波长关系曲线,就得到红外光谱。 一、红外光区的划分 红外光谱在可见光区和微波光区之间,波长范围约为 0.75 ~ 1000μm,根据仪器技术和应用不同,习惯上又将红外光区分为三个区:近红外光区(0.75 ~ 2.5μm ),中红外光区(2.5 ~25μm ),远红外光区(25 ~ 1000μm )。 近红外光区(0.75 ~ 2.5μm ) 近红外光区的吸收带主要是由低能电子跃迁、含氢原子团(如O—H、N—H、C—H)伸缩振动的倍频吸收等产生的。该区的光谱可用来研究稀土和其它过渡金属离子的化合物,并适用于水、醇、某些高分子化合物以及含氢原子团化合物的定量分析。中红外光区(2.5 ~ 25μm ) 绝大多数有机化合物和无机离子的基频吸收带出现在该 光区。由于基频振动是红外光谱中吸收最强的振动,所以该区最适于进行红外光谱的定性和定量分析。同时,由于中红外光谱仪最为成熟、简单,而且目前已积累了该区大量的数据资料,因此它是应用极为广泛的光谱区。通常,中红外光谱法又简称为红外光谱法。 远红外光区(25 ~ 1000μm )该区的吸收带主要是由气体分子中的纯转动跃迁、 振动-转动跃迁、液体和固体中重原子的伸缩振动、某些变角振动、骨架振动以及晶体中的晶格振动所引起的。由于低频骨架振动能很灵敏地反映出结构变化,所以对异构体的研究特别方便。此外,还能用于金属有机化合物(包括络合物)、氢键、吸附现象的研究。但由于该光区能量弱,除非其它波长区间内没有合适的分析谱带,一般不在此范围内进行分析。 红外吸收光谱一般用T~ 曲线或T~ 波数曲线表示。纵坐标
第六章红外吸收光谱法 一选择题 1分子光谱是由于___B___而产生的。 A 电子的发射 B 电子相对于原子核的运动以及核间相对位移引起的振动和转动 C 质子的运动 D 离子的运动 2溶剂对电子光谱的影响较为复杂,改变溶剂的极性,__B_____。 A 不会引起吸收带形状的变化 B 会使吸收带的最大吸收波长发生变化 C 精细结构并不消失 D 对测定影响不大 3红外光谱法中的红外吸收带的波长位置与吸收谱带的强度,可以用来_____A__。 A 鉴定未知物的结构组成或确定其化学基团及进行定量分析与纯度鉴定 B 确定配位数 C 研究化学位移 D 研究溶剂效应 4红外光谱的谱带较多,能较方便地对单组分或多组分进行定量分析,但红外光谱法的灵敏度较低,尚不适于____B___的测定。 A 常量组分 B 微量组分 C 气体试样 D 固体和液体试样 5 在有机化合物的红外吸收光谱分析中,出现在4000~1350cm-1频率范围的吸收峰可用于鉴定官能团,这一段频率范围称为_____A_。 A.指纹区,B.基团频率区,C.基频区,D.和频区。 6光学分析法主要根据物质发射、吸收电磁辐射以及物质与电磁辐射的相互作用来进行分析的。电磁辐射(电磁波)按其波长可分为不同区域,其中中红外区
波长为B______。 A 12820~4000cm-1 B 4000~200 cm-1 C 200~33 cm-1 D 33~10 cm-1 7 下列羰基化合物中C=O伸缩振动频率最高的是:C A RCOR’ B RCOCl C RCOF D RCOBr 8. 红外光谱法中的红外吸收带的波长位置与吸收谱带的强度,可以用来____A___。 A. 鉴定未知物的结构组成或确定其化学基团及进行定量分析与纯度鉴定; B. 确定配位数; C. 研究化学位移; D. 研究溶剂效应. 二填空题 1 共轭效应使共轭体具有共面性,且使电子云密度平均化,造成双键略有伸长,单键略有缩短。因此,双键的红外吸收频率往___低_____波数方向移动。 2 在化合物R—C—H与R—C—F中,前者的C=O的伸缩振动产生的吸收峰的波数比后者的____低____;而在化合物R—C—R与R—C—NH2中,前者的C=O 的伸缩振动产生的吸收峰的波数比后者的______高__。 3在有机化合物中,常常因取代基的变更或溶剂的改变,使其吸收带的最大吸收波长发生移动,向长波方向移动称为___红(长)移______,向短波方向移动称为_____蓝(短)移______。 4 红外光谱是由于分子振动能级的跃迁而产生,当用红外光照射分子时,要使分子产生红外吸收,则要满足两个条件:(1)_____红外光辐射的频率与分子中某基团的震动频率相同 (2)_在震动的过程中,分子必须有偶极矩的改变 5红外光谱的强度与_______分子或基团的极性强弱______________成正比。
傅里叶红外光谱分析 第一节一般原理 电子能级跃迁所产生的吸收光谱,主要在近紫外区和可见区,称为可见-紫外光谱;键振动能级跃迁所产生的吸收光谱,主要在中红外区,称为红外光谱;自旋的原子核在外加磁场中可吸收无线电波而引起能级的跃迁,所产生的吸收光谱称为核磁共振谱。 第二节紫外光谱 一、紫外光谱的基本原理 用波长范围200 nm~800 nm的光照射含有共轭体系的的不饱和化合物的稀溶液时,部分波长的光被吸收,被吸收光的波长和强度取决于不饱和化合物的结构。以波长l为横座标,吸收度A为纵座标作图,得紫外光谱,或称电子光谱。 是化合物紫外光谱的特征常数。 紫外光谱中化合物的最大吸收波长λ max 可见-紫外光谱适用于分析分子中具有π键不饱和结构的化合物。 二、紫外光谱在有机结构分析中的应用 随着共轭体系的延长,紫外吸收向长波方向移动,且强度增大(π→π*),因此可判断分子中共轭的程度。 利用紫外光谱可以测定化合物的纯度或含量。 第三节红外光谱 一、红外光谱的基本原理 用不断改变波长的红外光照射样品,当某一波长的频率刚好与分子中某一化学键的振动频率相同时,分子就会吸收红外光,产生吸收峰。用波长(λ)或波长的倒数—波数(cm-1)为横坐标,百分透光率(T%)或吸收度(A)为纵坐标做图,得到红外吸收光谱图(IR)。分子振动所需能量对应波数范围在400 cm-1~4000 cm-1。
二、红外吸收峰的位置和强度 分子中的一个化学键可有几种不同的振动形式,而产生不同的红外吸收峰,键的振动分为两大类。 伸缩振动,用n表示,原子间沿键轴方向伸长或缩短。 弯曲振动用δ表示,形成化学键的两个原子之一与键轴垂直方向作上下或左右弯曲。 组成化学键的原子的质量越小,键能越高,键长越短,振动所需能量越大,吸收峰所在的波数就越高。 红外光谱的吸收峰分为两大区域: 4000 cm-1~1330 cm-1区域:特征谱带区,是红外光谱分析的主要依据。 1330 cm-1~650 cm-1区域:指纹区。每一化合物在指纹区都有它自己的特征光谱,对分子结构的鉴定能提供重要信息。 (很强);s(强);m(中强);w(弱);红外吸收峰的强弱用下列符号表示:v s v (很弱);b(宽峰)。 w 凡能使键增强的因素,引起峰位向高波数方向移动,反之,则向低波数方向移动。 三、各类化合物的红外光谱举例 (一)烃类化合物 注:烷烃,即饱和烃,是只有碳碳单键和碳氢键的链烃。烷烃的通式为CnH2n+2。 烯烃是指含有C=C键(碳-碳双键)(烯键)的碳氢化合物,单链烯烃分子通式为CnH2n 炔烃,为分子中含有碳碳三键的碳氢化合物的总称,其官能团为碳-碳三键(C≡C),分子通式为CnH2n-2
总结 当一束具有连续波长的红外光通过物质,物质分子中某个基团的振动频率或转动频率和红外光的频率一样时,分子就吸收能量由原来的基态振(转)动能级跃迁到能量较高的振(转)动能级,分子吸收红外辐射后发生振动和转动能级的跃迁,该处波长的光就被物质吸收。所以,红外红外光谱光谱法实质上是一种根据分子内部原子间的相对振动和分子转动等信息来确定物质分子结构和鉴别化合物的 分析方法。将分子吸收红外光的情况用仪器记录下来,就得到红外光谱图。红外光谱图通常用波长(λ)或波数(σ)为横坐标,表示吸收峰的位置,用透光率(T%)或者吸光度(A)为纵坐标,表示吸收强度。 当外界电磁波照射分子时,如照射的电磁波的能量与分子的两能级差相等,该频率的电磁波就被该分子吸收,从而引起分子对应能级的跃迁,宏观表现为透射光强度变小。电磁波能量与分子两能级差相等为物质产生红外吸收光谱必须满足条件之一,这决定了吸收峰出现的位置。 红外吸收光谱产生的第二个条件是红外光与分子之间有偶合作用,为了满足这个条件,分子振动时其偶极矩必须发生变化。这实际上保证了红外光的能量能传递给分子,这种能量的传递是通过分子振动偶极矩的变化来实现的。并非所有的振动都会产生红外吸收,只有偶极矩发生变化的振动才能引起可观测的红外吸收,这种振动称为红外活性振动;偶极矩等于零的分子振动不能产生红外吸收,称为红外非活性振动。 分子的振动形式可以分为两大类:伸缩振动和弯曲振动。前者是指原子沿键轴方向的往复运动,振动过程中键长发生变化。后者是指原子垂直于化学键方向的振动。通常用不同的符号表示不同的振动形式,例如,伸缩振动可分为对称伸缩振动和反对称伸缩振动,分别用 Vs 和Vas 表示。弯曲振动可分为面内弯曲 振动(δ)和面外弯曲振动(γ)。从理论上来说,每一个基本振动都能吸收与 红外光谱仪其频率相同的红外光,在红外光谱图对应的位置上出现一个吸收峰。实际上有一些振动分子没有偶极矩变化是红外非活性的;另外有一些振动的频率
红外识谱歌 红外可分远中近,中红特征指纹区,1300来分界,注意横轴划分异。看图要知红外仪,弄清物态液固气。样品来源制样法,物化性能多联系。识图先学饱和烃,三千以下看峰形。2960、2870是甲基,2930、2850亚甲峰。1470碳氢弯,1380甲基显。二个甲基同一碳,1380分二半。面内摇摆720,长链亚甲亦可辨。烯氢伸展过三千,排除倍频和卤烷。末端烯烃此峰强,只有一氢不明显。化合物,又键偏,~1650会出现。烯氢面外易变形,1000以下有强峰。910端基氢,再有一氢990。顺式二氢690,反式移至970;单氢出峰820,干扰顺式难确定。炔氢伸展三千三,峰强很大峰形尖。三键伸展二千二,炔氢摇摆六百八。芳烃呼吸很特征,1600~1430。1650~2000,取代方式区分明。900~650,面外弯曲定芳氢。五氢吸收有两峰,700和750;四氢只有750,二氢相邻830;间二取代出三峰,700、780,880处孤立氢醇酚羟基易缔合,三千三处有强峰。C-O伸展吸收大,伯仲叔醇位不同。1050伯醇显,1100乃是仲,1150叔醇在,1230才是酚。1110醚链伸,注意排除酯酸醇。若与π键紧相连,二个吸收要看准,1050对称峰,1250反对称。苯环若有甲氧基,碳氢伸展2820。次甲基二氧连苯环,930处有强峰,环氧乙烷有三峰,1260环振动,九百上下反对称,八百左右最特征。缩醛酮,特殊醚,1110非缩酮。酸酐也有C-O键,开链环酐有区别,开链强宽一千一,环酐移至1250。羰基伸展一千七,2720定醛基。吸电效应波数高,共轭则向低频移。张力促使振动快,环外双键可类比。二千五到三千三,羧酸氢键峰形宽,920,钝峰显,羧基可定二聚酸、酸酐千八来偶合,双峰60严相隔,链状酸酐高频强,环状酸酐高频弱。羧酸盐,偶合生,羰基伸缩出双峰,1600反对称,1400对称峰。1740酯羰基,何酸可看碳氧展。1180甲酸酯,1190是丙酸,1220乙酸酯,1250芳香酸。1600兔耳峰,常为邻苯二甲酸。氮氢伸展三千四,每氢一峰很分明。羰基伸展酰胺I,1660有强峰;N-H变形酰胺II,1600分伯仲。伯胺频高易重叠,仲酰固态1550;碳氮伸展酰胺III,1400强峰显。胺尖常有干扰见,N-H伸展三千三,叔胺无峰仲胺单,伯胺双峰小而尖。1600碳氢弯,芳香仲胺千五偏。八百左右面内摇,确定最好变成盐。伸展弯曲互靠近,伯胺盐三千强峰宽,仲胺盐、叔胺盐,2700上下可分辨,亚胺盐,更可怜,2000左右才可见。硝基伸缩吸收大,相连基团可弄清。1350、1500,分为对称反对称。氨基酸,成内盐,3100~2100峰形宽。1600、1400酸根展,1630、1510碳氢弯。盐酸盐,羧基显,钠盐蛋白三千三。矿物组成杂而乱,振动光谱远红端。钝盐类,较简单,吸收峰,少而宽。注意羟基水和铵,先记几种普通盐。1100是硫酸根,1380硝酸盐,1450碳酸根,一千左右看磷酸。硅酸盐,一峰宽,1000真壮 观。勤学苦练多实践,红外识谱不算难
红外光谱分析 红外光谱与分子的结构密切相关,是研究表征分子结构的一种有效手段,与其它方法相比较,红外光谱由于对样品没有任何限制,它是公认的一种重要分析工具。在分子构型和构象研究、化学化工、物理、能源、材料、天文、气象、遥感、环境、地质、生物、医学、药物、农业、食品、法庭鉴定和工业过程控制等多方面的分析测定中都有十分广泛的应用。 红外光谱可以研究分子的结构和化学键,如力常数的测定和分子对称性等,利用红外光谱方法可测定分子的键长和键角,并由此推测分子的立体构型。根据所得的力常数可推知化学键的强弱,由简正频率计算热力学函数等。分子中的某些基团或化学键在不同化合物中所对应的谱带波数基本上是固定的或只在小波段范围内变化,因此许多有机官能团例如甲基、亚甲基、羰基,氰基,羟基,胺基等等在红外光谱中都有特征吸收,通过红外光谱测定,人们就可以判定未知样品中存在哪些有机官能团,这为最终确定未知物的化学结构奠定了基础。 由于分子内和分子间相互作用,有机官能团的特征频率会由于官能团所处的化学环境不同而发生微细变化,这为研究表征分子内、分子间相互作用创造了条件。 分子在低波数区的许多简正振动往往涉及分子中全部原子,不同的分子的振动方式彼此不同,这使得红外光谱具有像指纹一样高度的特征性,称为指纹区。利用这一特点,人们采集了成千上万种已知化合物的红外光谱,并把它们存入计算机中,编成红外光谱标准谱图库,人们只需把测得未知物的红外光谱与标准库中的光谱进行比对,就可以迅速判定未知化合物的成份。 下面将对红外光谱分析的基本原理做一个简单的介绍。 红外吸收光谱是物质的分子吸收了红外辐射后,引起分子的振动-转动能级的跃迁而形成的光谱,因为出现在红外区,所以称之为红外光谱。利用红外光谱进行定性定量分析的方法称之为红外吸收光谱法。 红外辐射是在 1800年由英国的威廉.赫谢(Willian Hersher) 尔发现的。一直到了1903年,才有人研究了纯物质的红外吸收光谱。二次世界大战期间,由于对合成橡胶的迫切需求,红外光谱才引起了化学家的重视和研究,并因此而迅速发展。随着计算机的发展,以及红外光谱仪与其它大型仪器的联用,使得红外光谱在结构分析、化学反应机理研究以及生产实践中发挥着极其重要的作用,是“四大波谱”中应用最多、理论最为成熟的一种方法。 红外光谱法的特点: 1?气态、液态和固态样品均可进行红外光谱测定;
红外光谱与核磁的分析原理及应用 姓名:贾姸妍 ,学号:201120679,专业:材料化学 摘要红外光谱主要是由于分子振动的非谐振性使分子振动从基态向高能级跃迁时产生的,记录的主要是含氢基团X-H(X=C、N、O)振动的倍频和合频吸收。不同基团(如甲基、亚甲基、苯环等)或同一基团在不同化学环境中的近红外吸收波长与强度都有明显差别,NIR光谱具有丰富的结构和组成信息,非常适合用于碳氢有机物质的组成与性质的测量。核磁共振是指原子核在外加恒力磁场作用下产生能级分裂,从而对特定的电磁波发生共振吸收的现象。因而通过测定和分析受测物质对电磁波的吸收情况就可以判定它含有哪种原子,以及原子之间的距离多大,并据此分析出它的三维结构。本文主要介绍了红外光谱和核磁的分析原理及应用,还对其发展做了展望! 关键词红外光谱核磁共振原理应用展望 一、红外光谱 1.1 红外光谱概述 物质分子吸收红外线(中红外区、即基本振动-转动区)产生吸收光谱,主要是由于振动和转动能级跃迁引起的,因此红外吸收光谱又称振转光谱。 1.2 红外光谱的表示方法 纵坐标为吸收强度,透过率(T %)或吸光度(A),横坐标为吸收峰的位置,用波长λ(m )或波数1/λ单位:cm-1,可以用峰数,峰位,峰形,峰强来描述。 应用:有机化合物的结构解析。定性:基团的特征吸收频率;定量:特征峰的强度。
1.3 红外吸收光谱产生的条件 1. 红外辐射光的频率与分子振动的频率相当,才能满足分子振动能级跃迁所需的能量,而产生吸收光谱。△E=E激 - E基 = △V ×h ×v,△V =±1,△V 是振动光谱的跃迁选率,IR主要观察的是 V=0→ V=1的吸收峰,其振动频率等于红外辐射的频率,称为基频峰。 2. 振动过程中必须是能引起分子偶极矩变化的分子才能产生红外吸收光谱。对称分子:没有偶极矩,辐射不能引起共振,无红外活性。如:N2、O2、Cl2 等。非对称分子:有偶极矩,红外活性。 值得注意的是:不是所有的振动都能引起红外吸收,只有偶极矩(μ)发生变化的,才能有红外吸收。 1.4 红外光谱图的分析步骤 (1)首先依据谱图推出化合物碳架类型:根据分子式计算不饱和度,公式: 不饱和度Ω=n 4+1+(n 3 -n 1 )/2其中: n 4 :化合价为4价的原子个数(主要是C原子), n 3 :化合价为3价的原子个数(主要是N原子), n 1 :化合价为1价的原子个数(主要是H,X原子) (2)分析3300~2800 cm-1区域C-H伸缩振动吸收;以3000 cm-1为界:高于3000 cm-1为不饱和碳C-H伸缩振动吸收,有可能为烯,炔,芳香化合物,而低于3000 cm-1一般为饱和C-H伸缩振动吸收; (3)若在稍高于3000 cm-1有吸收,则应在 2250~1450 cm-1频区,分析不饱和碳碳键的伸缩振动吸收特征峰,其中: 炔 2200~2100 cm-1 烯 1680~1640 cm-1 芳环 1600,1580,1500,1450 cm-1 若已确定为烯或芳香化合物,则应进一步解析指纹区,即1000~650 cm-1的频区,以确定取代基个数和位置(顺反,邻、间、对); (4)碳骨架类型确定后,再依据其他官能团,如 C=O, O-H, C-N 等特征吸收来判定化合物的官能团;