
1.目的
规范ABI 7500荧光定量PCR仪操作,保证安全操作,延长仪器寿命
2.范围
适用于ABI 7500荧光定量PCR仪
3.职责
操作人负责本规程实施,部门负责人监督实施。
4.规程
4.1 实验程序运行:
4.1.1首先打开电脑,进入操作系统后,打开ABI 7500荧光定量PCR仪电源。双击桌面上7500 software V2.0.6。弹出Login对话框,默认的User Name为GUEST,点击Login as GUEST,点击OK运行软件。
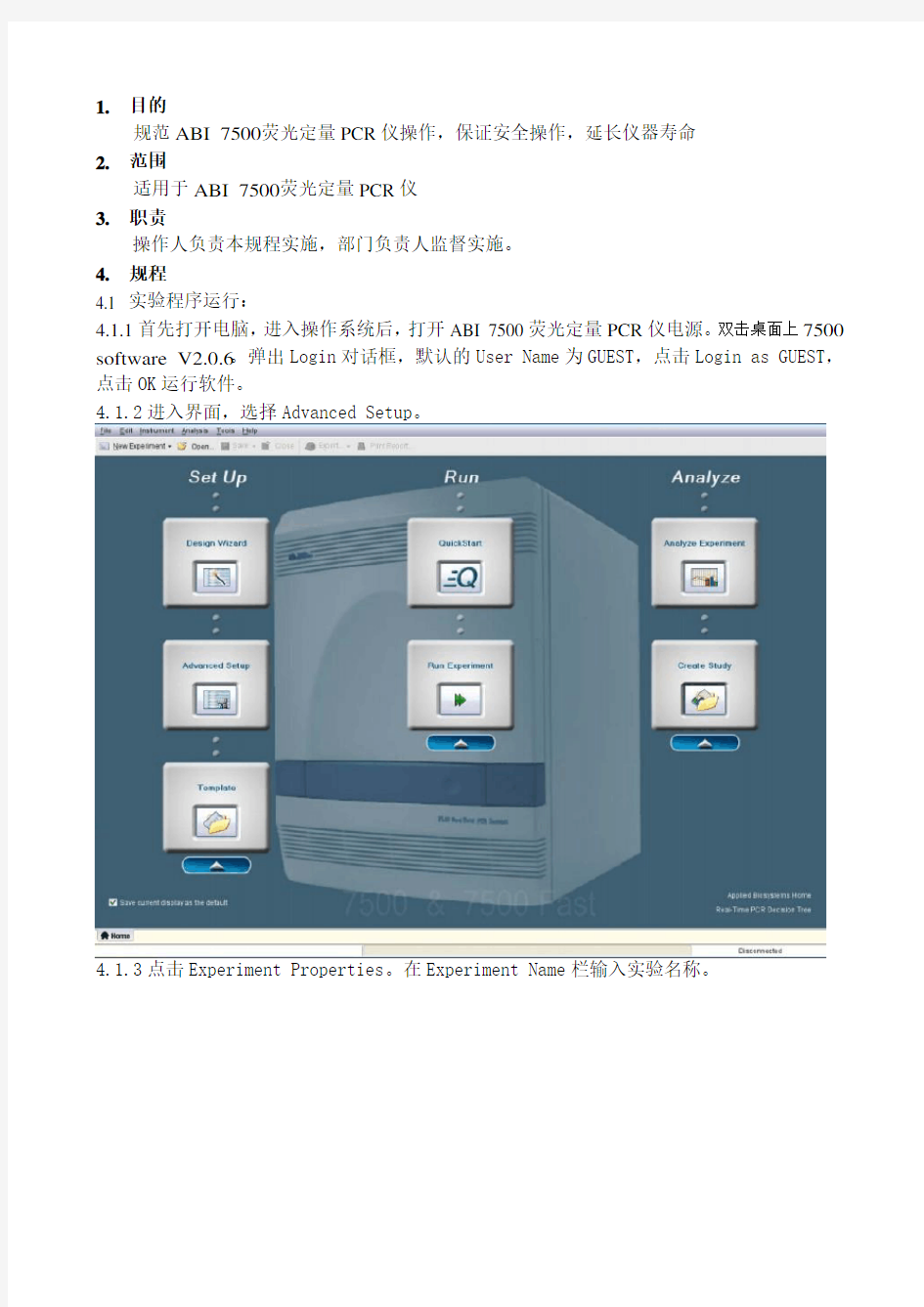
4.1.2进入界面,选择Advanced Setup。
4.1.3点击Experiment Properties。在Experiment Name栏输入实验名称。
4.1.4点击Plate Setup,点击Define Targets as Samples。设定Target Name的Reporter 为FAM。
4.1.5点击Assign Targets and Samples。设定96孔板。
4.1.5点击Run Method。设定反应程序。
4.1.6点击Reaction Setup设定反应体系。
4.1.7点击Run菜单,点击START RUN。开始运行PCR反应。
4.1.8点击Analysis开始分析实验数据。点击Amplification Plot,可以看到扩增曲线。点击Plate Layout的View Well Table可以看到CT值。
4.2 ABI7500荧光定量PCR仪使用及维护注意事项
4.2.1 实验室的环境:
a.电源:UPS或稳压器。
b.通风:仪器的通风应该没有阻挡。
c.温度:实验室应该配有空调。
d.湿度:20-80%。
e.空间:易于操作,安全。
4.2.2 关闭并打开计算机和仪器电源开关:
如果主机和计算机一直在开机使用,每周应该进行一次以下操作:关闭主机电源开关,关闭计算机,然后重新打开计算机和仪器电源开关。
4.2.3 使用不脱毛的布块擦拭仪器表面:重要!切勿使用有机溶剂清洁ABI7500荧光定量PCR仪。每周一次。
4.2.4 执行背景校正(Background calibration):使用背景校正板。每月一次。
4.2.5 执行纯荧光校正(Pure Dye Calibration):使用纯荧光反应板。每半年一次。
4.2.6 执行目标区(ROI)校正:使用ROI校正反应板。每半年一次。
4.2.7 去除样本块中的污染物(需要时):当一个或多个反应孔连续显示出不正常的高信号,并表明可能存在荧光污染物时,可执行此步骤。
4.2.8 确认已去除样本块中的污染物:运行背景校正板,确认污染已除去,并使用最新的背景校正。清洗样本块后。
4.2.9更换卤素灯:重要!当您拿取卤素灯时,需要时请戴上无粉手套。
5.相关文件:无
6.记录:
6.1《设备使用记录》FSD-ER-003
6.2《设备仪器维修保养记录》FSD-ER-021
药品微生物限度检验方法标准操作规程
标准操作规程 目的:建立一个药品微生物限度检验标准操作规程。 范围:适用于本企业生产的所有品种,本企业所有洁净生产区域,QC微生物限度检查室,洁净工作室等。 责任者:QC主任、化验员。 规程: 本规程引至《中国药典》2000年版。 1. 概述:微生物限度检查系指非规定灭菌制剂及其原辅料受到微生物污染程度的一种检查方法,包括染菌量及控制菌的检查。我公司QC设无菌操作室,用于微生物限度检查。无菌操作室的管理及使用制度见本文附录一。 2. 抽样:供试品应按批号随即抽样,一般抽样量为检验用量(2个以上最小包装单位)的3倍。抽样时,凡发现有异常可疑的样品,应缺陷选用疑问的样品,但因机构损伤明显破裂的包装不得作为样品,凡已能从药品、瓶口(外盖内侧及瓶口周围)外观看出长螨、长霉、虫蛀及变质的药品,可直接判为不合格,无需要再抽样检验。 3. 供试品的保存:供试品在检验之前,应保存在阴凉干燥处,以防供试品中的污染菌因保藏条件所引起致死、损伤或繁殖。供试品在检验之前,应该保持原有包装状态,严禁开启,包装已开启的样品不得作为供试品。 4. 检查: 4.1. 使用设备:电热恒温培养箱、电热恒温水温箱、试管、刻度吸管、量筒、三角瓶、培养皿、试管架、注射器、针头、注射器盒、研钵、75%酒精棉球、紫外灯(365nm波长)。 4.2. 检查的全过程应严格遵守无菌操作,严防再污染。使用设备、仪器、人员及无菌操作室常用的消毒、灭菌方法见本文附录二。除另有规定外,供试品制备成供试液后,均在均匀状态取样。制成供试液后,应该在60分
钟内注皿操作完毕。 标准操作规程 4.3. 培养:除另有规定外,本检查法中细菌培养温度为30-35℃,霉菌、酵母菌培养温度为25-28℃,控制菌培养温度为36±1℃,检验结果的报告以1g、1ml或10cm2为单位。 4.4. 复检 4.4.1. 菌数测定不合格者应复检,控制菌检查以一次检出为准,不再复试,但应保留检出菌株一个月备查。 4.4.2. 以复试项下不合格项目为准,作单项复试。复试需另取同批号样品,测定2次。 4.4.3. 复试报告,以3次测定结果的算术平均值报告。 4.5. 检验报告 4.5.1. 检验报告以1g、1ml或10cm2为单位。 4.5.2. 测定菌数报告,以每次测定结果全部平均值报告。 4.5.3. 控制菌按检验结果报告,如未检出控制菌时,报告为“按规定抽样检验结果未检出XX菌”,如抽样中任意一样品要检出控制菌时,报告为“按规定抽样,检出XX菌,不符合药品微生物限度标准。” 4.6. 培养基、试药及稀释剂的相关内容见本文件附录三。 4.7. 供试液的制备:按供试液的理化特性与生物学特性可采取适宜的方法制成供试液。 4.7.1. 供试品的取样及注意事项 供试品取样应有一定数量,以使检验结果具有代表性,正常的供试品一般每批应随机抽取两瓶或两盒以上的包装单位,检验时每次应分取两瓶(盒)以上的样品共10g或10ml。 供试品在检验前,应严格保持包装的原有状态,不得启开,并放在阴凉干燥处,防止微生物再繁殖,以免影响检验结果,凡已将原包装启开,则无代表性应另取样。 供试品稀释后须在1-2小时内操作完毕,防止微生物繁殖或死亡。 供试品稀释成供试液后,应在均匀状态下取样,凡因抑菌或不溶于水的剂型,其供试品应作特殊处理后进行检验。 4.7.2. 液体供试品:取供试品10ml,加入稀释剂90ml中,混匀,作为
ST-360酶标仪标准操作规程 一、目的 为保证ST-360酶标仪的正常运转和使用。 二、范围 适用ST-360酶标仪操作与基本保养。 三、责任 实验室工作人员严格按操作程序执行。 四、定义 ST-360酶标仪是一种8通道垂直光路光密度检测仪,可用来进行标准光密度测定与凝集反应测定。 五、检测原理 ST-360酶标仪利用了垂直光密度检测的概念,即光束经过整个标本的垂直测光发,光的吸收与板孔中吸光物质的多少呈正比。公式为: A = (a/s)×m A = 吸光度值 a = 物质的克分子吸收率 m = 吸光物质的质量 s = 垂直于光路的横切面积 六、操作程序 (一)开机 在确保电源接通的情况下,直接打开仪器右后面的电源开关待自检完成后,按下面板上的“测量方式”键,根据所提示的方法,再按右面板上的“6”字键即可, (二)电脑程序 (1)启动科华软件右上方的“接口”连接,及进入了测定窗口。 (2)放入需要检测的板架。 (3)根据检测板架的标本排放顺序,依次设定好标本号,质控号,阴阳性号位。 (4)编程完成后,用鼠标先择好项目后点击测量键,仪器即进入检测状态。 (5)测量完备后仪器会显示所有的吸光度值,清点击“结果入库”,再测定下一项目或退出。 七、常见故障及排除 该仪器的维修和保养主要由工程师进行,以下仅为普通故障,可酌情进行排除 错误原因建议采取的方法 开机后电源不通检查电源是否接好,保险丝是否烧断 滤光盘出错光耦找不到检查是否有东西阻碍盘转动或电机损坏,请与工程师联系 1 检查酶标板是否装平在板架上 2 检查是否有异物阻碍板架
损。 4 返回光耦找不到 无灯灯泡损坏换灯泡 滤光片出错滤光片能量底换滤光片 前置出错能量太高,暗信号低检查光缆是否接好,电源线是否接地,与服务商联系 八、参考文件 ST-360酶标仪使用说明书 九、技术特性 重量:11kg 尺寸:440mm×340mm×180mm 电源:200-240V, 50/60Hz 电流:1.3A(100-200V);0.7A(200-240).。 保险丝:2×3.5A 使用温度范围:+10C------40C 酶标板:建议使用平底酶标板 光谱范围:400---750mm 示值范围:0—3.5Abs 显示分辨率:0.001Abs 准确度:±2.0%或±0.007吸收单位 线性:±2.0%或±0.007吸收单位 预热速度:需1分钟自检 读板速度:3秒/ 板 显示:240(W)×180(H)全点阵中文液晶显示 键盘:22键 十、附件 无 编写:审核:批准: 批准日期:
标准操作规程 目的:建立一个药品微生物限度检验标准操作规程。 范围:适用于本企业生产的所有品种,本企业所有洁净生产区域,QC微生物限度检查室,洁净工作室等。 责任者:QC主任、化验员。 规程: 本规程引至《中国药典》2000年版。 1. 概述:微生物限度检查系指非规定灭菌制剂及其原辅料受到微生物污染程度的一种检查方法,包括染菌量及控制菌的检查。我公司QC设无菌操作室,用于微生物限度检查。无菌操作室的管理及使用制度见本文附录一。 2. 抽样:供试品应按批号随即抽样,一般抽样量为检验用量(2个以上最小包装单位)的3倍。抽样时,凡发现有异常可疑的样品,应缺陷选用疑问的样品,但因机构损伤明显破裂的包装不得作为样品,凡已能从药品、瓶口(外盖内侧及瓶口周围)外观看出长螨、长霉、虫蛀及变质的药品,可直接判为不合格,无需要再抽样检验。 3. 供试品的保存:供试品在检验之前,应保存在阴凉干燥处,以防供试品中的污染菌因保藏条件所引起致死、损伤或繁殖。供试品在检验之前,应该保持原有包装状态,严禁开启,包装已开启的样品不得作为供试品。 4. 检查: 4.1. 使用设备:电热恒温培养箱、电热恒温水温箱、试管、刻度吸管、量筒、三角瓶、培养皿、试管架、注射器、针头、注射器盒、研钵、75%酒精棉球、紫外灯(365nm波长)。 4.2. 检查的全过程应严格遵守无菌操作,严防再污染。使用设备、仪器、人员及无菌操作室常用的消毒、灭菌方法见本文附录二。除另有规定外,供试品制备成供试液后,均在均匀状态取样。制成供试液后,应该在60分钟内注皿操作完毕。 标准操作规程
4.3. 培养:除另有规定外,本检查法中细菌培养温度为30-35℃,霉菌、酵母菌培养温度为25-28℃,控制菌培养温度为36±1℃,检验结果的报告以1g、1ml或10cm2为单位。 4.4. 复检 4.4.1. 菌数测定不合格者应复检,控制菌检查以一次检出为准,不再复试,但应保留检出菌株一个月备查。 4.4.2. 以复试项下不合格项目为准,作单项复试。复试需另取同批号样品,测定2次。 4.4.3. 复试报告,以3次测定结果的算术平均值报告。 4.5. 检验报告 4.5.1. 检验报告以1g、1ml或10cm2为单位。 4.5.2. 测定菌数报告,以每次测定结果全部平均值报告。 4.5.3. 控制菌按检验结果报告,如未检出控制菌时,报告为“按规定抽样检验结果未检出XX菌”,如抽样中任意一样品要检出控制菌时,报告为“按规定抽样,检出XX菌,不符合药品微生物限度标准。” 4.6. 培养基、试药及稀释剂的相关内容见本文件附录三。 4.7. 供试液的制备:按供试液的理化特性与生物学特性可采取适宜的方法制成供试液。 4.7.1. 供试品的取样及注意事项 供试品取样应有一定数量,以使检验结果具有代表性,正常的供试品一般每批应随机抽取两瓶或两盒以上的包装单位,检验时每次应分取两瓶(盒)以上的样品共10g或10ml。 供试品在检验前,应严格保持包装的原有状态,不得启开,并放在阴凉干燥处,防止微生物再繁殖,以免影响检验结果,凡已将原包装启开,则无代表性应另取样。 供试品稀释后须在1-2小时内操作完毕,防止微生物繁殖或死亡。 供试品稀释成供试液后,应在均匀状态下取样,凡因抑菌或不溶于水的剂型,其供试品应作特殊处理后进行检验。 4.7.2. 液体供试品:取供试品10ml,加入稀释剂90ml中,混匀,作为供试液。油剂可加适量 聚山梨酯80,混匀,吸取相当于10g或10ml供试品,标准操作规程 再稀释成100ml作为供试液;合剂(系指含王桨或蜂蜜者,下同)可用供试品作为供试液。 4.7.3. 固体、半固体或黏稠液供试品:称取供试品10g,置0.9%无菌氯化钠溶液100ml中,用匀浆仪或其他适宜的方法混匀后作为供试液。在制备过程中,必要时可加适量聚山梨酯80,并适当加温,但不应超过45℃。 (1)非水溶性供试品:取供试品5g(5ml)加入含溶化的无菌司盘80 5g、单硬脂酸甘油酯3g、聚山梨酯80 10g混合物的烧杯中,用无菌玻棒搅拌成团后,慢慢加入45℃左右的0.9%无菌氯化钠溶
操作规程编号:YTO-FS-PD313 气体检测仪安全操作规程通用版 In Order T o Standardize The Management Of Daily Behavior, The Activities And T asks Are Controlled By The Determined Terms, So As T o Achieve The Effect Of Safe Production And Reduce Hidden Dangers. 标准/ 权威/ 规范/ 实用 Authoritative And Practical Standards
气体检测仪安全操作规程通用版 使用提示:本操作规程文件可用于工作中为规范日常行为与作业运行过程的管理,通过对确定的条款对活动和任务实施控制,使活动和任务在受控状态,从而达到安全生产和减少隐患的效果。文件下载后可定制修改,请根据实际需要进行调整和使用。 一、适用范围 1. 本规程规定了XP314、XP702、XP500、ESP210等型号的检漏仪使用的安全要求。 2. 本规程适用于抢修中心一至四队、抽水队、调压维修队、调压维护队各班组。 二、安全操作规程 1. 设备操作人员必须熟知设备的构造、性能、特点,掌握设备的使用方法方准使用。 2. 设备应保持进气口/排气孔的通畅,进口处的过滤网需根据使用环境经常清理、更换。 3. 避免人为的经常用高浓度可燃性气体对设备进行冲击,以防传感器中毒。 4. 禁止设备的进气口/排气口外接压缩气体(气 体>1atm),以免损坏内部气泵、气室。 5. 操作时应用皮套对设备进行保护,以防跌落损坏机壳及内部元件。 6. 设备长时间不使用时,应将电池从设备中取出(充
多功能酶标仪SpectraMax i3的标准操作规程Standard Operation of SpectraMax i3 部门Department 签名/日期Signature/Date 起草人:Prepared by 樊小川,Xiaochuan Fan QC 审核人:Reviewed by 黄思佳,Sijia Huang QC 审核人:Reviewed by 褚夫兰,Fulan Chu QA 批准人:Approved by 张伯彦,Boyan Zhang 质量负责人 1 目的 建立多功能酶标仪SpectraMax i3的标准操作程序,规范SpectraMax i3 多功能酶标仪检测时的操作。 2 适用范围
本规程适用于所有对多功能酶标仪SpectraMax i3的操作 3 术语或定义 多功能酶标仪:指功能较强、精度较高的单体台式酶标仪,可检测吸光度(Abs)、荧光强度(FL)、时间分辨荧光(TRF)、化学发光(Lum)等。 4 责任 4.1 仪器负责人负责多功能酶标仪的日常及定期维护,出现故障时负责联系厂家维修,保 证运行正常。 4.2 实验操作人员需严格按照本规程执行,保证仪器正常使用,每次用完后填写仪器使用 记录,且使用后及时清理台面,保持仪器洁净。 5 EHS要求 N/A 6 程序 6.1 仪器安装 仪器与电脑连接完毕并连接电源以后,按仪器背面的按钮可以直接启动仪器,经过几分钟后的仪器自检后就可以开始用于检测。在连有电源的情况下,保持24小时开机,不要罩防尘罩以保持透气,隔1-2月关机重启一次。 6.2 SoftMax Pro软件操作基本步骤 6.2.1 打开软件 点击“SoftMax Pro 6.3”图标,打开SoftMax Pro 软件,出现"Plate Setup Helper"对话框。若无则点击图标。 6.2.2 连接仪器 点击‘Choose a diffecient instrument’,打开‘Instrument Connection’对话框,在“Availible Instruments”菜单中选择仪器连接线与电脑所接的串口号(COM)。 选择所购买的酶标仪型号SpectraMax i3或添加模块卡盒型号。最后点击“OK”键连接。 6.2.3 仪器检测参数设定 点击图标后出现“Settings”对话框,对话框最上方出现Read Mode(读板模式)和Read Type(读板类型)两个选项,读板模式有ABS(光吸收)、FL(荧光强度)、LUM(化学发光)和TRF(时间分辨荧光),读板类型有终点检测(Endpoint)、动力学(Kinetic)、单孔扫描(Well Scan)和光谱扫描(Spectrum)四种。使用者根据实验
制药GMP管理文件 一、引用标准:中华人民共和国S药典(2005年版)一部。 二、目的:本标准规定了微生物限度检查法标准操作规程。 三、适用范围:适用于微生物限度的检查。 四、责任者:质检人员。 正文: 1、简述微生物限度检查法系检查非规定灭菌制剂及其原料、辅料受微生物污染程度的方法。检查项目包括细菌数、霉菌数、酵母菌数及控制菌检查。 微生物限度检查应在环境洁净度10000级下的局部洁净度100级的单向流空气区域内进行。检验全过程必须严格遵守无菌操作,防止再污染。单向流空气区域、工作台面及环境应定期按《医药工业洁净室(区)悬浮粒子、浮游菌和沉降菌的测试方法》的现行国家标准进行洁净度验证。 供试品检查时,如果使用了表面活性、中和剂或灭活剂,应证明其有效性及对微生物的生长和存活无影响。 除另有规定外,本检查法中细菌培养温度为30~35℃;霉菌、酵
母菌培养温度为23~28℃;控制菌培养温度为35~37℃。 检验结果以1g、1ml、10g、10ml或10㎝2为单位报告。 检验量:检验量即一次试验所用的供试品量(g、ml、㎝2)。除另有规定外,一般供试品的检验量为10g或10ml;贵重药品、微量包装药品的检验量可以酌减。要求检查沙门氏菌的供试品,其检验量应增加10g或10ml。 检验时,应从2个以上最小包装单位中抽取供试品。一般应随机抽取不少于检验用量(两个以上最小包装单位)的3倍量供试品。2、供试液的制备 根据供试品的理化特性与生物学特性,采取适宜的方法制备供试液。供试液制备若需用水浴加温时,温度不应超过45℃供试液从制备至加入检验用培养基,不得超过1小时。 除另有规定外,常用的供试液制备方法如下。 (1),液体供试品取供试品10ml,加PH7.0无菌氯化钠-蛋白胨缓冲液至100ml,混匀,作为1:10的供试液了。油剂可加入适量的无菌聚山梨酯80使供试品分散均匀。水溶性液体制剂也可用混合的供试品原液作为供试液。 (2)固体、半固体或黏稠性供试品取供试品10g,加PH7.0无菌氯化钠-蛋白胨缓冲液对至100ml,用匀浆仪或其他适宜的方法,混匀,作为1:10的供试液,必要时加适量的无菌聚山梨酯80,并置水浴中适当加温使供试品分散均匀。 (3)用特殊供试液制备方法的供试品
多功能酶标仪基本操作规程 一、可见与紫外光原始吸光值的直接测定方法 1、首先打开连接酶标仪的电插板上的全部开关。打开酶标仪主机背面电源线上端的开关。 2、再打开电脑开关。(注意,一定要先开仪器,后开电脑,以免仪器连接出现问题。) 3、在电脑主屏幕上选择[Magellan6]。 4、仪器自检后,酶标板托架自动伸出(注意仪器前部不要放置物品,以免档住托架的伸出)。将酶 标板按数字正确的方向(A1位于左上角)放在托架上。 5、点击仪器下部最右侧的[move plate in] 图标,酶标板将自动进入仪器中。(注意:千万不要用手 将酶标板推入仪器,造成仪器损坏)。 6、在屏幕上选Start measurement。点击绿色箭头。 7、在Select a File窗口左上角选Obtain Raw Date 然后点击绿色箭头。 8、在plate 栏中的plate definition 下拉条中,对板的类型进行选择。酶标的吸光度测定,一般情况 下选xxxxx xx Flat Transparent (x孔,平底,透明板)。(注意测定紫外吸收时要使用可以透过紫外光的透明板)如果板要加盖子,就要再选中Plate with cover。 9、在Measurements 栏内双击Absorbance ,出现Absorbance的对话框。 10、在Absorbance的对话框中: ⑴在Wavelength栏中Measurement项输入测定波长值;Reference项,在需要扣除背景波长时选中并 输入背景波长值。一般情况不选. ⑵在Multiple read per well栏中对于吸光值的测定可不选 ⑶在Read 栏中: Number of flashes 项一般选10;Settle time(使平静时间)项对于96或384孔 板一般选0;对于其他孔数的板可考虑输入适当的值;孔数越少的板,Settle time 设置时间要较长,以防止在测定过程中板移动距离大,对液面平稳的影响。 ⑷在Label栏中Name后输入你为此块板自定义的英文名;也可不设置。 11、在Part of plate 栏中,用鼠标左键拉框,选择要测定的样品孔(使待测定的样品孔变为黄色), (注意:待测孔只可横向或纵向连续选择,不可以被间断)。如果选择错误需要更改,不要做任何删除,只要再直接重新选择即可。点击本栏中的Detail 对所选的样品孔进行确认后,点击OK,(如果选孔有错误,选择Cancel 返回上页再重复以上操作。) 12、点击OK后,箭头变绿,点击绿色箭头,在Measurement 的workspace处输入(日、月、年- 自定义文件名wsp)再点击Start,仪器开始自动测定。 13、测定结束后,点击File 选择print,直接打印测定参数与结果,或在最上方Edit选择Copy to Excel, 然后打开下方出现的Excel表(显示为板式数据)并打印结果。 14、关机,退出当前界面,点击左下角Exit Megellan 回到主屏幕。关电脑,关仪器电源和插板电 源。 二、荧光值的直接测定方法 1、首先打开连接酶标仪的电插板上的全部开关。打开酶标仪主机背面电源线上端的开关。 2、再打开电脑开关。(注意,一定要先开仪器,后开电脑,以免仪器连接出现问题。) 3、在电脑主屏幕上选择[Magellan6]。 4、仪器自检后,酶标板托架自动伸出(注意仪器前部不要放置物品,以免档住托架的伸出)。将酶 标板按数字正确的方向(A1位于左上角)放在托架上。 5、点击仪器下部最右侧的[move plate in] 图标,酶标板将自动进入仪器中。(注意:千万不要用手 将酶标板推入仪器,造成仪器损坏)。 6、在屏幕上选Start measurement。点击绿色箭头。 7、在Select a File窗口左上角选Obtain Raw Date 然后点击绿色箭头。 8、在plate 栏中的plate definition 下拉条中,对板的类型进行选择。荧光酶标的测定,一般情况下 选xxxxx xx Flat black (x孔,平底,黑板。6孔板测定时没有黑板可选,可选择6孔,平底,透明板)。
便携式四合一气体检测仪操作规程 1 范围: 本规程规定了设备启动前,对罐内气体实施检测,四合一气体检测仪的检查准备,检测操作步骤及安全注意事项。 本规程适用于机械清洗项目对各类储油罐清洗前的气体检测操作。 2规范性引用文件 SY6503-2000 可燃气体检测报警器使用规范 3 四合一气体检测仪检测前的检查准备 3.1检查电池电量是否充足(3.3V以上),不充足及时充电; 3.2检查进气口气滤有无杂物堵住,堵住需清理干净或更换; 4 操作步骤: 4.1开机操作: 4.1.1按[MODE]键并保持1秒,LCD显示“on”,LED亮,峰鸣器响一声,仪器开机; 4.1.2LCD显示版本号,同时进行预热和自检。 4.1.3预热和自检完成致10秒倒计时结束,仪器进入检测模式,确认仪器运行正常。 4.1.4确认确实在抽新鲜空气,确认氧气指示计的指示值确实为20.9%。 4.1.5将取样管端部插入测试点中,待测试值变化稳定后,读数并记
录。 4.1.6从测试点中拿出取样管,置于空气中,待LED显示值回复到空气中状态后,再进行下一测试点测试。 4.2关机操作: 4.2.1按住按键不放,LCD显示5秒倒计时,倒计时结束后LCD显示“off”,随后仪器无显示,仪器关机。 5注意事项: 5.1仪器更换电池或简单维修时应在安全场所进行。 5.2传感器和仪器要注意防水和杂质。 5.3仪器长期不工作时,应关机,置于干燥、无尘、符合储存温度的环境中。 5.4调整好的仪器不要随便打开盖。
硫化氢气体检测报警仪操作规程 1 范围: 本标准规定了设备启动前,对罐内气体实施检测,硫化氢检测仪的检查准备,检测操作步骤及安全注意事项。 本标准适用于机械清洗项目对各类储油罐清洗前的气体检测操作。 2规范性引用文件 《COWS施工手册》 3 硫化氢检测仪检测前的检查准备 3.1检查电池电量是否充足,不充足更换; 3.2检查进气口不被杂物堵住,堵住清理干净; 4 操作步骤: 4.1开机操作 4.1.1确认电池已经装入仪器,按住按键3秒,LCD显示“on”,红色LED亮,蜂鸣器响一声,振动器振动,仪器开机。 4.1.2LCD显示版本号,同时进行预热和自检。 4.1.310秒倒计时预热和自检完成后,仪器进入检测模式,显示实时读数。 4.2关机操作 按住按键不放,LCD显示5秒倒计时,倒计时结束后LCD显示“off”,随后仪器无显示,仪器关机。 4.3检测模式说明:
酶标仪使用方法 一、仪器准备 1.将MK3酶标仪后部的电源开关打开,仪器将显示自检,基础酶联,软件版本号。 2.等待数秒后,荧屏显示“基础酶联,准备和时间”。表示仪器正常,处于等待状态。 操作规程 1.工作人员心须详细阅读仪器操作使用说明书。 2.将被测样品板放入酶标盘中,同时打开与酶标仪相连的打印机开关。 3.按“测量模式”键:进入选择波长程序 荧屏显示:“基础酶联” “1.单波长检测” 按“↑”“↓”选择单波长.双波长检测. 4.按“输入”键:进入选择好的文件名状态。 若选择单波长检测, 荧屏显示:“1.单波长检测” “滤光片 405” 再用数字键选择需要的波长. 若选择双波长检测, 荧屏显示:“2.双波长检测” “1.滤光片 450” 再用数字键选择需要的第一检测波长.按”输入”键, 荧屏显示: “2双波长检测” “2.滤光片 630” 再用数字键选择需要的第二检测波长.按”输入”键, 荧屏显示:“2双波长检测” “无试剂空白” 5.继续按”输入”键, 荧屏显示:“2双波长检测” “最终结果”(单波长无此步骤) 6.按”输入”键,返回到荧屏显示“基础酶联,准备和时间” 7.按”开始”键, 启动阅读功能,酶标仪对样品板开始进行测试。 8.读数完毕,被测孔子板复位,荧屏显示“正在传送数据”,等待数秒后,打印机开始打印测试结果。当打印完毕后,关闭打印机开关,荧屏回到主菜单状态。此时将
酶标仪右侧开关打至“O”即可。 二、计算机控制 1.将MK3酶标仪后部的电源开关打开,仪器将显示自检,基础酶联,软件版本号2.等待数秒后,荧屏显示“基础酶联,准备和时间”。表示仪器正常,处于等待状态。 3.在lab-35计算机的桌面上打开“思桥检验科管理系统”,输入用户名“system”及密码“system”. 4.进入系统后,选择“酶标仪”菜单。在下拉框中选择“酶标项目设置” (1)在面板当中进行单,双波长的设置,点击“仪器通迅设置”。 (2)在“仪器通迅设置”面板上,默认为单波长的方式,如要选择双波长,勾选双波长的选框。 (3)在主滤光片及副滤光片上选择相应的所需波长大小。 (4)选择完成后,点击“确认”键,系统显示“设置成功”,按“确定”退回。 (5)点击“退出”键,系统显示“酶标仪器设置成功”,按“确定”键返回到“酶标项目设置”的面板上。 (6)在“酶标仪”的下拉框中选择“酶标仪操作”,在此面板中完成读板,数据存储及打印的工作。 5. (1)点击“连机”,在状态栏显示“连机成功”,表明计算机已与酶标仪连接成功。 (2)点击“启动”,在状态栏显示“计算机远程控制成功”,表明计算机已远程控制酶标仪。如未显示此项,则读板功能不能完成,数据传输异常。 (3)顺利完成上面两项后,继续点击“读板”键,启动酶标仪读板功能。数秒后,酶标仪开始读板,完成读板后,在“状态”栏显示“结果数据分离成功”,并在面板的样品栏显示读板后的数据。(在此“酶标仪操作”面板未关闭之前,可连续读板,如关闭面板需重复“连机”,“启动“) (4)点击“入库”键,系统显示“入库完毕”,按“确定”返回。此项完成了数据的存储。 (5)点出“计算“键,系统显示“计算完毕”, 按“确定”返回。此项完成后才可以打印。 (6)点出“打印”键,完成打印到此波长选择设置成功,点击“关闭”键,退出“酶标项目设置” (7)当打印完毕后,关闭打印机开关。此时将酶标仪右侧开关打至“O”即可。
H2S气体检测仪使用操作规程 1、H2S气体检测仪设置 ⑴打开仪表开关的同时按住翻页按钮。 ⑵翻页和复位按钮修改口令使出现需要的口令,然后按下开关按钮确定口令进入设置功能模块。 2、低报警设置 ⑴用翻页和复位按钮设置低报警值(10ppm)。 ⑵按下开关按钮接受设置值并进入高报警页。 3、高报警设置 ⑴用翻页和复位按钮设置低报警值(20ppm)。 ⑵按下开关按钮接受设置值并进入STEL/TWA使能页。 4、H2S气体检测仪使用步骤 ⑴校准检查 a.新鲜空气中打开仪表。 b.确认读数指示当前没有气体存在。 c.校验导管一端接检验气瓶、一端接仪表测试口。 d.打开标定气瓶,校验显示屏上的读数是否在校准气筒的限制范围之内。假如校验检测气体浓度超过仪表报警点,必须有一个报警指示显示。 ⑵H2S测量
a.检测仪在检测界面能显示1%的气体浓度。仪表保持在这页,直到其他页面被选或仪表关闭。 b.假如气体浓度超过报警设置点,发出报警声,报警灯闪烁,报警类型和报警图标交换闪烁。 c.低报警:只要气体浓度降低到不报警浓度点以下仪表自动复位,按下复位按钮可保持5秒的消音,气体浓度一直在低报警以上时仪表一直报警。 d.高报警:在气体浓度降到高报警点以下不会复位,按下复位按钮可保持5秒的消音,当气体浓度一直保持在高报警点以上,报警继续。 三、干粉灭火器使用操作规程 1、穿戴好劳动保护用品,准备好工具用具。 2、检查出粉管是否畅通,是否老化,检查灭火机重量或压力是否符合铭牌规定标准。 3、灭火器必须置于上风头使用,喷管对准火源根部。 4、发现着火首先切断油、气、电源,放掉容器内压力,隔离或搬掉易燃物。 5、操作完毕,将工具用具擦洗干净收回。
Infinite M200 F200多功能酶标仪标准操作规程 一. 目的 为规范多功能酶标仪的基本操作、维护保养、异常处理程序,防止人为操作失误,确保分析天平正常运转,特制定本程序。 二. 适用范围 本程序适用于Infinite M200 F200多功能酶标仪。 三.责任 1. 本程序的实施者为多功能酶标仪操作者,各实验室负责人对本规程的实施情况进行 监督。 2. 日常运行及维护、定期维护、定期点检及保养由多功能酶标仪操作者负责。 四.操作步骤 1.依次打开酶标仪、电脑主机、显示器电源,待电脑正常启动后双击打开icontrol软件。 2.根据实验需要选择更换率光片。 3. 选择Creat/edit a method,点击下一步。 4. 再选择是编辑一个新方法(creat new),在原有方法的基础上进行编辑(Edit), 选择之后点击continue进入下一步。 5.在终点检测、动力学检测、多标测定之中选择终点检测,点击下方的Measurement paraments按钮进入下一步。 6.此时会弹出一个Measurement paraments对话框,共有:检测功能模式(General)、 板型(plate)、检测参数设定(Meas. Params)、温度控制(Temperature)、振板 (Shaking)等一共5个选项。 7. 在检测功能模式下选择光吸收(Absorbance)、荧光(Fluorescence Intensity)、 发光(Luminescence)其中的一种,下面以做光吸收为例。 8.先选择光吸收, 点击Plate进入板型选项对话框,再点击Browse选择相应的板型(光 吸收用ft, 荧光用fb, 发光用fw)。 9.再点击Meas. Params进入检测参数设定选项对话框,输入或者选择相应的检测波长。 10.再依次点击Temperature、Shaking选择想要设定的温度范围及振板方式;也可不作 选择。 11.这些都设定好之后点击确定,再点击Continue进入下一步。
gentleMACS 组织处理器操作规程 1.确保gentleMACS 组织处理器接通电源。 2.预定义的程序是由内部存储器提供的。另一种方法是:插入HyralACS程序卡,直接运行程序卡程序。或复制程序卡中程序到仪器内部存储器,再运行程序。通用的gentleMACS 程序A、B 、C、D 、E依次用于坚硬程度递增的样本,即A程序处理柔软组织,E程序处理最坚硬的组织。 3.将样品转移到特定型号的Tube管中,确保管盖盖紧。 样本使用量:推荐样本体积为300 μL -10 mL ,重量为10 mg –4000 mg,gentleMACS Protocols推荐为准。根据组织类型确定最大投入量,对于特别坚硬的组织先切成小片(5x5 mm)再放入Tube管中。 Tube管的选择:C Tubes主要用于制备单细胞悬浮制备, M Tubes主要用于分子分离。 4.确保正确安装Tube管,将其垂直、倒置放入套管中。正确的放入Tube管确保证Tube管保持在旋转和轴向力的位置。 5. gentleMACS 组织处理器通过显示器完成程序的复制、编辑、删除等操作。 6.选择一个由仪器存储器提供的程序或程序卡中的程序。 运行程序: ?使用箭头图标选择程序 显示:Program name and tube name ?开始运行程序 运行期间会显示Program name and remaining time ?运行结束后,程序可以继续使用 ?(准备运行) 运行期间,绿色指示灯亮
7.按下开始按钮启动程序。 8.显示器指示当前程序的程序名称和剩余时间(s)。 9.程序结束显示5秒。随后,显示器指示刚刚使用过的程序,若按下开始按钮,程序可以立即被应用来处理下一个样本。 10.程序结束后,从套管垂直拔出含有样品的Tube管。
多功能酶标仪SpectraMax-i3的操作规程编号 M-SOP-2-0083 No. 标准操作规程版本号 Standard Operating Procedure 01 Version 多功能酶标仪SpectraMax i3的标准操作规程 多功能酶标仪SpectraMax i3的标准操作规程 Standard Operation of SpectraMax i3 部门签名/日期 Department Signature/Date 起草人: XX, Xiaochuan X Prepared by QC 审核人: XX, Sijia XX Reviewed by QC 审核人: XX, Fulan X Reviewed by QA 批准人: XX, Boyan XX Approved by 质量负责人 颁发部门执行日期质量保证部-QA Issued by Effective Date 替换文件复审日期 Version 00 Replaced For Review Date 分发部门 QA,QC Distributed to 1 of 7 编号 M-SOP-2-0083 No. 标准操作规程版本号 Standard Operating Procedure 01 Version 多功能酶标仪SpectraMax i3的标准操作规程 1 目的 建立多功能酶标仪SpectraMax i3的标准操作程序,规范SpectraMax i3 多功能酶标仪 检测时的操作。 2 适用范围
本规程适用于所有对多功能酶标仪SpectraMax i3的操作 3 术语或定义 多功能酶标仪:指功能较强、精度较高的单体台式酶标仪,可检测吸光度(Abs)、荧 光强度(FL)、时间分辨荧光(TRF)、化学发光(Lum)等。 4 责任 4.1 仪器负责人负责多功能酶标仪的日常及定期维护,出现故障时负责联系厂家维修,保 证运行正常。 4.2 实验操作人员需严格按照本规程执行,保证仪器正常使用,每次用完后填写仪器使用 记录,且使用后及时清理台面,保持仪器洁净。 5 EHS要求 N/A 6 程序 6.1 仪器安装 仪器与电脑连接完毕并连接电源以后,按仪器背面的按钮可以直接启动仪器,经过几分钟后的仪器自检后就可以开始用于检测。在连有电源的情况下,保持24小时开机,不要罩防尘罩以保持透气,隔1-2月关机重启一次。 6.2 SoftMax Pro软件操作基本步骤 6.2.1 打开软件 点击“SoftMax Pro 6.3”图标,打开SoftMax Pro 软件,出现 "Plate Setup Helper"对话框。若无则点击图标。
药品微生物限度检验方法标准操作规 程
标准操作规程 目的:建立一个药品微生物限度检验标准操作规程。 范围:适用于本企业生产的所有品种,本企业所有洁净生产区域,QC微生物限度检查室,洁净工作室等。 责任者:QC主任、化验员。 规程: 本规程引至《中国药典》。 1. 概述:微生物限度检查系指非规定灭菌制剂及其原辅料受到微生物污染程度的一种检查方法,包括染菌量及控制菌的检查。我公司QC设无菌操作室,用于微生物限度检查。无菌操作室的管理及使用制度见本文附录一。 2. 抽样:供试品应按批号随即抽样,一般抽样量为检验用量(2个以上最小包装单位)的3倍。抽样时,凡发现有异常可疑的样品,应缺陷选用疑问的样品,但因机构损伤明显破裂的包装不得作为样品,凡已能从药品、瓶口(外盖内侧及瓶口周围)外观看出长螨、长霉、虫蛀及变质的药
品,可直接判为不合格,无需要再抽样检验。 3. 供试品的保存:供试品在检验之前,应保存在阴凉干燥处,以防供试品中的污染菌因保藏条件所引起致死、损伤或繁殖。供试品在检验之前,应该保持原有包装状态,严禁开启,包装已开启的样品不得作为供试品。 4. 检查: 4.1. 使用设备:电热恒温培养箱、电热恒温水温箱、试管、刻度吸管、量筒、三角瓶、培养皿、试管架、注射器、针头、注射器盒、研钵、75%酒精棉球、紫外灯(365nm波长)。 4.2. 检查的全过程应严格遵守无菌操作,严防再污染。使用设备、仪器、人员及无菌操作室常见的消毒、灭菌方法见本文附录二。除另有规定外,供试品制备成供试液后,均在均匀状态取样。制成供试液后,应该在60分钟内注皿操作完毕。 标准操作规程 4.3. 培养:除另有规定外,本检查法中细菌培养温度为30-35℃,霉菌、酵母菌培养温度为25-28℃,控制菌培养温度为36±1℃,检验结果的报告以1g、1ml或10cm2为单位。 4.4. 复检
气体检测仪安全操作规程(正 式) Standardize The Management Mechanism To Make The Personnel In The Organization Operate According To The Established Standards And Reach The Expected Level. 使用备注:本文档可用在日常工作场景,通过对管理机制、管理原则、管理方法以及管理机构进行设置固定的规范,从而使得组织内人员按照既定标准、规范的要求进行操作,使日常工作或活动达到预期的水平。下载后就可自由编辑。 一、适用范围 1. 本规程规定了XP314、XP702、 XP500、ESP210等型号的检漏仪使用的安全要 求。 2. 本规程适用于抢修中心一至四队、抽水 队、调压维修队、调压维护队各班组。 二、安全操作规程 1. 设备操作人员必须熟知设备的构造、性
能、特点,掌握设备的使用方法方准使用。 2. 设备应保持进气口/排气孔的通畅,进口处的过滤网需根据使用环境经常清理、更换。 3. 避免人为的经常用高浓度可燃性气体对设备进行冲击,以防传感器中毒。 4. 禁止设备的进气口/排气口外接压缩气体(气体>1atm),以免损坏内部气泵、气室。 5. 操作时应用皮套对设备进行保护,以防跌落损坏机壳及内部元件。 6. 设备长时间不使用时,应将电池从设备中取出(充电电池应在充满电后),存放于干燥处。 7. 禁止在危险场所对设备进行充电或更换电池。
8. 严禁将设备的构造及电路改动,以免发生意外。 请在这里输入公司或组织的名字 Please enter the name of the company or organization here
1.目的 规范酶标仪的使用、维护与保养。 2.范围 适用于以下型号的酶标仪。 3.职责 使用人员对本规程的实施负责,部门负责人监督实施。 4.使用规程 4.1开关机 4.1.1打开电源开关,电源开关位于仪器右后方的电源接口的正上方。 4.1.2当操作者按下电源开关时,仪器正面左侧的绿色三角形电源指示灯会闪烁十数秒,这 是仪器正在进行自检,闪烁停止后,电源指示灯呈绿色发光状态时,仪器处于待机状态。 4.2启动软件 4.2.1双击桌面上“Magellan”图标,选择检测到的仪器—“Infinite 200”,点击“OK”; 4.2.2在桌面中央对话框的下侧点击“取消”,即进入Magellan主界面 4.2.3在界面下侧点击温度控制图标,设定目标温度—设置—开;点击当前温度,选择自动, 可以实时观察仪器内温度,(注:实验开始前需将仪器提前预热到目标温度) 4.2.4将样品板放到托架上,A1孔处于左上方;然后按右下角绿色三角形按钮继续,选择获 得原始数据—继续,进入测量流程编辑窗口 4.2.5在Plate下拉菜单中选择测量使用的板的类型,在Part of Plate中框选样品区域; 在指令栏左侧选择需要检测的指令,如:1)双击“摇动”,设置持续时间3 s,波幅 1.5 mm;2)双击“温度设置”,设置37 ℃,点开“等温度达到”,范围设置36.5 ℃ —37 ℃;3)双击“多点测定循环”,设置持续时间1-2 h,勾选使用多点测定间隔,时间1-2 min;4)双击“荧光强度”,设置为490 nm—520 nm,点击Star,开始检测 4.3注意事项 4.3.1仪器使用完关机后到下一次开机中间至少间隔0.5 h 4.3.2检测完成后及时取出微孔板、比色杯
1 目的 建立微生物限度检查的操作规程,为微生物检查人员提供正确的标准操作方法。 2 范围 适用于原辅材料、内包装材料、半成品、成品的微生物限度检查。 3 责任 QA对本规程的有效执行承担监督检查责任,QC对本规程的实施负责。 4 程序 4.1 简述: 微生物限度检查法系指检查非规定灭菌制剂及其原、辅料受到微生物 污染程度的一种检查方法,包括染菌量及控制菌的检查。螨,属于节肢动物门,蛛形纲,蜱螨目。种类繁多,分布甚广。其生活习性各异,分为自由生活和寄生生活两种类型。在土壤、池沼、江河和湖海里,动、植物体上,贮藏食品和药品中,都可能有它们的存在。药品可因其原料、生产过程或包装、运输、贮存、销售等条件不良,受到螨的污染。螨可蛀蚀损坏药品,使药品变质失效,并可直接危害人体健康或传播疾病。能引起皮炎及消化系统、泌尿系统、呼吸系统等的疾病。因此,药品特别是中成药,必须进行活螨检查。 4.2 器皿、仪器及用具。 4.2.1 玻璃器皿: 250ml锥形瓶、250ml具塞三角烧瓶、研钵(陶瓷制,直径10-12cm)、培养皿(90mm)、量筒(100ml)、试管(18×180mm)及塞、吸管(1ml分度0.01,10ml 分度0.1)、注射器(20或30ml)、注射针头、载玻片、盖玻片、 玻璃消毒缸(带盖)。 4.2.2 用具:大、小橡皮乳头(放于干净带盖的容器中,并应定期用70%-75%乙 醇溶液浸泡),无菌衣、帽、口罩、手套灭菌,备用, 显微镜、放大镜(5-10倍)、实体显微镜、解剖针(尖端宜尖细且粗糙,否则不易挑取体表光滑的螨体)、发丝针(由一根长约10cm的小金属棒,将其一端磨成细尖,另取长约1.5cm的头发一根,以其长度的一半紧贴在金属棒的尖端上,用细线将其缠紧,然后粘上加拿大树胶或油漆,即得。适用于挑取行走缓慢且体表刚毛较多的螨体)、小毛笔(即绘图毛笔。适用于挑取活动快的螨类,笔锋宜尖细,以免螨体夹在笔毛之间)、载玻片、盖玻片、酒精灯、培养皿或小搪瓷盘(内衬黑色纸片)、扁形称量瓶(高3cm、宽6cm)。 4.2.3 仪器:匀浆仪、培养箱、鼓风干燥箱、台式灭菌器、恒温水浴锅、超净工