
第1课时 动量定理 动量守恒定律及其应用
[知 识 梳 理])
知识点一、动量、动量定理 1.动量
(1)定义:运动物体的质量和速度的乘积叫做物体的动量,通常用p 来表示。 (2)表达式:p =m v 。 (3)单位:kg ·m/s 。
(4)标矢性:动量是矢量,其方向和速度方向相同。 2.冲量
(1)定义:力和力的作用时间的乘积叫做这个力的冲量。
(2)表达式:I=Ft。单位:N·s。
(3)标矢性:冲量是矢量,它的方向由力的方向决定。
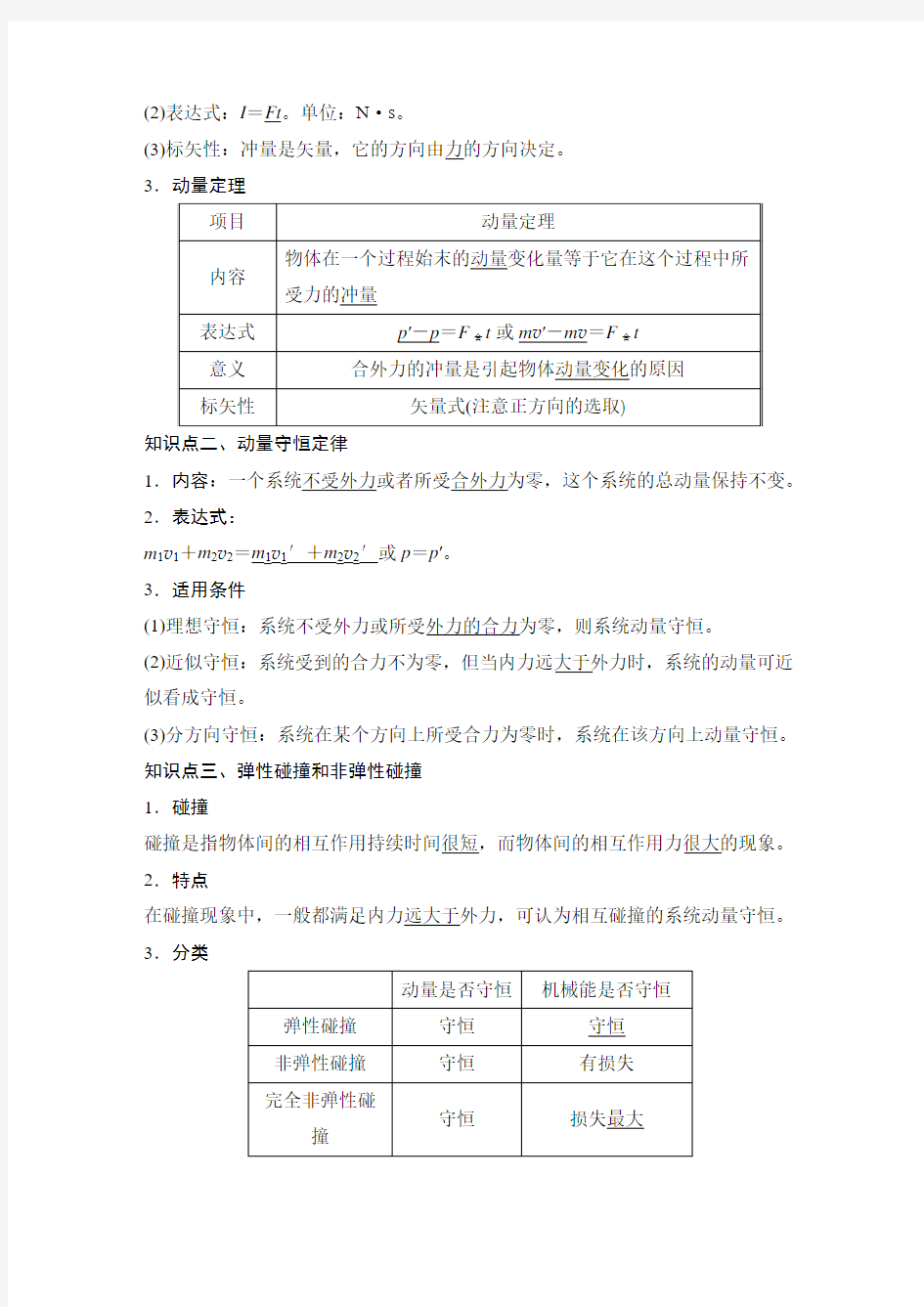
3.动量定理
知识点二、动量守恒定律
1.内容:一个系统不受外力或者所受合外力为零,这个系统的总动量保持不变。2.表达式:
m1v1+m2v2=m1v1′+m2v2′或p=p′。
3.适用条件
(1)理想守恒:系统不受外力或所受外力的合力为零,则系统动量守恒。
(2)近似守恒:系统受到的合力不为零,但当内力远大于外力时,系统的动量可近似看成守恒。
(3)分方向守恒:系统在某个方向上所受合力为零时,系统在该方向上动量守恒。知识点三、弹性碰撞和非弹性碰撞
1.碰撞
碰撞是指物体间的相互作用持续时间很短,而物体间的相互作用力很大的现象。2.特点
在碰撞现象中,一般都满足内力远大于外力,可认为相互碰撞的系统动量守恒。3.分类
思维深化
判断正误,正确的画“√”,错误的画“×”。
(1)一个物体的运动状态变化,它的动量一定改变。()
(2)合外力的冲量是物体动量发生变化的原因。()
(3)系统的动量守恒时,机械能也一定守恒。()
(4)动量守恒定律表达式m1v1+m2v2=m1v1′+m2v2′一定是矢量式,应用时一定要规定正方向,且其中的速度必须相对同一个参考系。()
答案(1)√(2)√(3)×(4)√
[题组自测])
题组一动量、冲量、动量定理的理解
1.下列说法正确的是()
A.速度大的物体,它的动量一定也大
B.动量大的物体,它的速度一定也大
C.只要物体的运动速度大小不变,物体的动量就保持不变
D.物体的动量变化越大则该物体的速度变化一定越大
答案 D
2.质量为m的物体放在光滑水平地面上,在与水平方向成θ角的恒力F作用下,由静止开始运动,经过时间t,速度为v,在此时间内推力F和重力的冲量大小分别为()
A.Ft,0 B.Ft cos θ,0
C.m v,0 D.Ft,mgt
解析冲量的计算一定要与功的计算区别开来,功的大小不但取决于力F的大小、物体的位移s的大小,还与力F和物体运动的方向的夹角θ有关。而力的冲量与力和物体运动的方向的夹角θ没有关系,可直接由公式进行计算,求得F的冲量为Ft,重力的冲量为mgt。
答案 D
3.(多选)质量为m的物体以初速度v0开始做平抛运动,经过时间t,下降的高度为h,速度变为v,在这段时间内物体动量变化量的大小为()
A.m(v-v0) B.mgt
C .m v 2-v 2
0 D .m 2gh
解析 由动量定理得I =Δp ,即mgt =Δp ,故B 正确;由p =m v 知,Δp =m ·Δ
v ,而Δv =v 2-v 20=2gh ,所以Δp =m ·v 2-v 20=m 2gh ,故C 、D 正确。
答案 BCD
题组二 动量守恒定律的理解及应用
4.(多选)下列相互作用的过程中,可以认为系统动量守恒的是( )
解析 动量守恒的条件是相互作用的物体系统不受外力或所受外力的合力为零,而相互作用过程中内力远大于外力时也可认为动量守恒。图A 中,滑轮男孩推滑轮女孩的过程中,内力远大于外力,因此系统的动量可认为守恒;图B 和图D 中,在两物体相互作用的过程中,没有满足内力远大于外力的条件,系统的动量不守恒;图C 中,太空中无空气阻力作用,太空人和子弹在相互作用过程中动量守恒。 答案 AC
5.滑雪运动是人们酷爱的户外体育活动,现有质量为m 的人站立于雪橇上,如图1所示。人与雪橇的总质量为M ,人与雪橇以速度v 1在水平面上由北向南运动(雪橇所受阻力不计)。当人相对于雪橇以速度v 2竖直跳起时,雪橇向南的速度大小为( )
图1
A.
M v 1-M v 2M -m B.M v 1
M -m
C.
M v 1+M v 2
M -m
D .v 1
解析 根据动量守恒条件可知人与雪橇系统水平方向动量守恒,人跳起后水平方向速度不变,雪橇的速度仍为v 1。 答案 D
6.A 球的质量是m ,B 球的质量是2m ,它们在光滑的水平面上以相同的动量运动。B 在前,A 在后,发生正碰后,A 球仍朝原方向运动,但其速率是原来的一半,碰后两球的速率比v A ′∶v B ′为( ) A .1∶2 B .1∶3 C .2∶1 D .2∶3
解析 设碰前A 球的速率为v ,根据题意,p A =p B ,即m v =2m v B ,得碰前v B =v
2,
碰后v A ′=v 2,由动量守恒定律,有m v +2m ×v 2=m ×v 2+2m v B ′,解得v B ′=3
4v
所以v A ′v B ′=v
23
4v =23。选项D 正确。
答案
D
考点一 动量定理的理解与应用 1.应用动量定理时应注意
(1)动量定理的研究对象是一个质点(或可视为一个物体的系统)。
(2)动量定理的表达式是矢量式,在一维情况下,各个矢量必须选同一个正方向。 2.动量定理的应用 (1)用动量定理解释现象
①物体的动量变化一定,此时力的作用时间越短,力就越大;时间越长,力就越小。
②作用力一定,此时力的作用时间越长,动量变化越大;力的作用时间越短,动量变化越小。
(2)应用I =Δp 求变力的冲量。
(3)应用Δp =F ·Δt 求恒力作用下的曲线运动中物体动量的变化量。
【例1】 如图2所示,质量为m =2 kg 的物体,在水平力F =16 N 的作用下,由静止开始沿水平面向右运动。已知物体与水平面间的动摩擦因数μ=0.2,若F
作用t 1=2 s 后撤去,撤去F 后又经t 2=2 s ,物体与竖直墙壁相碰,若物体与墙壁作用时间t 3=0.1 s ,碰撞后反向弹回的速度v ′=6 m/s ,求墙壁对物体的平均作用力大小。(g 取10 m/s 2)
图2
解析 解法一:程序法
以物体为研究对象,在t 1时间内其受力情况如图甲所示,选F 的方向为正方向。 由牛顿第二定律:F -μmg =ma 1① 撤去F 时的速度:v 1=a 1t 1② 撤去F 后受力情况如图乙所示
由牛顿第二定律:-μmg =ma 2③
物体开始碰墙时的速度为v 2,则v 2=v 1+a 2t 2④
对碰墙过程,设墙对物体的平均作用力大小为F -
,选水平向左为正方向,由动量
定理:F -
t 3=m v ′-m (-v 2)⑤
联立①②③④⑤并代入数据解得:F -
=280 N 。 解法二:全过程整体考虑
取从物体开始运动到碰撞后反向弹回的全过程用动量定理,并取F 方向为正方向,则由动量定理:
Ft 1-μmg (t 1+t 2)-F -
t 3=-m v ′
代入数据整理解得:F -
=280 N 。 答案 280 N
1.用动量定理解题的基本思路
2.对过程较复杂的运动,可分段用动量定理,也可整个过程用动量定理。
【变式训练】
1.物体在恒定的合力作用下做直线运动,在时间t1内动能由零增大到E k1,在时间t2内动能由E k1增加到2E k1,设合力在时间t1内做的功为W1,冲量为I1,在时间t2内做的功是W2,冲量为I2则()
A.I1
C.I1>I2,W1 解析根据动能定理有W1=E k1-0=E k1,W2=2E k1-E k1=E k1,所以W1=W2;根据动量定理和动量与动能的关系式p=2mE k,有I1=2mE k1-0=2mE k1,I2=2mE k1-2mE k1=(2-2)mE k1,显然I1>I2。 答案 B 考点二动量守恒定律的条件及应用 1.动量守恒定律适用条件 (1)前提条件:存在相互作用的物体系。 (2)理想条件:系统不受外力。 (3)实际条件:系统所受合外力为0。 (4)近似条件:系统内各物体间相互作用的内力远大于系统所受的外力。 (5)方向条件:系统在某一方向上满足上面的条件,则此方向上动量守恒。2.动量守恒定律的表达式 (1)m1v1+m2v2=m1v1′+m2v2′,相互作用的两个物体组成的系统,作用前的动量和等于作用后的动量和。 (2)Δp1=-Δp2,相互作用的两个物体动量的增量等大反向。 (3)Δp=0,系统总动量的增量为零。 【例2】如图3所示,两块厚度相同的木块A、B,紧靠着放在光滑的桌面上,其质量分别为2.0 kg、0.9 kg,它们的下表面光滑,上表面粗糙,另有质量为0.10 kg的铅块C(大小可以忽略)以10 m/s的速度恰好水平地滑到A的上表面,由于摩擦,铅块C最后停在木块B上,此时B、C的共同速度v=0.5 m/s。求木块A的最终速度和铅块C刚滑到B上时的速度。 图3 解析铅块C在A上滑行时,木块一起向右运动,铅块C刚离开A时的速度设为v C′,A和B的共同速度为v A,在铅块C滑过A的过程中,A、B、C所组成的系统动量守恒,有m C v0=(m A+m B)v A+m C v C′ 在铅块C滑上B后,由于B继续加速,所以A、B分离,A以v A匀速运动,在铅块C在B上滑行的过程中,B、C组成的系统动量守恒,有m B v A+m C v C′=(m B +m C)v 代入数据解得v A=0.25 m/s,v C′=2.75 m/s。 答案0.25 m/s 2.75 m/s 动量守恒定律的解题步骤 【变式训练】 2.[2014·江苏卷,12C(3)]牛顿的《自然哲学的数学原理》中记载,A 、B 两个玻璃球相碰,碰撞后的分离速度和它们碰撞前的接近速度之比总是约为15∶16。分离速度是指碰撞后B 对A 的速度,接近速度是指碰撞前A 对B 的速度。若上述过程是质量为2m 的玻璃球A 以速度v 0碰撞质量为m 的静止玻璃球B ,且为对心碰撞,求碰撞后A 、B 的速度大小。 解析 设A 、B 球碰撞后的速度分别为v 1和v 2 由动量守恒定律知:2m v 0=2m v 1+m v 2,且由题意知v 2-v 1v 0 =1516 解得v 1=1748v 0,v 2=31 24v 0 答案 1748v 0 3124v 0 考点三 碰撞模型的规律及应用 1.碰撞的特点和种类 (1)碰撞的特点 ①作用时间极短,内力远大于外力,满足动量守恒; ②满足能量不增加原理; ③必须符合一定的物理情境。 (2)碰撞的种类 ①完全弹性碰撞:动量守恒,动能守恒,质量相等的两物体发生完全弹性碰撞时交换速度; ②非完全弹性碰撞:动量守恒、动能不守恒; ③完全非弹性碰撞:动量守恒,动能不守恒,碰后两物体共速,系统机械能损失最大。 2.碰撞现象满足的规律 (1)动量守恒定律。 (2)机械能不增加。 (3)速度要合理。 ①若碰前两物体同向运动,则应有v 后>v 前,碰后原来在前的物体速度一定增大,若碰后两物体同向运动,则应有v 前′≥v 后′。 ②碰前两物体相向运动,碰后两物体的运动方向不可能都不改变。 【例3】[(2014·新课标全国卷Ⅰ,35(2)]如图4,质量分别为m A、m B的两个弹性小球A、B静止在地面上方,B球距离地面的高度h=0.8 m,A球在B球的正上方。先将B球释放,经过一段时间后再将A球释放。当A球下落t=0.3 s时,刚好与B球在地面上方的P点处相碰。碰撞时间极短,碰后瞬间A球的速度恰为零。已知m B=3m A,重力加速度大小g=10 m/s2,忽略空气阻力及碰撞中的动能损失。求: 图4 (1)B球第一次到达地面时的速度; (2)P点距离地面的高度。 解析(1)设B球第一次到达地面时的速度大小为v B,由运动学公式有 v B=2gh① 将h=0.8 m代入上式,得 v B=4 m/s② (2)设两球相碰前后,A球的速度大小分别为v1和v1′(v1′=0),B球的速度分别为v2和v2′。由运动学规律可得v1=gt③ 由于碰撞时间极短,重力的作用可以忽略,两球相碰前后的动量守恒,总动能保持不变,规定向下的方向为正,有 m A v1+m B v2=m B v2′④ 1 2m A v21+ 1 2m B v22= 1 2m B v2′2⑤ 设B球与地面相碰后的速度大小为v B′,由运动学及碰撞的规律可得v B′=v B ⑥ 设P点距地面的高度为h′,由运动学规律可得 h′=v B′2-v22 2g⑦ 联立②③④⑤⑥⑦式,并代入已知条件可得h′=0.75 m⑧ 答案 (1)4 m/s (2)0.75 m 碰撞问题解题策略 (1)抓住碰撞的特点和不同种类碰撞满足的条件,列出相应方程求解。 (2)可熟记一些公式,例如“一动一静”模型中,两物体发生弹性正碰后的速度满足: v 1=m 1-m 2m 1+m 2v 0、v 2=2m 1m 1+m 2v 0 。 (3)熟记弹性正碰的一些结论,例如,当两球质量相等时,两球碰撞后交换速度;当m 1?m 2,且v 20=0时,碰后质量大的速率不变,质量小的速率为2v 。当m 1?m 2,且v 20=0时,碰后质量小的球原速率反弹。 【变式训练】 3.三个完全相同的小球A 、B 、C ,质量满足m A =m B =m C =2 kg ,静止在光滑地面上并沿“一”字形依次排开,如图5所示。用锤子轻轻敲击A 球,使之获得一个向右的速度v 0=4 m/s ,A 、B 两球碰撞后粘合在一起,再与C 球碰撞,最后C 球获得v C =2 m/s 的向右的速度。 图5 (1)求第一次碰撞后A 、B 两球粘合在一起的共同速度; (2)第二次碰撞是不是弹性碰撞? (3)求两次碰撞过程,系统损失的能量ΔE 。 解析 (1)A 、B 两球相碰满足动量守恒,则有m v 0=2m v 1 可得两球共同速度v 1=2 m/s 。 (2)A 、B 两球与C 球相碰也满足动量守恒,则有2m v 1=m v c +2m v 2可得A 、B 两球跟C 球相碰后的速度v 2=1 m/s 第二次碰撞损失的机械能ΔE 2=12〃2m v 21-12〃2m v 22-12 m v 2C =2 J ,则有机械能损失, 所以第二次碰撞不是弹性碰撞。 (3)第一次碰撞损失的机械能 ΔE 1=12m v 20-12 〃2m v 2 1=8 J 根据能量守恒得ΔE =ΔE 1+ΔE 2=8 J +2 J =10 J 答案 (1)2 m/s (2)不是弹性碰撞 (3)10 J 考点四 动量观点和能量观点的综合应用 1.动量的观点和能量的观点 动量的观点:动量定理和动量守恒定律 能量的观点:动能定理和能量守恒定律 2.动量守恒定律与机械能守恒定律的比较 【例4】 [(2014·山东卷,39(2)]如图6所示,光滑水平直轨道上两滑块A 、B 用橡皮筋连接,A 的质量为m 。开始时橡皮筋松弛,B 静止,给A 向左的初速度v 0。一段时间后,B 与A 同向运动发生碰撞并粘在一起。碰撞后的共同速度是碰撞前瞬间A 的速度的两倍,也是碰撞前瞬间B 的速度的一半。求: 图6 (1)B 的质量; (2)碰撞过程中A 、B 系统机械能的损失。 解析 (1)以初速度v 0的方向为正方向,设B 的质量为m B ,A 、B 碰撞后的共同速度为v ,由题意可知:碰撞前瞬间A 的速度为v 2,碰撞前瞬间B 的速度为2v ,由 动量守恒定律得m v 2+2m B v =(m +m B )v ① 由①式得m B =m 2② (2)从开始到碰后的全过程,由动量守恒定律得 m v 0=(m +m B )v ③ 设碰撞过程A 、B 系统机械能的损失为ΔE ,则 ΔE =12m (v 2)2+12m B (2v )2-1 2 (m +m B )v 2④ 联立②③④式得ΔE =16m v 2 0。 答案 (1)12m (2)1 6m v 20 利用动量和能量的观点解题的技巧 (1)若研究对象为一个系统,应优先考虑应用动量守恒定律和能量守恒定律(机械能守恒定律)。 (2)若研究对象为单一物体,且涉及功和位移问题时,应优先考虑动能定理。 【变式训练】 4.如图7所示,半径为R 的1/4的光滑圆弧轨道竖直放置,底端与光滑的水平轨道相接,质量为m 2的小球B 静止在光滑水平轨道上,其左侧连接了一轻质弹簧,质量为m 1的小球A 从D 点以速度2gR 向右运动,重力加速度为g ,试求: 图7 (1)小球A 撞击轻质弹簧的过程中,弹簧最短时B 球的速度是多少; (2)要使小球A 与小球B 能发生二次碰撞,m 1与m 2应满足什么关系。 解析 (1)当两球速度相等时弹簧最短,由动量守恒定律得m 1v 0=(m 1+m 2)v 1 解得v 1=m 12gR m 1+m 2。 (2)由动量守恒定律得 m 1v 0=m 2v 2-m 1v 1′ 由能量守恒定律得 12m 1v 20=12m 2v 22+12 m 1v 1′2 发生第二次碰撞的条件是v 2<v 1′ 解得m 1<m 2 3。 答案 (1) m 12gR m 1+m 2 (2)m 1<m 2 3 1.玻璃杯从同一高度落下,掉在水泥地上比掉在草地上容易碎,这是由于玻璃杯与水泥地面撞击的过程中 ( ) A .玻璃杯的动量较大 B .玻璃杯受到的冲量较大 C .玻璃杯的动量变化较大 D .玻璃杯的动量变化较快 解析 玻璃杯从相同高度落下,落地的速度大小是相同的,落地后速度变为零,所以无论落在水泥地面上还是草地上,玻璃杯动量的变化量是相同的,又由动量定理知受到的冲量也是相同的,所以A 、B 、C 都错;由动量定理Ft =m v ′-m v ,落在水泥地面上,作用时间短,动量变化快,受力大,杯容易碎。 答案 D 2.在光滑的水平面上,有a 、b 两球,其质量分别为m a 、m b ,两球在t 0时刻发生正碰,并且在碰撞过程中无机械能损失,两球在碰撞前后的速度图象如图8所示,下列 图8 关系正确的是 ( ) A .m a >m b B .m a <m b C .m a =m b D .无法判断 解析 由动量守恒定律得m a v a =m a v a ′+m b v b ′,由于v a ′<0,则b 球获得的动量大于a 球最初的动量。若m a =m b ,则两球交换速度,与图象不符;由E k =p 22m 知,若m a >m b ,则b 球的动能将会大于a 球最初的动能,违背能量守恒定律,则必然满足m a <m b 。 答案 B 3.(2014·北京东城区示范校联考)如图9所示,静止在光滑水平面上的木板A ,右端有一根轻质弹簧沿水平方向与木板相连,木板质量M =3 kg 。质量m =1 kg 的铁块B 以水平速度v 0=4 m/s 从木板的左端沿板面向右滑行,压缩弹簧后又被弹回,最后恰好停在木板的左端。在上述过程中弹簧具有的最大弹性势能为 ( ) 图9 A .3 J B .4 J C .6 J D .20 J 解析 设铁块与木板共速时速度大小为v ,铁块相对木板向右运动的最大距离为L ,铁块与木板之间的摩擦力大小为f 。铁块压缩弹簧使弹簧最短时,由能量守恒可得12m v 20=fL +12(M +m )v 2+E p 。由动量守恒,得m v 0=(M +m )v 。从铁块开始运 动到最后停在木板左端过程,由能量关系得12m v 20=2fL +1 2(M +m )v 2。联立解得E p =3 J ,故选项A 正确。 答案 A 4.如图10所示,两个小球A 和B 质量分别是m A =2.0 kg ,m B =1.6 kg ,球A 静止在光滑水平面上的M 点,球B 在水平面上从远处沿两球的中心连线向着球A 运动,假设两球相距L ≤18 m 时存在着恒定的斥力F , L >18 m 时无相互作用力。当两球相距最近时,它们间的距离为d =2 m ,此时球 图10 B的速度是4 m/s。求: (1)球B的初速度大小; (2)两球之间的斥力大小; (3)两球从开始相互作用到相距最近时所经历的时间。 解析(1)当两球相距最近时两球速度相同,即 v A=v B=4 m/s 由动量守恒定律可得:m B v B0=m A v A+m B v B 代入数据解得v B0=9 m/s。 (2)两球从开始相互作用到它们之间距离最近时它们之间的相对位移Δs=L-d,由功能关系可得: F〃Δs=1 2m B v2B0- 1 2m A v2A- 1 2m B v2B 代入数据解得F=2.25 N。 (3)设两球从开始相互作用到两球相距最近时的时间为t,根据动量定理,对A球有:Ft=m A v A-0 代入数据解得t=m A v A F=3.56 s。 答案(1)9 m/s(2)2.25 N(3)3.56 s 5.(2014·全国大纲卷,24)冰球运动员甲的质量为80.0 kg。当他以5.0 m/s的速度向前运动时,与另一质量为100 kg、速度为3.0 m/s的迎面而来的运动员乙相撞。碰后甲恰好静止。假设碰撞时间极短,求: (1)碰后乙的速度的大小; (2)碰撞中总机械能的损失。 解析(1)设运动员甲、乙的质量分别为m、M,碰前速度大小分别为v、V,碰后乙的速度大小为V′。由动量守恒定律有m v-MV=MV′ 代入数据得V′=1.0 m/s (2)设碰撞过程中总机械能的损失为ΔE,应有 1 2m v 2+ 1 2MV 2= 1 2MV′ 2+ΔE V′=1.0 m/s,代入上式解得ΔE=1 400 J。答案(1)1.0 m/s(2)1 400 J 基本技能练 1.在如图1所示的装置中,木块B 与水平桌面间的接触是光滑的,子弹A 沿水平方向射入木块后留在其中,将弹簧压缩到最短。若将子弹、木块和弹簧合在一起作为系统,则此系统在从子弹开始射入到弹簧被压缩至最短的整个过程中 ( ) A .动量守恒,机械能守恒 B .动量不守恒,机械能不守恒 C .动量守恒,机械能不守恒 D .动量不守恒,机械能守恒 解析 子弹射入木块是瞬间完成的,这个过程相当于子弹与木块发生一次完全非弹性碰撞,动量守恒,机械能不守恒,一部分动能转化为内能。之后木块(连同子弹)压缩弹簧,将其动能转化为弹性势能,这个过程机械能守恒,但由于左侧挡板的支持力的冲量作用,使系统的动量不断减少,动量不守恒。所以整个过程中,动量和机械能均不守恒。 答案 B 2.(多选)如图2所示,A 、B 两物体的质量m A >m B ,中间用一段细绳相连并有一被压缩的弹簧,放在平板小车C 上后,A 、B 、C 均处于静止状态。若地面光滑,则在细绳被剪断后,A 、B 从C 上滑离之前,A 、B 在C 上向相反方向滑动过程中 ( ) A .若A 、 B 与 C 之间的摩擦力大小相同,则A 、B 组成的系统动量守恒,A 、B 、C 组成的系统动量也守恒 B .若A 、B 与 C 之间的摩擦力大小不相同,则A 、B 组成的系统动量不守恒,A 、B 、C 组成的系统动量也不守恒 C .若A 、B 与C 之间的摩擦力大小不相同,则A 、B 组成的系统动量不守恒,但 图1 图2 A、B、C组成的系统动量守恒 D.以上说法均不对 解析当A、B两物体组成一个系统时,弹簧的弹力为内力,而A、B与C之间的摩擦力为外力。当A、B与C之间的摩擦力等大、反向时,A、B组成的系统所受外力之和为零,动量守恒;当A、B与C之间的摩擦力大小不相等时,A、B组成的系统所受外力之和不为零,动量不守恒。而对于A、B、C组成的系统,由于弹簧的弹力,A、B与C之间的摩擦力均为内力,故不论A、B与C之间的摩擦力的大小是否相等,A、B、C组成的系统所受外力之和圴为零,故系统的动量守恒。 答案AC 3.(多选)质量都为m的小球a、b、c以相同的速度分别与另外三个质量都为M 的静止小球相碰后,a球被反向弹回,b球与被碰球粘合在一起仍沿原方向运动,c球碰后静止,则下列说法正确的是() A.m一定小于M B.m可能等于M C.b球与质量为M的球组成的系统损失的动能最大 D.c球与质量为M的球组成的系统损失的动能最大 解析由a球被反向弹回,可以确定三小球的质量m一定小于M;当两小球发生完全非弹性碰撞时损失的动能最大,b球与被碰球粘合在一起,发生的是完全非弹性碰撞。 答案AC 4.(多选)一只小球沿光滑水平面运动,垂直于墙面撞到竖直墙上。小球撞墙前后的动量变化量为Δp,动能变化量为ΔE。关于Δp和ΔE下列说法正确的是 () A.若Δp最大,则ΔE也最大 B.若Δp最大,则ΔE一定最小 C.若Δp最小,则ΔE也最小 D.若Δp最小,则ΔE一定最大 解析当小球原速率返回时,Δp最大,而ΔE=0,选项B正确,A错误;当小 球撞到墙后速度减为零时,Δp 最小,而ΔE 最大,选项D 正确,C 错误。 答案 BD 5.物体的动量变化量的大小为5 kg ·m/s ,这说明 ( ) A .物体的动量在减小 B .物体的动量在增大 C .物体的动量大小也可能不变 D .物体的动量大小一定变化 解析 动量是矢量,动量变化了5 kg 〃m/s ,物体动量的大小可以增大,也可以减小,还可能不变。若物体以大小为5 kg 〃m/s 的动量做匀速圆周运动时,物体的动量大小保持不变,当末动量方向与初动量方向间的夹角为60°时,物体的动量变化量的大小为5 kg 〃m/s 。 答案 C 6.(多选)光滑水平地面上,A 、B 两物体质量都为m ,A 以速度v 向右运动,B 原来静止,左端有一轻弹簧,如图3所示,当A 撞上弹簧,弹簧被压缩最短时 ( ) A .A 、 B 系统总动量仍然为m v B .A 的动量变为零 C .B 的动量达到最大值 D .A 、B 的速度相等 解析 系统水平方向动量守恒,A 正确;弹簧被压缩到最短时A 、B 两物体具有相同的速度,D 正确、B 错误;但此时B 的速度并不是最大的,因为弹簧还会弹开,故B 物体会进一步加速,A 物体会进一步减速,C 错误。 答案 AD 7.(多选)两个小球A 、B 在光滑水平面上相向运动,已知它们的质量分别是m 1=4 kg ,m 2=2 kg ,A 的速度v 1=3 m/s(设为正),B 的速度v 2=-3 m/s ,则它们发生正碰后,其速度可能分别是 ( ) A .均为1 m/s B .+4 m/s 和-5 m/s C .+2 m/s 和-1 m/s D .-1 m/s 和+ 5 m/s 图3 解析 由动量守恒,可验证四个选项都满足要求。再看动能情况: E k =12m 1v 21 +12m 2v 22=12×4×9 J +12×2×9 J =27 J E k ′=12m 1v ′21+12 m 2v ′2 1 由于碰撞过程动能不可能增加,所以应有E k ≥E k ′,可排除选项B 。选项C 虽满足E k ≥E k ′,但A 、B 沿同一直线相向运动,发生碰撞后各自仍能保持原来速度方向(v A ′>0,v B ′<0),这显然是不符合实际的,因此C 错误。验证选项A 、D 均满足E k ≥E k ′,故答案为选项A(完全非弹性碰撞)和选项D(弹性碰撞)。 答案 AD 8.质量是60 kg 的建筑工人,不慎从高空跌下,由于弹性安全带的保护,使他悬挂起来。己知安全带的缓冲时间是1.2 s ,安全带长5 m ,取g =10 m/s 2,则安全带所受的平均冲力的大小为 ( ) A .500 N B .600 N C .1 100 N D .100 N 解析 安全带长5 m ,人在这段距离上做自由落体运动,获得速度v =2gh =10 m/s 。受安全带的保护经1.2 s 速度减小为0,对此过程应用动量定理,以向上为正方向,有(F -mg )t =0-(-m v ),则F =m v t +mg =60×101.2 N +60×10 N =1 100 N 。 答案 C 能力提高练 9.(2014·重庆卷,4)一弹丸在飞行到距离地面5 m 高时仅有水平速度v =2 m/s ,爆炸成为甲、乙两块水平飞出,甲、乙的质量比为3∶1,不计质量损失,取重力加速度g =10 m/s 2,则下列图中两块弹片飞行的轨迹可能正确的是( ) 第2课时核外电子排布与元素周期表、原子半径 [学习目标定位] 1.了解核外电子排布规律与元素周期表中周期、族划分的关系,并能解释它们之间的变化规律。2.了解原子半径的意义及其测定方法,知道原子半径与原子核外电子排布的关系,并能解释原子半径在周期表中的变化规律。 一、核外电子排布与元素周期表 1.原子核外电子排布与周期的划分 (1)填写下表: (2)观察分析上表,讨论原子核外电子排布与周期划分的本质联系。 ①根据能级能量的差异,可将能量相近的能级分为七个能级组,同一能级组内,各能级能量相差较小,各能级组之间能量相差较大。 ②每一个能级组对应一个周期,且该能级组中最大的电子层数等于元素的周期序数。 ③一个能级组最多容纳的电子数等于对应的周期所含的元素种数。 2.原子核外电子排布与族的划分 (1)将下列各主族元素的价电子数、价电子排布式填入表中: (2)以第4周期副族元素为例,填写下表: (3)依据上述表格,分析讨论族的划分与原子核外电子排布的关系。 族的划分依据与原子的价电子数目和价电子排布密切相关。 ①同主族元素原子的价电子排布相同,价电子全部排布在最外层的n s或n s n p轨道上。族序数与价电子数相同。 ②稀有气体的价电子排布为1s2或n s2n p6。 ③过渡元素(副族和第Ⅷ族)同一纵行原子的价电子排布基本相同。价电子排布式为(n-1)d1~10n s1~2,第ⅢB~ⅦB族的族序数与价电子数相同,第ⅠB、ⅡB族的族序数=n s轨道上的电子数,第Ⅷ族的价电子数分别为8、9、10。 3.原子核外电子排布与区的划分 (1)最外层电子排布与周期表的关系 ①原子的电子层数=能级中最高能层序数=周期序数 ②主族元素原子的最外层电子数=主族元素原子的价电子数=主族序数 (2)对价电子认识的误区提醒 ①价电子不一定是最外层电子,只有主族元素的价电子才是最外层电子。对于过渡元素还包括部分内层电子。 ②元素的价电子数不一定等于其所在族的族序数。这只对主族元素成立,对部分过渡元素是不成立的。 ③同一族元素的价电子排布不一定相同,如过渡元素中的镧系元素和锕系元素就不相同,在第Ⅷ族中部分元素的价电子排布也不相同。 例 高中物理原子结构、原子核检测题 1.下列说法正确的是( ) A.γ射线比α射线的贯穿本领强 B.外界环境温度升高,原子核的半衰期变大 C.太阳辐射的能量主要来自太阳内部的重核裂变反应 D.原子核发生一次β衰变,该原子外层就失去一个电子 解析:选A γ射线比α射线的贯穿本领强,选项A正确;外界环境不影响原子核的半衰期,选项B 错误;太阳辐射的能量主要来自太阳内部的轻核聚变反应,选项C错误;β衰变是原子核内的中子转化为质子时放出的负电子,与原子的外层电子无关,选项D错误。 2.232 90Th经过一系列α衰变和β衰变后变成208 82Pb,则208 82Pb比232 90Th少( ) A.16个中子,8个质子B.8个中子,16个质子 C.24个中子,8个质子D.8个中子,24个质子 解析:选A 208 82Pb比232 90Th质子数少(90-82)=8个,核子数少(232-208)=24个,所以中子数少(24- 8)=16个,故A正确,B、C、D错误。 3.下列说法正确的是( ) A.光子像其他粒子一样,不但具有能量,也具有动量 B.比结合能越大,原子核越不稳定 C.将由放射性元素组成的化合物进行高温分解,会改变放射性元素的半衰期 D.原子核的质量大于组成它的核子的质量之和,这个现象叫做质量亏损 解析:选 A 光子像其他粒子一样,不但具有粒子性,而且也有波动性,则不但具有能量,也具有动量,故A正确;比结合能越大,原子核越稳定,B错误;放射性元素的半衰期与外界因素没有任何关系,只和本身性质有关,C错误;原子核的质量小于组成它的核子的质量之和,这个现象叫做质量亏损,故D错误。 4.[多选](2019·天津高考)我国核聚变反应研究大科学装置“人造太阳” 2018年获得重大突破,等离子体中心电子温度首次达到1亿度,为人 类开发利用核聚变能源奠定了重要的技术基础。下列关于聚变的说法 正确的是( ) A.核聚变比核裂变更为安全、清洁 B.任何两个原子核都可以发生聚变 C.两个轻核结合成质量较大的核,总质量较聚变前增加 D.两个轻核结合成质量较大的核,核子的比结合能增加 解析:选AD 与核裂变相比,轻核聚变没有放射性污染,安全、清洁,A正确;只有原子序数小的轻核才能发生聚变,B错误;轻核聚变成质量较大的原子核,比结合能增加、总质量减小,故C错误,D正确。 原子核的组成 时间:45分钟 一、选择题(1~6题为单选,7~9题为多选) 1.关于γ射线,下列说法不正确的是( B ) A.它是处于激发态的原子核放射的 B.它是原子内层电子受到激发时产生的 C.它是一种不带电的光子流 D.它是波长极短的电磁波 解析:γ射线是处于激发态的原子核发出的波长极短的电磁波,是一种光子. 2.如图为查德威克实验示意图,由天然放射性元素钋(Po)放射的α射线轰击铍时会产生粒子流A,用粒子流A轰击石蜡时,会打出粒子流B,经研究知道( A ) A.A为中子,B为质子 B.A为质子,B为中子 C.A为γ射线,B为中子 D.A为中子,B为γ射线 解析:用放射源钋的α射线轰击铍时,能发射出一种穿透力极强的中性射线,这就是所谓铍“辐射”,即中子流,中子轰击石蜡,将氢中的质子打出,即形成质子流,所以A 为中子,B为质子,所以A正确. 3.32He可以作为核聚变材料(核聚变是利用轻核聚合为较重核释放出巨大能量为人类提供能源),下列关于32He的叙述正确的是( C ) A.32He与31H互为同位素 B.32He原子核内中子数为2 C.32He原子核外电子数为2 D.32He代表原子核内有2个质子和3个中子的氦原子 解析:32He核内质子数为2,31H核内质子数为1.两者质子数不等,不是同位素,A错误.32 He核内中子数为1,B错误,C正确.32He代表原子核内有2个质子和1个中子的氦原子,D 错误. 4.放射性元素放出的射线,在电场中分成A、B、C三束,如图所示,其中( C ) A.C为氦原子核组成的粒子流 B.B为比X射线波长更长的光子流 C.B为比X射线波长更短的光子流 D.A为高速电子组成的电子流 解析:根据射线在电场中的偏转情况,可以判断,A射线向电场线方向偏转,应为带正电的粒子组成的射线,所以是α射线;B射线在电场中不偏转,所以是γ射线;C射线在电场中受到与电场方向相反的作用力,应为带负电的粒子,所以是β射线. 5.图中曲线a、b、c、d为气泡室中某放射物发生衰变放出的部分粒子的径迹,气泡室中磁感应强度方向垂直于纸面向里.以下判断可能正确的是( D ) A.a、b为β粒子的径迹 B.a、b为γ粒子的径迹 C.c、d为α粒子的径迹 D.c、d为β粒子的径迹 解析:γ粒子不带电,不会发生偏转,故B错.由左手定则可判定,a、b粒子带正电,c、d粒子带负电,又知α粒子带正电,β粒子带负电,故A、C均错,D正确. 6.若用x代表一个中性原子的核外电子数,y代表此原子的原子核内的质子数,z代表此原子的原子核内的中子数,则对234 90Th的原子来说( B ) A.x=90,y=90,z=234 B.x=90,y=90,z=144 元素周期表中的规律 一、元素周期表 1、周期表结构 横行——周期:共七个周期,三短三长一不完全。 各周期分别有2,8,8,18,18,32,26种元素。前三个周期为短周期,第四至第六这三个周期为长周期,第七周期还没有排满,为不完全周期。 纵行——族:七主七副一零一VIII,共16族,18列。要记住零族元素的原子序数以便迅速由原子序数确定元素名称。 周期:一二三四五六七 元素种类:28818183226 零族:2He10Ne 18Ar 36Kr54Xe86Rn 二、元素周期表中元素及其化合物的递变性规律 1.原子结构与元素周期表的关系 电子层数= 周期数 主族元素最外层电子数= 主族序数= 最高正化合价 由上述关系,就可以由原子结构找出元素在周期表中的位置,也可以由位置确定原子结构。 2、规律性 由此可见,金属性最强的元素在周期表的左下角即Cs(Fr具有放射性,不考虑),非金属性最强的元素在右上角即F。对角线附近的元素不是典型的金属元素或典型的非金属元素。 3、元素周期表中之最 原子半径最小的原子:H原子 质量最轻的元素:H元素; 非金属性最强的元素:F 金属性最强的元素:Cs(不考虑Fr) 最高价氧化物对应水化物酸性最强的酸:HClO4 最高价氧化物对应水化物碱性最强的碱:CsOH 形成化合物最多的元素:C元素 所含元素种类最多的族:ⅢB 地壳中含量最高的元素:O元素,其次是Si元素 地壳中含量最高的金属元素:Al元素,其次是Fe元素 含H质量分数最高的气态氢化物:CH4 与水反应最剧烈的金属元素:Cs元素 与水反应最剧烈的非金属元素:F元素 常温下为液态的非金属单质是Br2,金属单质是Hg …… 4、特殊性 第一章:原子结构与元素周期律 教案编写日期:2012-2-16 课程授课日期: 应到人数: 实到人数: 教学目标: 过程与方法: 通过亲自编排元素周期表培养学生的抽象思维能力和逻辑思维能力;通过对元素原子结构、位置间的关系的推导,培养学生的分析和推理能力。 通过对元素周期律和元素周期表的关系的认识,渗透运用辩证唯物主义观点分析现象和本质的关系。 情感态度价值观: 通过学生亲自编排元素周期表培养学生的求实、严谨和创新的优良品质;提高学生的学习兴趣 教学方法:通过元素周期表是元素周期律的具体表现形式的教学,进行“抽象和具体”这一科学方法的指导。 教学重难点:同周期、同主族性质的递变规律;元素原子的结构、性质、位置之间的关系。 教学过程: 中子N (核素) 原子核 质子Z → 元素符号 原子结构 : 决定原子呈电中性 电子数(Z 个): 化学性质及最高正价和族序数 体积小,运动速率高(近光速),无固定轨道 核外电子 运动特征 电子云(比喻) 小黑点的意义、小黑点密度的意义。 排布规律 → 电子层数 周期序数及原子半径 表示方法 → 原子(离子)的电子式、原子结构示意图 随着原子序数(核电荷数)的递增:元素的性质呈现周期性变化: ①、原子最外层电子数呈周期性变化 元素周期律 ②、原子半径呈周期性变化 ③、元素主要化合价呈周期性变化 ④、元素的金属性与非金属性呈周期性变化 ①、按原子序数递增的顺序从左到右排列; 元素周期律和 排列原则 ②、将电子层数相同的元素排成一个横行; 元素周期表 ③、把最外层电子数相同的元素(个别除外)排成一个纵行。 ①、短周期(一、二、三周期) 周期(7个横行) ②、长周期(四、五、六周期) 周期表结构 ③、不完全周期(第七周期) A ~ⅦA 共7个) 元素周期表 族(18个纵行) ②、副族(ⅠB ~ⅦB 共7个) ③、Ⅷ族(8、9、10纵行) ④、零族(稀有气体) 同周期同主族元素性质的递变规律 ①、核电荷数,电子层结构,最外层电子数 ②、原子半径 决定 编排依据 具 体 表 现 形式 X) (A Z 七 主 七 副零和八 三长三短一不全 14、2 原子结构和原子核 主备人:贾宝善备课组长:周春燕备课时间:2013/11/25 授课时间:2013/12/11 学习目标: 1.了解人们对原子结构的认识过程 2.氢原子的能级图 3.氢光谱 原子的核式结构 卢瑟福由α粒子散射实验提出:在原子的中心有一个很小的核,叫原子核,原子的全部正电荷和几乎全部质量都集中在原子核里,带负电的电子在核外空间运动。我们把这样的原子模型称为“核式结构模型”。 五、天然放射现象 1.天然放射现象:某些元素能自发地放出射线的现象叫做天然放射现象。这些元素称为放射性元素。 2.种类和性质 α射线——高速的α粒子流,α粒子是氦原子核,速度约为光速1/10,贯穿能力最弱,电离能力最强。 β射线——高速的电子流,β粒子是速度接近光速的负电子,贯穿能力稍强,电离能力稍弱。γ射线——能量很高的电磁波,γ粒子是波长极短的光子, 贯穿能力最强,电离能力最弱。 六、原子核的衰变 1.衰变:原子核自发地放出某种粒子而转变为新核的变化. 2.衰变规律:α衰变X→ Y+ He ; β衰变X→ Y+ e 3.α衰变的实质:某元素的原子核同时发出由两个质子和两个中子组成的粒子(即氦核)2 H+2 n→ He β衰变的实质:某元素的原子核内的一个中子变成质子发射出一个电子。即n → H+ e+ (为反中微子) 4.γ射线:总是伴随α衰变或β衰变产生的,不能单独放出γ射线.γ射线不改变原子核的电荷数和质量数.实质是元素在发生α衰变或β衰变时产生的某些新核由于具有过多的能量(核处于激发态),向低能级跃迁而辐射出光子. 七、半衰期 1.放射性元素的原子核有半数发生衰变需要的时间。它是大量原子核衰变的统计结果,不是一个原子发生衰变所需经历的时间。 2.决定因素:由原子核内部的因素决定,与原子所处的物理状态(如压强、温度等)或化学状态(如单质或化合物)无关. 八、原子核的人工转变 1.质子的发现:N+ He→ O+ H 元素周期表的规律 一、原子半径 同一周期(稀有气体除外),从左到右,随着原子序数的递增,元素原子的半径递减; 同一族中,从上到下,随着原子序数的递增,元素原子半径递增。 二、主要化合价(最高正化合价和最低负化合价) 同一周期中,从左到右,随着原子序数的递增,元素的最高正化合价递增(从+1价到+7价),第一周期除外,第二周期的O、F元素除外最低负化合价递增(从-4价到-1价)第一周期除外,由于金属元素一般无负化合价,故从ⅣA族开始。元素最高价的绝对值与最低价的绝对值的和为8 三、元素的金属性和非金属性 同一周期中,从左到右,随着原子序数的递增,元素的金属性递减,非金属性递增;同一族中,从上到下,随着原子序数的递增,元素的金属性递增,非金属性递减; 四、单质及简单离子的氧化性与还原性 同一周期中,从左到右,随着原子序数的递增,单质的氧化性增强,还原性减弱;所对应的简单阴离子的还原性减弱,简单阳离子的氧化性增强。同一族中,从上到下,随着原子序数的递增,单质的氧化性减弱,还原性增强;所对应的简单阴离子的还原性增强,简单阳离子的氧化性减弱。元素单质的还原性越强,金属性就越强;单质氧化性越强,非金属性就越强。 五、最高价氧化物所对应的水化物的酸碱性 同一周期中,从左到右,元素最高价氧化物所对应的水化物的酸性增强(碱性减弱); 同一族中,从上到下,元素最高价氧化物所对应的水化物的碱性增强(酸性减弱)。 元素的最高价氢氧化物的碱性越强,元素金属性就越强;最高价氢氧化物的酸性越强,元素非金属性就越强。 六、单质与氢气化合的难易程度 同一周期中,从左到右,随着原子序数的递增,单质与氢气化合越容易; 同一族中,从上到下,随着原子序数的递增,单质与氢气化合越难。 七、气态氢化物的稳定性 同一周期中,从左到右,随着原子序数的递增,元素气态氢化物的稳定性增强; 同一族中,从上到下,随着原子序数的递增,元素气态氢化物的稳定性减弱。 此外还有一些对元素金属性、非金属性的判断依据,可以作为元素周期律的补充: 随同一族元素中,由于周期越高,价电子的能量就越高,就越容易失去,因此排在下面的元素一般比上面的元素更具有金属性。元素的气态氢化物越稳定,非金属性越强。 同一族的元素性质相近。 以上规律不适用于稀有气体。 八、位置规律判断元素在周期表中位置应牢记的规律: (1)元素周期数等于核外电子层数; (2)主族元素的族数等于最外层电子数。 九、阴阳离子的半径大小辨别规律 三看: 一看电子层数,电子层数越多,半径越大, 二看原子序数,当电子层数相同时,原子序数越大半径反而越小 三看最外层电子数,当电子层数和原子序数相同时最外层电子书越多半径越小 r(Na)>r(Mg)>r(Al)>r(S)>r(Cl)、r(Na+ ) >r(Mg2+ )>r(Al3+ )、r(O2- ) >r(F-) r(S2—)>r(Cl—)>r(Ar) >r(K+)>r(Ca2+)、r(O2—)> r(F—)> r(Na+)> r(Mg2+)> r(Al3+) r(Na+ ) 第十九章原子核 1原子核的组成 一、天然放射现象 1.贝可勒尔的发现 铀和含铀的矿物都能发出一种看不见的射线,这种射线可以穿透黑纸使照相底片感光.物质发射射线的性质称为放射性,具有放射性的元素称为放射性元素. 2.玛丽·居里和皮埃尔·居里夫妇的发现 他们发现了两种放射性更强的元素,为了纪念她的国家波兰,一种元素命名为钋(Po),另一种元素命名为镭(Ra). 3.天然放射现象 自然界中原子序数大于或等于83的元素都能自发地放出射线,这种能自发地发出射线的现象叫做天然放射现象. 二、射线的本质 1.三种射线 在射线经过的空间施加磁场,射线分成三束,其中两束在磁场中向不同的方向偏转,说明这两束是带电粒子流,另一束在磁场中不偏转,说明这一束不带电,这三束射线分别叫做α射线、β射线、γ射线. 2.三种射线的比较 若在射线经过的空间施加电场(方向与射线的出射方向垂直),射线能分成三束吗? 提示:能分成三束,三种射线的带电情况各不相同,它们在电场中受力情况不同,故可偏转为三束. 三、原子核的组成 1.质子的发现 卢瑟福用α粒子轰击氮原子核,发现了质子,质子的实质是氢原子核. 2.中子的发现 卢瑟福的学生查德威克通过实验证实了中子的存在. 3.原子核的组成 原子核由质子和中子组成,质子和中子统称为核子. 4.原子核的电荷数 原子核所带的电荷量总是质子电荷的整数倍,通常用这个整数表示原子核的电荷量,叫做原子核的电荷数. 5.原子核的质量数 质子和中子的总数目叫做原子核的质量数. 6.原子核的符号 A X,其中X表示元素的符号,A表示核的质量数,Z表示核的电荷数. Z 7.同位素 课时跟踪检测(三十八) 原子结构与原子核 对点训练:原子的核式结构 1.卢瑟福通过对α粒子散射实验结果的分析,提出了原子内部存在( ) A .电子 B .中子 C .质子 D .原子核 2.如图所示是α粒子(氦原子核)被重金属原子核散射的运动轨迹,M 、N 、P 、Q 是轨迹上的四点,在散射过程中可以认为重金属原子核静止。图中所标出的α粒子在各点处的加速度方向正确的是( ) A .M 点 B .N 点 C .P 点 D .Q 点 3.(多选)物理学家通过对实验的深入观察和研究,获得正确的科学认知,推动物理学的发展。下列说法符合事实的是( ) A .赫兹通过一系列实验,证实了麦克斯韦关于光的电磁理论 B .查德威克用α粒子轰击 714N 获得反冲核 817O ,发现了中子 C .贝克勒尔发现的天然放射性现象,说明原子核有复杂结构 D .卢瑟福通过对阴极射线的研究,提出了原子核式结构模型 4.原子从一个能级跃迁到一个较低的能级时,有可能不发射光子。例如在某种条件下,铬原子的n =2能级上的电子跃迁到n =1能级上时并不发射光子,而是将相应的能量转交给n =4能级上的电子,使之脱离原子,这一现象叫做俄歇效应,以这种方式脱离了原子的电 子叫做俄歇电子,已知铬原子的能级公式可简化表示为E n =-A n 2,式中n =1,2,3,…表示不同能级,A 是正的已知常数,上述俄歇电子的动能是( ) A.1116 A B.716A C.316A D.1316 A 5.(多选) 19世纪初,爱因斯坦提出光子理论,使得光电效应现象得以完美解释,玻尔的氢原子模型也是在光子概念的启发下提出的。关于光电效应和氢原子模型,下列说法正确的是( ) A .光电效应实验中,入射光足够强就可以有光电流 B .若某金属的逸出功为W 0,该金属的截止频率为W 0h C .保持入射光强度不变,增大入射光频率,金属在单位时间内逸出的光电子数将减小 D .一群处于第四能级的氢原子向基态跃迁时,将向外辐射六种不同频率的光子 6.(多选)已知氢原子的基态能量为E 1,n =2、3能级所对应的能量分别为E 2和E 3,大 1 原子核的组成 (一)教学目的 1.常识性了解射线的应用,强射线对人体的危害及防护。 2.常识性了解原子核的组成。 3.进行物理学研究方法的启蒙教育。 (二)教具 录像机,监视器,原子弹和氢弹爆炸的录像剪接带。(若没有上述器材可用原子弹、氢弹爆炸的挂图代替) (三)教学过程 进行新课 原子核的组成 (1)电子的发现和放射性现象的发现 我们已经学过,物质是由分子、原子构成的,原子已经是很小很小的微粒了,其直径只有10-10米,所以在十九世纪以前,人们一直认为原子是不可再分的中性粒子。1897年英国物理学家汤姆生在研究阴极射线时发现了电子,而电子比原子小得多,因而人们才认识到原子内部还有结构。 〈电子的发现把人们带入了原子内部的世界〉 在同一时期人们还发现了天然放射性现象,对放射性现象的进一步研究,人们认识到原子核内部还有结构,原子核由比它更小的粒子组成。可见人类对客观世界的认识是没有止尽的。我们先来学习放射性现象。 〈放射性现象的发现把人们带入了原子核内部的世界〉 (2)放射性现象 ①什么是放射性现象? 像铀(U)、钋(Po)、镭(Ra)等元素能自发地放出一些人眼看不见的、能穿透黑纸使照相底片感光的射线,这种现象叫放射性现象。这些元素叫放射性元素。 ②射线究竟是什么? 在放射性现象中放出的射线是什么东西呢?它们除了能穿透黑纸使照相底片感光的性质以外,还有些什么性质呢?比如:这些射线带不带电呢?为了了解它们的性质,还得通过实验。 我们做什么样的实验,才能判断它们带不带电呢?(放射性现象中放出的射线若是带电的,射线在磁场中将像通电导体那样发生偏转,由偏转的方向和磁体的N、S 极位置还可判断射线带的是什么电。) 我们利用已经掌握的知识可以去探索还不知道的现象和规律,最基本的研究方法是通过实验。把放射性元素装在一个壁很厚的铅盒里(射线穿不透),在盒壁上有一个小孔,放射线可由此孔射出,然后把它们放到两个很强的磁极之间,再用照相底片把射线的轨道记录下来。从照相底片上看到,放射线分成了三束,其中两束向相反方向偏转,说明这两束射线带异种电荷;中间一束不偏转,说明它不带电,是中性的。 这三种射线有哪些性质呢?它们的实质是什么呢? 〈射线由两种带异种电荷的粒子和一种不带电的中性粒子组成〉 (3)三种射线 ①α射线 根据射线的偏转方向和磁场方向的关系可以确定,偏转较小的一束由带正电荷的粒子组成,我们把它叫做α射线,α射线由带正电的α粒子组成。科学家们研究发现每个α粒子带的正电荷是电子电荷的2倍,α粒子质量大约等于氦原子的质量。进一步研究表明α粒子就是氦原子核。 〈α射线的实质就是高速运动的氦核流〉 由于α粒子的质量较大,所以α射线的穿透本领最小,我们用一张厚纸就能把它挡住。 ②β射线 与α射线偏转方向相反的那束射线带负电荷,我们把它叫做β射线。研究发现β射线由带负电的粒子(β粒子)组成。进一步研究表明β粒子就是电子。 〈β射线的实质就是高速运动的电子流〉 实验还表明,β射线的穿透本领较强,很容易穿透黑纸,还能穿透几厘米厚的铝板。 ③γ射线 第五章原子结构元素周期律 第一节原子结构原子核外电子排布 【高考新动向】 【考纲全景透析】 一、原子的构成 1. 原子的构成 原子的组成表示式:X,其中X为原子符号,A为质量数,Z为质子数,A-Z为中子数。2.基本关系 ①质子数=核电荷数=核外电子数 ②阳离子中:质子数=核外电子数+电荷数 ③阴离子中:质子数=核外电子数-电荷数 ④质量数=质子数+中子数 3.元素、核素、同位素之间的关系如下图所示: 元素、核素和同位素的概念的比较 二、 原子核外电子排布 1.电子层的表示方法及能量变化 圆圈表示原子核,圆圈内标示出核电荷数,用弧线表示电子层,弧线上的数字表示该电子层的电子数。要注意无论是阳离子还是阴离子,圆圈内的核电荷数是不变的,变化的是最外层电子数。 离核由近及远→电子能量由低到高 2.核外电子分层排布的规律 核外电子的分层运动,又叫核外电子的分层排布,其主要规律有: (1)能量规律 原子核外电子总是先排能量最低的电子层,然后由里向外,依次排布在能量逐步升高的电子层(能量最低原理)。即排满了K 层才排L 层,排满了L 层才排M 层。 (2)分层排布规律 ①原子核外每个电子层最多容纳2n 2 个电子。 ②原子最外层电子数不超过8个电子(K 层为最外层不能超过2个电子)。 ③原子次外层电子数不超过18个电子(K 层为次外层不能超过2个电子)。 【热点难点全析】 〖考点一〗原子的构成及概念比较 1.构成原子的粒子 2.组成原子的各种粒子及相互关系 (1)原子或分子:质子数(Z)=核电荷数=核外电子数 (2)阳离子:核外电子数=质子数-所带电荷数 (3)阴离子:核外电子数=质子数+所带电荷数 3.同位素、同素异形体、同系物、同分异构体的比较 〖提醒〗(1)质子数与核外电子数之间的关系,对于原子不易出错,对于阴、阳离子容易出错。应清楚阳离子核外电子数少于质子数,阴离子核外电子数多于质子数。 (2)元素、同位素、同素异形体、同系物、同分异构体的判断关键是描述的对象。如: ①具有相同质子数的两微粒不一定是同种元素,如Ne和H2O。 ②质子数相同而中子数不同的两微粒不一定互为同位素,如14N2和13C16O。 ③2H2和3H2既不是同位素,也不是同素异形体。 【典例1】铀(U)是重要的核工业原料,其中23592U是核反应堆的燃料,下列关于23592U和23892U的说 第一节原子核的组成 (一)教学目的 1.常识性了解射线的应用,强射线对人体的危害及防护。 2.常识性了解原子核的组成。 3.进行物理学研究方法的启蒙教育。 (二)教具 录像机,监视器,原子弹和氢弹爆炸的录像剪接带。(若没有上述器材可用原子弹、氢弹爆炸的挂图代替) (三)教学过程 进行新课 原子核的组成 (1)电子的发现和放射性现象的发现 我们已经学过,物质是由分子、原子构成的,原子已经是很小很小的微粒了,其直径只有10-10米,所以在十九世纪以前,人们一直认为原子是不可再分的中性粒子。1897年英国物理学家汤姆生在研究阴极射线时发现了电子,而电子比原子小得多,因而人们才认识到原子内部还有结构。 〈电子的发现把人们带入了原子内部的世界〉 在同一时期人们还发现了天然放射性现象,对放射性现象的进一步研究,人们认识到原子核内部还有结构,原子核由比它更小的粒子组成。可见人类对客观世界的认识是没有止尽的。我们先来学习放射性现象。 〈放射性现象的发现把人们带入了原子核内部的世界〉 (2)放射性现象 ①什么是放射性现象? 像铀(U)、钋(Po)、镭(Ra)等元素能自发地放出一些人眼看不见的、能穿透黑纸使照相底片感光的射线,这种现象叫放射性现象。这些元素叫放射性元素。 ②射线究竟是什么? 在放射性现象中放出的射线是什么东西呢?它们除了能穿透黑纸使照相底片感光的性质以外,还有些什么性质呢?比如:这些射线带不带电呢?为了了解它们的性质,还得通过实验。 我们做什么样的实验,才能判断它们带不带电呢?(放射性现象中放出的射线若是带电的,射线在磁场中将像通电导体那样发生偏转,由偏转的方向和磁体的N、S极位置还可判断射线带的是什么电。) 我们利用已经掌握的知识可以去探索还不知道的现象和规律,最基本的研究方法是通过实验。把放射性元素装在一个壁很厚的铅盒里(射线穿不透),在盒壁上有一个小孔,放射线可由此孔射出,然后把它们放到两个很强的磁极之间,再用照相底片把射线的轨道记录下来。从照相底片上看到,放射线分成了三束,其中两束向相反方向偏转,说明这两束射线带异种电荷;中间一束不偏转,说明它不带电,是中性的。 这三种射线有哪些性质呢?它们的实质是什么呢? 〈射线由两种带异种电荷的粒子和一种不带电的中性粒子组成〉 (3)三种射线 ①α射线 根据射线的偏转方向和磁场方向的关系可以确定,偏转较小的一束由带正电荷的粒子组成,我们把它叫做α射线,α射线由带正电的α粒子组成。科学家们研究发现每个α粒子带的正电荷是电子电荷的2倍,α粒子质量大约等于氦原子的质量。进一步研究表明α粒子就是氦原子核。 〈α射线的实质就是高速运动的氦核流〉 由于α粒子的质量较大,所以α射线的穿透本领最小,我们用一张厚纸就能把它挡住。 ②β射线 与α射线偏转方向相反的那束射线带负电荷,我们把它叫做β射线。研究发现β射线由带负电的粒子(β粒子)组成。进一步研究表明β粒子就是电子。 〈β射线的实质就是高速运动的电子流〉 实验还表明,β射线的穿透本领较强,很容易穿透黑纸,还能穿透几厘米厚的铝板。 化学元素周期表规律 (一)元素周期律和元素周期表 1.元素周期律及其应用 (1)发生周期性变化的性质 原子半径、化合价、金属性和非金属性、气态氢化物的稳定性、最高价氧化物对应水化物的酸性或碱性。 (2)元素周期律的实质 元素性质随着原子序数递增呈现出周期性变化,是元素的原子核外电子排布周期性变化的必然结果。也就是说,原子结构上的周期性变化必然引起元素性质上的周期性变化,充分体现了结构决定性质的规律。 2.比较金属性、非金属性强弱的依据 (1)金属性强弱的依据 1/单质跟水或酸置换出氢的难易程度(或反应的剧烈程度)。反应越易,说明其金属性就越强。 2/最高价氧化物对应水化物的碱性强弱。碱性越强,说明其金属性也就越强,反之则弱。 3/金属间的置换反应。依据氧化还原反应的规律,金属甲能从金属乙的盐溶液中置换出乙,说明甲的金属性比乙强。 4/金属阳离子氧化性的强弱。阳离子的氧化性越强,对应金属的金属性就越弱。 (2)非金属性强弱的依据 1/单质跟氢气化合的难易程度、条件及生成氢化物的稳定性。越易与反应,生成的氢化物也就越稳定,氢化物的还原性也就越弱,说明其非金属性也就越强。 2/最高价氧化物对应水化物酸性的强弱。酸性越强,说明其非金属性越强。 3/非金属单质问的置换反应。非金属甲把非金属乙对应的阴离子从其盐溶液中置换出来,说明甲的非金属性比乙强。 如Br2 + 2KI == 2KBr + I2 4/非金属元素的原子对应阴离子的还原性。还原性越强,元素的非金属性就越弱。 3.常见元素化合价的一些规律 (1)金属元素无负价。金属单质只有还原性。 (2)氟、氧一般无正价。 (3)若元素有最高正价和最低负价,元素的最高正价数等于最外层电子数;元素的最低负价与最高正价的关系为:最高正价+|最低负价|=8。 (4)除某些元素外(如N元素),原子序数为奇数的元素,其化合价也常呈奇数价,原子序数为偶数的元素,其化合价也常呈偶数价,即价奇序奇,价偶序偶。 若元素原子的最外层电子数为奇数,则元素的正常化合价为一系列连续的奇数,若有偶数则为非正常化合价,其氧化物是不成盐氧化物,如NO;若原子最外层电子数为偶数,则 正常化合价为一系列连续的偶数。 4.原子结构、元素性质及元素在周期表中位置的关系1/原子半径越大,最外层电子数越少,失电子越易,还原性越强,金属性越强。 2/原子半径越小,最外层电子数越多,得电子越易,氧化性越强,非金属性越强。 3/在周期表中,左下方元素的金属性大于右上方元素;左下方元素的非金属性小于右上方元素。 专题20 原子结构和原子核 1.(2020届安徽省宣城市高三第二次调研)下面列出的是一些核反应方程式 30 309 4 1214 417 15144267+28P Si+X Be+He C+Y N He O+Z →→→,其中( ) A .X 是质子,Y 是中子,Z 是正电子 B .X 是正电子,Y 是中子,Z 是质子 C .X 是正电子,Y 是质子,Z 是中子 D .X 是中子,Y 是正电子,Z 是质子 【答案】B 【解析】根据核反应的质量数和电荷数守恒可知,X 的质量数为0,电荷数为1,则X 为正电子;Y 的质量数为1,电荷数为0,为中子;Z 的质量数为1, 电荷数为1,为质子。 故选B 。 2.(2020届东北三省四市教研联合体高三模拟)下列关于原子核的叙述中正确的是( ) A .居里夫人通过α粒子轰击铝原子核,首次发现了中子 B .核反应堆中的“慢化剂”是为了减慢反应速度,防止反应过于剧烈 C .轻核聚变过程中,会有质量亏损,要释放能量 D .原子核的质量越大,比结合能就越小 【答案】C 【解析】 A .查德威克在α粒子轰击铍核实验中发现了中子,故A 错误; B .核反应堆中的“慢化剂”是减慢中子速度,故B 错误; C .轻核聚变过程中,会有质量亏损,由爱因斯坦质能方程可知,要释放能量,故C 正确; D .比结合能为结合能与核子数的比值,则原子核的质量越大,比结合能不一定越小,故D 错误。 故选C 。 3.(2020届福建泉州市普通高中高三第一次质量检测)活体生物由于需要呼吸,其体内的14C 含量大致不变,死后停止呼吸,体内的14C 含量开始减少。由于碳元素在自然界的各个同位素的比例一直都很稳定,人们可通过测定古木的14C 含量,来估计它的大概年龄,这种方法称之为碳定年法。14C 衰变为14N 的半衰期约为5730年,某古木样品中14C 的比例约为现代植物所制样品的二分之一。下列说法正确的是( ) A .该古木的年龄约为5730年 B .14 C 与14N 具有相同的中子数 C .14C 衰变为14N 的过程中放出β射线 D .升高古木样品所处环境的温度将加速14C 的衰变 第九章 4 第十九章原子核 新课标要求 1.内容标准 (1)知道原子核的组成。知道放射性和原子核的衰变。会用半衰期描述衰变速度,知道半衰期的统计意义。 (2)了解放射性同位素的应用。知道射线的危害和防护。 例1 了解放射性在医学和农业中的应用。 例2 调查房屋装修材料和首饰材料中具有的放射性,了解相关的国家标准。 (3)知道核力的性质。能简单解释轻核与重核内中子数、质子数具有不同比例的原因。会根据质量数守恒和电荷守恒写出核反应方程。 (4)认识原子核的结合能。知道裂变反应和聚变反应。关注受控聚变反应研究的进展。 (5)知道链式反应的发生条件。了解裂变反应堆的工作原理。了解常用裂变反应堆的类型。知道核电站的工作模式。 (6)通过核能的利用,思考科学技术与社会的关系。 例3 思考核能开发带来的社会问题。 (7)初步了解恒星的演化。初步了解粒子物理学的基础知识。 例4 了解加速器在核物理、粒子物理研究中的作用。 2.活动建议: (1)通过查阅资料,了解常用的射线检测方法。 (2)观看有关核能利用的录像片。 (3)举办有关核能利用的科普讲座。 新课程学习 19.1 原子核的组成 ★新课标要求 (一)知识与技能 1.了解天然放射现象及其规律。 2.知道三种射线的本质,以及如何利用磁场区分它们。 3.知道原子核的组成,知道核子和同位素的概念。 (二)过程与方法 1.通过观察,思考,讨论,初步学会探究的方法。 2.通过对知识的理解,培养自学和归纳能力。(三)情感、态度与价值观 1.树立正确的,严谨的科学研究态度。 2.树立辨证唯物主义的科学观和世界观。 ★教学重点 天然放射现象及其规律,原子核的组成。 ★教学难点 知道三种射线的本质,以及如何利用磁场区分它们。★教学方法 第10章原子结构与元素周期律 思考题 1.量子力学原子模型是如何描述核外电子运动状态的? 解:用四个量子数:主量子数——描述原子轨道的能级; 角量子数——描述原子轨道的形状, 并与主量子数共同决定原子轨道的能级; 磁量子数——描述原子轨道的伸展方向; 自旋量子数——描述电子的自旋方向。 2.区别下列概念:(1)Ψ与∣Ψ∣2,(2)电子云和原子轨道,(3)几率和几率密度。解:(1)Ψ是量子力学中用来描述原子中电子运动状态的波函数,是薛定谔方程的解; ∣Ψ∣2反映了电子在核外空间出现的几率密度。 (2)∣Ψ∣2 在空间分布的形象化描述叫电子云,而原子轨道与波函数Ψ为同义词。 (3)∣Ψ∣2表示原子核外空间某点附近单位体积内电子出现的几率,即称几率密度,而某一微小体积dV内电子出现的几率为∣Ψ∣2·dV。 3.比较波函数角度分布图与电子云角度分布图,它们有哪些不同之处? 解:不同之处为 (1)原子轨道的角度分布一般都有正负号之分,而电子云角度分布图均为正值,因为Y 平方后便无正负号了。 (2)除s轨道的电子云以外,电子云角度分布图比原子轨道的角度分布图要稍“瘦”一些,这是因为︱Y︱≤ 1,除1不变外,其平方后Y2的其他值更小。 4.科顿原子轨道能级图与鲍林近似能级图的主要区别是什么? 解:Pauling近似能级图是按能级高低顺序排列的,把能量相近的能级组成能级组,依1、2、3…能级组的顺序,能量依次增高。按照科顿能级图中各轨道能量高低的顺序来填充电子,所得结果与光谱实验得到的各元素原子中电子排布情况大致相符合。 科顿的原子轨道能级图指出了原子轨道能量与原子序数的关系,定性地表明了原子序数改变时,原子轨道能量的相对变化。从科顿原子轨道能级图中可看出:原子轨道的能量随原子序数的增大而降低,不同原子轨道能量下降的幅度不同,因而产生能级交错现象。但氢原子轨道是简并的,即氢原子轨道的能量只与主量子数n有关,与角量子数l无关。 5.判断题: (1)当原子中电子从高能级跃迁至低能级时,两能级间的能量相差越大,则辐射出的电磁波波长越大。 化学元素周期表的规律总结?比如金属性非金属性等 元素周期表中元素及其化合物的递变性规律 1 原子半径 (1)除第1周期外,其他周期元素(惰性气体元素除外)的原子半径随原子序数的递增而减小; (2)同一族的元素从上到下,随电子层数增多,原子半径增大。 2 元素化合价 (1)除第1周期外,同周期从左到右,元素最高正价由碱金属+1递增到+7,非金属元素负价由碳族-4递增到-1(氟无正价,氧无+6价,除外); (2)同一主族的元素的最高正价、负价均相同 (3) 所有单质都显零价 3 单质的熔点 (1)同一周期元素随原子序数的递增,元素组成的金属单质的熔点递增,非金属单质的熔点递减; (2)同一族元素从上到下,元素组成的金属单质的熔点递减,非金属单质的熔点递增 4 元素的金属性与非金属性 (1)同一周期的元素电子层数相同。因此随着核电荷数的增加,原子越容易得电子,从左到右金属性递减,非金属性递增; (2)同一主族元素最外层电子数相同,因此随着电子层数的增加,原子越容易失电子,从上到下金属性递增,非金属性递减。 5 最高价氧化物和水化物的酸碱性 元素的金属性越强,其最高价氧化物的水化物的碱性越强;元素的非金属性越强,最高价氧化物的水化物的酸性越强。 6 非金属气态氢化物 元素非金属性越强,气态氢化物越稳定。同周期非金属元素的非金属性越强,其气态氢化物水溶液一般酸性越强;同主族非金属元素的非金属性越强,其气态氢化物水溶液的酸性越弱。 7 单质的氧化性、还原性 一般元素的金属性越强,其单质的还原性越强,其氧化物的阳离子氧化性越弱;元素的非金属性越强,其单质的氧化性越强,其简单阴离子的还原性越弱。 一、原子半径 同一周期(稀有气体除外),从左到右,随着原子序数的递增,元素原子的半径递减; 同一族中,从上到下,随着原子序数的递增,元素原子半径递增。 第三讲原子结构与原子核 ——课后自测诊断卷 1.[多选](2019·江苏七市三模)中微子是一种不带电、质量很小的粒子。早在1942年我国物理学家王淦昌首先提出证实中微子存在的实验方案。静止的铍核(74Be)可能从很靠近它的核外电子中俘获一个电子(动能忽略不计)形成一个新核并放出中微子,新核处于激发态,放出γ光子后回到基态。通过测量新核和γ光子的能量,可间接证明中微子的存在。则( ) A.产生的新核是锂核(73Li) B.反应过程吸收能量 C.中微子的动量与处于激发态新核的动量大小相等 D.中微子的动能与处于激发态新核的动能相等 解析:选AC 根据题意可知发生的核反应方程为74Be+0-1e→73Li+νe,所以产生的新核是锂核,反应过程放出能量,故A正确,B错误;根据动量守恒可知中微子的动量与处于激发态新核的动量大小相等,方向相反,故C正确; 因为中微子的动量与处于激发态新核的动量大小相等,质量不等,根据E k=p2 2m ,可知中微子的动能与处于激发态新核 的动能不相等,故D错误。 2.[多选](2019·武汉质检)我国自主研发的钍基熔盐是瞄准未来20~30年后核能产业发展需求的第四代核反应堆,是一种液态燃料堆,使用钍铀核燃料循环,以氧化盐为冷却剂,将天然核燃料和可转化核燃料熔融于高温氯化盐中,携带核燃料在反应堆内部和外部进行循环。钍232不能直接使用,需要俘获一个中子后经过2次β衰变转化成铀233再使用,铀233的一种典型裂变方程是233 92U+10n→142 56Ba+8936Kr+310n。已知铀233的结合能为E1、钡142的结合能为E2、氪89的结合能为E3,则( ) A.铀233比钍232少一个中子 B.铀233、钡142、氪89三个核中氪89的结合能最小,比结合能却最大 C.铀233、钡142、氪89三个核中铀233的结合能最大,比结合能也最大 D.铀233的裂变反应释放的能量为ΔE=E1-E2-E3 解析:选AB 设钍核的电荷数为a,则钍232俘获一个中子后经过2次β衰变转化成铀233,则a=92-2=90,则钍232中含有中子数为232-90=142,铀233含有中子数为233-92=141,则铀233比钍232少一个中子,选项A正确;铀233、钡142、氪89三个核中氪89质量数最小,结合能最小,因核子数较小,则比结合能却最大,选项B 正确,C错误;铀233的裂变反应中释放的能量等于生成物的结合能减去反应物的结合能,选项D错误。 3.[多选](2019·南京、盐城三模)下列对物理知识的理解正确的有( ) A.α射线的穿透能力较弱,用厚纸板就能挡住 B.动能相等的质子和电子,它们的德布罗意波长也相等 C.放射性元素钋的半衰期为138天,100 g的钋经276天,已发生衰变的质量为75 g D.质子、中子、α粒子的质量分别为m1、m2、m3,两个质子和两个中子结合成一个α粒子,释放的能量是(m1+m2-m3)c2 解析:选AC γ射线电离最弱,穿透最强,α射线电离最强,穿透最弱,用厚纸板就能挡住,故A正确;动能相同的质子和电子,它们的动量大小可以用公式p=2m·E k判断,质子与电子的质量不同,所以动能相等的电子与高中化学第1章第2节原子结构与元素周期表第2课时核外电子排布与元素周期表原子半径教案鲁科版选修3
高中物理原子结构、原子核检测题
高中物理第十九章原子核1原子核的组成课后作业含解析新人教版选修3_5
元素周期表中的规律
原子结构与元素周期律知识点
原子结构和原子核
元素周期表的规律总结
人教版高中物理选修3-5学案设计-原子核的组成
原子结构与原子核
高中物理选修3-5教学设计3:19.1 原子核的组成教案
原子结构 原子核外电子排布
物理选修3-5教学案原子核的组成
化学元素周期表规律
2020高考物理一轮复习 专题20原子结构和原子核(解析版)
原子结构和元素周期律(精)
首 页 基本要求
原子结构和元素周期律
重点难点 讲授学时 内容提要
1
基本要求
[TOP]
1.1 了解原子结构的有核模型和 Bohr 模型;电子的波粒二象性、测不准原理;了解了解元素和健康的 关系。 1.2 熟悉原子轨道和概率密度的观念;熟悉原子轨道的角度分布图、径向分布函数图的意义和特征;熟 悉电子组态与元素周期表的关系,有效核电荷、原子半径及电负性变化规律。 1.3 掌握 n、l、m、s 4 个量子数的意义、取值规律及其与电子运动状态的关系;掌握基态原子电子组态 书写的三条原则,正确书写基态原子电子组态和价层电子组态。
2
重点难点
[TOP]
2.1 重点 2.1.1 原子轨道、概率密度的观念;n、l、m、s 4 个量子数;电子组态和价层电子组态。熟悉的意义和 特征;熟悉电子组态与元素周期表的关系,有效核电荷、原子半径及电负性变化规律。 2.1.2 原子轨道的角度分布图和径向分布函数图;了解原子结构的有核模型和 Bohr 模型;了解了解元 素和健康的关系。 2.1.3 电子组态的书写、与元素周期表的关系;元素性质的变化规律。 2.2 难点 2.2.1 电子的波粒二象性、测不准原理;波函数和原子轨道。 2.2.2 原子轨道的角度分布图和径向分布函数图。 2.2.3 熟悉电子组态与元素周期表的关系。
3
讲授学时
[TOP]
建议 4~6 学时
1
内容提要
[TOP]
第一节
第二节
第三节
第四节
第五节
4.1 第一节 氢原子的结构 4.1.1 氢光谱和氢原子的玻尔模型 α 粒子散射实验提供了原子结构的有核模型,但卢瑟福模型没有解决原子核外的空间如何被电子所 占有问题。 量子力学基于两点认识原子结构:一是量子化现象,二是测不准原理。 普朗克提出,热物体吸收或释放能量不连续,称量子化的。 氢原子的线状光谱也表现了原子辐射能量的量子化。 玻尔假定: 电子沿着固定轨道绕核旋转; 当电子在这些轨道上跃迁时就吸收或辐射一定能量的光子。 轨道能量为
E??
4.1.2 电子的波粒二象性
RH , n=1,2,3,4,… n2
波粒二象性是指物质既有波动性又有粒子性的特性。光子的波粒二象性关系式 λ=h/mc= h/p 德布罗意的微观粒子波粒二象性关系式
??
h h ? p mv
微观粒子的波动性和粒子性通过普朗克常量 h 联系和统一起来。 微观粒子的波动性被电子衍射实验证实。电子束的衍射现象必须用统计性来理解。衍射中电子穿越 晶体投射到照相底片上, 图像上亮斑强度大的地方电子出现的概率大; 电子出现少的地方亮斑强度就弱。 所以,电子波是概率波,反映电子在空间某区域出现的概率。 4.1.3 测不准原理 海森堡指出,无法同时确定微观粒子的位置和动量,它的位置越准确,动量(或速度)就越不准确; 反之,它的动量越准确,位置就越不准确: △x· △px≥h/4π 式中△x 为坐标上粒子在 x 方向的位置误差,△px 为动量在 x 方向的误差。 测不准原理表明微观粒子不存在确定的运动轨迹,可以用量子力学来描述它在空间出现的概率及其 它全部特征。
2物理:新人教版选修3-5 19.1原子核的组成(教案)(2篇)
原子结构与元素周期律(精)
化学元素周期表的规律总结
(江苏专用)2020高考物理复习专题五动量与原子物理学第三讲原子结构与原子核——课后自测诊断卷【带答案】