
第13章氢和稀有气体
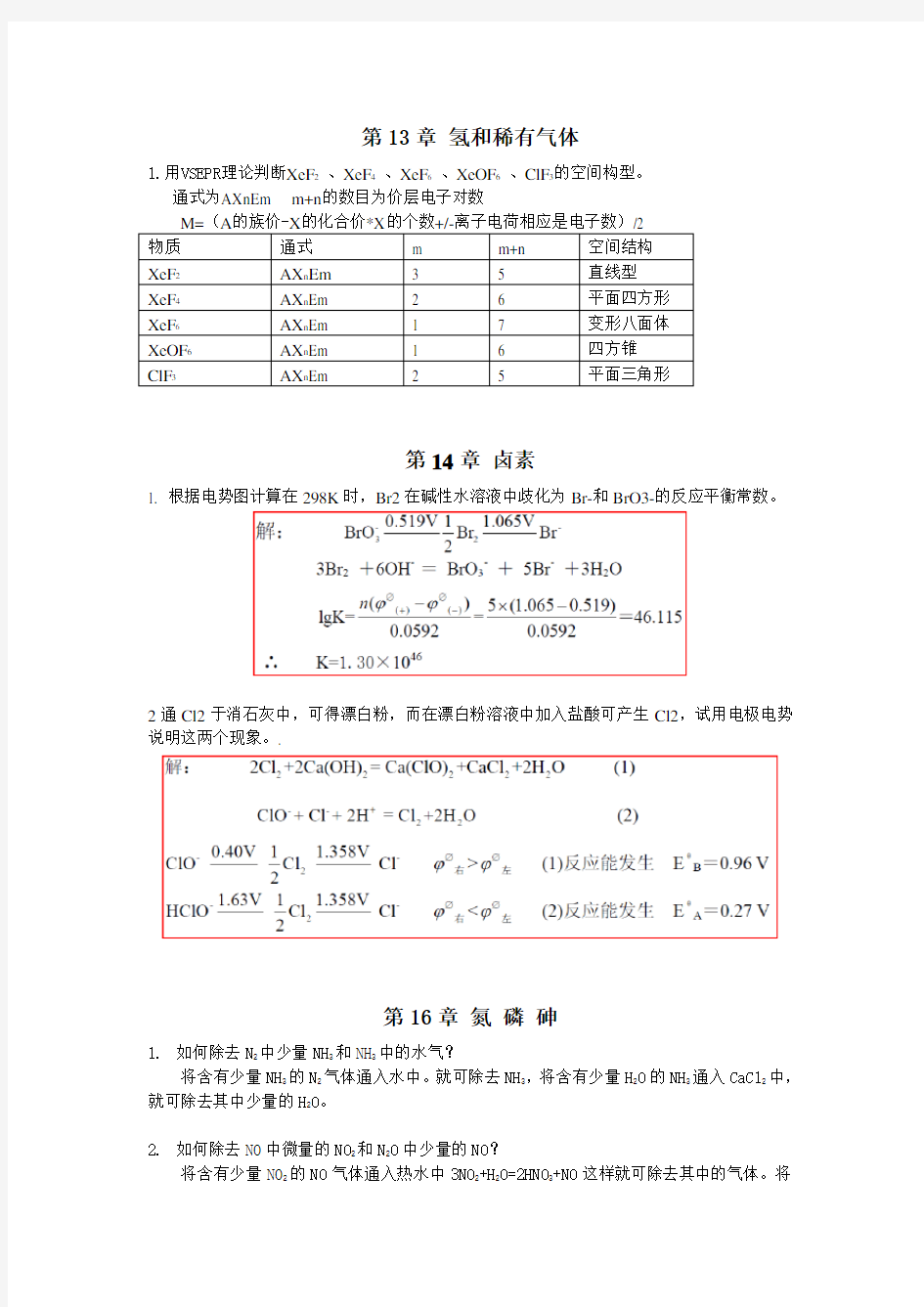
1.用VSEPR理论判断XeF2、XeF4、XeF6、XeOF6、ClF3的空间构型。
通式为AXnEm m+n的数目为价层电子对数
M=(A的族价-X的化合价*X的个数+/-离子电荷相应是电子数)/2
第14章卤素
1. 根据电势图计算在298K时,Br2在碱性水溶液中歧化为Br-和BrO3-的反应平衡常数。
2通Cl2于消石灰中,可得漂白粉,而在漂白粉溶液中加入盐酸可产生Cl2,试用电极电势说明这两个现象。.
第16章氮磷砷
1.如何除去N2中少量NH3和NH3中的水气?
将含有少量NH3的N2气体通入水中。就可除去NH3,将含有少量H2O的NH3通入CaCl2中,就可除去其中少量的H2O。
2.如何除去NO中微量的NO2和N2O中少量的NO?
将含有少量NO2的NO气体通入热水中3NO2+H2O=2HNO3+NO这样就可除去其中的气体。将
N2O和少量的NO气体通入水中。就可除去其中少量的NO。
3.给下列物质按碱性减弱顺序排序,并给予解释:
NH3 N2H4 NH3OH PH3 AsH3
答:NH3是所有气态氢化物中唯一显碱性的物质,按N—P—AS 顺序,其气态氢化物的碱性依次减弱,酸性依次增强,故碱性NH3>PH3>ASH3,而同一种元素的氢化物,化合价越低,碱性越强,故NH3>N2H4>NH2OH ,综上可知碱性顺序为NH3>N2H4>NH3OH(碱性)>PH3(酸性)>AsH3 (酸性)
4.为了测定铵态氮肥中的含氮量,称取固体样品0.2471g,加过量NaOH溶液并进行蒸馏,用50.00mL 0.01050mol/L HCl吸收蒸出的氨气,然后用0.1022mol/L NaOH溶液滴定吸收液中剩余的HCl,滴定中消耗了11.69mL NaOH溶液,试计算肥料中氮的百分含量。
解: HCl与NH3按1:1反应生成NH4Cl,未反应的HCl的物质的量
n(HCL)=0.05000×0.1050-0.01169×0.1022mol=0.00406mol
即氮肥中的N 元素的物质的量
n(N )=0.00406mol
故N﹪= n(N ) ×14/0.2471×100﹪=0.00406×14/0.2471×100﹪=22.976﹪
5. 红磷长时间放置在空气中逐渐潮解,与NaOH、Ca Cl2在空气中潮解,实质上有什么不同?潮解的红磷为什么可以用水洗涤来进行处理?
答:红磷长时点放置在空气中逐渐潮解是因为它与空气中的O2形成吸水氧化物吸水而潮解,NaOH, CaCl2空气中逐渐潮解是因为它们直接吸收了空气中的水份而潮解.
第17章碳硅硼
1.将含有Na2CO3和NaHCO3的固体混合物60.0g溶于少量水后稀释到
2.00L,测得该溶液的pH 为10.6,试计算原来的混合物中含Na2CO3及NaHCO3各多少克?
2.如何鉴别下列物质:
(1)Na2CO3、Na2SiO3、Na2B4O7·10H2O
(2)NaHCO3、Na2CO3
(3)CH4、SiH4
4.把1.5gH3BO3溶于100mL水中,所得溶液的pH是多少?
5把足量Na2CO3加入75吨纯的硬硼钙石中,假定转化率为85%,问所得硼砂的质量是多少?
第18章非金属元素
1.非金属元素在原子结构和氧化态表现上有何特征?
电负性大,价电子多
半径小,易获得电子
显负价,为N-8,N为族数
2.非金属单质有几种结构类型?
分子晶体或原子晶体——共价特征。
单原子分子构成的单质(稀有气体);
双原子分子构成的单质(卤素、O2、N2);
多原子分子构成的单质(硫、磷等);
巨型大分子(原子晶体)构成的单质(碳、硅等)。
3.非金属单质在形成化合物时有哪些主要性质?
易形成单或多原子阴离子(S2-、Sx2-);
氧化物多为酸性,易与碱形成含氧酸盐
单质不易与水(F2除外)、稀酸作用,可与氧化性酸及碱作用。
4.影响无氧酸强度的主要因素有哪些?为什么酸性:HF 影响因素:键能和电子亲合能。 即与H直接相连的非金属元素原子的电子云密度,若该原子的电子云密度越大,对质子的吸引力越强,酸性越小,反之则酸性越大。因为电子亲合能F>OH- ,所以酸性H2O 因为键能为HF>HCl>HBr>HI,所以酸性: HF 5.已知下列数据: Δf Gοm (H2S,aq)=-27.9kJ/mol Δf Gοm (S2-,aq)=85.8kJ/mol Δf Gοm (H2Se,aq)=22.2kJ/mol Δf Gοm (Se2-,aq)=129.3kJ/mol 试计算下列反应的Δr Gοm和平衡常数K: (1)H2S(aq)→2H+(aq)+S2-(aq) (2)H2Se(aq)→2H+(aq)+Se2-(aq) 两者中哪一个酸性较强? 5.试解释下列各组酸强度的变化顺序: (1)HI>HBr>HCl>HF (2)HClO4>H2SO4>H3PO4>H4SiO4 (3)HNO3>HNO2 (4)HIO4>H5IO6 (5)H2SeO4>H2TeO6 7. 第19章金属通论 1.金属元素在自然界中有哪几种主要存在形式? 少数贵金属以单质或硫化物。(如Au、Ag、Hg、铂系) 轻金属:氧化物和含氧酸盐。(如以CO32-、PO43-、 SO42-) 重金属:氧化物、硫化物、SiO32-、CO32- 第20章 s区金属 1.碱金属元素在形成化合物时有哪些主要特征? ns1 结构,周期表中最左侧的一族元素。半径大,电负性小,是周期表中最活泼的金属元素。以失去电子,以形成M+离子型化合物为主要特征。 从Li到Cs活泼性增大。 2.碱土金属和碱金属元素比,在性质变化上有何规律? Li、Be有哪些特殊性? ns2结构,与碱金属比,金属键增强,硬度增大,熔点高,金属活泼性降低,但仍是活泼金属,活泼性仅次于碱金属。以形成M2+的离子型化合物为主要特征。 Li、Be的特殊性: ① ?Li+ /Li特别的负,这与Li+的水合能特别大有关。 ② LiOH、Be(OH)2溶解度小。 ③化合物共价性强。 3.碱金属和碱土金属的氢化物有何特征? 离子型氢化物,都是强还原剂。 两个基本特征: ①大多数氢化物不稳定,加热分解放出氢气,可作储氢材料 ②与水作用氢气,可作为野外产生氢气的原料。 4..何谓焰色反应?焰色反应有何用途? 碱金属和碱土金属中钙、锶、钡的挥发性化合物在高温火焰中电子易被激发而呈现特殊的颜色,这就是焰色反应 用途 ①根据火焰的颜色定性的鉴别碱金属和碱土金属中钙、锶、钡这些元素的存在与否 ②制造各种焰火 5.碱金属和碱土金属在形成配合物的性质上有何特征? 碱金属离子接受电子对的能力较差,一般难形成配合物,只能形成少量螯合物。 碱土金属离子的电荷密度较高,具有比碱金属离子强的接受电子的能力 6. 利用铍、镁化合物性质的不同鉴别下列各组物质. (1) Be(OH)2和Mg(OH)2 解: 加入过量的强碱, 能够溶解的是Be(OH)2, 不溶的是Mg(OH)2 Be(OH)2 + 2OH-〔Be(OH)42-〕 (2) BeCO3和MgCO3 解: 加入(NH4)2CO3, BeCO3生成可溶性络盐(NH4)6〔Be4O(CO3)6〕],MgCO3不发生反应;或者加热分解,BeCO3在低于100度时就开始分解,而MgCO3在540度时才开始分解。 (3)BeF2和MgF2 解:加入水,BeF2易溶与水,MgF2水解生成Mg(OH)2沉淀;或者加入HF,BeF2生成络离子BeF42-,而MgF2不易生成络离子。 BeF2 + 2HF === H2〔BeF4〕 第21章 p区金属 1.P区金属在在氧化态表现和变化规律上有何特征? 由于ns、np电子可同时成键,也可仅由np电子参与成键,因此它们在化合物中常有两种氧化态,且其氧化值相差为2。 2.Al2Cl6与B2H6的结构有何相似与不同?为什么?为什么AlF3不二聚? 相同点:中心原子均为sp3杂化,均为桥式结构。 不同点: B2H6 中的氢桥键为3c-2e Al2Cl6 中的氯桥键为3c-4e B、Al半径不同;H、Cl的结构不同。 AlF3为离子型化合物。 3.锗分族元素在氧化态表现上有何特征?在形成化合物时与C、Si有何不同?锗分族+Ⅱ和+Ⅳ氧化态化合物的氧化还原性变化有何规律? 氧化态从Ge到Pb低氧化态趋于稳定。 C、Si以形成共价型化合物为主要特征。 Ge、Sn、Pb离子性增强,有低价的盐如Sn2+、 Pb2+。 锗族元素自相成链能力差,除Ge外,Sn、Pb无类似于C、Si的氢化物。 4.锑和铋在自然界主要以何种物质存在?与氮、磷比有什么不同? 辉锑矿(Sb2S3)和辉铋矿(Bi2S3)是锑和铋在自然界中的主要存在形式。Sb、Bi为亲硫元素。 氮主要以单质存在;磷以含氧酸盐存在。 5.已知Al2O3和Fe2O3的标准生成热分别为-1670kJ/mol和-822kJ/mol,计算Al与Fe2O3反应的反应热,由计算结果说明了什么? 第22章 ds区金属 1. 电解法精练铜的过程中,粗铜(阳极)中的铜溶解,纯铜在阴极上沉积出来,但粗铜中的Ag、Au、Pt 等杂质则不溶解而沉于电解槽底部形成阳极泥,Ni、Fe、Zn等杂质与铜一起溶解,但并不在阴极上沉积起来,为什么? 答:Ni、Fe、Zn 的还原性比铜强,所以铜离子的氧化性强于锌离子等,故铜在阴极上沉积出来,而其他离子不能。 2.为什么Cu2+不稳定,易歧化,而Hg2+则较稳定。试用电极电势的数据和化学平衡的观点加以阐; 答:Cu的电极电势图为:Cu2+——Cu+(+0.158V)——Cu(+0.522V)所以可发生歧化反应。Hg的为Hg2+——Hg2+(0.905V)——Hg(0.7986V),不可歧化 3. (1)用一种方法区别锌盐和铝盐: 答:分别向两种盐的溶液中加入过量氨水,生成沉淀而后溶解的是锌盐,只得到白色沉淀的为铝盐 (2)用两种方法区别锌盐和镉盐; 答:a 分别向两种盐的溶液中加入适量碱,均生成沉淀继续加碱,溶解的是锌盐,不溶的为镉盐b 分别向两种盐的溶液中通入硫化氢气体,生成沉淀的是锌盐,得到黄色沉淀的为镉盐 (3)用三种方法区别镁盐和锌盐。 答:A 向两种盐的溶液中加入过量的碱,先出现白色沉淀而后溶解的是锌盐,而得到白色沉淀的是镁盐;b 分别向两种盐的溶液中加入硫化氢气体,得到白色沉淀的是锌盐,无变化的是镁盐c 分别向两种盐的溶液中加入过量氨水,先得到白色沉淀又溶解的为锌盐,只有白色沉淀的为镁盐。 第23章 d区金属(一) 1.为什么第一过渡金属中锰和铜的熔点相对较低? Mn的价电子构型:3d54s2 Cu的价电子构型:3d104s1 3d轨道为半充满和全充满的稳定构型,参与形成金属键的能力弱,因而熔点较低。 2.Cr(Ⅲ)的氧化物和氢氧化物分别为什么颜色?有何主要性质?Cr(Ⅲ)和 Al(Ⅲ)有何相似和不同? Cr(OH)3:灰蓝色。 Cr2O3:绿色。 Cr(OH)3、 Cr2O3主要性质: (1) 微溶性。(2) 两性。(3) 还原性。 Cr(Ⅲ)和 Al(Ⅲ)有何相似和不同: 相似: M2O3、M(OH)3均为两性; M(OH)3均为胶状沉淀。 不同: M2O3、M(OH)3颜色不同; [M(H2O)6]3+颜色不同;形成配合物的能力不同。Al3+不形成氨配合物; Cr(Ⅲ)有还原性, Al(Ⅲ)没有。 3.什么是羰基化合物?为什么中性的金属原子可以和中性的CO分子形成较稳定的化合物? 铁钴镍都可与CO形成低价的羰基化合物,这类化合物具有挥发性,用于提纯金属。羰基配合物组成特点:单核羰基配合物中,金属原子的价电子数和CO提供的配位电子数总和等于18,为反磁性物质。如:Fe(CO)5 Cr(CO)6 Mo(CO)6 Ni(CO)4 4. 在含有Cl-离子和CrO42-离子(它们的浓度均为1.0*10-3mol/L)的混合溶液中逐滴加入 AgNO3溶液,问何种物质先沉淀,两者能否分开? 解:沉淀类型不同 KθSP(AgCl)=1.8×10-10 KθSP(Ag2CrO4)=2.0*10-12 开始生成AgCl沉淀时所需Ag+的浓度为: [Ag+]= KθSP(AgCl)/[ Cl-] = 1.8×10-10/1.0×10-3=1.8×10-7( mol/L)开始生成Ag2CrO4沉淀时所需Ag+的浓度为: [Ag+]=K ] /[CrO AgCrO Ksp) ( =10 * 0.1/ 10 * 0.2=4.47×10-4( mol/L) 可见,生成AgCl沉淀时所需Ag+的浓度小,因此Cl-先于Ag+生成沉淀 当开始生成Ag2CrO4沉淀时,所需的Cl-浓度为: [ Cl-]= KθSP(AgCl) ÷ [Ag+]=1.8×10-10÷4.47×10-4=4.0×10-7( mol/L)即[ Cl-]>1.0×10-5( mol/L) CrO42-开始沉淀时,Cl-已沉淀完全,因此两者能用AgNO3溶液分开。 5. 75 mL 2 mol/L的硝酸银溶液恰使溶20g有六水合氯化铬(Ⅲ)中的氯完全生成AgCl沉 淀,请根据此数据写出六水合氯化铬的化学式。 解:n(Ag+)=2×75×10-3=0.15 mol n(CrCl3·6H2O)=20/266.5=0.075 mol 根据题意:沉淀的氯的个数=0.15/0.075=2 因此六水合氯化铬的化学式为:[Cr(H2O)5Cl] Cl2·H2O(蓝绿色) 6. 有一钴的配合物,其中各组分的含量分别为Co:23.16% H:4.17% N:33.01% O:25.15% Cl:13.95%。如将配合物加热则失去氨,失重为该配合物质量的26.72%。试求:该配合物有几个氨分子,以及该配合物的最简式。 解:此配合物的原子数为: Co:H:N:O:Cl=23.16/58.94:4.71/1:33.01/14:25.15/16:13.95/35.5=1:12:5:4:1 式量为=58.94+12+14×5+16×4+35.5=240.44 W(NH3)=26.72%×240.44=64.25 即化学式中氨的分子数为:64.25/17≈4 因此配合物的化学式为: 7.顺磁性:(1)[Cu(NH3)4]SO4·H2O (3)K3[Fe(CN)6] 反磁性:(2)K4[Fe(CN)6]·3H2O (4)[Co(NH3)6]Cl (5)Ni(CO)4 第24章 d区金属(二) 1.一纯的铂化物,经测定相对分子质量为301,化合物中含Pt 64.8%,Cl 23.6%,NH35.6%,H2O 6.0%: (1)指出此化合物的分子式 ∵ n Pt=1 n Cl=2 n NH3=1 n H2O=1 ∴分子式为[Pt(NH3)H2O·Cl]Cl (2)画出可能的结构 (3)讨论各种结构的相对稳定性(略) 第25章 f区金属—镧系与锕系金属 1.什么是镧系收缩?镧系收缩带来哪些结果? 镧系元素的原子半径和离子半径随着原子序数的增加而逐渐减小的现象称为镧系收缩。 主族:原子序数每增加一,半径平均减少10Pm 副族:原子序数每增加一,半径平均减少10Pm f区:原子序数每增加一,半径平均减少1Pm 2.从镧系元素的电极电势数据可对镧系金属的活泼性得出什么结论? (1)由镧系元素标准电极电势可知,镧系元素金属的活泼性仅次于碱金属和碱土金属。(??<-2V) (2) ??相近,活泼性相似。 (3) 由La到Lu递减,即La最活泼。 3.镧系金属的水合离子为何有颜色?其水合离子的颜色为什么呈现出规律性? 离子的颜色与未成对电子数有关,4f亚层未充满的镧系金属离子,颜色主要是 4f亚层中的电子跃迁引起的,发生这种f-f 跃迁需要吸收一定的波长. 第十七章卤素 总体目标: 1.掌握卤素单质、氢化物、含氧酸及其盐的结构、性质、制备和用途 2.掌握卤素及其化合无各氧化态间的关系 各节目标: 第一节卤素单质 1.了解卤素单质的物理性质,如:颜色、状态、熔点、沸点、溶解性等等 2.掌握卤素单质的化学性质,包括与水作用、与金属的反应、与非金属反应、与氢气的反应及其递变规律;了解卤素单质的用途 3.运用元素电势图来判断卤素及其化合物的氧化—还原性 第二节卤化氢和氢卤酸 掌握卤化氢的酸性、还原性、热稳定性及其变化规律;卤化氢的制备方法 第三节卤化物、卤素互化物和拟卤素 了解卤化物的分类;金属卤化物、卤素互化物和拟卤素的主要性质和制备 第四节卤素的含氧化合物 了解卤素含氧酸及其盐酸性、氧化性强度及变化规律 Ⅱ习题 一选择题 1.某元素的电势图为:E A ?M4+-0.15M2+-0.14M,下列说法中正确的是() A. M2+不能发生歧化反应 B. M2+是强氧化剂 C. M是强还原剂 D. M4+与M 反应生成M2+ 2.碘的电子结构式是[Kr]5S25P5 ,指出下列哪种化学式的化合物不能存在() A.IF 5 B.IF 7 C.Na 3 H 2 IO 6 D.HIF 3.下列关于(CN) 2 的反应中,不象卤素单质反应的是() A.(CN) 2 +H 2 O==HCN+HCNO B.可在空气中燃烧 C.与银、汞、铅反应得难溶盐 D.与卤素反应生成CNCl、CNBr等 4.下列叙述正确的是() A.无论在酸性还是在碱性介质中,卤素电对X 2 |Xˉ不变 B.由于卤素阴离子(Xˉ)具有还原性,所以能用电解卤化物水溶液的方法制备卤素单质 C. 卤素阴离子可以作为路易斯碱而构成配合物的内界 D.氟的电负性最大,所以F 2 分子中的共价键是所有共价键中最强的 5.在含Iˉ的溶液中通入Cl 2 ,产物可能是() A.I 2和Clˉ B.ClO 3 和Clˉ C.ICl 2 ˉ D.以上产物均有可能 6.将氟气通入水中,生成的产物可能有() A.O 2、O 3 和HF B.OF 2 和HF C.H 2 O 2 和HF D.以上诸种 7.冷的氯水中微粒的种类有() A.5种 B.6种 C.7种 D.8种 8.卤素互化物一般由较重卤素和较轻卤素构成,在卤素互化物分子中,较轻卤素原子个数一般为() A.1 B.2 C.1、3、5、7(奇数) D.2、4、6(偶数) 9.下列物质受热产生Cl 2 的是() A.Cl 3O 5 B.ClO 2 C.Cl 2 O 2 D.Cl 2 O 10.关于SnCl 2和SnCl 4 的熔沸点高低,正确的是() A.SnCl 2高于SnCl 4 B. SnCl 2 低于SnCl 4 C.两者差不多一样高 D.外界条件不同,熔、沸点高低不同 11.制备F 2 实际所采用的方法是() A.电解HF B.电解CaF 2 C.电解KHF 2 D.电解NH 4 F 12.实验室制备Cl 2 最常用的方法是() A.KMnO 4与浓盐酸共热 B.MnO 2 与稀盐酸反应 C.MnO 2与浓盐酸共热 D. KMnO 4 与稀盐酸反应 13.实验室制得的氯气含有HCl和水蒸气,欲通过二个洗气瓶净化,下列洗气瓶中试剂选择及顺序正确的是() A.NaOH,浓H 2SO 4 B.CaCl 2 ,浓H 2 SO 4 C.H 2O,浓H 2 SO 4 D. 浓H 2 SO 4 ,H 2 O 14.下列各对试剂混合后能产生氯气的是() A.NaCl与浓H 2SO 4 B.NaCl与MnO 2 目录绪论第一篇物质结构基础第1章原子结构与元素周期系1-1 道尔顿原子论1-2 相对原子质量(原子量)1-2-1 元素、原子序数和元素符号1-2-2 核素、同位素和同位素丰度1-2-3 原子的质量1-2-4 元素的相对原子质量(原子量)1-3 原子的起源和演化1-4 原子结构的玻尔行星模型1-4-1 氢原子光谱1-4-2 玻尔理论1-5 氢原子结构(核外电子运动)的量子力学模型1-5-1 波粒二象性1-5-2 德布罗意关系式1-5-3 海森堡不确定原理1-5-4 氢原子的量子力学模型1-6 基态原子电子组态(电子排布)1-6-1 构造原理1-6-2 基态原予电子组态1-7 元素周期系1-7-1 元素周期律、元素周期系及元素周期表1-7-2 元素周期表1-8 元素周期性1-8-1 原子半径1-8-2 电离能1-8-3 电子亲和能1-8-4 电负性1-8-5 氧化态习题第2章分子结构2-1 路易斯结构式2-2 单键、双键和叁键——σ键和π键——价键理论(一)2-3 价层电子互斥模型(VSEPR)2-4 杂化轨道理论--价键理论(二)2-4-1 杂化轨道理论要点2-4-2 sp3杂化2-4-3 sp2杂化2-4-4 sp杂化2-5 共轭大π键2-6 等电子体原理2-7 分子轨道理论2-8 共价分子的性质2-8-1 键长2-8-2 共价半径2-8-3 键能2-8-4 键角2-8-5 键的极性与分子的极性2-9 分子间力2-9-1 范德华力2-9-2 氢键2-9-3 分子间作用力的其他类型2-9-4 范德华半径2-10 分子对称性(选学材料)2-10-1 对称性2-10-2 对称操作与对称元素2-10-3 分子的对称类型2-10-4 分子的性质与对称性的关系习题第3章晶体结构3-1 晶体3-1-1 晶体的宏观特征3-1-2 晶体的微观特征--平移对称性3-2 晶胞3-2-1 晶胞的基本特征3-2-2 布拉维系3-2-3 晶胞中原子的坐标与计数3-2-4 素晶胞与复晶胞-体心晶胞、面心晶胞和底心晶胞3-2-5 14种布拉维点阵型式……第4章配合物第二篇化学热力学与化学动力学基础第5章化学热力学基础第6章化学平衡常数第7章化学动力学基础第三篇水溶液化学原理第8章水溶液第9章酸碱平衡第10章沉淀平衡第11章电化学基础第12章配位平衡习题答案(选)附表元素周期表无机化学(第四版)(下册)——面向21世纪课程教材作者:北京师范大学、华中师范大学南京师范大学无机化学教研室编出版社:高等教育出版社日期:2003-1-1开本:16 版次:2010年5月第18次印刷页数:556页装帧:平装ISBN:9787040115833定价:47.50元内容简介本书分上下两册出版。上册分三篇:物质结构、化学热力学、水溶液化学原理;介绍了原子结构与周期律,分子结构,晶体化学,配合物,热力学函数,化学平衡,化学动力学基础,酸碱、沉淀、氧化还原、配合四大平衡等化学原理内容。编者认为,化学原理应该成为大一学生学习其他化学课程的基础,不能跟中学课程或后续课程在同一层次上重复,力争使第四版教材具有推陈出新、层次分明、重点突出、留有余地、易教好学、适用面宽等特点。下册含4、5、6篇非金属元素化学、金属元素化学和无机化学选论。本版书大大加强了元素化学的实用性知识,并增加了部分研究性习题,激发学生学习元素化学的兴趣。目录第四篇元素化学(一)非金篇第13章氢和稀有气体13.1 氢13.2 稀有气习题第14章卤素14.1 卤素的通性14.2 卤素单质14.3 氟氯溴碘的化合物14.4 砹的化学习题第15章氧族元素15.1 氧族元素的通性15.2 氧及其化合物15.3 硫及其化合物15.4 硒和碲习题第16章氮磷砷16.1 元素的基本性质16.2 氮和氮的化合物16.3 磷及其化合物16.4 砷习题第17章碳硅硼17.1 透性17.2 碳17.3 硅17.4 硼17.5 碳化物、硅化物和硼化物习题第18章非金属元素小结第五篇元素化学(二)金属第19章金属通论第20章S区金属(碱金属和碱土金属)第21章P区金属第22章ds区金属第23章d区金属(一)第四周期d金属第24章d区金属(二)第五、第六周期d区金属第25章f区金属镧系与锏系金第六篇无机化学选论第26章无机合成化学简介第27章特殊类型的无机化合物第28章生物无机化学简介第29章无机固体化学简介第30章核化学习题答案人名索引主题词索引后记 北京化工大学 Model of Final Examination of 《Inorganic Chemistry》 (bi-lingual course) C H M 2 1 7 0 T Course code 课程代码 Class No.: Name and ID: Items (题号) 一二三四五六Total score(总分) Score(得分) 一、是非题:(判断下列叙述是否正确,正确的在括号中画√,错误的画×。不必 写在答题纸上。)(本大题共10小题,每题1分,共10分) ( )1.在一定温度条件下,化学反应的恒压反应热只与系统的始态和终态有 关,因此化学反应热是状态函数。 ( )2.按照金属键理论,金属能导电传热是因为存在导带,而金属镁中只有 满带和空带,所以金属镁晶体不能导电。 ( )3.对一个化学反应,其速率常数总是随温度的升高而增大,因此增加反 应温度总有利于反应的正向进行。 ( )4.任何反应都是由元反应或由元反应复合而成的,只要了解了化学反应 的反应机理,由反应机理可得出其总的反应速率方程式。 ( )5.通常情况下,一个过程的自发进行方向在反应机理不发生变化的情况 下,高温时由熵变决定,低温下由焓变决定。 ( )6.当一个原子得到电子时,半径增大,极化力变小,极化率增大。 ( )7.电子亲和能是指一个原子得到电子后放出的能量,由于原子核在外层 有正电场存在,对电子有吸引能力,因此电子亲和能一定小于零。 ( )8.凡中心原子以sp3形式杂化的分子,其空间构型都是正四面体。 8 ( )9.经实验测定,配合物K[Fe(CN)]的磁距为2.41,接近于 36 =2.83。因此此配合物中未成对电子数为2。 ( )10.因CaF的溶度积常数比CaCO的溶度积常数小,因此CaF 232 的溶解度一 定比CaCO的溶解度小。 3 二、选择题:(在下列各题中,选择出符合题意的答案,将其代号填入括号内。)(本大题共20题,每题1.5分,共30分) ( )1.已知 298 K时,Sn(s) + Cl 2(g)→SnCl2(s)的△r H(1) = -349.8 kJ·mol-1,SnCl 2(s) + Cl2(g) →SnCl4 (l) 的 △r H(2) = -195.4 kJ·mol-1, 则1 2Sn(s) + Cl2(g)→1 2 (g) 的△r H SnCl为: 4 A.-545.2 kJ·mol-1;B.-272.6 kJ·mol-1; C.154.4 kJ·mol-1-1 ;D.-154.4 kJ·mol。 ( )2.下列叙述中错误的是。 A.配位平衡是指溶液中配离子解离为中心离子和配体的解离平衡; B.配离子在溶液中的行为像弱电解质; C.对同一配离子而言K·K = 1; D.配位平衡是指配合物在溶液中解离为内界和外界的解离平衡。 ( )3.将10.7g NH Cl溶解于1L 0.1mol·L-1 NH·H 432 O中,该溶液的pH值为多少?K b(NH3·H2O)=1.8×10-5。 A.9.26; B.8.96; C.9.56; D.11.13。 ,最适合溶解CuS的溶液是: ( )4.CuS的K sp(CuS)=4×10-36 A.HNO;B.浓HCl;C.稀HCl;D.HAc。 3 ( )5.在下列过渡元素的氯化物水溶液中,那一种溶液的颜色最浅。 A.CuCl2;B.CoCl; C.MnCl;D.NiCl。 222( )6.在酸性溶液中,下列各组离子能在水溶液中稳定共存的是那一组2+2- A.Ba、Cr2O7;B.Mn2+3+ 、Cr; C.S2-3+2+ 、Fe;D.Sn、Fe3+。 大学无机化学第六章试 题及答案 Document serial number【NL89WT-NY98YT-NC8CB-NNUUT-NUT108】 第六章化学键理论 本章总目标: 1:掌握离子键、共价键和金属键的基本特征以及它们的区别; 2:了解物质的性质与分子结构和键参数的关系; 3:重点掌握路易斯理论、价电子对互斥理论、杂化轨道理论以及分子轨道理论。 4:熟悉几种分子间作用力。 各小节目标: 第一节:离子键理论 1:掌握离子键的形成、性质和强度,学会从离子的电荷、电子构型和半径三个方面案例讨论离子的特征。 2:了解离子晶体的特征及几种简单离子晶体的晶体结构,初步学习从离子的电荷、电子构象和半径三个方面来分析离子晶体的空间构型。 第二节:共价键理论 1;掌握路易斯理论。 2:理解共价键的形成和本质。掌握价键理论的三个基本要点和共价键的类型。3:理解并掌握价层电子对互斥理论要点并学会用此理论来判断共价分子的结构,并会用杂化轨道理论和分子轨道理论来解释分子的构型。 第三节:金属键理论 了解金属键的能带理论和三种常见的金属晶格。 第四节:分子间作用力 1:了解分子极性的判断和分子间作用力(范德华力)以及氢键这种次级键的形成原因。 2;初步掌握离子极化作用及其强度影响因素以及此作用对化合物结构及性质的影响。 习题 一选择题 1.下列化合物含有极性共价键的是()(《无机化学例题与习题》吉大版) 2 C. Na 2 O 2.下列分子或离子中键能最大的是() A. O 2 C. O 2 2+ D. O 2 2- 3. 下列化合物共价性最强的是()(《无机化学例题与习题》吉大版) C. BeI 2 4.极化能力最强的离子应具有的特性是() A.离子电荷高,离子半径大 B.离子电荷高,离子半径小 C.离子电荷低,离子半径小 D.离子电荷低,离子半径大 5. 下列化合物中,键的极性最弱的是()(《无机化学例题与习题》吉大版) 3 C. SiCl 4 6.对下列各组稳定性大小判断正确的是() +>O 22- B. O 2 ->O 2 C. NO+>NO D. OF->OF 7. 下列化合物中,含有非极性共价键的离子化合物是()(《无机化学例题与习题》吉大版) 3 C. Na 2 O 2 8.下列各对物质中,是等电子体的为() 和O 3 B. C和B+ C. He和Li D. N 2 和CO 9. 中心原子采取sp2杂化的分子是()(《无机化学例题与习题》吉大版) 3 C. PCl 3 10.下列分子中含有两个不同键长的是() A .CO 2 3 C. SF 4 11. 下列分子或离子中,不含有孤电子对的是()(《无机化学例题与习题》吉大版) A. H 2O B. H 3 O+ C. NH 3 D. NH 4 + 12.氨比甲烷易溶于水,其原因是() A.相对分子质量的差别 B.密度的差别 C. 氢键 D.熔点的差别 13. 下列分子属于极性分子的是()(《无机化学例题与习题》吉大版) A. CCl 43 C. BCl 3 D. PCl 5 14.下列哪一种物质只需克服色散力就能使之沸腾( ) 15. 下列分子中,中心原子采取等性杂化的是()(《无机化学例题与习题》吉大版) 《无机化学上》试题(三) 一、选择题(每小题1分,共20分) 1.下列哪种溶液可做缓冲溶液 (A). HAc+HCl(少量) (B). HAc+NaOH(适量) (C). HAc+NaCl(少量) (D). HAc+KCl(少量) 2.下列各分子中,中心原子在成键时以sp3不等性杂化的是 (A). BeCl2 (B). PH3 (C). BF3 (D). SiCl4 3.第二周期从Li到Ne原子的电离势总变化趋势是 (A). 从小变大 (B). 从大变小 (C). 从Li到N增加,从N到Ne下降 (D). 没有多大变化 4.含有П46离域大п键的是 (A). ClO3-; (B). SO32-; (C). SO3; (D). SOCl2 5.下列化合物中哪种分子偶极矩为零 (A). H2O; (B). H2S; (C). NCl3; (D). BF3 6.一个电子排布为1S22S22P63S23P63d24S2的元素其最可能的价态是(A). +1; (B). +2; (C). +4; (D). +7 7.根据晶体场理论,高自旋配合物的理论判据是 (A). 分裂能≈ 成对能; (B). 分裂能 > 成对能 (C). 分裂能 > 成键能 (D). 分裂能 < 成对能 8.在配合物[Co(en)(C2O4)2]- 中,中心原子Co的配位数为 (A). 2; (B). 4; (C). 6; (D). 3 9.MA2B2C2型配合物有几种空间异构体 (A). 2; (B). 4; (C). 5; (D). 3 10.在相同温度时,已知下列反应的平衡常数 H2(g) +S(s) H2S(g) (K1) S(s) +O2(g) SO2(g) (K2) 则反应 H2(g) +SO2(g) O2(g) +H2S(g) 的平衡常数为 (A). K1 + K2; (B). K1 - K2; (C). K1 ? K2; (D). K1 / K2 11.已知FeO(s)+C(s)=CO(g)+Fe(s)反应的△rHo为正,△rSo为正(假 定△rHo和△rSo不随温度而变),下列说法正确的是 (A). 低温下自发过程,高温下非自发过程 第二章物质的状态 1.某气体在293K与9.97×104Pa时占有体积1.910-1dm3其质量为0.132g,试求这种气体的 相对分子质量,它可能是何种气体? 解 4.一容器中有4.4 g CO2,14 g N2,12.8g O2,总压为2.026105Pa,求各组分的分压。 解 9.有一高压气瓶,容积为30 dm3,能承受2.6×107Pa,问在293K时可装入多少千克O2而不致发生危险? 解 第五章氢和稀有气体 3.写出工业制氢的三个主要化学方程式和实验室中制备氢气最简便的方法?答 14.完成并配平下列反应方程式: (1)XeF4 + ClO- 3 → (2)XeF4 + Xe → (3)Na4XeO6 + MnSO4 + H2SO4→ (4)XeF4 + H2O → (5)XeO3 + Ba(OH)2→ (6)XeF6 + SiO2→ 答①XeF4 +2 ClO- 3+2 H2O=Xe + 2ClO- 4 + 4HF ③5Na4XeO6 + 2MnSO4 +7 H2SO4 =5XeO3 +2 NaMnO4 + 7 H2O + 9Na2SO4 ⑤2XeO3 +2 Ba(OH)2 = Ba2XeO6 + Xe + O2 + 2H2O 第六章化学热力学初步 2. 计算体系的热力学能变化,已知: (1)体系吸热1000J,对环境做540J的功; (2)体系吸热250J,环境对体系做635J的功; 解 3. 在298K 和100kPa 恒压下,2 1 mol 的OF 2同水反应,放出161.5kJ 热量,求 反应 OF 2(g) + H 2O(g) → O 2(g) + 2HF(g) 的△rH θm 和△rU θ m 。 解 12. 已知下列键能数据 键 N ≡N N —F N —Cl F —F Cl —Cl 键能/ kJ ·mol 1 - 942 272 201 155 243 试由键能数据求出标准生成热来说明NF 3在室温下较稳定而NCl 3却易爆炸。 解 13. 已知下列数据 △f H θm (CO 2,g )= —393.5 kJ ·mol 1 - 食品营养学 食物可以定义为含有许多天然的化学成分以提供人类色、香、味和营养的可食物质,而食物中提供人体营养的有机和无机化学成分称为营养素。 从化学性质和生理功能可将营养素分为六大类,即蛋白质,脂肪,碳水化合物(糖和淀粉)、矿物质、维生素和水,这些物质因为是人体生存所必需而被称为必需营养素。现在有人把膳食纤维看作第七大营养素,而抗氧化成分为半必需营养素。这些营养素为机体提供能量、构建和维持机体组织、调节机体的各种生理过程。 第一章消化吸收 Nutrition Nutrition might be defined as the process whereby we obtain the essential nutrients and use them to make many substances our bodies need.This process would include eating and digesting food and absorbing and using,or metabolizing,,the nutrients it contains. 营养:谋求养身,即人类获得必需的营养素并利用他们来合成人体需要物质的过程,它包括人体摄入、消化、吸收、利用或代谢营养物质的过程,是人类通过摄取食物满足机体生理需要的生物学过程。 Nutrients Nutrients are the chemical components of food which perform nutritive functions: Fats脂肪 Proteins蛋白质 Carbohydrates碳水化合物 Minerals矿物质 Vitamins维生素 Water水 Dietary fiber,Antioxidants膳食纤维和抗氧化成分 Function of foods and nutrients: Provide energy for activities build and maintain body tissue(组织) Regulate body processes(调节生理过程) Good Nutrition 1、What is good nutrition? Good nutrition implies that we are obtaining from our food all of the essential nutrients in the amounts needed to keep our bodies functioning and to maintain optimum(最适宜的)health. A very simplified definition of good nutrition might be“eating the right foods in the right amounts,and can keep us to finish our work(physical and mental)efficiently.” 好的营养是指人体从食物中获得保持人体正常生理功能和最佳健康状况所需数量的必需营养素。简单地说,吃正好数量的适宜食物,以使人体能有效地完成体力和脑力工作。 Digestion Digestion is the mechanical and chemical breaking down of food into smaller components,(usually inside a body,)to a form that can be absorbed. 消化是食物在消化道管内被分解为小分子物质的过程。 消化方式分为机械性消化和化学性消化。 机械性消化是指通过消化管得运动,将食物磨碎,并使食物与消化液充分混合,同时将食物向消化管远端推出;化学性消化是指通过消化液的各种化学作,将食物中得营养成分分解成小分子物质。通常这两种消化方式同时进行,相互配合。 Gastrointestinal Tract(胃肠道)—stomach、intestine 吸收(absorption)是食物经消化后,透过消化管黏膜,进入血液和淋巴循环的过程。 第十三章硼族元素 总体目标: 1.掌握硼单质、氢化物、卤化物和含氧化物的性质、用途和制备方法 2. 通过硼及其化合物的结构和性质,掌握缺电子化合物的成键特征 3.掌握铝及其化合物的结构、性质和制备 4. .认识铍和铝的相似性 各节目标: 第一节硼单质及其化合物 1.掌握硼单质的结构、化学性质、用途和制备方法 2.掌握乙硼烷、硼酸(H3BO3)、硼砂和三卤化硼的性质、结构和制备方法 3.通过硼及其化合物的结构和性质,掌握缺电子化合物的成键特点和桥键的形成 第二节铝单质及其化合物 1.掌握铝及其化合物的主要性质和AlCl3的结构,了解铝的提取和冶炼 2.认识铍和铝的相似性,如金属单质、无水卤化物、水合卤化物、氢氧化物 第三节镓、铟、铊 了解镓、铟、铊单质及其重要化合物的性质 习题 一、选择题 ⒈下列有关硼、铝性质的叙述,错误的是( ) A.都是缺电子原子 (OH)3是弱酸,Al(OH)3是两性偏碱性C.其三卤化物分子都是平面三角形结构 D.都是亲氧元素 ⒉在下列a—Al2O3的制备方法中,不妥的是( ) A.灼烧Al(OH)3 B.灼烧Al(NO3)3 C.高温电解Al2(SO4)3 D.金属铝在氧中燃烧 ⒊下列铝的化合物不能用湿法制得的是( ) A. Al2(CO3)3 (SO4)3 C.AlCl3 (Ac)3 4. 以下矿物中含有铝的是( ) A.冰晶石 B.孔雀石 C.白云石 D.方铅矿 5. 下列化合物属于缺电子化合物的是 ( ) (吉林大学《无机化 学例题与习题》) B. H[BF4] C. B2O3 D. Na[Al(OH)4] 6. 在硼的化合物中,硼原子的最高配位数不超过4,这是因为( ) A .硼原子半径小 B.配位原子半径大 C.硼与配位原子电负性差小 D. 硼原子无价层d轨 道 7. 下列关于BF3的叙述中,正确的是( ) 易形成二聚体为离子化合物 C. BF3为路易斯酸 D. BF3常温下为液体 8. 下列金属单质中,熔点最低的是( ) (吉林大学《无机化学例 题与习题》) A. Cu B. Zn C. Na D. Ga 9. 下列化合物中,熔点最低的是( ) (吉林大学《无机化学 例题与习题》) A. BCl3 B. CCl4 C. SiCl4 D. SnCl4 10. 下列物质中水解并能放出H2的是 ( ) (吉林大学《无机化 学例题与习题》) 无机化学(上) 知识点总结 第一章 物质存在的状态 一、气体 1、气体分子运动论的基本理论 ①气体由分子组成,分子之间的距离>>分子直径; ②气体分子处于永恒无规则运动状态; ③气体分子之间相互作用可忽略,除相互碰撞时; ④气体分子相互碰撞或对器壁的碰撞都是弹性碰撞。碰撞时总动能保持不变,没有能量损失。 ⑤分子的平均动能与热力学温度成正比。 2、理想气体状态方程 ①假定前提:a 、分子不占体积;b 、分子间作用力忽略 ②表达式:pV=nRT ;R ≈8.314kPa 2L 2mol 1-2K 1- ③适用条件:温度较高、压力较低使得稀薄气体 ④具体应用:a 、已知三个量,可求第四个; b 、测量气体的分子量:pV=M W RT (n=M W ) c 、已知气体的状态求其密度ρ:pV=M W RT →p=MV WRT →ρMV RT =p 3、混合气体的分压定律 ①混合气体的四个概念 a 、分压:相同温度下,某组分气体与混合气体具有相同体积时的压力; b 、分体积:相同温度下,某组分气体与混合气体具有相同压力时的体积 c 、体积分数:φ= 2 1 v v d 、摩尔分数:xi= 总 n n i ②混合气体的分压定律 a 、定律:混合气体总压力等于组分气体压力之和; 某组分气体压力的大小和它在混合气体中体积分数或摩尔数成正比 b 、适用范围:理想气体及可以看作理想气体的实际气体 c 、应用:已知分压求总压或由总压和体积分数或摩尔分数求分压、 4、气体扩散定律 ①定律:T 、p 相同时,各种不同气体的扩散速率与气体密度的平方根成反比: 2 1 u u =21p p =2 1 M M (p 表示密度) ②用途:a 、测定气体的相对分子质量;b 、同位素分离 二、液体 无机化学双语教育的感悟 0引言 近年来,无机化学学科发展迅速,世界范围内,科研成果层出不穷,我国的原始创新能力显著增强。但是,笔者结合多年无机化学科研实践,发现前沿的、具有国际高水平的文献,大多为英文文献,国际学术会议及国际学术交流也大都使用英语。特别是最新研究成果,科学家们所使用的某些名词术语尚无固定的翻译,不利于学术交流,不利于课堂教学,但如果采用双语进行教学交流,可以避免对科学名词产生误解和不准确的翻译。采用双语教学,不但可以使学生充分了解到无机化学日新月异的发展成果,而且还可以使现阶段的本科教学充分和国际接轨,有助于拓展高等教育的国际交流,促进高等学校培养创新性人才[1]。因此,建立完整完善的无机化学双语教学内容体系和双语教学团队,积极研究、试行无机化学双语教学和推进双语教学、研究与示范,提高教学质量,克服我国高等院校普通英语教学多年存在的教学效益低、学生外语应用能力差及外语教学与专业教学脱节的弊端,对获取国际先进研究成果信息、提高国内科研成果在国际上的影响力以及培养具有国际竞争力的各类人才十分必要,意义重大。以下结合近年来的双语教学实践探索,从教学方法、教学内容、教学手段和教学评价等方面谈谈实施双语课程教学的几点体会。 1教学方法 1.1循序渐进的教学方法 在课堂上,同时使用中文和英文两种语言教学。英文和中文的课堂讲授比例,应注意循序渐进的推行,逐步增大英文比例。在双语教学初期,中文占70%,英文占30%,70%的中文是考虑到学生学习课程的重要任务是为了获得相关专业知识,同时也便于双向交流,特别是在教学过程的初期阶段尤为重要。当课程教学推进到一半左右,开始使用英语比例达70%以上,课堂教学组织全部用英语,讲授内容重点、难点既用英文,又用中文讲;内容展示英文比例达到80-90%,重难点内容及重要的英文专业术语就近列出其规范的中文。内容展示比例较高是为了让学生有更多的机会沉浸式学习英语,在不知不觉中提高英语水平。就近列出中文意义目的在于抓住重点难点,适应学生将来进一步学习如考研的需要,因为目前大部分研究生入学课程考试仍是采用中文。 1.2联系实际,培养兴趣和创新能力 化学是一门紧密联系人们生产、生活的学科,教学不能脱离现实生活。“兴趣是最好的老师”,双语教学无机化学课程,本身是学生比较感兴趣,大多数同学都会有新鲜感而愿意接受;如果在课堂上再进 第十八章 氢 稀有气体 总体目标: 1.掌握氢及氢化物的性质和化学性质 2.了解稀有气体单质的性质及用途 3.了解稀有气体化合物的性质和结构特点 各节目标: 第一节 氢 1.掌握氢的三种成键方式 2.掌握氢的性质、实验室和工业制法及用途 3.了解离子型氢化物、分子型氢化物和金属性氢化物的主要性质 第二节 稀有气体 1.了解稀有气体的性质和用途 2.了解稀有气体化合物的空间构型 习题 一 选择题 1.稀有气体不易液化是因为( ) A.它们的原子半径大 B.它们不是偶极分子 C.它们仅仅存在较小的色散力而使之凝聚 D.它们价电子层已充满 2.用VSEPR 理论判断,中心原子价电子层中的电子对数为3的是( ) A .PF 3 B.NH 3 C.-34PO D.-3NO 3.用价电子对互斥理论判断,中心原子周围的电子对数为3的是( )(吴成 鉴《无机化学学习指导》) A.SCl2 B.SO3 C .XeF4 D. PF5 4.用价电子对互斥理论判断,中心原子价电子层中的电子对数为6的是() A.SO2 B. SF6 C. 3 AsO D. BF3 4 5. XeF2的空间构型是() A.三角双锥 B.角形 C. T形 D.直线型 6.下列稀有气体的沸点最高的是()(吴成鉴《无机化学学习指导》) A.氪 B.氡 C.氦 D.氙 7.能与氢形成离子型氢化物的是()(吴成鉴《无机化学学习指导》) A.活泼的非金属 B.大多数元素 C.不活泼金属 D.碱金属与碱土金属 8.稀有气体原名惰性气体,这是因为() A.它们完全不与其它单质或化合物发生化学反应 B.它们的原子结构很稳定,电离势很大,电子亲合势很小,不易发生化学反应 C.它们的价电子已全部成对 D.它们的原子半径大 9.下列各对元素中,化学性质最相似的是()(吉林大学《无机化学例题与习题》) A.Be 与Mg B.Mg与Al C Li与Be D.Be与Al 10.下列元素中,第一电离能最小的是()(吉林大学《无机化学例题与习题》) A.Li B.Be C. Na D.Mg 11.下列化合物中,在水中的溶解度最小的是()(吉林大学《无机化学例题与习题》) 第一章物质的结构 1-20 氦首先发现于日冕。1868年后30年间,太阳是研究氦的物理,化学性质的唯一源泉。 (a)观察到太阳可见光谱中有波长为4338A,4540A,4858A,5410A,6558A 的吸收(1A=10-10m来分析,这些吸收是由哪一种类氢原子激发造成的?是 He,He +还是He2+ ? (b)以上跃迁都是由n i=4向较高能级(n f)的跃迁。试确定 n f值,求里德堡常数R He i+。(c)求上述跃迁所涉及的粒子的电离能I(He j+),用电子伏特为单位。 (d)已知 I(He+)/ I(He)=2.180。这两个电离能的和是表观能A(He2+),即从He 得到He2+的能量。A(He2+)是最小的能量子。试计算能够引起He 电离成He2+所需要的最低能量子。在太阳光中,在地球上,有没有这种能量子的有效源泉? (c=2.997925×108 ms-1;h=6.626×10-34Js;1eV=96.486KJ.mol-1=2.4180×1014Hz) 38、第8周期的最后一个元素的原子序数为:148。电子组态:8S26P6 39、二维化的周期表可叫宝塔式或滴水钟式周期表。这种周期表的优点是能够十分清楚地看到元素周期系是如何由于核外电子能级的增多而螺旋发展的,缺点是每个横列不是一个周期,纵列元素的相互关系不容易看清。 40、“类铝”熔点在1110K~1941K之间,沸点在1757~3560K之间,密度在1.55g/m3 ~4.50 g/m3之间。 41、最高氧化态+3,最低氧化态-5。 1、解:O=O (12e-); H-O-O-H 14(e-); C=O (10e-);0=C=O(16e-);Cl-N-Cl(26e-);F–S - F (34e-) F F 2、解:共13种,如: 有关药学专业无机化学双语教学的一些思考 无机化学是我校药学方向的学生入学后接触的第一门化学基础必修课,它不仅为学生学习后继课程打下必要的自然科学基础,还对培养学生理科素质、科学思维方法和综合能力具有重要意义。其教学效果既要保证让学生学好化学基础知识,又要根据学生今后的专业发展方向提供一些和专业有关的知识和技能。因此如何正确对待基础课程双语教学的方向,如何开展双语教学,是我们一直在思考的问题。目前无机化学教研室已开展了两轮无机化学理论课和一轮实验课的双语教学,总结了很多经验,但也存在不少问题。本文藉此机会,谈谈对本校药学专业无机化学双语教学定位的一些体会。 一、无机化学双语教学的意义 无机化学是化学中最古老的分支,其理论与技术渗透到医学和药学的各个学科。目前无机化学仍然发展迅速,新的领域不断被开拓,与国际交流广泛,英文科技文献和书籍繁多。面向现代化、面向未来的医药科技人才,必须掌握最新的信息和最先进的东西,而这些信息的获取大多来自英文报道。因此21世纪的化学教育应面向世界,其中英语作为工具在学科教学中的作用将越来越突出。双语教学有助于学生对无机化学课程全面、准确地了解和最新信息的获取,使得学生具有一定的阅读原版教材的能力。其次,通过双语教学,学生有了应用英语的机会,为专业学习服务,而专业学习的趣味性又能促进学生发展英语能力,提高英语应用水平。 二、发展具有自身特色的无机化学双语教学 国际通行的一般意义的双语教学的基本要求是:在教育过程中,有计划、有系统地使用两种语言作为教学媒体,使学生在整体学识、两种语言能力以及这两种语言所代表的文化学习及成长上,均能达到顺利而自然的发展。在这里,第二种语言是教学的语言和手段而不是教学的内容或科目。所以,在无机化学双语教学的实施过程中,正确处理好语言教学和教学语言的关系,是我们首要坚持的原则。就一门具体的课程而言,教学的主要目的是传授学科知识和培养科学能力,因此要保证能够完成无机化学基本知识的传授,而不能为了使学生容易接受而降低课程难度或缩减授课内容。经过两轮的教学,我们希望药学专业无机化学的双语教学能够达到以下目的:基础,实用;以技能为主,英语为辅;追求质量,办出特色。 (一)以打好基础,培养学生长期学习兴趣为目标 大学一年级学生学习热情较高,易接受新生事物。对开始接触双语教学的学生的调查表明,大多数学生认为双语教学有新鲜感,有助于英语水平的提高和今后专业英语的学习,每周用于无机化学的课外学习时间超过4小时。但学生们的英语水平差别较大,又是初次接触双语教学,面对大量的专业词汇容易产生畏难情绪。而且无机化学本身还具有这些特点:①大部分内容抽象。学生对无机化学的绝大部分内容没有直接的感官印象,需要教师借助图、表来把抽象的内容形象化。②逻辑性强,如果对前一章节的不了解就会影响到下一章节的学习。因此如何激发学生长期的学习兴趣,是高质量地完成无机化学双语教学的重要保证。 为了能够使学生尽快适应,从陌生到熟悉双语教学,我们采用在过渡型双语教学模式的基础上,循序渐进,采取不同方式逐步深入教学。将多媒体课件的应用与其他教学方法相结合,如课堂提问、例题训练与精解等。要求学生课前预习指定内容,熟悉该部分的专业词汇;授课 第一章 一些基本概念和定律 本章总目标: 1:学习物质的聚集状态分气态、固态、液态三种,以及用来表示这三种聚集态的相关概念。 2;重点掌握理想气体状态方程、道尔顿分压定律以及拉乌尔定律。 各小节目标 第一节:气体 1:了解理想气体的概念,学习理想气体的状态方程推导实际气体状态方程的方法。 2:掌握理想气体状态方程的各个物理量的单位及相关的计算。 理想气体:忽略气体分子的自身体积,将分子看成是有质量的几何点;假设分子间没有相互吸引,分子之间及分子与器璧之间发生的碰撞时完全弹性的,不造成动能损失。 3:掌握Dalton 分压定律的内容及计算。 第二节:液体和溶液 1:掌握溶液浓度的四种表示方法及计算 ○1物质的量浓度(符号:B c 单位1mol L -?):溶液中所含溶质B 的物质的量除 以溶液的体积。 ○2质量摩尔浓度(B B A n b m =,单位:1mol kg -?):溶液中溶质B 的物质的量除以溶剂的质量。 ○ 3质量分数(B B m m ω=):B 的质量与混合物的质量之比。 ○4摩尔分数(B B n n χ=):溶液中溶质的物质的量与溶液的总物质的量之比。 2:了解非电解质稀溶液的依数性及其应用。 第三节:固体 1:了解常见的四种晶体类型 2:掌握四类晶体的结构特征及对物质性质的影响,比较其熔沸点差异。 Ⅱ 习题 一 选择题: 1.如果某水合盐的蒸汽压低于相同温度下的蒸汽压,则这种盐可能发生的现象是() (《无机化学例题与习题》吉大版) A.气泡 B.分化 C.潮解 D.不受大气组成影响 2.严格的讲,只有在一定的条件下,气体状态方程式才是正确的,这时的气体称为理想气体。这条件是() A.气体为分子见的化学反应忽略不计 B.各气体的分压和气体分子本身的体积忽略不计 C.各气体分子的“物质的量”和气体分子间的引力忽略不计 D.各气体分子间的引力,气体分子的体积忽略不计 3.在300K,把电解水得到的并经干燥的H 2和O 2 的混合气体40.0克,通入60.0L 的真空容器中,H 2和O 2 的分压比为() A.3:1 B.2:1 C.1:1 D.4:1 4.在下述条件中,能使实际气体接近理想的是() A.低温、高压 B.高温、低压 C.低温、低压 D.高温、高压 5.某未知气体样品为5.0克,在温度为1000C时,压力为291KPa时体积是0.86L,该气体的摩尔质量是() A.42g/mol B.52g/mol C.62g/mol D.72g/mol 6.处于室温一密闭容器内有水及与水相平衡的水蒸气。现充入不溶于水也不与水反应的气体,则水蒸气的压力()(《无机化学例题与习题》吉大版) A.增加 B.减少 C.不变 D.不能确的 7.将300K、500KPa的氧气5L。400K、200KPa的氢气10L和200K、200KPa的氮气3L,三种气体压入10L容器中维持300K,这时气体的状态是() A.氧气的压力降低,氮气、氢气压力增加 B.氢气的压力降低,氮气、氧气的压力增加 C.氮气的压力不变,总压力比混合前低 D.氧气、氮气、氢气的压力降低,总压力比混合前低 8.土壤中NACL含量高时植物难以生存,这与下列稀溶液的性质有关的是()(《无机化学例题与习题》吉大版) A. 蒸汽压下降 B.沸点升高 C. 冰点下降 D. 渗透压 9.一种元素的相对原子质量,是该元素的一定质量与核素12 6 C的摩尔质量的1/12的比值,这一质量是() A.原子质量 B.各核素原子质量的平均质量 C.平均质量 D.1mol原子平均质量 10.在一次渗流试验中,一定物质的量的未知气体通过小孔渗相真空,需要的时间为5S,在相同条件下相同物质的量的氧气渗流需要20S。则未知气体的相对分子质量为() (《无机化学例题与习题》吉大版) A.2 B.4 C.8 D.16 11.下述理想气体常数R所用单位错误的是() mol-1?K-1 B. 8.314KJ?mol-1?K-1 C. 8.314KPa?L? mol-1?K-1 12.下列说法正确的是() A.44gCO 2和32gO 2 所含的分子数相同,因而体积不同 B.12gCO 2和12gO 2 的质量相等,因而“物质的量”相同 C.1molCO 2和1molO 2 的“物质的量”相同,因而它们的分子数相同 第九章 氧化还原反应 本章总目标: 1:牢固掌握氧化还原的基本概念,熟练掌握氧化还原反应式配平的方法。 2:理解标准电极电势的意义,能运用标准电极电势来判断氧化剂和还原剂的强弱,氧化还原反应的方向和计算平衡常数 3:会用能斯特方程式来讨论离子浓度变化时电极电势的改变和对氧化还原反应的影响 各小节目标 第一节:氧化还原反应与原电池 1:掌握化合价、氧化数的概念,以及原电池的符号表示方法。 2:能判断原电池的正、负极以及会表示电池的电动势,可以配平电极反应式,书写电池反应方程式。 第二节:电池反应的热力学 1:可以判断原电池反应的自发性:r m G zEF θ ?=-,E>0反应以原电池的方式进行。 2:掌握 E θ 和电池反应的 K θ 的关系的计算; 2.303ln ln lg RT RT zE F RT K E K K zF zF θθθθθ=?= =. 3:掌握利用能斯特方程来求算电极电势:。0.059lg V E E z θ??? ?=+???? 氧化型还原型 第三节:影响电极电势的因素 学会运用能斯特方程来从酸度、沉淀物生成和配位化合物生成三方面来讨论这些因素对电池电动势的影响。 第四节:化学电源与电解 1:认识几种常见的化学电源---锌锰电池、银锌电池、铅蓄电池、燃料电池、镍氢电池、锂电池和锂离子电池。 2:了解分解电压和超电压的概念。 第五节:图解法讨论电极电势 1:会看元素电势图。 2;可以根据元素电势图判断酸性的强弱、计算电对的电极电势 112212......n n n z E z E z E E z z z θθθθ +++= +++、判断某种氧化态的稳定性学会绘制和利用自由能-氧化数图。 习题 一 选择题 1.将反应K 2Cr 2O 7+HCl → KCl+CrCl 3+Cl 2+H 2O 完全配平后,方程式中Cl 2的系数是( )(《无机化学例题与习题》吉大版) A. 1l B.2 C.3 D.4 2.下列化合物中,氧呈现+2价氧化态的是( )(《无机化学例题与习题》吉大版) A. Cl 2 O 5 B.Br O 7 C.H Cl O 2 D.F 2O 3.将反应KMnO 4+ HCl → Cl 2+ Mn Cl 2+ KCl+H 2O 配平后方程式中HCl 的系数是( )(《无机化学例题与习题》吉大版) A.8 B.16 C.18 D.32 4.某氧化剂YO(OH)2+中元素Y 的价态为+5,如果还原7.16×10-4mol YO(OH)2+溶液使Y 至较低价态,则需要用0.066 mol/L 的Na 2SO 3溶液26.98ml 。还原产物中Y 元素的氧化态为( )(《无机化学例题与习题》吉大版) A. -2 B.-1 C.0 D.+1 5.已知电极反应ClO 3-+6H+6e ═Cl -+3H 2O 的△rG θm =-839.6 kJ/ mol,则E 0 ClO3-/ Cl-值 为( )(《无机化学例题与习题》吉大版) A. 1.45V B.0.73V C.2.90V D.-1.45V 6.使下列电极反应中有关离子浓度减小一半,而E 值增加的是( )(《无机化学例题与习题》吉大版) A. Cu 2+ + 2e - ═ Cu B. I 2 + 2e - ═ 2I - C.2H + + 2e - ═ H 2 D.Fe 3+ + e - ═ Fe 2+ 7.将有关离子浓度增大5倍,E 值保持不变的电极反应是( )(《无机化学例题与习题》吉大版) A. Zn 2+ + 2e - ═ Zn B. MnO 4- + 8 H + + 5e - ═ Mn 2+ + 4H 2O C. Cl 2 + 2e - ═ 2Cl - D. Cr 3+ + e - ═ Cr 2+ 8.将下列反应设计成原电池时,不用惰性电极的是( )(《无机化学例题与习题》吉大版)大学无机化学第十六章试题及答案
大学无机化学 上册
北京化工大学《无机化学》(双语)期末考试模拟试卷-A
大学无机化学第六章试题及答案
无机化学试题上
(上册)课后武大无机化学习题答案
食品营养学双语版_重点版
大学无机化学第十二章试题及答案
无机化学_知识点总结
无机化学双语教育的感悟
大学无机化学第十七章试题及答案解析
2015北师大版无机化学习题答案(上册)
[药学,双语,教学]有关药学专业无机化学双语教学的一些思考
大学无机化学第一章试题及答案(供参考)
(完整word版)大学无机化学第九章试题及答案