
菌落计数及报告方法
1、目的
建立微生物实验中菌落计数及报告规范,从实际生长的菌落数中计算出较为科学的结果
2、方法说明本文件采用平板计数法,产品中污染的细菌种类不同,每种细菌都有它一定的生理特性,培养时对营养要求,培养温度、培养时间、pH值、需氧性质等均有所不同。在实际工作中,不可能做到满足所有菌的要求,因此所测定的结果,只包括在本方法所使用的条件下生长的微生物总数。
3、参考文件GB7918.2-1987化妆品微生物标准检验方法细菌总数测定
4、菌落计数方法先用肉眼观察,点数菌落数,然后再用放大5~10倍的放大镜检查,以防遗漏。记下各平皿的菌落数后。求出同一稀释度各平皿生长的平均菌落数。若平皿中有连成片状的菌落或花点样菌落蔓延生长时,该平皿不宜计数。若片状菌落不到平皿中的一半,而其余一半中菌落数分布又很均匀,则可将此半个平皿菌落计数后乘2,以代表全皿菌落数。
5菌落计数及报告方法
5.1 首先选取平均菌落数在30~300之间的平皿,作为菌落总数侧定的范围。当只有一个稀释度的平均菌落数符合此范围时,即以该平皿菌落数乘其稀释倍数(见表中例1) ,
5.2 若有两个稀释度,其平均菌落数均在30~300个之间,则应求出两者菌落总数之比值来决定。若其比值小于或等于2 ,应报告其平均数,若大于2则报告其中较小的菌落数( 见表中例2及例3),
5.3 若所有稀释度的平均菌落数均大于300 个,则应按稀释度最高的平均菌落数乘以稀释倍数报告之(见表中例4),
5.4 若所有稀释度的平均菌落数均少于30个,则应按稀释度最低的平均菌落数乘以稀释倍数报告之(见表中例5),
5.5 若所有稀释度的平均菌落数均不在30~300个之间,其中一个稀释度大于300个,而相邻的另一稀释度小于30个时,则以接近30 或300的平均菌落数乘以稀释倍数报告之(见表中例6),
5.6 若所有的稀释度均无菌生长,报告数为每克或每毫升小于10 个。
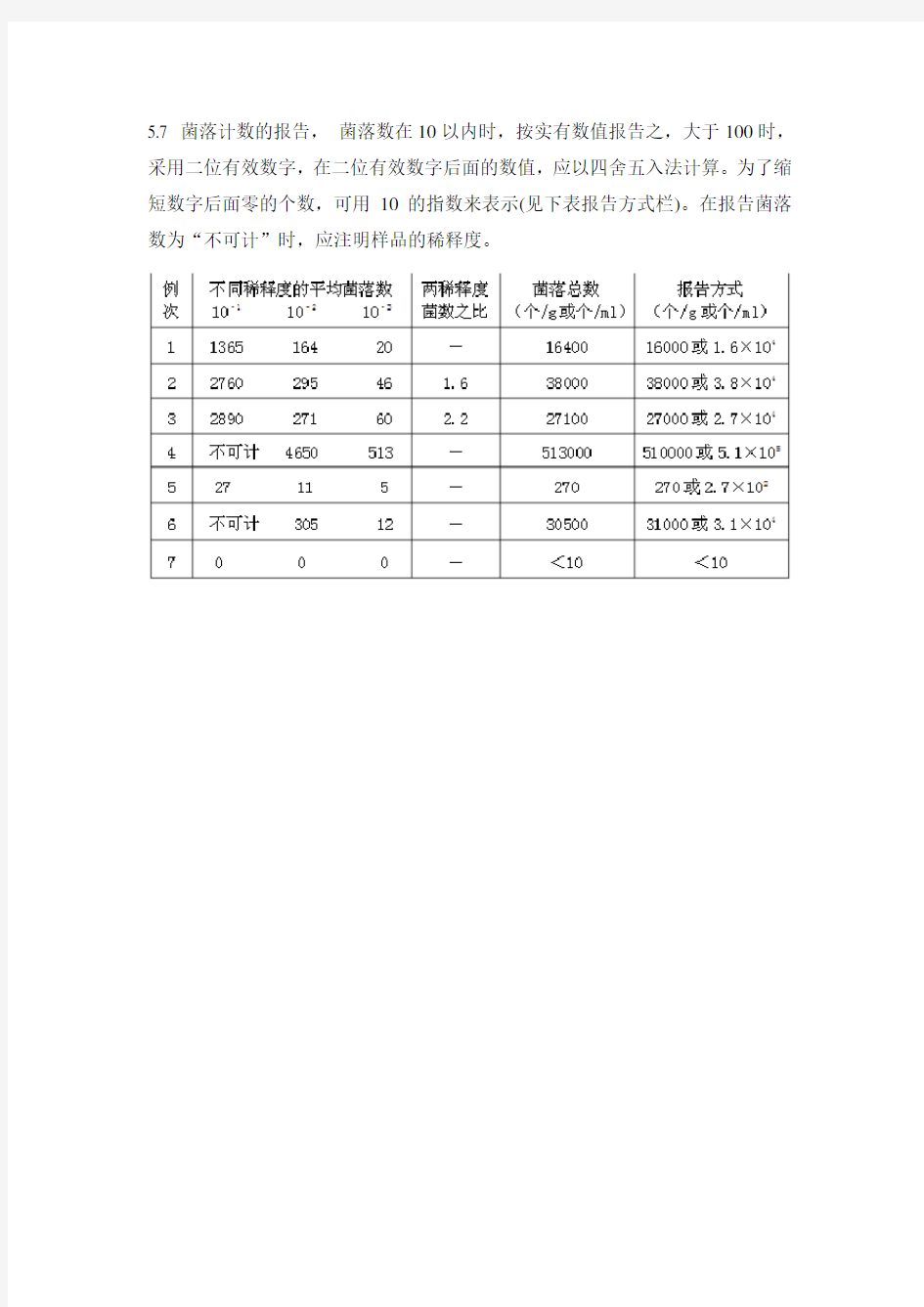
5.7 菌落计数的报告,菌落数在10以内时,按实有数值报告之,大于100时,采用二位有效数字,在二位有效数字后面的数值,应以四舍五入法计算。为了缩短数字后面零的个数,可用10的指数来表示(见下表报告方式栏)。在报告菌落数为“不可计”时,应注明样品的稀释度。
平板菌落计数法 一、目的要求 学习平板菌落计数的基本原理和方法。 二、基本原理 平板菌落计数法是将等测样品经适当稀释后,其中的微生物充分分散为单个细胞,取一定量的稀释液接种到平板上,经过培养,由每个单细胞生长繁殖而形成的肉眼可见的菌落,即一个单菌落应代表原样品中的一个单细胞。统计菌落数,根据其稀释倍数和取样接种量即可换算出样品中的含菌数。但是,由于待测样品往往不易完全分散成单个细胞,所以,长成的一个单菌落也可能来自样品中的2~3或更多个细胞。因此平板菌落计数的结果往往偏低。现在常使用菌落形成单位。 该计数法的缺点是操作较繁,结果需要培养一段时间才能取得,而且测定结果易受多种因素的影响,但是这种计数方法最大的优点是可以获得活菌的信息,所以被广泛用于生物制品检验,以及食品、饮料和水等含菌指数或污染度的检测。 三、器材 大肠杆菌悬液,LB琼脂培养基,1mL、5mL无菌吸管,无菌平皿,无菌水,无菌试管,试管架和记号笔等。 四、操作步骤 1、编号 取无菌平皿9套,分别标明为10-4、10-5、10-6各三套,另取6支无菌试管分别标记为10-1、10-2、10-3、10-4、10-5、10-6。 2、稀释 用1mL无菌吸管吸取1mL已充分混匀的大肠杆菌菌悬液,精确地放0.5mL至10-1的试管中,此即为10倍稀释,将多余的菌液放回原菌液中。 将10-1试管充分振荡、混匀。另取一支1ml吸管插入10-1试管中来回吹吸菌液三次,进一步将菌体分散、混匀。动作不要太猛太快,吸时插入,吹时提出,再用此吸管吸取10-1菌液1mL,精确地放0.5mL至10-2试管中,此即为100倍稀释,依次类推, 3、取样
平板菌落计数法 农资101 1031240125 周瑶 实验原理 平板菌落计数法是将待测样品经适当稀释之后,其中的微生物充分分散成单个细胞,取一定量的稀释样液接种到平板上,经过培养,由每个单细胞生长繁殖而形成肉眼可见的菌落,即一个单菌落应代表原样品中的一个单细胞。统计菌落数,根据其稀释倍数和取样接种量即可换算出样品中的含菌数。但是,由于待测样品往往不易完全分散成单个细胞,所以,长成的一个单菌落也可能来自样品中的2—3或更多个细胞。因此平板菌落计数的结果往往偏低。为了清楚地阐述平板菌落计数的结果,现在已倾向使用菌落形成单位(cfu)而不以绝对菌落数来表示样品的活菌含量。 平板菌落计数法虽然操作较繁,结果需要培养一段时间才能取得,而且测定结果易受多种因素的影响,但是,由于该计数方法的最大优点是可以获得活菌的信息,所以被广泛用于生物制品检验(如活菌制剂),以及食品、饮料和水〔包括水源水〕等的含菌指数或污染程度的检测。 实验方法 1、样品稀释液的制备 准确称取待测样品l0g,放入装有90ml无菌水并放有小玻璃珠的250ml三角瓶中,用手或置摇床上振荡20 min,使微生物细胞分散,静置20-30s,即成10-1稀释液;再用1ml 无菌吸管,吸取10-1稀释液lml,移入装有9ml无菌水的试管中,吹吸3次,让菌液混合均匀,即成10-2稀释液;再换一支无菌吸管吸取10-2稀释液1 ml,移入装有9ml无菌水的试管中,也吹吸三次,即成l0-3稀释液;以此类推,连续稀释,制成10-4、10-5、10-6、10-7、10-8、10-9等一系列稀释菌液。放菌液时吸管尖不要碰到液面,即每一支吸管只能接触一个稀释度的菌悬液,否则稀释不准确,结果误差较大。 用稀释平板计数时,待测菌稀释度的选择应根据样品确定。样品中所含待测菌的数量多时,稀释度应高,反之则低。通常测定细菌菌剂含菌数时,采用10-7、10-8、10-9稀释度,测定土壤细菌数量时,采用10-4、10-5、10-6稀释度,测定放线菌数量时,采用l0-3、10-4、10-5稀释度,测定真菌数量时,采用10-2、10-3、10-4稀释度。 2、平板接种培养平板接种培养有浇注平板培养法和涂布平板培养法两种方法。 (1) 浇注平板培养法(以细菌为例) 1) 取样 用三支1ml无菌吸管分别吸取10-4、10-5、和10-6的稀释菌悬液各1ml,对号放入编好号的无菌平皿中,每个平皿放0.2ml。 不要用1ml吸管每次只靠吸管尖部吸0.2ml稀释菌液放入平皿中,这样容易加大同一稀释度几个重复平板间的操作误差。
实验十一稀释平板计数法 实验目的 学习稀释平板菌落计数的基本原理和方法。 实验内容 用稀释平板菌落计数法对菌悬液进行计数。 实验原理 平板菌落计数法是将待测样品经适当稀释之后,其中的微生物充分分散成单个细胞,取一定量的稀释样液接种到平板上,经过培养,由每个单细胞生长繁殖而形成肉眼可见的菌落,即一个单菌落应代表原样品中的一个单细胞。统计菌落数,根据其稀释倍数和取样接种量即可换算出样品中的含菌数。但是,由于待测样品往往不易完全分散成单个细胞,所以,长成的一个单菌落也可能来自样品中的2—3或更多个细胞。因此平板菌落计数的结果往往偏低。为了清楚地阐述平板菌落计数的结果,现在已倾向使用菌落形成单位(cfu)而不以绝对菌落数来表示样品的活菌含量。 平板菌落计数法虽然操作较繁,结果需要培养一段时间才能取得,而且测定结果易受多种因素的影响,但是,由于该计数方法的最大优点是可以获得活菌的信息,所以被广泛用于生物制品检验(如活菌制剂),以及食品、饮料和水〔包括水源水〕等的含菌指数或污染程度的检测。 实验器材 酿酒酵母菌悬液 马铃薯培养基 1m1吸管,平皿,试管,试管架,恒温培养箱等。 实验步骤 1.无菌器材的准备 (1) 无菌培养皿:取培养皿9套,包扎、灭菌。 (2) 无菌移液管的准备:取1m1移液管,在后部管口处用铁丝塞入棉花少许(长约1~1.5cm ),以防将菌液吸出,同时也可避免将外面的微生物吹入。棉花要塞得松紧适宜吹时能通气但不使棉花滑下为准。然后将移液管尖端放在4~5cm宽的长纸条一端呈45o角折叠纸条包住尖端,用左手捏住管身,右手将吸管压紧,在桌面上向前滚动,以螺旋式包扎起来,上端剩余纸条折叠打结后干热灭菌。 (3) 无菌水:取6支试管,分别装入4.5m1蒸馏水,加棉塞,灭菌。 2.样品稀释液的制备 (1) 编号 取无菌平皿9套,分别用记号笔标明10-4、10-5、10-6(稀释度)各3套。另取6支盛有4.5m1无菌水的试管,依次标是10-1、10-2、10-3、10-4、10-5、10-6。
产品说明 一、概述 XK97-A型菌落计数器是一种数字显示式半自动细菌检验仪器。由计数器、探笔、计数池等部分组成。计数器采用CMOS集成电路设计制造。黑色纵深背景式记数池内,采用节能环形荧光灯侧射照明,菌落对比清楚。按照细菌计数检验规程规定,仪器显示器设计为三位数,当一只培养皿中菌落生长数超过300个时,应将检验样品稀释重作,以保证计数的准确性。本仪器可减轻实验人员的劳动强度,提高工效和工作质量。产品广泛用于食品、饮料、药品、生物制品、卫生用品、饮用水、工业废水、临床标本中细菌数的检验。是各级卫生防疫站、环境监测站、食品卫生监督检验所、医院、生物制品所、药检所、食品厂、日化厂及大专院校、科研单位实验室的必备仪器。 二、主要参数 ·计数器容量:0~999 ·光源灯功率:16W ·总功耗:<20W ·电源电压:220V±10%,50Hz ·体积:280×230×90 ·重量:1.4kg 三、使用方法 a .接通电源,拨动开关计数池内灯亮,显示屏显示“001”,将探笔插头插入仪器的插孔内,按下“复位”键调零使仪器进入工作状态。 b.放入待检培养皿。 c.用探笔在培养皿底面对所有的菌落逐个点数。每点一个应听到“嘟”声才说明有效,否则应重点。此时,点到的菌落被标上颜色,显示数字自动累加。 d.用放大镜仔细检查,确认点数无遗漏,计数即已完毕。 e.显示屏内的数字即为该培养皿的菌落数。 f.记录数字后取出培养皿。按“复位”键,显示屏进入初始状态。 四、注意事项 a.仪器应放置在平整牢固的台面上使用。 b.点数菌落时,探笔不要过于倾斜,轻轻点下至有弹跳感时,数字即被输入。 c.仪器应防潮、防剧烈震动、防直接日光曝晒、防酸碱侵蚀,用后应加防尘罩。 d.注意防止细菌培养物污染计数池。 e.仪器及探笔均不能随意拆卸。若发现故障,应请有经验的技术人员检修。
菌落计数器计数方法详解 菌落计数器由计数器、探笔、计数池等部分组成,计数器采用CMOS集成电路精心设计,LED数码管显示,字高13mm,清晰明亮,配合专用探笔,计数灵敏准确,菌落对比清楚。便于观察。可广泛用于食品、饮料、药品、生物制品、化妆品、卫生用品、饮用水、生活污水、工业废水、临床标本中细菌数的检验。那么菌落计数器都是怎样进行计数的呢?上海巴玖来为您详细讲解菌落计数器的计数方法。 1.计数器测定法 即用血细胞计数器进行计数。取一定体积的样品细胞悬液置于血细胞计数器的计数室内,用显微镜观察计数。由于计数室的容积是一定的(O.1mm3),因而根据计数器刻度内的细菌数,可计算样品中的含菌数。本法简便易行,可立即得出结果(本法不仅适于细菌计数,也适用于酵母菌及霉菌孢子计数)。 2.电子计数器计数法 电子计数器的工作原理是测定小孔中液体的电阻变化,小孔仅能通过一个细胞,当一个细胞通过这个小孔时,电阻明显增加,形成一个脉冲,自动记录在电子记录装置上。 该法测定结果较准确,但它只识别颗粒大小,而不能区分是否为细菌。因此,要求菌悬液中不含任何碎片。 3.活细胞计数法 常用的有平板菌落计数法,是根据每个活的细菌能长出一个菌落的原理设计的。取一定容量的菌悬液,作一系列的倍比稀释,然后将定量的稀释液进行平板,根据培养出的菌落数,可算出培养物中的活菌数。此法灵敏度高,是一种检测污染活菌数的方法,也是目前国际上许多国家所采用的方法。使用该法应注意:①一般选取菌落数在30~300之间的平板进行计数,过多或过少均不准确;②为了防止菌落蔓延,影响计数,可在培养基中加入O.001%2,3,5一氯化三苯基四氮唑(TTC);③本法限用于形成菌落的微生物。 广泛应用于水、牛奶、食物、药品等各种材料的细菌检验,是常用的活菌计数法。 4.比浊法 比浊法是根据菌悬液的透光量间接地测定细菌的数量。细菌悬浮液的浓度在一定
操作步骤 l.编号取无菌平皿9套,分别用记号笔标明10-4、10-5、10-6。(稀释度)各3套。另取6支盛有4.5mL无菌水的试管,依次标是10-1、10-2、10-3、10-4、10-5、10-6。 2.稀释用lmL无菌吸管吸取lmL已充分混匀的大肠杆菌菌县液(待测样品),精确地放0.5ml 至10-1的试管中,此即为10倍稀释。将多余的菌液放回原菌液中。将10-1试管置试管振荡器上振荡,使菌液充分混匀。另取一支lml吸管插入10- 1试管中来回吹吸菌悬液三次,进一步将菌体分散、混匀。吹吸菌液时不要太猛太快,吸时吸管伸人管底,吹时离开液面,以免将吸管中的过滤棉花浸湿或使试管内液体外溢。用此吸管吸取10-1菌液lmL,精确地放0.5mL至10-2试管中,此即为100倍稀释。……其余依次类推。放菌液时吸管尖不要碰到液面,即每一支吸管只能接触一个稀释度的菌悬液,否则稀释不精确,结果误差较大。 3.取样用三支1mL无菌吸管分别吸取10-4、10-5和10-6的稀释菌悬液各lmL,对号放入编好号的无菌平皿中,每个平皿放0.2mL。不要用lmL吸管每次只靠吸管尖部吸0.2mL稀释菌液放入平皿臼,这样容易加大同一稀释度几个重复平板间的操作误差。 4.倒平板.尽快向上述盛有不同稀释度菌液的平皿中倒入融化后冷却至45℃左右的牛肉膏蛋白胨培养基约15毫升/平皿,置水平位置迅速旋动平皿,使培养基与菌液混合均匀,而又不使培养基荡出平皿或溅到平皿盖上。由于细菌易吸附到玻璃器皿表面,所以菌液加入到培养皿后,应尽快倒入融化并于已冷却至45℃左右的培养基,立即摇匀,否则细菌将不易分散或长成的菌落连在一起,影响计数。待培养基凝固后,将平板倒置于37℃恒温培养箱中培养。 5.计数培养48h后,取出培养平板,算出同一稀释度三个平板上的菌落平均数,并按下列公式进行计算,每毫升中菌落形成单位(cfu)=同一稀释度三次重复的平均菌落数×稀释倍数×5。一般选择每个平板上长有30~300个菌落的稀释度计算每毫升的含菌量较为合适。同一稀释度的三个重复对照的菌落数不应相差很大,否则表示试验不精确。实际工作中同一稀释度重复对照平板不能少于三个,这样便于数据统计,减少误差。 由10-4、10-5、10-6三个稀释度计算出的每毫升菌液中菌落形成单位数也不应相差太大。平板菌落计数法,所选择倒平板的稀释度是很重要的。一般以三个连续稀释度中的第二个稀释度倒平板培养后所出现的平均菌落数在50个左右为好,否则要适当增加或减少稀释度加以调整。 平板菌落计数法的操作除上述倾注倒平板的方式以外,还可以用涂布平板的方式进行。二者操作基本相同,所不同的是后者先将牛肉膏蛋白胨培养基融化后倒平板,待凝固后编号,并于37℃左右的温箱中烘烤30min,或在超静工作台上适当吹干,然后用无菌吸管吸取稀释好的菌液对号接种于不同稀释度编号的平板上,并尽快用无菌玻璃涂棒将菌液在平板上涂布均匀,平放于实验台上20~30min,使菌液渗入培养基表层内,然后倒置37℃的恒温箱中培养24~48h。涂布平板用的菌悬液量一般以0.1ml较为适宜,如果过少菌液不易涂布开,过多则在涂布完后或在培养时菌液仍会在平板表面流动,不易形成单菌落。五、实验报告1.结果2.将培养后菌落计数结果填入下表2.思考题(1)为什么融化后的培养基要冷却至45℃左右才能倒平板? (2)要使平板菌落计数准确,需要掌握哪几个关键?为什么? (3)试比较平板菌落计数法和显微镜下直接计数法的优缺点及应用。(4)当你的平板上长出的菌落不是均匀分散的而是集中在一起时,你认为问题出在哪里? (5)用倒平板法和涂布法计数,其平板上长出的菌落有何不同?为什么要培养较长时间(48h)后观察结果?
实验六细菌计数法 菌落总数就是指在一定条件下(如需氧情况、营养条件、pH、培养温度和时间等)每克(每毫升)检样所生长出来的细菌菌落总数。按国家标准方法规定,即在需氧情况下,37℃培养48h,能在普通营养琼脂平板上生长的细菌菌落总数,所以厌氧或微需氧菌、有特殊营养要求的以及非嗜中温的细菌,由于现有条件不能满足其生理需求,故难以繁殖生长。因此菌落总数并不表示实际中的所有细菌总数,菌落总数并不能区分其中细菌的种类,所以有时被称为杂菌数,需氧菌数等。 目录 菌落总数介绍 检验方法 说明(一)样品的处理和稀释: (二)倾注培养 (三)计数和报告 菌落总数介绍 菌落是指细菌在固体培养基上生长繁殖而形成的能被肉眼识别的生长物,它是由数以万计相同的细菌集合而成。当样品被稀释到一定程度,与培养基混合,在一定培养条件下,每个能够生长繁殖的细菌细胞都可以在平板上形成一个可见的菌落。菌落总数测定是用来判定食品被细菌污染的程度及卫生质量,它反映食品在生产过程中是否符合卫生要求,以便对被检样品做出适当的卫生学评价。菌落总数的多少在一定程度上标志着食品卫生质量的优劣。 检验方法 菌落总数的测定,一般将被检样品制成几个不同的10倍递增稀释液,然后从每个稀释液中分别取出1mL置于灭菌平皿中与营养琼脂培养基混合,在一定温度下,培养一定时间后(一般为48小时),记录每个平皿中形成的菌落数量,依据稀释倍数,计算出每克(或每ml)原始样品中所含细菌菌落总数。基本操作一般包括:样品的稀释--倾注平皿--培养48小时--计数报告。国内外菌落总数测定方法基本一致,从检样处理、稀释、倾注平皿到计数报告无何明显不同,只是在某些具体要求方面稍有差别,如有的国家在样品稀释和倾注培养进,对吸管内液体的流速,稀释液的振荡幅度、时间和次数以及放置时间等均作了比较具体的规定。检验方法参见:GB4789.2-94 《中华人民共和国国家标准食品卫生微生物学检验菌落总数测定》SN0168-92 《中华人民共和国进出口商品检验行业标准出口食品菌落计数》 说明 (一)样品的处理和稀释: 1.操作方法:以无菌操作取检样25g(或25ml),放于225mL灭菌生理盐水或其他稀释液的灭菌玻璃瓶内(瓶内预置适当数量的玻璃珠)或灭菌乳钵内,经充分振要或研磨制成1:10的均匀稀释液。固体检样在加入稀释液后,最好置灭菌均质器中以8000~10000r/min的速度处理1min,制成1:10的均匀稀释液。用1ml灭菌吸管吸取1:10稀释液1ml,沿管壁徐徐注入含有9ml灭菌生理盐水或其他稀释液的试管内,振摇试管混合均匀,制成1:100的稀释液。另取1ml灭菌吸管,按上项操作顺序,制10倍递增稀释液,如此每递增稀释一次即换用1支1ml灭菌吸管。2.无菌操作:操作中
菌落计数器的计数方法 菌落计数器由计数器、探笔、计数池等部分组成,计数器采用CMOS集成电路精心设计,LED数码管显示,字高13mm,清晰明亮,配合专用探笔,计数灵敏准确,菌落对比清楚。便于观察。可广泛用于食品、饮料、药品、生物制品、化妆品、卫生用品、饮用水、生活污水、工业废水、临床标本中细菌数的检验。那么菌落计数器都是怎样进行计数的呢?上海巴玖来为您详细讲解菌落计数器的计数方法。 1.计数器测定法 即用血细胞计数器进行计数。取一定体积的样品细胞悬液置于血细胞计数器的计数室内,用显微镜观察计数。由于计数室的容积是一定的(O.1mm3),因而根据计数器刻度内的细菌数,可计算样品中的含菌数。本法简便易行,可立即得出结果(本法不仅适于细菌计数,也适用于酵母菌及霉菌孢子计数)。 2.电子计数器计数法 电子计数器的工作原理是测定小孔中液体的电阻变化,小孔仅能通过一个细胞,当一个细胞通过这个小孔时,电阻明显增加,形成一个脉冲,自动记录在电子记录装置上。 该法测定结果较准确,但它只识别颗粒大小,而不能区分是否为细菌。因此,要求菌悬液中不含任何碎片。 3.活细胞计数法 常用的有平板菌落计数法,是根据每个活的细菌能长出一个菌落的原理设计的。取一定容量的菌悬液,作一系列的倍比稀释,然后将定量的稀释液进行平板,根据培养出的菌落数,可算出培养物中的活菌数。此法灵敏度高,是一种检测污染活菌数的方法,也是目前国际上许多国家所采用的方法。使用该法应注意:①一般选取菌落数在30~300之间的平板进行计数,过多或过少均不准确;②为了防止菌落蔓延,影响计数,可在培养基中加入O.001%2,3,5一氯化三苯基四氮唑(TTC);③本法限用于形成菌落的微生物。 广泛应用于水、牛奶、食物、药品等各种材料的细菌检验,是常用的活菌计数法。 4.比浊法
大肠菌群是经常用来衡量食品卫生情况的重要指标,绝大部分食品都会要 求检测的项目。在食品微生物实验室里,大肠菌群和菌落总数的检测频次应该是最高的,但检测过程中总会有一些小问题困扰着大家,以下来讲解一下大肠 菌群平板计数法的注意事项。 方法选择 相比于MPN计数法,平板计数法更适用于大肠菌群含量较高的食品。但大肠菌群多少算是含量较高呢国标里没有明确规定,但通常认为,产品大肠菌群以100CFU/g(mL)为界,超过这个含量一般认为是含量较高。但具体什么时候选用平板计数法进行大肠菌群的检测,大部分情况还是要看你的产品执行的标准。假如产品标准要求大肠菌群含量的单位为CFU/g(mL),那必须选用平板计数法。若是/g(mL)或者MPN/100g(mL),就应选择MPN计数法,MPN法具体选用哪版国标 此处不再赘述。因此,根据自己产品的情况选择适当的检测方法。 培养基的要求 平板计数法使用的培养基为结晶紫中性胆盐琼脂培养基,简称VRBA。无论是国标,还是培养基的使用说明中都明确表示,VRBA是不需要进行灭菌的,煮沸2min即可使用。特地点出这一点是因为很多朋友都在问VRBA的灭菌条件,对不灭菌的培养基不信任,害怕出现检测异常,那是因为这些小伙伴们对其中的原理不清楚。大肠菌群的定义是在一定培养条件下能够在发酵乳糖、产酸产气的需氧和兼性厌氧的革兰氏阴性无芽孢杆菌,因此大肠菌群是不能形成芽孢的,在VRBA培养基煮沸的过程中,即使有大肠菌群存在也会被杀灭,所以从培养基带入污染的可能性是没有的。当然盛装培养基的容器是需要进行灭菌的,以免容器引入污染。另外,VRBA是一种选择性的培养基,含有的结晶紫对革兰氏阳性菌有比较强的抑制作用而对革兰氏阴性菌几乎没有作用,而且平板培养产生的菌落还需要进行复发酵的验证,因此VRBA培养基就不需要进行灭菌了。但值得注意 的是,VRBA需要现配现用,配制出的培养基应当在3h之内使用完毕。 稀释度的确定 国标中要求选择2-3个适宜的连续稀释度。什么样的稀释度是合适的呢这要根据计数来决定。计数环节要求选择菌落数在15CFU-150CFU的平板进行计数,
平板菌落计数法 (一)目的要求 学习平板菌落计数的基本原理和方法。 (二)基本原理 平板菌落计数法是将待测样品经适当稀释之后,其中的微生物充分分散成单个细胞,取一定量的稀释样液接种到平板上,经过培养,由每个单细胞生长繁殖而形成肉眼可见的菌落,即一个单菌落应代表原样品中的一个单细胞。统计菌落数,根据其稀释倍数和取样接种量即可换算出样品中的含菌数。但是,由于待测样品往往不易完全分散成单个细胞,所以,长成的一个单菌落也可来自样品中的2~3或更多个细胞。因此平板菌落计数的结果往往偏低。为了清楚地阐述平板菌落计数的结果,现在已倾向使用菌落形成单位(colony-forming units,cfu)而不以绝对菌落数来表示样品的活菌含量。 平板菌落计数法虽然操作较繁,结果需要培养一段时间才能取得,而且测定结果易受多种因素的影响,但是,由于该计数方法的最大优点是可以获得活菌的信息,所以被广泛用于生物制品检验(如活菌制剂),以及食品、饮料和水(包括水源水)等的含菌指数或污染程度的检测。
(三)器材 1.菌种大肠杆菌菌悬液。 2.培养基牛肉膏蛋白陈培养基。 3.仪器或其他用具1mL无菌吸管,无菌平皿,盛有4.5ml无菌水的试管,试管架,恒温培养箱等。 (四)操作步骤 l.编号 取无菌平皿9套,分别用记号笔标明10-4、10-5、10-6。(稀释度)各3套。另取6支盛有4.5mL无菌水的试管,依次标是10-1、10-2、10-3、10-4、10-5、10-6。 2.稀释 用lmL无菌吸管吸取lmL已充分混匀的大肠杆菌菌县液(待测样品),精确地放0.5mL至10-1的试管中,此即为10倍稀释。将多余的菌液放回原菌液中。 将10-1试管置试管振荡器上振荡,使菌液充分混匀。另取一支lml吸管插入10 1试管中来回吹吸菌悬液三次,进一步将菌体分散、混匀。吹吸菌液时不要太猛太快,吸时吸管伸人管底,吹时离开液面,以免将吸管中的过滤棉花浸湿或使试管内液体外溢。用此吸管吸取10-1菌液lmL,精确地放0.5mL至10-2试管中,此即为100倍
稀释平板计数法 实验目的 学习稀释平板菌落计数的基本原理和方法。 实验内容 用稀释平板菌落计数法对菌悬液进行计数。 实验原理 平板菌落计数法是将待测样品经适当稀释之后,其中的微生物充分分散成单个细胞,取一定量的稀释样液接种到平板上,经过培养,由每个单细胞生长繁殖而形成肉眼可见的菌落,即一个单菌落应代表原样品中的一个单细胞。统计菌落数,根据其稀释倍数和取样接种量即可换算出样品中的含菌数。但是,由于待测样品往往不易完全分散成单个细胞,所以,长成的一个单菌落也可能来自样品中的2—3或更多个细胞。因此平板菌落计数的结果往往偏低。为了清楚地阐述平板菌落计数的结果,现在已倾向使用菌落形成单位(cfu)而不以绝对菌落数来表示样品的活菌含量。 平板菌落计数法虽然操作较繁,结果需要培养一段时间才能取得,而且测定结果易受多种因素的影响,但是,由于该计数方法的最大优点是可以获得活菌的信息,所以被广泛用于生物制品检验(如活菌制剂),以及食品、饮料和水〔包括水源水〕等的含菌指数或污染程度的检测。 实验器材 酿酒酵母菌悬液 马铃薯培养基 1m1吸管,平皿,试管,试管架,恒温培养箱等。 实验步骤 1.无菌器材的准备 (1) 无菌培养皿:取培养皿9套,包扎、灭菌。 (2) 无菌移液管的准备:取1m1移液管,在后部管口处用铁丝塞入棉花少许(长约1~1.5cm ),以防将菌液吸出,同时也可避免将外面的微生物吹入。棉花要塞得松紧适宜吹时能通气但不使棉花滑下为准。然后将移液管尖端放在4~5cm宽的长纸条一端呈45o角折叠纸条包住尖端,用左手捏住管身,右手将吸管压紧,在桌面上向前滚动,以螺旋式包扎起来,上端剩余纸条折叠打结后干热灭菌。 (3) 无菌水:取6支试管,分别装入4.5m1蒸馏水,加棉塞,灭菌。 2.样品稀释液的制备 (1) 编号 取无菌平皿9套,分别用记号笔标明10-4、10-5、10-6(稀释度)各3套。另取6支盛有4.5m1无菌水的试管,依次标是10-1、10-2、10-3、10-4、10-5、10-6。
菌落计数及报告方法 1、目的 建立微生物实验中菌落计数及报告规范,从实际生长的菌落数中计算出较为科学的结果 2、方法说明本文件采用平板计数法,产品中污染的细菌种类不同,每种细菌都有它一定的生理特性,培养时对营养要求,培养温度、培养时间、pH值、需氧性质等均有所不同。在实际工作中,不可能做到满足所有菌的要求,因此所测定的结果,只包括在本方法所使用的条件下生长的微生物总数。 3、参考文件GB7918.2-1987化妆品微生物标准检验方法细菌总数测定 4、菌落计数方法先用肉眼观察,点数菌落数,然后再用放大5~10倍的放大镜检查,以防遗漏。记下各平皿的菌落数后。求出同一稀释度各平皿生长的平均菌落数。若平皿中有连成片状的菌落或花点样菌落蔓延生长时,该平皿不宜计数。若片状菌落不到平皿中的一半,而其余一半中菌落数分布又很均匀,则可将此半个平皿菌落计数后乘2,以代表全皿菌落数。 5菌落计数及报告方法 5.1 首先选取平均菌落数在30~300之间的平皿,作为菌落总数侧定的范围。当只有一个稀释度的平均菌落数符合此范围时,即以该平皿菌落数乘其稀释倍数(见表中例1) , 5.2 若有两个稀释度,其平均菌落数均在30~300个之间,则应求出两者菌落总数之比值来决定。若其比值小于或等于2 ,应报告其平均数,若大于2则报告其中较小的菌落数( 见表中例2及例3), 5.3 若所有稀释度的平均菌落数均大于300 个,则应按稀释度最高的平均菌落数乘以稀释倍数报告之(见表中例4), 5.4 若所有稀释度的平均菌落数均少于30个,则应按稀释度最低的平均菌落数乘以稀释倍数报告之(见表中例5), 5.5 若所有稀释度的平均菌落数均不在30~300个之间,其中一个稀释度大于300个,而相邻的另一稀释度小于30个时,则以接近30 或300的平均菌落数乘以稀释倍数报告之(见表中例6), 5.6 若所有的稀释度均无菌生长,报告数为每克或每毫升小于10 个。
全自动菌落计数器RTAC-1型 RTAC-1型全自动菌落计数器是瑞韬科技根据多年技术积累产品经验,专为基层实验室设计的一款经济实用型菌落计数器,能轻松胜任大多数场合的基本计数:高精度的CCD镜头、全封闭自动定位样品仓、高效准确的菌落分析软件,性价比突出。 1200万像素CCD镜头,全封闭LED冷光源自动样品仓 全新设计的全封闭自动样品箱。辅以平板光源、带状光源和自动进出仓装置,彻底解决了因外界光线对玻璃培养皿折射光斑的干扰而影响统计精度的技术难题。 AutoCount TM菌落智能识别技术,使计数更方便快捷,统计结果更准确。自动菌落计数准确与否的关键是算法,本产品采用“瑞韬科技”专利的AutoCount TM菌落智能识别技术,无论是透明琼脂平板还是深色有色培养基都能轻松处理,且能对纸片进行有效的计数。 快速高效,极大地提高实验效率 “RTAC-1”型全自动菌落计数器采用真彩动态 CCD 和高速图像传输接口,常规平皿统计只需3秒。当原始样品菌浓较高,未做梯度稀释,直接培养形成的数千菌落,也可在5秒内自动计算出。 强大的区域选择功能
当培养皿中有局部片状菌落生长,而其他区域又分布均匀时,可通过区域选择工具,排除污染区域的菌落数。通过平皿直径和稀释度数据,迅速换算为全皿菌落总数。 仪器主要功能与技术指标 ▲培养皿类型:50-160mm ▲成像 ○ CCD规格:1200万像素,32位真彩 ○分辨率:0.04mm(更符合人工检测实际效果避免过度检测) ○图像拍摄:焦距、白平衡、色温可调 ▲光源 ○拍摄箱:全封闭、无日光干扰、自动居中、暗箱拍摄 ○光源:LED双冷光源拍摄系统 ▲统计功能 ○菌落识别技术:AutoCount TM菌落智能识别技术。 ○平皿类型:倾注、涂布、膜滤平皿、3M纸片。 ○菌落统计速度:300个菌落约3秒。 ○全皿菌落统计:菌落总数统计,并按多档尺寸分类显示。 ○区域选择统计:可选择任意圆形圈定区域进行统计。 ○鼠标点击统计:快速标记、添加菌落,适合培养皿边缘菌落的计数。 ○人工辅助修正:删除任意区域内的误选菌落。 ○统计效果调整:可人为调整菌落分析的精度。 ○直径分类统计:设置直径范围,统计特定大小的菌落。 ○颜色识别统计:根据色度、亮度、饱和度筛选特定菌落。 ○统计数据处理:培养样本稀释度输入实现自动换算。 ○大肠菌群计数:根据国家标准GB/T4789.3-2008大肠菌群平板计数和Petrifilm测试片法,实现大肠菌群自动计数。 ○大肠杆菌计数:根据国家标准GB/T4789.38-2008大肠杆菌Petrifilm测试片计数法,实现大肠杆菌自动计数。 ○金黄色葡萄球菌计数:根据国家标准GB/T4789.37-2008 Baird-Parker 平板计数和金黄色葡萄球菌Petrifilm测试片法,实现金黄色葡萄球菌自动计数。
1、计数器测定法: 即用血细胞计数器进行计数。取一定体积的样品细胞悬液置于血细胞计数器的计数室内,用显微镜观察计数。由于计数室的容积是一定的(O.1mm3),因而根据计数器刻度内的细菌数,可计算样品中的含菌数。本法简便易行,可立即得出结果。 本法不仅适于细菌计数,也适用于酵母菌及霉菌孢子计数。 2、电子计数器计数法: 电子计数器的工作原理是测定小孔中液体的电阻变化,小孔仅能通过一个细胞,当一个细胞通过这个小孔时,电阻明显增加,形成一个脉冲,自动记录在电子记录装置上。 该法测定结果较准确,但它只识别颗粒大小,而不能区分是否为细菌。因此,要求菌悬液中不含任何碎片。 3、活细胞计数法 常用的有平板菌落计数法,是根据每个活的细菌能长出一个菌落的原理设计的。取一定容量的菌悬液,作一系列的倍比稀释,然后将定量的稀释液进行平板培养,根据培养出的菌落数,可算出培养物中的活菌数。此法灵敏度高,是一种检测污染活菌数的方法,也是目前国际上许多国家所采用的方法。使用该法应注意:①一般选取菌落数在30~300之间的平板进行计数,过多或过少均不准确;②为了防止菌落蔓延,影响计数,可在培养基中加入O.001%2,3,5一氯化三苯基四氮唑(TTC);③本法限用于形成菌落的微生物。 广泛应用于水、牛奶、食物、药品等各种材料的细菌检验,是最常用的活菌计数法。 4、比浊法 比浊法是根据菌悬液的透光量间接地测定细菌的数量。细菌悬浮液的浓度在一定范围内与透光度成反比,与光密度成正比,所以,可用光电比色计测定菌液,用光密度(OD值)表示样品菌液浓度。 此法简便快捷,但只能检测含有大量细菌的悬浮液,得出相对的细菌数目,对颜色太深的样品,不能用此法测定。 5、测定细胞重量法 此法分为湿重法和干重法。湿重法系单位体积培养物经离心后将湿菌体进行称重;干重法系单位体积培养物经离心后,以清水洗净放人干燥器加热烘干,使之失去水分然后称重。 此法适于菌体浓度较高的样品,是测定丝状真菌生长量的一种常用方法。 6、测定细胞总氮量或总碳量 氮、碳是细胞的主要成分,含量较稳定,测定氮、碳的含量可以推知细胞的质量。此法适于细胞浓度较高的样品。 7、颜色改变单位法(colour change unit,简称CCU) 这种方法通常用于很小,用一般的比浊法无法计数的微生物,比如支原体等,因为支原体的液体培养物是完全透明的,呈现为清亮透明红色,因此无法用比浊法来计数,由于支原体固体培养很困难,用cfu法也不容易计数,因此需要用特殊的计数方法,即CCU法。它是以微生物在培养基中的代谢活力为指标,来计数微生物的相对含量的,下面以解脲脲原体为例,简单介绍其操作: (1).取12只无菌试管,每一管装1.8ml解脲脲原体培养基。 (2).在第一管加入0.2ml待测解脲脲原体菌液,充分混匀,从中吸取0.2ml加入第二管,依次类推,10倍梯度稀释,一直到最末一管 (3).于37度培养,以培养基颜色改变的最末一管作为待测菌液的CCU,也就是支原体的最大代谢活力,比如第六管出现颜色改变,他的相对浓度就是10的6次方CCU/ml. 一般来说,比浊法和菌落计数法就可以满足绝大多数细菌的计数,但是对支原体这样比较特殊的微生物,用CCU法比较合适。
平板菌落计数法 样品的稀释 固体和半固体食品:以无菌操作取25g样品,放入装有225 mL生理盐水的无菌均质杯内,于8000 ~10000r/min均质1min~2min,制成1:10样品匀液,或放入225 mL生理盐水的无菌均质袋中,用拍击式均质器拍打1min~2min,制成1:10的样品匀液。 液体食品:以无菌吸管吸取样品25mL放入装有225mL生理盐水的无菌玻璃瓶(瓶内预置适当数量的玻璃珠)中,充分混匀,制成1:10的样品匀液。 用1 mL无菌吸管或微量移液器吸取1:10的样品匀液1 mL加到装有9 mL PBS 的稀释管中,充分混匀制成1:100的样品匀液。 制备十倍递增系列稀释样品匀液。每递增稀释1次,换用1支1mL无菌吸管或吸头。 根据对样品污染状况的估计,选择2~3个适宜的连续稀释度的样品匀液(液体样品可以选择原液),每个稀释度分别吸取1mL样品均匀加入两个无菌平皿内。同时分别取1mL稀释液加入两个无菌平皿内作空白对照。 及时将15~20ml冷却至46℃平板计数琼脂培养基(可放置于46℃±1℃恒温水浴箱内保温)倾注平板,并转动平皿使其混合均匀。 琼脂凝固后,将平板翻转,置36±1℃培养48±2h。水产品30±1℃培养72±3h。 如果样品中可能含有在琼脂培养基表面弥漫生成的菌落时,可在凝固后的琼脂表面覆盖一薄层琼脂培养基(4mL),凝固后翻转平板,进行培养。 菌落计数 可用肉眼观察,必要时用放大镜检查,记录稀释倍数和相应的菌落数量。菌落计数以菌落形成单位((CFU)表示。 选取菌落数在30~300之间、无蔓延菌落生成的平板计数菌落总数。低于30,CFU的平板记录具体菌落数,大于300的可记录为多不可计。每个稀释度的菌落数应采用两个平板的平均数。 其中一个平板有较大片状菌落生长时,则不宜采用,而应以无片状菌落生长的平板作为该稀释度的菌落数;若片状菌落不到平板一半,而另一半又分布均匀,则可以半个平板的菌落数乘2代表一个平板的菌落数。
食品微生物学检验菌落总数测定 一、培养基和试剂 1、平板计数琼脂(plate count agar,PCA)培养基 成分 胰蛋白胨 5.0 g 酵母浸膏 2.5 g 葡萄糖 1.0 g 琼脂 15.0 g 蒸馏水 1000 mL pH 7.0±0.2 制法:将上述成分加于蒸馏水中,煮沸溶解,调节pH。分装试管或锥形瓶,121 ℃高压灭菌15 min。 2、磷酸盐缓冲液 成分 磷酸二氢钾(KH2PO4) 34.0 g 蒸馏水 500 mL pH 7.2 制法:贮存液:称取34.0 g的磷酸二氢钾溶于500 mL蒸馏水中,用大约175 mL的1 mol/L 氢氧化钠溶液调节pH,用蒸馏水稀释至1 000 mL后贮存于冰箱。 稀释液:取贮存液1.25 mL,用蒸馏水稀释至1 000 mL,分装于适宜容器中,121 ℃高压灭菌15 min。 3、无菌生理盐水 成分 氯化钠 8.5 g 蒸馏水 1 000 mL 制法:称取8.5g氯化钠溶于1 000 mL蒸馏水中,121 ℃高压灭菌15 min。 二、操作步骤 样品的稀释 1、固体和半固体样品:称取25 g 样品置盛有225 mL 磷酸盐缓冲液或生理盐水的无菌均质杯内,8000 r/min~10000 r/min 均质1 min~2 min,或放入盛有225 mL 稀释液的无菌均质袋中,用拍击式均质器拍打1 min~2 min,制成1:10 的样品匀液。 2、液体样品:以无菌吸管吸取25 mL 样品置盛有225 mL 磷酸盐缓冲液或生理盐水的无菌锥形瓶(瓶内预置适当数量的无菌玻璃珠)中,充分混匀,制成1:10 的样品匀液。 3、用1 mL 无菌吸管或微量移液器吸取1:10 样品匀液1 mL,沿管壁缓慢注于盛有9 mL 稀释液的无菌试管中(注意吸管或吸头尖端不要触及稀释液面),振摇试管或换用1 支无菌吸管反复吹打使其混合均匀,制成1:100 的样品匀液。 4、按3操作程序,制备10 倍系列稀释样品匀液。每递增稀释一次,换用1 次1 mL 无菌吸管或吸头。 5、根据对样品污染状况的估计,选择2 个~3 个适宜稀释度的样品匀液(液体样品可包括原液),在进行10 倍递增稀释时,吸取1 mL 样品匀液于无菌平皿内,每个稀释度做两个平皿。同时,分别吸取1 mL 空白稀释液加入两个无菌平皿内作空白对照。 6、及时将15 mL~20 mL 冷却至46 ℃的平板计数琼脂培养基(可放置于46 ℃±1 ℃恒温水浴箱中保温)倾注平皿,并转动平皿使其混合均匀。 培养
标题:TYJ-2A型菌落计数器操作规程 分发部门:总经理室、质量技术部、行政部(存档) TYJ-2A型菌落计数器操作规程 一目的 规范TYJ-2A型菌落计数器的操作过程,特制定本规程。 二范围 适用于TYJ-2A型菌落计数器的操作及保养。 三责任 TYJ-2A型菌落计数器的操作人员按本规程操作,QC主管对本规程的有效执行承担监督检查责任。 四规程 4.1 主要参数 计数器容量:0-999 发光显示窗字高:16mm 光源灯功率:16w 总功率:小于20w 电源电压:220V,50Hz 体积:200×270×70 重量:1.5kg 4.2 使用方法 4.2.1 将电源插头插入实验室220伏电源插座内。 4.2.2 将控笔插入仪器上的控笔插孔内 4.2.3 将电源开关拨向“开”,计数池内灯亮。同时显示窗内显示明亮的“000”,表示允
2/2 TYJ-2A型菌落计数器操作规程QC-O-125 许进行计数。 4.2.4 将待验的培养皿,皿底朝上放入计数池内。 4.2.5 用探笔在培养皿底面对所有的菌落逐个点数。此时,菌落处被标上颜色,显示窗内数字自动累加。 4.2.6 用放大镜仔细检查、确认点数无遗漏,计数即已完毕。 4.2.7 显示窗内的数字即为该培养皿内的菌落数 4.2.8 记录数字后取出培养皿,按“复0”按钮,显示恢复“000”,为另一培养皿的计数做好准备。 4.3 注意事项 4.3.1 仪器应放置在平整牢固的实验台上使用 4.3.2 点数菌落时,探笔不要过于倾斜,轻轻点下至有弹跳感时,数字即被输入。 4.3.3 仪器应防潮、防强烈震动、防直接日光暴晒防酸碱侵蚀,用后应加防尘罩。 4.3.4 注意防止细菌培养物污染计数池。 4.3.5 仪器及探笔均不能随意拆卸,若发现故障、应请有经验的技术人员检修。
实验四微生物平板菌落计数法 一、实验目的 学习并掌握平板菌落计数的基本原理和方法。 二、实验原理 平板菌落计数法是将待测样品经适当稀释之后,其中的微生物充分分散成单个细胞,取一定量的稀释样液接种到平板上,经过培养,由每个单细胞生长繁殖而形成肉眼可见的菌落,即一个单菌落应代表原样品中的一个单细胞。统计菌落数,根据其稀释倍数和取样接种量即可换算出样品中的含菌数。但是,由于待测样品往往不易完全分散成单个细胞,所以,长成的一个单菌落也可能来自样品中的2~3或更多个细胞。因此平板菌落计数的结果往往偏低,为了清楚地阐述平板菌落计数的结果,现在已倾向使用菌落形成单位(cfu)而不以绝对菌落数来表示样品的活菌含量。 平板菌落计数法虽然操作较繁,结果需要培养一段时间才能取得,而且测定结果易受多种因素的影响,但是该计数方法的最大优点是可以获得活菌的信息,所以被广泛用于生物制品检验(如活菌制剂),以及食品、饮料和水(包括水源水)等的含菌指数或污染程度的检测。 三、实验器材 1 .菌种:酵母菌。 2 .培养基:YEB培养基。 3 .仪器或其他用具: 1ml 无菌吸管,无菌平皿,盛有 4.5ml 无菌水的试管,试管架,恒温培养箱等。 四、实验步骤 1 .编号 取无菌平皿 9 套,分别用记号笔标明 10-4、 10-5、 10-6(稀释度)各 2 套,另取 6 支盛有 4.5ml 无菌水的试管,依次标是 10-1、 10-2、 10-3、 10-4、 10-5、 10-6。 2 .稀释 用 1ml 无菌吸管吸取 1ml 已充分混匀的大肠杆菌菌悬液(待测样品),精确地放0.5ml 至 10-1的试管中,此即为 10 倍稀释。将多余的菌液放回原菌液中。
微生物学检验菌落总数的测定 1 原理 微生物活体数量的测定方法,常用平板培养计数法。它是通过将样品制成均匀的一系列 不同稀释度的稀释液,再取一定的稀释液接种,使其均匀分布于培养皿中特定的培养基内,最后根据在平板上长出的菌落数计算出每克(或mL )样品中的活菌数量。 2 材料和仪器 2.1 平皿:φ90mm 。 2.2 无菌锥形瓶:容量250mL ,500 mL 。 2.3 无菌吸管:1mL (具0.01mL 个度),10mL (具0.1mL 刻度)或微量移液器及吸头。 2.4 灭菌锅。 2.5 恒温培养箱 2.6 涂棒。 2.7 酒精灯。 2.8 超净工作台。 2.9 磁力搅拌器。 2.10 漩涡振荡器 3 检验程序 菌落总数的检验程序见下图。 方法①↙ ↘方法② ↘ ↙
4 操作步骤 4.1 培养基和试剂的配制 4.1.1 平板计数琼脂培养基:LB培养基(最常用) 牛肉膏5g 蛋白胨10g 氯化钠5g 琼脂20g 蒸馏水1L pH 7.0~7.2 将上述成分加于蒸馏水中,煮沸溶解,调节pH值,分装锥形瓶中,121℃高压灭菌30分钟。 4.1.2 无菌生理盐水的配制: 称取8.5g氯化钠溶解于1000mL蒸馏水中,121℃高压灭菌30分钟。 4.2 样品的稀释: 4.2.1 固体样品:称取10g固体样品置于盛有90mL无菌生理盐水的无菌锥形瓶中(内装 数粒无菌玻璃珠),在旋转式摇床上200r/min充分振荡30min,制成1:10的样品均液,即10-1稀释液。 4.2.2用1mL无菌吸管或微量移液器吸取1:10样品均液1mL(吸取前需要摇匀1:10稀 释液),缓慢加入盛有9mL无菌生理盐水的无菌试管中(注意吸管或吸头尖端不能触及稀释液面),用漩涡振荡器振荡,混合均匀,制成1:100的样品稀释均液。 4.2.3按照4.2.2操作程序,制备10倍系列样品稀释液,每递增稀释一次,换用一次1mL 无菌吸管或吸头。 4.2.4 根据对样品活菌数量的估计,选择3~4个适宜稀释度的样品均液(比如10-6,10-7,10-8,10-9稀释液)。 4.2 平板接种与培养 接种方法1: 用1mL无菌吸管或微量移液器分别吸取不同稀释度的菌悬液1mL于一个无菌培养皿中(每个稀释度做三个重复),再在培养皿中分别倒入10~15mL已融化并冷却至45~50℃的培养基,盖好平皿盖子,趁热轻轻转动培养皿,使菌液与培养基充分混合均匀,冷凝后在恒温培养箱中倒置培养24~28h,培养温度为36℃±1℃。同时以无菌水作空白对照。 注:比如1000亿CFU样品稀释梯度可选择为:10-8,10-9,10-10。 接种方法2: 用1mL无菌吸管或微量移液器吸取0.2mL稀释液均液于计数培养基平板上,将稀释液涂布均匀,吸附,在恒温培养箱中倒置培养24~28h,培养温度为36℃±1℃。同时以无菌水作空白对照。(计算时需要把0.2mL的倍数也计算在稀释倍数内) 注:比如1000亿CFU样品稀释梯度可选择为:10-7,10-8,10-9。 4.3 菌落计数 可用肉眼观察,必要时借用放大镜或菌落计数器,以防遗漏。记录稀释倍数和相应的菌落数量。菌落计数以菌落形成单位(colony-forming units,CFU)表示 4.3.1 选取菌落数在30~300之间,无蔓延菌落生长的平板计数菌落总数。低于30CFU的平板记录具体菌落数,大于300的可记录为多不可计。每个稀释度的菌落数应采用3个平行平板的平均数。