
P
t ℃
溶
解
度g
姓名 班级 组别 评价 化学导学案 备课人 王国良 上课时间 2月28日 审核人 赵海新 课题 溶解度的表示方法 课型 预习展示
学习目标 1、知道溶解度的涵义与固体溶解度的表示方法。
2、了解温度对固体溶解度的影响以及溶解度曲线的意义。
重点难点 1、固体溶解度的表示方法 2、正确认识溶解性与溶解度的表示联系及区别
。导 学 过 程
教师复备 【创设情境】
我们知道,固体物质溶解度只受外界因素----温度的影响,我们可以通过实验方法测出物质在不同温度时的溶解度,又该如何表示出来呢? 【自主探究】
知识点一:溶解度的表示方法:
(一)、列表法:由实验测出不同物质在不同温度下的溶解度,制成表格得到溶解度表。 练习:根据溶解度表格完成下列问题:
①查某物质在某温度时的溶解度或某物质溶解度对应的温度:
NaCl 在20℃的溶解度就是 ,在100℃时的溶解度就是 ;
KNO 3 在20℃的溶解度就是 ,在100℃时的溶解度就是 。 溶解度为41、4g 时,NH 4Cl 饱与溶液所处的温度就是 ;溶解度为110g 时,KNO 3 饱与溶液所处的温度就是 。
②通过对比某物质在不同温度时的溶解度来判断物质溶解度受温度影响情况。 KCl 、NH 4NO 3、KNO 3等大多数物质,溶解度随温度升高而增大; NaCl 等物质溶解度受温度影响较小;
Ca(OH)2等少数物质溶解度随温度升高而减小。 ③可以比较同一温度时不同物质溶解度大小。
60℃时,表中几种物质溶解度由大到小的顺序为: 。 过渡:通过溶解度表可快捷、准确查找某些温度时某物质的溶解度,但却不能查出25℃、83℃等指定温度下某物质的溶解度,所以并不能反应出连续温度对应物质的溶解度。
温度℃ 0
10
20 30 40 50 60 70 80 90 10 溶解
度 g
NaCl 35、7 35、
8
36、0 36、
3 36、
6 37、
0 37、
3 37、
8 38、
4 39、
0 39、
8 KCl 27、6 31、
34、0 37、0 40、0 42、6 45、5 48、3 51、1 54、0 56、7 NH 4Cl 29、4 33、
3
37、2 41、4 45、8 50、4 55、2 60、2 65、6 71、3 77、3 KNO 3 13、3 20、
9 31、6 45、8 63、9 85、5 110
138
169
202
246
Ca(OH)2 0、185 0、
176 0、165
0、153
0、141
0、138
0、116
0、106
0、094
0、085
0、077
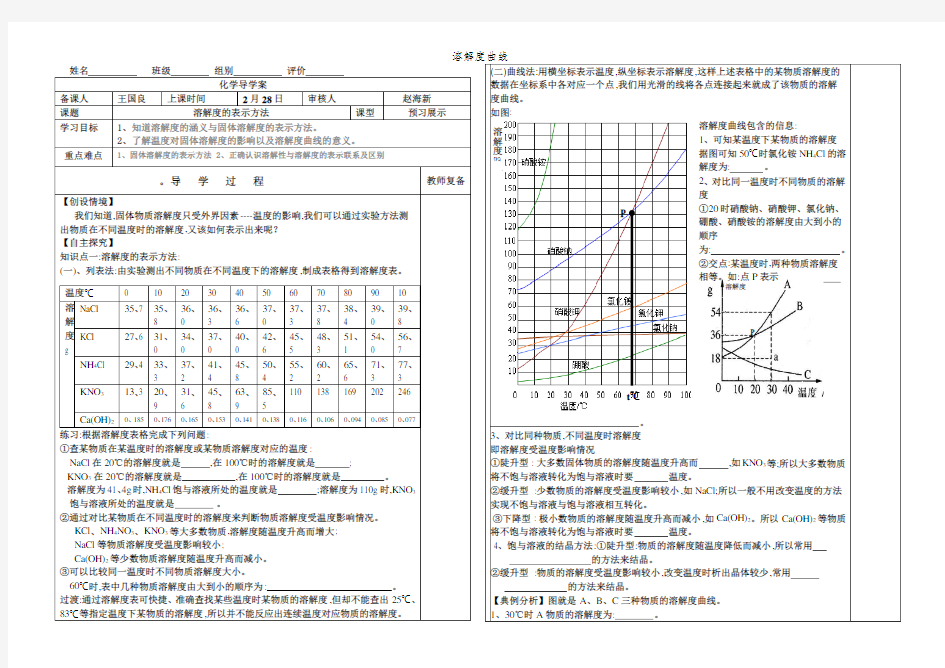
(二)曲线法:用横坐标表示温度,纵坐标表示溶解度,这样上述表格中的某物质溶解度的数据在坐标系中各对应一个点,我们用光滑的线将各点连接起来就成了该物质的溶解度曲线。 如图:
溶解度曲线包含的信息:
1、可知某温度下某物质的溶解度 据图可知50℃时氯化铵NH 4Cl 的溶
解度为: 。
2、对比同一温度时不同物质的溶解度
①20时硝酸钠、硝酸钾、氯化钠、硼酸、硝酸铵的溶解度由大到小的顺序
为: 。 ②交点:某温度时,两种物质溶解度相等。如:点P 表示 。
3、对比同种物质,不同温度时溶解度 即溶解度受温度影响情况
①陡升型 : 大多数固体物质的溶解度随温度升高而 ,如KNO 3等;所以大多数物质将不饱与溶液转化为饱与溶液时要 温度。
②缓升型 :少数物质的溶解度受温度影响较小,如NaCl;所以一般不用改变温度的方法实现不饱与溶液与饱与溶液相互转化。
③下降型 : 极小数物质的溶解度随温度升高而减小,如Ca(OH)2。所以Ca(OH)2等物质将不饱与溶液转化为饱与溶液时要 温度。
4、饱与溶液的结晶方法:①陡升型:物质的溶解度随温度降低而减小,所以常用 的方法来结晶。
②缓升型 :物质的溶解度受温度影响较小,改变温度时析出晶体较少,常用 的方法来结晶。
【典例分析】图就是A 、B 、C 三种物质的溶解度曲线。 1、30℃时A 物质的溶解度为: 。
溶解度
P
温度0
甲乙
甲
乙
冰水
C ()
溶解
度
(g)
2、P 点表示的意义: 。
3、30℃时,A 、B 、C 三种物质溶解度由大到小的顺序 。
4、将20℃时C 物质的近饱与溶液变为饱与溶液的方法有: 、 、 。
5、35℃时,A 、B 、C 的饱与溶液各w g,均冷却至20℃时,
析出晶体最多的就是 ,最少的就是 ,没有晶体 析出的就是 。
题组训练
A 组:
1、图3就是X 、Y 两种固体物质的溶解度曲线。下列说法中正确的就是( )
A.t 1℃时X 的溶解度大于Y 的溶解度
B.t 2℃时X 的溶解度等于Y 的溶解度
C.t 3℃时X 的饱与溶液降温至t 2℃时,变为不饱与溶液
D.t 4℃时Y 的不饱与溶液升温至t 2℃时,变为饱与溶液
2、右图就是A 、B 、C 三种物质的溶解度曲线。下列叙述正确的就是( ) A.t 3℃时,三种物质溶解度大小顺序为 A>B>C B.t l ℃时,A 的饱与溶液中溶质的质量分数为10% C.t 3℃时,C 的饱与溶液降温到t 2℃时变成不饱与溶液 D.t 1℃时,A 的饱与溶液升温到t 3℃时有晶体析出
3、图就是a 、b 两种固体物质的溶解度曲线,下列说法中不正确的就是( )
A 、a 的溶解度大于b 的溶解度
B 、在t ℃时,a 、b 的饱与溶液中溶质的质量分数相同
C 、当a 中含有少量b 时,可以用结晶法提纯a
D 、a 、b 都属于易溶物质
B 组:
1、右图为a 、b 两种物质的溶解度曲线。请根据图中内容回答下列问题:
(1)随着温度的升高,a 物质的溶解度的变化趋势就是 。 (2)曲线a 与b 的交叉点M 表示的含义就是 (3)37℃时a 物质的溶解度为 g,80℃时40g a 物质溶
于50g 水中所形成的溶液就是 溶液(选填“饱与”或“不饱与”)。 2、右图为A 、B 、C 三种物质的溶解度曲线。 (1)0℃时,A 的溶解度就是 g 。
(2)在 ℃时, A 、B 两物质的溶解度相等。
(3)把A 、B 、C 的饱与溶液从t 2℃降至t 1℃时,没有晶体析出的就是 。 3、甲乙两种固体的溶解度曲线如右图所示。在一个大烧杯中装着含有甲与 乙的两种饱与溶液,而且杯中还有少量甲与乙的固体存在。现将温度
由80℃降到20℃。下列说法正确的就是( )
A.杯中固体甲与固体乙都减少
B.杯中固体甲减少、固体乙增多
C.溶液中甲、乙溶质都减少
D.溶液中溶质甲减少、溶质乙增多
C 组
1、右图表示X 、Y 两种不含结晶水的固体物质的溶解度曲线。根据图示,判断下列说法中错误的就是( )。 (A)X 、Y 都就是易溶物质
(B)t ℃时,X 、Y 的饱与溶液中溶质的质量分数相等 (C)将t 1“℃时X 、Y 的饱与溶液均分别降温到t ℃,X 溶液中析出晶体的质量比Y 的多
(D)当X 的饱与溶液中含有少量Y 时,不能通过降温结晶的方法提纯X
2、甲、乙两种固体的溶解度曲线如下图。现将两试管分别装入甲、乙两种物质的饱与溶液(试管底部均有未溶解的固体),再放进盛有冰水的烧杯里,则下列说法正确的就是( ) A 甲溶液中溶质的质量分数增大 B 乙溶液中剩余的固体减少
C 试管里甲、乙物质的溶解度都增大
D 试管里甲、乙两溶液中的溶质都减少 达标测评
1、右图为A 、B 、C 三种物质的溶解度曲线,请据图判断下列叙
述中不正确...
的就是 A.t 1℃时,B 物质的溶解度为40g
B.t 2℃时,三种物质的溶解度由大到小的顺序为:A ﹥B ﹥C
C.要将C 的不饱与溶液转化为饱与溶液可以采取降温的方法
D.要使A 从其浓溶液中析出,可采用冷却热饱与溶液法
2、下图就是a 、b 、c 三种物质的溶解度曲线,a 与c 的溶解度曲线相交于
P 点。据图回答:(1)P 点的含义就是_______________________。
(2)t 2℃时,30ga 物质加入到50g 水中不断搅拌,能形成80g 溶液不?_____(填写“能”或“不能”)
(3)t 2℃时,a 、b 、c 三种物质的溶解度按由小到大的顺序排列 就是__________(填写物质序号)。
溶解度/g 2040600
t t A
B
C
溶解度曲线的意义及其应用 溶解度曲线的意义与应用可从点、线、面和交点四方面 来分析。 1.点 溶解度曲线上的每个点表示的是某温度下某种物质的溶 解度。即曲线上的任意一点都对应有相应的温度和溶解度。温度在横坐标上可以找到,溶解度在纵坐标上可以 找到。溶解度曲线上的点有三个方面的作用: (1)根据已知温度查出有关物质的溶解度; (2)根据物质的溶解度查出对应的温度; (3)比较相同温度下不同物质溶解度的大小或者饱和溶液中溶质的质量分数的大小。 2.线 溶解度曲线表示某物质在不同温度下的溶解度或溶解度 随温度的变化情况。曲线的坡度越大,说明溶解度受温 度影响越大;反之,说明受温度影响较小。溶解度曲线也有三个方面的应用: (1)根据溶解度曲线,可以看出物质的溶解度随着温度的变化而变化的情况。 (2)根据溶解 度曲线,比较在一定温度范围内的物质的溶解度大小。(3)根据溶解度曲线,选择分离某些可溶性混合物的方法。 3.面 对于曲线下部面积上的任何点,依其数据配制的溶液为
对应温度时的不饱和溶液;曲线上部面积上的点,依其数据配制的溶液为对应温度时的饱和溶液,且溶质有剩余。如果要使不饱和溶液(曲线下部的一点)变成对应温度下 的饱和溶液,方法有两种:第一种方法是向该溶液中添加溶质使之到达曲线上;第二种方法是蒸发一定量的溶剂。4.交点 两条溶解度曲线的交点表示该点所示的温度下两物质的 溶解度相同,此时两种物质饱和溶液的溶质质量分数也 相同。 例题(98年广西区)X、Y、Z三种固体物质的溶解度曲线见右图。 下列说法中,不正确的是( )。 (A)分别将X、Y、Z的饱和溶液的温度从t ℃降低到t ℃,只有Z无晶体析出 (B) t℃时,用l00克水配制相同质量、相同溶质质量分数的X、Y、Z的溶液,所需溶质质量最多不超过S (C)当X中含有少量Y时,可用结晶法提纯X (D) t℃时,三种物质的饱和溶液中溶质的质量分数XYZ 解析这是一道难度较大的综合选择题,它综合了饱和溶液、不饱和溶液、蒸发结晶、物质的提纯及质量分数与 溶解度的换算等知识。解题的关键是看懂溶解度曲线图 并明确溶解度曲线的意义。
1. A. 10℃时,等质量的甲和乙的饱和溶液中溶质质量相等 2. B. 30℃时,甲物质饱和溶液中,溶质质量分数为60% 3. C. 20℃时,将10g甲物质加入50g水中,得到60g溶液 4. D. 从混有少量乙的甲物质中提取较纯净的甲,最适宜采用冷却热饱和溶液结晶法 答案 B 解析 分析:A、某温度下物质的溶解度相等,则饱和溶液中溶质的质量分数相等,据此计算解答; B、根据饱和时质量分数的计算式×100%分析解答; C、据该温度下甲的溶解度分析解答; D、据甲、乙的溶解度受温度影响情况分析提纯甲的方法. 解答:A、10℃时,甲、乙的溶解度相等,饱和溶液中溶质的质量分数相等,所以等质量的甲和乙的饱和溶液中溶质质量相等,正确; B、30℃时,甲物质的溶解度是60g,所以饱和溶液中,溶质质量分数为×100%<60%,故错误; C、20℃时甲的溶解度大于20g,所以将10g甲物质加入50g水中可完全溶解,得到60g不饱和溶液,正确; D、甲的溶解度受温度影响较大,乙的溶解度受温度影响较小,所以此混有少量乙的甲中提取交纯净的甲,适宜采用冷却热饱和溶液的方法,正确; 故选B. 点评:本题考查了学生对溶解度概念、溶解度曲线知识的运用,能较好培养学生分析、解决问题的能力. 2.如图所示为甲、乙两种固体的溶解度曲线,下列说法错误的是 1. A. 40℃时.甲的溶解度大于乙的溶解度 2. B. 20℃时,甲、乙两种物质的溶解度相等 3. C. 甲、乙两种物质的溶解度都随温度的升高而增大 4. D. 20℃时,把30g甲物质加入100g水中,充分溶解后所得溶液为饱和溶液 答案 C 解析 分析:A、根据某一温度时物质溶解度的比较方法考虑;B、根据曲线中交点的含义考虑;C、根据溶解度曲线观察即可;D、根据20℃时甲的溶解度进行计算即可.解答:A、从40℃向上做垂线,与曲线的交点在上面的溶解度就大,所以40℃时甲的溶解度大于乙的溶解度,故A说法正确; B、曲线中交点表示该温度时两种物质的溶解度相等,所以20℃时,甲、乙两种物质的溶解度相等,故B说法正确; C、由溶解度曲线图可知甲物质的溶解度随温度的升高而增大,乙物质的溶解度随温度的升高而减小,故C说法错误; D、20℃时甲的溶解度是25g,即100g水中最多溶解25g甲物质,所以20℃时,把30g甲物质加入100g水中,只能溶剂25g,所以溶液是饱和溶液,故D说法正确. 故选C. 点评:解答本题关键是要知道溶解度曲线的交点含义,知道溶解度大小的比较方法,知道物质溶于水所得溶液质量需要根据溶解度进行分析.
初三化学溶解度曲线知识点(完整)
溶解度t/℃ 21m m 溶解度曲线知识点 一、正确理解溶解度曲线的含义 溶解度曲线就是在直角坐标系中,用来描述物质的溶解度随温度变化而变化的曲线。根据溶解度曲线可进行溶液的配制,混合物的分离与提纯,以及进行物质结晶或溶解的计算。下面,我们从溶解度曲线的特点入手,对溶解度作进一步的理解。 (一)点 1.曲线上的点:表示对应温度下该物质的溶解度。如:下图中a 表示A 物质在t 1℃时溶解度为m 1g 。 2.曲线上方的点:表示在对应温度下该物质的饱和溶液中存在不能继续溶解的溶质。如:图中b 表示在t 1℃时,A 的饱和溶液中有(m 2-m 1)g 未溶解的溶质。
3.曲线下方的点:表示在对应温度下该物质的不饱和溶液。如:图中C 表示在t 1℃时,A 的不饱和溶液中,还需要加入(m 1-m 3)g A 物质才达到饱和。 4.曲线交点:表示在对应温度下不同物质的溶解度相同。如图中d 表示在t 2℃,A 、B 两物质的溶解度都为m 4g 。 (二)线 如图中A 物质的溶解度随温度升高而明显增大,A 曲线为“陡升型”。如KNO 3等大多数固体物质。 图中B 物质的溶解度随温度变化不大,B 曲线为“缓升型”,如NaCl 等少数固体物质。 图中C 物质的溶解度随温度升高而减小,C 曲线为“下降型”,如气体及Ca(OH)2等极少数固体物质。 二、掌握溶解度曲线的应用 溶解度
1.溶解度曲线上的每一点,代表着某温度下某物质的溶解度,因此利用溶解度曲线可以查出某物质在不同温度下的溶解度,并根据物质的溶解度判断其溶解性。 2.可以比较在同一温度下不同物质溶解度的相对大小。 3.根据溶解度曲线的形状走向,可以看出某物质的溶解度随温度的变化情况。并根据此情况可以确定从饱和溶液中析出晶体或进行混合物分离提纯的方法。例如:某物质的溶解度曲线“陡”,表明该物质溶解度随温度变化明显,提纯或分离该物质时适合采用降温结晶法。某物质溶解度曲线“平缓”,提纯或分离该物质时适合采用蒸发溶剂法。 4.从溶解度曲线上的交点,可以判断哪些物质在该点所示的温度下具有相同的溶解度。 5.利用溶解度曲线可以确定一定质量的某物质的饱和溶液降温时析出晶体的质量。
中考化学溶解度及溶解度曲线专题复习 1. X 、Y 、Z三种物质的溶解度曲线如图所示。将t2℃ 时三种物质的饱和溶液降 温至t1℃ ,溶液中溶质质量分数大小关系正确的是 ( 第1题图 A.X>Y>Z B.Y>Z>X C.Z>Y>X D.X=Y>Z 【答案】B 2.我国古代劳动人民常将草木灰(主要成分K2CO3和生石灰在水中混合,用上层清 液漂白丝帛。清液的主要成分及溶解度如图所示。 (1)t1 ℃时3种物质的饱和溶液中溶质质量分数由小到大的顺序是。 (2)20 ℃时,向4个盛有50 g水的烧杯中,分别加入一定质量的氢氧化钾并充 分溶解。4组实验数据如下: 实验序号 A B C D 加入氢氧化钾的质量 7 14 56 70 /g
溶液质量/g 57 64 106 106 第2题图 由上述实验数据可知: ① 所得溶液是不饱和溶液的是(填序号); ②20℃时,将C继续恒温蒸发25 g水,过滤,得到质量为 g的固体。 【答案】(1)Ca(OH2 KOH K2CO3 (2 ①AB ② 28 3.下表是Ca(OH2 和NaOH的溶解度数据。请回答下列问题: 温度/℃0 20 40 60 80 100 溶解度/g Ca(OH2 0.19 0.17 0.14 0.12 0.09 0.08 NaOH 31 91 111 129 313 336
(1)依据上表数据,绘制Ca(OH2 和NaOH的溶解度曲线,下图中能表示NaOH溶 解度曲线的是(填“A”或“B”)。 第3题图 (2)要想把一瓶接近饱和的Ca(OH2溶液变成饱和溶液,可采取措施有(填序 号)。 ① 蒸发水② 升高温度③ 降低温度④ 加入水⑤ 加入氢氧化钙 (3)现有60 ℃时含有Ca(OH2 和NaOH两种溶质的饱和溶液,若要得到较纯净的NaOH晶体,应采取的物理方法是。 (4)现有20 ℃时Ca(OH2的饱和溶液(甲溶液),向其中加入一定量CaO后恢复20 ℃,得到乙溶液,溶液中溶质的质量分数的关系为甲乙(填“>”、“<”或“=”)。 【答案】(1) A ( 2 ①②⑤ (3)冷却热饱和溶液(4) = 4.溶液在生产和生活中有重要意义,某兴趣小组为了研究物质的溶解和结晶,做了如下所述过程的实验:
“溶解度曲线”的意义及应用简析 “溶解度曲线”连续几年都是山西省中考的命题热点,明确其意义并能熟练应用很有必要。下面就溶解度曲线的意义及应用作一个简要的概括和评析,希望能帮助初学者将抽象的问题与图像联系,更好地理解溶解度及相关概念。 溶解度S (克) 一、溶解度曲线的意义 1、确定某物质某温度下的溶解度。 2、判断某物质的溶解度随温度变化的趋势 3、 可以看出改变温度析出的晶体量的多少 如右图所示,高温下溶解度为S 2,低温下为S 1的晶体为S 2-S 1(100克水中)。 4、 判断某点时的溶液是否饱和 从图中明显看出,在曲线上和曲线以上部分所含该物质已等于或大于该温度时的溶解度,此时溶液为饱和溶液,在曲线下则为不饱和溶液。 5、判断饱和溶液和不饱和溶液相互转化的方法 溶解度S (克) 温度 温度 (图一) (图二) 如图一,A 点处表示的是不饱和溶液,若要将其变为饱和溶液,只需从A 点向溶解度曲线引一横一竖两条线,即可看出转化方法:降温和增或加溶质、蒸发溶剂(可理解为相对增加溶质)。反之,从曲线上某一点(饱和)向下向右引两条直线,即可看出由饱和溶液到不饱和溶液转化的方法(图二):升温或增加溶剂(相当于相对地减少溶质)。 6、判断改变温度时,溶液的各量的变化 如上图二,若要判断从饱和溶液A 到B 时溶液中各量的变化情况,可以看由A 到B 那条线上只是改变温度,溶质、溶剂并没有增减。其它经常考查的溶液的质量、溶解度、饱和与否、溶质的质量分数变化也能做出判断,依次为不变、增大、不饱和、不变。 7、比较同一温度下不同物质的溶解度 从该温度处引一条垂直于温度轴的直线与溶解度曲线 有交点,哪个交点在上就表示哪种物质的溶解度大。常常 考查的是(如右图):a 的溶解度比b 的大。但是从图上很 容易看出,因为两图像上升过程中有交点,故两物质溶解度 的大小应为三种情况,交点前一种,交点后一种,交点处二 者相等。 8、交点处的意义 交点表示在此温度下两种物质的溶解度相同。还可以表示在此温度下,两种物质的饱和溶液溶质的质量分数相同。当然,两种物质的饱和溶液若质量相同,所含溶质的质量也相同。 9、判断分离(或提纯)物质的方法 S(g)
溶解度曲线专题复习 溶解度是初中化学中的一个重要概念,溶解度曲线综合题是近年中考的热点题型。这类题目涵盖面广,综合性强。能较好地考查学生的观察能力、获取信息的能力及知识应用能力。是中考化学的重点,也是学生的失分点。在2011年各地中考化学试题中,出现了许多与溶解度曲线相关的试题,现归纳如下,以供参考。 一、溶解度的意义 例1 (2011·嘉兴)将a、b两种物质的饱和溶液升高温度后,发现a溶液有晶体析出,b溶液没有明显现象。再向b溶液加入少许b晶体,晶体消失。则图1中能正确表示a、b两物质溶解度曲线的是() 解析:由题意知a物质的溶解度随温度的升高而减小,而b物质的溶解度随温度的升高而增大,所以同时符合的图像只有选项C。 答案:C 点评:正确理解溶解度曲线的意义,是解答本题的关键。 二、判断或比较溶解度的大小 例2 (2011·四川省眉山市)如图2所示是a、b、c三种物质的溶解度曲线,a与c的溶解度曲线相交于P点。据图回答: (1)P点的含义是。 (2)t1℃时30g a物质加入到50g水中不断搅拌,能形成80g溶液吗(填“能”或“不能”)。 (3)t2℃时,a、b、c三种物质的溶解度按由小到大的顺序排列的是___ (填物质序号)。 解析:(1)在溶解度曲线上两线相交的点表示:在该温度下两种物质的溶解度相同。(2)t1℃时a物质的溶解度为20克,即t1℃时100克水中达到饱和状态时最多能溶解a物质的质量为20克,在50克水中最多能溶解10克,所以只能形成60克溶液。(3)在t2℃线与溶解度曲线的交点越靠上的物质的溶解度越大。所以应是:cba。 答案:(1)在t1℃时,ac的溶解度相等(2)不能(3)cba 点评:本题考查了有关溶解度的一些问题,要理解溶解度的概念,清楚交点的意义。 三、判断晶体的析出 例3 (2011·河北)根据图3所示的溶解度曲线判断,下列说法正确的是() A.甲物质的溶解度大于乙物质的溶解度 B.甲物质的不饱和溶液温度升高后变成饱和溶液 C.将t2℃甲、乙两物质的饱和溶液温度降低到t1℃时都会析出晶体 ℃时,甲物质的饱和溶液和乙物质的饱和溶液中含有相等质量的溶质 解析:A中没有温度限制,所以不能比较甲、乙溶解度;B中甲的溶解度随着温度的升高而增大,所以甲物质的不饱和溶液温度升高之后,还是不饱和溶液;C因为甲乙两物质的溶解度都随着温度的升高而增大,所以饱和溶液降低温度后都会有晶体析出;D中t2℃时两物质的溶解度相同,所以等质量的饱和溶液中含有相等质量的溶质,但是题中并没有说等质量的饱和溶液,所以错了。 答案:C 点评:该题是一个传统题,历年来考的形式基本相同。 例4 (2011·江苏省南通市)固体物质W在水、乙醇两种溶剂中的溶解度随温度变化的曲线,如图4所示。下列说法错误的是( ) A.物质W能溶解在水和乙醇中 ℃时,物质w在水中的溶解度为mg ℃时,物质W在水中与在乙醇中的溶解度相同 D.将t1℃时物质w的饱和水溶液升温至t2℃有晶体析出 解析:A选项中物质W能溶解在水和乙醇中是正确的;B选项中t1℃时,物质w在水中的溶解度为m g是正确的;C选项中t2℃时,物质W在水中与在乙醇中的溶解度曲线相交,说明t2℃时,物质W在水中与在乙醇中的溶解度相同是正确的;D选项根据溶解度曲线的特点,物质W随着温度的升高溶解度增大,将t1℃时物质w的饱和水溶液升温至t2℃时饱和溶液变成不饱和溶液,没有晶体析出。 答案:D 点评:本题主要考查溶解度和溶解度曲线的相关知识,本题的亮点是一种物质溶解在不同的溶剂中,解答本题要明确溶解度概念的“四要素”和溶解度曲线的意义。 四、判断饱和溶液和不饱和溶液的转化 例5 (2011·盐城)如图5为A、B、C三种固体物质(不含结晶水)的溶解度曲线。下列说法错误的是()
溶解度曲线 Document serial number【UU89WT-UU98YT-UU8CB-UUUT-UUT108】
P t ℃ 溶 解 度 姓名 班级 组别 评价 化学导学案 备课人 王国良 上课时间 2月28日 审核人 赵海新 课题 溶解度的表示方法 课型 预习展示 学习目标 1、知道溶解度的涵义和固体溶解度的表示方法。 2、了解温度对固体溶解度的影响以及溶解度曲线的意义。 重点难点 1、固体溶解度的表示方法 2、正确认识溶解性与溶解度的表示联系及区别 。导 学 过 程 教师复 备 【创设情境】 我们知道,固体物质溶解度只受外界因素----温度的影响,我们可以通过实验方法测出物质在不同温度时的溶解度,又该如何表示出来呢 【自主探究】 知识点一:溶解度的表示方法: (一)、列表法:由实验测出不同物质在不同温度下的溶解度,制成表格得到溶解度表。 练习:根据溶解度表格完成下列问题: ①查某物质在某温度时的溶解度或某物质溶解度对应的温度: NaCl 在20℃的溶解度是 ,在100℃时的溶解度是 ; KNO 3在20℃的溶解度是 ,在100℃时的溶解度是 。 溶解度为时,NH 4Cl 饱和溶液所处的温度是 ;溶解度为110g 时,KNO 3 温度℃ 0 10 20 30 40 50 60 70 80 90 10 溶解度 g NaCl KCl NH 4Cl KNO 3 110 138 169 202 246 Ca(OH )2 饱和溶液所处的温度是 。 ②通过对比某物质在不同温度时的溶解度来判断物质溶解度受温度影响情况。 KCl 、NH 4NO 3、KNO 3等大多数物质,溶解度随温度升高而增大; NaCl 等物质溶解度受温度影响较小; Ca(OH)2等少数物质溶解度随温度升高而减小。 ③可以比较同一温度时不同物质溶解度大小。 60℃时,表中几种物质溶解度由大到小的顺序为: 。 过渡:通过溶解度表可快捷、准确查找某些温度时某物质的溶解度,但却不能查出25℃、83℃等指定温度下某物质的溶解度,所以并不能反应出连续温度对应物质的溶解度。 (二)曲线法:用横坐标表示温度,纵坐标表示溶解度,这样上述表格中的某物质溶解度的数据在坐标系中各对应一个点,我们用光滑的线将各点连接起来就成了该物质的溶解度曲线。 如图: 溶解度曲线包含的信息: 1、可知某温度下某物质的溶解度 据图可知50℃时氯化铵NH 4Cl 的溶解度为: 。 2、对比同一温度时不同物 质的溶解度 ①20时硝酸钠、硝酸钾、氯化钠、硼酸、硝酸铵的溶解度由大到小的顺序 为: 。 溶解 P
专题五溶解度曲线 1.a、b两种物质的溶解度曲线如图所示。下列说法不正确的是 A.将t1℃时b的饱和溶液加水可变为不饱和溶液 B.将t2℃时a的饱和溶液降温至t1℃,溶液质量不变 C.t2℃时,两种物质的饱和溶液中溶质质量分数a>b D.将t2℃时a、b的饱和溶液分别降温至t1℃,两溶液的溶质质量分数相等 2.下图是甲、乙、丙三种固体物质的溶解度曲线,下列说法错误的是 A.t2℃时,甲、乙两种物质的溶解度相等 B.甲的溶解度随温度的升高而增大 C.分别将t3℃时甲、乙、丙的饱和溶液降温至t1℃,则所得的三种溶液中溶质的质量分 数大小关系是乙>甲>丙 D.t1℃时,丙的饱和溶液中溶质的质量分数为40% 3.下图是甲、乙、丙三种固体物质的溶解度曲线,将甲、乙、丙三种物质t2℃时的饱和溶液 降温至t1℃,所得溶液的溶质质量分数关系正确的是 A.甲>乙>丙 B.甲=乙=丙 C.甲=乙>丙 D.丙>甲=乙 4.(多选)甲、乙两固体物质的溶解度曲线如图所示,下列说法正确的是 A.t1℃时,甲物质的溶解度为20g B.t1℃时,30g甲加入到50g水中最多可得70g溶液 C.t2℃时,乙物质的饱和溶液升温变成不饱和溶液 D.t2℃时,甲乙两物质的饱和溶液分别降温到t1℃时,所得溶液溶质质量分数的大小关 系是:甲<乙 5.(多选)甲、乙两种固体物质的溶解度曲线如图所示。20℃时,进行了如下图所示的实验,
下列叙述正确的是 A.甲的溶解度大于乙的溶解度 B.实验过程中,属于不饱和溶液的是A溶液和C溶液 C.实验过程中,只有B溶液和D溶液属于饱和溶液 D.实验过程中,B溶液与E溶液中溶质的质量分数相同 6.(多选)甲、乙、丙三种不含结晶水的固体物质的溶解度曲线如图所示,下列说法中正确 的是 A.t2℃时将50g甲物质放入50g水中,充分搅拌后得到100g甲溶液 B.t2℃时配制等质量的三种物质的饱和溶液,甲所需要的水最少 C.分别将t2℃时三种物质的饱和溶液降温到t1℃,所得溶液中溶质的质量分数的大小关 系是乙>甲>丙 D.分别将t2℃时三种物质的饱和溶液降温到t1℃,甲溶液中析出的晶体最多丙溶液中无 晶体析出 7.甲、乙、丙三种物质的溶解度曲线如下图所示。据图回答: (1)50℃时,乙物质的溶解度是 g; (2)30℃时,三种物质的溶解度由大到小的顺序为; (3)要使接近饱和的丙物质溶液变为饱和,可采取的一种措施是; (4)当溶液的浓度都用溶质的质量分数(m)表示时,下列说法中不正确的
溶解度曲线图试题题型 总结 Document serial number【UU89WT-UU98YT-UU8CB-UUUT-UUT108】
正确的说法: 1、t2℃时,甲、乙两饱和溶液溶质质量分数相等, 2、甲、乙饱和溶液变为不饱和溶液,可升温。而丙的饱和溶液变为不 饱和溶液,可降温。 3、t2℃时,甲、乙两种物质各50g分别加入到100g水中,充分溶解 得到溶液质量都是140g。 4、t2℃时,质量相同的甲、乙饱和溶液分别升温至t3℃,为达到饱 和状态需要加入甲的质量大于乙。 5、当甲中混有少量乙时可用降温结晶的方法提纯。 6、若要将N点的甲溶液转变为M点的甲溶液,可在恒温条件下采用蒸 发溶剂法。 7、分别将t3℃时,甲、乙、丙的饱和溶液降温至t1℃,则所得三种 溶液中溶质质量分数大小关系:乙>甲>丙。 不正确的说法:
1、t3℃时,甲、乙两饱和溶液的溶质质量相等。 2、将乙的溶液由t3℃降低到t2℃,乙溶液中一定有固体析出。 3、t3℃时,将甲、乙的饱和溶液降温到t2℃时,析出晶体的质量一定大于乙。 4、将甲、乙、丙的饱和溶液从t3℃降温到t2℃溶液中均有固体析出。 5、t3℃时,甲、乙、丙三种物质的饱和溶液中溶质质量由大到小的顺 序是:甲>乙>丙。 6、t3℃时,甲溶液的溶质质量分数一定大于乙溶液的溶质质量分数。 7、t3℃时,将47g甲完全溶于100g水中,得到甲的饱和溶液。 8、t2℃时,甲、乙饱和溶液的溶质质量分数都为40%。 9、t2℃时,甲、乙的饱和溶液分别降温至t0℃,甲溶液饱和,乙溶液不饱和。 10、t3℃时,甲、乙、丙三种物质的饱和溶液,分别蒸发相等质量的水 后恢复到t3℃,析出溶质质量:丙>乙>甲。 11、将t2℃时,甲、乙、丙三种物质的饱和溶液降温至t1℃时,所得溶 液溶质质量分数关系是:乙>甲=丙。
【考纲说明】 掌握有关溶解度的意义与图像分析。 1、掌握溶解度的影响因素。 2、本章节所占分值为4~5分 【趣味链接】 2006年5月,江油市华超建筑集团向四川省广元市合瑞化工有限公司签订合同,购买生石灰635吨,每吨300元,运输由华超集团负责,收货后付款。合瑞公司发货时,过一次称,华超集团收货时,再在地磅房过一次磅,总误差不能大于5吨。开始时,一切顺利。可后来华超集团的技术人员发现,车队运回来的不是生石灰——氧化钙CaO,而是熟石灰——氢氧化钙Ca(OH)2,便打电话问是怎么回事。合瑞公司回答说:“这几天连续下雨,你们的卡车又没有篷布,可能在运输过程中遭了雨淋。反正你们建房时还要往生石灰里加水,总不能直接用生石灰抹墙吧。”华超集团想想也是,就继续收货。因为他们知道,CaO+H2O(水)=Ca(OH)2,而工地使用的就是加水搅拌了的熟石灰。 货物收完后,华超集团发现,所收的货物为635吨,不多不少,正好。可是别忙,技术人员指出,生石灰变成熟石灰时,重量要增加。原来,生石灰的相对分子质量是56,熟石灰的相对分子质量是74,也就是说,1吨生石灰与水反应能生成74/56=1.32吨熟石灰。收了635吨熟石灰,说明合瑞公司只发了635/1.32=481吨生石灰!华超集团打电话说只付481吨生石灰的货款14万元。凭空少了5万。 【知识梳理】 一、溶解度 1、固体的溶解度 (1)溶解度的定义:在一定温度下,某固态物质在100g溶剂里达到饱和状态时所溶解的质量 四要素: ①条件:一定温度②标准:100g溶剂③状态:达到饱和④质量:溶解度的单位:克 (2)溶解度的含义: 20℃时NaCl的溶液度为36g含义: 在20℃时,在100克水中最多能溶解36克NaCl 或在20℃时,NaCl在100克水中达到饱和状态时所溶解的质量为36克 (3)影响固体溶解度的因素:①溶质、溶剂的性质(种类)②温度 大多数固体物的溶解度随温度升高而升高;如KNO 3
溶解度曲线的意义及应用 一、溶解度曲线的概念 在直角坐标系中,用横坐标表示温度(t),纵坐标表示溶解度(S),由t—S的坐标画出固体物质的溶解度随温度变化的曲线,称之为溶解度曲线。 二、溶解度曲线的意义 1、点曲线上的点叫饱和点,①曲线上任一点表示对应温度下(横坐标)该物质的溶解度(纵坐标);②两曲线的交点表示两物质在交点的温度下溶解度相等。 2、线溶解度曲线表示物质的溶解度随温度变化的趋势。其变化趋势分为三种: ①陡升型大多数固体物质的溶解度随温度升高而增大,如KNO3; ②缓升型少数物质的溶解度随温度升高而增幅小,如NaCl; ③下降型极小数物质的溶解度随温度升高而减小,如Ca(OH)2。 3、面⑴溶解度曲线下方的面表示不同温度下该物质的不饱和溶液。 ⑵溶解度曲线上方的面表示相应温度下的过饱和溶液(不作要求)。 三、溶解度曲线的应用 1.判断或比较某一物质在不同温度下溶解度的大小。 例1:(2010?南昌)右图为氯化钠、碳酸钠(俗称纯碱) 在水中的溶解度曲线。 (1)当温度为10℃时,碳酸钠的溶解度为; (2)当温度时,氯化钠的溶解度大于碳酸钠的溶解 度; (3)生活在盐湖附近的人们习惯“夏天晒盐,冬天捞碱”。 请你解释原因:“夏天晒盐”。 例2、(2009?泰州)右图是A、B两种物质的溶解度曲线,根据图示回答下列问题: ℃时,向两只盛有100g水的烧杯中,分别加 (1)t 入A、B两种物质至不能溶解为止,所得溶液的溶质 质量分数较大的是___________溶液(填“A”或“B””)。 (2)t2℃时,欲配制等质量的A、B两种物质的饱 和溶液,所需水的质量关系是A________B。(填写 “>”、“<”或“=”,下同) (3)将t2℃的A、B两种物质的饱和溶液各200g, 降温至t1℃,析出晶体的质量关系是A______B。 (4)将t2℃的A、B两种物质的饱和溶液各200g,升温至t3℃,欲使它们仍为饱和溶液,若不改变溶剂质量,所需加入固体溶质的质量关系是A_______B。
16溶解度曲线与溶液的稀释 姓名:___________班级:___________考号:___________ 一、单选题 1.(2019·锦州)T℃时,向盛有100g水的两烧杯中分别加入60g甲、乙两种固体,搅拌后固体甲完全溶解,放置一段时间后,甲溶液中有固体析出,溶解度曲线如图所示。下列说法正确的是() A.搅拌的目的是增大物质的溶解度 B.将T℃的甲、乙两种饱和溶液降温,溶质质量分数都减小 C.甲溶于水的过程中一定放出热量 D.乙是可溶性物质 【答案】C 【解析】本题主要考察溶解度曲线图的相关知识 A、搅拌的目的是加速溶解,不能增大溶解度;故选项错误; B、将T℃的甲、乙两种饱和溶液降温,甲溶液溶质质量分数减小,乙溶液溶质质量分数不变;故选项错误; C、T℃时,向盛有100g水的两烧杯中加入60g甲固体,全部溶解,放置一段时间后,甲溶液中有固体析出,结合溶解度曲线图,可知甲物质溶于水一定是放出热量;故选项正确; D、由溶解度曲线图可知:20℃时,乙物质的溶解度大于10g,乙物质是易溶性物质;故选项错误;故选:C。 2.(2019·铁岭)常温下,对100mL氯化钠饱和溶液进行图示实验。下列错误的是()
A.实验1后,甲、乙中溶液的溶质质量分数相等 B.实验2后,乙中比甲中氯化钠的溶解度大 C.实验2后,甲中溶液为氯化钠的不饱和溶液 D.实验2后,甲、乙中溶液所含溶质质量相等 【答案】B 【解析】A、实验1后,甲、乙中溶液的溶质质量分数相等正确,故A正确; B、实验2后,乙中比甲中氯化钠的溶解度大错误,因为温度不变,溶解度不变,故B 不正确; C、实验2后,甲中溶液为氯化钠的不饱和溶液正确,因为加入了溶剂,故C 正确; D、实验2后,甲、乙中溶液所含溶质质量相等正确,因为乙中的溶质不再溶解,故D正确。故选B。 3.(2019·安徽)A、B两种固体物质的溶解度曲线如图所示,下列说法正确的是() A.恒温蒸发溶剂的方法不可以使B得到饱和溶液析出晶体 B.将t2℃时A、B的饱和溶液分别降温至t1℃,A成为不饱和溶液 C.t2℃时,用等质量的A、B分别配制成饱和溶液,所得溶液的质量A>B D.t2℃时,将150g A的饱和溶液稀释成质量分数为20%的溶液,需水100g 【答案】D
溶解度曲线及其应用 1.溶解度曲线上每一点表示该物质在不同温度下的不同的溶解度。 2.溶解度曲线上的任意一点表示在该温度下某物质的溶解度是多少克。 3.不同物质溶解度曲线的交点处,表示不同物质在相对应的同一温度下的溶解度相同。 4.溶解度曲线上方的一点,表示在指定温度下,溶液中的溶质质量已超过该物质的溶解度,溶液是过饱和的;溶解度曲线下方的一点,表示在指定温度下,溶液中溶质质量还没有达到溶解度的量,溶液是不饱和的。 5.溶解度曲线的特征是: (1)大部分固体物质的溶解度曲线左低右高,溶解度随温度的升高而增加; (2)少数固体物质的溶解度曲线较平缓,溶解度受温度的影响小,如食盐; (3)极少数固体物质的溶解度曲线是左高右低,溶解度随温度的升高而降低,如熟石灰。 6.溶解度曲线的应用: (l)由已知温度查某物质对应的溶解度; (2)由物质的溶解度查该物质所处的温度; (3)比较同一温度下不同物质的溶解度; (4)设计混合物分离或提纯的方法,例如提纯NaCl可用蒸发溶剂法,分离NaCl 和NaNO3可用降温结晶法。 下面举一例来说明溶解度曲线的应用。 图中曲线a、b、c分别表示a、b、c三种物质的溶解度曲线,试回答: (1)t1℃时,a、b、c溶解度大小的顺序是______。 (2)m点表示在t3℃下,a溶液是______溶液,b溶液是______溶液,c溶液是______ 溶液。 (3)n点表示在t2℃时,______和______物质的______相同。 (4)在t3℃时,a、b、c分别在50g水里达到饱和,冷却到t1℃,析出晶体最多的是______。 (5)从a的热饱和溶液中提取a最好的方法是______;要从c溶液中提取c最好采用的方法是______。 (6)为了从混有少量的c物质的a物质的溶液中提取纯净的a可采用的方法是______。 溶解度练习题 一、溶液的形成 1、溶液 (1)溶液的概念: (2)溶液的基本特征:均一性、稳定性 注意:a、溶液不一定无色,如CuSO4溶液为蓝色FeSO4溶液为浅绿色Fe2(SO4)3溶液为黄色
溶解度/g t/℃ 21O m 3 m 4 m 1 m 2 B c a b A 溶解度的定义:在一定温度下,某固态物质在100g 溶剂里达到饱和状态时所溶解的质量。 影响固体溶解度的因素: 1:溶质、溶剂的性质种类 2:温度 大多数固体物的溶解度随温度升高而升高。如硝酸钾。 少数固体物质的溶解度受温度的影响很小。如氯化钠。 极少数物质的溶解度随温度升高而降低。如氢氧化钙。 结晶的两种方法:蒸发溶剂、降低温度 饱和和不饱和之间的相互转化: 1、 溶解度曲线点 ①曲线上的点:表示对应温度下该物质的溶解度。如:下图中a 表示A 物质在t 1℃时溶解 度为m 1g 。 曲线上方的点:表示在对应温度下该物质的饱和溶液中存在不能继续溶解的溶质。如:图中b 表示在t 1℃时,A 的饱和溶液中有(m 2-m 1)g 未溶解的溶质。 曲线下方的点:表示在对应温度下该物质的不饱和溶液。如:图中C 表示在t 1℃时,A 的不饱和溶液中,还需要加入(m 1-m 3)gA 物质才达到饱和。 ②曲线交点:表示在对应温度下不同物质的溶解度相同。如图中d 表示在t 2℃,A 、B 两物质的溶解度都为m 4g 。 2、溶解度曲线线 溶解度/g C B A O
如图中A物质的溶解度随温度升高而明显增大,A曲线为“陡升型”。如KNO3等大多数固体物质: 图中B物质的溶解度随温度变化不大,B曲线为“缓升型”,如NaCl等少数固体物质。 图中C物质的溶解度随温度升高而减小,C曲线为“下降型”,如气体及Ca(OH)2等极少数固体物质。 1 如图分别表示甲、乙两种物质的溶解度曲线,下列说法不正确的是 A.t1℃时,甲的溶解度小于乙的溶解度 B.M点处甲、乙的溶解度相等 C.t1℃时,向盛有50 g水的烧杯中加入22 g甲,充分溶解后所得的溶液为饱和溶液 D.t2℃时,甲、乙饱和溶液的溶质质量分数为:甲<乙 2 如图是甲、乙两种固体的溶解度曲线,下列说法正确的是 A.甲的溶解度等于乙的溶解度 B.升高温度可以将甲的不饱和溶液变为饱和溶液 C.20 ℃时,100 g乙的饱和溶液中溶质质量是30 g D.40 ℃时,分别用100g水配制甲、乙的饱和溶液,所需甲的质量大于乙的质量 3 右图是甲、乙、丙三种物质的溶解度曲线,将甲、乙、丙三种物质t l℃时的饱和溶液升温至t2℃,所得溶液的溶质质量分数关系正确的是 A.甲>乙>丙 B.甲=乙=丙 C.甲=乙>丙 D.丙>甲=乙 4 甲、乙两种物质的溶解度曲线如图所示.下列叙述正确的是()
溶解度曲线中考试题解析 【知识点的认识】 所谓固体溶解度曲线如图所示: 就是用纵坐标表示溶解度(用字母S表示,单位为克/g),横坐标表示温度(用字母t表示,单位为℃),根据物质在不同温度时的溶解度不同,画出的物质溶解度随温度变化的曲线。固体溶解度曲线的作用可从点、线、面和交点四方面来理解。具体如下: 1.点,溶解度曲线上的每个点(即饱和点)表示的是某温度下某种物质的溶解度。即曲线上的任意一点都对应有相应的温度和溶解度。温度在横坐标上可以找到,溶解度在纵坐标上可以找到。溶解度曲线上的点有三个方面的作用: (1)根据已知的温度可以查出有关物质的溶解度; (2)根据物质的溶解度也可以查出它所对应的温度; (3)可以判断或比较相同温度下,不同物质溶解度的大小(或饱和
溶液中溶质的质量分数的大小)。 2.线,溶解度曲线表示某物质在不同温度下的溶解度或溶解度随温度的变化情况。曲线的坡度越大,说明溶解度受温度影响越大;反之,说明受温度影响较小。溶解度曲线也有三个方面的应用: (1)根据溶解度曲线,可以看出物质的溶解度随着温度的变化而变化的情况。一般规律是:大部分固体随温度升高溶解度增大,如硝酸钾;只有少数固体溶解度受温度影响不大,如食盐(氯化钠);极少数物质溶解度随温度升高反而减小,如熟石灰。 (2)根据溶解度曲线,判断或比较某一物质在不同温度下的溶解度大小。 (3)根据溶解度曲线,选择分离、提纯某些可溶性混合物的方法(即选用蒸发结晶还是降温结晶);并且,还可以判断或比较析出晶体的质量大小(即曲线越陡,析出的晶体就越多)。 3.面,对于曲线下部面积上的任何点,依其数据配制的溶液为对应温度时的不饱和溶液;曲线上部面积上的点,依其数据配制的溶液为对应温度时的饱和溶液,且溶质有剩余。如果要使不饱和溶液(曲线下部的一点)变成对应温度下的饱和溶液,方法有两种:第一种方法是向该溶液中添加适量的溶质使之到达曲线上;第二种方法是蒸发掉过量的溶剂。 3.交点,两条溶解度曲线的交点表示该点所示的温度下,两物质的溶解度是相同的;并且,此时两种物质饱和溶液的溶质质量分数也相同的。 【命题方向】
溶解度曲线的应用 1、两种不同物质在不同温度区间,溶解度大小比较 例1:温度在 时 a 物质的溶解度大于b 物质的溶解度; 温度在 时 a 物质的溶解度等于b 物质的溶解度; 温度在 时 a 物质的溶解度小于b 物质的溶解度; 例2:物质a 的溶解度大于物质b 的溶解度 这句话对吗? 2、两种可溶物质的分离与提纯所采取不同的方法 例题 (10邵阳13)右图表示的是a 、b 两种固体物质的溶解度曲线,下列叙述正确的是 ( ) A. a 的溶解度大于b 的溶解度 B .a 、b 两物质的溶解度受温度影响都很小 C. 在t ℃时,a 、b 两物质的饱和溶液中溶质质量分数相等 D. 当b 中含少量a 时,可用冷却热饱和溶液的方法提纯b 见D 选项,要讲解: ① 大量的a 中含有少量的b ② 大量的b 中含有少量的a ③ 如右图中,大量A 中含少量的B 3、明白溶解度曲线上面点、上方点、下方点的含义 例题: ① 溶解度曲线上面点P 点表示饱和溶液 ② 溶解度曲线上方点C 点表示过饱和溶液 ③ 溶解度曲线下方点B 点表示不饱和溶液 4、通过比较溶解度的大小,数的大小。 例1、如图是A 、B 、C ① t 1℃时,A 、B 、C (填写序号,下同) ② t 2℃时,A 、B 、C 是 ______ ;(填写序号,下同) 要掌握简单的溶解度计算,判断实际溶液是饱和溶液还是不饱和溶液; ③ t 1℃时,30g A 物质加入到50g 水中不断搅拌,形成溶液的质量是 g ;此时是______溶液 要注意:饱和溶液溶质质量分数按此时的溶解度来计算、比较大小,不饱和溶液则要将原原温度下的溶解度数值进行平移过来,再比较此时溶解度的大小,即是此时溶质质量分数的大小。 ④ 将t 1℃时A 、B 、C 三种物质饱和溶液的温度升高到t 2℃时,三种溶液的溶质的质量分数由大到小的顺序是 。 例题2、a 、b 、c 三种物质的溶解度曲线如图6-11所示。现有t 1℃时的a 、b 、c 三种物质的饱和溶液,将其都升温至t 2℃时,下列说法错误的是 ( ) A .c 溶液中有晶体析出 B .a 、b 溶液均为不饱和溶液 C .c 溶液中溶质的质量分数变小 D .a 溶液中溶质的质量分数最大 5、温度对不同物质溶解度影响的程度的三种情况及相关题型。 ①物质的溶解度随温度的变化影响较大;曲线比较陡峭;例如硝酸钾、硝酸铵等物质; ②物质的溶解度随温度的变化影响不大;曲线比较平直;例如氯化钠、氯化钾等 ③ 物质的溶解度随温度的升高反而减小。反常物质。例如氢氧化钙。 【应用】 某物质由不饱和与饱和相互转化时,所采用的不同方法;是升温析出晶体还是降温析出晶体;谁析出的晶体多;两种可溶物质的分离应采用的正确方法; 例题3、右图是a 、b 、c 三种物质(均不含结晶水)的溶解度曲线,请你回答: (1)0℃时,a 、b 、c 三种物质中溶解度最大的是 ______; (2)将t 1℃时三种物质的饱和溶液升温至t 2℃时,有晶体析出的是______; (3)t 2℃时,将30g a 物质加入到50g 水中充分溶解,所形成溶液的质量是______g ; (4)将t 2℃时a 、b 、c 三种物质饱和溶液的温度降温到t 1℃时,三种溶液的溶质质量分数大小关系是_____________; (5)将t 1℃时a 、b 、c 三种物质饱和溶液的温度升温到t 2℃时,三种溶液的溶质质量分数大小关系是_____________; 例题4、如图是甲、乙、丙三种物质(均不含结晶水)的溶解度曲线.现有t 2℃时甲、乙、丙三种物质的饱和溶液(无固体存在),请根据下图回答: (1)t 1℃时,将三种饱和溶液分别恒温蒸发相同质量的水,析出晶体最多的是 ______; (2)将三种饱和溶液分别从t 2℃降温到t 1℃时,所得溶液中溶质的质量分数由大到小的顺序为___________; (3)当甲中含有少量的丙时,可用________方法提纯甲.
溶解度曲线中考试题解析 一、溶解度的意义 例1 (2011·嘉兴)将a、b两种物质的饱和溶液升高温度后,发现a溶液有晶体析出,b溶液没有明显现象。再向b溶液加入少许b晶体,晶体消失。则图1中能正确表示a、b 两物质溶解度曲线的是() 解析:由题意知a物质的溶解度 随温度的升高而减小,而b物质的溶 解度随温度的升高而增大,所以同时 符合的图像只有选项C。 答案:C 点评:正确理解溶解度曲线的意义,是解答本题的关键。 二、判断或比较溶解度的大小 例2 (2011·四川省眉山市)如图2所示是a、b、c三种物质的溶解度曲线,a与c 的溶解度曲线相交于P点。据图回答: (1)P点的含义是。 (2)t1℃时30g a物质加入到50g水中不断搅拌,能形成80g溶液 吗?(填“能”或“不能”)。 (3)t2℃时,a、b、c三种物质的溶解度按由小到大的顺序排列的是___ (填物质序号)。 解析:(1)在溶解度曲线上两线相交的点表示:在该温度下两种物质的溶解度相同。(2)t1℃时a物质的溶解度为20克,即t1℃时100克水中达到饱和状态时最多能溶解a物质的质量为20克,在50克水中最多能溶解10克,所以只能形成60克溶液。(3)在t2℃线与溶解度曲线的交点越靠上的物质的溶解度越大。所以应是:cba。 答案:(1)在t1℃时,ac的溶解度相等(2)不能(3)cba 点评:本题考查了有关溶解度的一些问题,要理解溶解度的概念,清楚交点的意义。 三、判断晶体的析出
例3 (2011·河北)根据图3所示的溶解度曲线判断,下列说法正确的是() A.甲物质的溶解度大于乙物质的溶解度 B.甲物质的不饱和溶液温度升高后变成饱和溶液 C.将t2℃甲、乙两物质的饱和溶液温度降低到t1℃时都会析出晶 体 D.t2℃时,甲物质的饱和溶液和乙物质的饱和溶液中含有相等质量 的溶质 解析:A中没有温度限制,所以不能比较甲、乙溶解度;B中甲的溶解度随着温度的升高而增大,所以甲物质的不饱和溶液温度升高之后,还是不饱和溶液;C因为甲乙两物质的溶解度都随着温度的升高而增大,所以饱和溶液降低温度后都会有晶体析出;D中t2℃时两物质的溶解度相同,所以等质量的饱和溶液中含有相等质量的溶质,但是题中并没有说等质量的饱和溶液,所以错了。 答案:C 点评:该题是一个传统题,历年来考的形式基本相同。 例4 (2011·江苏省南通市)固体物质W在水、乙醇两种溶剂中的溶解度随温度变化的曲线,如图4所示。下列说法错误的是( ) A.物质W能溶解在水和乙醇中 B.t1℃时,物质w在水中的溶解度为mg C.t2℃时,物质W在水中与在乙醇中的溶解度相同 D.将t1℃时物质w的饱和水溶液升温至t2℃有晶体析出 解析:A选项中物质W能溶解在水和乙醇中是正确的;B选项中t1℃时,物质w在水中的溶解度为m g是正确的;C选项中t2℃时,物质W在水中与在乙醇中的溶解度曲线相交,说明t2℃时,物质W在水中与在乙醇中的溶解度相同是正确的;D选项根据溶解度曲线的特点,物质W随着温度的升高溶解度增大,将t1℃时物质w的饱和水溶液升温至t2℃时饱和溶液变成不饱和溶液,没有晶体析出。 答案:D 点评:本题主要考查溶解度和溶解度曲线的相关知识,本题的亮点是一种物质溶解在不同的溶剂中,解答本题要明确溶解度概念的“四要素”和溶解度曲线的意义。
固体的溶解度及溶解度曲线 (2005)5.许多同学喜欢吃家庭腌制的小菜,腌制小菜的一般方法是:将食盐、香料等一起放入水中煮制得浓盐水,盐水冷却后放入洗净待腌制的鲜菜,腌制过程中还要不断打开缸盖晒缸并及时补充食盐,一段时间后,即得成品小菜。若室温时食盐的溶解度为36 g。关于小菜腌制过程中的下列说法,错误的是( ) A.煮制浓盐水时,10 kg水最多可得到浓盐水13.6 kg B.腌菜的过程中,原来的浓盐水会逐渐变稀 C.晒缸的目的一是防止腌菜腐败变质,二是促使水分蒸发以保持盐水的浓度 D.补充食盐的目的是保持盐水的浓度,以利于食盐往蔬菜中渗透(2006)4.(3分)氯化钠和硝酸钾两种物质的溶解度随温度(0~100 ①若两物质的溶解度相等,此时所对应的温度范围在 之间; ②20℃时,氯化钠饱和溶液的质量分数硝酸钾饱和溶液的质量分数(填“>”、“<”或“=”); ③某同学欲从含有少量氯化钠的硝酸钾中分离出硝酸钾,他应采取的方法是 。 (2007)16.右图是A、B两物质的溶解度曲 线,分别得到的下列信息中,正确的是 A.图中阴影部分表明A、B两溶液都是饱和 溶液 B.t1℃时,A、B两饱和溶液的溶质质量分数 相等 C. t2℃时,B物质的溶解度大于t1℃时A物 质的溶解度 D. t2℃时,等质量的A、B两饱和溶液降温到t1℃时析出溶质的质量相同
(2008)4.(4分)右图是A、B两种固体物质的溶解度 曲 线。请分析曲线中A、B两种物质溶解度随温度的变化 情况后,回答下面问题: (1)我们一般将20℃时溶解度大于l0g的物质称为 易溶物质,小于l0g的物质称为可溶物质。那么,B物质 应属于; (2)比较A、B两种物质的溶解度曲线,可看出A、 B两物质溶解性的共同点是; (3)有同学认为“同一温度时,可配得质量分数相同的A、B两种物质的饱和溶液”。你的观点是,理由是 (2009)(2)(5分)控制变量是科学探究的重要方法之一。小华同学实验中发现:把质量相等的不同物质放入同样一杯水中,有的溶解快,有的溶解多,有的溶解又快又多。是哪些因素影响着物质溶解的快慢与多少呢? 请你参考下表硝酸钾的溶解度随温度的变化关系,以硝酸钾为 影响因素: ②实施方案: ③通过实验得出。实验中,控制不变的因素是。(2010)17.室温下,称取氯化钠和碳酸钠各30g放入同一烧杯中,加入lOOg水充分搅拌后静置,得到二者的混合溶液。请参照氯化钠、碳酸钠两物质的溶解度表判断,以下结论不正确的是 A.20℃时,氯化钠的溶解度大于碳酸钠的溶解度 B.20℃时,未溶解固体是氯化钠和碳酸钠的混合物 C.30℃时,溶液中氯化钠和碳酸钠的质量分数相同 D.30℃时,溶液为氯化钠和碳酸钠的不饱和溶液