特殊细菌药敏试验的规范化操作
一、目前我国细菌药敏试验现状
20年以来,我国在卫生部和各地临床检验中心和检验学会的共同努力下引进CLSI药敏系列标准,使全国微生物实验室能在同一标准下进行质量控制活动。当前,微生物实验室对常见临床分离细菌的药物敏感试验的水平已有了显著的提高,但对特殊细菌的药敏试验的各个环节的规范操作还不能得到普及,对目前还无折点的细菌能否做药敏试验,以及如何判断细菌的药物敏感和耐药,仍然概念模糊,有待进一步规范和普及。
目前常见错误做法:
(一)铜绿假单孢菌的药敏判断标准用于其他非发酵细菌;嗜血杆菌的标准用于卡他莫拉菌等的错误做法时有发生。
(二)借用同属细菌敏感标准
(三)借用同类抗生素的敏感标准
二、各菌属的药物敏感性报告及试验方法的CLSI药敏标准
(一)“嗜麦芽”菌属药敏报告标准
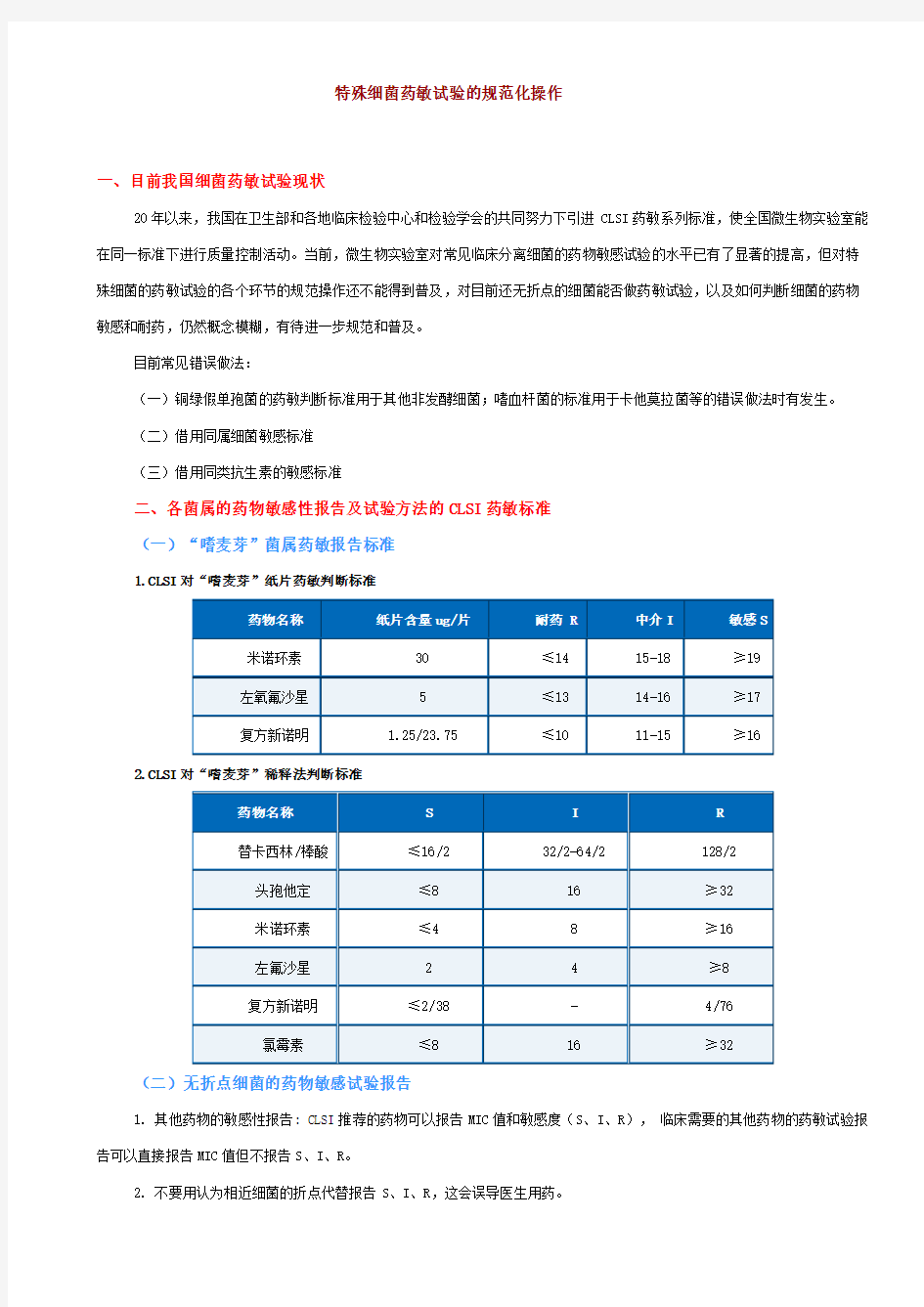
1.CLSI对“嗜麦芽”纸片药敏判断标准
药物名称纸片含量ug/片耐药 R 中介I 敏感S
米诺环素30 ≤1415-18 ≥19
左氧氟沙星 5 ≤1314-16 ≥17
复方新诺明 1.25/23.75 ≤1011-15 ≥16
2.CLSI对“嗜麦芽”稀释法判断标准
药物名称S I R
替卡西林/棒酸≤16/232/2-64/2 128/2
头孢他定≤816 ≥32
米诺环素≤48 ≥16
左氟沙星 2 4 ≥8
复方新诺明≤2/38- 4/76
氯霉素≤816 ≥32(二)无折点细菌的药物敏感试验报告
1. 其他药物的敏感性报告: CLSI推荐的药物可以报告MIC值和敏感度(S、I、R),临床需要的其他药物的药敏试验报告可以直接报告MIC值但不报告S、I、R。
2. 不要用认为相近细菌的折点代替报告S、I、R,这会误导医生用药。
(三)洋葱伯克霍德菌的药物敏感试验
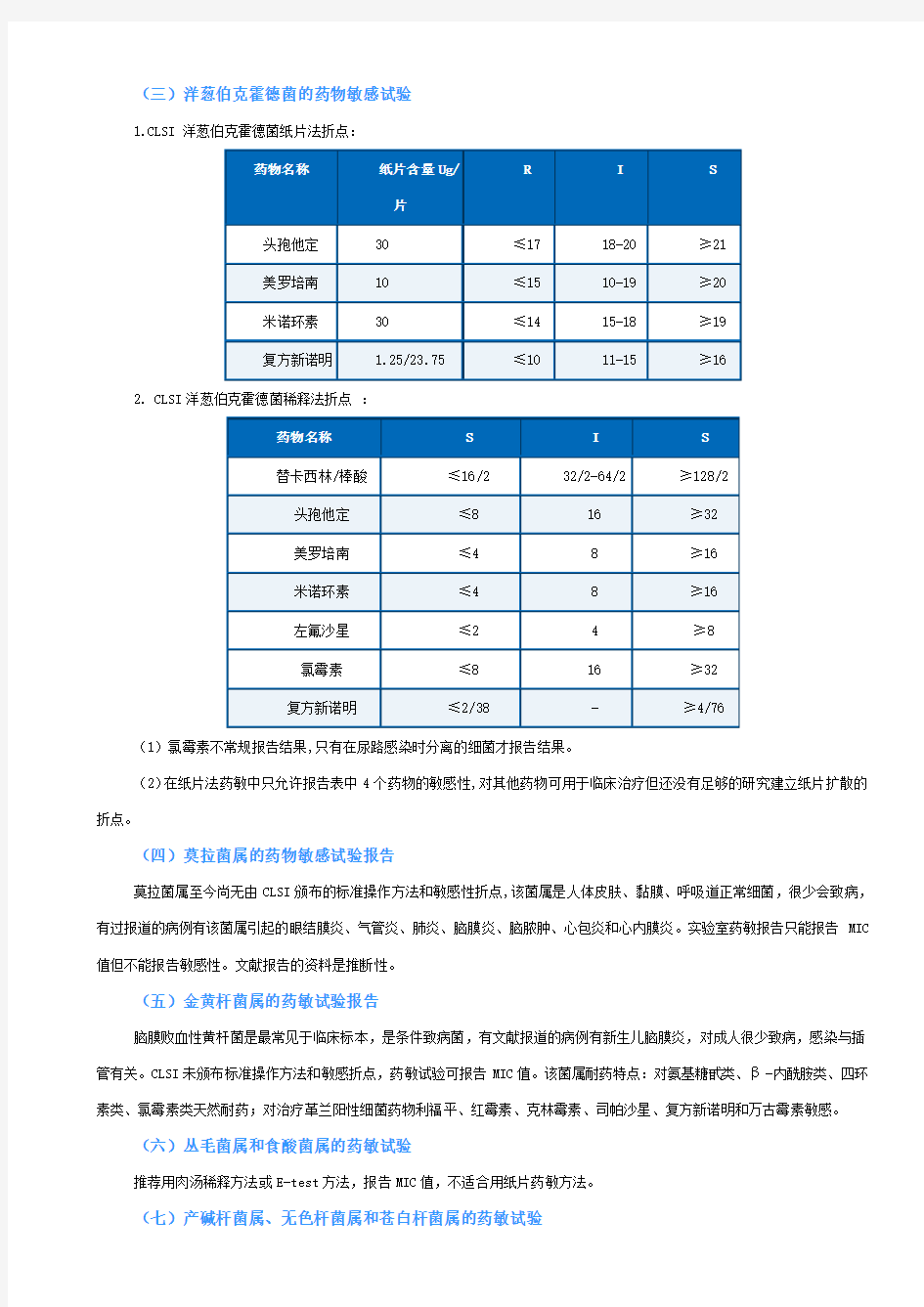
1.CLSI 洋葱伯克霍德菌纸片法折点:
R I S
药物名称纸片含量Ug/
片
头孢他定30 ≤1718-20 ≥21
美罗培南10 ≤1510-19 ≥20
米诺环素30 ≤1415-18 ≥19
复方新诺明 1.25/23.75 ≤1011-15 ≥16
2. CLSI洋葱伯克霍德菌稀释法折点:
药物名称S I S
替卡西林/棒酸≤16/232/2-64/2 ≥128/2
头孢他定≤816 ≥32
美罗培南≤48 ≥16
米诺环素≤48 ≥16
左氟沙星≤2 4 ≥8
氯霉素≤816 ≥32
复方新诺明≤2/38- ≥4/76(1)氯霉素不常规报告结果,只有在尿路感染时分离的细菌才报告结果。
(2)在纸片法药敏中只允许报告表中4个药物的敏感性,对其他药物可用于临床治疗但还没有足够的研究建立纸片扩散的折点。
(四)莫拉菌属的药物敏感试验报告
莫拉菌属至今尚无由CLSI颁布的标准操作方法和敏感性折点,该菌属是人体皮肤、黏膜、呼吸道正常细菌,很少会致病,有过报道的病例有该菌属引起的眼结膜炎、气管炎、肺炎、脑膜炎、脑脓肿、心包炎和心内膜炎。实验室药敏报告只能报告MIC 值但不能报告敏感性。文献报告的资料是推断性。
(五)金黄杆菌属的药敏试验报告
脑膜败血性黄杆菌是最常见于临床标本,是条件致病菌,有文献报道的病例有新生儿脑膜炎,对成人很少致病,感染与插管有关。CLSI未颁布标准操作方法和敏感折点,药敏试验可报告MIC值。该菌属耐药特点:对氨基糖甙类、β-内酰胺类、四环素类、氯霉素类天然耐药;对治疗革兰阳性细菌药物利福平、红霉素、克林霉素、司帕沙星、复方新诺明和万古霉素敏感。
(六)丛毛菌属和食酸菌属的药敏试验
推荐用肉汤稀释方法或E-test方法,报告MIC值,不适合用纸片药敏方法。
(七)产碱杆菌属、无色杆菌属和苍白杆菌属的药敏试验
目前无药敏解释标准,建议采用稀释法药敏试验方法,报告MIC值,根据MIC和组织浓度判断敏感性。
1.粪产碱杆菌是产碱杆菌的代表株对氨苄西林、氨曲南和庆大霉素耐药。
2.木糖氧化无色杆菌木糖氧化亚种是临床常见的分离株,对氨苄西林、氨基糖甙类、非抗假单孢菌的头孢菌素、氟喹诺酮和氯霉素耐药,但对派拉西林、替卡西林/棒酸、亚胺陪南、复方新诺明及抗假单孢菌头孢菌素敏感。
3.人苍白杆菌是苍白杆菌属代表菌,对β-内酰胺类耐药,但对亚胺陪南、复方新诺明、氨基糖甙类、氟喹诺酮类和四环素敏感。
(八)布鲁杆菌属药敏试验
不推荐做体外药敏试验,β-内酰胺类耐药和氟喹诺酮类有高的体外活性与临床疗效不一致。热病推荐首选药物是多西环素加庆大霉素或链霉素。
(九)军团菌药敏试验
目前无标准的试验方法和解释标准,肉汤稀释和E-test方法报告MIC值可作参考。首选用药大环内脂类、喹诺酮类,对β-内酰胺类体外敏感但体内疗效差。
(十)弯曲菌科细菌的药敏试验
1.弯曲菌科包括弯曲菌属、弓形菌属和螺菌属。目前无解释标准。CLSI M100-S16 2006年文件仅提供了质控菌株对部分抗生素的可接受范围和质量控制标准操作程序。
2.常寄生于人的牙周黏膜,可引起人胃肠炎和腹泻,胎儿弯曲菌可引起免疫低下患者菌血症。热病推荐对空肠弯曲菌首选药物为红霉素、阿奇霉素、克拉霉素、多西霉素和克林霉素。幽门螺杆菌对克林霉素的折点是1ug/ml并与临床疗效一致,甲硝唑在体外敏感试验没有标准。
(十一)厌氧细菌的药敏试验
由于大多数用于厌氧细菌感染的药物对临床有很好的预期效果,所以并不推荐做常规的厌氧菌药敏试验,但在严重厌氧菌感染而常规治疗疗效差的情况下有必要测定致病菌的MIC值,指导用药;在新药评价时需要做厌氧菌的药敏试验,用MIC值评价药效学。
随着厌氧细菌感染率的增长,厌氧细菌的耐药性也在不断增长,特别是脆弱拟杆菌已有报道对亚胺培南和甲硝唑的耐药株报道,几乎所有的脆弱拟杆菌均产生β-内酰胺酶,部分菌株产生超广谱β-内酰胺酶。越来越多的梭杆菌产生β-内酰胺酶导致对β-内酰胺酶抗生素耐药。
(十二)真菌的药敏试验
由于真菌药物敏感试验影响因素颇多,如真菌生长的速度、药物在体内的代谢、培养条件等,所以真菌药敏试验结果与疗效的一致性至今是本领域需要探讨的重要课题。
1.酵母样真菌药敏试验
(1)酵母样真菌的药敏折点 1992年,NCCLS起草了《酵母菌的液体稀释法抗真菌药物敏感试验参考方案》文件名称为
M-27P,用于检测引起深部感染的酵母样真菌,包括念珠菌、光滑球似酵母和新生隐球菌等菌对两新霉素-B(AmB)、5-氟胞嘧啶(5-FC)、氟康唑(FCZ)、伊曲康唑(ICZ)等的敏感性;1995年NCCLS对该草案作了修正,增加了微量稀释法起名为(M-27T);
1995-1997年NCCLS对终点判断方法进行了修定,形成了《酵母菌稀释法抗真菌药敏试验实施方案》(M-27A);2002年NCCLS 统一了微量稀释法中24h和48h终点判断方法,增加了新的抗真菌泊沙抗唑(posaconazole)、雷夫康唑(ravuconazole)和伏力康唑(vuliconazole VCZ)的试验方法和MIC参照范围,并将该方案修定出版,名为M-27A2。
(2)CLSI对酵母样真菌现有的标准
药物名称S SDD I R
FCZ 8 16-32 - ≥64
ICZ ≤0.125 0.25-0.5 - ≥1
5-FC ≤4- 8-16 ≥32
AmB - - - -
VCZ ≤1- 2 ≥4
(3)CLSI对酵母样真菌纸片法判断标准
敏感性FCZ VCZ
S ≥19≥17
SDD 15-18 14-16
R ≤14≤13
2. 丝状真菌药敏试验
(1)丝状真菌的药敏折点:初始方案产生于1998年,命名为M-38P,该方案包括微量稀释法和洪量稀释法,对曲霉菌、镰刀菌、波氏假阿利什曼等丝状真菌有较好的一致性;2003年NCCLS对某些最低抑菌浓度(MIC)判定方法及影响因素作了多中心的研究和修正,并增加了新三唑类药物的试验方案,从此产生了现在用于实验室药敏试验和新药评价的常规方法M-38A。
(2)丝状真菌药敏报告:CLSI颁布的M-38P是丝状真菌肉汤稀释法抗真菌药敏试验,内容并无丝状真菌敏感性折点,只是描述了测试方案,包括试剂配制、操作方法、质量控制等程序。
3.关于真菌药敏报告
(1)Candida.Krusel(克柔假丝酵母)对氟康唑天然耐药,现已颁布的氟康唑对念珠菌的判断标准不适用,不管体外药敏结果均应报告耐药。
(2)AMB对念珠菌目前无判断标准。
(3)伊曲康唑的折点仅适用于黏膜念珠菌感染,对侵袭性感染时全身性用药并不适用,建议仅报告MIC不报告S、I和R。
(4)对5-FC现有的标准是基于联合用药情况下的敏感折点,如单独用药,该标准不适用。
(5)卡泊芬净至今无体内外相关性好和重见性稳定的药敏试验方法,至今无评定标准,但有报道可用MEC,即最低有效浓度(能使真菌形态发生改变的最低药物浓度),用于评价药物的有效性。
4.E-test方法适合哪些真菌的药敏试验
E-test方法可适合多种真菌的药敏测试,包括酵母样真菌,如念珠菌、隐球菌状真菌,如曲霉菌、镰刀菌、毛霉菌、根
霉菌、梨头霉、外瓶霉、帚霉等的药敏测试。
5.正确报告FUNGUS-3的规范方法
(1)FUNGUS-3试条中氟胞嘧啶只有2个稀释浓度,一个高浓度,一个低浓度,报告以敏感度报告;
(2)当两个浓度均有菌生长,并生长超过80%,报告耐药“R”。
(3)当高浓度真菌被抑制80%或以上,低浓度孔真菌完全生长或生长80%报告“SDD”。
(4)当两个浓度均无真菌生长报告敏感“S”。
(5)可通过肉眼判读或是使用ATB仪器自动判读来观察生长情况:肉眼判读前,建议把试条放在黑暗的背景下(可从bioMerieux得到ATB FUNGUS 3可视化判读器)。对于每一个抗真菌制剂,从低浓度开始,与生长对照比较,在结果记录纸上记下每一个杯的生长得分。
(6)正确报告FUNGUS-3的药敏结果的方法:对于两性霉素B,最小抑菌浓度(MIC)是生长完全被抑制的测试杯的浓度(得分为“0”的测试杯);对于氟康唑(FCA), 伊曲康唑(ITR)和伏立康唑(VRC),鉴于可能存在拖尾生长,最小抑菌浓度(MIC)对应的测试杯得分可以是生长得分为“2”,“1”,或是“0”分。需要注意的是:在杯状凹外围的生长迹象应记录
为“0”或“1”分。例ATB FUNGUS 2如下图
三.MIC在真菌感染临床治疗中的指导意义
在临床应用中,按日剂量与MIC比值大于50的剂量用于严重真菌感染,日剂量与MIC值比值为25的剂量用于一般真菌感染的原则被应用。也有文献提示,临床实践证明当抗真菌药物MIC值大于2ug时,疗效差,死亡率高。含MIC的真菌药敏报告对临床治疗更有价值。
(一)抗真菌药敏试验与临床的相关性
ICZ法中MIC≤0.125ug/ml敏感,0.25-0.5ug/ml剂量依赖敏感,≥1.0ug/ml为耐药。如给药400mg/d,MIC1.56ug/ml为耐药; MCZ治疗泌尿系统白念感染,如耐药,其MIC可上升100倍;KCZ治疗CMCC,白念如果耐药,对其他唑类可交叉耐药。
5-FC耐药的MIC为≥32ug/ml,敏感值为≤4ug/ml;AmB试验耐药菌株有白念、热带、葡萄牙念珠菌,MIC大于0.8ug/ml 可以死亡,NCCLS法不太适合。但耐药一般为>1.0ug/ml。
FCZ试验中一般剂量依赖耐药为16-32ug/ml,但64ug/ml即为耐药。也可以说,组织药物浓度的测定是联系药敏试验和临床用药的桥梁。
以FLC为例:
剂量组织浓度
100mg/d 6μg/ml
400mg/d 20-30μg/ml
800mg/d 40-60μg/ml
Rex JH, Clin Microb Rev 1993, 6: 367-381
(二)体外抗真菌药敏试验与体内疗效的一致性
NCCLS M27-A试验研究中:600余株念珠菌MIC值,分离自150余例AIDS的食管念珠菌病,一致性好;治疗失败者,MIC 值大于64 μg/ml,并显示MIC值与临床疗效成90-60原则,即:药敏试验敏感菌株:90%对治疗有效;药敏试验耐药菌株:60%对治疗有效(Mahmoud A.G, JCM 1996, 34:489-495;Rex J,CID 2002, 35: 982-989)。
体外抗真菌药敏试验指导用药,以FLC为例:
MIC 剂量
<4μg/ml 100mg/d
4-8μg/ml 200mg/d
8-16μg/ml 400mg/d
16-32μg/ml 800mg/d
Hopenthal et al, Diagn Microb Infect Dis, 2004, 48:153-160
(三)真菌药敏试验的应用原则
当疾病为孤立的粘膜念珠菌病时,建议经验性治疗,不做药敏;当为复发的粘膜念珠菌病时,建议菌种鉴定,如果治疗失败应该考虑到药敏;当高危患者中念珠菌定植时,建议菌种鉴定,建立当地药敏试验流行病学资料,应该经验性治疗,当为念珠菌血症及深部感染时,建议鉴定,应用唑类药物时应该考虑药敏试验,并定期掌握当地药敏试验流行病学资料;当患者为深部感染需要延长治疗时,建议对所有菌株都测药敏(Hopenthal et al, Diagn Microb Infect Dis, 2004, 48:153-160)。
四、细菌药敏试验的规范化操作总结
(一)对任何细菌微生物实验室都可以进行药敏试验。
(二)对任何无折点的药物和相应细菌不能报告敏感性但都可以报告MIC。
(三)含MIC的药敏报告对临床更有参考价值。
细菌分离培养方法及操作步骤无菌取血液或脏器、淋巴结划线接种于鲜血琼脂平板或血清琼脂平面培养基、普通肉汤培养基,37℃恒温培养24 h,观察其生长特性。目前细菌分离培养的常用方法有平板划线分离法、加热分离法与实验动物分离法。 平板划线接种法 这就是目前临床上最常用的分离接种方法。它可以从被检病料中通过划线可使细菌分离、分散生长而形成单个菌落(有利于从含有多种细菌的标本中分离出目的菌),以便挑选可疑菌落作纯培养加以鉴定。具体操作: 1、右手持接种环,在酒精灯上火焰灭菌; 图1 病料采集图2 接种环灭菌 2、待接种环冷却后,挑取被检料少许,左手持琼脂平板,以食指为
支点,用拇指与无名指将平皿揭开一空隙。大约20℃时,迅速地将接种环轻轻地涂布在培养基的边缘。 3、在涂布处来回移动作曲线形划线接种。(注意:划线时,以腕力使接种环在琼脂平板表面划动,尽量不要划破培养基,划的线条要密,但不能重复旧线,以免培养物形成菌 苔。) 图3 平板划线接种法 4、划线完毕,合上平皿盖,将琼脂平板倒置,放入37℃温箱内培养
18-24小时。 注意:分离培养用的平板培养基应表面干燥,可于临用前置37℃孵育箱内30分钟,这样表面即干燥有利于分离培养,又使培养基预温,对培养某些较娇弱的细菌有利。 细菌药敏试验方法操作步骤药敏试验就是抗菌药使用以前必不可少的一个基本环节,一个正确的药敏结果能够科学的指导养殖户用药,减少抗菌素使用的盲目性,从而减少养殖户损失。在临床实际生产中具备重要意义。 1、在“超净台”中,用经(酒精灯)火焰灭菌的接种环挑取适量细菌培养物,以划线方式将细菌涂布到平皿培养基上。具体方式; 用灭菌接种环取适量细菌分别在平皿边缘相对四点涂菌,以每点开始划线涂菌至平皿的1/2。然后,找到第二点划线至平皿的1/2,依次划线,直至细菌均匀密布于平皿。 图4 接种环划线
病原学 细 菌 各 论 总 结 衛卋琦 2014.04.01
第六章球菌 葡萄球菌属 链球菌属 球菌肺炎球菌脑膜炎奈瑟菌 奈瑟球菌属 淋病奈瑟菌 链球菌 生物学性状形态染色G+ 培养特性营养要求高、不分解菊糖、不被胆汁溶解 分类 1、按溶血现象:甲型溶血性链球菌α(多为条件致病 菌)、乙型溶血链球菌β(致病力强)、丙型链球菌(一 般不致病); 2、按抗原结构:A∽V 20种,对人致病90%属A群; 3、按需氧量:需氧性、兼性厌氧性和厌氧性对人致病主 要为前两者; 抗原构造 抵抗力 不强 60℃ 30min可以杀死,对一般消毒剂敏感 乙型溶血性链球菌对青霉素、红霉素、磺胺类药敏感 致病性致病物质 1、致热外毒素; 2、链球菌溶血素:1、链球菌溶血素O(SLO)可引起心 肌损伤,能加重心肌炎的病变;2、链球菌溶血素S(SLS)对白细胞、血小板和多种组织细胞有破坏作用; 3、M蛋白; 4、透明质酸酶; 5、链激酶使血块溶解或阻止血浆凝固,利于细菌扩 散;重组链激酶已用于心肌梗死; 6、链道酶使脓液稀薄,利于细菌扩散;用于脓胸、输 卵管炎等疾患,解除组织粘连; 所致疾病1、化脓性感染 2、猩红热 3、风湿热和急性肾小球炎
免疫性感染后可获一定免疫力(主要为抗M蛋白抗体)。因其型别多,各型之间无交叉免疫作用,故常发生反复感染 微生物学检查1、直接镜检 2、分离培养与鉴定 3、抗链球菌溶血素O抗体实验 4、 分子生物学法 防治原则 积极治疗,减少传染源。对急性咽峡炎和扁桃体炎患者应早期、彻底治疗,防止风湿病和急性肾小球炎等疾病发生。对A群链球菌感染 者首选青霉素G。 传播途 径 飞沫 肺炎链球菌 生物学性状形态染色G+ 无鞭毛和芽胞有荚膜(人工培养无) 培养特性兼性厌氧性,营养要求高。可分解菊糖,能被胆汁溶解。分类90个血清型 1-3致病力强 抗原构造 与分型 荚膜多糖抗原 C物质 抵抗力 弱 56℃ 20min可杀死。有荚膜抗干燥。对一般消毒剂、 青霉素、红霉素、林可霉素等敏感。 致病性 致病物质荚膜,有抗吞噬作用。 所致疾病大叶型肺炎 免疫性病后有牢固的型特异性免疫 微生物 学检查 1、直接涂片染色镜检 2、分离培养与鉴定 3、动物实验 防治原 则 用荚膜多糖疫苗预防接种、治疗主要采用大剂量青霉素或林可霉素。 奈瑟菌属 项目脑膜炎奈瑟菌淋病奈瑟菌 生物学性1、形态与染色:呈肾形或豆1、形态与染色:G-双球菌,与脑
肺泡灌洗液细菌培养及药敏结果分析 发表时间:2018-02-02T15:22:23.477Z 来源:《临床医学教育》2017年12月作者:邹单东韦柳华程红革[导读] 下呼吸道感染是临床较为常见的感染,病原菌种类多、耐药性强。 广西医科大学第四附属医院广西柳州545005 [摘要] 目的:了解肺泡灌洗液中细菌种类及耐药情况,为临床合理用药提供依据。方法:美国Microscan Autoscan-4微生物分析仪对细菌作鉴定及药敏试验。结果:灌洗液细菌培养阳性率56.2%;195例细菌中革兰阴性菌占90.8%,革兰阳性菌占9.2%;主要细菌依次是铜绿假单胞菌、肺炎克雷伯菌、鲍曼不动杆菌。主要革兰阴性菌对亚胺培南耐药率为0~15.1%,大肠埃希菌、肺炎克雷伯菌产超广谱β-内酰 胺酶 (ESBLs)阳性率为62.5%、64.1%,耐甲氧西林金黄色葡萄球菌(MRSA)检出率为60.0%,细菌多药耐药现象严重。结论:不同细菌对抗菌药物的耐药性不同,灌洗液细菌培养及药敏试验可为临床合理用药提供依据。 [关键词] 肺泡灌洗液;细菌分布;耐药性 [Abstract] Objection: in order to understand the type of bacteria and susceptibility test results in irrigating solution, and provide an according to rational use of drug for clinical.Methods: the instrument of identification and susceptibility test is Microscan Autoscan-4, USA.Result: the positive rate of irrigating solution is 56.2%; the Gram-negative bacteria has 90.8% in these 195 bacterias, and Gram-positive bacteria has 9.2%; the main type of these bacteria are Pseudomonas aeruginosa, Pneumonia crayresearch bacteria and baumanii . the tate of the bacterias, which resist to imipenem, is 0~15.1% in these Gram-negative bacterias; the rate of Pneumonia crayresearch bacteria and baumanii, which product ESBLs, is 62.5%、64.1%,respectively; and the rate of MRSA is 60.0%. and the phenomenon of multidrug resistant is Very serious.Conclusion: the drug resistance of bacteria is differrent, the bacterial culture and susceptibility test results of irrigating solution can provide basis of rational drug use for clinical. [Key words] irrigating solution; Bacteria distribution; drug resistanc 下呼吸道感染是临床较为常见的感染,病原菌种类多、耐药性强。目前病原诊断普遍采用痰培养,但因其易污染,痰液质量难以保障,临床价值有限。肺泡灌洗液与痰液相比,对下呼吸道感染诊断具有更高特异性和敏感性,同时细菌药敏结果对临床抗感染治疗更具价值【l】。因此,我们对2010年从肺泡灌洗液中分离到的195例细菌的药敏结果进行回顾性分析,以期为临床抗感染治疗提供依据,现将结果报道如下。 1 材料和方法 1.1 标本来源 251例灌洗液为2010年我院住院患者予以纤支镜支气管肺泡灌洗治疗后采集所得。同一患者多次分离到的细菌不重复计入。 1.2 细菌鉴定和药敏试验采用Microscan Autoscan-4微生物分析仪对细菌作鉴定和药敏试验。药敏试验判断标准、结果解释、MRSA、ESBLs检测参照美国临床实验室标准化协会(CLSI)标准【2】。定期用标准菌株做药敏质量控制。 1.3 数据处理数据均由WHONET 5.4软件分析处理所得。 2 结果 2.1 细菌分布 251例灌洗液细菌培养阳性率为56.2%(141/251)。共分离细菌195例,革兰阴性菌占90.8%,革兰阳性菌占9.2%,细菌构成比见表1。 2.2药敏结果大肠埃希菌、肺炎克雷伯菌产ESBLs株为10例、25例,阳性率为62.5%、64.1%,MRSA 6例,检出率为60.0%。主要细菌对抗菌药物的耐药率,见表2。
药敏试验: 用药敏实验进行药物敏感度的测定,以便准确有效的利用药物进行治疗。目前,临床微生物实验室进行药敏试验的方法主要有纸片扩散法,稀释法(包括琼脂和肉汤稀释法),抗生素浓度梯度法(E-test 法),和自动化仪器等。 简介: 体外抗菌药物敏感性试验简称药敏试验(AST),是指在体外测定药物抑菌或杀菌能力的试验。 根据美国国家临床实验室标准化委员会(NCCLS)近期推荐的标准,对非苛氧菌(肠杆菌科细菌、铜绿假单胞菌、和其他非肠科杆菌、葡萄球菌属细菌、肠球菌属细菌)和苛氧菌(嗜血杆菌属细菌、淋病奈瑟菌、肺炎链球菌和其他链球菌)选择常规药敏试验的首选药物(A 组抗生素)或临床使用的主要抗生素(B组抗生素)进行药敏试验。 抗菌药对细菌性传染病的控制起到了非常重要的作用,但由于养殖过程中不科学的、盲目的滥用抗菌药,很多致病性细菌产生了耐药性,使得抗菌药对细菌性疾病的控制效果越来越差,不但造成药物浪费,而且还延误病情,给养殖户造成了很大的经济损失。 随着新型致病菌的不断出现,抗菌药的防治效果越来越差。并且各种致病菌对不同的抗菌药物的敏感性不同,同一细菌的不同菌株对不同抗菌药物的敏感性也有差异。长期以来,各种致病菌耐药性的产生使各种常用抗菌药物往往失去药效,以及不能很好的掌握药物对细菌的敏感度,所以一个正确的结果,可供临床医师选用抗菌药物的参
考,并提高疗效。农业部动物检疫所青岛易邦生物工程有限公司动物疫病诊疗中心总结出几套适合基层进行药敏试验的操作方法,现简单介绍如下。 实验步骤: 实验材料 普通营养琼脂培养基:可去生化试剂店购买,做不同细菌的药敏试验可选择不同的培养基,如做大肠杆菌的药敏试验可选择普通营养琼脂或麦糠凯培养基。做沙门氏菌可选择血清培养基。 药敏试纸:购买或自制(详见实验准备) 细菌:待做药敏试验的细菌 仪器:接种环、酒精灯、打孔器、牛津杯、移液器、滴头 实验准备 2.1 药敏片的准备:购买或自制 2.1.1 制备方法:取新华1号定性滤纸,用打孔机打成6毫米直径的圆形小纸片。取圆纸片50片放入清洁干燥的青霉素空瓶中,瓶口以单层牛皮纸包扎。经15磅15-20分钟高压消毒后,放在37℃温箱或烘箱中数天,使完全干燥。 2.1.2 抗菌药纸片制作:在上述含有50片纸片的青霉素瓶内加入药液0.25毫升,并翻动纸片,使各纸片充分浸透药液,翻动纸片时不能将纸片捣烂。同时在瓶口上记录药物名称,放37℃温箱内过夜,干燥后即密盖,如有条件可真空干燥。切勿受潮,置阴暗干燥处存放,有效期3-6个月。
细菌分离培养方法及操作步骤 无菌取血液或脏器、淋巴结划线接种于鲜血琼脂平板或血清琼脂平面培养基、普通肉汤培养基,37℃恒温培养24 h,观察其生长特性。目前细菌分离培养的常用方法有平板划线分离法、加热分离法和实验动物分离法。 平板划线接种法 这是目前临床上最常用的分离接种方法。它可以从被检病料中通过划线可使细菌分离、分散生长而形成单个菌落(有利于从含有多种细菌的标本中分离出目的菌),以便挑选可疑菌落作纯培养加以鉴定。具体操作: 1、右手持接种环,在酒精灯上火焰灭菌; 图1 病料采集图2 接种环灭菌 2、待接种环冷却后,挑取被检料少许,左手持琼脂平板,以食指为支点,用拇指和无名指将平皿揭开一空隙。大约20℃时,迅速地将接种环轻轻地涂布在培养基的边缘。
3、在涂布处来回移动作曲线形划线接种。(注意:划线时,以腕力使接种环在琼脂平板表面划动,尽量不要划破培养基,划的线条要密,但不能重复旧线,以免培养物形成菌苔。) 图3 平板划线接种法 4、划线完毕,合上平皿盖,将琼脂平板倒置,放入37℃温箱内培养18-24小时。 注意:分离培养用的平板培养基应表面干燥,可于临用前置37℃孵育箱内30分钟,这样表面即干燥有利于分离培养,又使培养基预温,对培养某些较娇弱的细菌有利。
细菌药敏试验方法操作步骤 药敏试验是抗菌药使用以前必不可少的一个基本环节,一个正确的药敏结果能够科学的指导养殖户用药,减少抗菌素使用的盲目性,从而减少养殖户损失。在临床实际生产中具备重要意义。 1、在“超净台”中,用经(酒精灯)火焰灭菌的接种环挑取适量细菌培养物,以划线方式将细菌涂布到平皿培养基上。具体方式;用灭菌接种环取适量细菌分别在平皿边缘相对四点涂菌,以每点开始划线涂菌至平皿的1/2。然后,找到第二点划线至平皿的1/2,依次划线,直至细菌均匀密布于平皿。 图4 接种环划线 2、以无菌操作将灭菌的不锈钢小管(外径为4毫米、孔径与孔距均为3毫米,管的两端要光滑,也可用玻璃管、瓷管),放置在培养基上打孔,将孔中的培养基用针头挑出,并以火焰封底,使培养基能充分的与平皿融合(以防药液渗漏,影响结果)。
实训细菌的药物敏感性试验 教学目标 使学生掌握细菌药物敏感性试验的操作方法,能够利用本试验方法选择敏感药物治疗兽医临床常见的细菌性传染病。 材料准备 1.器材:温箱、天平、打孔机、滤纸、无菌试管及吸管、镊子、接种环、酒精灯等。 2.试剂:蒸馏水。 3.培养基:普通琼脂平板。 4.菌种:金黄色葡萄球菌及大肠杆菌的固体培养物。 5.药品:链霉素、金霉素、新霉素、红霉素等抗菌药物。 6.硫酸钡标准管:取1%~1.5%氯化钡0.5ml加1%硫酸溶液99.5ml,充分混匀即成,用前充分振荡。 方法步骤 将抗菌药物置于接种待检菌的固体培养基上,抗菌药物通过向培养基内的扩散,抑制敏感细菌的生长,从而出现抑菌环。由于药物扩散的距离越远,达到该距离的药物浓度越低,由此可根据抑菌环的大小,判定细菌对药物的敏感度。 (一)含药纸片的制备 1.滤纸片最好选用新华1号定性滤纸,用打孔机打成直径6mm的滤纸片,放在小瓶中或平皿中,在121.3℃灭菌15min,再置100℃干燥箱内烘干备用。 2.药液的配制用无菌蒸馏水将各药稀释成以下浓度:磺胺100mg/ml、青霉素100IU/ml、链霉素、金霉素、新霉素、红霉素、多粘菌素1000μg/ml。 3.含药纸片的制备将灭菌的滤纸片用无菌的镊子摊布于灭菌平皿中,按每张滤纸片饱和吸水量为0.01ml计算,50张滤纸片加入药液0.5ml。要不时翻动,使纸片充分吸收药液,浸泡1~2h后于37℃温箱中烘干备用。对青霉素、金霉素纸片的干燥宜采用低温真空干燥法,干燥后立即放入瓶中加塞,放干燥器内或置-20℃冰箱中保存。纸片的有效期一般为4~6个月。 (二)测验方法 1.钩取金黄色葡萄球菌和大肠杆菌菌落各4~5个,分别接种于肉汤培养基中,37℃培养4~6h。 2.用灭菌生理盐水稀释培养菌液,使其浊度相当于硫酸钡标准管。装有以上两种成分的试管须相同,硫酸钡应用前需充分振动。 3.用无菌棉拭子蘸取上述肉汤培养液,在试管壁上挤压除去多余的液体,在琼脂培养基表面均匀涂抹。每种细菌分别接种1~2个琼脂平板。
细菌药物敏感试验实验报告 药物敏感性试验的基本原则 1药敏试验检测获得性耐药,不必测试天然耐药: 天然耐药是细菌菌种固有的特征,耐药基因一般位于染色体,可以长期稳定遗传,表现为对某类或某种药物的天然耐药。天然耐药信息一般由基础医学和临床文献提供。部分天然耐药,体外试验条件下可能无法检测出来,因而导致假敏感,如果报告将成为极重要错误,严重误导临床。常见菌种对各类药物的天然耐药见文献。实验室全体人员应熟知这些信息,可将其发给临床学习和参考。 2药敏试验测试的前提条件: 实验室应具备相应检测的人员能力、客观条件、结果解释依据。标本处理、菌株分离鉴定、药敏试验操作等环节规范、标准、结果可信;具备对结果的解释能力,能够提供临床会诊服务。临床常规工作,分离株(可能)有临床意义而非定植或污染时,才可进行药敏试验。 错误示例:来自痰标本的溶血葡萄球菌,未作标本质量评估和半定量培养,进行药敏试验;来自粪便标本肠球菌属进行药敏试验等。 3测试结果应准确: 实验室应遵照CLSI文件或相关规范建立本医院药敏试验的质量管理
体系。质控菌株、频率、质控范围符合相关要求;定期参加实验室室间比对项目。建议保留菌株,以便复核。 具体的专业要求 1标本类型 临床微生物学的一大特点是标本种类繁多,而不同药物在这些部位的分布不同。标本的规范采集、质量保证、立即运送和有效保藏有赖于临床、实验室以及相关各方的密切合作。在规范临床送检的前提下,实验室进行药敏试验和报告药敏结果时,应首先考虑标本的特殊性。实际工作中需重点考虑的标本如下。 1.脑脊髓液: 正常和疾病状态不能穿透血脑屏障的药物,常规不应报告。报告审核时,对于分离自脑脊髓液的菌,下列药物不能报告:仅有口服剂型的抗菌药物、一、二代头孢菌素(除外静脉用头孢呋辛)、头霉素类、克林霉素、大环内酯类、四环素类和喹诺酮类。
临床细菌培养结果与药敏试验敏感性和耐药分析 发表时间:2016-07-09T12:43:14.773Z 来源:《医师在线》2016年5月第9期作者:夏芳 [导读] 通过对药材水分、灰分及浸出物的考察,制定了土五加的检查成分,有效地控制药材质量,从源头进行监控,保证药材的来源。夏芳 河南省南阳油田总医院河南南阳 473132 摘要:目的了解我院临床所送标本分离菌株的特征及耐药情况,为临床提供“经验”用药的依据。方法收集2015年1月—2015年10月我院临床各科送检的1782份标本所分离出的病原菌鉴定结果与药敏实验作分析。结果 1782份标本由21个科室所送标本组成,共检出阳性标本555例,检出率为31.1%。革兰氏阴性菌439株,占分离菌的79.1%;革兰氏阳性菌检出116株,占分离菌的20%。革兰氏阴性杆菌中以大肠埃希菌分离率最高,为25.4%,依次为铜绿假单胞菌11.5 % ,阴沟杆菌9.1% 肺炎克雷伯菌8.6% ,鲍曼不动杆菌5.2%; 革兰式阳性球菌以表皮葡萄菌为主,耐甲氧西林金黄色葡萄球菌阳性率为23.8%,耐甲氧西林凝固酶阴性球菌为44.1%,大肠埃希菌产ESBLS为66%,肺炎克雷伯菌产ESBLS为39.6%,奇异变形杆菌产ESBLS为50%,革兰氏阴性菌耐药相当严重,大部分耐药在50%以上。结论定期对临床所选标本的细菌培养和药敏鉴定结果进行分析,有助于临床合理用药,减少耐药菌的发生,降低医疗费用和改善医患关系有重要意义。 关键词:细菌培养药敏试验 抗生素的合理使用已是人们关注的焦点,而合理使用抗生素的前提对于临床医生来说,基于两点出发:一是经验性用药;二是在细菌培养后,在药敏的指导下用药。而我们所说的“经验”性用药,是建立在细菌培养和药敏的回顾性总结的基础上而言的,所以检验科的微生物室应及时的总结临床所送标本分离菌构成特征及耐药情况,为临床提供“经验”用药的依据,为减少耐药菌的产生,降低医疗费用和改善医患关系有重要意义。基于这一目的,我们收集了2015年1月至2015年10月我院临床各科送检的1782份标本所分离出的病原菌鉴定结果及药敏试验结果,报告如下: 材料与方法 一、标本来源:住院与门诊共计21个科室,所送检的标本包括:血、尿、便、痰、分泌物、引流物、穿刺液、胸腹水等共计1782份。 二、材料与试剂:BACTEC9120全自动血培养仪、DL-96细菌鉴定系统、使用配套鉴定及药敏分析卡。 三、方法:各种标本以无菌方法接种于相应的培养基中,至于全自动培养箱孵育,如有细菌生长则进行鉴定和药敏试验,细菌的分离、鉴定严格按全国临床检验操作规程进行,药敏试验采用纸片法和MIC法。 四、统计学处理:用WHONET5.4统计软件进行处理和分析。 结果 一、1782份标本细菌的检出率 1782份标本由21个科室送检标本组成,共检出阳性标本555例,检出率为31.1%。临床各科送检标本数与检出率 本次分离出的555株细菌,革兰氏阴性菌439株,占分离菌的79.1%;革兰氏阳性菌116株,占分离菌的20.9%。
c l s i m s药敏试验解读 This manuscript was revise d on November 28, 2020
表1A. 美国临床微生物学实验室在非苛养菌常规试验和报告中应考虑的具有FDA 临床适应证的抗菌药物建议分组 总注释: A.对四环素敏感的菌株被认为对多西环素和米诺环素也敏感。然而,某些对四环素 中介或耐药的菌株可能对多西环素、米诺环素或二者敏感。 B.利福平不能单独用于抗菌治疗。 C.分离于泌尿道菌株不被常规报告。 D.头孢噻吩仅被用于预报口服药物结果,包括头孢氨苄、头孢泊肟、头孢氨苄和氯 碳头孢。以前关于头孢噻吩结果可预报其他头孢菌素敏感性建议仍然正确,但近年来还没有数据证实此建议。 E.当测试粪便中分离的沙门菌和志贺菌株时,只有氨苄西林、一种氟喹诺酮类和复 方新诺明可用于常规报告。另外,对肠道外感染沙门菌粉分离株,应测试并报告一种三代头孢菌素,假如需要,也可测试和报告氯霉素。分离于肠道内和肠道外伤寒样沙门菌(伤寒沙门菌和副伤寒沙门菌A-C)需进行药敏试验。分离于肠道内非伤寒样沙门菌不需进行常规药敏试验。 F.从CSF中分离菌株,试验和报告头孢噻肟和头孢曲松,以取代头孢唑林。 G.其他非肠杆菌科细菌包括假单胞菌和其他非苛养、非发酵葡萄球菌的革兰阴性杆 菌,但不包括铜绿假单胞菌、不动杆菌、洋葱伯克霍尔德菌和嗜麦芽窄食单胞菌,因为对这些菌种的建议试验和报告药物表格已分开。 鼻疽伯克霍尔德菌和假鼻疽伯克霍尔德菌试验和报告药物建议请参阅CLSIM45文件。 H.仅对金黄色葡萄球菌包括耐甲氧西林金黄色葡萄球菌(MRSA) I.青霉素敏感的葡萄球菌对葡萄球菌感染具有临床疗效的其他β-内酰胺类药物也敏 感。青霉素耐药葡萄球菌对青霉素酶不稳定青霉素类耐药。除具有抗-MRSA活性新的头孢菌素外,苯唑西林耐药葡萄球菌对当前所有使用的β-内酰胺类药物均耐
常见细菌药物敏感性试验报告规范中国专家共识 微生物学检验为感染性疾病的诊断、治疗和控制提供了必不可少的证据。因此微生物学检验报告是临床和实验室等多方共同关注的焦点。国内临床微生物学检验发展较为薄弱,报告存在着种种不足。同时,临床与实验室的沟通存在一定不足,密切协作非常必要。基于实际存在的问题,为规范国内临床微生物学检验药物敏感性试验报告,加强临床与实验室合作,发挥检验医师作用,特制订本共识,以期指导相关报告的规范化,减少错误,增加专业信息,提高服务质量,为临床医学诊、治、控提供坚实的科学依据。本共识限于常见细菌的药物敏感性报告。 一、药物敏感性试验的意义和基本原则 (一)意义 药物敏感性试验可以检测细菌对于抗细菌药物的敏感性,为临床用药、新药研究、监测耐药变迁、发现耐药机制等提供客观证据[1]。对于经验治疗,依据一方面来自医生自身的经验,一方面是实验室长期不断提供的数据积累。临床需要考虑不同感染的病原谱和常见病原对不同药物的敏感性;对于靶向治疗,特定分离株的具体药敏试验结果可以用于判断经验治疗选药合理性、经验治疗效果分析、调整治疗选药依据等。 (二)基本原则 1.药敏试验检测获得性耐药,不必测试天然耐药: 天然耐药是细菌菌种固有的特征,耐药基因一般位于染色体,可以长期稳定遗传,表现为对某类或某种药物的天然耐药[2]。天然耐药信息一般由基础医学和临床文献提供。部分天然耐药,体外试验条件下可能无法检测出来,因而导致假敏感,如果报告将成为极重要错误,严重误导临床。常见菌种对各类药物的天然耐药见文献[3,4]。实验室全体人员应熟知这些信息,可将其发给临床学习和参考。 2.药敏试验测试的前提条件[5]: 实验室应具备相应检测的人员能力、客观条件、结果解释依据。标本处理、菌株分离鉴定、药敏试验操作等环节规范、标准、结果可信;具备对结果的解释能力,能够提供临床会诊服务。临床常规工作,分离株(可能)有临床意义而非定植或污染时,才可进行药敏试验。错误示例:来自痰标本的溶血葡萄球菌,未作标本质量评估和半定量培养,进行药敏试验;来自粪便标本肠球菌属进行药敏试验等。 3.测试结果应准确: 实验室应遵照C L S I文件或相关规范建立本医院药敏试验的质量管理体系。质控菌株、频率、质控范围符合相关要求;定期参加实验室室间比对项目。建议保留菌株,以便复核。 二、具体的专业要求 (一)标本类型 临床微生物学的一大特点是标本种类繁多,而不同药物在这些部位的分布不同。标本的规范采集、质量保证、立即运送和有效保藏有赖于临床、实验室以及相关各方的密切合作。
医院细菌培养及药敏试验中常见问题 范文 Common problems in hospital bacterial culture and dru g sensitivity test 编订:JinTai College
医院细菌培养及药敏试验中常见问题范文 前言:毕业论文是普通中等专业学校、高等专科学校、本科院校、高等教育自学考试本科及研究生学历专业教育学业的最后一个环节,为对本专业学生集中进行科学研究训练而要求学生在毕业前总结性独立作业、撰写的论文。本文档根据毕业论文内容要求和特点展开说明,具有实践指导意义,便于学习和使用,本文下载后内容可随意调整修改及打印。 感染性疾病较常见,其中大多数为细菌感染和病毒感染,除病毒病原检测较困难未普及外,细菌培养及药敏试验是一项成熟普及的技术。详细内容请看下文毕业论文范文:医院细菌培养及药敏试验中常见问题。 按理所有感染性疾病均应根据培养及药敏结果选用抗生素,即细菌感染性疾病的病原学培养率应达到100%才是最理想的,由于有的病例需多次培养,故按培养次数占病例数百分比还应超过100%,只有这样,该试验指导临床的价值才能真正体现。 然而,由于许多原因,许多医院的感染性疾病的病原微生物标本送培养率都在50%以下,应当重复送检的标本更少,
同时,有限的送培标本还存在标本合格率低即采集时机、方法、采集途径、采集量的不科学问题,及时采集后的保护、送检时间、条件也有不当造成污染或病原体破坏而影响培养阳性率的情况,故在临床工作中正是由于感染性疾病病原送培率低、送培质量难保证,故造成了培养结果难以指导临床选药、经验性使用抗生素的现象极为普遍的情况,遇疗效不好则频繁更换,不仅疗效不佳,而且这又是产生和促进细菌耐药性增加的因素之一。 固定化、商品化的药敏试剂盒限制了抗生素药敏试验范围, 有时结果形同虚“试”。 微生物室把临床标本中的细菌培养出来后,做药敏试验 是购买商品化的药敏试验盒来进行的,而生产商家在药敏试剂板中只随机或意向性固定了近20中左右的抗生素,也就是说,药物敏感范围只能按药敏板中的抗生素种类做,不可能在本院使用时改变,如果这20种抗生素的种类均耐药,那么20种以外抗生素又哪些敏感呢?指导作用甚微,临床上又只得经验性 用药。 -------- Designed By JinTai College ---------
特殊细菌药敏试验的规范化操作 一、目前我国细菌药敏试验现状 20年以来,我国在卫生部和各地临床检验中心和检验学会的共同努力下引进CLSI药敏系列标准,使全国微生物实验室能在同一标准下进行质量控制活动。当前,微生物实验室对常见临床分离细菌的药物敏感试验的水平已有了显著的提高,但对特殊细菌的药敏试验的各个环节的规范操作还不能得到普及,对目前还无折点的细菌能否做药敏试验,以及如何判断细菌的药物敏感和耐药,仍然概念模糊,有待进一步规范和普及。 目前常见错误做法: (一)铜绿假单孢菌的药敏判断标准用于其他非发酵细菌;嗜血杆菌的标准用于卡他莫拉菌等的错误做法时有发生。 (二)借用同属细菌敏感标准 (三)借用同类抗生素的敏感标准 二、各菌属的药物敏感性报告及试验方法的CLSI药敏标准 (一)“嗜麦芽”菌属药敏报告标准 1.CLSI对“嗜麦芽”纸片药敏判断标准 2.CLSI对“嗜麦芽”稀释法判断标准 (二)无折点细菌的药物敏感试验报告 1. 其他药物的敏感性报告: CLSI推荐的药物可以报告MIC值和敏感度(S、I、R),临床需要的其他药物的药敏试验报告可以直接报告MIC值但不报告S、I、R。 2. 不要用认为相近细菌的折点代替报告S、I、R,这会误导医生用药。
(三)洋葱伯克霍德菌的药物敏感试验 1.CLSI 洋葱伯克霍德菌纸片法折点: 2. CLSI洋葱伯克霍德菌稀释法折点: (1)氯霉素不常规报告结果,只有在尿路感染时分离的细菌才报告结果。 (2)在纸片法药敏中只允许报告表中4个药物的敏感性,对其他药物可用于临床治疗但还没有足够的研究建立纸片扩散的折点。 (四)莫拉菌属的药物敏感试验报告 莫拉菌属至今尚无由CLSI颁布的标准操作方法和敏感性折点,该菌属是人体皮肤、黏膜、呼吸道正常细菌,很少会致病,有过报道的病例有该菌属引起的眼结膜炎、气管炎、肺炎、脑膜炎、脑脓肿、心包炎和心内膜炎。实验室药敏报告只能报告MIC 值但不能报告敏感性。文献报告的资料是推断性。 (五)金黄杆菌属的药敏试验报告 脑膜败血性黄杆菌是最常见于临床标本,是条件致病菌,有文献报道的病例有新生儿脑膜炎,对成人很少致病,感染与插管有关。CLSI未颁布标准操作方法和敏感折点,药敏试验可报告MIC值。该菌属耐药特点:对氨基糖甙类、β-内酰胺类、四环素类、氯霉素类天然耐药;对治疗革兰阳性细菌药物利福平、红霉素、克林霉素、司帕沙星、复方新诺明和万古霉素敏感。 (六)丛毛菌属和食酸菌属的药敏试验 推荐用肉汤稀释方法或E-test方法,报告MIC值,不适合用纸片药敏方法。 (七)产碱杆菌属、无色杆菌属和苍白杆菌属的药敏试验
微生物培养、药敏试验的流程及意义 一、微生物培养及药敏试验的总述 微生物培养就是使用体外试验的方法检测可能导致感染的病原菌,并给以药敏结果,为临床医生针对某一特定的临床感染提供依据。而药敏试验则是承接微生物培养的一项工作,即对于培养得到的病原菌进行体外试验检测细菌对于抗菌药物的耐药性,来预测抗菌药物的临床治疗效果,从而为临床医生提供选用抗菌药物的依据来治疗感染。 对于检测到的可能的致病菌进行药敏试验时选择的药物是参照美国的CLSI推荐的标准制定的。尤其,使用全自动微生物分析仪进行药敏试验时有固定的药敏组合,不是人为可以随意添加或减少的。 (一)微生物的培养和药敏试验的流程基本为: ①将标本进行处理(不是所有的标本都需要处理); ②将标本接种于不同的培养皿中在不同条件的培养箱中进行培养(不同的标本所含菌的种类不同,不同菌的生长条件不同,因此需要接种于不同的培养皿中); ③24h后观察培养皿中细菌的生长情况: a.此时若无细菌培养,继续放回培养箱中培养24h,若仍然无细菌生长则判定为阴性结果,因此阴性结果出具的时间为48h以后。 b.若有细菌生长,要根据形态和气味等对细菌进行初步的判定,若能判定出细菌的种类,则进行相应的药敏试验。贴有药敏片的培养皿在培养箱中培养24h后进行药敏结果的解读,然后报告结果,这种微生物培养及药敏结果报告出具的时间就是48h以后。 由于不同的细菌的生长的速度不同,有些细菌在培养24h后不能完全判定结果甚者24h 培养后无法观察到明显的细菌生长的则需要继续培养24h,即连续培养48h后同样根据菌落的形态、气味等来观察判定细菌的种类然后进行药敏试验。这种微生物培养和药敏试验结果出具需要72h以后。 而血液、骨髓等标本则是利用不同于上述培养方式的方法进行培养。它有专门的培养瓶和仪器。这种仪器会自动监测培养瓶中的变化来判定有无细菌生长,若有细菌生长仪器会发出警报。在培养5天内任何时间发出警报的培养瓶都要抽取瓶中的物质在培养皿中进行接种培养,同样在菌种鉴定后进行药敏试验;若在培养5天内不发出警报的培养瓶则视为阴性结果。因此血培养出具结果的时间为5~7天。 菌落的鉴定需要有雄厚的工作经验和熟练的相关基础知识。常规鉴定的方法有形态特征和理化特性。形态特征包括显微形态和培养特征;理化特性包括营养类型、碳氮源利用能力、各种代谢反应、酶反应和血清学反应。在微生物室学习时发现,很多时候在不太确定细菌的种类时,检验人员也会结合理化特性来判定细菌种类。 (二)革兰氏染色、应用及意义 由于微生物的生长有时间限定,因此微生物培养和药敏试验没有急查的说法。最快的结果也只能是通过涂片来判定有无细菌生长和细菌染色后的颜色和形态,来给临床医生的用药提供依据。 革兰氏阳性菌和阴性菌因为细胞壁的结构不同,在革兰氏染色时染成不同的颜色。革兰氏阳性菌显示紫色、革兰氏阴性菌显红色或粉色。由于细胞壁的结构不同,导致这两类细菌在染色性、抗原性、毒性、对某些药物的敏感性等方面均有较大差异。一般情况下,大多数化脓性球菌都属于革兰氏阳性菌,它们能产生外毒素使人致病,而大多数肠道菌多属于革兰氏阴性菌,它们差生内毒素,靠内毒素使人致病。 在治疗上,大多数革兰氏阳性菌对青霉素敏感(结核杆菌对青霉素不敏感),革兰氏阴性菌对青霉素不敏感(但奈瑟氏菌中德流行性脑膜炎双球菌和淋病双球菌对青霉素敏感),
细菌药敏试验实验报告解读 “医院有的药物不做药敏实验,医院没有的药物做什么药敏实验?”在临床上经常能听到临床医生们抱怨。“药敏报告显示敏感的药物,而临床治疗无效?”有时也让大夫们感到不解。这些问题使得临床医师不知道如何选择抗菌药物,那么如何正确解读药敏报告,合理选择抗菌药物报告呢。 我们先来了解几个概念: 最低抑菌浓度(MIC):测量抗菌药物的抗菌活性大小的一个指标,指在体外培养细菌18至24小时后能抑制培养基内病原菌生长的最低药物浓度。 最小杀菌浓度(MBC):抗菌药物能能使受试菌最初的活菌总数减少99.9%以上所需要的最低抗菌药物浓度。 折点:是最低抑菌浓度或者抑菌圈直径,用于区分离株为敏感、剂量依赖性敏感、中介、非敏感还是耐药 敏感(S):通过折点来定义,指当对感染部位采用推荐剂量时,具有MIC值等于或低于敏感折点(或抑菌圈等于或高于敏感折点)的菌株通常可被抗菌药物所达到的浓度水平所抑制,产生可能的临床疗效。 中介(I):通过折点来定义,包括这些MlC或者抑菌圈直径在中介范围内的菌株,其抗菌药物MIC接近于血液和组织中通常可达到的水平,而抗菌药物治疗的疗效可能低于敏感株。耐药(R):通过折点来定义,指按常规用药方案,在药物通常可达到的浓度水平时,菌株不能被抑制,表明MIC值或抑菌圈直径可能在一个产生了某种特殊的耐药机制(如β-内酰胺酶)的范围内,而且治疗研究显示该药的临床疗效不可靠。 多重耐药(MDR):是指有多重耐药性的病原菌。其定义为一种微生物对三类(比如氨基糖苷类、大环内酯类、β-内酰胺类、喹诺酮类等)或三类以上抗菌药物同时耐药,而不是同一类的三种。 泛耐药(XDR):广泛耐药细菌指细菌对常用抗菌药物几乎全部耐药,革兰氏阴性杆菌仅对黏菌素和替加环素敏感,革兰氏阳性球菌仅对糖肽类和利奈唑胺敏感。 全耐药(PDR):泛耐药细菌指对所有分类的抗菌药物全部耐药,革兰氏阴性杆菌对包括黏菌素和替加环素在内的全部抗菌药物耐药,革兰氏阳性球菌对包括糖肽类和利奈唑胺在内的全部抗菌药物耐药。 药敏试验目的 使用体外试验的方法检测细菌的耐药性,预测抗菌药物临床治疗效果并为临床医生针对某一特定感染问题选用药物提供依据。 判断标准
表1A. 美国临床微生物学实验室在非苛养菌常规试验和报告中应考虑的具有 FDA 临床适应证的抗菌药物建议分组
总注释: A.对四环素敏感的菌株被认为对多西环素和米诺环素也敏感。然而,某些对四 环素中介或耐药的菌株可能对多西环素、米诺环素或二者敏感。 B.利福平不能单独用于抗菌治疗。 C.分离于泌尿道菌株不被常规报告。 D.头孢噻吩仅被用于预报口服药物结果,包括头孢氨苄、头孢泊肟、头孢氨苄 和氯碳头孢。以前关于头孢噻吩结果可预报其他头孢菌素敏感性建议仍然正确,但近年来还没有数据证实此建议。 E.当测试粪便中分离的沙门菌和志贺菌株时,只有氨苄西林、一种氟喹诺酮类 和复方新诺明可用于常规报告。另外,对肠道外感染沙门菌粉分离株,应测试并报告一种三代头孢菌素,假如需要,也可测试和报告氯霉素。分离于肠道内和肠道外伤寒样沙门菌(伤寒沙门菌和副伤寒沙门菌A-C)需进行药敏试验。分离于肠道内非伤寒样沙门菌不需进行常规药敏试验。 F.从CSF中分离菌株,试验和报告头孢噻肟和头孢曲松,以取代头孢唑林。 G.其他非肠杆菌科细菌包括假单胞菌和其他非苛养、非发酵葡萄球菌的革兰阴 性杆菌,但不包括铜绿假单胞菌、不动杆菌、洋葱伯克霍尔德菌和嗜麦芽窄食单胞菌,因为对这些菌种的建议试验和报告药物表格已分开。 鼻疽伯克霍尔德菌和假鼻疽伯克霍尔德菌试验和报告药物建议请参阅CLSIM45文件。 H.仅对金黄色葡萄球菌包括耐甲氧西林金黄色葡萄球菌(MRSA) I.青霉素敏感的葡萄球菌对葡萄球菌感染具有临床疗效的其他β-内酰胺类药 物也敏感。青霉素耐药葡萄球菌对青霉素酶不稳定青霉素类耐药。除具有抗-MRSA活性新的头孢菌素外,苯唑西林耐药葡萄球菌对当前所有使用的β-内酰胺类药物均耐药。因此,仅测试青霉素和头孢西丁或苯唑西林二者中任一种,则可推测对各种β-内酰胺类药物的敏感或耐药性。除具有抗-MRSA 活性药物外,不建议常规测试其他β-内酰胺类药物。
教你看懂药敏和菌培报告单! 药敏试验是如何测定的根据美国临床标准委员会 推荐的纸片扩散法测定。将含有一定量抗菌药的纸片贴在涂有细菌的琼脂平板表面,35℃培养过夜,测量纸片周围抑菌圈的大小确定细菌对药物的敏感性,抑菌圈越大敏感性越高。不同细菌对不同抗菌药敏感性的判定标准不同,例如头孢噻肟对肠杆菌科细菌的抑菌圈≤14 mm为R, 15 mm-22 mm为I,≥23 mm为S;苯唑西林对金黄色葡萄球菌抑菌圈≤10 mm 为R, 11 mm-12 mm为I, ≥13 mm为S。药敏试验报告中S、I、R 指的是什么S(susceptible),是指细菌对抗菌药敏感,使用常规剂量时的平均血浓度超过MIC 5倍以上,用常规剂量通常有效; I(intermediate)是指细菌对抗菌药中度敏感,常规剂量时平均血浓度等于或略高于MIC,需用高剂量或对体内药物浓缩部位的感染可能有效; R(resistance)是指细菌对某种抗菌药耐药,药物对细菌的MIC 高于应用常规剂量时的血浓度,应用常规剂量治疗通常无效。测试抗菌药物的品种是如何选定的抗菌药有近200种,药敏试验中没必要也不可能包括每种抗菌药。所测试的抗菌药纸片的种类是根据各类细菌对抗菌药的敏感性 及临床可能选用的药物而确定的,同类药物通常只选择1-2
个代表品种。NCCLS对各种细菌的药敏试验中宜测试的药物品种进行了推荐,如测定葡萄球菌属的药敏试验应包括苯唑西林、青霉素、红霉素、克林霉素、复方磺胺甲噁唑(SMZ-TMP)和万古霉素;此外可根据情况增加其他品种如氯霉素、环丙沙星、庆大霉素、利福平和呋喃妥因等。为什么肠球菌属细菌药敏报告的测定药物这么少对头孢菌素类和多种抗菌药天然耐药,故药敏试验中所包括的抗菌药品种较少,NCCLS 推荐的测试品种为氨苄西林或青霉素、万古霉素(去甲万古霉素),此外亦可增加庆大霉素、氯霉素、红霉素、利福平、环丙沙星和呋喃妥因等,后两者适用于尿标本。 细菌对多种抗菌药物敏感时,如何选择最有效药物应根据感染部位、病情严重程度、药物的抗菌作用及药动学特点选择抗菌药。是否所有阳性培养均有临床意义 并非所有阳性培养都是真正的病原菌,原因可能有: ①所报告细菌为污染菌,细菌培养结果的临床意义大小与所取标本有关,如为关节液、胸腔积液、等无菌标本则临床意义较大,但即使血培养阳性也可能为污染菌,据报道单次血培养凝固酶阴性葡萄球菌、草绿色链球菌、肠球菌阳性,污染可能性分别为85%、52%、22%。某些标本易受污染如痰标本易于受咽喉部携带菌的污染,尿培养易受下尿道、尿道口寄居菌污染。②可能为应用抗菌药后的菌群交替,
药敏试验结果解读及临床应用 一、药敏试验的目的 药敏试验是使用体外试验的方法检测细菌的耐药性,预测抗菌药物的临床治疗效果,在药物种类的选择上为临床医生提供帮助,以实施个体化治疗。 当前,“对症下药”已经变得难以奏效。首先,致病菌的种类发生了改变,一种疾病可以由多种病原菌所引起,包括致病菌和条件致病菌;其次,感染人群发生变化,从健康人群到老年人、长期使用激素、免疫抑制剂及放疗、化疗的人群,临床症状常常不典型;最后,早期不规使用抗生素,也会导致临床症状不典型。 与此同时,“对菌下药”又难以获得满意效果。耐药菌尤其是多重耐药菌的出现,使临床医师按照抗生素的作用机制选择1~2种抗菌药物不能覆盖常见的病原菌。因此,药敏试验成为临床工作的重要手段之一。 二、哪些细菌需要做药敏试验? 对任何分离的可疑病原菌,若不能从该菌的种属特征可靠地推知其对抗菌药物的敏感性,就需要进行药敏试验。以下情况不必进行药敏试验:正常定植菌与感染的关系不明确时;污染菌;已知细菌对某种抗生素天然耐药;已知细菌对某种抗生素全部敏感。检验地带网三、药敏试验中药物的选择 主要根据细菌种类和抗生素作用机制选药。选择试验的药物应具有确切的临床疗效,试验药物的体外试验结果可以接受,并且试验药物具有代表性。 目前我国临床实验室采用美国国家标准化委员会(NCCLS)/美国临床实验室标准化研究所(Clinical and Laboratory Standards Institute , CLSI)药敏试验执行标准选药。NCCLS抗生素选择分组为: A组:为首选药物,作常规试验和报告。 B组:为首选药物,可与A组药物平行作药敏试验,但只在以下情况下进行选择性报告:细菌对A组抗生素耐药,病人对A组抗生素过敏,严重感染或多部位、多种细菌混合感染,要获得耐药性监测资料。 C组:为备选药物,作为替代或补充,在下列情况下使用:对一个或多个首选药耐药的地区流行株感染,对不常见菌感染的治疗,控制传染病的流行,获得耐药性监测资料。 U组:为备选药物,仅用于尿路感染的治疗。 四、药敏试验所采用的方法 常用的试验方法包括纸片扩散法、稀释法、自动化仪器法、E-TEST(浓度梯度法)。 五、细菌的主要耐药机制 1、产生水解酶,如β-酰胺酶、钝化酶。 2、细菌上与抗生素的结合靶位改变,如青霉素结合蛋白2a。 3、细菌表面通道蛋白改变,可以使其渗透性发生改变。 4、细菌产生泵出机制。 5、其他机制,如病原菌产生生物被膜、休眠状态等。 六、临床常见病原菌的归属和分类 临床常见病原菌主要包括以下四大类: 1、革兰阳性球菌:如葡萄球菌属、肠球菌属。 2、革兰阴性杆菌:如肠杆菌科细菌(大肠埃希菌、肺炎克雷伯菌、肠杆菌属、枸橼酸杆菌属)和非发酵菌(铜绿假单孢菌、不动杆菌)。