
物理化学实验最大气泡压力法测定溶液表面张力C210 2010-04-12
T=286.15K P=85.02kPa
一、实验目的
1.掌握最大气泡法测定溶液表面张力的原理和方法
2.测水溶液的表面张力并计算定不同浓度正丁醇计算吸附量
3.加深对表面张力、表面自由能、表面张力和吸附量关系的理解
二、实验原理
处于溶液表面的分子,受到不平衡的分子间力的作
用而具有表面张力s.
气泡最大压力法测定表面张力装置见实物;实
验中通过滴水瓶滴水抽气使得体系压力下降,大气压与
体系压力差△p逐渐把毛细管中的液面压至管口,形成
气泡。如果毛细管半径很小,则形成的气泡基本上是
球形的;当气泡开始形成时,表面几乎是平的,这时曲
率半径最大;随着气泡的形成,曲率半径逐渐变小,直到
形成半球形,这时曲率半径R和毛细管半径r相等,曲
率半径达最小值,根据拉普拉斯公式得:附加压力达最大
值ΔP max =σ/r min。气泡进一步长大,R变大,附加压力
则变小,直到气泡逸出。
加入表面活性物质时溶液的表面张力会下降,溶质
在表面的浓度大于其在本体的浓度,此现象称为表面吸
附现象;
单位溶液表面积上溶质的过剩量称为表面吸附量Γ, Γ=-(c/RT)*( dσ/dc).
对可形成单分子层吸附的表面活性物质,溶液的表面吸附量Γ与溶液本体浓度c之间的关系符合朗格谬尔吸附等温式: Γ=Γ∞*kc/1+kc
朗格谬尔吸附等温式的线性形式为: c/Γ=c/Γ∞+1/kΓ∞
Γ∞为饱和吸附时,单位溶液表面积上吸附的溶质的物质的量,则每个溶质分子在溶液表面上的吸附截面积为:A m=1/(N A*Γ∞)
三、仪器与试剂
恒温槽装置;数字式微压差计;
抽气瓶l个;表面张力测定仪
烧杯(1000mL);T形管1个;
电导水;
正丁醇(A.R.)及其不同浓度的标准溶液;
四、实验步骤
1.仪器常数的测定
将表面张力测定仪清洗干净;在干净的表面张力测定仪中装入电导水,使毛细管上端塞子塞紧时,毛细管刚好与液面垂直相切;抽气瓶装满水,连接好后旋开下端活塞使水缓慢滴出;控制流速使气泡从毛细管平稳脱出(每个气泡4-6秒),记录气泡脱出瞬间数字微压差计的最大数值,取三次并求平均值。
2.测定正丁醇溶液的表面张力
用同样的方法测定不同浓度的正丁醇溶液的最大压差,由稀到浓依次测定;每个浓度的溶液测量前,表面张力测定仪和毛细管一起用该溶液荡洗二至三次;每份溶液恒温至少3-5min之后,开始读数。3. 重复测定电导水的数据。
注意事项:仪器系统不能漏气;测定用的毛细管一定要洗干净,否则气泡可能不能连续稳定的流过,而使压差计读数不稳定,如发生此种现象,毛细管应重洗;毛细管端口一定要刚好垂直切入液面,不能离开液面,但亦不可深插;在数字式微压差测量仪上,应读出气泡单个逸出是的最大压力差;正丁醇溶液要准确配置,使用过程防止挥发损失;从毛细管口脱出气泡每次应为一个,即间断脱出;表面张力和温度有
关,因此要等溶液恒温后再测量。 五、实验记录及数据处理 恒温槽温度298.25K
1. 查室温下水的表面张力 s( H 2O ) (25℃、σH2O =71.97dyn/cm = 71.97mN/m ) 计算仪器常数: k=σ/ΔP max =71.97e-3/5204=1.38297e-5m r=6.915e-6m
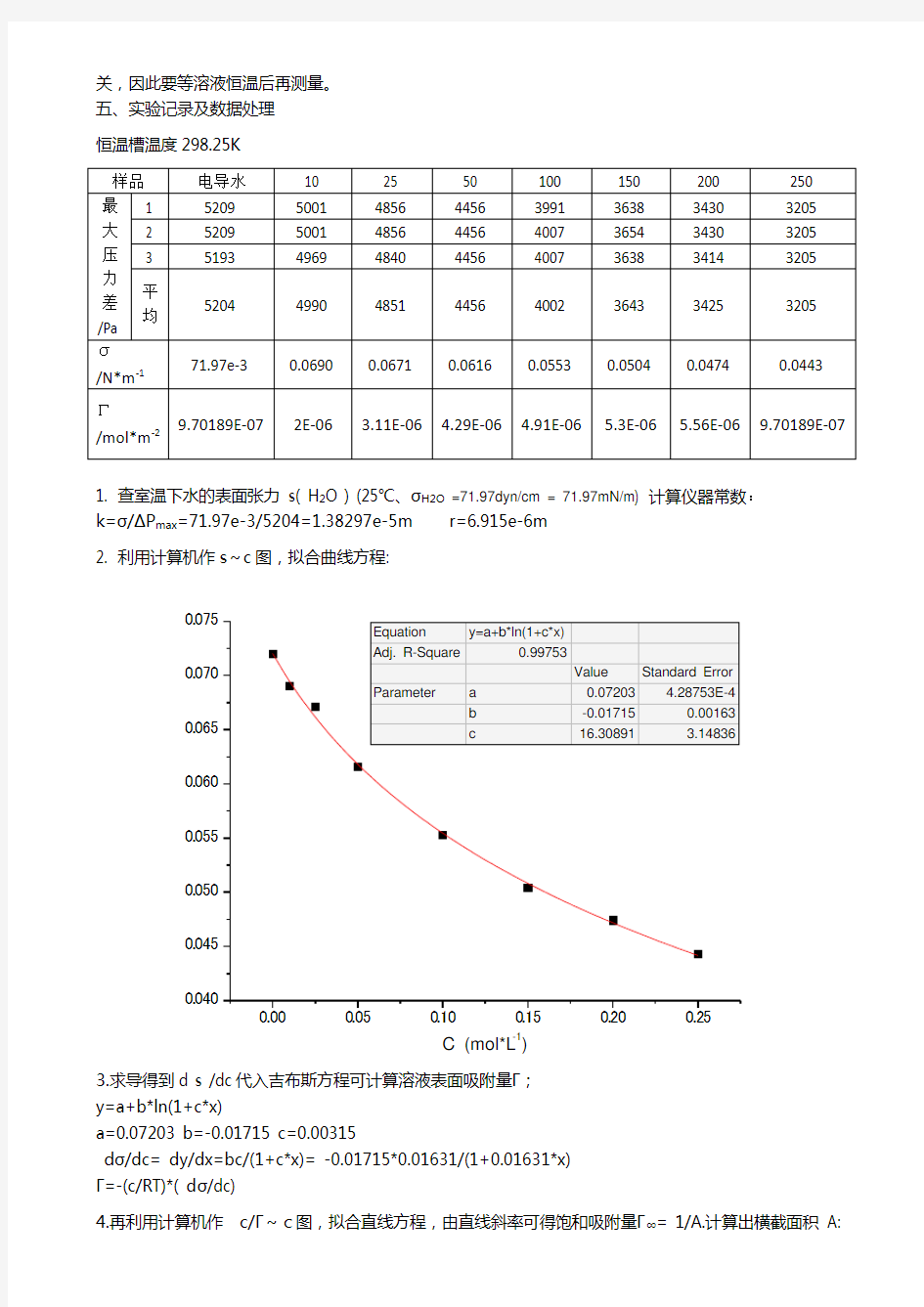
2. 利用计算机作s ~c 图,拟合曲线方程:
0.040
0.0450.0500.0550.0600.0650.070
0.075σ (N *m -1
)
C (mol*L -1
)
3.求导得到d s /dc 代入吉布斯方程可计算溶液表面吸附量Γ; y=a+b*ln(1+c*x)
a=0.07203 b=-0.01715 c=0.00315
d σ/dc= dy/dx=bc/(1+c*x)= -0.01715*0.01631/(1+0.01631*x) Γ=-(c/RT)*( d σ/dc)
4.再利用计算机作 c/Γ~c图,拟合直线方程,由直线斜率可得饱和吸附量Γ∞= 1/A.计算出横截面积 A:
Γ∞=6.9186 e-6 mol*m-2
A m=1/(L*Γ∞)=2.24e-19m2
六、思考题
1.本实验结果的准确与否关键决定于哪些因素?
仪器系统的气密性;测定用的毛细管是否干净,实验中气泡是否平稳流过;毛细管端口一定要刚好垂直切入液面,不能离开液面,但亦不可深插(1mm的水柱产生的压强约是10pa);从毛细管口脱出气泡每次应为一个,即间断脱出;表面张力和温度有关,要等溶液恒温后再测量。
2.毛细管内径均匀与否对结果有无影响?
P s dV=σdA s dA s=8πRdR dV=4πR2dR Ps=2σ/R 曲率半径愈小,受到的附加压力愈大,曲率半径等于毛细管口半径时,附加压力最大,再测定的时毛细作用中吸入的液体的量与内径均匀程度有关,所以有影响。
3.气泡如出的很快或连续3-4个一齐出,对结果各有什么影响?毛细管尖端为何要刚好接触液面?
气泡出的很快,压强变化过快,压差计将不能很好的响应压强的变化;气泡连续出会导致压差计读数不稳定。离开液面将不会有气泡产生,
4.本实验s-c图形应该是一怎样的图形?将所得的结果与手册上查到结果进行比较试分析产生误差的原因。
s-c图形应该是一条曲线,物质不同曲线不同
从毛细管口脱出气泡每次应为一个,控制的不是很好,测出的数据有16pa的偏差。
七、实验讨论
1.如果液面是弯曲,其表面的作用力不是水平的,将有一个合力,当液面为凸时,合力指向液体内部,当液面为凹时,合力指向液体外部,这就是附加压力的来源。由于附加压力而引起的液面与管外液面有高度差的现象称为毛细管现象。
2.毛细管清洁处理应特别的予以重视,热风吹干及电炉烘烤的办法应当避免,荡洗是好办法,但应尽量彻底。毛细管内部可借助洗耳球,但必须细心,不应使液体进入洗耳球内。
在实验中,按浓度从小到大的顺序测定,降低不同浓度溶液之间的影响。
3. 测定液体表面张力除气泡的最大压力法外,常用的还有毛细管上升法、滴重法等。
4. Γ>0 正吸附,Γ<0 负吸附,Γ=0 无吸附作用,
5.数据处理用不同的软件,得到的结果有一定的差别,Excel2003、2007、及WPS的拟合结果会有一点差别,更精确的数据处理软件是Origin和Matlab
6.实验中观察毛细管的半径是比较大的,在洗毛细管时不用洗耳球,液体就可流下,但计算得到的半径是r=6.915e-6m相当的小。
溶液中的吸附作用和表面张力的测定 ——最大气泡压力法 【摘要】本实验采用最大气泡压力法测定了一系列不同浓度的正丁醇溶液的表面张力,并根据Gibbs吸附公式和Langmuir等温方程式的到了表面张力与溶液吸附作用的关系,用作图法求出了正丁醇分子横截面积,从实验上进一步了解表面张力的性质以及表面张力和吸附的关系,并得到了一个测量表面张力的简单有效而又精确的方法。 【关键词】最大气泡法表面张力吸附作用 一、前言 正丁醇是一种表面活性物质,可以使溶液表面张力下降。利用最大气泡压力法,可以测量出正丁醇溶液的表面张力。根据表面张力与气泡压力的关系,由σ-c曲线可以求出溶液界面上的吸附量和单个正丁醇分子的横截面积(S)。 1、物体表面的分子和内部分子能量也不同,表面层的分子受到向内的拉力,有自动缩小的趋势,表面分子的能量比内部分子大。体系产生新的表面(A)所需耗费功(W)的量,其大小应与A成正比。在等温下形成1m2新的表面所需的可逆功为,称为单位表面的表面能,其单位为N·m-1,通常称为表面张力。 2、纯液体情形下,表面层的组成与内部的组成相同,因此液体降低体系表面自由能的途径是缩小其表面积。对于溶液,溶质会影响表面张力,调节溶质在表面层的浓度来降低表面自由能。根据能量最低
原理,溶质能降低溶液的表面张力时,表面层中溶质的浓度应比溶液内部大。反之同理 。这种表面浓度与溶液里面浓度不同的现象叫“吸附”。 Gibbs 用热力学的方法推导出吸附与溶液的表面张力及溶液的浓度间的关系式 =T c RT c ??? ??- ??σ 当( )?σ ?c T <0时, >0,称为正吸附。反之,( )?σ ?c T >0时, <0,称 为负吸附。 正丁醇溶液浓度极小时,溶质分子平躺在溶液表面上,当浓度增加到一定程度时,被吸附了的表面活性物质分子占据了所有表面形成了单分子的饱和吸附层。 在一定温度下,吸附量与溶液浓度之间的关系由Langmuir 等温方程式表示:ΓΓ=?+?∞K C K C 1 或 C C K ΓΓΓ=+ ∞∞ 1 以 C Γ ~C 作图可得一直线,由直线斜率即可求出Γ∞。在饱和吸附情况下,正丁醇分子在气-液界面上铺满一单分子层,则可求得正丁醇分子的横截面积S N 01 = ∞Γ~ 3、最大气泡压力法:当表面张力仪中的毛细管截面与欲测液面相齐时,液面沿毛细管上升。当此压力差在毛细管端面上产生的作用 力稍大于毛细管口溶液的表面张力时,气泡就从毛细管口逸出。 张力与浓度的关系图
表面张力的测量方法 英才学院 1236305 张雍淋 6121810519 液体表面张力测量在化学、医药、生物工程等领域具有重要意义, 根据液体表面张力的大小可以确定表面活性并计算表面活性剂在溶液表面的吸附量;在合金液体体系中,借助于表面张力还可以评价金相组织及孕育效果等重要参数。目前,测量液体表面张力系数有毛细上升法、最大气泡压力法、液滴法等。 1. 毛细上升法 这个方法,研究的比较早,在理论和实际上都比较成熟。如图 1所示,干净的毛细管浸入液体内部时,如果液体间的分子力小于液体与管壁间的附着力,则液体表面呈凹形。此时表面张力产生的附加力为向上的拉力,并使毛细管内的液面上升, 直到液柱的重力与表面张 力相平衡。 图 1 212cos ()g r r gh πσθπρρ=- 1()2cos g ghr ρρσθ-=
其中:σ—液体的表面张力;r-毛细管的内径;θ-接触角; ρ 1ρ-液体和气体的密度;h-液柱的高度;g-当地的重力加速度。在 和 g 实际应用中一般用透明的玻璃管,如果玻璃被液体完全润湿,可以近似的认为θ= 0。 毛细上升法是测定表面张力最准确的一种方法,国际上也一直用此方法测得的数据作为标准。应用此方法时,要注意选择管径均匀, 透明干净的毛细管,并对毛细管直径进行仔细的标定;毛细管要经过仔细彻底的清洗,毛细管浸入液体时要与液面垂直。 2.最大气泡压力法 如图 2 所示,向插入液体的毛细管轻轻的吹入惰性气体(如 N 2等)。如果选用的毛细管半径很小,在管口形成的气泡基本上是球形的。并且当气泡为半球时,球的半径最小等于毛细管半径 r ;在其前后曲率半径都比r大,如图2 所示。当气泡为半球时,泡内的压力最大,管内外最大压差可由差压计测量得到。 图2
最大气泡压力法测定溶液表面张力 实验日期:2013/4/1 一、数据记录 室温:24.5℃ 压强:82.83kPa 测量温度:25±0.1℃ 单位:Pa 项目 组数 1 2 3 ave 电导水 676 671 676 674.33 0.01M 659 657 657 657.67 O.O25M 631 630 630 630.33 0.05M 573 574 573 573.33 0.1M 513 516 516 515.00 0.15M 464 464 464 464.00 0.2M 430 431 433 431.33 0.25M 401 402 401 401.33 0.5M 313 311 315 313.00 二、数据处理 1、电导水的气泡压力 次数 1 2 3 平均值 压强差/Pa 676 671 676 674 由化学手册查得20℃下,水的表面张力为0.0728 N/m , △P=610 Pa ,求得毛细管常数 2、正丁醇气泡压力 浓度/ mol/L 气泡最大压力差 △P/ Pa 表面张力σ N/m 1 2 3 平均值 0.01 659 657 657 657.67 7.10E-02 0.025 631 630 630 630.33 6.81E-02 0.05 573 574 573 573.33 6.19E-02 0.10 513 516 516 515.00 5.56E-02 0.15 464 464 464 464.00 5.01E-02 0.20 430 431 433 431.33 4.66E-02 0.25 401 402 401 401.33 4.33E-02 0.50 313 311 315 313.00 3.38E-02 计算正丁醇表面张力的公式: m P K 41008.1674 0728 .0-?==?=σP *K ?=σ
液体表面张力的测定 龚聪(同组人:郭舒隽) 2012.11.8 摘要 我们采用最大气泡压力法测定了不同浓度正丁醇溶液的表面张力,发现随着溶液浓度的升高,表面张力下降,说明正丁醇是一种表面活性物质。 引言 从毛细管鼓出空气泡时,为了克服溶液因表面张力产生的附加压力,毛细管内的压力(大气压)要高于样品管中的压力。附加压力与表面张力成正比,与气泡的曲率半径成反比: 2p= r σ?(1),其中,p ?为附加压力;σ为表面张力;r 为气泡的曲率半径。若毛细 管很小,则形成的气泡基本上是球形的。当气泡开始形成时,表面几乎是平的,这时气泡的半径r 最大;随着气泡的形成,r 逐渐变小,直到气泡成为半球形时,r 等于毛细管的半径R ,附加压力最大,气泡进一步增大,r 变小,附加压力减小,直到气泡逸出。 最大的附加压力m ax 2=p R σ?(2),表面张力m ax =2 R p σ?(3)。 在测量过程中,我们使毛细管端面与液面相切,这样可以忽略鼓泡所需克服的静压力,表面张力可直接用式(3)计算。 对于同一支毛细管, 2 R 称为仪器常数,可用K 表示。我们用表面张力已知的标准物质 ——水来测定仪器的K 值:22= H O H O K p σ?(4)。式(3)可写为m ax =K p σ??(5)。 实验仪器与试剂 表面张力测定仪1套;100m L 容量瓶8个;500m L 烧杯一个;胶头滴管1个;洗瓶1个;碱式滴定管1支 -1 0.5mol L ?正丁醇溶液 实验装置如下图所示
方法 1. 正丁醇溶液的配制 分别向八支100m L 的容量瓶中加入4、8、12、16、20、28、36和40mL 的-10.5mol L ?正丁醇溶液,定容以配制0.02、0.04、0.06、0.08、0.10、0.14、0.18和0.20-1mol L ?的待测溶液并编号0-8。 2. 仪器常数K 的测定 洗净样品管和毛细管; 样品管中装入适量蒸馏水,调节样品管液面高度,使水面与毛细管端面相切; 打开数字压力计电源开关,旋转滴液漏斗上的活塞,使系统与大气相通,按下数字压力计上的“采零”键。关闭活塞,隔绝大气,打开漏斗活塞,水沿漏斗流下,系统的压力开始减小,此时有气泡从毛细管端逸出。控制出气泡的速度,每出一个气泡,压力计读数由小变大,再由大变小,读取6~7个该过程的最大示数。 3. 测定不同浓度正丁醇水溶液的m ax p ? 按照步骤2,从低浓度到高浓度分别测定正丁醇水溶液的m ax p ?。更换溶液时用待测溶液润洗样品管2~3次。 4. 关闭电源,倒掉所配溶液,用蒸馏水洗涤容量瓶和样品管。整理仪器。 数据 表格 1 计算 在本次实验条件下,标准物质—水在16.4°C 下的表面张力为-3 -1 68.7410N m ??。1 由式(4)得仪器常数22-3-4 3 68.7410 = = =2.18100.315010 H O H O K p σ???? 1 数据来源:《大学化学实验——有机及物理化学实验分册》(天津大学出版社)附录三,附表6-13
4+ 总的来说,报告做得很整齐,在内容上应该更加用心改进。 实验报告 实验题目:焦利氏秤法测量液体的表面张力 实验目的:学习并掌握用焦利氏秤法测量液体的表面张力的方法,加深对液 体表面张力的理解。 实验原理: 液体表层内分子力的宏观表现,使液面具有收缩的趋势。想象在液面上划一条线,表面张力就表现为直线两侧的液体以一定的拉力相互作用。这种张力垂直于该直线且与线的长度成正比,比例系数称为表面张力系数。 把金属丝AB 弯成如图 (a)所示的形状,将其悬挂在灵敏的测力计上,浸到液体中,缓缓提起测力计时,金属丝就会拉出一层与液体相连的液膜,由于表面张力的作用,测力计的读数逐渐达到一最大值F (超过此值,膜即破裂)。。由于液膜有两个表面,若每个表面的力为F ',则由 '2F mg F += 得 2 'mg F F -= (1) 表面张力F ’的大小与分界线的长度成正比。即 l F σ=' (2)
σ称为表面张力系数,单位是N/m 。表面张力系数与液体的性质,杂质和温度有关。测定表面张力系数的关键是测量表面张力F ',应用焦利氏秤液膜即将破裂可以方便地测量表面张力F '。 实验器材:焦利氏秤,自来水,肥皂水,金属丝,金属圈,钢板尺。 实验内容: 1、确定焦利氏秤上锥形弹簧的劲度系数k ; 2、测量自来水的表面张力系数; 3、测量肥皂水的表面张力系数。 数据记录处理: 1、确定焦利氏秤上锥形弹簧的劲度系数k m/g 0.0 0.5 1.0 1.5 2.0 2.5 3.0 3.5 4.0 4.5 5.0 x/cm 2.87 3.38 3.86 4.36 4.88 5.42 5.93 6.48 7.00 7.53 8.06 (1)作图法: 1 2 3 4 5 m/g x/cm 我仔细看了一下图,有个疑问,在m=0g ,应该x=2.87cm ,但是从图例反应出的是m=0g ,x=0cm ,是不是x 坐标轴没有设置对?? (2)由作图法,计算斜率得k1=0.957g/cm=0.937N/m
一、实验目的 1.掌握最大气泡压力法测定表面张力的原理与技术。 2.通过对不同浓度乙醇溶液表面张力的测定,加深对表面张力、表面自由能、表面张力与吸附量关系的理解。 二、实验原理 1、在一定温度下纯液体的表面张力为定值,当加入溶质形成溶液时,表面张力发生变化,其变化的大小决定于溶质的性质与加入量的多少。根据能量最低原理,溶质能降低溶剂的表面张力时,表面层溶质的浓度比溶液内部大;反之,溶质使溶剂的表面张力升高时,它在表面层中的浓度比在内部的浓度低,这种表面浓度与内部浓度不同的现象叫做溶液的表面吸附。在指定的温度与压力下,溶质的吸附量与溶液的表面张力及溶液的浓度之间的关系遵循吉布斯吸附等温式: Γ = –(c/RT)*(dγ/dc)① 式中,Г为溶液在表层的吸附量;γ为表面张力;c为吸附达到平衡时溶液在介质中的浓度。 根据朗格谬尔(Langmuir)公式: Γ =Γ∞Kc/(1+Kc)② Γ∞为饱与吸附量,即表面被吸附物铺满一层分子时的Γ∞ c/Γ =(1+Kc)/(Γ∞K)= c/Γ∞+1/Γ∞K ③ 以c/Г对c作图,则图中该直线斜率为1/Г∞。 由所得的Г∞代入A m=1/Г∞L可求被吸附分子的截面积(L为阿伏伽德罗常数)。 2、本实验用气泡最大压力法测定溶液的表面张力,其仪器装置如图1所示: 图1、最大气泡压力法测量表面张力的装置示意图 1、恒温套管; 2、毛细管(r在0.15~0.2mm); 3、U型压力计(内装水); 4、分液漏斗; 5、吸滤瓶; 6、连接橡皮管。
将待测表面张力的液体装于表面张力仪中,使毛细管的端面与液面相切,液面即沿毛细管上升,打开抽气瓶的活塞缓缓抽气,毛细管内的液面上受到一个比A瓶中液面上大的压力,当此压力差——附加压力(△P=P大气–P系统)在毛细管端面上产生的作用力稍大于毛细管液体的表面张力时,气泡就从毛细管口脱出,此附加压力与表面张力成正比,与气泡的曲率半径成反比,其关系式为: ΔP=2γ/R ④ 式中,ΔP为附加压力;γ为表面张力;R为气泡的曲率半径。 如果毛细管半径很小,则形成的气泡基本上是球形的。当气泡开始形成时,表面几乎是平的,这时曲率半径最大;随着气泡的形成,曲率半径逐渐变小,直到形成半球形,这时的曲率半径R与毛细管的半径r相等,曲率半径最小值,根据上式这时附加压力达最大值。气泡进一步长大,R变大,附加压力则变小,直到气泡逸出。 根据上式,R=r时的最大附加压力为: ΔP最大= 2γ/r ⑤ 实际测量时,使毛细管端刚与液面接触,则可忽略气泡鼓起所需克服的静压力,这样就可以直接用上式进行计算。 当将其它参数合并为常数K时,则上式变为: γ=KΔP最大⑥ 式中仪器常数K可用已知表面张力的标准物质测得。 三、仪器药品 1、仪器:最大泡压法表面张力仪1套,洗耳球1个,移液管(50ml与10ml)各一支,烧杯(500mL)。 2、药品:正丁醇(分析纯),蒸馏水。 四、实验步骤 1、仪器的准备与检漏 将表面张力仪容器与毛细管先用洗液洗净,再顺次用自来水与蒸馏水漂洗,烘干后按图5-9接好,检查是否漏气。 2、仪器常数的测定 调节液面与毛细管相切,并调节分液漏斗,使气泡由毛细管尖端成单泡逸出,且速度控制在每分钟形成气泡5~10个(数显微压差测量仪为5~10s),当气泡刚脱离管端的一瞬间,压力计中液位差达到最大值,当显示的最大值比较稳定时,记下数据,重复调节2次并记下相应的数值。再由手册查出实验温度时水的表面张力,求得仪器常数K。 3、表面张力随溶液浓度变化的测定
学号:201114120222 基础物理化学实验报告 实验名称:溶液表面张力的测定 应用化学二班班级 03 组号 实验人姓名: xx 同组人姓名:xxxx 指导老师:杨余芳老师 实验日期: 2013-11-12 湘南学院化学与生命科学系 一、实验目的
1、测定不同浓度正丁醇(乙醇)水溶液的表面张力; 2、了解表面张力的性质,表面自由能的意义及表面张力和吸附的关系; 3、由表面张力—浓度曲线(σ—c 曲线)求界面上吸附量和正丁醇分子的横截面积S ; 4、掌握最大气泡法测定表面张力的原理和技术。 二、实验原理 测定液体表面张力的方法很多,如毛细管升高法、滴重法、环法、滴外形法等等。本实验采用最大泡压法,实验装置如图一所示。 图一中A 为充满水的抽气瓶;B 为直径为0.2~0.3mm 的毛细管;C 为样品管;D 为U 型压力计,内装水以测压差;E 为放空管;F 为恒温槽。 图一 最大泡压法测液体表面张力仪器装置图 将毛细管竖直放置,使滴口瓶面与液面相切,液体即沿毛细管上升,打开抽气瓶的活栓,让水缓缓滴下,使样品管中液面上的压力渐小于毛细管内液体上的压力(即室压),毛细管内外液面形成一压差,此时毛细管内气体将液体压出,在管口形成气泡并逐渐胀大,当压力差在毛细管口所产生的作用力稍大于毛细管口液体的表面张力时,气泡破裂,压差的最大值可由U 型压力计上读出。 若毛细管的半径为r ,气泡从毛细管出来时受到向下的压力为: 式中,△h 为U 型压力计所示最大液柱高度差,g 为重力加速度,ρ为压力计所贮液体的密度。 气泡在毛细管口所受到的由表面张力引起的作用力为2πr?γ,气泡刚脱离管口时,上述二力相等: 若将表面张力分别为和的两种液体用同一支毛细管和压力计用上法测出各 g h p p p ρ?=-=系统大气m ax r g h r p rr πρππ22m ax 2=?=γπρππr g h r p r 22m ax 2 =?=g h r ργ?=2
实验报告 班级微电子101姓名贺鸿浩学号10105110 日期2011.10.24 室温26.2℃气压102.29kpa成绩教师 实验名称液体表面张力系数的测量 【实验目的】 1.了解液体表面性质 2.学习采用液体表面张力系数测定仪的使用方法 3.学习用拉脱法测表面张力系数的原理和方法 【实验仪器】 液体表面张力测定装置、砝码盘和砝码、圆环型吊片、卡尺、温度计 图1液体表面张力测定装置 【实验原理】 1. 拉脱法 测量一个已知周长的金属圆环或金属片从待测液体表面脱离时所需的拉力,从而求得该液体表面张力系数的方法称为拉脱法。所需的拉力是由液体表面张力、环的内外径及液体材质、纯度等因素决定。 2. 吊环法和吊片法比较 (1)吊环法:使用金属细线制成吊环时,在液膜被拉破的瞬间接触角不接近于零,此时所测得的力是表面张力向下的分量,因而所得表面张力系数误差较大,必须用修正公式对测量结果进行修正。 (2)吊片法:虽然液膜被拉破的瞬间接触角趋近于零,但在具体测量时,由于吊片在拉脱
过程中容易发生倾斜,实验时吊片的长度上限为3—4cm ,而在测量力时,则希望力大 一点,有利于提高测量精确度。 (3)片状吊环:新设计有一定厚度的片状吊环。经过对不同直径吊环的多次试验,发现当 吊环直径等于或略大于 3.3cm 时,在液膜被拉破的瞬间液体与金属环之间的接触角接 近于零,此时接触面总周长约为20cm 左右。在保持接触角为零时,能得到一个 较大的待测力。 3. 实验原理 使用片状吊环,在液膜拉破前瞬间,考虑一级近似,认为液体的表面张力为: f = f 1 + f 2 = αл(D 1+ D 2) 这里α为表面张力系数,D 1、D 2分别为吊环的外径和内径。 片状吊环在液膜拉破前瞬间有: 此时传感器受到的拉力F 1和输出电压U 1成正比,有: U 1 = BF 1 片状吊环在液膜拉破后瞬间有: F 2 = mg 同样有 U 2 = BF 2 片状吊环在液膜拉破前后电压的变化值可表示为: U 1- U 2 = △U = B · △F = B (F 1- F 2)= B αл(D 1+ D 2) 由上式可以得到液体的表面张力系数为:1212() U U B D D απ-=+ 这里U 1:液膜拉断前瞬间电压表的读数,U 2:膜拉断后瞬间电压表的读数 实验内容(用拉脱法测量水的表面张力): 1.力敏传感器进行定标,用最小二乘法作直线拟合,求 出传感器灵敏度B 。 2.游标卡尺测量金属圆环的内、外直径。 3.金属环状吊片挂在传感器的小钩上,调节升降台,将 液体升至靠近环片的下沿,观察环状吊片下沿与待测液面 是否平行,将金属环状吊片取下后,调节吊片上的细丝, 使吊片与待测液面平行。(注意 :吊环中心、玻璃皿中心 最好与转轴重合。) 4.调节容器下的升降台,使其渐渐上升,将环片的下沿部分全部浸没于待测液体。然后反 向调节升降台,使液面逐渐下降。这时,金属环片和液面间形成一环形液膜,出现“浸润” 现象,继续下降液面,测出环形液膜即将拉断前一瞬间数字电压表读数值 U1和液膜拉断后 一瞬间数字电压表读数值U2。(注意 :液膜断裂应发生在转动的过程中,而不是开始转动 或转动结束时,因为此时振动较厉害,应多次重复测量。) 【实验步骤】 1.开机预热(15分钟) 2.将水盛入玻璃器皿内(1cm 左右),用双面胶与升降台面贴紧固定。 3.将砝码盘挂在力敏传感器的钩上 图2液膜的收缩
实验D-13 滴重法测定液体的表面张力 实验目的 用滴重法测量液体的表面张力,学会用校正因子表,迭代计算毛细管的半径。 实验原理 当液体在滴重计(滴重计市售商品名屈氏粘力管)口悬挂尚未下滴时: r :若液体润湿毛细管时为外半径,若不润湿时应使用内半径。 σ: 液体的表面张力。 m :液滴质量(一滴液体)。 g ;重力加速度,当采用厘米.克.秒制时为 981cm /S 2 但从实际观察可知,测量时液滴并未全部落下,有部分收缩回去,故需对上式进行校正: m ’为滴下的每滴液体质量(用分析天平称量)。 f 称为哈金斯校正因子,它是r /v 1/3 的函数;v 是每滴液体的体积;可由每滴液体的质 量除液体密度得到。在上式中r 和f 是未知数,可采用已知表面张力的液体(如蒸馏水)做实验,采用迭代法得到: 设每滴水质量为m ’,体积为v ;先用游标卡尺量出滴重计管端的外直径D ;可得半 径r 0;用r 0作初值;求得r 0/ v 1/3 ;查哈金斯校正因子表(插值法)得f 1;用水的表面 张力σ和f 1代入12'r f m g πσ=;求的第一次迭代结果r 1;再由r 1/ v 1/3 查表得f 2 ;再代 入: 22'r f m g πσ=求得第二次迭代值r 2,同法再由r 2/ v 1/3 代入查表求f 3 ,这样反复迭代 直至相邻两次迭代值的相对误差:┃(r i-1-r i )/ r i ┃≤eps (eps 表示所需精度,如1‰)这时的r 就是要求的结果,记录贴在滴重管上的标签上,半径就标定好了。 求得半径r 后,对待测液体只要测得每滴样品重和密度,就可由r/ v 1/3查表得f ;由: 2'r f m g πσ= 就可求得样品的表面张力。 纯水的表面张力见最大泡压法实验;水和酒精的密度数据见恒温技术与粘度实验。 仪器与药品 屈氏粘力管一根。测液体比重用比重瓶一个。游标卡尺一根(公用)。50ml 和100ml 烧杯各一个。酒精,表面活性剂溶液(每组一个,实验室编好号)。 实验步骤 1.用游标卡尺测量滴重计的外半径。测量酒精从上刻度到下刻度滴下液滴的总质量W 和滴数
实验七 最大气泡法测定液体的表面张力 卓冶13 李金阳 (一)、实验目的 1.掌握最大气泡法测定液体的表面张力的原理和方法。 2.熟悉表面张力的意义和性质,测定不同浓度液体的表面张力。 3.熟悉表面吸附的性质及与表面张力的关系。 (二)、实验原理 溶剂中加入溶质后,溶剂的表面张力要发生变化,加入表面活性物质(能显著降低溶剂表面张力的物质)则它们在表面层的浓度要大于在溶液内部的浓度,加入非表面活性物质则它们在表面层的浓度比溶液内部低。这种表面浓度与溶液内部浓度不同的现象叫溶液的吸附。显然,在指定的温度压力下,溶质的吸附量与溶液的表面张力及溶液的浓度有关。从热力学可知,它们之间的关系遵守吉布斯吸附等温方程: T dc d RT c ??? ??- =Γσ (7—1) 式中:Γ—为溶质在单位面积表面层中的吸附量(mol ·m - 2); σ—为溶液的表面张力(N ·m -2 ); c —为溶液浓度(mol ·m -3 );; R —气体常数,8.314J ·mol -1·K -1 ; T —为绝对温度(K )。 当 )/(dc d σ< 0时,Γ > 0,即溶液的表面张力随着溶液浓度的增加而下降时,吸附量为 正值,称为正吸附,反之,当)/(dc d σ> 0时,Γ< 0称为负吸附。吉布斯吸附等温方程式 应用范围很广,但上述形式只适用于稀溶液。通过实验测得不同浓度溶液的表面张力1σ、 2σ……即可求得吸附量Γ。 本实验采用最大气泡压力法测定正丁醇水溶液的表面张力值。试验装置如图(7—1) 所示。 图7—1 表面张力测定装置 1—样品管 2—毛细管 3—压瓶 4—精密数字压力计 5—大气平衡管 6—活塞 图7—2 气泡曲率半径的变化规律 将欲测表面张力的溶液装入样品管中,使毛细管的端口与液面相切,液体即沿毛细管上升,打开减压瓶3的活塞6,使里面的水慢慢的滴出,则系统内的压力慢慢减小,毛细管2液面上受到一个比样品管中液面上大的压力,此时毛细管内液面就会下降,直到在毛细管端面形成一个稳定的气泡。开始时气泡表面很平,曲率半径很大,随着气泡的形成,曲率半
[实验目的] 1.用拉脱法测量室温下液体的表面张力系数 2.学习力敏传感器的定标方法 [实验原理] 测量一个已知周长的金属片从待测液体表面脱离时需要的力,求得该液体表面张力系数的实验方法称为拉脱法.若金属片为环状吊片时,考虑一级近似,可以认为脱离力为表面张力系数乘上脱离表面的周长,即 F=α·π(D1十D2 ) (1) 式中,F为脱离力,D1,D2分别为圆环的外径和内径,α为液体的表面张力系数. 硅压阻式力敏传感器由弹性梁和贴在梁上的传感器芯片组成,其中芯片由四个硅扩散电阻集成一个非平衡电桥,当外界压力作用于金属梁时,在压力作用下,电桥失去平衡,此时将有电压信号输出,输出电压大小与所加外力成正此,即 △U=KF (2) 式中,F为外力的大小,K为硅压阻式力敏传感器的灵敏度,△U为传感器输出电压的大小。 [实验装置] 图1-1为实验装置图,其中,液体表面张力测定仪包括硅扩散电阻非平衡电桥的电源和测量电桥失去平衡时输出电压大小的数字电压表.其他装置包括铁架台,微调升降台,装有力敏传感器的固定杆,盛液体的玻璃皿和圆环形吊片,实验证明,当环的直径在3cm附近而液体和金属环接触的接触角近似为零时.运用公式(1)测量各种液体的表面张力系数的结果较为正
确。 [实验内容] 一、必做部分 1、力敏传感器的定标 每个力敏传感器的灵敏度都有所不同,在实验前,应先将其定标,步骤如下:打开仪器地电源开关,将仪器预热。(2)在传感器梁端头小钩中,挂上砝码盘,调节电子组合仪上的补偿电压旋钮,使数字电压表显示为零。(3)在砝码盘上分别如0.5g、1.0g、1.5g、2.0g、2.5g、3.0g等质量的砝码,记录相应这些砝码力F作用下,数字电压表的读数值U.(4)用最小二乘法作直线拟合,求出传感器灵敏度K. 2、环的测量与清洁 (1)用游标卡尺测量金属圆环的外径D1和内径D2 (关于游标卡尺的使用方法请阅实验1) (2)环的表面状况与测量结果有很大的关系,实验前应将金属环状吊片在NaOH溶液中浸泡20-30秒,然后用净水洗净。 3、液体的表面张力系数 (1)将金属环状吊片挂在传感器的小钩上,调节升降台,将液体升至靠近环片的下沿,观察环状吊片下沿与待测液面是否平行,如果不平行,将金属环状片取下后,调节吊片上的细丝,使吊片与待测液面平行。 (2)调节容器下的升降台,使其渐渐上升,将环片的下沿部分全部浸没于待测液体,
宁波工程学院 物理化学实验报告 实验名称最大气泡压力法测定溶液的表面张力 一、实验目的 1.掌握最大气泡压力法测定表面张力的原理和技术。 2.通过对不同浓度乙醇溶液表面张力的测定,加深对表面张力、表面自由能、表面张力和吸附量关系的理解。 二、实验原理 1、表面浓度与内部浓度不同的现象叫做溶液的表面吸附。在指定的温度和压力下,溶质的吸附量与溶液的表面张力及溶液的浓度之间的关系遵循吉布斯吸附等温式: Γ = –(c/RT)*(dγ/dc)① 式中,Г为溶液在表层的吸附量;γ为表面张力;c为吸附达到平衡时溶液在介质中的浓度。 根据朗格谬尔(Langmuir)公式: Γ =Γ∞Kc/(1+Kc)② Γ∞为饱和吸附量,即表面被吸附物铺满一层分子时的Γ∞ c/Γ =(1+Kc)/(Γ∞K)= c/Γ∞+1/Γ∞K ③ 以c/Г对c作图,则图中该直线斜率为1/Г∞。 由所得的Г∞代入A m=1/Г∞L可求被吸附分子的截面积(L为阿伏伽德罗常数)。 2、本实验用气泡最大压力法测定溶液的表面张力,其仪器装置如图1所示: 图1、最大气泡压力法测量表面张力的装置示意图 1、恒温套管; 2、毛细管(r在0.15~0.2mm); 3、U型压力计(内装水); 4、分液漏斗; 5、吸滤瓶; 6、连接橡皮管。
将待测表面张力的液体装于表面张力仪中,使毛细管的端面与液面相切,液面即沿毛细管上升,打开抽气瓶的活塞缓缓抽气,毛细管内的液面上受到一个比A瓶中液面上大的压力,当此压力差——附加压力(△P=P大气–P系统),附加压力与表面张力成正比,与气泡的曲率半径成反比,其关系式为: ΔP=2γ/R ④ 式中,ΔP为附加压力;γ为表面张力;R为气泡的曲率半径。 根据上式,R=r时的最大附加压力为: ΔP最大= 2γ/r ⑤ 实际测量时,使毛细管端刚与液面接触,则可忽略气泡鼓起所需克服的静压力,这样就可以直接用上式进行计算。 当将其它参数合并为常数K时,则上式变为: γ=KΔP最大⑥ 式中仪器常数K可用已知表面张力的标准物质测得。 三、仪器药品 1、仪器:最大泡压法表面张力仪1套,洗耳球1个,移液管(50ml和10ml) 各一支,烧杯(500mL)。 2、药品:正丁醇(分析纯),蒸馏水。 四、实验步骤 1、仪器的准备与检漏 将表面张力仪容器和毛细管先用洗液洗净,再顺次用自来水和蒸馏水漂洗,烘干后按图5-9接好,检查是否漏气。 2、仪器常数的测定 调节液面与毛细管相切,并调节分液漏斗,使气泡由毛细管尖端成单泡逸出,且速度控制在每分钟形成气泡5~10个(数显微压差测量仪为 5~10s),当气泡刚脱离管端的一瞬间,压力计中液位差达到最大值,当显示的最大值比较稳定时,记下数据,重复调节2次并记下相应的数值。再由手册查出实验温度时水的表面张力,求得仪器常数K。 3、表面张力随溶液浓度变化的测定 在上述体系中,按浓度从高到低的顺序依次测定预先配好的正丁醇溶液的△P最大值,每次置换溶液前都先用溶液润洗2次,再按2方法 测定。 五、实验数据记录及处理 1、实验数据的记录
溶液表面张力的测定(拉环法) 一实验目的 (1)了解表面自由能、表面张力的意义及表面张力与吸附的关系。(2)通过测定不同浓度乙醇水溶液的表面张力,计算吉布斯表面吸附量和乙醇分子的横截面积,掌握拉环法测定表面张力的原理和技术。二实验原理 (1)表面张力 在温度、压力、组成恒定时,每增加单位表面积,体系的吉布斯自由能的增值称为表面吉布斯自由能(J·m-2),用γ表示。也可以看作是垂直作用在单位长度相界面上的力,即表面张力(N·m-1)。位表面层上分子比同数量内层分子引起体系自由能的增加量称为比表面自由能。比表面和表面张力在数值和量纲上一致,故常用表面张力度量比表面自由能。 (2)影响表面张力的因素 液体的表面张力与温度有关,温度越高,表面张力越小。液体的表面张力与液体的浓度有关,在溶剂中加入溶质,表面张力就会发生变化。 (3)表面张力与吸附量的关系 表面张力的产生是由于表面分子受力不均衡引起的,当加入一种物质后,对某些溶液(包括内部和表面)及固体的表面结构会带来强烈的影响,则必然引起表面张力的改变。如果溶质加入能降低表面吉布斯自由能时,边面层溶质浓度比内部大;反之增加表面吉布斯自由
能时,则溶液在表面的浓度比内部小。由此可见,在指定温度和压力下,溶质的吸附量与溶液的表面张力有关,即吉布斯等温吸附方程: Γ= -(dγ/dc)T(c/RT) 其中Γ为溶质的表面超额,c 为溶质的浓度,γ为溶液的表面张力 a若dγ/dc<0,Γ>0,为正吸附,表面层溶质浓度大于本体溶液,溶质是表面活性剂。 b若dγ/dc>0,Γ<0,为负吸附,表面层溶质浓度小于本体溶液,溶质是非表面活性剂。 溶液的饱和吸附量: c/Γ= c/Γ∞+1/KΓ∞ 分子的截面积: S B = 1/(Γ∞L) L=6.02×1034 (4)吊环法测表面张力的原理 测表面张力的方法很多,有毛细管上升法,滴重法,最大气泡压力法,吊环法等。吊环法是将吊环浸入溶液中,然后缓缓将吊环拉出溶液,在快要离开溶液表面时,溶液在吊环的金属环上形成一层薄膜,随着吊环被拉出液面,溶液的表面张力将阻止吊环被拉出,当液膜破裂时,吊环的拉力将达到最大值。自动界面张力仪将记录这个最大值P。按照公式校正后,可以得出溶液的表面张力数值γ。校正因子: F=0.7250+(0.01452P/C2D+0.04534-1.679r/R)1/2式中P:界面张力仪显示读数值mN·m-1
系 级 姓名 日期 No. 评分: 实验题目:焦利氏秤法测量液体的表面张力 实验目的:学习并掌握用焦利氏秤法测量液体的表面张力的方法,加深对液体表 面张力的理解。 实验原理: 液体表层内分子力的宏观表现,使液面具有收缩的趋势。想象在液面上划一条线,表面张力就表现为直线两侧的液体以一定的拉力相互作用。这种张力垂直于该直线且与线的长度成正比,比例系数称为表面张力系数。 把金属丝AB 弯成如图 (a)所示的形状,将其悬挂在灵敏的测力计上,浸到液体中,缓缓提起测力计时,金属丝就会拉出一层与液体相连的液膜,由于表面张力的作用,测力计的读数逐渐达到一最大值F (超过此值,膜即破裂)。。由于液膜有两个表面,若每个表面的力为F ',则由 '2F mg F += 得 2 'mg F F -= (1) 表面张力F ’的大小与分界线的长度成正比。即 l F σ=' (2)
系级姓名日期No. 评分: σ称为表面张力系数,单位是N/m。表面张力系数与液体的性质,杂质和温度有关。测定表面张力系数的关键是测量表面张力F',应用焦利氏秤液膜即将破裂可以方便地测量表面张力F'。 实验器材:焦利氏秤,自来水,肥皂水,金属丝,金属圈,钢板尺。 实验内容: 1、确定焦利氏秤上锥形弹簧的劲度系数k; 2、测量自来水的表面张力系数; 3、测量肥皂水的表面张力系数。 数据记录处理: 1、确定焦利氏秤上锥形弹簧的劲度系数k m/g 0.0 0.5 1.0 1.5 2.0 2.5 3.0 3.5 4.0 4.5 5.0 x/cm 2.87 3.38 3.86 4.36 4.88 5.42 5.93 6.48 7.00 7.53 8.06 (1)作图法:
. . 物理化学实验备课材料 实验17 液体表面力的测定 一、基本介绍 液体的表面力是指液体与它的蒸气成平衡时体系的界面力。液体表面力常常是在空气中测定的。当气相是一个处于低压或中压的惰性气体时,一般液体表面力值与气相的组成几乎无关。液体的表面力,源于液体相界面分子受力不平衡,意为相表面的单位长度收缩力,用“σ"表示,其单位是焦耳/平方米(J·m-2)或牛/米(N·m-1).液体表面力的测定,不仅可以加深对表面力这一物系热力学性质的认识,而且可以研究表面活性剂的表面活性、分子的横截面积、分子长度等。 二、实验目的1、掌握最大气泡法测定表面力的原理,了解影响表面力测定的因素。 2、测定不同浓度正丁醇溶液的表面力,计算吸附量, 由表面力的实验数据求分子的截面积及吸附层的厚度。 三、实验原理 1、溶液中的表面吸附 从热力学观点来看,液体表面缩小是一个自发过程,这是使体系总自由能减小的过程,欲使液体产生新的表面ΔA,就需对其做功,其大小应与ΔA 成正比: -W′=σ·ΔA (1) 如果ΔA为1m2,则-W′=σ是在恒温恒压下形成1m2新表面所需的可逆功,所以σ称为比表面吉布斯自由能,其单位为J·m-2。也可将σ看作为作用在界面上每单位长度边缘上的力,称为表面力,其单位是N·m-1。在定温下纯液体的表面力为定值,当加入溶质形成溶液时,表面力发生变化,其变化的大小决定于溶质的性质和加入量的多少。根据能量最低原理,溶质能降低溶剂的表面力时,表面层中溶质的浓度比溶液部大;反之,溶质使溶剂的表面力升高时,它在表面层中的浓度比在部的浓度低,这种表面浓度与部浓度不同的现象叫做溶液的表面吸附。在指定的温度和压力下,溶质的吸
物理化学实验最大气泡压力法测定溶液表面张力C210 2010-04-12 T=286.15K P=85.02kPa 一、实验目的 1.掌握最大气泡法测定溶液表面张力的原理和方法 2.测水溶液的表面张力并计算定不同浓度正丁醇计算吸附量 3.加深对表面张力、表面自由能、表面张力和吸附量关系的理解 二、实验原理 处于溶液表面的分子,受到不平衡的分子间力的作 用而具有表面张力s. 气泡最大压力法测定表面张力装置见实物;实验中 通过滴水瓶滴水抽气使得体系压力下降,大气压与体系 压力差△p逐渐把毛细管中的液面压至管口,形成气泡。 如果毛细管半径很小,则形成的气泡基本上是球形的; 当气泡开始形成时,表面几乎是平的,这时曲率半径最 大;随着气泡的形成,曲率半径逐渐变小,直到形成半球 形,这时曲率半径R和毛细管半径r相等,曲率半径达 最小值,根据拉普拉斯公式得:附加压力达最大值ΔP max =σ/r min。气泡进一步长大,R变大,附加压力则变小, 直到气泡逸出。 加入表面活性物质时溶液的表面张力会下降,溶质 在表面的浓度大于其在本体的浓度,此现象称为表面吸 附现象; 单位溶液表面积上溶质的过剩量称为表面吸附量Γ, Γ=-(c/RT)*( dσ/dc). 对可形成单分子层吸附的表面活性物质,溶液的表面吸附量Γ与溶液本体浓度c之间的关系符合朗格谬尔吸附等温式: Γ=Γ∞*kc/1+kc 朗格谬尔吸附等温式的线性形式为: c/Γ=c/Γ∞+1/kΓ∞ Γ∞为饱和吸附时,单位溶液表面积上吸附的溶质的物质的量,则每个溶质分子在溶液表面上的吸附截面积为:A m=1/(N A*Γ∞) 三、仪器与试剂 恒温槽装置;数字式微压差计; 抽气瓶l个;表面张力测定仪 烧杯(1000mL);T形管1个; 电导水; 正丁醇(A.R.)及其不同浓度的标准溶液; 四、实验步骤 1.仪器常数的测定 将表面张力测定仪清洗干净;在干净的表面张力测定仪中装入电导水,使毛细管上端塞子塞紧时,毛细管刚好与液面垂直相切;抽气瓶装满水,连接好后旋开下端活塞使水缓慢滴出;控制流速使气泡从毛细管平稳脱出(每个气泡4-6秒),记录气泡脱出瞬间数字微压差计的最大数值,取三次并求平均值。 2.测定正丁醇溶液的表面张力 用同样的方法测定不同浓度的正丁醇溶液的最大压差,由稀到浓依次测定;每个浓度的溶液测量前,表面张力测定仪和毛细管一起用该溶液荡洗二至三次;每份溶液恒温至少3-5min之后,开始读数。 3. 重复测定电导水的数据。 注意事项:仪器系统不能漏气;测定用的毛细管一定要洗干净,否则气泡可能不能连续稳定的流过,而使压差计读数不稳定,如发生此种现象,毛细管应重洗;毛细管端口一定要刚好垂直切入液面,不能离开液面,但亦不可深插;在数字式微压差测量仪上,应读出气泡单个逸出是的最大压力差;正丁醇溶液要准确配置,使用过程防止挥发损失;从毛细管口脱出气泡每次应为一个,即间断脱出;表面张力和温度有关,因此要等溶液恒温后再测量。
学号:201214140123 基础物理化学实验报告 实验名称:溶液表面张测定 12届药学班级1组号 实验人姓名:李楚芳 同组人姓名:罗媛,兰婷 指导老师:邓斌 实验日期:2014-05-30
湘南学院化学与生命科学系 一、 实验目的: 1.加深理解表面张力的性质,表面吉布斯能的意义以及表面张力和吸附的关系。 2. 掌握最大气泡法测定表面张力的原理和技术。 二、 主要实验原理,实验所用定律、公式以及有关文献数据: 当加入溶质后,溶剂的表面张力要发生变化。根据能量最低原理,若溶液质能降低溶剂的表面张力,则表面层溶质的浓度应比溶液内部的浓度大;如果所加溶质能使溶剂的表面张力增加,那么,表面层溶液质的浓度应比内部低。这种现象为溶液的表面吸附。用吉布斯公式(Gibbs )表示: T c σ )d d (RT c Γ- = (1)式 式中,Г为表面吸附量(mol.m -2);σ为表面张力(J.m -2);T为绝对温度(K);C为溶液浓度(mol/L );)(dc d σ T 表示在一定温度下表面张力随浓度的改变率。
当 )( dc d σ T < 0,Г>0,溶质能增加溶剂的表面张力,溶液表面层的浓度大于内部的浓度,称为正吸附作用。 )( dc d σ T >0,Г<0,溶质能增加溶剂的表面张力,溶液表面层的 浓度小于内部的浓度,称为负吸附作用。 可见,通过测定溶液的浓度随表面张力的变化关系可以求得不同浓度下溶液的表面吸附量。 本实验采用最大气泡压力法测定正丁醇水溶液的表面张力值。将欲测表面张力的液体装入试管中,使毛细管的端面与液面相切,液体即沿毛细管上升,直到液柱的压力等于因表面张力所产生的上升力为止。若管内增加一个与此相等的压力,毛细管内液面就会下降,直到在毛细管端面形成一个稳定的气泡;若所增加的压力稍大于毛细管口液体的表面张力,气泡就会从毛细管口被压出。可见毛细管口冒出气泡的需要增加的压力与液体的表面张力成正比。 σ=K △p 式中K 与毛细管的半径有关,对同一支毛细管是常数,可由已知表面张力的液体求得。本实验通过蒸馏水来测得。 由实验测得不同浓度时的表面张力,以浓度为横坐标,表面张力为纵坐标,得σ-c 图,过曲线上任一点作曲线的切线和水平线交纵坐标于b1,b2两点,则曲线在该点的斜率为 c b b c 0b b d d 2121c σ--=--=
南昌大学物理实验报告 课程名称:大学物理实验 实验名称:液体表面张力系数的测定 学院:管理学院专业班级: 学生姓名:学号: 实验地点:基础实验大楼608 座位号: 实验时间:第三周星期天下午四点开始
液体表面张力系数的测定实验报告 【实验目的】 1.了解水的表面性质,用拉脱法测定室温下水的表面张力系数。 2.学会使用焦利氏秤测量微小力的原理和方法。 【实验仪器】 焦利秤,砝码,烧杯,温度计,镊子,水,游标卡尺等。 【实验原理】 液体表面层内分子相互作用的结果使得液体表面自然收缩.犹如紧张的弹性薄膜。由于液面收缩而产生的沿着切线方向的力称为表面张力。设想在液面上作长为L的线段,线段两侧液面便有张力f相互作用,其方向与L垂直,大小与线段长度L成正比。即有: =α F? L f α称为液体表面张力系数,单位:N/m。 将一表面洁净的长为L、宽为d的矩形金属片(或金属丝)竖直浸入水中,然后慢慢提起一张水膜,当金属片将要脱离液面,即拉起的水膜刚好要破裂时,则有F=mg+f。其中,F为拉出时所用的力,mg为金属片和带起的水膜的总质量,f为表面张力。实验中利用金属圆环,则: f=F-mg 【实验步骤】 1.安装好仪器,挂好弹簧.调节底板的三个水平调节螺丝,使焦利秤立柱竖直。在主尺顶部挂入吊钩再安装弹簧和配重圆柱体.使小指针被夹在两个配重圆柱中间,配重圆柱体下端通过吊钩钩住砝码托盘。调整小游标的高度使小游标左侧的
基准线大致对准指针,锁紧固定小游标的锁紧螺钉.然后调节微调螺丝使指针与镜子框边的刻线重合.当镜子边框上刻线、指针和指针的像重合时(即称为“三线对齐”),读出游标0线对应刻度的数值L 0. 2.测母弹簧的倔强系数K :依次增加1.0g 砝码.即将质量为1.0g ,2.0g .3.0g ,…,9.0g 的砝码加在下盘内。调整小游标的高度.每次都重新使三线对齐,分别记下游标0线所指示的读数L1.L2,…,L9;再逐次减少1.0g 砝码.调整小游标的高度.每次都重新使三线对齐,分别记下游标。线所指示的读数L9’,L8’,….L0’,取二者平均值,用逐差法求出弹簧的倔强系数。即 2 L -i i i '= L L )-(5154 i i i L L L +=∑=? 3.测(F 一mg)值。将洁净的金属圆环挂在弹簧下端的小钩子上,调整小游标的高度使三线对齐.记下此时游标0线指示读数S 0。把装有蒸馏水的烧杯置于焦利平台上,调节平台位置,使金属片浸入水中,转动平台旋钮使平台缓缓下降,下降的过程中金属圆环底部会拉成水膜,在水膜还没有破裂时需调节三线对齐,然后再使平台下降一点,重复刚才的调节,直到平台稍微下降,金属圆环刚好脱出液面为止,记下此时游标0线所指示的读数S ,算出△S=S —S 0的值,即为在表面张力作用下弹簧的伸长量,重复测量5次,求出平均值,此时有F-mg=f=K △S 代入可得: ) (21d d s k +?= πγ