
《生化制品技术》实验大纲
一、实验目的
本实验是《生化制品技术》课程的配套实验,目的是增加学生对生物药物及生物技术制药的感性认识及提高学生的实验操作能力。要求学生熟悉并掌握生物药物的制备过程和生物技术制药的基本操作方法。
二、适用专业及层次
适用于生物制药技术专业学生
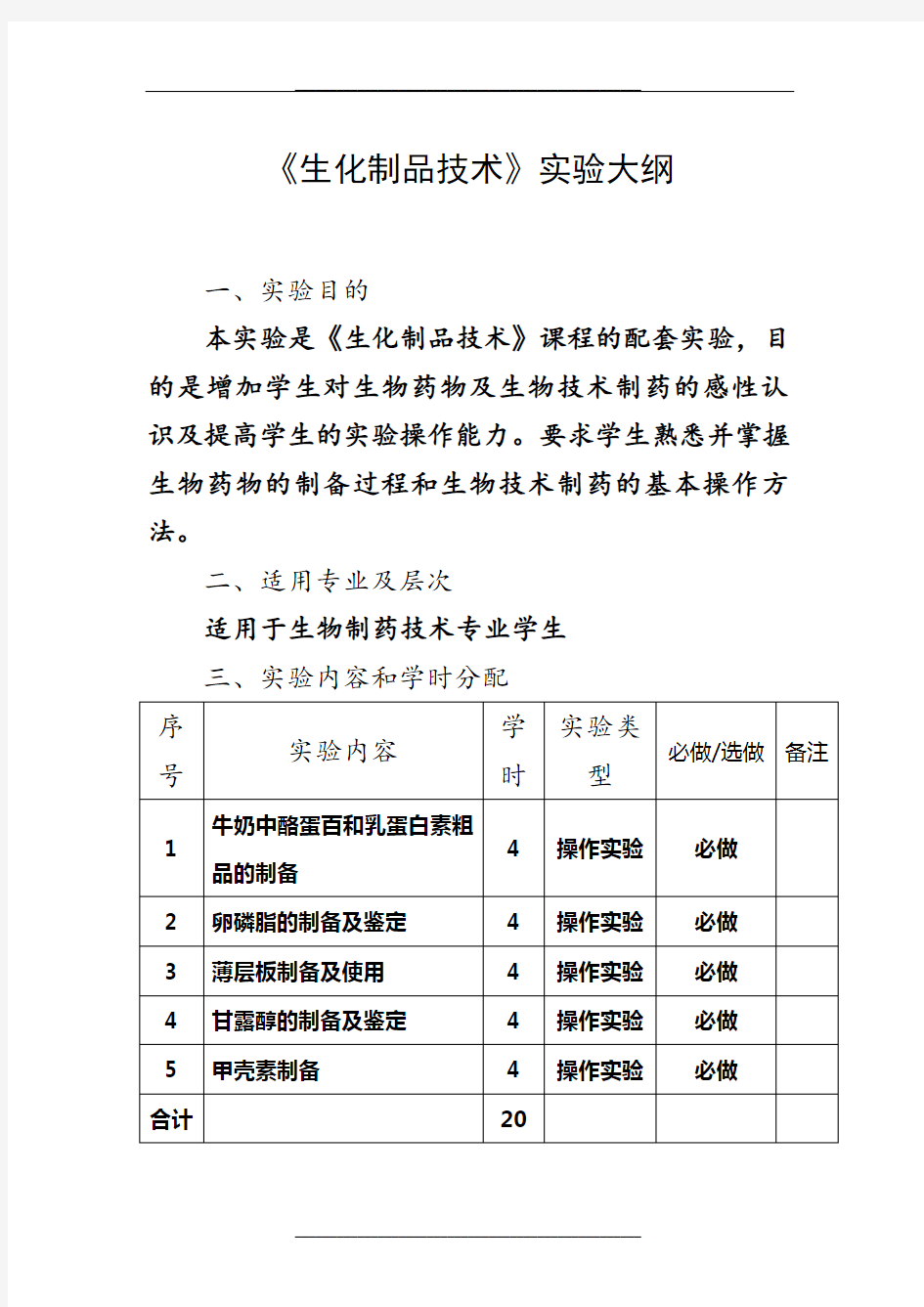
三、实验内容和学时分配
实验一牛奶中酪蛋白和乳蛋白素粗品的制备
一、实验目的
1.掌握盐析法的原理和操作。
2.掌握等电点沉淀法的原理和基本操作。
二、实验原理
乳蛋白素是一种广泛存在于乳品中,合成乳糖所需要的重要蛋白质。牛奶中主要的蛋白质是酪蛋白(caseins),酪蛋白在pH4.8左右会沉淀析出,但乳蛋白素在pH3左右才会沉淀。利用此一性质,可先将pH降至4.8,或是在加热至40℃的牛奶中加硫酸钠,将酪蛋白沉淀出来。酪蛋白不溶于乙醇,这个性质被利用来从酪蛋白粗制剂中除去脂类杂质。将去除掉酪蛋白的滤液的pH调至3左右,能使乳蛋白素沉淀析出,部分杂质即可随澄清液出去。在经过一次pH沉淀后,即可得粗乳蛋白素。
三、实验器材
烧杯(250ml和100ml)、玻璃试管(10mm×100mm)、离心管(50ml)、磁力搅拌器、pH计、离心机、水浴锅。
四、试剂和材料
脱脂牛乳或低脂牛乳、无水硫酸钠、0.1mol/L HCL、0.1mol/L NaOH、滤纸、pH试纸、浓盐酸、乙酸缓冲溶液0.2mol/L (pH4.6)、乙醇。
五、操作步骤
1.盐析或等电点沉淀制备酪蛋白
(1)将50ml牛乳倒入250ml烧杯中,于40℃水浴中加热并搅拌。
(2)向上述烧杯中缓缓加入(约10min内分次加入)10g无水硫酸钠,再继续搅拌10min(或加热到40℃,再在搅拌下慢慢地加入50ml40℃左右的乙酸缓冲液,直到pH达到4.8左右,将悬浮液冷却至室温,放置5min)。
(3)将溶液用细布过滤,分别收集沉淀和滤液。沉淀悬浮于30ml乙醇中,倾于布氏漏斗中,过滤出去乙醇溶液,抽干。将沉淀从布氏漏斗中移出,在表面皿上摊开以除去乙醇,干燥后得到的是酪蛋白。准确称重。
2.等电点沉淀法制备乳蛋白素
(1)将制备酪蛋白操作步骤(3)所得滤液置于100ml烧杯中,一边搅拌,一边利用pH计以浓盐酸调整pH至3±0.1。
(2)将溶液倒入离心管中,6000r/min离心15min,倒掉上层液。
(3)在离心管内加入10ml去离子水,振荡,使管内下层物重新悬浮,并以0.1mol/L氢氧化钠溶液调整pH至8.5~9.0(以pH试纸或pH计判定),此时大部分蛋白质均会溶解。
(4)将上述溶液以6000r/min离心10min,上层液倒入50ml烧杯中。
(5)将烧杯置于磁搅拌加热板上,一边搅拌,一边利用pH计以0.1mlo/L 盐酸调整pH至3±0.1。
(6)将上述溶液以6000r/min离心10min,倒掉上层液。取出沉淀干燥,并称重。
六、结果与讨论
1.计算出每100ml牛乳所制备出的酪蛋白数量,并与理论产量(3.5g)相
比较。求出实际获得率(%)。
2.计算出100ml牛乳所制备出的乳蛋白素数量。
实验二卵磷脂的制备及鉴定
一、实验目的
学习从蛋黄中制备卵磷脂的方法和基本操作。
二、实验原理
利用卵磷脂可溶于乙醇的性质,将卵黄溶于乙醇,卵磷脂从卵黄中转移到乙醇溶液中,可分离提取出来,而蛋白质等某些杂质从沉淀物中除去。但由于乙醇溶剂抽提时,其他物质也一起被抽提,如甘油三脂、甾醇等。利用卵磷脂不溶于丙酮的性质,用丙酮从粗卵磷脂溶液中沉淀磷脂,能使卵磷脂与其他脂质和胆固醇分离开来。无机盐和卵磷脂可生产络合物沉淀,因此可利用金属盐沉淀剂将卵磷脂从溶液中分离出来,由此除去蛋白质、脂肪等杂质,再用适当溶剂萃取出无机盐和其他磷脂杂质,这样可大大提高卵磷脂纯度。
三、实验器材
离心机、旋转蒸发仪、布式漏斗、抽滤瓶、真空干燥箱、层析缸、紫外分光光度计。
四、试剂和材料
95%乙醇、丙酮、10%ZnCl2、2%氯仿、碘、甲醇、0.1%乙醇、无水乙醇。
五、操作步骤
1、粗提
室温下,取适量的鸡蛋卵黄用2倍于卵黄体积的95%乙醇进行提取,混合搅拌,离心分离(3000r/min,5min),将沉淀物重复提取3次,回收上清夜;然后减压蒸馏(45℃)至近干,用少量石油醚洗下粘壁的黄色油状物质;加入丙酮,抽滤,分离出沉淀物,真空干燥(40℃,30min),得到淡黄色的粗卵磷脂,称重。
2、精制
取一定量的卵磷脂粗品,用无水乙醇溶解,得到约10%的乙醇粗提液,加入相当于卵磷脂质量的10%的ZnCl2水溶液,室温搅拌0.5h;分离沉淀物,加入适量冰丙酮(4℃)洗涤,搅拌1h,再用丙酮反复研洗,直到丙酮洗液为近无色止,得到白色蜡状的精卵磷脂;干燥;称重。
3、鉴定
(1)薄层色谱分析将卵磷脂样品与对照品分别配成2%氯仿溶液,用GF254硅胶板进行层析,展开剂为氯仿∶甲醇∶水(65∶25∶4),层析完毕后,取出薄板,干燥,碘蒸汽显色。
(2)紫外吸收光谱测定将一定量卵磷脂样品溶于无水乙醇,配成0.1%乙醇溶液,用紫外分光光度计扫描其在90~400nm的吸收光谱,可测得卵磷脂的紫外最大吸收峰。卵磷脂紫外最大吸收峰在215nm波长。
六、结果与讨论
1.计算卵磷脂得率,讨论影响卵磷脂得率的主要因素。
2.根据薄层色谱图谱、紫外吸收光谱分析所制备的卵磷脂的纯度。
实验三薄层板的制备及使用
实验一薄层色谱板的制备和使用
目的要求:
通过实验进一步理解薄层色谱技术理论,熟悉掌握薄层色谱板的制备和使用方法。
一、薄层层析的基本原理
把吸附剂(固定相)均匀地铺在一块玻璃板上,将待分离的样品溶液点加在一薄层板的一端,在密闭的容器中用适当的溶剂(流动相)展开,由于吸附剂对不同物质的吸附力大小不同及溶剂对不同物质溶解分配系数不同,当溶剂流过时,各物质在吸附剂和溶剂之间发生连续不断地吸附,解吸附,再吸附,再解吸附。不易被吸附或易被溶剂溶解的物质相对移动得快一些。经过一段时间的展开,不同的物质被彼此分开,最后形成相互分离的斑点。将展开完毕的薄层板从密闭容器中取出后,应用特定的试药或方法将斑点显色,从而达到定性和定量的目的。
二、薄层板的制备
1.玻璃板
用一块玻璃板涂上很薄的吸附剂,如硅胶或氧化铝等,玻璃板要求薄厚一致,大小相同,表面光滑平整,一般玻璃只要合乎这些要求就可。如果找不到平整均一的,将旧光学照像底片截成同样大小也可以。用前先将玻璃用肥皂和水洗干净,必要时浸泡在清洗液中,然后水洗烤干,用纱布擦光。
玻璃板大小有各种规格,一般有20×20、20×10、20×5厘米,也有更小的,可根据需要自行设计。宽度要求至少能点开两三个样品,每两点之间相隔至少1.5厘米,玻板长度一般要满足展开10厘米的距离。点样的起点应距底边至少1.5厘米的距离。
2.吸附剂
应用最广泛的为硅胶和氧化铝,市场上有专供薄层色谱用的吸附剂,规格分不含粘合剂的硅胶H,氧化铝H和含有粘合剂熟石膏的硅胶G,氧化铝G,如市售硅胶G含13%熟石膏,氧化铝分中性、酸性、碱性三种。吸附剂的粒度范围最好在180-200目之间,太小了流速慢,太大则影响分离效果。如不合要求,应过筛。
3.薄层板的涂布
最简单的涂布方法是用两条比玻璃板厚0.25毫米的玻璃条或有机玻璃条(或在同样厚度的玻璃条下粘一层胶布),将玻璃板夹住,把调好的吸附剂浆液平铺在薄层板上,然后用一有机玻璃条或直尺,迅速均匀地向前推进,就象推血片一样,只要推进的速度均匀一致,即可得到薄厚均匀的薄层板,如在一块玻璃板末端再接一块相同的玻璃板,把剩余的装液接过去,可使涂层边缘整齐,厚度一致,吸附剂浆液的加水量和搅拌时间是涂布成败的关键,像12×8平方厘米的玻璃板需要2~3克硅胶G,加4~6毫升水即可,只要技术熟练即能涂成厚薄一致,光滑平整的一块薄层板。不同性质不同批号的吸附剂,加水量和搅拌时间有时可有差异,应根据情况摸出规律。为了达到涂布的各板厚度均匀一致,最好采用涂布器进行薄层的涂布。
为了增加薄层的牢固性及易于保存,可在涂布过程中加入某些粘合剂以增加薄层的硬度。
一般采用添加剂羧甲基纤维素钠(CMC—Na),应用方法是取CMC-Na 1克溶于100毫升水中,加热煮沸溶解,按比例与硅胶搅匀,铺板。涂成之后先把玻板放在平面上,室内干固,再对光检查,看是不是均匀,有无气泡,平整光洁度如何,合格的上烤箱110℃加热30分钟进行活化,冷却后贮于干燥器内备用。
在进行实验时,应尽量可能采用同批号涂布活化的薄层板,以减少因活化不一致引起的Rf值发生差异,目前国内市场已有成品供应,如黄岩化学分析材料厂即有各种类型的薄层板出售。
三、薄层板的使用
1.点样
将样品溶于适当的溶剂中(应尽量避免有水),取微量注射器或玻璃毛细管截齐后,吸取一定量的检样,轻轻接触到薄层上,使样品自动吸到薄层上,点的直径不要超过0.3厘米,一次不能点完,待干后再点,稍有过分就会损伤板面,影响展开后的斑点形状。每两个样点之间相距至少1.5厘米。点样的起点距薄板底边至少1.5厘米,以免样点浸入展开溶剂中,同块薄板上各样点应保持在与底边平行的一条直线上,为控制好点样距离,应用薄层点样尺架。
《生物制药技术》实验指导 实验三四环素、金霉素的薄层层析鉴定(验证型) 实验目的: 掌握薄层层析的原理,四环素族抗生素的定性鉴定方法。 实验原理: 层析(色谱,chromatograpby)是相当重要、且相当常见的一种技术,在把微细分散的固体或是附着于固体表面的液体作为固定相,把液体(与上述液体不相混合的)或气体作为移动相的系统中(根据移动相种类的不同,分为液相层析和气相层析二种),使试料混合物中的各成分边保持向两相分布的平衡状态边移动,利用各成分对固定相亲和力不同所引起的移动速度差,将它们彼此分离开的定性与定量分析方法,称为层析,亦称色谱法。用作固定相的有硅胶、活性炭、氧化铝、离子交换树脂、离子交换纤维等,或是在硅藻土和纤维素那样的无活性的载体上附着适当的液体。将作为固定相的微细粉末状物质装入细长形圆筒中进行的层析称为柱层析(column chromatography),在玻璃板上涂上一层薄而均的支持物(硅胶、纤维素和淀粉等)作为固定相的称为薄层层析(thin layer chromatography),或者用滤纸作为固定相的纸上层析。层析根据固定相与溶质(试料)间亲和力的差异分为吸附型、分配型、离子交换型层析等类型。但这并不是很严格的,有时常见到其中间类型。此外,近来也应用亲和层析,即将与基质类似的化合物(通常为共价键)结合到固定相上,再利用其特异的亲和性沉淀与其对应的特定的酶或蛋白质。 分配层析在支持物上形成部分互溶的两相系统。一般是水相和有机溶剂相。常用支持物是硅胶、纤维素和淀粉等亲水物质,这些物质能储留相当量的水。被分离物质在两相中都能溶解,但分配系数不同,展层时就会形成以不同速度向前移动的区带。一种溶质在两种互不混溶的溶剂系统中分配时,在一定温度下达到平衡后,溶质在固定相和流动相溶剂中的浓度之比为一常数,称为分配系数。当欲被分离的各种物质在固定相和流动相中的分配系数不同时,它们就能被分离开。分配系数大的移动快(阻力小)。 薄层层析是以薄层材料为支持物,在密闭容器中,样品在其上展开。当斑点不易为肉眼观察时,可利用适当的显色剂,或通过紫外灯下产生荧光的方法进行观察。通过这种展开操作,各成分呈斑点状移动到各自的位置上,再根据Rf值的测定进行鉴定。薄层色谱法具有分离与鉴定的双重功能,通过薄层图谱与对照品的图谱相比较,除了能鉴出有效成分或特征成分外,还以完整的色谱图作为一个整体对制剂加以鉴别。薄层色谱分析法由于简便、快速,能有效地、直观地反映药品地真实性、稳定性,现已成为药物制剂的鉴别和质量控制的行之有效的方法之一。薄层层析是鉴别抗生素的方法之一,层析后进行显色,并绘制层析图谱,根据层析图谱对抗生素进行鉴定。本实验以四环素、金霉素标准品溶液作为对照对发酵液进行鉴定。 材料、试剂和器材: 仪器和设备: 玻璃层析缸;层析板(薄层层析硅胶烟台芝罘区黄务硅胶开发实验厂有售);吹风机;紫外投射仪;离心机(1.5ml转子) 试剂:
实验1 氨基酸纸层析 一、实验目的 通过对氨基酸的分离和鉴定,掌握纸层析的基本原理及操作方法。 二、实验原理 层析法又称色谱法。是一项重要的分离技术。利用混合物中各组分理化性质的不同,使各组分以不同程度分配在两相中。 层析的种类: 根据原理分为: a 分配层(纸层析) b 吸附层析 c 亲和层析 d 离子交换层析 根据支持物分为: a 纸层析 b 柱层析 c 薄层层析 d 凝胶过滤层析 分配层析的原理: 各种物质在两种互不溶解的溶剂中的分配系数不同,从而达到分离的目的。 分配层析用于分离在水和有机溶剂中都可溶的混合物。 一种物质在两相中达到平衡时,在两相中的浓度之比是一个常数。 物质在流动相里的浓度 物质在固定相里的浓度 纸层析: 分配的过程:一部分溶质随有机相移动离开原点进入无溶质区,并进行重新分配,不断向前移动。随着有机相不断向前移动,溶质不断地在两相间进行可逆的分配。由于各种物质的分配系数不同,随展层溶剂移动的速率也不同,从而达到分离的目的。移动速度可用比移(Rf )值表示: 色斑中心至上样原点中心的距离 K D = 图1 氨基酸纸层析示意图 R f =
溶剂前缘至上样原点中心的距离 载体:滤纸 固定相:滤纸吸附的水 流动相:水饱和酚 极性:谷氨酸>丙氨酸>脯氨酸 对于水-饱和酚的溶剂体系,氨基酸极性越小,KD 值越大,Rf值也越大,一定时间内随流动相迁移的距离远,反之迁移距离小。 三、实验材料 仪器 ⑴层析缸;⑵层析滤纸;⑶电吹风机;⑸喷雾器;⑹毛细管。 试剂 ⑴氨基酸标准液(6mg/mL);⑵氨基酸混合液(6mg/mL) ⑶展层剂:水饱和苯酚溶液。 ⑷显色剂:0.3%茚三酮丙酮溶液 四、操作步骤 1、层析滤纸的准备 用铅笔在层析滤纸上距离一端2-3cm处划线并标记点样位置。 2、点样(少量多次) 用毛细管平口端蘸取少量样品溶液,点样于滤纸的相应位置,要求样品斑点直径不超过0.5cm,干燥后再点样,重复3次。 3、展层 将滤纸放入层析缸,使滤纸浸入液面以下,但不要使液面没过点样线。展层50-60分钟,取出,用铅笔绘出前沿线。 4、显色 滤纸吹干,用喷雾器把茚三酮溶液均匀细致地喷洒在滤纸有效面上,吹干。
高级动物生化试题 问答题: 1. 简述非编码RNA(non-coding RNA)的种类、结构特点及其主要功能。 非编码RNA的种类结构和功能 1tRNA转运RNA(transfer RNA,tRNA) 结构特征之一是含有较多的修饰成分,核酸中大部分修饰成分是在tRNA中发现的。修饰成分在tRNA分子中的分布是有规律的,但其功能不清楚。5’末端具有G(大部分)或C。3’末端都以ACC的顺序终结。有一个富有鸟嘌呤的环。有一个反密码子环,在这一环的顶端有三个暴露的碱基,称为反密码子(anticodon).反密码子可以与mRNA链上互补的密码子配对。有一个胸腺嘧啶环。tRNA具有三叶草型二级结构以及“L”型三级结构,tRNA 的不同种类及数量可对蛋白质合成效率进行调节。tRNA负责特异性读取mRNA中包含的遗传信息,并将信息转化成相应氨基酸后连接到多肽链中。 tRNA为每个密码子翻译成氨基酸提供了结合体,同时还准确地将所需氨基酸运送到核糖体上。鉴于tRNA在蛋白质合成中的关键作用,又把tRNA称作第二遗传密码。tRNA还具有其他一些特异功能,例如,在没有核糖体或其他核酸分子参与下,携带氨基酸转移至专一的受体分子,以合成细胞膜或细胞壁组分;作为反转录酶引物参与DNA合成;作为某些酶的抑制剂等。有的氨酰-tRNA还能调节氨基酸的生物合成。 2rRNA核糖体RNA(ribosomal RNA, rRNA) 核糖体RNA是细胞中最为丰富的RNA,在活跃分裂的细菌细胞中占80%以上。
他们是核糖体的组分,并直接参与核糖体中蛋白质的合成。核糖体是rRNA 提供了一个核糖体内部的“脚手架”,蛋白质可附着在上面。这种解释很直接很形象,但是低估了rRNA在蛋白质合成中的主动作用。较后续的研究表明,rRNA并非仅仅起到物理支架作用,多种多样的rRNA可起到识别、选择tRNA以及催化肽键形成等多种主动作用。例如:核糖体的功能就是,按照mRNA的指令将氨基酸合成多肽链。而这主要依靠核糖体识别tRNA 并催化肽键形成而实现。可以说核糖体是一个大的核酶( ribozyme)。而核糖体的催化功能主要是由rRNA来完成的,蛋白质并没有直接参与。 3 tmRNA tmRNA主要包括12个螺旋结构和4个“假结”结构,同时还包括一 个可译框架序列的单链RNA结构。tmRNA中H1由5’端和3’端两个末端形成,与tRNA的氨基酸受体臂相似。H1和H2的5’部分之间有一个由10-13nt 形成的环,类似tRNA中的二氢尿嘧啶环,称为“D”环。H3和H4,H6和H7,H8和H9,H10和H11之间分别形成Pk1,pK2,pK3,pK4。H4和H5之间则由一段包含编码标记肽ORF的单链RNA连接。H12由5个碱基对和7nt 形成的环组成,类似tRNA中的TΨC臂和TΨC环,称为“T”环。tmRNA 结构按照功能进行划分可分为tRNA类似域(TLD)和mRNA类似域(MLD),TLD主要包括H1,H2,H12,“D”环和“T”环,MDL则包括ORF和H5,这两部分分别具有类似tRNA和mRNA的功能。tmRNA是一类普遍存在于各种细菌及细胞器(如叶绿体,线粒体)中的稳定小分子RNA。它具有mRNA分子和tRNA分子的双重功能,它在一种特殊的翻译模式——反式翻译模式中发挥重要作用。同时,它与基因的表达调控以及细胞周期的调控等生命过程密切相关,是细菌体内蛋白质合成中起“质量控制”的重要分子之一。识别翻译或读码有误的核糖体,也识别那些延迟停转的核糖体,介导这些有问
实验一基因的PCR扩增技术 一、实验目的与原理简介 聚合酶链式反应(polymerase chain reaction)是体外克隆基因的重要方法,它可在几个小时内使模板分子扩增百万倍以上。因此能用于从微量样品中获得目的基因,同时完成了基因在体外的克隆,是分子生物学及基因工程中极为有用的研究手段。 常规PCR反用于已知DNA序列的扩增,具体可分为三个主要过程:一、变性。通过升高温度使DNA双链模板分子中氢断裂,形成单链DNA分子,温度为94℃,时间1min。二、复性。降低温度使DNA单链分子同引物结合。温度为55℃,时间1min。三、延深。升高温度,在DNA聚合酶最佳活性的条件下在引物3端加入dNTP,实现模板的扩增,温度为72℃,时间2min。同时第一步变性前要在94℃下预变性5分钟,使DNA双链完全解开。经过 25-35个循环之后,在72℃下继续延伸10分钟。 PCR反应包含的七种基本成分: 1)热稳定性DNA聚合酶:Taq DNA聚合酶是最常适用的酶,商品化Taq DNA酶的特异性活性约为80000单位/mg. 2)寡核苷酸引物:寡核苷酸引物的设计是影响PCR扩增反应的效率与特异性的关键因素。 3)脱氧核苷三磷酸(dNTP):标准的PCR反应体系应包括4种等摩尔浓度的脱氧核苷三磷酸,即dATP、dTTP、dCTP和dGTP。每种dNTP的浓度一般在200-250μl之间,高浓度的dNTP对扩增反应会起抑制作用,可能是dNTP与Mg2+螯合有关。 4)二价阳离子:一般需要Mg2+来激活热稳定的DNA聚合酶,由于dNTP与寡聚核酸结Mg2+合,因而反应体系中阳离子的浓度一般要超过dNTP和引物来源的磷酸盐基团的摩尔浓度。Mg2+的最佳浓度为1.5mmol/L。 5)维持PH值的缓冲液:用Tris-Cl在室温将PCR缓冲液的PH值调至8.3-8.8之间,标准PCR缓冲液浓度在10mmol/L。在72℃温育时,反应体系的温度将下降1个多单位,致使缓冲液的PH值接近7.2。 6)一价阳离子:标准PCR缓冲液内含有50mmol/L的KCl,它对扩增大于500bp长度的DNA是有益的。 7)模板DNA:含有靶序列的模板DNA可以以单链或双链形式加入到PCR混合液中,闭环DNA的及增效率略低于线性DNA。 学习PCR反应的基本原理和基本技术。 了解引物设计的一般要求。 二、材料和试剂 10Х扩增缓冲液 4种dNTP贮存液(20mmol/L,PH 8.0) Tap DNA 聚合酶 5端引物(20μmol/L)及3端引物(20μmol/L) 模板DNA 琼脂糖凝胶 PCR仪(Bio-Rad公司)移液枪(0.5-10μL 5-50μL)枪头微量移液管 一、实验操作 1)按照以下次序,将各成分加到微量离子管内混合: 10Х扩增缓冲液2.5μl M g2+1.5μl 5端引物1μl
污水处理生化调试技术方案 一污泥的培养 方法有同步与异步培养与接种,同步是培奍与驯化同时进行或交替进行,异步是先培后驯化,接种是利用类似污水的剩余污泥接种。 活性污泥可用糞便水经曝气培养而得,因为粪便污水中,细菌种类多,本身含有的营养丰富,细菌易于繁殖。?通常为了缩短培菌周期,我们会选择接种培养。?先说粪便水培菌?具体步骤:?将经过过滤的粪便水投入曝气池,再用生活污水或河水稀释,至BOD约为300-400,进行连续曝气。这样过二,三天后,为补充微生物的营养物质和排除由微生物产生的代谢产物,应进行换水,换水根据操作情况分为间断和连续操作。?1.间断操作:?当第一次加料曝气并出现模糊的活性污泥绒絮后,就可停止曝气,使混合液静止沉淀,经1-1.5小时后排放上清液,把排放的上清液约占总体积的60-70%。?然后再加生活污水和粪便水,这时的粪便水可视曝气池内的污泥量来调整,这样一直下去,直至SV达到30%。一般需2周,水温低时时间要延长。 在每次换水时,从停止曝气,沉淀到重新曝气的总时间要控制在2小时之内为宜?成熟的污泥应具有良好的混凝,沉降性能,污泥内有大量的菌胶菌和终生?纤毛类原生动物,如钟虫,等枝虫,盖纤虫等,并可使污水的生化需氧量去除率达90%左右 2.连续操作:?在第一次加料出现绒絮后,就不断地往曝气池投加生活污水或河水,添加粪便水的控制原则与间断投配相同。往曝气池的投加的水量,应保证池内的水量能每天更换一次,随着培奍的进展,逐渐加大水量使在培养后期达到每天更换二次。在曝气池出水进入二次沉淀池后不久(0.5-1)就开始回流污泥,污泥的回流量为曝气池进水量的50%?驯化的方法:可在进水中逐渐增加被处理的污水的比例,或提高浓度,使生物逐渐适应新的环境开始时,被处理污水的加入量可用曝气池设计负荷的20-30%,达到较好的处理效率后,再继续增加,每次以增加设计负荷的10-20%为宜,每次增加负荷后,须等生物适应巩固后再继续增加,直至满负荷为止。?如果被处理工业污水中,缺氮和磷以及其它营养物时,可根据BOD:N:P为100:5:1的比例来调整。?个人认为在此阶段,必要的超赿管路要具备,工艺没设计的可用消防管代替。 而且各种分析要跟上去,和种参数需及时测定,特别是镜检,因为有经验的人可能通过镜检和数据就可以很好的完成任务,另外良好的心理素质也比较重要,有些现象要果断处理,有些则需等侍再认定上面是异步法,同步就是在污泥培养过程中,不断加入工业污水,使污泥在增长过程中逐渐适应工业污水的环境,这样虽可缩短培养和驯化的时间,但在这一过程中发生的问题,又缺实践经验则难以判断问题出在哪一个环节上。 若有条件,就是接种培养,这样可缩短时间,若是相似的污水的污泥,更可提高驯化效果。 二、试运行
食品生物化学实验要求 1. 学生做实验前必须写好实验预习报告,做好实验预习,无实验预习报告者不许 进入实验室。每大组实验人数 28-29 人, 4 人一小组。 2. 实验试剂的配制,现场由教师指导,学生操作完成。学生在试剂配制过程中, 掌握试剂配置的基本步骤,基本方法和注意事项。 3. 实验室所有设备都必须按说明书使用,器皿要小心使用,按规范要求操作,如 有损坏,照价赔偿。 4. 卫生要求:每次试验完毕小组成员务必将本试验台及地面收拾整洁,器皿摆放 整齐有序,如哪组成员发现没有搞好自己组的环境卫生,这次试验的所有组员的实验报告都会扣分。 一、 10 食品科学食品生物化学实验项目表 1. 淀粉的显色、水解和老化( 4 学时) 2. 蛋白质的功能性质( 4 学时) 3. 牛奶中酪蛋白等电点测定和氨基酸的分离鉴定( 4 学时) 4. 或果胶的提取( 4 学时) 5. 酶的性质实验( 4 学时) 实验总课时: 16 学时 二、食品生物化学实验指导书 实验一淀粉的显色、水解和老化 一、实验目的和要求 1 、了解淀粉的性质及淀粉水解的原理和方法。 2 、掌握淀粉水解的条件和产物的实验方法。 3 、淀粉的老化原理和方法 二、实验原理 1 、淀粉与碘的反应直链淀粉遇碘呈蓝色,支链淀粉遇碘呈紫红色,糊精遇碘呈 蓝紫、紫、橙等颜色。这些显色反应的灵敏度很高,可以用作鉴别淀粉的定量和定性的方法,也可以用它来分析碘的含量。纺织工业上用它来衡量布匹退浆的完全度,它还可以用来测定水果果实(如苹果等)的淀粉含量。
近年来用先进的分析技术(如X 射线、红外光谱等)研究碘跟淀粉生成的蓝色物,证明碘和淀粉的显色除吸附原因外,主要是由于生成包合物的缘故。直链淀粉是由α - 葡萄糖分子缩合而成螺旋状的长长的螺旋体,每个葡萄糖单元都仍有羟基暴露 在螺旋外。碘分子跟这些羟基作用,使碘分子嵌入淀粉螺旋体的轴心部位。碘跟淀粉的这种作用叫做包合作用,生成物叫做包合物。 在淀粉跟碘生成的包合物中,每个碘分子跟 6 个葡萄糖单元配合,淀粉链以直径0.13 pm 绕成螺旋状,碘分子处在螺旋的轴心部位。 淀粉跟碘生成的包合物的颜色,跟淀粉的聚合度或相对分子质量有关。在一定的聚合度或相对分子质量范围内,随聚合度或相对分子质量的增加,包合物的颜色的变化由无色、橙色、淡红、紫色到蓝色。例如,直链淀粉的聚合度是 200 ~ 980 或 相对分子质量范围是 32 000 ~ 160 000 时,包合物的颜色是蓝色。分支很多的支 链淀粉,在支链上的直链平均聚合度 20 ~ 28 ,这样形成的包合物是紫色的。糊 精的聚合度更低,显棕红色、红色、淡红色等。下表就是淀粉的聚合度和生成碘包合物的颜色。 表 2-1 淀粉的聚合度和生成碘包合物的颜色 葡萄糖单位的聚合度 3.8 7.4 12.9 18.3 20.2 29.3 34.7 以上 包合物的颜色无色淡红红棕红紫色蓝紫色蓝色 淀粉跟碘生成的包合物在 pH=4 时最稳定,所以它的显色反应在微酸性溶液里最明显。 2 、淀粉的水解淀粉是一种重要的多糖,是一种相对分子量很大的天然高分子化 合物。虽属糖类,但本身没有甜味,是一种白色粉末,不溶于冷水。在热水里淀粉颗粒会膨胀,有一部分淀粉溶解在水里,另一部分悬浮在水里,形成胶状淀粉糊。淀粉进入人体后,一部分淀粉收唾液所和淀粉酶的催化作用,发生水解反应,生成麦芽糖;余下的淀粉在小肠里胰脏分泌出的淀粉酶的作用下,继续进行水解,生成麦芽糖。麦芽糖在肠液中麦芽糖酶的催化下,水解为人体可吸收的葡萄糖,供人体组织的营养需要。反应过程为:( C 6 H 12 O 5 )m → (C 6 H 10 O 5)n → C 12 H 22 O 11 → C 6 H 12 O 6 淀粉糊精麦芽糖葡萄糖 葡萄糖是淀粉最重要的下游产品之一,工业生产中常常使用玉米淀粉水解来加工结晶葡萄糖。 3 、淀粉的老化淀粉加入适量水,加热搅拌糊化成淀粉糊(α - 淀粉),冷却或 冷冻后,会变得不透明甚至凝结而沉淀,这种现象称为淀粉的老化。将淀粉拌水制
《生化制品技术》实验大纲 一、实验目的 本实验是《生化制品技术》课程的配套实验,目的是增加学生对生物药物及生物技术制药的感性认识及提高学生的实验操作能力。要求学生熟悉并掌握生物药物的制备过程和生物技术制药的基本操作方法。 二、适用专业及层次 适用于生物制药技术专业学生 三、实验内容和学时分配
实验一牛奶中酪蛋白和乳蛋白素粗品的制备 一、实验目的 1.掌握盐析法的原理和操作。 2.掌握等电点沉淀法的原理和基本操作。 二、实验原理 乳蛋白素是一种广泛存在于乳品中,合成乳糖所需要的重要蛋白质。牛奶中主要的蛋白质是酪蛋白(caseins),酪蛋白在pH4.8左右会沉淀析出,但乳蛋白素在pH3左右才会沉淀。利用此一性质,可先将pH降至4.8,或是在加热至40℃的牛奶中加硫酸钠,将酪蛋白沉淀出来。酪蛋白不溶于乙醇,这个性质被利用来从酪蛋白粗制剂中除去脂类杂质。将去除掉酪蛋白的滤液的pH调至3左右,能使乳蛋白素沉淀析出,部分杂质即可随澄清液出去。在经过一次pH沉淀后,即可得粗乳蛋白素。 三、实验器材 烧杯(250ml和100ml)、玻璃试管(10mm×100mm)、离心管(50ml)、磁力搅拌器、pH计、离心机、水浴锅。 四、试剂和材料 脱脂牛乳或低脂牛乳、无水硫酸钠、0.1mol/L HCL、0.1mol/L NaOH、滤纸、pH试纸、浓盐酸、乙酸缓冲溶液0.2mol/L (pH4.6)、乙醇。 五、操作步骤
1.盐析或等电点沉淀制备酪蛋白 (1)将50ml牛乳倒入250ml烧杯中,于40℃水浴中加热并搅拌。 (2)向上述烧杯中缓缓加入(约10min内分次加入)10g无水硫酸钠,再继续搅拌10min(或加热到40℃,再在搅拌下慢慢地加入50ml40℃左右的乙酸缓冲液,直到pH达到4.8左右,将悬浮液冷却至室温,放置5min)。 (3)将溶液用细布过滤,分别收集沉淀和滤液。沉淀悬浮于30ml乙醇中,倾于布氏漏斗中,过滤出去乙醇溶液,抽干。将沉淀从布氏漏斗中移出,在表面皿上摊开以除去乙醇,干燥后得到的是酪蛋白。准确称重。 2.等电点沉淀法制备乳蛋白素 (1)将制备酪蛋白操作步骤(3)所得滤液置于100ml烧杯中,一边搅拌,一边利用pH计以浓盐酸调整pH至3±0.1。 (2)将溶液倒入离心管中,6000r/min离心15min,倒掉上层液。 (3)在离心管内加入10ml去离子水,振荡,使管内下层物重新悬浮,并以0.1mol/L氢氧化钠溶液调整pH至8.5~9.0(以pH试纸或pH计判定),此时大部分蛋白质均会溶解。 (4)将上述溶液以6000r/min离心10min,上层液倒入50ml烧杯中。 (5)将烧杯置于磁搅拌加热板上,一边搅拌,一边利用pH计以0.1mlo/L 盐酸调整pH至3±0.1。 (6)将上述溶液以6000r/min离心10min,倒掉上层液。取出沉淀干燥,并称重。 六、结果与讨论 1.计算出每100ml牛乳所制备出的酪蛋白数量,并与理论产量(3.5g)相
《分子生物学检验技术》实验指导 【实验目的】 把握动物组织DNA提取的方法; 把握紫外分光光度法检测、鉴定DNA浓度和纯度的方法。 【实验原理】 获得相当纯度和完整性的基因组DNA,可用于DNA酶切图谱、多态性分析、基因诊断、构建基因组文库等。因此,DNA样品质量的好坏将直截了当关系到实验的成败。较理想的DNA样品应达到以下三点要求:①不应存在对酶有抑制作用的有机溶剂和过高浓度的金属离子;②最大程度地降低蛋白质、多糖和脂类分子的污染;③排除RNA分子的污染和干扰。 DNA以核蛋白形式存在于细胞中,提取DNA的原则是即要将DNA与蛋白质、脂类和糖类等成分分离,又要保持DNA分子的完整。本实验中,用阴离子去垢剂十二烷基磺酸钠(SDS)消化破裂细胞膜、核膜,并使组织蛋白变性沉淀,DNA从核蛋白中游离分开;为操纵组织中脱氧核糖核酸酶(DNase)对DNA的降解,加入柠檬酸钠或乙二胺四乙酸二钠(EDTA-Na2)以除去兴奋该酶的金属离子,SDS也能使DNase变性失活;蛋白酶K可水解蛋白质,消化D NA酶;分离后的DNA用饱和酚/氯仿抽提除去蛋白质,接着用氯仿抽提以除去DNA溶液中微量酚的污染;最后用无水乙醇沉淀DNA,得到欲提取的基因组DNA。
260nm处DNA有最大吸取峰,测DNA的A260,可运算其浓度。而蛋白质在280nm处有最大吸取峰,可测定A260nm/A280nm比值,检测DNA的纯度,该比值介于1.8~2.0之间。 【实验器材和试剂】 1、动物 小白鼠 2、设备 移液器、台式离心机、水浴箱、陶瓷研钵等;751紫外分光光度计、石英比色皿、洗瓶、滤纸等。 3、试剂 (1)基因组DNA提取试剂盒(北京康为世纪生物科技公司):包括Buffer CL、Buffer PP、Buffer GE、RNase A、Proteinase K (7)生理盐水,4℃贮存 (8)无水乙醇、70%乙醇 【操作步骤】 1、制备肝匀浆 迅速处死小白鼠,称取新奇肝脏组织50 mg,用预冷生理盐水洗去血液,滤纸吸干后剪碎组织,将剪碎组织放于组织匀浆器或研钵中研磨,同时加入300 μl Buffer CL。将肝匀浆液放入EP管,加入1.5 μl蛋白酶K,漩涡震荡10 s,55℃孵育直到组织溶解(约1小时)。 2、提取DNA (1)加入1.5 μl RNase A,颠倒混匀,37℃孵育15-60 min。
生化制品技术实验指 导
《生化制品技术》实验大纲 一、实验目的 本实验是《生化制品技术》课程的配套实验,目的是增加学生对生物药物及生物技术制药的感性认识及提高学生的实验操作能力。要求学生熟悉并掌握生物药物的制备过程和生物技术制药的基本操作方法。 二、适用专业及层次 适用于生物制药技术专业学生 三、实验内容和学时分配
实验一牛奶中酪蛋白和乳蛋白素粗品的制备 一、实验目的 1.掌握盐析法的原理和操作。 2.掌握等电点沉淀法的原理和基本操作。 二、实验原理 乳蛋白素是一种广泛存在于乳品中,合成乳糖所需要的重要蛋白质。牛奶中主要的蛋白质是酪蛋白(caseins),酪蛋白在pH4.8左右会沉淀析出,但乳蛋白素在pH3左右才会沉淀。利用此一性质,可先将pH降至4.8,或是在加热至40℃的牛奶中加硫酸钠,将酪蛋白沉淀出来。酪蛋白不溶于乙醇,这个性质被利用来从酪蛋白粗制剂中除去脂类杂质。将去除掉酪蛋白的滤液的pH 调至3左右,能使乳蛋白素沉淀析出,部分杂质即可随澄清液出去。在经过一次pH沉淀后,即可得粗乳蛋白素。 三、实验器材 烧杯(250ml和100ml)、玻璃试管(10mm×100mm)、离心管(50ml)、磁力搅拌器、pH计、离心机、水浴锅。 四、试剂和材料 脱脂牛乳或低脂牛乳、无水硫酸钠、0.1mol/L HCL、0.1mol/L NaOH、滤纸、pH试纸、浓盐酸、乙酸缓冲溶液0.2mol/L (pH4.6)、乙醇。 五、操作步骤 1.盐析或等电点沉淀制备酪蛋白
(1)将50ml牛乳倒入250ml烧杯中,于40℃水浴中加热并搅拌。 (2)向上述烧杯中缓缓加入(约10min内分次加入)10g无水硫酸钠,再继续搅拌10min(或加热到40℃,再在搅拌下慢慢地加入50ml40℃左右的乙酸缓冲液,直到pH达到4.8左右,将悬浮液冷却至室温,放置5min)。 (3)将溶液用细布过滤,分别收集沉淀和滤液。沉淀悬浮于30ml乙醇中,倾于布氏漏斗中,过滤出去乙醇溶液,抽干。将沉淀从布氏漏斗中移出,在表面皿上摊开以除去乙醇,干燥后得到的是酪蛋白。准确称重。 2.等电点沉淀法制备乳蛋白素 (1)将制备酪蛋白操作步骤(3)所得滤液置于100ml烧杯中,一边搅拌,一边利用pH计以浓盐酸调整pH至3±0.1。 (2)将溶液倒入离心管中,6000r/min离心15min,倒掉上层液。 (3)在离心管内加入10ml去离子水,振荡,使管内下层物重新悬浮,并以0.1mol/L氢氧化钠溶液调整pH至8.5~9.0(以pH试纸或pH计判定),此时大部分蛋白质均会溶解。 (4)将上述溶液以6000r/min离心10min,上层液倒入50ml烧杯中。 (5)将烧杯置于磁搅拌加热板上,一边搅拌,一边利用pH计以 0.1mlo/L盐酸调整pH至3±0.1。 (6)将上述溶液以6000r/min离心10min,倒掉上层液。取出沉淀干燥,并称重。 六、结果与讨论 1.计算出每100ml牛乳所制备出的酪蛋白数量,并与理论产量(3.5g)相比较。求出实际获得率(%)。
动物生物化学复习题 1、天然蛋白质氨基酸的结构要点? 答:在与羧基相连的α-碳原子上都有一个氨基,称为α-氨基酸。α—碳原子不是手性碳原子的是哪个氨基酸? 答:甘氨酸 具有紫外吸收特性的氨基酸有哪些? 答:酪氨酸、色氨酸、苯丙氨酸 吸收波长是多少? 答:280nm 核酸的紫外吸收波长是多少? 答:260nm 2、全酶包括哪几部分? 答:酶蛋白与辅助因子 辅基与辅酶的异同点? 答:与酶蛋白结合梳松,用透析、超滤等方法可将其与酶蛋白分开者称为辅酶;与酶蛋白结合紧密,不能用透析发分离的称为辅基。 正常情况下,大脑获得能量的主要途径是什么? 答:葡萄糖的有氧氧化 糖酵解是在细胞的是在细胞的哪个部位进行的?
答:细胞的胞液中 3、糖异生的概念和意义? 答: 概念:由非糖物质转变为葡萄糖或糖原的过程。 意义:由非糖物质合成糖以保持血糖浓度的相对恒定;有利于乳酸的利用;可协助氨基酸代谢。 生糖氨基酸、丙酮酸、乳酸、乙酰COA哪个不能异生成糖? 答:乙酰COA 4、什么是呼吸链? 答:又称电子传递链,是指底物上的氢原子被脱氢酶激活后经过一系列的中间传递体,最后传递给被激活的氧分子而生成水的全部体系。各种细胞色素在呼吸链中传递电子的顺序? 答:B-C1-C-AA3-O2 两条呼吸链的磷氧比分别是多少? 答:NADH呼吸链:P/O~2.5(接近于3) FADH2呼吸链:P/O~1.5(接近于2) 氰化物中毒是由于抑制了哪种细胞色素? 答:Cytaa3(细胞色素氧化酶) 5、为了使长链脂酰基从胞浆转运到线粒体内进行脂肪酸的β-氧 化,所需要的载体是什么? 答:肉碱
6、氨基酸脱下的氨基通常以哪种化合物的形式暂存和运输?答:谷氨酰胺 参与尿素循环的非蛋白氨基酸有哪几种? 答:瓜氨酸和鸟氨酸 7、RNA 和 DNA 彻底水解后的产物有哪些不同? 答:DNA彻底水解产物:磷酸,脱氧脱氧核糖,鸟嘌呤,腺嘌呤, 胞嘧啶,胸腺嘧啶。 RNA彻底水解产物:磷酸,核糖核酸,鸟嘌呤,腺嘌呤,尿嘧啶,胸腺嘧啶 双链DNA 解链温度的增加,提示其中碱基含量高的是哪几种碱基?答:C和G(胞嘧啶和鸟嘌呤) 8、蛋白质一级结构的概念? 答:蛋白质的一级结构是指多肽链上氨基酸残基的排列顺序,即氨基酸序列。 维系蛋白质一级结构的化学键主要是什么键? 答:肽键 9、蛋白质变性后可出现哪些变化? 答:破坏次级键和二硫键,不改变蛋白质的一级结构。如:溶解度降低,易形成沉淀析出,结晶能力丧失,分子形状改变,酶失去活力,激素蛋白失去原来的生理功能。
生物化學實習 1 緒論 (一) 原理 1. 光依據其波長來分類: (1) 200nm~400nm 短波屬於紫外光 (2) 400nm~700nm 可見光波長 (3) 700nm~900nm 長波屬於近紅外光 2. 光通過溶液時,特定波長的光被吸收,眼睛察覺到的是沒有被吸收的波長。 核黃素會吸收450nm 的光,紅光與黃光會通過溶液而被肉眼所見。
第一單元 生化實驗基本原理及技術 2 圖1-1光譜儀 光譜儀可用來鑑定及定量純或不純的溶液中所含有的特定化合物,主要原理是基於兩個物理定律:1.柏朗定律;2.比爾定律 。 1. 柏朗定律:每單位厚度溶液其吸收入射光的比率為定值,被溶液吸收的入射光量與入射光強度無關。被每單位厚度溶液吸收的入射光比率為定值,每一單位厚度溶液若吸收10%的光,則光經過每一單位厚度溶液時,其強度即減少10%。 I =I 0 ? e -αι I :穿透光強度 I 0:入射光強度 α :溶液吸光係數 ι:光路徑長度 柏朗定律中以對數為底轉換公式,將吸光係數α轉換成比例常數K → log 10 I 0 / I =K ι log 10 I 0 / I = 吸光值(absorbance ;A) 或光密度值(optical density ; OD)
生物化學實習 3 2. 比爾定律:光經過吸光物質所產生的吸光值,與溶液中每單位面積所含的吸光物質數目成比例。 比爾定律描述比例常數K 與待測吸光溶液中溶質的濃度有關。 K =εc ε:消光指數 c :吸光物質濃度 I = I 0? 10-εc ι log 10 I 0 / I = A =log 1010εc ι= εc ι 當ι(光路徑長度)=1 cm 時 log 10 I 0 / I = A =log 1010εc = εc 特定溶質在特定波長下,消光係數ε為一常數。因此,當吸光物質的濃度變成兩倍,於相同的光路徑下,被吸收的光量也會變成兩倍。 圖1-2 22 μM 溶於0.1M 磷酸鈉,pH 7.06,1公分 光路徑(light path)的條件下測定 波長 吸 光 值
《动物生物化学实验》复习题 一.填空题 1、生物化学实验的常用技术包括、、等。 2、牛奶中的主要蛋白质是,其占牛奶蛋白质总量的,其在pH值为的缓冲液中容易沉淀。 3、将制备酪蛋白时所得乳清,徐徐加热。即出现沉淀。此为乳清中的 和。 4、Folin-酚试剂由和组成。 5、福林酚法测定蛋白质含量时,样品蛋白质含量的适宜范围为ug/mL。 6、酶促反应速度最大时的环境温度称为,能使酶活性降低或丧失的物质称为,而对淀粉酶起此作用的物质是。 7、酶促反应速度最大时的pH称为,能使酶活性从无到有或使酶活性增加的物质称为,而对淀粉酶起此作用的物质是。 8、淀粉酶具有高度的性,催化蔗糖水解。 9、高浓度的硫酸铵一方面破坏了IgG分子表面的,而另一方面中和了其分子表面的,致使分子之间容易碰撞而沉淀。 10、DNA主要存在于,在细胞中,它与结合形成。 11、脱氧核糖核蛋白体在 mol/L的NaLl溶液中溶解度小,在mol/L的NaLl溶液中溶解度大。 12、不连续的聚丙烯酰胺凝胶电泳具有较高的分辨率,是因为电泳时会产生三大效应,即,和电荷效应。 13、使用硫酸铵分级沉淀的优点:系数小而且大,不易引起蛋白质。 二.是非题 ()1、酪蛋白在稀碱溶液中易溶解。 ()2、酪蛋白是一种不含硫的蛋白质。 ()3、Folin-酚法是一种光谱技术,主要仪器是可见光分光光度计。 ()4、Folin-酚法测定蛋白质含量时,样品应进行适当稀释。 ()5、Folin-酚法是测定蛋白质含量的常用方法。 ()6、Folin-酚法应该用同种蛋白质做对照。 ()7、做温度对淀粉酶活性影响时,沸水浴中试管取出后即可直接加入碘液观察
运动生物化学实验指导 实验一实验基本技术操作 一、实验目的 (一)了解实验室规则及注意事项。 (二)学习运动生物化学实验常用仪器的使用及清洗方法。 (三)学习721型分光光度计的使用方法。 二、实验原理 运动生物化学是研究人体运动时体内的化学变化。运动生物化学的实验方法基本上是化学的方法,用定量及定性的分析方法来观察机体内物质代谢的规律,所以实验时必须做到定性的洁净及定量的精确,因此实验取样要准确、样品要无污染。 对于相同物质和相同波长的单色光来说,溶液的光密度和溶液的浓度呈正比。配制各种浓度的CuSO4溶液,然后在780nm波长下比色,测定各种浓度的CuSO4溶液吸光度值,并制作曲线图。 三、实验器材 试管、CuSO4溶液、蒸馏水、721分光光度计、移液管、吸耳球等。 四、实验步骤 (一)玻璃仪器的清洗。 (二)使用移液管的移液操作及721分光光度计的使用。 取4支大试管,编号,按表7-1进行操作: 表7-1 CuSO4溶液的测定 以CuSO4溶液浓度为横坐标,吸光度值为纵坐标,将3种不同浓度的CuSO4溶液的光密度值分别点在坐标纸上,通过3点绘制成曲线图,并对实验结果进行分析。 五、注意事项 (一)玻璃仪器清洗后注意检查,管壁不能留有水珠。 (二)使用移液管吸取液体时一定要缓慢平稳,不要太快、太猛。 六、作业与思考 (一)玻璃仪器的清洗有哪些基本要求? 实验二血红蛋白的测定 血红蛋白(Hb)是红细胞中的一种重要蛋白质,1分子的Hb是由4分子的亚铁血红素和1分子的珠蛋白结合而成的。 Hb的主要生理功能是运输氧气(O2)、二氧化碳(CO2)和对酸性物质(H+)起缓冲作用,参与体内的酸碱平衡调节。运动时机体需氧增加,故血红蛋白增加,有利于为组织提供氧气,促进物质的有氧代谢和带走CO2,而且也能起中和酸性的作用。如果血红蛋白下降,氧供应减少,影响运动能力。 运动员安静时血红蛋白值与正常人没有明显差异。一般人Hb的正常值男性为120-160g/L;女性110-150g/L。临床上常用判断贫血的标准,即成年男性低于120 g/L;成年女性低于110 g/L;而14岁以下的少年、儿童,不论男女,均以低于120 g/L作为贫血。
食品生物化学实验要求 1.学生做实验前必须写好实验预习报告,做好实验预习,无实验预习报告者不 许进入实验室。每大组实验人数28人,4人一小组。 2.实验试剂的配制,现场由教师指导,学生操作完成。学生在试剂配制过程中, 掌握试剂配置的基本步骤,基本方法和注意事项。 3.实验室所有设备都必须按说明书使用,器皿要小心使用,按规范要求操作, 如有损坏,照价赔偿。 4.卫生要求:每次试验完毕小组成员务必将本试验台及地面收拾整洁,器皿摆 放整齐有序,如哪组成员发现没有搞好自己组的环境卫生,这次试验的所有组员的实验报告都会扣分。 一、10食品科学食品生物化学实验项目表 1. 淀粉的显色、水解和老化(4学时) 2. 蛋白质的功能性质(4学时) 3. 牛奶中酪蛋白等电点测定和氨基酸的分离鉴定(4学时) 4. 或果胶的提取(4学时) 5. 酶的性质实验(4学时) 实验总课时:16学时
二、食品生物化学实验指导书 实验一淀粉的显色、水解和老化 一、实验目的和要求 1、了解淀粉的性质及淀粉水解的原理和方法。 2、掌握淀粉水解的条件和产物的实验方法。 3、淀粉的老化原理和方法 二、实验原理 1、淀粉与碘的反应直链淀粉遇碘呈蓝色,支链淀粉遇碘呈紫红色,糊精遇碘呈蓝紫、紫、橙等颜色。这些显色反应的灵敏度很高,可以用作鉴别淀粉的定量和定性的方法,也可以用它来分析碘的含量。纺织工业上用它来衡量布匹退浆的完全度,它还可以用来测定水果果实(如苹果等)的淀粉含量。 近年来用先进的分析技术(如X射线、红外光谱等)研究碘跟淀粉生成的蓝色物,证明碘和淀粉的显色除吸附原因外,主要是由于生成包合物的缘故。直链淀粉是由α-葡萄糖分子缩合而成螺旋状的长长的螺旋体,每个葡萄糖单元都仍有羟基暴露在螺旋外。碘分子跟这些羟基作用,使碘分子嵌入淀粉螺旋体的轴心部位。碘跟淀粉的这种作用叫做包合作用,生成物叫做包合物。 在淀粉跟碘生成的包合物中,每个碘分子跟6个葡萄糖单元配合,淀粉链以直径0.13 pm绕成螺旋状,碘分子处在螺旋的轴心部位。 淀粉跟碘生成的包合物的颜色,跟淀粉的聚合度或相对分子质量有关。在一定的聚合度或相对分子质量范围内,随聚合度或相对分子质量的增加,包合物的颜色的变化由无色、橙色、淡红、紫色到蓝色。例如,直链淀粉的聚合度是200~980或相对分子质量范围是32 000~160 000时,包合物的颜色是蓝色。分支很多的支链淀粉,在支链上的直链平均聚合度20~28,这样形成的包合物是紫色的。糊精的聚合度更低,显棕红色、红色、淡红色等。下表就是淀粉的聚合度和生成碘包合物的颜色。 表 2-1 淀粉的聚合度和生成碘包合物的颜色 淀粉跟碘生成的包合物在pH=4时最稳定,所以它的显色反应在微酸性溶液里最明显。 2、淀粉的水解淀粉是一种重要的多糖,是一种相对分子量很大的天然高分子化合物。虽属糖类,但本身没有甜味,是一种白色粉末,不溶于冷水。在热水里淀粉颗粒会膨胀,有一部分淀粉溶解在水里,另一部分悬浮在水里,形成胶状淀粉糊。淀粉进入人体后,一部分淀粉收唾液所和淀粉酶的催化作用,发生水解反应,生成麦芽糖;余下的淀粉在小肠里胰脏分泌出的淀粉酶的作用下,继续进行水解,生成麦芽糖。麦芽糖在肠液中麦芽糖酶的催化下,水解为人体可吸收的葡萄糖,供人体组织的营养需要。反应过程为:(C6H12O5)m→(C6H10O5)n→C12H22O11→C6H12O6 淀粉糊精麦芽糖葡萄糖
《动物生物化学》 教学大纲 学时:54学时理论学分:4.5学分 适用对象:动物科学、动物医学二年级学生 先修课程:动物学、化学(有机化学、无机化学、分析化学) 考核要求:平时20%(小测、实验)、期中考试(20%)、期末考试(60%) 使用教材及主要参考书: 《生物化学》(第二版),天津农学院主编,中国农业出版社,2002年4月 王镜岩主编,《生物化学》(第三版上下册),高等教育出版社,2002年9月 黄锡泰、于自然主编(第二版),〈现代生物化学〉,化学工业出版社,2005年7月 周顺伍,《动物生物化学》(第三版),中国农业出版社,1999年十月 本课程是农业院校动物医学、动物科学本科专业以及相关专业的一门重要专业基础课。动物生物化学是研究动物生命的化学,是研究生物分子、特别是生物大分子相互作用、相互影响以表现生命活动现象原理的科学。通过本课程的学习,不仅使学生了解生命现象的基本知识和生命运活动的基本规律,而且可以掌握与动物生理学、动物饲养学、动物遗传学、动物育种学、药理学临床诊断学等专业基础课以及后续专业课程相关的必备基本理论和技能。并初步有在今后学习中运用和解决问题的能力。 一、教学的基本任务 根据本课程特点,在教学过程中,教师一定要把基本概念,基本理论讲解的清楚、易懂,对重点章节要讲深、讲透,并注重各章节的相互联系。通过学习,使学生不仅能掌握生命活动的基本规律,而且能对物质的代谢途径、关键步骤、关键环节有深刻的认识,并且对物质的代谢又有相互关系的整体概念。从而培养学生具有一定的分析和解决问题的能力。通过实验教学培养学生具备初步的科学研究能力。 章节课程内容学时 第一章绪论 1 第二章第三章第四章第五章第六章第七章第八章第九章第十章蛋白质的结构与功能 酶 糖类代谢 生物氧化 脂类代谢 含氮小分子的代谢 核酸的结构 核酸的生物学功能 生物膜和动物激素的信号调节 8 6 6 4 5 8 5 5 6 二、课程内容与要求 绪论 (一)教学目的 通过本章的学习要掌握生物化学的基本概念、研究内容及生物化学与动物医学和动物科学的关系,了解生物化学的发展史。 (二)教学内容 1.生物化学的概念; 2.生物化学的发展; 3.生物化学与畜牧和兽医 第二章蛋白质的结构与功能 (一)教学目的
生物化学实验报告 姓名:吴瑞 学号: 3120016004 专业年级: 2012级临床医学(妇幼保健) 组别:第四实验室 生物化学与分子生物学实验教学中心
一、实验室规则 1.实验前应认真预习实验指导,明确实验目的和要求,写出预实验报告。 2.进入实验室必须穿白大衣。严格遵守实验课纪律,不得无故迟到或早退。不得高声说话。严禁拿实验器具开玩笑。实验室内禁止吸烟、用餐。 3.严格按操作规程进行实验。实验过程中自己不能解决或决定的问题,切勿盲目处理,应及时请教指导老师。 4.严格按操作规程使用仪器,凡不熟悉操作方法的仪器不得随意动用,对贵重的精密仪器必须先熟知使用方法,才能开始使用;仪器发生故障,应立即关闭电源并报告老师,不得擅自拆修。 5.取用试剂时必须“随开随盖”,“盖随瓶走”,即用毕立即盖好放回原处,切忌“张冠李戴”,避免污染。 6.爱护公物,节约水、电、试剂,遵守损坏仪器报告、登记、赔偿制度。 7.注意水、电、试剂的使用安全。使用易燃易爆物品时应远离火源。用试管加热时,管口不准对人。严防强酸强碱及有毒物质吸入口内或溅到别人身上。任何时候不得将强酸、强碱、高温、有毒物质抛洒在实验台上。 8.废纸及其它固体废物严禁倒入水槽,应倒到垃圾桶内。废弃液体如为强酸强碱,必须事先用水稀释,方可倒入水槽内,并放水冲走。 9.以实事求是的科学态度如实记录实验结果,仔细分析,做出客观结论。实验失败,须认真查找原因,而不能任意涂改实验结果。实验完毕,认真书写实验报告,按时上交。 10.实验完毕,个人应将试剂、仪器器材摆放整齐,用过的玻璃器皿应刷洗干净归置好,方可离开实验室。值日生则要认真负责整个实验室的清洁和整理,保持实验整洁卫生。离开实验室前检查电源、水源和门窗的安全等,并严格执行值日生登记制度。