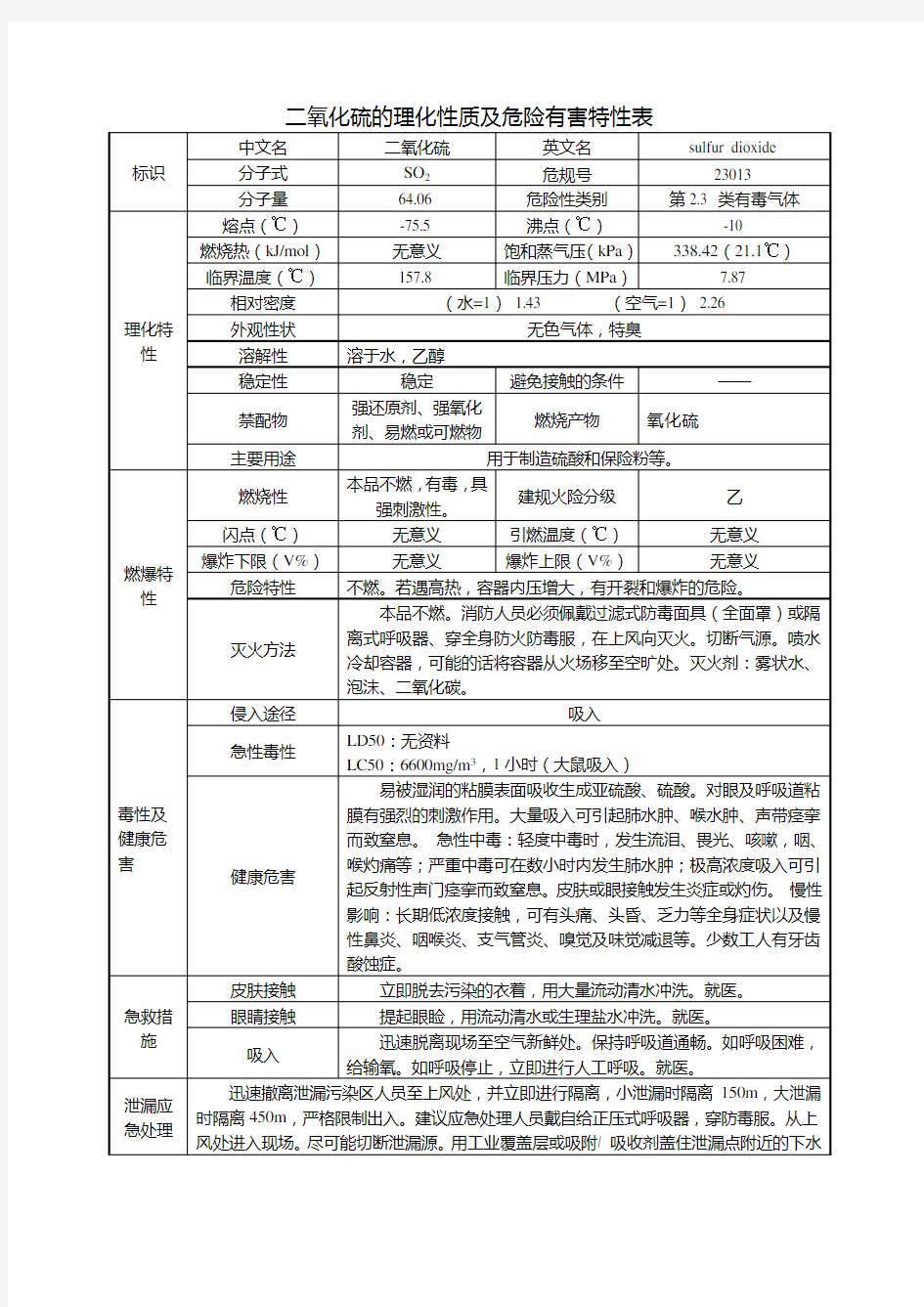

二氧化硫的理化性质及危险有害特性表
标识中文名二氧化硫英文名sulfur dioxide 分子式SO2危规号23013
分子量64.06 危险性类别第2.3 类有毒气体
理化特
性
熔点(℃)-75.5 沸点(℃)-10
燃烧热(kJ/mol)无意义饱和蒸气压(kPa)338.42(21.1℃)临界温度(℃)157.8 临界压力(MPa)7.87 相对密度(水=1)1.43 (空气=1)2.26
外观性状无色气体,特臭
溶解性溶于水,乙醇
稳定性稳定避免接触的条件——
禁配物
强还原剂、强氧化
剂、易燃或可燃物
燃烧产物氧化硫主要用途用于制造硫酸和保险粉等。
燃爆特
性
燃烧性
本品不燃,有毒,具
强刺激性。
建规火险分级乙闪点(℃)无意义引燃温度(℃)无意义
爆炸下限(V%)无意义爆炸上限(V%)无意义危险特性不燃。若遇高热,容器内压增大,有开裂和爆炸的危险。
灭火方法
本品不燃。消防人员必须佩戴过滤式防毒面具(全面罩)或隔离式呼吸器、穿全身防火防毒服,在上风向灭火。切断气源。喷水
冷却容器,可能的话将容器从火场移至空旷处。灭火剂:雾状水、
泡沫、二氧化碳。
毒性及健康危害侵入途径吸入
急性毒性
LD50:无资料
LC50:6600mg/m3,1小时(大鼠吸入)
健康危害
易被湿润的粘膜表面吸收生成亚硫酸、硫酸。对眼及呼吸道粘膜有强烈的刺激作用。大量吸入可引起肺水肿、喉水肿、声带痉挛
而致窒息。急性中毒:轻度中毒时,发生流泪、畏光、咳嗽,咽、
喉灼痛等;严重中毒可在数小时内发生肺水肿;极高浓度吸入可引
起反射性声门痉挛而致窒息。皮肤或眼接触发生炎症或灼伤。慢性
影响:长期低浓度接触,可有头痛、头昏、乏力等全身症状以及慢
性鼻炎、咽喉炎、支气管炎、嗅觉及味觉减退等。少数工人有牙齿
酸蚀症。
急救措
施皮肤接触立即脱去污染的衣着,用大量流动清水冲洗。就医。
眼睛接触提起眼睑,用流动清水或生理盐水冲洗。就医。
吸入
迅速脱离现场至空气新鲜处。保持呼吸道通畅。如呼吸困难,给输氧。如呼吸停止,立即进行人工呼吸。就医。
泄漏应急处理
迅速撤离泄漏污染区人员至上风处,并立即进行隔离,小泄漏时隔离150m,大泄漏时隔离450m,严格限制出入。建议应急处理人员戴自给正压式呼吸器,穿防毒服。从上风处进入现场。尽可能切断泄漏源。用工业覆盖层或吸附/ 吸收剂盖住泄漏点附近的下水
道等地方,防止气体进入。合理通风,加速扩散。喷雾状水稀释、溶解。构筑围堤或挖坑收容产生的大量废水。如有可能,用一捉捕器使气体通过次氯酸钠溶液。漏气容器要妥善处理,修复、检验后再用。
操作注意事项
严加密闭,提供充分的局部排风和全面通风。操作人员必须经过专门培训,严格遵守操作规程。建议操作人员佩戴自吸过滤式防毒面具(全面罩),穿聚乙烯防毒服,戴橡胶手套。远离易燃、可燃物。防止气体泄漏到工作场所空气中。避免与氧化剂、还原剂接触。搬运时轻装轻卸,防止钢瓶及附件破损。配备泄漏应急处理设备。
包装方
法包装类别:O52
包装方法:钢质气瓶;安瓿瓶外普通木箱。
储存注意事项
储存于阴凉、通风的库房。远离火种、热源。库温不宜超过30℃。应与易(可)燃物、氧化剂、还原剂、食用化学品分开存放,切忌混储。储区应备有泄漏应急处理设备。
运输注意事项
本品铁路运输时限使用耐压液化气企业自备罐车装运,装运前需报有关部门批准。铁路运输时应严格按照铁道部《危险货物运输规则》中的危险货物配装表进行配装。采用刚瓶运输时必须戴好钢瓶上的安全帽。钢瓶一般平放,并应将瓶口朝同一方向,不可交叉;高度不得超过车辆的防护栏板,并用三角木垫卡牢,防止滚动。严禁与易燃物或可燃物、氧化剂、还原剂、食用化学品等混装混运。夏季应早晚运输,防止日光曝晒。公路运输时要按规定路线行驶,禁止在居民区和人口稠密区停留。铁路运输时要禁止溜放。
防护措
施
工程控制:严加密闭,提供充分的局部排风和全面通风。提供安全淋浴和洗眼设备。
呼吸系统防护:空气中浓度超标时,佩戴自吸过滤式防毒面具(全面罩)。紧急事态抢救或撤离时,建议佩戴正压自给式呼吸器。眼睛防护:呼吸系统防护中已作防护。
身体防护:穿聚乙烯防毒服。
手防护:戴橡胶手套。
其他防护:工作现场禁止吸烟、进食和饮水。工作完毕,淋浴更衣。保持良好的卫生习惯。
苏教版化学1第4专题第一单元 《二氧化硫的性质和作用》教学设计 王海英 (江苏省新海高级中学江苏连云港222006) 一、教学设计 本节课的设计以新课程理念为指导,改变以往对元素化合物知识的学习模式:结构→性质→用途,而是从现实实际和观察到的现象出发,让学生通过观察分析→推测性质→实验验证→得出结论,体现探究式学习方式。本节课以“酸雨”为背景,课前循环播放的优美风景图片与一组环境污染图片的对比,视觉冲击深深触动学生的心灵,接着课堂创设“模拟酸雨”的情境,引发学生的探究欲,并由此引出相关问题,设计展开四个探究活动:①二氧化硫可溶于水且溶液显酸性。 ②探究SO 的还原性。③探究二氧化硫的氧化产物。④探究二氧化硫的漂白性。这 2 些场景的创设,有效地激发了学生的学习热情;将知识问题化,通过化学实验、分析化学原理、类比迁移等化学方法使问题得以解决;遵循学生的认知规律,由浅入深,由现象到本质,使教学目标得以达成。 二、教材分析 本课时是苏教版《化学1》专题4第一单元的第一课时。二氧化硫是高中化学学习的重要氧化物之一,是一种既具有氧化性又具有还原性的酸性氧化物,是工业生产硫酸环节中的一种重要的物质,也是学生初步认识环境污染中大气污染的一种主要物质。通过实验手段探究其性质,提高学生学习化学的兴趣、培养学生的探究精神;通过了解二氧化硫对环境的危害,加强学生的环保意识;通过对二氧化硫用途的学习,有助于学生辩证看待事物。 三、教学目标 知识与技能: (1)了解二氧化硫的作用,了解可逆反应的概念; (2)掌握二氧化硫的化学性质; (3)培养学生用新概念重新理解旧知识的能力(可逆反应的概念);培养学生设计实验、动手实验、观察现象,并根据实验现象得出可能的规律的能力。 过程与方法 通过二氧化硫的组成及价态,分析其可能的性质,并设计实验探究,激发学生学习化学的兴趣、探索新知识的欲望,且在实验研究中培养求实,进取的优良品质。 情感态度价值观 通过图片展示环境污染的情景,对学生进行防止环境污染、保护环境的教育,使其意识到自己的义务和责任。 教学重点:二氧化硫的性质教学难点:实验方案的设计 四、教学过程 1.引入新课 【教师投影】一组美丽的画面 【教师引入】清山秀水惹人醉,如画美景不胜收。美丽的风景需要我们珍惜和保护,否则我们将会看到另一番景象。 【教师投影】一组被酸雨污染的画面
目录 表- 石油醚的理化性质及危险特性 (1) 表- 石油原油的理化性质及危险特性 (2) 表- 石脑油的理化性质及危险特性 (3) 表- 正庚烷的理化性质及危险特性 (4) 表- 正辛烷的理化性质及危险特性 (5) 表- 异辛烷的理化性质及危险特性 (6) 表- 甲基环己烷的理化性质及危险特性 (7) 表- 二氯乙烷的理化性质及危险特性 (8) 表- 苯的理化性质及危险特性 (9) 表- 溶剂苯的理化性质及危险特性 (10) 表- 粗苯的理化性质及危险特性 (11) 表- 甲苯的理化性质及危险特性 (12) 表- 甲醇的理化性质及危险特性 (13) 表- 乙醇的理化性质及危险特性 (14) 表- 正丙醇的理化性质及危险特性 (15) 表- 异丙醇的理化性质及危险特性 (16) 表- 叔丁醇的理化性质及危险特性 (17) 表- 正戊醛的理化性质及危险特性 (18) 表- 2-丁酮的理化性质及危险特性 (19) 表- 甲基异丁基(甲)酮的理化性质及危险特性 (20) 表- 双丙酮醇的理化性质及危险特性 (21)
表- 甲基叔丁基醚的理化性质及危险特性 (23) 表- 乙二醇二甲醚的理化性质及危险特性 (24) 表- 四氢噻吩的理化性质及危险特性 (25) 表- 甲酸正丙酯的理化性质及危险特性 (26) 表- 甲酸异丙酯的理化性质及危险特性 (27) 表- 甲酸正丁酯的理化性质及危险特性 (28) 表- 甲酸异丁酯的理化性质及危险特性 (29) 表- 乙酸乙酯的理化性质及危险特性 (30) 表- 乙酸正丙酯的理化性质及危险特性 (31) 表- 乙酸异丙酯的理化性质及危险特性 (32) 表- 乙酸正丁酯的理化性质及危险特性 (33) 表- 乙酸异丁酯的理化性质及危险特性 (34) 表- 丙烯酸甲酯的理化性质及危险特性 (35) 表- 丙烯酸乙酯的理化性质及危险特性 (36) 表- 异丁烯酸甲酯的理化性质及危险特性 (37) 表- 甲基丙烯酸乙酯的理化性质及危险特性 (38) 表- 碳酸(二)甲酯的理化性质及危险特性 (39) 表- 钛酸(四)乙酯的理化性质及危险特性 (40) 表- 钛酸(四)正丙酯的理化性质及危险特性 (41) 表- 钛酸(四)异丙酯的理化性质及危险特性 (42) 表- 乙腈的理化性质及危险特性 (43)
乙酸 Acetic Acid 其它名称:中文:醋酸 英文: 国内危规编号:81601 UN编号:2789 包装分类:Ⅱ包装标志:20 熔点(℃):16.7 沸点(℃):118.1 相对密度(水=1):1.05 相对密度(空气=1):2.07 稳定性:稳定聚合性:不聚合 爆炸上限(%):17.0 爆炸下限(%):4.0 分子式:C2H4O2 闪点(℃):39 危险性类别:8.1类酸性腐蚀品污染类别:D 船型:3 舱型:2G 溶解性:溶于水、醚、甘油,不溶于二硫化碳 外观性状:无色透明液体,有刺激性酸味 灭火方法:雾状水、二氧化碳、抗溶性泡沫、干粉 危险特性:易燃,其蒸气与空气形成爆炸性混合物,遇明火、高热能引起爆炸,与强氧化剂可发生反应。 应急措施:057 盐酸 Hydrochloric Acid 其它名称:中文:氢氯酸,盐镪水,焊锡药水 英文:chlorichydro Acid 国内危规编号:81013 UN编号:1789 包装分类:Ⅰ包装标志:20 熔点(℃):-114.8(纯洁) 沸点(℃):108.6(20%) 相对密度(水=1):1.20 相对密度(空气=1):1.26 稳定性:稳定聚合性:不聚合 爆炸上限(%):无意义爆炸下限(%):无意义 分子式:HCl 闪点(℃):无意义 危险性类别:8.1类酸性腐蚀品污染类别:D 船型:3 舱型:1G 溶解性:与水互溶,溶于碱液 外观性状:无色或微黄色发烟液体,有刺激的酸味
灭火方法:雾状水、砂土 危险特性:能与一些活性金属粉末发生反应,放出氢气。具有较强的腐蚀性,与大事发生中和反应,放出大量热。 应急措施:057 硫酸 Sulfuric Acid 其它名称:中文: 英文: 国内危规编号:81007 UN编号:1830 包装分类:I 包装标志:20 熔点(℃):10.5 沸点(℃):330.0 相对密度(水=1):1.83 相对密度(空气=1):3.4 稳定性:稳定聚合性:不聚合 爆炸上限(%):无意义爆炸下限(%):无意义 分子式:HSO4 闪点(℃):无意义 危险性类别:8.1类酸性腐蚀品污染类别:C 船型:3 舱型:2G 溶解性:与水互溶,溶于碱液 外观性状:无色透明油状液体 灭火方法:砂土、干粉、二氧化碳,禁用水、 危险特性:能易燃物和有机物接触发生剧烈反应,放出氢气。具有较强的腐蚀性,与水放出大量热。 应急措施:057 硝酸 Nitric Acid 其它名称:中文: 英文: 国内危规编号:81002 UN编号:2031 包装分类:I 包装标志:20 熔点(℃):-42(无水) 沸点(℃):86(无水) 相对密度(水=1):1.50(无水) 相对密度(空气=1):2.17 稳定性:稳定聚合性:不聚合 爆炸上限(%):无意义爆炸下限(%):无意义
《二氧化硫的性质及其性质比较》教学设计 一、课题分析 二氧化硫既是工业上制备硫酸的原料气之一,也是污染环境的一种气体。其化学性质的多样性——酸性、氧化性、还原性、漂白性,成为教学中的重难点,更是高考命题的热点和切入点。在教学过程中学生对二氧化硫的化学性质有许多模糊甚至错误的认识——如能否与BaCl2或CaCl2溶液反应;与Ba(NO3)2、Ca(ClO)2溶液发生什么样的反应;漂白原理及其检验方法……。 本节课试图通过比较法对二氧化硫的化学性质进行阐释,以期达到明确概念,澄清“模糊”的目的;巩固氧化还原反应和离子反应的知识;利用历年综合性的高考试题,将知识点和考点联系起来,加深对二氧化硫化学性质的认识,从而提升根据题设背景提取题给信息、综合分析和快捷解决问题的能力。 二、教学目标 1.知识与技能 (1)知道常见化学试剂的颜色及其变化 (2)掌握二氧化硫的化学性质 (3)巩固氧化还原反应配平和离子方程式书写的技能 2.过程与方法 (1)掌握比较法在化学学习中的应用 比较法是处理和解决问题的一种重要方法,通过对物质或事物的纵横比较得出科学的结论。比较法有“同中求异”和“异中求同”: 同中求异——将同类问题或事件进行分析比较,找到其不同点 异中求同——将异类问题或事件进行分析比较,找到其相同点 (2)明确知识点与高考考点的联系 (3)强化提升审题能力和综合分析能力,训练破题的技巧与方法 3.情感、态度价值观 (1)运用思辨和实证的思维方法,明确二氧化硫的“利”与“害”,趋利避害 (2)懂得规范操作和科学表述的重要性 三、教学过程 (1)实验 将二氧化硫分别通入BaCl2(aq)、BaCl2-NH3(aq)、H2S(aq)、石蕊(aq)、Ba(NO3)2(aq)、MnO4—/H+(aq)、I2-淀粉(aq)、Br2(aq)、FeCl3(aq)、品红(aq)中。 1.现象描述 2.书写相关的化学方程式或离子方程式 将二氧化硫换成二氧化碳 分析比较现象,综合得出结论 (2)漂白性概念辨析 1.使品红褪色的气体就是SO2?检验SO2的操作? 2.SO2能使石蕊溶液先红后褪吗? 3.SO2使溴水和酸性高锰酸钾溶液褪色是其漂白作用吗?为什么? 4.SO2使NaOH-酚酞溶液的红色是其漂白作用吗? (3)还原性 1.还原性:S2—>SO2或H2SO3或HSO3—>I— 2.遇到氧化剂,勿忘还原性
三氯氧磷-基本信息 中文名称:三氯氧磷 英文名称:phosphorus oxychloride 别名:氧氯化磷;氯化磷酰;磷酰氯;三氯氧化磷 CAS No.:10025-87-3 分子式:POCl3 分子量:153.33 危险标记:20(酸性腐蚀品) 包装类别:O52 包装方法:闭口厚钢桶,采用2~3毫米厚的钢板焊接制成,桶身套有两道滚箍。螺纹口、盖、垫圈等封口件配套完好,每桶净重不超过300 公斤;玻璃瓶或塑料桶(罐)外全开口钢桶;玻璃瓶或塑料桶(罐)外普通木箱或半花格木箱;磨砂口玻璃瓶或螺纹口玻璃瓶外普通木箱;安瓿瓶外普通木箱。 三氯氧磷-理化性质 主要成分:含量:工业级≥99.0%。 外观与性状:无色透明发烟液体,有辛辣气味。 熔点(℃):1.2 沸点(℃):105.1
相对密度(水=1):1.68 相对蒸气密度(空气=1): 蒸气压(kPa):5.33(27.3℃) 闪点: 燃烧热(kJ/mol): 化合物在水中的溶解度(S): 稳定性和反应活性:稳定 危险特性:遇水猛烈分解, 产生大量的热和浓烟, 甚至爆炸。对很多金属尤其是潮湿空气存在下有腐蚀性。 溶解性: 禁配物:强还原剂、活性金属粉末、水、醇类。 三氯氧磷-应急处置 皮肤接触:立即脱去污染的衣着,用大量流动清水冲洗至少15分钟。就医。 眼睛接触:立即提起眼睑,用大量流动清水或生理盐水彻底冲洗至少15分钟。就医。 吸入:迅速脱离现场至空气新鲜处。保持呼吸道通畅。如呼吸困难,给输氧。如呼吸停止,立即进行人工呼吸。就医。 食入:用水漱口,无腐蚀症状者洗胃。忌服油类。就医。
呼吸系统防护:可能接触其蒸气时,必须佩戴自吸过滤式防毒面具(全面罩)或隔离式呼吸器。紧急事态抢救或撤离时,建议佩戴空气呼吸器。 眼睛防护:呼吸系统防护中已作防护。 身体防护:穿橡胶耐酸碱服。 手防护:戴橡胶耐酸碱手套。 其他防护:工作现场禁止吸烟、进食和饮水。工作完毕,淋浴更衣。单独存放被毒物污染的衣服,洗后备用。保持良好的卫生习惯。 泄漏应急处理:迅速撤离泄漏污染区人员至安全区,并立即隔离150m,严格限制出入。建议应急处理人员戴自给正压式呼吸器,穿防酸碱工作服。不要直接接触泄漏物。尽可能切断泄漏源。小量泄漏:用砂土、蛭石或其它惰性材料吸收。大量泄漏:构筑围堤或挖坑收容。在专家指导下清除。 有害燃烧产物:氯化氢、氧化磷、磷烷。 灭火方法:灭火剂:干粉、干燥砂土。禁止用水。 三氯氧磷-管理方法 操作的管理:密闭操作,注意通风。操作尽可能机械化、自动化。操作人员必须经过专门培训,严格遵守操作规程。建议操作人员佩戴自吸过滤式防毒面具(全面罩),穿橡胶耐酸碱服,戴橡胶耐酸碱手套。避免产生烟雾。防止烟雾和蒸气释放到工作场所空气中。避免与还原剂、活性金属粉末、醇类接触。尤其要注意避免与水接触。搬运时要轻装轻卸,防止包装及容器损坏。配备泄漏应急处理设备。倒空的容器可能残留有害物。
《二氧化硫的性质》说课稿 大家好!我今天要说课的题目是《二氧化硫的性质》,本次说课我将分四个部分,它们分别是教材分析、教法分析、学法指导以及教学过程。 在教材分析中我将对教材从教材地位、教学背景、教学内容、教学目标以及重点、难点及其依据五个角度进行分析。 本节内容选自人教版新教材高一必修1课本第四章非金属及其化合物第三节硫和氮的氧化物的其中一部分内容,安排课时为15分钟。本节课所要接触到的非金属硫是学生学习了氯,溴,碘,硅,钠,镁,铝,铁,铜及其化合物的基础上,接触的又一种重要的化学元素,学生可以联系前面学习其他元素及其化合物的学习方法,类比运用到硫及其二氧化硫性质的学习上。本节课内容是建立在上节课的实验基础上的,上节课上一节课学生已经到实验室做了二氧化硫溶于水以及其使品红褪色的实验,并让同学们课后与小组同学进行共同探讨,得出小组讨论结果。本节课采用“实验回顾—现象分析—问题讨论—实验结果”的总体思路来安排教学内容,对上一节课的整个实验过程进行分步回顾讨论,师生通过对实验现象的回顾共同探讨出二氧化硫的物理性质和化学性质,其中本节课探讨的化学性质包括二氧化硫与水的反应与其漂白性。因此本节课为后面下一节课二氧化硫其他化学性质的学习奠定了很好的基础。 根据新课标和新课程改革的要求,配合教学大纲,以及结合课本教材,确定本节教学目标如下,它们分别是:知识与技能目标、过程与方法目标以及情感态度与价值观目标。 首先我们来看知识与技能目标: 在知识目标中使学生了解二氧化硫的物理性质,掌握二氧化硫的化学性质。 然后过程与方法目标: 在过程与方法目标中学生学会通过自己小组所得出结果与正确的实验结果进行对比,然后发现问题、解决问题,培养学生独立思考解决问题的能力;学生学会通过自己小组所得出结果与正确的实验结果进行对比,然后发现问题、解决问题,培养学生独立思考解决问题的能力。 最后我们来看情感态度与价值观目标: 在情感态度与价值观目标中让学生描述自己所做的实验现象,培养学生实事求是的科学态度;让学生在实验现象与实验结果的探讨中,培养学生的逻辑思维能力以及组员协作精神;让学生课后做巩固练习,培养学生学以致用的学习态度。 在了解了教学目标后,让我们再看一下本节课的重点、难点及其依据部分。 本节课的重点是二氧化硫与水的反应,难点是可逆反应,这样设计是因为二氧化硫与水反应是二氧化硫重要的化学性质,必须重点掌握。而二氧化硫与水反应又是可逆反应,可逆反应这个概念学生第一次接触,都比较陌生,对于刚接触可逆反应的高一学生来说是一个难点。在整个教学过程中,我将采用板书设计以及时间分配来强调和突破重难点,同时也采用学生实践的方法来强调重点。
项目 标识 理化性质 燃烧爆炸危 险性 甲烷理化特性表 内容 中文名甲烷别名沼气 分子式CH4 危险货物类别第类易燃气体 分子量危险货物编号21007 CAS 74-82-8 UN 编号1971 外观与性状无色无臭气体。 主要用途用作燃料和用于炭黑、氢、乙炔、甲醛等的制造。 溶解性微溶于水,溶于醇、乙醚。 熔点 (℃) 燃烧热 (kJ/mol) 沸点 (℃) 饱和蒸汽压 (kPa) ℃ ) 相对密度 (水=1) (-164 ℃) 临界温度 (℃ ) 相对密度 (空气 =1) 临界压力 (MPa) 火灾危险类别甲类稳定性 闪点 (℃) -188 聚合危害 引燃温度 (℃) 538 避免接触的条件 爆炸下限 (V/%) 燃烧 (分解 )产物一氧化碳、二氧化碳。爆炸上限 (V/%) 15 禁忌物强氧化剂、氟、氯。燃爆危险本品易燃,具窒息性。 包装与储存运输 毒性与健康 危害性危险特性 灭火方法 包装标志 包装方法 储存注意事项 运输注意事项 接触极限 毒性 健康危害 侵入途径 环境危害 皮肤接触 眼睛接触 易燃,与空气混合能形成爆炸性混合物,遇热源和明火有燃烧爆炸的危险。与五氧化 溴、氯气、次氯酸、三氟化氮、液氧、二氟化氧及其它强氧化剂接触剧烈反应。 切断气源。若不能切断气源,则不允许熄灭泄漏处的火焰。喷水冷却容器,可能的话 将容器从火场移至空旷处。灭火剂:雾状水、泡沫、二氧化碳、干粉。 包装类别052 钢质气瓶。 储存于阴凉、通风的库房。远离火种、热源。库温不宜超过 30℃。应与氧化剂等分开存 放,切忌混储。采用防爆型照明、通风设施。禁止使用易产生火花的机械设备和工 具。储区应备有泄漏应急处理设备。 采用刚瓶运输时必须戴好钢瓶上的安全帽。钢瓶一般平放,并应将瓶口朝同一方向, 不可交叉;高度不得超过车辆的防护栏板,并用三角木垫卡牢,防止滚动。运输时运 输车辆应配备相应品种和数量的消防器材。装运该物品的车辆排气管必须配备阻火装 置,禁止使用易产生火花的机械设备和工具装卸。严禁与氧化剂等混装混运。夏季应 早晚运输,防止日光曝晒。中途停留时应远离火种、热源。公路运输时要按规定路线 行驶,勿在居民区和人口稠密区停留。铁路运输时要禁止溜放。中国 MAC(mg/m 3):未制定标准 前苏联 MAC(mg/m 3):300 TLVIN: ACGIH 窒息性气体 TLVWN:未制定标准 LD50:无资料 LC50:无资料 甲烷对人基本无毒,但浓度过高时,使空气中氧含量明显降低,使人窒息。当空气中甲 烷达 25%~ 30%时,可引起头痛、头晕、乏力、注意力不集中、呼吸和心跳加速、共 济失调。若不及时脱离,可致窒息死亡。皮肤接触液化本品,可致冻伤。 若有冻伤,就医治疗。 急救措施防护措施 迅速脱离现场至空气新鲜处。保持呼吸道通畅。如呼吸困难,给输氧。如呼吸停止, 吸入 立即进行人工呼吸。就医。 食入 工程控制生产过程密闭,全面通风。 呼吸系统防护一般不需要特殊防护,但建议特殊情况下,佩戴自吸过滤式防毒面具(半面罩)。眼睛防护一般不需要特殊防护,高浓度接触时可戴安全防护眼镜。 身体防护穿防静电工作服。 手防护戴一般作业防护手套。
二氧化硫的性质和作用 【知识要点】 1.物理性质: 二氧化硫是一种色有气味的有毒气体,易液化;密度比空气,溶于水,常温、常压下1体积水大约能溶解体积的二氧化硫。 2.化学性质: 二氧化硫是一种酸性氧化物,它的水溶液pH 7(填>,<,=)。 (1)SO2是酸性氧化物:(请与CO2对比学习) a.与水反应:(H2SO3容易被氧化,生成硫酸)b. 与氧化钙反应: c.与碱反应:与NaOH溶液反应 与Ca(OH)2溶液反应 (2)SO2的漂白性: SO2气体通入到品红溶液中,现象____________;然后给溶液加热,现象_。 结论:____能漂白某些有色物质,这是由于它能与某些有色物质反应,生成_________的无色物质。而________时,这些无色物质又会发生_________,恢复原来颜色。 (3)SO2的强还原性: a.与氧气: b.与双氧水: c. 与氯水(溴水或碘水): d. 与酸性KMnO4 (4)SO2的弱氧化性: 与硫化氢气体: 3.二氧化硫的污染 a、SO2是污染大气的主要物质之一,主要来自于。 b、形成硫酸型酸雨(空气中硫的氧化物随雨水降下就成为酸雨,酸雨的pH<5.6。 正常的雨水由于溶解CO2形成弱酸H2CO3,pH约为5.6) c、硫酸型酸雨的形成有两条途径: d.、酸雨的危害: (1)酸雨进入江河湖泊,会导致__________难以生存,影响___________的繁殖 (2)酸雨落至土壤中,使其中的____、____、_____等营养元素溶出,并迅速流失,使土壤肥力____,并被逐渐酸化,农作物和树木的成长遭到破坏。 (3)酸雨会使桥梁、雕塑等建筑物的腐蚀加快。 e、防治酸雨减少酸雨的产生可采用的措施有:燃料脱硫;少用煤作燃料;开发新能源。 一、SO2中S元素处于中间价态,既有氧化性又有还原性(以还原性为主) a.弱氧化性:与硫化氢反应 b.较强还原性:可被多种氧化剂(如O2、Cl2、Br2、I2、HNO3、KMnO4、H2O2等)氧化 SO2与O2反应 SO2与H2O2反应 SO2使氯水褪色: SO2使溴水褪色:
(1)苯:别名纯苯、净苯、氢化苯。 1)性质及用途 理化性质:无色透明液体,有强烈芳香味,不溶于水,溶于醇、醚、丙酮等多数有机溶剂,易燃液体。 一般包装:易燃液体,小开口钢桶。 稳定性和危险性:易燃,蒸汽能与空气形成爆炸性混合物,遇热或明火易着火、爆炸。蒸汽比空气重,可扩散到相当远距离。 毒理学指标:急性中毒伴有头痛、头晕、恶心、呕吐、轻度兴奋、步态蹒跚等状态,严重者可发生昏迷、抽搐、血压下降,以致呼吸和循环衰竭;慢性中毒主要表现有神经衰弱综合征,造血系统改变,白细胞、血小板减少,重者出现再生障碍性贫血,少数病例在慢性中毒后可发生白血病,皮肤脱脂、干燥、皲裂、皮炎。 主要用途:用作溶剂及合成苯的衍生物、香料、染料、塑料、医药、炸药、橡胶。 2)安全防护措施 工程控制:生产过程密闭,加强通风;提供安全淋浴和洗眼设备。 呼吸系统防护:空气中浓度超标时,应佩戴自吸过滤式防毒面罩。紧急事态抢救或撤离时,应该佩戴空气呼吸器或氧气呼吸器。 眼睛防护:佩戴化学安全防护眼镜。身体防护:穿防毒物渗透工作服。手防护:佩戴橡胶手套。其它:工作现场禁止吸烟、进食和饮水。工作完毕,淋浴更衣。 3)应急措施 急救措施:对于急性中毒者,应迅速将中毒患者移到新鲜空气处,立即脱去被苯污染的衣服,用肥皂水清洗污染处的皮肤,注意保暖。
泄露处置:迅速撤离污染区人员至安全区,切断火源,应急处理人员带防毒面具和手套,穿一般消防防护服,在确保安全的情况下堵漏,用雾状水扑灭小面积火灾,驱散蒸汽及泄漏的液体,用活性炭、沙土或其它惰性材料吸收,然后用无火花工具收集运至废物处理场所,也可用不燃性分散剂制成的乳液刷洗,经稀释后排入废水处理系统。 消防方法:用泡沫、二氧化碳、干粉、沙土进行消防。 环境监测方法:水质检测管法、气体检测管法、便携式气相色谱法、快速检测管法《突发性环境污染事故应急监测与处理处置技术》、气体速测管。 (2)乙基苯:别名乙苯。 1)性质及用途理化性质:无色液体,有芳香气味。不溶于水,可混溶于乙醇、醚等多数有机溶剂。稳定性和危险性:易燃,其蒸气与空气可形成爆炸性混合物。遇明火、高热或与氧化剂接触,有引起燃烧爆炸的危险。与氧化剂接触会猛烈反应。流速过快,容易产生和积聚静电。其蒸气比空气重,能在较低处扩散到相当远的地方,遇明火会引着回燃。毒理学性质:乙苯毒性较低,但对皮肤、眼睛和呼吸道的刺激作用比甲苯强。吸入、食入或经皮肤吸收可引起中毒,出现头痛、咳嗽、呼吸困难,神志不清、腹痛、视力模糊、肌肉抽搐或肢体痉挛等症状,很快昏迷不醒,甚至死亡。大量乙苯泄漏进入水中时,由于比水轻,漂浮在水面。可造成鱼类和水生生物死亡,被污染水体散发出异味。主要用途:用于有机合成和用作溶剂。 2)安全防护措施呼吸系统防护:空气中浓度超标时,应该佩戴自吸过滤式防毒面罩(半面罩)。紧急事态抢救或撤离时,应该佩戴空气呼吸器或氧气呼吸器。眼睛防护:戴化学安全防护眼镜。身体防护:穿防毒渗透工作服。
二氧化硫的性质和应用 班级:姓名:2017/6/19 【教学目标】1、掌握二氧化硫的物理性质和化学性质 2、了解二氧化硫的应用及危害 3、了解酸雨的形成和防护 【知识梳理】 1.物理性质:二氧化硫是一种色有气味的有毒气体,易液化;密度比空气,溶于水,常温、常压下1体积水大约能溶解体积的二氧化硫。2.化学性质: (1)SO2是酸性氧化物:(请与CO2对比学习) a.与水反应: (H2SO3容易被氧化,生成硫酸) b.与碱反应:与NaOH溶液反应 与Ba(OH)2溶液反应 c.与某些盐溶液反应:与Na2CO3溶液反应 (2)SO2中S元素处于中间价态,既有氧化性又有还原性(以还原性为主) a.较强还原性:可被多种氧化剂(如O2、Cl2、Br2、I2、H2O2、HNO3、KMnO4等)氧化 ①SO2使溴水褪色: SO2+Br2+2H2O==H2SO4+2HBr ②SO2使氯水褪色: ③SO2与O2反应: ④SO2与H2O2反应: ⑤SO2使KMnO4溶液褪色: b.弱氧化性:与硫化氢反应 (3)SO2的漂白性:使品红褪色 3.二氧化硫的污染 SO2是污染大气的主要物质之一,主要来自于。 空气中硫的氧化物和氮的氧化物随雨水降下就成为酸雨,酸雨的pH<5.6。 正常的雨水由于溶解CO2形成弱酸H2CO3,pH约为5.6 硫酸型酸雨的形成有两条途径,反应方程式分别为: ① ② 【课堂练习】1.左图是古时用燃烧硫的方法漂白布料的 图片。请同学们分析其原理。 2.下列可以用来鉴别SO2和CO2的方法是[ ] A、通入紫色石蕊试液 B、观察颜色 C、通入澄清石灰水 D、通入品红溶液中 3.检验SO2气体中是否混有CO2气体,下列方法可采用的是() A.通过品红溶液B.通过澄清石灰水 C.先通过NaOH溶液,再通过澄清石灰水
二氧化硫的性质实验探究 一、实验教学目标 知识目标: (一)通过简单介绍二氧化硫的实验室制法,使学生掌握好实验室制取二氧化硫的反应原理,实验装置,并利用设计的装置制取二氧化硫,用于动手实验,提高学生分析和解决实际 问题的能力。 (二)通过分组实验探究,归纳出二氧化硫的性质。 能力目标: 让学生通过动手、观察、比较、思考提高归纳、总结、应用等各方面的能力。 情感目标: (一)培养学生良好的学习习惯,善于探索的思维方法,把课堂主动权交给学生。 (二)通过实验探究,培养学生求实、创新、合作的科学品质。 (三)通过师生、生生合作学习,研究性学习,体验探究成功的乐趣,激发学生探究欲。 (四)通过探究二氧化硫的性质实验,使学生掌握科学的试验方法,培养学生的逻辑思维 能力和动手能力。 (五)了解二氧化硫的物理性质;掌握二氧化硫的特殊性、漂白性和还原性。 (六)通过改进实验培养实验设计能力、观察能力、分析能力、探究能力和合作学习能力, 二、实验内容设计 实验探究1:用干燥的矿泉水瓶收集一瓶二氧化硫,然后向矿泉水瓶中注入蒸馏水,请 仔细观察实验现象,为什么注射蒸馏水而不是自来水? 实验探究2:向变瘪的矿泉水瓶中注入石蕊溶液,观察实验现象,这说明什么? 实验探究3:用干燥的试管收集二氧化硫,用橡胶塞塞住,然后用注射器吸10mL的品红溶液向试管注入品红溶液,观察实验现象,这说明什么? 实验探究4:用干燥的试管收集二氧化硫,用橡胶塞塞住,然后用注射器吸10mL的酸性高锰酸钾溶液向试管注入酸性高锰酸钾溶液,观察实验现象,这说明什么? 实验探究5:给实验探究3和实验探究4的试管加热,对比实验,认真观察实验现象;然后向其滴加酸性氯化钡溶液,观察实验现象,这又说明什么? 三、实验方法设计 教学目标的达成,需要适当的教学方法。本节课是实验教学课,所以以实验为主,通过 分组实验、活动探究、演示实验、对比探究、合作交流、讨论归纳相结合的教学方法。给学 生自己动手实验,让学生积极的思考,最后由学生自己来归纳总结。让学生在体会实验探究
常用危险化学品理化特性 乙酸 Acetic Acid 其它名称:中文:醋酸 英文: 国内危规编号:81601 UN编号:2789 包装分类:Ⅱ 包装标志:20 熔点(℃ :16.7 沸点(℃ :118.1 相对密度(水 =1 :1.05 相对密度(空气 =1 :2.07 稳定性:稳定聚合性:不聚合 爆炸上限(% :17.0 爆炸下限(% :4.0 分子式 :C 2 H 4 O 2 闪点(℃ :39 危险性类别:8.1类酸性腐蚀品污染类别:D 船型:3 舱型:2G 溶解性:溶于水、醚、甘油,不溶于二硫化碳
外观性状:无色透明液体,有刺激性酸味 灭火方法:雾状水、二氧化碳、抗溶性泡沫、干粉 危险特性:易燃,其蒸气与空气形成爆炸性混合物,遇明火、高热能引起爆炸, 与强氧化剂可发生反应。 应急措施:057 盐酸 Hydrochloric Acid 其它名称:中文:氢氯酸,盐镪水,焊锡药水 英文:chlorichydro Acid 国内危规编号:81013 UN编号:1789 包装分类:Ⅰ 包装标志:20 熔点(℃ :-114.8(纯洁沸点(℃ :108.6(20% 相对密度(水 =1 :1.20 相对密度(空气 =1 :1.26 稳定性:稳定聚合性:不聚合 爆炸上限(% :无意义爆炸下限(% :无意义 分子式 :HCl 闪点(℃ :无意义 危险性类别:8.1类酸性腐蚀品污染类别:D 船型:3 舱型:1G 溶解性:与水互溶 , 溶于碱液
外观性状:无色或微黄色发烟液体,有刺激的酸味 灭火方法:雾状水、砂土 危险特性:能与一些活性金属粉末发生反应,放出氢气。具有较强的腐蚀性,与大事发生中和反应,放出大量热。 应急措施:057 硫酸 Sulfuric Acid 其它名称:中文: 英文: 国内危规编号:81007 UN编号:1830 包装分类:I 包装标志:20 熔点(℃ :10.5 沸点(℃ :330.0 相对密度(水 =1 :1.83 相对密度(空气 =1 :3.4 稳定性:稳定聚合性:不聚合 爆炸上限(% :无意义爆炸下限(% :无意义 分子式 :HSO 4 闪点(℃ :无意义 危险性类别:8.1类酸性腐蚀品污染类别:C
( 安全管理 ) 单位:_________________________ 姓名:_________________________ 日期:_________________________ 精品文档 / Word文档 / 文字可改 危险化学品理化性质与装卸安 全控制(2021新版) Safety management is an important part of production management. Safety and production are in the implementation process
危险化学品理化性质与装卸安全控制 (2021新版) 港口装卸的危险化学品品种繁多,其中大部分为甲、乙类火灾危险物质,普遍具有易燃、易爆、有毒和易挥发等特点,掌握货物的理化性质与港口装卸生产安全控制有着十分密切的关系。要想在生产、装卸、交付、搬运、储藏过程中确保生产安全,需全面掌握该货物的理化特性、燃爆特性、危险特性、泄漏处置、健康危害、人身防护等知识。从货物自身的理化性质有针对性地选择出科学的装卸工艺,严格遵守工艺规程,全面分析生产的环节注意事项,做好科学的安全控制,才能保证人身安全、货物安全、设备安全、环境安全,为港口危险化学品装卸生产安全提供可靠的安全保证。 一、健康危害 危险化学品货物大多数有毒害性,易对人身体产生健康伤害。
其主要侵入途径有吸入、食入和经皮肤吸收。为保护工作人员身体健康,接触或进入有毒害性货物的生产现场、灌装车间、储藏库房等。需要做以下工作都必须执行严禁吸烟、进食、饮水。进入有限空间或高浓度作业区需有人监护。根据货物不同的特性,选用不同级别的防护用品。 1.呼吸系统 对呼吸系统的防护可以采用隔离式呼吸器,过滤式呼吸器等。 2.眼睛防护 对眼睛的防护设备主要有化学安全防护眼镜,安全防护面罩、安全防护眼镜、安全护目镜等。 3.身体防护 对身体的防护设备主要有:带面罩式胶布防毒衣、连衣式胶布防毒衣、橡胶工作服、防毒物渗透工作服、透气型防毒服、耐酸碱工作服、防静电工作服。 4.手和脚防护 对手防护设备主要有:橡胶手套、乳胶手套、耐酸碱手套、防
目录 8.1类酸性腐蚀品 发烟硝酸的理化性质和危险特性(表-) (1) 硝酸的理化性质及危险特性(表-) (2) 发烟硫酸的理化性质及危险特性(表-) (3) 硫酸的理化性质及危险特性(表-) (4) 亚硫酸的理化性质和危险特性(表-) (5) 盐酸的理化性质及危险特性(表-) (6) 氢氟酸的理化性质及危险特性(表-) (7) 氢溴酸的理化性质和危险特性(表-) (8) 溴水的理化性质及危险特性(表-) (9) 氟硅酸的理化性质及危险特性(表-) (10) 氟硼酸的理化性质及危险特性(表-) (11) 氯化亚砜的理化性质和危险特性(表-) (12) 三氯化铝的理化性质及危险特性(表-) (13) 三氯化锑的理化性质和危险特性(表-) (14) 四氯化钛的理化性质和危险特性(表-) (15) 五氧化(二)磷的理化性质和危险特性(表-) (16) 甲酸的理化性质及危险特性(表-) (17) 三氟乙酸的理化性质和危险特性(表-) (18) 苯酚磺酸的理化性质及危险特性(表-) (19) 苯甲酰氯的理化性质及危险特性(表-) (20)
正磷酸的理化性质及危险特性(表-) (22) 亚磷酸的理化性质和危险特性(表-) (23) 多聚磷酸的理化性质和危险特性(表-) (24) 氨基磺酸的理化性质及危险特性(表-) (25) 氯铂酸的理化性质和危险特性(表-) (26) 硫酸羟胺的理化性质和危险特性(表-) (27) 硫酸氢钾的理化性质和危险特性(表-) (28) 亚硫酸氢钠的理化性质和危险特性(表-) (29) 三氯化铝溶液的理化性质及危险特性(表-) (30) 硫酸镁的理化性质及危险特性(表-) (31) 三氯化铁的理化性质及危险特性(表-) (32) 三氯化铁溶液的理化性质及危险特性(表-) (33) 三氯化碘的理化性质和危险特性(表-) (34) 乙酸的理化性质及危险特性(表-) (35) 乙酸溶液的理化性质及危险特性(表-) (36) 醋酐的理化性质及危险特性(表-) (37) 三氯乙酸的理化性质及危险特性(表-) (38) 丙烯酸的理化性质及危险特性(表-) (39) 甲基丙烯酸的理化性质及危险特性(表-) (40) 丁酸的理化性质和危险特性(表-) (41) 丁烯二酸酐的理化性质及危险特性(表-) (42)
二氧化硫的性质和作用 一、教学目标 [知识目标]了解二氧化硫的物理性质;了解可逆反应的概念 掌握二氧化硫的化学性质 [能力目标]能够熟练运用比较法、实验探究法自主学习新知识; [情感目标]通过本节课的学习,培养学生科学研究的态度,认真仔细,实事求是的作风,增强环保意识。 二、教学重点、难点 [教学重点]二氧化硫的化学性质 [教学难点]研究某物质的程序和方法 [教学过程设计] [引入]多媒体展示:有关酸雨污染的图片,引出形成酸雨的首要物质-二氧化硫。投影给出本节课的学习目标和重难点。 [实验探究] 学生:每四人成一个小组进行探究实验,老师事先制好二氧化硫气体,每组分一试管,学生按学案所示步骤进行实验,记录实验现象,并讨论其中显示的二氧化硫的有关性质。学案中有关探究内容如下:
教师:将学生分成若干小组,让其按学案进行实验,同时巡视,指出个别同学操作中出现的一些不当之处,如闻气味的方法,加热试管中液体的方法,滴加溶液的方法等。 [交流汇报] 教师:在不同组中各挑一个学生汇报实验现象以及讨论所得的结论,然后让其他组进行补充。 学生:分小组实验时按小组讨论实验中体现的二氧化硫的性质,并记录在学案上。 生1:有刺激性气味,无色 生2:试管中水面上升,说明二氧化硫能溶于水 生3:水溶液呈酸性,说明二氧化硫可与水反应,生成酸。 生4:….. [探究结论] 师生共同总结二氧化硫的物理性质和化学性质 首先,按照学生观察到的和书上介绍的可知二氧化硫的物理性质,投影:一种无色,有刺激性气味,有毒,比空气重,容易液化,易溶于
水的气体。 其次,讨论二氧化硫作为酸性氧化物的性质时,运用类推和比较的学习方法,通过与二氧化碳的对比,投影: 在投影表格中给出CO2的有关方程式,由学生写出SO2的方程式,进一步得出二氧化硫的吸收方法,可以有浓的碱溶液或生石灰吸收;同时由两者与水的反应了解什么是可逆反应,指的是同时同条件下即可以向正反应方向进行又可以向逆方向进行的反应。 再次,讨论二氧化硫的氧化性和还原性时,从化合价的角度引导学生进行分析,投影: 投影打出二氧化硫、氯水、氧气反应的部分方程式,引导学生利用氧化还原反应的原理,分析这三个反应中二氧化硫体现的性质并补全方程式,推测出其使高锰酸钾褪色的原理是还原性,得出二氧化硫的一种检验方法。 最后,讨论二氧化硫的漂白性,强调原理和效果,由学生回忆已经学过的氯水的漂白性,进行对比后给出二氧化硫的漂白性:程度为暂时
( 安全技术 ) 单位:_________________________ 姓名:_________________________ 日期:_________________________ 精品文档 / Word文档 / 文字可改 危险化学品理化性质及应急措 施(新版) Technical safety means that the pursuit of technology should also include ensuring that people make mistakes
危险化学品理化性质及应急措施(新版) (1)苯:别名纯苯、净苯、氢化苯。 1)性质及用途 理化性质:无色透明液体,有强烈芳香味,不溶于水,溶于醇、醚、丙酮等多数有机溶剂,易燃液体。 一般包装:易燃液体,小开口钢桶。 稳定性和危险性:易燃,蒸汽能与空气形成爆炸性混合物,遇热或明火易着火、爆炸。蒸汽比空气重,可扩散到相当远距离。 毒理学指标:急性中毒伴有头痛、头晕、恶心、呕吐、轻度兴奋、步态蹒跚等状态,严重者可发生昏迷、抽搐、血压下降,以致呼吸和循环衰竭;慢性中毒主要表现有神经衰弱综合征,造血系统改变,白细胞、血小板减少,重者出现再生障碍性贫血,少数病例在慢性中毒后可发生白血病,皮肤脱脂、干燥、皲裂、皮炎。
主要用途:用作溶剂及合成苯的衍生物、香料、染料、塑料、医药、炸药、橡胶。 2)安全防护措施 工程控制:生产过程密闭,加强通风;提供安全淋浴和洗眼设备。 呼吸系统防护:空气中浓度超标时,应佩戴自吸过滤式防毒面罩。紧急事态抢救或撤离时,应该佩戴空气呼吸器或氧气呼吸器。 眼睛防护:佩戴化学安全防护眼镜。 身体防护:穿防毒物渗透工作服。 手防护:佩戴橡胶手套。 其它:工作现场禁止吸烟、进食和饮水。工作完毕,淋浴更衣。 3)应急措施 急救措施:对于急性中毒者,应迅速将中毒患者移到新鲜空气处,立即脱去被苯污染的衣服,用肥皂水清洗污染处的皮肤,注意保暖。 泄露处置:迅速撤离污染区人员至安全区,切断火源,应急处
《二氧化硫的性质》教学设计 最后的伊甸园 课题:二氧化硫的性质 教材版本:人教版 教学目标: 一、知识与技能 1.使学生了解二氧化硫的物理性质。 2.使学生掌握二氧化硫的化学性质。 二、过程与方法 1.使学生通过对实验现象的观察以及操作,讨论探究出二氧化硫的物理性质和化学性质,培养学生的实验探究能力、团队协作能力和思维的逻辑性。 2. 使学生学会通过阅读资料等途径,培养“发现问题、解决问题”的自主学习和终身学习的意识和能力。 教学内容: 二氧化硫的物理性质,二氧化硫与水反应的性质以及漂白性两个化学性质。 教学重点、难点: 重点:二氧化硫与水反应 难点:可逆反应 教学过程: 一、导入课题(1min)——第一张ppt (教师板书,写在主板书的位置:二氧化硫的性质) 教师:好,同学们!我们来继续上节课的学习,二氧化硫的性质。上节课同学们已经到实验室做了二氧化硫溶于水以及其使品红褪色的实验,下面我们来看一张图片(教师点击ppt)。 教师提问:本来是一朵红色漂亮的花为什么放到瓶子里之后突然就变成了白色的呢?是电视上我们看到的魔术吗? 学生发言:…… 教师:相信同学通过上节课的实验以及课后老师叫你们回去小组讨论实验现象之后,大家都应该知道为什么了吧?好,这节课我们就来探究二氧化硫这个能使红花变白花的神秘物质的物理性质和化学性质吧! 二、回顾实验,归纳性质 教师:现在我们来回顾一下上节课我们做的实验吧!课后大家也回去交流讨论了,
那么大家现在来说说二氧化硫到底有哪些物理和化学性质呢?大家把自己记录到的实验现象拿出来分享一下吧! 学生发言:…… (教师板书,写在副板书的位置,分类写下同学们所说的二氧化硫的物理性质和化学性质) 教师:好,那我们接下来进入二氧化硫物理性质的学习,看看同学们总结分析的实验现象对不对? 三、二氧化硫的物理性质(2min)——第二张ppt 教师:二氧化硫的物理性质有哪些呢?颜色?状态?气味?密度?毒性?还有一个很重要的性质,水溶性? (教师与学生共同讨论完成,教师一边点击ppt,一边让同学们插话说出二氧化硫的物理性质) (教师板书,写在主板书的位置:一、物理性质) 四、二氧化硫的物理性质——水溶性(2min)——第三张ppt (教师板书,写在主板书的位置:水溶性) 教师:现在我们来探究二氧化硫的水溶性。大家都还记得我们上节课怎么做这个实验了吧?将集满二氧化硫的试管倒扣在水中振荡。实验现象怎么样啦?哪位同学来说一下自己做到的实验现象啊? 学生回答:试管的液面上升。 (若该学生没有回答正确,继续叫下一个学生) 教师:很好,那么为什么试管液面会上升呢?大家有没有回去查阅资料啊?下面我们找个小组代表来说一下。 学生回答:(回答出大概意思) 教师:分析得很好,我们物理上也学习过大气压了,这对同学们来说应该不是很困难吧!这是由于SO2溶于水导致试管内气压减小,大气压把水压入试管中了。从这一步的实验当中我们知道了二氧化硫的水溶性怎么样了吧? 学生发言:二氧化硫溶于水 五、二氧化硫的化学性质——与水反应(4min)——第四张ppt(重点、难点)(教师板书,写在主板书的位置:二、化学性质 1.与水反应) 教师:但是SO2溶于水真的仅仅只是溶解吗?有没有发生化学反应啊?大家在接下来的实验当中发现了什么啊?(学生插话)我们来看看第二步的实验,用pH试纸测SO2水溶液的pH。大家做出来的现象怎么样啊? 学生发言:试纸变成了红色 教师提问:那么我们回忆一下初中所学过的知识,什么物质会使PH试纸变成红色啊? 学生发言:酸性物质 教师提问:那就是说SO2和H2O反应生成了酸性物质,导致试纸变红色了?这种酸性物质是什么呢?大家还记得以前学习CO2的知识吧,那么CO2与H2O反应生成什么啊?(学生插话回答,教师板书)。好,既然大家都知道CO2与H2O反应的方程式怎么写了。那么我们就根据类比的方法,写出SO2和H2O反应的方程式,哪位同学上来写一下啊?