
第2讲燃烧和灭火实验
【核心重点】
一、燃烧的条件(同时符合)二、灭火的原理(符合其一)(1)可燃物(1)清除可燃物
(2)与氧气(或空气)接触(2)隔绝氧气(或空气)
(3)达到燃烧所需的最低温度(也叫着火点)(3)降温至着火点以下
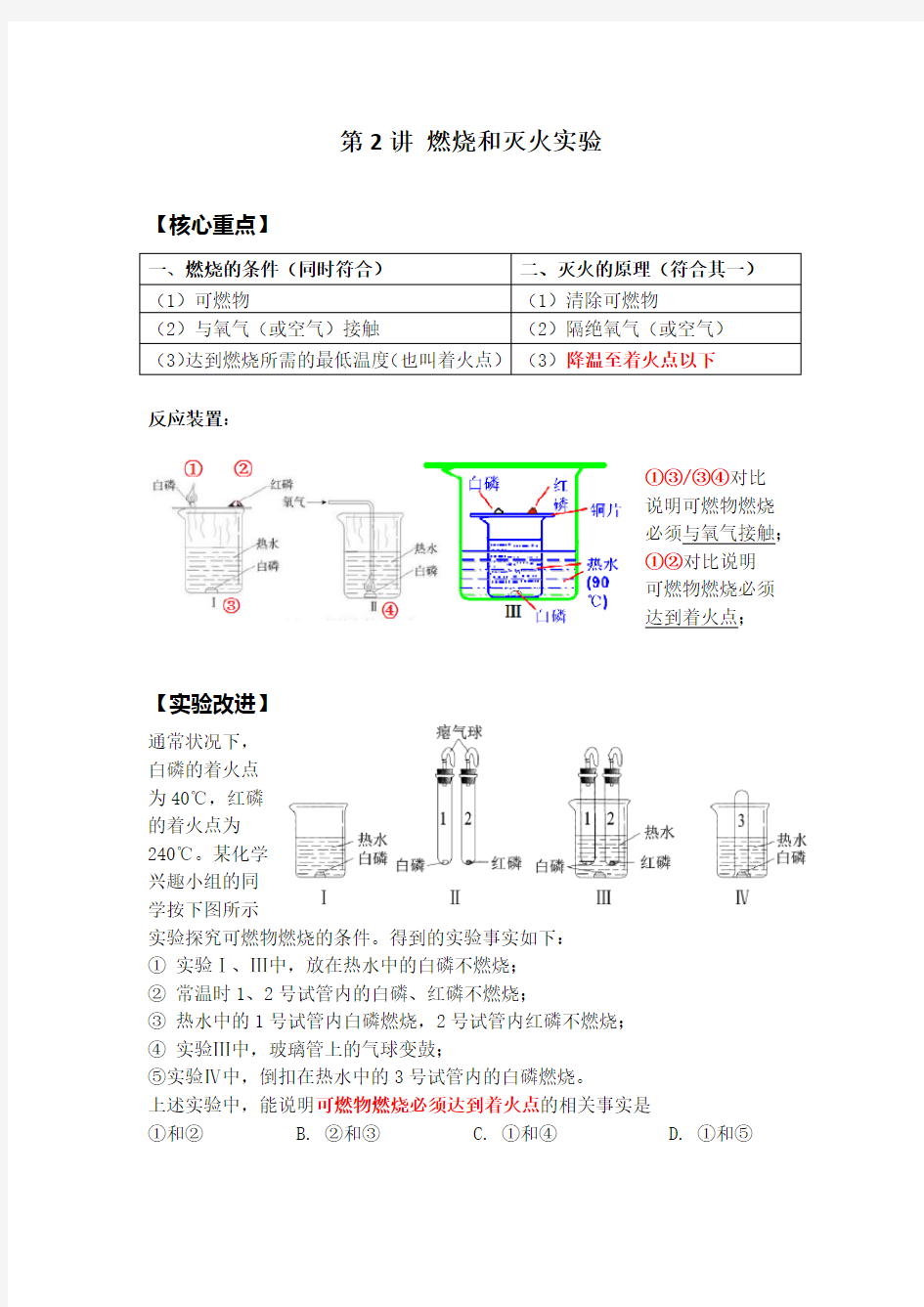
反应装置:
①③/③④对比
说明可燃物燃烧
必须与氧气接触;
①②对比说明
可燃物燃烧必须
达到着火点;
【实验改进】
通常状况下,
白磷的着火点
为40℃,红磷
的着火点为
240℃。某化学
兴趣小组的同
学按下图所示
实验探究可燃物燃烧的条件。得到的实验事实如下:
①实验Ⅰ、Ⅲ中,放在热水中的白磷不燃烧;
②常温时1、2号试管内的白磷、红磷不燃烧;
③热水中的1号试管内白磷燃烧,2号试管内红磷不燃烧;
④实验Ⅲ中,玻璃管上的气球变鼓;
⑤实验Ⅳ中,倒扣在热水中的3号试管内的白磷燃烧。
上述实验中,能说明可燃物燃烧必须达到着火点的相关事实是
①和② B. ②和③ C. ①和④ D. ①和⑤
【答案】B
【考查难点】
【实例训练】
某化学兴趣小组的同学利用如下图所示装置(固定装置已略去)探究燃烧等相关实验。已知,白磷(过量)的着火点40℃;该装置气密性良好,瓶内空气体积为230mL ,注射器中水的体积为50mL ,且生石灰适量。 实验步骤及部分现象记录如下表。请回答下列问题。 ⑴ 步骤Ⅰ中,导致小蜡烛熄灭的原因是 。 ⑵ 步骤Ⅱ中,可观察到气球的变化是 ;白磷燃烧的原因是 ;白磷燃烧的化学方程式为 。 ⑶ 在步骤Ⅲ中,该兴趣小组的同学继续实验,测定空气中氧气的含量。具体操作是:待白磷熄灭并冷却后,_______________,观察到_________________现象。
【答案】(1)生成CO 2受热上升,隔绝O 2 ;
(2)先变鼓,后变瘪;生石灰与水反应放热,使温度升高达到白磷着火点,并与O 2接触;4P+5O 2点燃 2P 2O 5
(3)打开弹簧夹;注射器中的水自动喷出来,还剩下约4mL 时停止下流。
实验现象
原因
Ⅰ 高蜡烛先熄灭 生成CO 2受热上升,隔绝O 2 Ⅱ 矮蜡烛先熄灭 CO 2密度大于空气,隔绝O 2
实验步骤 操作 现象 步骤Ⅰ 点燃燃烧匙中的小蜡烛后,立即伸入集气瓶中并塞紧塞子。 燃着的小蜡烛很快就熄灭了。 步骤Ⅱ 打开弹簧夹,由注射器向集气瓶中加入少量水,夹紧弹簧夹。
白磷燃烧。 步骤Ⅲ
…
…