
一、检测蛋白质与蛋白质相互作用
①技术()
,,即荧光共振能量转移技术。该技术的原理是用一种波长的光激发某种荧光蛋白后,它释放的荧光刚好又能激发另一种荧光蛋白,使其释放另一波长的荧光,如下图所示:
以下图为例,若要利用检测两种蛋白是否有相互作用,需将两种蛋白的基因分别与这两种荧光蛋白的基因融合,并在细胞内表达出两种融合蛋白。然后只需用紫外光对进行激发,并检测是否放出绿色荧光。如果能检测到绿色荧光,那么可以说明这两种蛋白可能有相互作用;反之,则是这两种蛋白没有相互作用。
②酵母双、三杂交技术()
酵母双杂交系统主要用于考察两种蛋白是否有相互作用,其原理是典型的真核生长转录因子,如4、4等都含有二个不同的结构域,即和。这些转录因子只有同时具有这两个结构域时才能起始转录。由此,设计不同的两个载体,一个含有基因(假设为A载体),另一个含有基因(假设为B载体)。
一般将一个已知蛋白的基因连在B载体上,作为诱饵(),将未知蛋白的基因连在A载体上,将这两个载体都转到特定的酵母细胞内,看未知蛋白与已知蛋白是否有相互作用。如果两者有相互作用,那么就可以启动报告基因的转录,从而使这个酵母细胞能在选择培养基上显现出来或者生存下来;如果两者无相互作用,那么报告基因就无法表达,那么这个酵母细胞就无法在择培养基上显现出来或者生存下来,如下图所示:
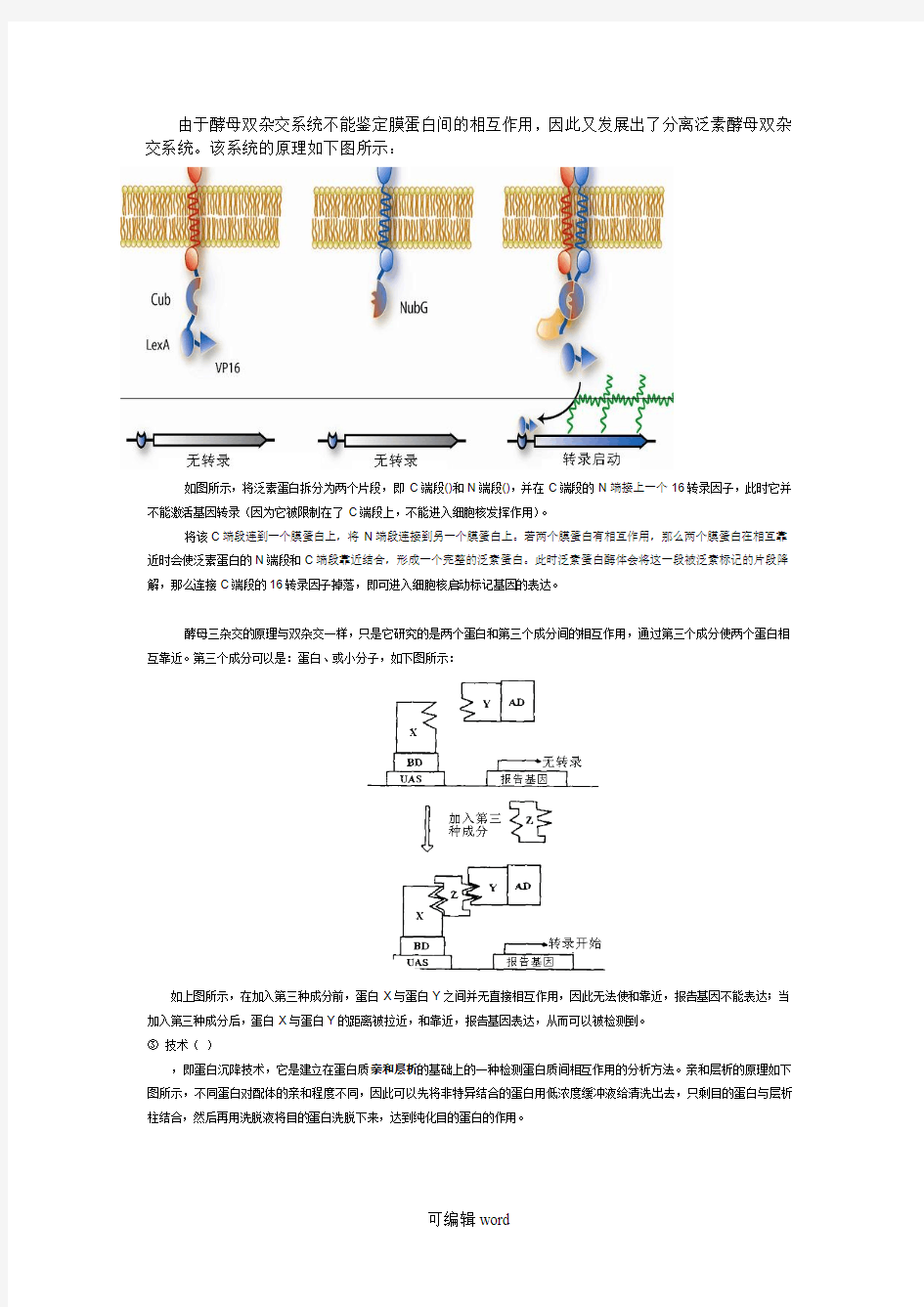
由于酵母双杂交系统不能鉴定膜蛋白间的相互作用,因此又发展出了分离泛素酵母双杂交系统。该系统的原理如下图所示:
如图所示,将泛素蛋白拆分为两个片段,即C端段()和N端段(),并在C端段的N端接上一个16转录因子,此时它并不能激活基因转录(因为它被限制在了C端段上,不能进入细胞核发挥作用)。
将该C端段连到一个膜蛋白上,将N端段连接到另一个膜蛋白上。若两个膜蛋白有相互作用,那么两个膜蛋白在相互靠近时会使泛素蛋白的N端段和C端段靠近结合,形成一个完整的泛素蛋白。此时泛素蛋白酶体会将这一段被泛素标记的片段降解,那么连接C端段的16转录因子掉落,即可进入细胞核启动标记基因的表达。
酵母三杂交的原理与双杂交一样,只是它研究的是两个蛋白和第三个成分间的相互作用,通过第三个成分使两个蛋白相互靠近。第三个成分可以是:蛋白、或小分子,如下图所示:
如上图所示,在加入第三种成分前,蛋白X与蛋白Y之间并无直接相互作用,因此无法使和靠近,报告基因不能表达;当加入第三种成分后,蛋白X与蛋白Y的距离被拉近,和靠近,报告基因表达,从而可以被检测到。
③技术()
,即蛋白沉降技术,它是建立在蛋白质亲和层析的基础上的一种检测蛋白质间相互作用的分析方法。亲和层析的原理如下图所示,不同蛋白对配体的亲和程度不同,因此可以先将非特异结合的蛋白用低浓度缓冲液给清洗出去,只剩目的蛋白与层析柱结合,然后再用洗脱液将目的蛋白洗脱下来,达到纯化目的蛋白的作用。
技术利用的是亲和层析技术以及特异的配体(如或者镍)。以下图为例,将的基因与蛋白X的基因融合,表达出融合蛋白。将该融合蛋白的溶液过带有配体的层析柱,那么这一融合蛋白就能结合在配体上,然后将待测蛋白的溶液过柱,并让其与融合蛋白反应一段时间。
接着开始进行洗脱。如果待测蛋白与蛋白X无相互作用,那么在开始清洗的时候就会被洗下来;如果在用洗脱液洗脱后才能在收集到的样品中发现待测蛋白(以及蛋白X),说明待测蛋白与蛋白X可能有相互作用。
④()
是基于发展而来,其原理如下图所示。将样品蛋白用非变性的胶分离,然后转膜、封闭、洗膜,加入待测蛋白,使其与已在膜上的样品蛋白进行相互作用。接着加入带有标记(如)的待测蛋白的抗体反应,最后进行显色(如加入的底物),观察实验结果。
⑤免疫共沉淀()()
免疫共沉淀是探测活体细胞内蛋白间的相互作用的一门技术。它的原理是当细胞在非变性条件下被裂解时,完整细胞内存在的许多蛋白质-蛋白质间的相互作用被保留了下来。如果用蛋白X的抗体免疫沉淀X,那么与X在体内有相互作用的蛋白Y也能沉淀下来。
的原理如下图所示,首先从细胞中提取蛋白质,获得蛋白提取液,并将其与抗体孵育,使抗体与蛋白X结合。将预处理过的G琼脂糖珠()加入到抗体与蛋白提取液的孵育液中反应,使抗体与G结合。通过离心将琼脂糖珠沉降到管底,去除上清液,然后再用缓冲液
将琼脂糖珠冲洗数次,最后用(或)进行检测。
二、检测蛋白质与相互作用
①()
的原理如下图所示。将的一个3’端用32p标记,然后将分成两份,一份直接用Ⅰ进行不完全酶切;另一份先与待测蛋白
混合反应一段时间,然后再用Ⅰ进行不完全酶切。然后将两份样品用变性的胶进行电泳,观察电泳结果。下图中,由于待测蛋
白与结合的部位无法被Ⅰ酶切降解,因此它的电泳结果中与直接用Ⅰ进行处理的样品相比,会缺少一段;如果待测蛋白与无相互作用,那么这两组的电泳结果应当一致。
②()
,,又称凝胶阻滞实验。其原理是与蛋白质结合的在胶(非变性胶)上比没有结合蛋白的移动速率要慢,因此通过电泳即可看到的变化,如下图所示。
③ a ()
该方法又成为原位筛选法,用于检测文库中的蛋白与探针之间的相互作用。其原理和实验流程如下图所示,首先是用噬菌体()侵染大肠杆菌,然后将这些大肠杆菌涂到平板上。接着进行转膜,将膜泡于水溶液中数小时,然后将该膜放于平板上,培养数小时(能诱导大肠杆菌表达文库蛋白)。将膜取出,进行变性、复性和封闭(过夜),然后与放射性标记的探针进行反应,最后洗膜、晾干并用胶片曝光。如果胶片上出现了条带,说明该文库蛋白与探针有相互作用;反之则说明两者无相互作用。
举世瞩目的基因组计划使大量的新基因不断被发现,然而单纯的基组DNA序列尚不能解答许多生命问题。基因是相对静态的,而基因编码的产物-蛋白质则是动态的,具有时空性和调节性,是生物功能的主要体现者和执行者。蛋白质的表达水平、存在方式以及相互作用等直接与生物功能相关。 在所有生命活动中,蛋白质之间的相互作用是必不可少的,它是细胞进行一切代谢活动的基础。细胞接受外源或是内源的信号,通过其特有的信号途径,调节其基因的表达,以保持其生物学特性。在这个过程中,蛋白质占有很重要的地位,它可以调控,介导细胞的许多生物学活性。 虽然有一些蛋白质可以以单体的形式发挥作用,但是大部分的蛋白质都是和伴侣分子一起作用或是与其他蛋白质形成复合物来发挥作用的。因此,为了更好地理解细胞的生物学活性,必须很好地理解蛋白质单体和复合物的功能,这就会涉及到蛋白质相互作用的研究。在现代分子生物学中,蛋白质相互作用的研究占有非常重要的地位。因此,揭示蛋白质之间的相互作用关系、建立相互作用关系的网络图,已成为蛋白质组学研究中的热点。 一、生物物理学方法 1. 融合蛋白pull-down实验 融合蛋白pull-down技术基本原理是将一种蛋白质固定于某种基质上(如Sepharose),当细胞抽提液经过该基质时,可与该固定蛋白相互作用的配体蛋白被吸附,而没有被吸附的“杂质”则随洗脱液流出。 被吸附的蛋白可以通过改变洗脱液或洗脱条件而回收下来。为了更有效地利用pull-down技术,可以将待纯化地蛋白以融合蛋白地形式表达,即将“诱饵”蛋白与一种易于纯化地配体蛋白相融合。1988年Smith等利用谷胱甘肽-S-转移酶(glutathione-S-transferase ,GST)融合标签从细菌中一步纯化出GST融合蛋白。从此GST融合蛋白在蛋白质相互作用研究领域里得到了极大的推广。 GST融合蛋白在经过固定有GST(glutathione)的色谱柱时,就可以通过GST与GSH的相互作用而被吸附。当再有细胞抽提物过柱,就可以得到能够与“诱饵”蛋白相互作用的兴趣蛋白。一般来说,GST融合蛋白pull-down方法用于两个方面:一是鉴定能与已知融合蛋白相互作用的未知蛋白质;二是鉴定两个已知蛋白质之间是否存在相互作用。 该方法比较简便,避免了使用同位素等危险物质,在蛋白质相互作用研究中有很广泛的应用。类似的融合蛋白很多,如与葡萄球菌蛋白A融合的“诱饵”蛋白可以通过固定有IgG的色谱柱进行纯化;与寡聚组氨酸肽段融合的“诱饵”蛋白可以通过结合Ni2+的色谱柱进行纯化;与二氢叶酸还原酶融合的“诱饵”蛋白可以通过固定有氨甲喋呤的色谱柱进行纯化等等。 2. 亲和印迹 亲和印迹是将聚丙烯酰胺凝胶电泳分离后的蛋白样品转移到硝酸纤维素膜上,然后检测哪种蛋白能与标记了的“诱饵”蛋白发生作用。此方法所要考虑的是如何保持膜上蛋白的生物活性,如何得到纯化的“诱饵”蛋白等。 3. 免疫共沉淀
检测两种蛋白质之间相互作用得实验方法比较 1、生化方法 ●免疫共沉淀免疫共沉淀就是以抗体与抗原之间得专一性作用为基础得用于研究蛋白质相互作用得经典方法.改法得优点就是蛋白处于天然状态,蛋白得相互作用可以在天然状态下进行,可以避免认为影响;可以分离得到天然状态下相互作用得蛋白复合体。缺点:免疫共沉淀同样不能保证沉淀得蛋白复合物时候为直接相互作用得两种蛋白。另外灵敏度不如亲与色谱高。 ●Far—Western 又叫做亲与印记。将PAGE胶上分离好得凡百样品转移到硝酸纤维膜上,然后检测哪种蛋白能与标记了同位素得诱饵蛋白发生作用,最后显影。缺点就是转膜前需要将蛋白复性。2?、等离子表面共振技术(Surfaceplasmonresonance)该技术就是将诱饵蛋白结合于葡聚糖表面,葡聚糖层固定于几十纳米厚得技术膜表面。当有蛋白质混合物经过时,如果有蛋白质同“诱饵”蛋白发生相互作用,那么两者得结合将使金属膜表面得折射率上升,从而导致共振角度得改变。而共振角度得改变与该处得蛋白质浓度成线性关系,由此可以检测蛋白质之间得相互作用。该技术不需要标记物与染料,安全灵敏快速,还可定量分析。缺点:需要专门得等离子表面共振检测仪器。 3、双杂交技术原理基于真核细胞转录因子得结构特殊性,这些转录因子通常需要两个或以上相互独立得结构域组成.分别使结合
域与激活域同诱饵蛋白与猎物蛋白形成融合蛋白,在真核细胞中表达,如果两种蛋白可以发生相互作用,则可使结合域与激活域在空间上充分接近,从而激活报告基因.缺点:自身有转录功能得蛋白会造成假阳性.融合蛋白会影响蛋白得真实结构与功能。不利于核外蛋白研究,会导致假隐性. 5、荧光共振能量转移技术指两个荧光法色基团在足够近(〈100埃)时,它们之间可发生能量转移得现象。荧光共振能量转移技术可以研究分子内部对某些刺激发生得构象变化,也能研究分子间得相互作用。它可以在活体中检测,非常灵敏,分辩率高,能够检测大分子得构象变化,能够定性定量得检测相互作用得强度。缺点此项技术要求发色基团得距离小于100埃。另外设备昂贵,还需要融合GFP给蛋白标记。?此外还有交联技术(cross-linKing),蛋白质探针技术,噬菌体展示技术(Phage display)以及生物信息学得方法来检测蛋白质之间相互作用。 1,酵母双杂交 1-5 酵母双杂交系统就是将待研究得两种蛋白质得基因分别克隆到酵 体,从表达产物分析两种蛋白质相互作用得系统 酵母双杂交得原理就是,把报告基因HIS3与l a c Z 整合到酵母细胞基因组中,并受转录因子
研究蛋白质与蛋白质相互作用方法总结-实验步骤 蛋白质与蛋白质之间相互作用构成了细胞生化反应网络的一个主要组成部分,蛋白-蛋白互作网络与转录调控网络对调控细胞及其信号有重要意义。把原来spaces空间上的一篇蛋白质与蛋白质间相互作用研究方法转来,算是实验技巧分类目录的首篇。(另补充2:检测两种蛋白质之间相互作用的实验方法比较) 一、酵母双杂交系统 酵母双杂交系统是当前广泛用于蛋白质相互作用组学研究的一种重要方法。其原理是当靶蛋白和诱饵蛋白特异结合后,诱饵蛋白结合于报道基因的启动子,启动报道基因在酵母细胞内的表达,如果检测到报道基因的表达产物,则说明两者之间有相互作用,反之则两者之间没有相互作用。将这种技术微量化、阵列化后则可用于大规模蛋白质之间相互作用的研究。在实际工作中,人们根据需要发展了单杂交系统、三杂交系统和反向杂交系统等。Angermayr等设计了一个SOS蛋白介导的双杂交系统。可以研究膜蛋白的功能,丰富了酵母双杂交系统的功能。此外,酵母双杂交系统的作用也已扩展至对蛋白质的鉴定。 二、噬茵体展示技术 在编码噬菌体外壳蛋白基因上连接一单克隆抗体的DNA序列,当噬菌体生长时,表面就表达出相应的单抗,再将噬菌体过柱,柱上若含目的蛋白,就会与相应抗体特异性结合,这被称为噬菌体展示技术。此技术也主要用于研究蛋白质之间的相互作用,不仅有高通量及简便的特点,还具有直接得到基因、高选择性的筛选复杂混合物、在筛选过程中通过适当改变条件可以直接评价相互结合的特异性等优点。目前,用优化的噬菌体展示技术,已经展示了人和鼠的两种特殊细胞系的cDNA文库,并分离出了人上皮生长因子信号传导途径中的信号分子。 三、等离子共振技术 表面等离子共振技术(Surface Plasmon Resonance,SPR)已成为蛋白质相互作用研究中的新手段。它的原理是利用一种纳米级的薄膜吸附上“诱饵蛋白”,当待测蛋白与诱饵蛋白结合后,薄膜的共振性质会发生改变,通过检测便可知这两种蛋白的结合情况。SPR技术的优点是不需标记物或染料,反应过程可实时监控。测定快速且安全,还可用于检测蛋白一核酸及其它生物大分子之间的相互作用。
《检测生物组织中的糖类》的教学设计 阳春市第一中学何方炎 一、教材分析: 1、教材的地位和作用 新教材把实验安排在学习蛋白质、糖类和脂质等知识内容之前,一方面为接下来的学习各类有机物奠定感性认识基础,另一方面,由于实验内容的设置上注重学生对材料的选择,对检测结果的预期和实验方案的设计,因此有利于培养了学生的实验探究的能力,为以后各章节的探究性实验的顺利开展搭建了一个较高的起点。 2、教学目标 (1)知识: ①尝试用化学试剂检测生物组织中的糖类。 ②推断组织液中有机物的种类和大致含量 (2)能力: ①学习实验探究的方法 ②初步掌握评价和报告实验结果的能力 (3)情感态度价值观:严谨认真合作学习敢于质疑善于反思 3、教学重点难点 重点:检测生物组织中的糖类的原理和方法。 难点:实验所用材料多,试剂种类和使用方法多,课堂容量大。 突破:面对全体学生,做好充分的准备:材料仪器准备,学生的情感和知识准备。课堂上发挥小组长的协助管理作用,合理有序地组织教学。 二、学情分析 1、学生的思维水平、学习能力已经发展到较高阶段,乐于并有能力接受自主探究的学习模式。 2、感兴趣,有实验操作的基础。 3、材料试剂多,任务繁重,合作学习显得尤为重要。 三、教法学法 1、学法:任务驱动,自主探究合作学习,分享交流。 2、教法:组织者,引导者,注意生成性问题的再探究。 四、教学过程 1、实验动员,知识准备 教师:介绍有关实验原理和检测方法(见板书) 学生:讨论交流,合作学习(讨论题见板书) 2、创设情景,任务驱动 提供一种水果组织(苹果),学生自带一样自己感兴趣的组织进行检测。
假设每个同学是一个营养师或检验员……如何准确检测出组织液各含哪种物质? 你要选择哪些实验器材和试剂? 3、作出预测设计实验 (1)先预测,再检测。 (2)设计记录表格,记录预测和实测结果。 4、分组探究,自主学习 小组长:组织分工,材料仪器的分配和管理。 组员:对提供的一种组织液和自带的组织用相应试剂进行检测。根据特定的颜色反应尝试分析其中有机物的种类,比较各种有机物的含量。 注意生成性问题的再探究(再探究课题见板书) 教师:不直接解疑,鼓励设计实验进行再探究 5、成果交流,评价反思 实验反思:预测与实测相符? 小组间的异同? 存在问题? 教师公布答案,并作出恰当的评价: (1)实验纪录表格的设计、实验结果和推论 (2)自主学习和合作能力 (3)创新思维和能力 6、拓展延伸,学以致用 讨论: 今天检测的生物材料中有机物的种类,含量一样吗?对你选择食物有什么启发? 依据课程的基本理念,注重与现实生活的联系,学以致用。 五、教学反思 1、以“自主性、探究性、合作性、完整性”为课堂教学的四个基本维度,以培养学生的科学素养为指导,侧重科学方法教育。 2、注重培养自疑自析的能力,“教为了不教”。 3、发挥小组长的协助作用。 4、试剂用量的差异,影响对实验结果的推断。 5、探究、创新能力的培养与课时的安排矛盾。 板书设计: 检测生物组织中的糖类 一、实验原理()+()()
一、检测蛋白质与蛋白质相互作用 ①FRET技术(in vivo) FRET,Fluorescence resonanceenergy transfer,即荧光共振能量转移技术。该技术得原理就是用一种波长得光激发某种荧光蛋白后,它释放得荧光刚好又能激发另一种荧光蛋白,使其释放另一波长得荧光,如下图所示: 以下图为例,若要利用FRET检测两种蛋白就是否有相互作用,需将两种蛋白得基因分别与这两种荧光蛋白得基因融合,并在细胞内表达出两种融合蛋白。然后只需用紫外光对CFP进行激发,并检测GFP就是否放出绿色荧光.如果能检测到绿色荧光,那么可以说明这两种蛋白可能有相互作用;反之,则就是这两种蛋白没有相互作用。 ②酵母双、三杂交技术(in vivo) 酵母双杂交系统主要用于考察两种蛋白就是否有相互作用,其原理就是典型得真核生长转录因子,如GAL4、GCN4等都含有二个不同得结构域,即AD与BD.这些转录因子只有同时具有这两个结构域时才能起始转录.由此,设计不同得两个载体,一个含有AD基因(假设为A载体),另一个含有BD基因(假设为B载体)。 一般将一个已知蛋白得基因连在B载体上,作为诱饵(Bait),将未知蛋白得基因连在A载体上,将这两个载体都转到特定得酵母细胞内,瞧未知蛋白与已知蛋白就是否有相互作用.如果两者有相互作用,那么就可以启动报告基因得转录,从而使这个酵母细胞能在选择培养基上显现出来或者生存下来;如果两者无相互作用,那么报告基因就无法表达,那么这个酵母细胞就无法在择培养基上显现出来或者生存下来,如下图所示:
由于酵母双杂交系统不能鉴定膜蛋白间得相互作用,因此又发展出了分离泛素酵母双杂交系统。该系统得原理如下图所示: 如图所示,将泛素蛋白拆分为两个片段,即C端段(Cub)与N端段(NubG),并在C端段得N端接上一个LexA—VP16转录因子,此时它并不能激活基因转录(因为它被限制在了C端段上,不能进入细胞核发挥作用)。 将该C端段连到一个膜蛋白上,将N端段连接到另一个膜蛋白上。若两个膜蛋白有相互作用,那么两个膜蛋白在相互靠近时会使泛素蛋白得N端段与C端段靠近结合,形成一个完整得泛素蛋白。此时泛素蛋白酶体会将这一段被泛素标记得片段降解,那么连接C端段得LexA-VP16转录因子掉落,即可进入细胞核启动标记基因得表达。 酵母三杂交得原理与双杂交一样,只就是它研究得就是两个蛋白与第三个成分间得相互作用,通过第三个成分使两个蛋白相互靠近。第三个成分可以就是:蛋白、RNA或小分子,如下图所示: 如上图所示,在加入第三种成分前,蛋白X与蛋白Y之间并无直接相互作用,因此无法使BD与AD靠近,报告基因不能表达;当加入第三种成分后,蛋白X与蛋白Y得距离被拉近,BD与AD靠近,报告基因表达,从而可以被检测到。 ③ Pulldown技术(invitro) Pulldown,即蛋白沉降技术,它就是建立在蛋白质亲与层析得基础上得一种检测蛋白质间相互作用得分析方法.亲与层析得原理如下图所示,不同蛋白对配体得亲与程度不同,因此可以先将非特异结合得蛋白用低浓度缓冲液给清洗出去,只剩目得蛋白与层析柱结合,然后再用洗脱液将目得蛋白洗脱下来,达到纯化目得蛋白得作用。
检测两种蛋白质之间相互作用的实验方法比较 1. 生化方法 ●免疫共沉淀免疫共沉淀是以抗体和抗原之间的专一性作用为基础的用于研究蛋白质相互作用的经典方法。改法的优点是蛋白处于天然状态,蛋白的相互作用可以在天然状态下进行,可以避免认为影响;可以分离得到天然状态下相互作用的蛋白复合体。缺点:免疫共沉淀同样不能保证沉淀的蛋白复合物时候为直接相互作用的两种蛋白。另外灵敏度不如亲和色谱高。 ●Far-Western 又叫做亲和印记。将PAGE胶上分离好的凡百样品转移到硝酸纤维膜上,然后检测哪种蛋白能与标记了同位素的诱饵蛋白发生作用,最后显影。缺点是转膜前需要将蛋白复性。 2. 等离子表面共振技术(Surface plasmon resonance)该技术是将诱饵蛋白结合于葡聚糖表面,葡聚糖层固定于几十纳米厚的技术膜表面。当有蛋白质混合物经过时,如果有蛋白质同“诱饵”蛋白发生相互作用,那么两者的结合将使金属膜表面的折射率上升,从而导致共振角度的改变。而共振角度的改变与该处的蛋白质浓度成线性关系,由此可以检测蛋白质之间的相互作用。该技术不需要标记物和染料,安全灵敏快速,还可定量分析。缺点:需要专门的等离子表面共振检测仪器。 3. 双杂交技术原理基于真核细胞转录因子的结构特殊性,这些转录因子通常需要两个或以上相互独立的结构域组成。分别使结合域和
激活域同诱饵蛋白和猎物蛋白形成融合蛋白,在真核细胞中表达,如果两种蛋白可以发生相互作用,则可使结合域和激活域在空间上充分接近,从而激活报告基因。缺点:自身有转录功能的蛋白会造成假阳性。融合蛋白会影响蛋白的真实结构和功能。不利于核外蛋白研究,会导致假隐性。 5. 荧光共振能量转移技术指两个荧光法色基团在足够近(<100埃)时,它们之间可发生能量转移的现象。荧光共振能量转移技术可以研究分子内部对某些刺激发生的构象变化,也能研究分子间的相互作用。它可以在活体中检测,非常灵敏,分辩率高,能够检测大分子的构象变化,能够定性定量的检测相互作用的强度。缺点此项技术要求发色基团的距离小于100埃。另外设备昂贵,还需要融合GFP给蛋白标记。 此外还有交联技术(cross-linKing),蛋白质探针技术,噬菌体展示技术(Phage display)以及生物信息学的方法来检测蛋白质之间相互作用。 1,酵母双杂交 1-5 酵母双杂交系统是将待研究的两种蛋白质的基因分别克隆到酵母表达质粒的转录激活因子(如GAL4等)的DNA结合结构域基因和转录激活因子(如GAL4等)激活结构域基因,构建成融合表达载体,从表达产物分析两种蛋白质相互作用的系统
DNA-蛋白质相互作用的研究方法2008-02-21 12:21一、凝胶阻滞试验 1.试验原理 又叫作DNA迁移率变动试验(DNA mobility shift assay),在凝胶电泳中,由于电场的作用,裸露的DNA朝正电极移动的距离与其分子量的对数成反比。如果此时DNA分子与某种蛋白质结合,那么,由于分子量增大,它在凝胶中的迁移作用便会受到阻滞,在特定电压和时间内朝正电极移动的距离也就相应缩短了。 2.主要步骤及内容 首先是用放射性同位素标记待检测的DNA片段(亦称探针DNA),然后同细胞蛋白质提取物一道温育,于是便有可能形成DNA-蛋白质复合物。将它加样到非变性的聚丙烯酰胺凝胶中,在控制使蛋白质仍与DNA保持结合状态的条件下进行电泳分离。应用放射自显影技术显现具放射性标记的DNA条带位置。如果细胞蛋白质提取物中不存在可同放射性标记的探针DNA结合的蛋白质,那么所有放射性标记都将集中出现在凝胶的底部,反之,将会形成DNA-蛋白质复合物,由于凝胶阻滞的缘故,其特有的放射性标记的探针DNA条带就将滞后出现在较靠近凝胶顶部的位置。 凝胶阻滞试验不仅可以用来鉴定在特殊类型细胞的提取物中,是否存在着能够同某一特定DNA片段结合的蛋白质分子(比如特异的转录因子等),而且还可以用来研究发生此种结合作用之精确的DNA序列的特异性。 其办法是在DNA-蛋白质结合反应体系中,加入超量的非标记的竞争DNA(competitor DNA)。如果它与同位素标记的探针DNA结合的是同一种蛋白质,那么由于竞争DNA与探针DNA 相比是极大超量的,这样绝大部分蛋白质都会被其竞争结合掉而使探针DNA仍处于自由的状态,所以在电泳凝胶的放射自显影图片上就不会出现阻滞的条带。相反地,如果反应中加入的竞争DNA并不能够同探针DNA竞争结合同一种蛋白质,于是探针DNA便仍然与特定蛋白质结合形成复合物,结果在电泳凝胶的放射自显影图片上就会呈现阻滞的条带。 在凝胶阻滞试验中使用竞争DNA,可以间接地阐明在体内发生的DNA与蛋白质之间的相互作用。例如,使用一种具有已知转录因子结合位点的竞争DNA,我们就可以判断通过特定的凝胶阻滞试验所检测到的蛋白质,是否就是属于此类转录因子,抑或是与之相关的其它因子。同样地,假如我们在竞争DNA上已知的转录因子结合位点处,事先引入一个或少数几个碱基突变,通过凝胶阻滞试验亦可有效地评估出这些突变对竞争DNA的性能及其与转录因子结合作用的影响。 二、DNaseI足迹试验(DNaseI footFIrinting assay) DNaseI足迹试验是一种测定DNA结合蛋白在DNA上的准确结合位点的技术。 首先是对包含一定顺式作用元件的双链DNA进行单链标记,然后用DNaseI水解单链标记的双链DNA,产生不同长度的片断,DNA结合蛋白与其特异序列结合处由于空间位阻,DNaseI对这部分DNA不能切割,即被DNaseI保护。DNaseI水解产物经尿素变性,PAGE 分离及放射性显影后,形成以相差一个核苷酸为梯度的一系列DNA条带,在此显影图中相
《检测生物组织中还原糖、脂肪和蛋白质》教案 一、实验原理 (1)鉴定实验设计的理念: 某些化学试剂 + 生物组织中有关有机化合物产生特定的颜色反应。 (2)具体原理: ①可溶性还原糖+ 斐林试剂→砖红色沉淀。 ②脂肪小颗粒 + 苏丹Ⅲ染液→橘黄色小颗粒。 ③蛋白质 + 双缩脲试剂→紫色反应。 二、目标要求 初步掌握鉴定生物组织中可溶性还原糖、脂肪、蛋白质的基本方法。 三、重点、难点 1.重点 ①初步掌握鉴定生物组织中可溶性还原糖、脂肪、蛋白质的基本方法。 ②通过实验的操作和设计培养学生的动手能力,掌握探索实验设计技巧,从而培养创新思维能力。 2.难点 根据此实验方法、原理,设计实验来鉴定常见食物的成分。 四、实验材料 1.可溶性还原糖的鉴定实验:选择含糖量较高、颜色为白色或近白色的植物组织,以苹果、梨为最好。 2.脂肪的鉴定实验:选择富含脂肪的种子,以花生种子为最好(实验前浸泡3h~4h)。 3.蛋白质的鉴定实验:可用浸泡1d~2d的黄豆种子(或用豆浆、或用鸡蛋蛋白)。 五、仪器、试剂 1.仪器:剪刀,解剖刀,双面刀片,试管,试管架,试管夹,大小烧杯,小量筒,滴管,玻璃漏斗,酒精灯,三脚架,石棉网,火柴,研钵,石英砂,纱布,载玻片,盖玻片,毛笔,吸水纸,显微镜。 2.试剂:①斐林试剂(0.1g/L的NaOH溶液+ 0.05g/mL的CuSO 溶液);②苏丹 4 Ⅲ染液;③双缩脲试剂;④体积分数为50%的酒精溶液;⑤蒸馏水。 六、方法步骤(演示教学课件) 1.制备试剂。 2.可溶性还原糖的鉴定、方法、步骤。 3.脂肪的鉴定、方法、步骤。 4.蛋白质的鉴定、方法、步骤。 七、教学过程 新课引入:我们在化学中学习过物质的鉴定,其原理是被鉴定的物质与所用的化学试剂要么发生颜色反应,要么产生沉淀,我们生物学上也采用此原理,在生物学中物质鉴定的理念是:某些化学试剂能够使生物组织中的有关有机化合物产生特定的颜色反应。 新课教学:(具体原理) ①可溶性还原糖+ 斐林试剂→砖红色沉淀。(水浴加热) ②脂肪小颗粒 + 苏丹Ⅲ染液→橘黄色小颗粒。(要显微镜观察)
蛋白质相互作用的概述 一、为什么要研究蛋白质相互作用 二、蛋白质相互作用亲和力:K d=[A][B]/[AB] 三、蛋白质相互作用的应用 A、利用抗原和抗体的相互作用:Western blot,免疫共沉淀,染色质沉淀,抗体筛库 B、利用已知的相互作用建立tag:GST pull down,Biotin-Avidin结合, C、直接利用蛋白质的相互作用:蛋白质亲和层析,酵母双杂交,phage display,Bait蛋白质筛表达库,蛋白质组 四、相互作用的生物学意义:蛋白质间的相互作用是细胞生命活动的基础。 五、生物学功能的研究:获得功能或失去功能 I、一些常用蛋白质相互作用技术 ?Traditional co-purification (chromatography co-purification and co-sedimentation) ?Affinity chromatography:GST pull down,Epitope-tag ?(co-)Immunoprecipitation ?Western和Far-Western blot Surface Plasmon Resonance Two-Hybrid System Fluorescence Resonance Energy Transfer (FRET) (实验过程及原理,注意事项,优缺点) III、研究实例讨论 一、酵母双杂交系统 作用:发现新的相互作用蛋白质;鉴定和分析已有的蛋白质间的相互作用;确定蛋白质相互作用的功能基团 具体过程:见书本 优点:是酵母细胞的in vivo相互作用;只需要cDNA,简单;弱的相互作用也能检测到 缺点:都是融合蛋白,万一融合出新的相互作用;酵母的翻译后修饰不尽相同,尤其是蛋白质的调控性修饰;自身激活报告基因;基因库德要求比较高,单向1/3是in frame 蛋白质毒性;第三者Z插足介导的相互作用;假阳性 酵母双杂交系统是当前广泛用于蛋白质相互作用组学研究的一种重要方法。其原理是当靶蛋白和诱饵蛋白特异结合后,诱饵蛋白结合于报道基因的启动子,启动报道基因在酵母细胞内的表达,如果检测到报道基因的表达产物,则说明两者之间有相互作用,反之则两者之间没有相互作用。将这种技术微量化、阵列化后则可用于大规模蛋白质之间相互作用的研究。在实际工作中,人们根据需要发展了单杂
蛋白质相互作用的主要研究方法 细胞接受外源或是内源的信号,通过其特有的信号途径,调节其基因的表达,以保持其生物学特性。在这个过程中,蛋白质占有很重要的地位,它可以调控, 介导细胞的许多生物学活性。虽然有一些蛋白质可以以单体的形式发挥作用,但是大部分的蛋白质都是和伴侣分子一起作用或是与其他蛋白质形成复合物来发挥作用的。因此,为了更好地理解细胞的生物学活性,必须很好地理解蛋白质单体和复合物的功能,这就会涉及到蛋白质相互作用的研究。在现代分子生物学中,蛋白质相互作用的研究占有非常重要的地位。 研究蛋白质相互作用时要根据不同的实验目的及条件选择不同的实施策略。研究已知蛋白间的相互作用人们关注的是蛋白间能否发生结合,实验本身更趋向于验证性,因此,应选择操作性强、可信度高、接近生理条件的技术方法,尽量减少实验本身带来的假阴性或假阳性。蛋白质相互作用方面的研究方法主要有免疫共沉淀、Far Western blotting、生物信息学、酵母双杂交系统、噬菌体展示、表面等离子共振、荧光能量转移等几种。 1 免疫共沉淀 免疫共沉淀(Co-Immunoprecipitation)是以抗体和抗原之间的专一性作用为基础的用于研究蛋白质相互作用的经典方法。是确定两种蛋白质在完整细胞内生理性相互作用的有效方法。其基本原理是:细胞裂解液中加入抗体,与抗原形成特异免疫复合物,经过洗脱,收集免疫复合物,然后进行SDS-PAGE及Western blotting分析。免疫共沉淀既可以用于检验已知的两个蛋白质在体内的相互作用,也可以找出未知的蛋白质相互作用,不管是两者的哪个,其原则都是一样的,都需要用特异性的抗体与其中的一种蛋白质结合,之后通过蛋白质A或蛋白质G琼脂糖微珠将复合物沉淀下来,然后用SDS-PAGE鉴定。免疫共沉淀中设置正确的对照非常重要,因为该方法可能出现假阳性的概率比较高,设置的对照包括:在对照组中使用对照抗体,以缺失目的蛋白的细胞系作为阴性对照等等。 在免疫共沉淀试验中要保证试验结果的真实性应注意以下几点:(1)确保共沉淀的蛋白是由所加入的抗体沉淀得到的,而并非外源非特异蛋白。单克隆抗体的使用有助于避免污染的产生。(2)要确保抗体的特异性。即在不表达抗原
Thermo Scientific Pierce Th S i tifi Pi
蛋 蛋白相互作用的研究方法和实践 实
罗 莎 Rosa Luo Ph.D. Application Scientist Biosciences Division Thermo Fisher Scientific China
酵母蛋白质相互作用图谱
Thick blue lines represent literature-derived interactions from PreBIND+MIPS in the HMS-PCI dataset. Thin orange lines represent potential novel interactions. Courtesy MDS Proteomics
2
蛋白质相互作用技术
Genetic Two Hybrid Phage Display Mutational analysis M t ti l l i Biochemical Immunoprecipitation (IP) Co-Immunoprecipitation (C IP) C I i it ti (Co-IP) Pull-Down Assays Far Western FRET (Fluorescence Resonance Energy Transfer) Chemical Crosslinking Label-transfer FeBABE F BABE mapping i Fluorescent Immunofluorescence colocalization
3
《检测生物组织中的糖类、脂肪和蛋白质》教学设计与反思 课题:《检测生物组织中的糖类、脂肪和蛋白质》(高中生物人教版必修一 ) 环节一 :明确本课学习目标。 1、知识与能力:认识是几种化学试剂和物质颜色反应特征;尝试用化学试剂检测生物组织中的糖类、脂肪和蛋白质。培养学生的动手能力观察能力逻辑思维能力和表达能力。 2、 过程与方法:通过分组实验,跟同学分工合作,相互协调团结协力共同探究的精神。让学生学会探究问题的基本方法和程序。 3、 情感态度与价值观:乐于参与学习,认识生物科学的价值,养成质疑、求实、创新及勇于实践的科学精神和态度,认同生命的物质性,了解健康的饮食习惯。培养学生团结分工合作的精神。 二、实验原理:某些化学试剂能够使生物组织中的有关有机化合物产生特定的颜色反应,从而将有关有机化合物鉴定出来。 1.检测生物组织中还原糖、脂肪和蛋白质 实验原理:还原糖 (加热)先浅蓝再棕色最后是 砖红色 脂肪 红色 蛋白质 紫色 (因为有肽键) 环节二:复习准备实验的基本要求 通读实验手册,明白三种物质的检测方法和原理。 环节三:老师讲解 老师:同学们这节课,按我们的计划开始做《检测生物组织中的糖类、脂肪和蛋白质》,根据课前制定的实验方案,分15个小组实验。先做验证实验:蛋白质、还原糖、淀粉和脂肪的检测,然后选取老师提供的待测物质探究这些物质里的主要成分,待测物质有豆浆、花生浆、马铃薯匀浆、新鲜猪肝匀浆、苹果汁、雪梨汁、橘子汁,每种物质都要探究主要含有糖类还是含有脂肪还是含有还原糖。同学们同时注意以下几点: 第一、配置菲林试剂的时候要注意用量,配好的斐林试剂不是全部倒入验证还原糖试剂里;为了节约能源,水浴加热的热水,到老师讲台取用已经烧好的热水,再加热。注意颜色的变化过程。 第二、验证脂肪的时候,滴加了A 液后、必须震荡,才能滴加B 液; 第三、注意药品不能随意混用,尤其是滴管是专用的; 第四、先做验证实验,再做探究实验; 第五、实验完成后,废液必须统一倒入指定的废液回收瓶,并清洗好仪器; 第六、必须如实记录实验现象。做切割花生切片的时候不要伤手了。 橘黄色 苏丹Ⅲ染液 苏丹Ⅳ染液 双缩脲试剂 斐林试剂
一、检测蛋白质与蛋白质相互作用 ① FRET技术(in vivo) FRET,Fluorescence resonance energy transfer,即荧光共振能量转移技术。该技术的原理是用一种波长的光激发某种荧光蛋白后,它释放的荧光刚好又能激发另一种荧光蛋白,使其释放另一波长的荧光,如下图所示: 以下图为例,若要利用FRET检测两种蛋白是否有相互作用,需将两种蛋白的基因分别与这两种荧光蛋白的基因融合,并在细胞内表达出两种融合蛋白。然后只需用紫外光对CFP进行激发,并检测GFP是否放出绿色荧光。如果能检测到绿色荧光,那么可以说明这两种蛋白可能有相互作用;反之,则是这两种蛋白没有相互作用。 ②酵母双、三杂交技术(in vivo) 酵母双杂交系统主要用于考察两种蛋白是否有相互作用,其原理是典型的真核生长转录因子,如GAL4、GCN4等都含有二个不同的结构域,即AD和BD。这些转录因子只有同时具有这两个结构域时才能起始转录。由此,设计不同的两个载体,一个含有AD基因(假设为A载体),另一个含有BD基因(假设为B载体)。 一般将一个已知蛋白的基因连在B载体上,作为诱饵(Bait),将未知蛋白的基因连在A载体上,将这两个载体都转到特定的酵母细胞内,看未知蛋白与已知蛋白是否有相互作用。如果两者有相互作用,那么就可以启动报告基因的转录,从而使这个酵母细胞能在选择培养基上显现出来或者生存下来;如果两者无相互作用,那么报告基因就无法表达,那么这个酵母细胞就无法在择培养基上显现出来或者生存下来,如下图所示:
由于酵母双杂交系统不能鉴定膜蛋白间的相互作用,因此又发展出了分离泛素酵母双杂交系统。该系统的原理如下图所示: 如图所示,将泛素蛋白拆分为两个片段,即C端段(Cub)和N端段(NubG),并在C端段的N端接上一个LexA-VP16转录因子,此时它并不能激活基因转录(因为它被限制在了C端段上,不能进入细胞核发挥作用)。 将该C端段连到一个膜蛋白上,将N端段连接到另一个膜蛋白上。若两个膜蛋白有相互作用,那么两个膜蛋白在相互靠近时会使泛素蛋白的N端段和C端段靠近结合,形成一个完整的泛素蛋白。此时泛素蛋白酶体会将这一段被泛素标记的片段降解,那么连接C端段的LexA-VP16转录因子掉落,即可进入细胞核启动标记基因的表达。 酵母三杂交的原理与双杂交一样,只是它研究的是两个蛋白和第三个成分间的相互作用,通过第三个成分使两个蛋白相互靠近。第三个成分可以是:蛋白、RNA或小分子,如下图所示: 如上图所示,在加入第三种成分前,蛋白X与蛋白Y之间并无直接相互作用,因此无法使BD和AD靠近,报告基因不能表达;当加入第三种成分后,蛋白X与蛋白Y的距离被拉近,BD和AD靠近,报告基因表达,从而可以被检测到。 ③ Pulldown技术(in vitro) Pulldown,即蛋白沉降技术,它是建立在蛋白质亲和层析的基础上的一种检测蛋白质间相互作用的分析方法。亲和层析的原理如下图所示,不同蛋白对配体的亲和程度不同,因此可以先将非特异结合的蛋白用低浓度缓冲液给清洗出去,只剩目的蛋白与层析柱结合,然后再用洗脱液将目的蛋白洗脱下来,达到纯化目的蛋白的作用。
实验教学设计 检测生物组织中的糖类、脂肪和蛋白质 组别:生科三班十组
组员:韩国良、林心恬、温淑娟、沙黑玛章节:高中生物人教版必修1第2章 目录 一、教材分析 (1) 二、学情分析 (1) 三、学习目标 (1) 1. 知识目标 (1) 2. 能力目标 (2) 3. 情感价值观目标 (2) 四、学习重、难点 (2) 五、教法、学法 (2) 六、教学准备 (2) 七、教学流程 (2) 八、课时安排 (4) 九、教学过程 (4) 1.实验目标 (4) 2. 实验原理 (4) 3. 材料器具 (4) 4. 方法步骤 (5) 5. 实验结果和分析 (7)
6. 注意事项 (8) 十、创新实验 (8) 十一、参考文献 (12) 检测生物组织中的糖类、脂肪和蛋白质 一、教材分析 这节课是普通高中课程标准实验教科书生物必修 1《分子与细胞》第 2 章第 1 节的一个实验。 1.课标要求 此实验在过渡教材中是一个验证性实验,而在课标教材中是一个重在培养学生探究意识的探究性实验,这是教材中第一个可以引导学生进行初步探究的实验,所以上好该实验不仅对培养学生的探究能力有重要作用,而且可以使学生体会探究思想,初步掌握科学探究的一般方法。 2.教材设计理念 课标教材把此实验安排在学习蛋白质、糖类和脂肪等知识内容之前,目的在于一方面为接下来学习各类有机物奠定感性认识基础,另一方面,由于实验内容的设置上注重学生对材料的选择,对检测结果的预期和实验方案的设计,因此有利于培养学生的实验探究能力,为以后各章节的探究性实验的顺利开展奠定了基础。本实验是一个面向全体学生的探究实验,力求使每一个学生在原有的水平上都有所收获、有所提高。 二、学情分析 高中生的思维水平、学习能力已经发展到较高阶段,乐于并有能力进行自主探究性的学习,实验的内容与日常饮食有关,注重与现实生活的联系,学生极易产生学习兴趣,设置不同层次的探究,以适应不同智力水平、性格、兴趣、思维方式学生的需要。但材料试剂多,规范操作细节多,合作学习显得尤为重要。 三、学习目标
?技术与方法? 生物技术通报 B I O TECHNOLO G Y BULL ET I N 2006年增刊 蛋白质相互作用研究方法及其应用 王海波 安学丽 张艳贞 王爱丽 李巧云 晏月明 (首都师范大学生命科学学院,北京 100037) 摘 要: 过去10年来,蛋白质组学得到迅速发展,蛋白质间的相互作用作为蛋白质组学的重要内容,更是成为国内外竞相研究的重点,研究方法的快速发展为蛋白质间相互作用的研究奠定了坚实基础。着重就经典的噬菌体展示、酵母双杂交以及新近发展起来的串联亲和纯化、荧光共振能量转移技术和表面等离子共振等蛋白质相互作用研究方法的原理及应用作一综述并展望其发展前景。 关键词: P DT Y2H T AP FPET SPR Approaches and Appli cati ons of Protei n 2Protei n I nteracti on Studi es W ang Haibo An Xueli Zhang Yanzhen W ang A ili L i Q iaoyun Yan Yue m ing (College of L ife Science,Capital N or m al U niversity,B eijing 100037) Ab s tra c t: W ith the fulfill of HGP (Hu man genom ic p r oject ),the study t op r otein is s p ring up.Pr otein -p r otein in 2 teracti on is one of i m portant subjects of Pr oteom ic,it is i m p licated in every cellular p r ocesses .Now many methods have de 2vel oped t o identify and characterize p r otein 2p r otein interacti ons .The main content of this paper is describe both classical and es pecially recent methods t o study p r otein 2p r otein interacti ons such as Yeast t w o 2hybrid syste m (Y2H ),Tande m affinity pur 2ificati on (T AP ),Fluorescence res onance energy transfer (FRET )and Surface p las mon res onance (SPR ),fr om the p rinci p le t o p r ocess of these technol ogies,s ome ne w achieve ment obtained by these methods als o intr oduced . Key wo rd s: P DT Y2H T AP FPET SPR 作者简介:王海波,硕士研究生,首都师范大学生命科学学院608实验室 通讯作者:晏月明,Tel:010*********;E 2mail:yany m2004@https://www.doczj.com/doc/0a17086048.html, 随着生命现象的研究逐渐由获取基因序列信息转向研究基因功能,一门新的学科———蛋白质组学应运而生。蛋白质组是一个在空间和时间上动态变化的整体,其功能往往是通过蛋白质之间或与核酸之间相互作用而表现出来的,这种相互作用存在于机体每个细胞的生命活动过程中,相互交叉形成网络,构成细胞中一系列重要生理活动的基础。因此,对于蛋白质相互作用的研究就成为蛋白质组学中最主要研究内容之一,迄今已发展了包括经典的噬菌体展示技术、酵母双杂交系统以及新近发展并广泛应用的串联亲和纯化和荧光共振能量转移技术、表面等离子共振技术等多种有效的研究蛋白质间相互作用的高通量分析方法,为蛋白质组学的发展奠定了坚实的基础。 1 噬菌体展示技术(P DT ) 大肠杆菌丝状噬菌体包括f1、fd 和M13,它们只感染含F 因子的大肠杆菌。1985年,美国M iss ouri 大学S m ith 博士等人 [1] 将R I 核酸内切酶基因片段 连接到丝状噬菌体fd 编码次要外壳蛋白的基因Ⅲ中,成功地得到了在外壳蛋白中融合表达了酶分子的噬菌体颗粒。后经验证,该噬菌体能被Eco R Ⅰ核酸内切酶抗体有效中和,说明展示在噬菌体外壳表面的酶分子具有与天然酶分子相同或极其相近的构象和活性,这一试验的成功标志着噬菌体展示技术(Phage dis p lay techniques,P DT )的诞生。 噬菌体展示技术是在噬菌体展示肽库建立之后才开始广泛应用到蛋白质相互作用研究的。1990年Scott 等人 [2] 利用噬菌体展示技术构建了随机多
《检测生物组织中的糖类、脂肪和蛋白质》教学设计一、教材分析 教材把此实验安排在学习蛋白质、糖类和脂肪等知识内容之前,目的在于一方面为接下来学习各类有机物奠定感性认识基础,另一方面,此实验在教材中是一个重在培养学生探究意识的探究性实验,这是教材中第一个可以引导学生进行初步探究的实验,实验内容的设置上注重学生对材料的选择,对检测结果的预期和实验方案的设计,因此有利于培养学生的实验探究能力,可以使学生体会探究思想,初步掌握科学探究的一般方法,为以后各章节的探究性实验的顺利开展奠定了基础。 二、学情分析 高中生的思维水平、学习能力已经发展到较高阶段,乐于并有能力进行自主探究性的学习,实验的内容与日常饮食有关,注重与现实生活的联系,学生极易产生学习兴趣,设置不同层次的探究,以适应不同智力水平、性格、兴趣、思维方式学生的需要。但材料试剂多,规范操作细节多,合作学习显得尤为重要。 三、学习目标 1、知识目标: 说明特定的化学试剂能够使生物组织中相应的有机化合物产生特定的颜色反应;简述实验探究的一般方法,主要是根据所选实验材料设计实验并做出预期实验结果。 2、能力目标: 尝试用化学试剂检测生物组织中的还原糖、脂肪、蛋白质和淀粉。 3、情感态度价值观目标: 参与合作学习,形成严谨认真、敢于质疑的科学态度。按照实验操作规则操作实验,养成良好的实验习惯。 四、学习重、难点
1.重点 ①初步掌握鉴定生物组织中可溶性还原糖、脂肪、蛋白质的基本方法。 ②通过实验的操作和设计培养学生的动手能力,掌握探索实验设计技巧,从而培养创新思维能力。 2.难点:根据此实验方法、原理,设计实验来鉴定常见食物的成分。 3.突破方法:面对全体学生,做好充分的准备:材料、仪器准备和学生知识准备。课堂上发挥小组长的协助管理作用,合理有序地组织教学。 五、教材实验中存在的问题及改进措施 1、实验的误区 此实验属于探究型实验,但是大多数教师在教学中为了缩短实验教学时间,简化了实验步骤,将其变成验证型实验。实验通常是对某一种实验材料只进行一类物质的检测,导致学生误认为一种材料中只含有一类物质。比如:用苹果或梨检测还原糖,用花生检测脂肪等。学生就会误认为苹果中只有还原糖而没有其他物质,花生中只有脂肪……而一般的教学观点是每个细胞中含有的化合物的种类相同,都会含有六类化合物,只是含量上有些差异。应该让学生自主进行实验探究,由他们自己发现材料中的物质含量的差别。这样既渗透了教学内容,又提升了学生的学习兴趣,提高了他们的生物实验素养。 2、实验材料: 苹果或梨匀浆因多酚氧化酶含量较高,组织液容易被氧化成褐色或者土黄色,将反应产生的颜色部分掩盖,影响实验结果的观察,故实验中准备白萝卜汁等供学生选择,另外,同时准备甘蔗汁引导学生鉴定其中是否含还原糖。