产品技术要求
一、项目概述
近年来,随着医院信息化的不断深入,医院步入了一个快速增长期。医院正逐步实现医院管理的科学化、现代化、数字化,与国际、国内信息化建设的新技术接轨。
我院目前已经建成多个运行不同业务的信息系统,如HIS、LIS、PACS、EMR 等,业务系统已经相当成熟。现因业务发展需要,采购数据中心存储设备1台。
二、项目要求
1.项目名称
数据中心存储设备
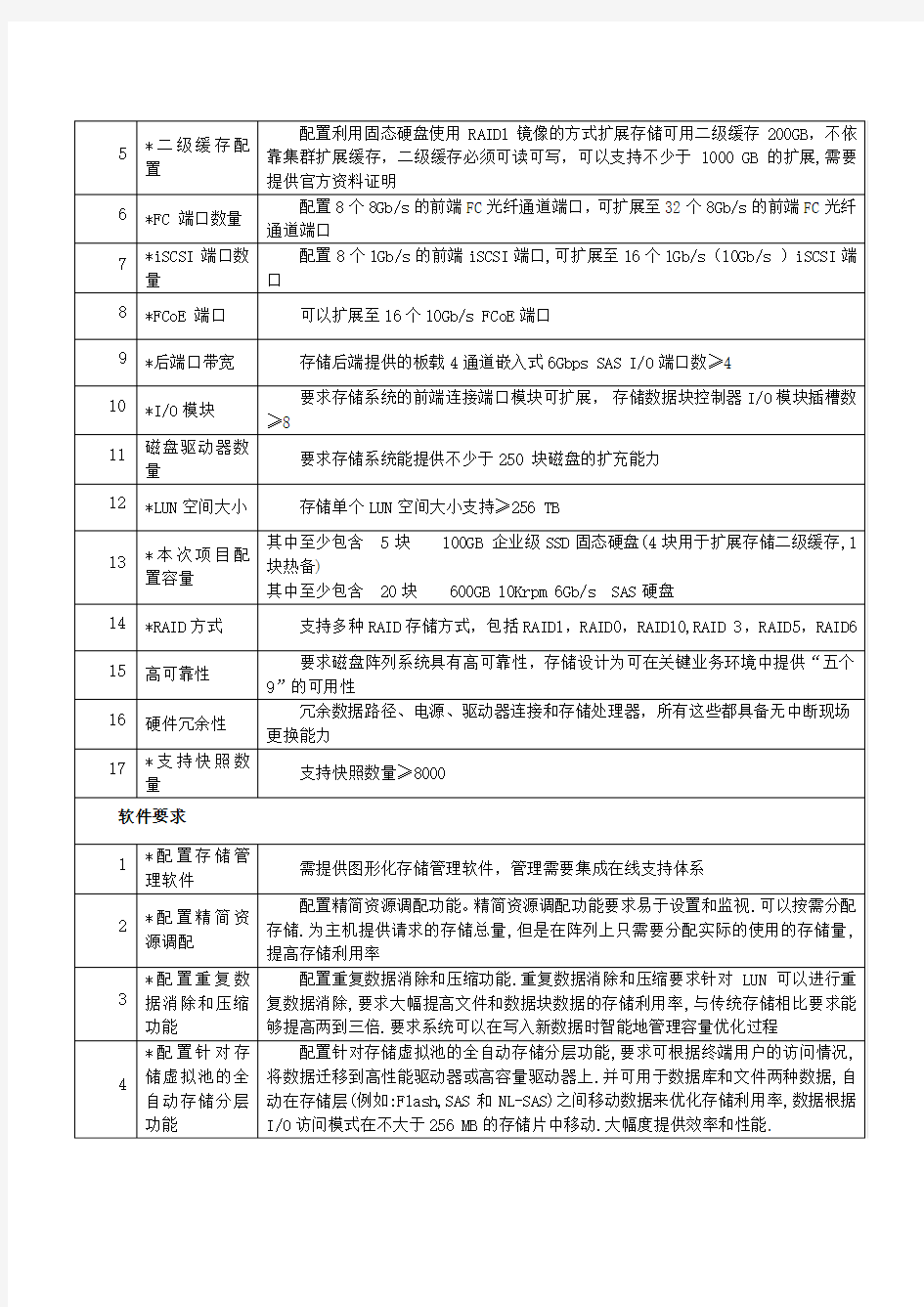
2.项目内容
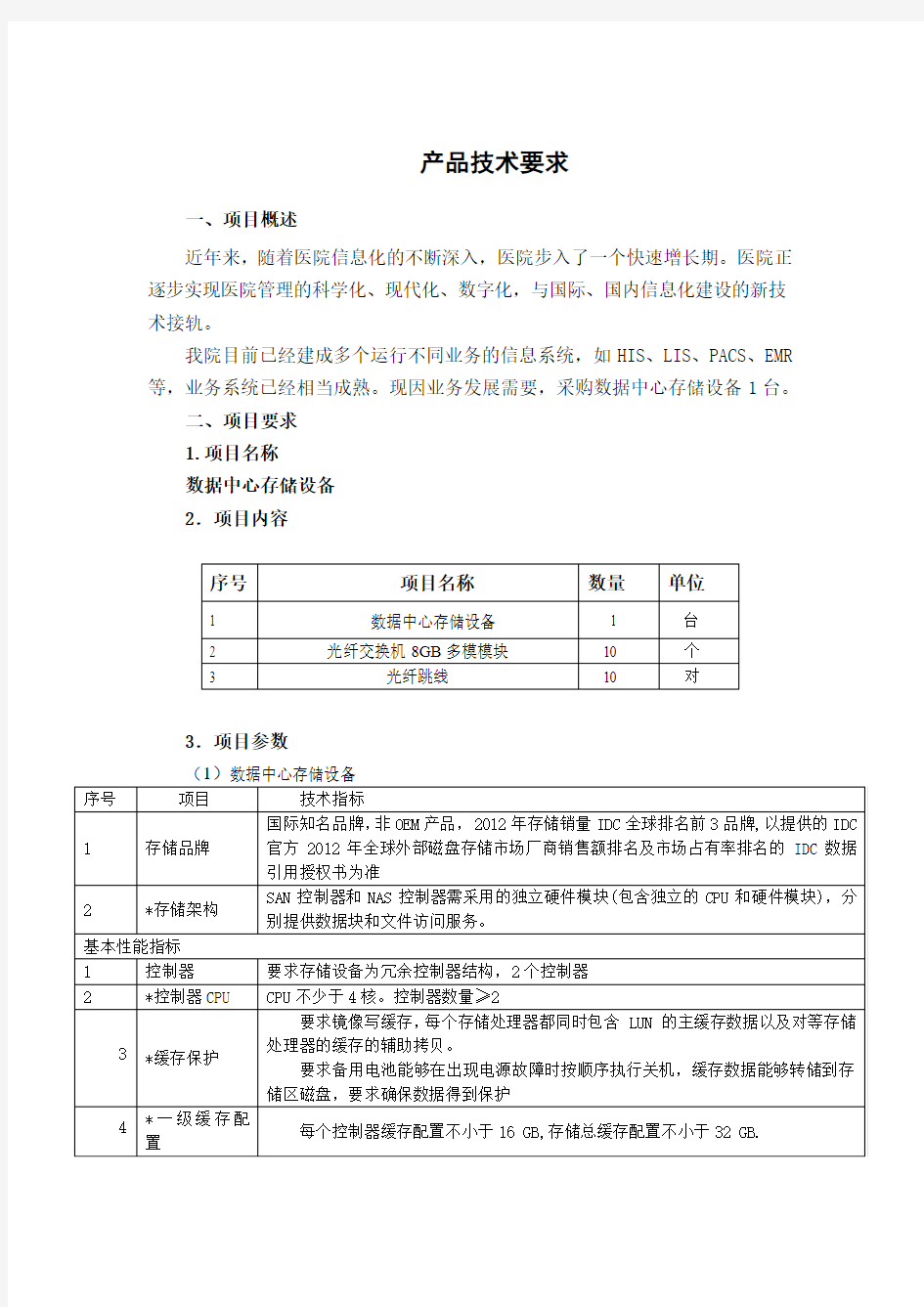
3.项目参数
数据中心存储设备
(2)****光纤交换机8GB多模模块
****光纤交换机8GB多模模块10个。
(3)光纤跳线
5米光纤跳线10对,用于本次采购存储设备到光纤交换机之间的连接。
XX电器有限公司 编号:产品技术规格书 品名: 产品型号: 产品编码: 编制:审核:批准: 日期:日期:日期: 名称: 地址:
1.基本信息 本承认书规定了进水阀的关键参数,性能要求,检验标准,测试标准,抽样判定规则及生产工艺、包装运输等 1.1产品概述: 本实用新型产品是属于水阀类,是一进一出单阀控制的进水阀,是一种用来控制流体的自动化基础元件,属于执行器;生活中用于控制水的流动或停止,一般会用到这种电磁阀。其工作原理是,电磁阀里有密闭的腔,当线圈通电时,电磁铁芯吸合,卸压孔打开,在进水咀介质的压力推动,打开主阀口,介质流通。当线圈断电时,弹簧复位并推动阀芯和伸缩套封住卸压孔,主阀口关闭,介质截止。这样通过控制电磁阀的电流就控制了机械运动。 1.2产品结构: 结构特点说明,各部件良好配合为关键。
2. 关键参数 1. 零件表面光洁,无缺陷,装配牢固可靠,无松动现象,其 性能应符合GB/T1291-91的要求; 2.额定电压为220V-240V 50/60Hz,额定电流为30±5mA(不通水状态); 3.绝缘等级为F级; 4.适用水压: 0.02-1.0MPa; 5.最大耐水压: 1.6MPa以下,历时10Min无渗漏; 6. 绝缘电阻: 导电部分和外露金属部分,非金属部分之间均大于100MΩ; 7. 匝间绝缘: 对线圈施加1500V,50Hz的脉冲电压,在示 波仪上观察到的是完整的正弦波; 8. 电气强度:绝缘电阻通过后,导电部分和外露 不通电金属和非金属之间施加3125V 50Hz高 压1Min的时间,不应击穿; 9. 流量要求:(根据客户要求); 10. 绕组温升: <75K; 11. 线圈电阻为4.1±0.3KΩ; 12. 寿命不小于30000次,常温,额定电压下通5S,断5S为一周期,厂家要每周做一次寿命试验: 1)0.02MPa时,5000次; 2)0.3MPa时,20000次; 3) 0.8MPa时,5000次; 13. 噪声,声压级小于55dB(A); 14.注公差的塑料件按MT5,金属件按IT14级验收; 15. 电磁部分的工作按连续工作考核。 3. 检验标准 3-1 检验依据: 00234015—《零部件图纸》 Q/HR 0501014 《材料通用要求》(现行) Q/HR 0501028 《塑料成型件通用要求》(现行) GB/T 2828.1-2003 《计数抽样检验程序第1部分:按接收质量限(AQL)检索的逐批检验抽样计划》 4.测试标准 依据R-CS-1203002家用电动洗碗机用电磁阀测试。
产品技术规范书 设备名称:SF6气体定性检漏仪 型号:XP-1A 数量:1台套 一、产品应用: XP-1A SF6气体定性检漏仪是30年以来检漏仪制造经验的顶点。作为迄今制造的最稳定与最灵敏的负电晕检漏仪,我们为提供此种工具而骄傲。我们把所有的经验及多年客户的反馈溶入到此产品中,希望为用户提供最好的一切:价格、性能及可靠性。 XP-1A SF6气体定性检漏仪的核心是一台先进的微处理机。它采用的数字信号处理技术使得它比采用的操纵电路及传感头信号更好成为可能。此外,电路中使用的元件数量约减少40%,从而提高了可靠性及性能。微处理机实时监视传感头和电池电压值,每秒钟可达4000次,能及时补偿即使是最微小变动的信号脉动。这使得该仪表在几乎一切环境的应用中,成为一种稳定而可靠的检测工具。 XP-1A SF6气体定性检漏仪在设计上增加了许多方便用户使用的性能。灵敏度的七级自由设置,使仪表从一级到七级增加64倍的灵敏度;独特的三色发光二极管把渐进的及广范围的泄漏大小的指示出来;指示灵敏度的等级;并提供有关电池电量的实际电压指示。触摸式键盘控制所有使用功能;新颖的外壳设计供使用者紧握,方便操作;安装使用时目视的直观指示器。 二、采用标准 本SF6气体定性检漏仪的制造、试验和验收除了应满足本技术要求外,还应符合如下标准: ●GB191 包装储运图示标志EQVISO780:1997 ●GB/T5048防潮包装 ●GB/T5832.2—1986 气体中微量水分的测定露点法 ●GB/T6388 运输包装收发货标志 ●GB/T6587.1—1986 电子测量仪器环境试验总纲 ●GB/T6587.2 电子测量仪器温度试验 ●GB/T6587.3 电子测量仪器湿度试验 ●GB/T6587.4 电子测量仪器振动试验 ●GB/T6587.5 电子测量仪器冲击试验
10kV电缆技术规范书 采 购 技 术 要 求
10kV电力电缆 技术规范书 1 总则 1.1一般规定 1.1.1 投标人应具备招标公告所要求的资质,具体资质要求详见招标文件的《商务部分》。 1.1.2 投标人或供货商应设计、制造和销售过铜芯或铝芯电缆的产品,且使用条件应与本工程相类似或较规定的条件更严格。近3年至少有1000km的10kV电缆产品运行业绩。1.1.3 投标人应仔细阅读招标文件,包括《商务部分》和《技术部分》的所有规定。由投标人提供的10kV电力电缆应与本规范中规定的要求相一致。卖方应仔细阅读包括本规范在内的招标文件中的所有条款。卖方提供货物的技术规范应符合招标书要求。 1.1.4 本规范提出了对10kV电力电缆技术上的规范和说明。 1.1.5 如果投标人没有以书面形式对本规范的条文提出异议,则意味着投标人提供的产品完全符合本技术规范书的要求。如有偏差,应在投标书中以技术专用部分附录的格式进行描述。 1.1.6 本规范所使用的标准如与投标人所执行的标准不一致时,按较高标准执行。 1.1.7 本规范将作为订货合同的附件。本规范未尽事宜,由合同双方在合同技术谈判时双方协商确定。 1.1.8 本规范中涉及的有关商务方面的内容,如与招标文件的《商务部分》有矛盾时,以《商务部分》为准。 1.1.9 本规范中的规定如与技术规范专用部分有矛盾时,以专用部分为准。 1.1.10 本规范提出的是最低限度的技术要求,并未对一切技术细节作出规定,也未充分引述有关标准和规范的条文,投标人应提供符合GB和IEC最新版本的标准和本规范的优质产品。 1.2投标人应提供的资格文件 以下列明了对投标人的资质的基本要求,投标人应按下面所要求的内容和顺序提供翔实的投标资料,否则视为非响应性投标。基本资质不满足要求、投标资料不翔实或严重漏项将导致废标。 1.2.1 拥有权威机构颁发的ISO9000系列的认证证书或等同的质量保证体系认证证书。 1.2.2 具有履行合同所需的生产技术和生产能力的文件资料。 1.2.3 有能力履行合同设备维护保养、修理及其他服务义务的文件。 1.2.4 投标人应提供国家电网公司认可的专业检测机构出具的不超过5年的与所招标型号相同/相近的电力电缆型式试验报告,型式试验报告中电缆的截面不得小于本次招标电缆的截面,报告应由具有资质的第三方权威检测机构出具。 1.2.5 投标人所提供的组部件和主要材料如需向外协单位外购时,投标人应列出外协单位清单,并就其质量作出承诺。同时提供外协单位相应的例行检验报告、投标人的进厂验收证明、外协单位的相应资质证明材料和长期供货合同。 1.3工作范围和进度要求 1.3.1 本规范适用于专用部分所有采购的电力电缆。具体为:提供符合本技术规范要求的
目录 1.名词解释 (1) 2.项目总体描述 (1) 2.1项目时间节点 (1) 2.2产品信息 (1) 3. 主要性能和技术要求 (2) 3.1一般要求 (2) 3.2性能要求 (2) 3.3试验和寿命 (2) 3.4成品性能 (2) 3.5验收规则 (2) 3.6执行法规和标准 (2) 4. 双方工作任务、时间要求及违约 (2) 4.1双方工作任务及时间要求: (2) 4.2风险责任的承担 (3) 4.3违约责任 (3) 5.交付物的提交 (3) 5.1甲方向乙方提供交付物的时间: (3) 5.2乙方向甲方提供的交付物及时间: (3) 6.双方数据交换的要求 (4) 7.知识产权及保密 (5) 8.测试要求 (5) 8.1样车/样机的测试 (5) 8.2样件的验收 (5) 9.投标书内容及要求 (6) 10.甲方技术联络人 (7)
1.名词解释 产 品:指乙方根据本产品开发技术要求规定,设计、生产的×××× 参考样件:技术要求:指甲方对产品结构、尺寸、性能、材料等的要求(非金属件含产品颜色、皮纹等)。 技术资料:指包括但不限于产品的设计、开发、试验、制造的图纸、CAD 数据、技术规范、分析报告、试验报告、样件等全部技术文件及实物,也包括在本产品开发技术要求履行过程涉及到的各方的专有技术、专利技术、企业秘密、生产信息、商业机密等资料。 产品数据:指描述产品结构、性能、材料、尺寸、公差、表面处理等特性的最终完整数据,它完全可以指导产品的后续工艺工装设计和产品制造。 电子文档:指用计算机数据对产品进行描述的文档。 黑盒子部件:指因需要特殊加工工艺,而只能由产品供应商定义的零部件。 其结构布置图、详细设计及零件标准将由供应商提供,主机厂仅负责零部件的装配尺寸和形状修正。 灰盒子零件:指的是由主机厂定义外表面及边界条件,由供应商完成具体内部结构详细设计的零部件。 2.项目总体描述 2.1 项目时间节点 随着项目的开展以上节点可能有所变化, 任何变动都将与乙方进行沟通,并应以书面形式进行确认。 2.2 产品信息 2.2.1以下为此协议所涉及的零件号及名称清单 2.2.2零部件简图 1) ×××××××××× 图1×××××××× 2) ××××××××××
产品技术要求要求模板 医疗器械产品技术要求编号: 口腔颌面锥形束计算机体层摄影设备 1.产品型号/规格及其划分说明 1.1 产品型号规格划分说明 1.2 应给出产品每种配置的详细技术规格(见附录A)。 1.3 软件发布版本 1.3.1 嵌入式软件 1.3.2 工作站软件 1.4 版本命名规则 明确软件完整版本的全部字段及字段含义 2.性能指标 2.1 电功率 2.1.1 最大输出电功率 2.1.2 标称电功率 CBCT摄影的标称电功率 2.2 加载因素及控制 2.2.1 X射线管电压 CBCT摄影的X射线管电压调节范围、方式、值偏差2.2.2 X射线管电流 —38—
CBCT摄影的X射线管电流调节范围、方式、值偏差 2.2.3 加载时间 CBCT摄影的加载时间调节范围、方式、值偏差 2.2.4 电流时间积 CBCT摄影的电流时间积调节范围、方式、值偏差 2.2.5 防过载 2.3 成像性能 注:扫描模式(见2.5.5)、扫描视野(见2.5.6)、三维体素(见2.5.7)如有多种选择,应分开制定。 2.4 机械装置性能 2.5 工作站软件功能 2.5.1 患者管理功能(如新增患者) 2.5.2 图像管理工具1(如放大、反转、标记、加亮、合并、保存)2.5.3 图像管理工具2(如图像尺寸测量) 2.5.4 DICOM 3.0要求 —37—
注册申请人应在随机文件中提供DICOM 3.0标准的符合性声明。 2.5.5 扫描模式的选择 2.5.5.1 基本或普通扫描模式 2.5.5.2 高分辨率或高清扫描模式 2.5.5.3 低剂量,短扫描或快速扫描模式 2.5.5.4 连续两次不同高度位置的扫描叠加以增大竖直方向视野的模式 2.5.6 扫描视野的选择 2.5.7 三维体素的选择 2.6 产品技术特点(与注册申请人声称及产品特点相关) 2.6.1 降低剂量 2.6.2 去除金属伪影 2.7 外观要求 2.8 环境试验要求 2.9 安全要求 2.9.1 产品应符合GB 9706.1-2007、GB 9706.3-2000、GB 9706.11-1997、GB 9706.12-1997、GB 9706.14-1997、GB 9706.15-2008、YY 0505-2012的要求。产品安全特征见附录A。 2.9.2 激光安全应符合GB 7247.1-2012的要求。 2.10 脚踏开关的要求 2.11 剂量 —38—
采购产品技术要求和验收标准 1.0 元器件入库前检验 1.1 严格执行采购控制程序,从合格的供方采购合格产品。 1.2 对进厂的采购产品都要按下面的检验项目、方法和标准进行 检验,。对安全件,至少应抽取10%的样品按表中的检验项目进行检验和试验:对关键元器件,至少应抽取5%的样品进行检验:对一般材料,只须进行确认。 检验/验证项目、方法和标准: 1.2.1 断路器: 依据标准:GB14048.2《低压断路器》 1.2.2 隔离开关、熔断器: 依据标准:GB14048.3《低压开关、隔离器、隔离开关及熔断器组合电器》
1.2.3 接触器: 依据标准:GB14048.6《接触器和电动机起动器》 1.2.4电流互感器: 依据标准:GB1208《电流互感器》 依据标准:GB14048.5《控制电路电器和开关元件》
检验/验证项目、方法和标准: 1.2.6母线: 依据标准:GB5585《电工用铜、铝及其合金母线》检验/验证项目、方法和标准:
依据标准:GB5023《额定电压450/750V及以下聚氯乙烯绝缘电缆》检验/验证项目、方法和标准: 1.2.8绝缘支撑件、母线框、母线夹板 依据标准:GB1408《固体绝缘材料工频电气强度试验方法》 检验/验证项目、方法和标准:
1.3凡符合1.2条的初步判定为合格品,如有一项不符即为不合格品,并 填 写入库前的检验记录。出现不合格则全检,合格放行,不合格退货。 1.4 如在出厂检验中出现机械或性能或电性能的缺陷时,最终判定为不合 格产 品,在出厂检验中作记录。 2.0 外协件入库前检验 2.1 外协的各种零部件必须按图纸检验相关尺寸及外观。 2.2 各种型号的低压柜柜体,到厂后都必须按图纸检验外型尺寸、漆的表面、 门的开启、接地螺栓的焊接、防护等级等,合格后方可入库。 3.0 生产过程中的自检 3.1 操作者在生产工程中应严格执行工艺文件,不得擅自更改或降低工艺标准,也不得随意执行未经批准而制定的其他标准。 3.2 在每个工序完成后,转入下道工序前,操作人应进行自检,确认该工序 合格后,在产品随工卡上加盖自己的工序章,并向检验员口头报验,检验员检验 合格,在随工卡盖章后,方可转入下道工序。 3.3 若检验人员检验后,判定某一项不合格,应进行返工,返工后必须重新检验,直到判定合格为止,加盖检验章,方可转入下道工序 4.0 对不合格品的处理方法 4.1 对采购产品和外协件初步判定为不合格品的,由检验员将检验结果(缺 陷描述)等,填写在采购产品进厂检验单中,做出标识,另行存放,按不合格品 控制程序执行。 4.2 过程产品发生不合格时,由检验员通知操作工返修,并在随工卡上作记 录,返工返修的产品重新报验合格为止,若产品确定为不合格,则应作好标识, 另行存放,按不合格品控制程序执行。 4.3 过程产品发生不合格时,由检验员将检验结果,填写在成品检验记录中, 按不合格品控制程序执行。
采购内容及技术要求 一、项目概述 项目名称:企业数据中心机房建设 占地面积:约36个平方 分布区域:分为中心机房区(35个平方),UPS电池房及操作办公区 二、项目建设范围 1)综合布线系统 IT机柜、上走线强弱电桥架、光纤熔接盘、24口屏蔽配线架、双绞线、光缆、光纤跳线、双绞线跳线等 2)精密空调系统 精密空调16kw,2台,上送风下回风; 3)UPS电源 强电配电柜,UPS主机(40KVA)、蓄电池组(满足满载1小时持续供电)、PDU、电池架等 4)动力环境监控系统 温湿度、水浸、电量监测、GSM短信报警、配电柜监测、精密空调监测、UPS主机监测、视频监控、门禁等
5)防雷接地系统 二、三级防雷、等点位接地、引入大楼综合接地等 6)气体灭火消防报警系统 气体灭火自动报警、温感、烟感、气体灭火装置、七氟丙烷等 7)机房装饰装修 天面微孔天花铝合金吊顶、墙面彩钢板饰面、防盗门、玻璃隔断平移门、照明及墙壁插座 8)配套 空调、电视机、KVM 9)其他 如果本技术规格书有明显未提到的细节,或在本技术规格书的条款中没有明显规定的,后期所有遗漏的责任由投标人承担,并不得因弥补遗漏增加费用,投标人投标时对该条款需提供承诺函,未提供或承诺含义不清,投标技术评分则为零分。 三、项目技术要求 (1)综合布线系统 品牌要求:双绞线、配线架、信息模块、跳线、面板指定品牌:美国康普、美国西蒙、法国罗格朗、台湾岳丰;光通信产品采用森豪、长飞、烽火;机柜采
用法国罗格朗、图腾 布线结构要求:采用EOR布线方式,并充分考虑网络配线架和光纤配线架数量,因配置数量不足导致综合布线工程无法满足项目需求,中标单位无偿配置齐全。 内容要求(包含但不限于):服务器机柜10套,按照EOR布线结构方式配置网络配线架、光纤配线架及相关线缆,弱电线缆采用上走线方式。 产品质量服务要求:必须具备并保证在工程完工时向厂商申请25年原厂质量及系统保证 技术要求: 1)综合布线线缆产品必须保证材料的防火、阻燃和防止由于燃烧释放出对人体有害的氯素有毒气体原因造成的人员不安全因素,其中低烟无卤线缆必须有国际或国内权威机构燃烧安全性检测报告,符合防火标准IEC60332-1的要求。 综合布线系统所选用的材料品牌必须为品牌表内的标准化产品,铜缆布线产品包括铜线缆、铜跳线、铜配线架、铜信息模块、信息面板、须采用端对端同一品牌产品。 铜布线系统,用户不接受其主要产品如双绞线、配线架、信息模块、跳线、面板,和主干光缆等采用OEM 方式的厂家产品。 综合布线产品的品牌具有25年及以上的历史,请提供相关证明文件。 2)综合布线产品的品牌具有REACH欧盟认证,并在国内具有自己独力产
保健食品产品技术要求规范(国食药监许[2010]423号) 发布日期:2011-02-10 来源:国家食品药品监督管理局 【发布单位】国家食品药品监督管理局 【发布文号】国食药监许[2010]423号 【发布日期】 2010-10-22 【生效日期】 2011-02-01 【效力】 【备注】各省、自治区、直辖市食品药品监督管理局(药品监督管理局):根据《食品安全法》及其实施条例对保健食品实行严格监管的要求,为进一步规范保健食品行政许可工作,提高保健食品质量安全控制水平,加强保健食品生产经营监督,指导保健食品产品技术要求编制工作,国家食品药品监督管理局组织制定了《保健食品产品技术要求规范》,现予印发,请遵照执行。国家食品药品监督管理局二○一○年十月二十二日 保健食品产品技术要求规范 一、根据《食品安全法》及其实施条例对保健食品实行严格监管的要求,为进一步规范保健食品行政许可工作,提高保健食品质量安全控制水平,加强保健食品生产经营监督,保障消费者食用安全,制定本规范。 二、国家食品药品监督管理局负责批准保健食品产品技术要求,并监督其执行。 三、保健食品产品技术要求应当符合国家有关法律法规、标准规范。 四、保健食品产品技术要求文本格式应当包括产品名称、配方、生产工艺、感官要求、鉴别、理化指标、微生物指标、功效或标志性成分含量测定、保健功能、适宜人群、不适宜人群、食用量及食用方法、规格、贮藏、保质期等序列(见附件1),并按照保健食品产品技术要求编制指南(见附件2)编制。 五、保健食品产品技术要求是产品质量安全的技术保障。生产企业应当按照保健食品产品技术要求组织生产经营,食品药品监督管理部门应当将保健食品产品技术要求作为开展监督执法的重要依据。 六、保健食品产品技术要求适用于保健食品新产品的注册申请和产品的再注册。
附件5 医疗软件产品技术审评规范(2017版) 本规范旨在指导企业提交医疗器械软件注册申报资料,同时规范医疗器械软件的技术审评要求。 本规范是对医疗器械软件的一般性要求,企业应根据医疗器械软件的特性提交注册申报资料,判断指导原则中的具体内容是否适用,不适用内容详述理由。企业也可采用其他满足法规要求的替代方法,但应提供详尽的研究资料和验证资料。 本规范是在现行法规和标准体系以及当前认知水平下、并参考了国外法规与指南、国际标准与技术报告制定的。随着法规和标准的不断完善,以及认知水平和技术能力的不断提高,相关内容也将适时进行修订。 本规范是对企业和审查人员的指导性文件,不包括审评审批所涉及的行政事项,亦不作为法规强制执行,应在遵循相关法规的前提下使用本规范。 本规范针对软件的特殊性,在现行法规要求下进一步明确了对医疗器械软件的要求,特别是对软件更新、软件版本的要求。本规范是医疗器械软件的通用规范,其他涉及软件医疗器械产品的规范可在本规范基础上进行有针对性的调整、修改和完善。 一、适用范围 本规范适用于第二类医疗器械软件的注册申报,适用的软件开发方式包括自主开发、部分采用现成软件和全部采用现成
软件。 医疗器械软件包括独立软件和软件组件。独立软件:作为医疗器械或其附件的软件;软件组件:作为医疗器械或其部件、附件组成的软件。 独立软件应同时具备以下三个特征:具有一个或多个医疗用途,无需医疗器械硬件即可完成预期用途,运行于通用计算平台。独立软件包括通用型软件和专用型软件,其中通用型软件基于通用数据接口与多个医疗器械产品联合使用,如PACS、中央监护软件等;而专用型软件基于通用、专用的数据接口与特定医疗器械产品联合使用,如Holter数据分析软件、眼科显微镜图像处理软件等。 软件组件应同时具备以下两个特征:具有一个或多个医疗用途,控制(驱动)医疗器械硬件或运行于专用(医用)计算平台。软件组件包括嵌入式软件和控制型软件,其中嵌入式软件(即固件)运行于专用(医用)计算平台,控制(驱动)医疗器械硬件,如心电图机所含软件、脑电图机所含软件等;而控制型软件运行于通用计算平台,控制(驱动)医疗器械硬件。 软件组件也可兼具处理功能。专用型独立软件可单独注册,也可随医疗器械产品注册,此时视为软件组件。 二、技术审查要点 (一)产品名称和结构组成的要求 1.独立软件 产品名称应为通用名称,并符合相关法规、规范性文件的要求,可以结合人体部位(如胸部、心脏等)、临床科室(如骨科、神经外科等)、处理对象(如CT图像、MRI图像、心电数
第二部分招标内容及要求 1.工程概况 2.招标内容 淮北市中泰广场项目空调末端设备采购。 3.设备名称、规格型号、数量,具体内容如下: 风机盘管及新风机组汇总表 所提供的服务包括货物的供货、运输、指导安装、技术及售后服务等。上述设备型号供参考,投标人可根据技术参数的要求,选择等于或优于本文件要求的产品投标。
4.技术要求 ①完整性:投标人所提供的设备应能满足空调系统等完整性的要求。需要招标人自行解决的设备、附件应在投标文件中列出,否则系统正常运行所缺的设备及附件,均视为免费及时提供。 ②适应性:投标人所提供的设备应能保证在使用地的自然环境、气候条件、公用设施等情况下全天候正常运行。 ③投标人所提供的设备必须是成套的、全新的、功能全的单元,并且必须是代表制造商最高水平的设计,同时应是先进的、工艺精良和高质量的产品。 ④所供设备按国产优质产品标准选用,满足通用性、体积小、互换性好,操作方便等要求。设备的通用性为“设备与使用的系统工程间衔接部件具有通用性,正常使用情况下易磨损或损坏部件应为市场通用的标准配件,如该设备不具备前述情况,在投标文件的货物性能详细说明中应载明”。 ⑤技术标准:符合国家和专业部门相关标准和规范。 ⑥末端设备详细技术要求 空调末端主要评价其内部及其配套的主要部件选配情况、技术参数、性能等指标。该部分的调试等工作由投标人负责。 1、关于风机盘管的基本技术要求 盘管供水温度7℃,回水温度12℃,盘管工作压力1.6兆帕。 性能参数:各风机盘管均要求提供最近一次国家有关部门测试报告。 性能差异:各投标单位用表格将招标要求与实际性能一一列出,有差异的应另附性能差异表。 2、空调机组(含新风机组)的基本技术要求 1)形式: 组合式空调机组应考虑可分段制造和运输,在现场根据紧固件连接各功能段,实现最终的功能。另外各投标人需考虑对招标文件中所有组合式空调机组现场拼装并就位的费用。 2)使用年限和使用条件 连续工作时间:全年工作**(由投标人填写)天,每天连续工作**(由投标
产品技术要求 编号: 医用帽 2020-5-10 发布2020-5-10 实施 XXXX有限公司发布
医疗器械产品技术要求编号: 医用帽 1.产品型号/规格及其划分说明 型号:/ 2.性能指标 2.1医用帽的型号规格应符合表1、的规定。 表 1(医用帽)单位为厘米 帽外围直径帽口直径 尺寸30 12 偏差±2±2 2.2外观 2.2.1医用帽应干燥、清洁、无霉斑,表面不允许有粘连、裂缝、孔洞等缺陷。 2.2.2医用帽连接部位可采用针缝、粘合或热合等加工方式。针缝的针眼应密封处理,针距每3cm 应为8针~14针,线迹应均匀、平直,不得有跳针。粘合或热合等加工处理后的部位,应平整、 密封,无气泡。 2.3结构见结构图 1
结构图1 2.3.1医用帽的结构应合理,穿脱方便,结合部位严密。 2.3.2帽子为圆形,帽口采用弹性橡筋收口,以适应多种头型。 2.4 断裂强力医用帽关键部位材料的断裂强力应不小于45N。注:关键部位为帽面。 2.5断裂伸长率医用帽关键部位材料的断裂伸长率应不小于15% 2.6应无异常气味。 2.7包装密封性要好,不允许漏气。 3.检验方法 3.1型号规格 使用通用量具,对医用帽样品进行测量,测定3件,其规格均应符合 2.1的要求。 3.2外观
3.2.1目视检查,应符 2.2.1的要求。 3.2.2目视检查,针距使用通用量具进行测量,应符合 2.2.2的要求。 3.3结构 目视检查,应符合 2.3的要求。 3.4断裂强力 医用帽关键部位材斜按照GB/T3923.1-1997规定的条样法进行试验,结果应符合 2.4的要求。 3.5断裂伸长率 医用帽关键部位材料按照GB/T3923.1-1997规定的条样法进行试验,结果应符合 2.5的要求。 3.6气味检验采取用鼻子闻的方法检验,符合 2.86的要求。 3.7包装密封性检验:参照GB15980标准要求,将小包装进入水中,轻轻挤压,不出气泡为合格。符合 2.7的要求。
医疗器械产品技术要求编号: XXXXXX 1产品型号/规格及其划分说明 1.1型号命名 P200 设计序号 产品代号 1.2结构组成(不同型号如有结构组成的差异,应分型号列明) XXXXXX(以下简称XX)主要由X射线管组件(组合式)、限束器、操作台、影像处 理系统、C形臂及可移动机架、医用X射线影像增强器组成。 1.3型号说明(如有多个型号此条适用,列表标明型号间差异) 表1型号说明 1.4工作条件 a)环境温度:10℃~40℃; b)相对湿度:30%~75%; c)大气压力:700hPa~1060hPa。 d)电源:AC220V±22V;50Hz±1Hz e)额定输入功率:xx VA。 2性能指标 2.1外观 2.2XXX ...... 2.X安全要求 XXX安全要求应符合GB9706.1-2007的要求,产品主要特征见附录C。(9706.1适用设备) XXX安全要求应符合GB4793.1-2007的要求,产品主要特征见附录C。(4793.1适用设备)
间(h )间(h ) 条件 中间 24 试验后通电 ※ 2.x 、2.x 、... - 2.x 、2.x 、... 72 试验后通电 ※ 2.X 电磁兼容 (9706.1适用设备) 电磁兼容应符合YY 0505-2012 的要求。 2.X 电磁兼容 (479 3.1适用设备) 电磁兼容应符合GB/T 18268.1-2010 的要求。 2.X 电磁兼容 (体外诊断类适用设备) 电磁兼容应符合GB/T 18268.1-2010及 GB/T 18268.26-2010 的要求。 2.X 环境试验 按 GB/T 14710-2009 中规定的气候环境Ⅱ组、机械环境Ⅱ组的要求及表 X 进行试验, 应符合要求。 表 X 试验要求及检验项目 试验要求 检测项目 电源电压(V ) 试验项目 持续时 恢复时 试验 通电 状态 初始检测 检测 最后 检测 额定值 额定值 -10% +10% 额定工作 低温试验 2 --- 试验时通电 ※ 全性能 - 2.x 、2.x 、... √ --- 低温贮 存试验 4 --- - AC220 额定工作 高温试验 2 --- 试验时通电 ※ --- 2.x 、2.x 、... --- √ 运行试验 4 --- 试验时通电 ※ --- 2.x 、2.x 、... --- √ 高温贮 存试验 4 4 试验后通电 ※ --- 2.x 、2.x 、... AC220 额定工作 湿热试验 4 --- 试验时通电 ※ --- AC220 湿热贮存 试验 48 --- 2.x 、2.x 、... AC220 振动试验 碰撞试验 运输试验 --- --- --- 试验后通电 ※ 试验后通电 ※ 试验后通电 ※ --- --- --- --- --- --- 2.x 、2.x 、... 2.x 、2.x 、... 2.x 、2.x 、... AC220 AC220 AC220 注:表中“※ ”按GB/T14710-2009的规定 3 检验方法 3.1 外观 用正常或矫正视力观察以及用手感检查,结果应符合2.1的要求。 1
技术文件目录 一、投标人技术情况表 (3) 二、总体技术方案 1、内科综合大楼公共标识指引牌技术方案 (4) a、门口招牌 (4) b、大堂总索引 (4) c、电梯索引 (4) d、电梯内索引 (4) e、楼层索引 (5) f、科室大牌 (5) g、科室分流牌 (5) h、静 (5) i、检验公共标识1 (6) j、检验公共标识2 (6) k、其他公共标识1 (6) l、其他公共标识2 (6) 2、内科综合大楼科室内标识指引牌技术方案 (7) a、科室门牌号 (7) b、洗手间 (7) c、科室吊牌 (7) d、护士站 (8) e、病房牌 (8) f、名称插条 (8) g、床号牌 (9) h、床头温馨提示牌 (8) i、床头温馨提示插牌 (9) j、病人一览表(大) (9) k、病人一览表( (10) l、标签盒 (10) 3、验收方案 (10)
投标人技术情况表
说明:请投标人正确填写本表,所填内容将作为评分的依据。其内容或数据应与对应的证明资料相符,如果不一致,可能导致该项的得分为0分。 内科综合大楼公共标识指引牌技术方案 a、门口招牌 材料:使用厚度为1mm的201号不锈钢,采用数控激光切割机开料,氩弧焊焊接成型 镀钛:使用电镀钛工艺,镀钛颜色按照采购人要求 安装:采用暗上方式安装,保证螺丝不外漏,每个独立部件有两个以上固定螺丝 售后服务:1、在质保期内对非人为因素引起的产品掉色、变色问题对产品进行更换 2、在质保期内用户提出质量问题后将在24小时内派员到达现场维修 b、大堂总索引 材料:使用厂生产的品牌的5mm奶白色亚克力,采用数控激光切割机开料 喷漆:使用亚克力专用油漆,油漆附着力达到GB-T 9286-1988 1级标准,油漆颜色按照采购人要求 丝印:使用与喷漆油漆相配的油墨,油墨附着力达到GB-T 9286-1988 1级标准,图案和文字清
关于印发化妆品产品技术要求规范的通知 国食药监许[2010]454 号 2010 年11 月26 日发 布各省、自治区、直辖市食品药品监督管理局(药品监督管理局): 为进一步规范化妆品行政许可工作,提高化妆品卫生质量安全控制水平,加强化妆品生产经营卫生监督,指导化妆品 产品技术要求编制工作,国家食品药品监督管理局组织制定了《化妆品产品技术要求规范》,现予印发,请遵照执行。 附件:1.国家食品药品监督管理局化妆品产品技术要求(文本格式) 2.化妆品产品技术要求编制指南 国家食品药品监督管理局 二0一0年十一月二十六日 化妆品产品技术要求规范 一、根据《化妆品卫生监督条例》,为进一步规范化妆品行政许可工作,提高化妆品卫生质量安全控制水平,加强化妆品生产经营卫生监督,保障消费者使用安全,制定本规范。
二、国家食品药品监督管理局负责批准化妆品产品技术要求,并监督其执行。 三、化妆品产品技术要求应当符合国家有关法律法规、标准规范。 四、化妆品产品技术要求应符合其文本格式的规定。文本格式应当包括产品名称、配方成分、生产工艺、感官指标、卫生化学指标、微生物指标、检验方法、使用说明、贮存条件、保质期等序列(见附件1),并按照《化妆品产品技术要 求编制指南》(见附件2 )编制。 五、化妆品产品技术要求是产品卫生质量安全的技术保障。生产企业应当按照化妆品产品技术要求组织生产经营,食品药品监督管理部门应当将化妆品产品技术要求作为开展卫生监督执法的重要依据。 六、化妆品产品技术要求适用于化妆品新产品的许可和产品延续。 七、化妆品产品技术要求编号。国产特殊用途化妆品按照HZ+GT+ 年份+0000 编制;进口特殊用途化妆品按照HZ+JT +年份+0000编制;进口非特殊用途化妆品按照HZ+JF+年份+0000编制。"HZ"表示"化妆品”,"GT"表示"国产特殊用途”, "JT"表示"进口特殊用途”,”JF"表示"进口非特殊用途”,"年份+0000"为化妆品批准文号(或备案号)的年份和顺序号。 八、本规范自2011 年4 月1 日起施行。 附件1 国家食品药品监督管理局 化妆品产品技术要求(文本格式) 产品技术要求编号)
制造商提供的设备技术文件部分应包括一下几点: 承包商在其投标文件中至少应提交下列文件和资料,这些文件和资料应该是以图纸、表格、文字相结合的形式出现,并应该是印刷制品,其文字应以中文形式出现,图纸或文件中各种单位必须使用国际单位。 (1)投标设备、材料与招标设备、材料技术条件差异表。(格式见后); (2)投标产品质量指标、技术性能、售后服务措施(包括以下内容): 1.投标设备的质量指标和技术参数; 2.投标设备的性能指标及说明; 3.设备制造采用原材料质量、检测手段及说明; 4.投标设备质量检测及检测手段; 5.投标设备的制作工艺及工艺设备的先进性、完备性及说明书; 6.设备运输和保护措施; 7.交货期、供货方案及措施; 8.售后服务承诺及措施、证明资料。 (3)质量承诺、保证体系及措施 设备制造企业认证(质量管理体系认证、环保认证和安全认证); 质量承诺及保证措施; (4)企业资质、信誉及业绩(包括以下内容); 设备制造企业所获资质; 信誉证书、荣誉证书、 业绩(包括设备的运行状况,并提交有效证明);(业绩表格式见后)(5)投标人认为必须提交的其他文件(包括以下内容): (1)对设备供货部分,承包商应提供尺寸齐全的设备外形图和安装图,包括设备重量、基础承载力以及最小安装间隙要求等。对系统供货部分,承包商除提供前述内容外,还应提供该系统的概念设计,包括PI图和系统控制流程图。 (2)各种设备主要技术性能和规格的文字和图表的说明。
(3)各种设备的设计、制造、测试所参照的主要标准。 (4)各种设备主要部件的材料组成的说明。 (5)出现技术偏差部分的图纸和文件说明。 (6)各种设备制造商名称及产地的清单,包括制造商的联系地址。 (7)承包商所建议的保证设备三年正常运行所需的备品备件(包括润滑剂)及专用维修工具以及制造商的地址和通信号码的清单。 (8)承包商计划的供货日程表。 (9)以及其它在投标时可能需要的资料。 请厂家按以上格式制作标书技术文件
医疗器械产品技术要求 编号: 医学影像处理软件 实施 1.3 版本命名规则 本公司软件产品命名规则为V X.Y.Z ?X:为发行版本,表示重大增强类软件更新,初始值为1,当软件进行了重大增强类软件更新,该号码加1,Y和Z归0。 ?Y:为子版本号,表示轻微增强类软件更新,初始值为0,当软件进行了轻微增强类软件更新,该号码加1,Z归0。 ?Z:为修正版本号,表示纠正类软件更新,初始值为0,当软件进行了纠正类软件更新,该号码加1。
1.4 产品适用范围 产品用于人体诊查图像、数据的管理、查看、传输和贮存,不包括自动诊断部分。 2 性能指标 2.1 通用要求 2.1.1 处理对象 50。
所需硬件环境最低配置如下: 2.1.5.2 放射影像模块 主要用于传送病人图像信息,主要组成:①普通设置,设置实体名称,设置端口号;②高级设置,需要用户密码登陆。
【上一个检查】 【下一个检查】 【窗口靠左半部显 【窗口靠右半部 【窗口靠上半部显示】 【窗口靠下半部显示】
1.1.2 使用限制 本产品为独立工作的通用型软件,使用者均需通过专业售前培训且能独立熟练操作软件,要求使用者拥有相关医学影像学教育背景。 1.1.3 用户访问控制 软件具有严格的权限管理机制,通过建立用户账号密码,对账号授不同的权限,不同科 1.1.7 可靠性 本产品产生的数据使用本地缓存、网关缓存和数据库存储三层保护,当软件出错时,可从本地硬盘或网关服务器或数据库中召回对应的数据,保障数据不丢失。 OR 1.1.8 维护性
由于本产品涉及DICOM影像传输技术和数据库技术,应通过产品手册或相关技术支持提供系统部署和维护方法。 Or 提供记录日志功能 本系统应该能够记录系统运行时所发生的所有错误,包括本机错误和网络错误。这些错误记录便于查找错误的原因。日志同时记录用户的关键性操作信息。 1.1.9 效率 1.1.10 运行环境 客户端——影像工作站和DICOM软件运行要求如下: ▲硬件环境要求:
保健食品产品技术要求规范 一、根据《食品安全法》及其实施条例对保健食品实行严格监管的要求,为进一步规范保健食品行政许可工作,提高保健食品质量安全控制水平,加强保健食品生产经营监督,保障消费者食用安全,制定本规范。 二、国家食品药品监督管理局负责批准保健食品产品技术要求,并监督其执行。 三、保健食品产品技术要求应当符合国家有关法律法规、标准规范。 四、保健食品产品技术要求文本格式应当包括产品名称、配方、生产工艺、感官要求、鉴别、理化指标、微生物指标、功效或标志性成分含量测定、保健功能、适宜人群、不适宜人群、食用量及食用方法、规格、贮藏、保质期等序列(见附件1),并按照保健食品产品技术要求编制指南(见附件2)编制。 五、保健食品产品技术要求是产品质量安全的技术保障。生产企业应当按照保健食品产品技术要求组织生产经营,食品药品监督管理部门应当将保健食品产品技术要求作为开展监督执法的重要依据。
六、保健食品产品技术要求适用于保健食品新产品的注册申请和产品的再注册。 七、保健食品产品技术要求编号按照BJ+G(或J)+年份+0000编制。“BJ”表示“保健食品”,“G(或J)”表示国产或进口,“年份+0000”为保健食品批准文号的年份和顺序号。 八、本规范自2011年2月1日起施行。 附件:1.国家食品药品监督管理局保健食品产品技术要求(文本格式) 2.保健食品产品技术要求编制指南
附件1: 国家食品药品监督管理局 保健食品产品技术要求(文本格式)(产品技术要求编号) 中文名称 汉语拼音名 【配方】 【生产工艺】 【感官要求】 【鉴别】 【理化指标】 【微生物指标】 【功效或标志性成分含量测定】 【保健功能】 【适宜人群】 【不适宜人群】 【食用量及食用方法】 【规格】 【贮藏】 【保质期】 ─────────────────────────────
目录 一、设备/材料技术性能的详细描述 1、概述............................................................ 2、产品性能........................................................ 二、供货范围 三、技术标准 四、技术数据表5 五、试验报告 六、技术文件 1、SGS技术文件.................................................... 2、CE认证证书..................................................... 3、质量控制体系.................................................... 七、技术服务 1、概述............................................................ 2、任务和责任...................................................... 3、技术服务........................................................ 4、培训............................................................ 5、设计联络........................................................ 八、资格审查文件 1. 主要产品名称、投标产品年(月)生产能力、分项产值、近期承接的主要任务(数量、交货期)及饱和程度。....................................... 2. 主要生产工装设备条件、数量及工艺技术水平。.................... 3. 主要试验设备名称、容量、数量、可试验项目。....................
关于印发化妆品产品技术要求规X的通知 国食药监许[2010]454号 各省、自治区、直辖市食品药品监督管理局(药品监督管理局): 为进一步规X化妆品行政许可工作,提高化妆品卫生质量安全控制水平,加强化妆品生产经营卫生监督,指导化妆品产品技术要求编制工作,国家食品药品监督管理局组织制定了《化妆品产品技术要求规X》,现予印发,请遵照执行。 附件:1.国家食品药品监督管理局化妆品产品技术要求(文本格式)2.化妆品产品技术要求编制指南 国家食品药品监督管理局二○一○年十一月二十六日 化妆品产品技术要求规X 一、根据《化妆品卫生监督条例》,为进一步规X化妆品行政许可工作,提高化妆品卫生质量
安全控制水平,加强化妆品生产经营卫生监督,保障消费者使用安全,制定本规X。 二、国家食品药品监督管理局负责批准化妆品产品技术要求,并监督其执行。 三、化妆品产品技术要求应当符合国家有关法律法规、标准规X。 四、化妆品产品技术要求应符合其文本格式的规定。文本格式应当包括产品名称、配方成分、生产工艺、感官指标、卫生化学指标、微生物指标、检验方法、使用说明、贮存条件、保质期等序列(见附件1),并按照《化妆品产品技术要求编制指南》(见附件2)编制。 五、化妆品产品技术要求是产品卫生质量安全的技术保障。生产企业应当按照化妆品产品技术要求组织生产经营,食品药品监督管理部门应当将化妆品产品技术要求作为开展卫生监督执法的重要依据。 六、化妆品产品技术要求适用于化妆品新产品的许可和产品延续。 七、化妆品产品技术要求编号。国产特殊用途化妆品按照HZ+GT+年份+0000编制;进口特殊用途化妆品按照HZ+JT+年份+0000编制;进口非特殊用途化妆品按照HZ+JF+年份+0000编制。"HZ"表示"化妆品","GT"表示"国产特殊用途","JT"表示"进口特殊用途","JF"表示"进口非特殊用途","年份+0000"为化妆品批准文号(或备案号)的年份和顺序号。 八、本规X自2011年4月1日起施行。 附件1 国家食品药品监督管理局化妆品产品技术要求(文本格式)(产品技术要求编号)_______