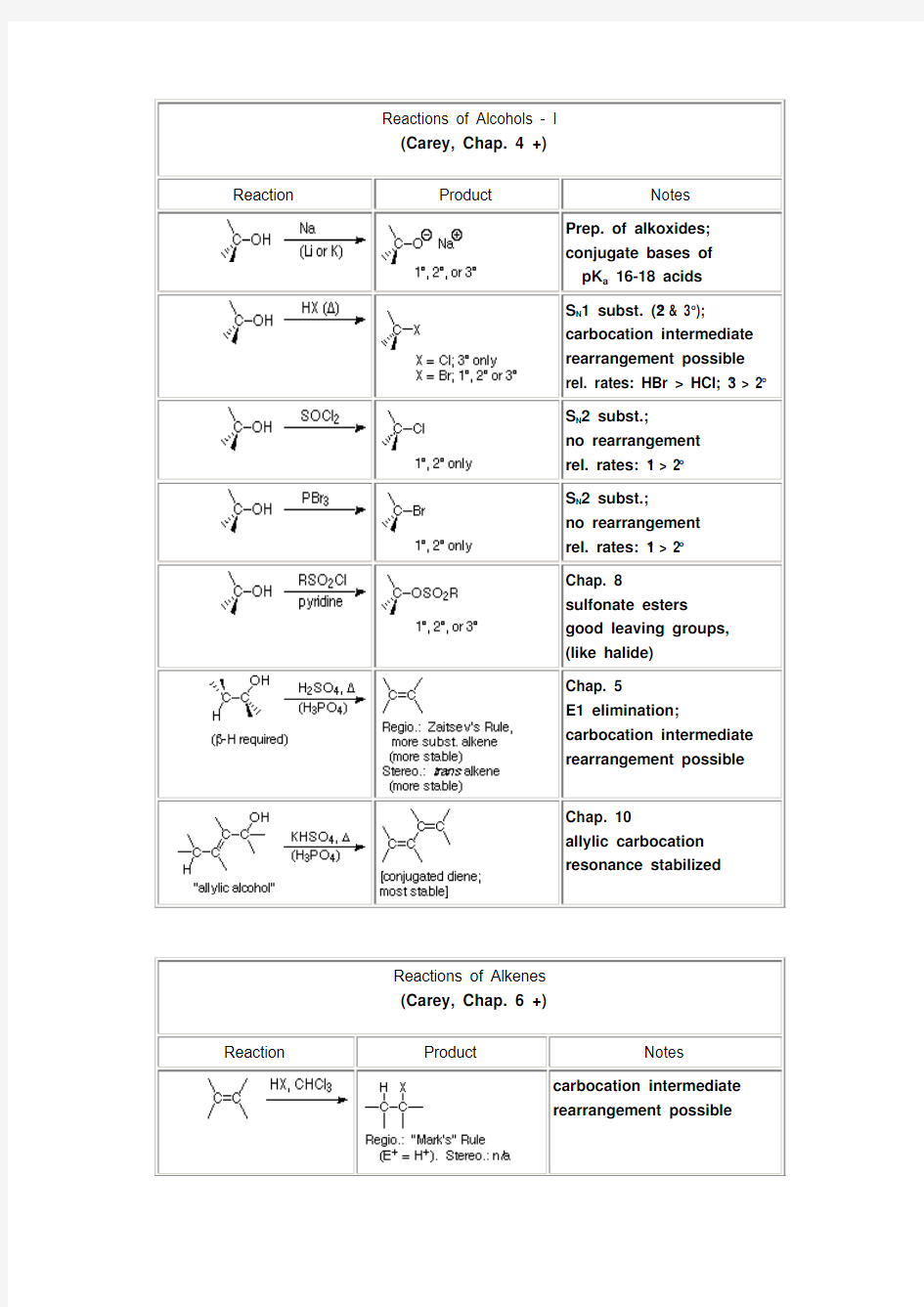

有机反应类型与官能团之间的转化 一、有机化学反应类型归纳 1.取代反应:有机物分子里的某些原子或原子团被其他原子或原子团所代替的反应。包括:卤代反应、硝化反应、磺化反应、卤代烃的水解反应、酯化反应、酯的水解反应、醇分子间脱水反应等。 2.加成反应:有机物分子中不饱和的碳原子跟其他原子或原子团直接结合生成新的化合物的反应。包括:与氢气的加成反应 (烯、二烯、炔的催化加氢;苯、苯的同系物、苯乙烯催化加氢;醛、酮催化加氢;油脂的加氢硬化)|、与卤素单质的加成反应、与卤化氢的加成反应、与水的加成反应等。 3.脱水反应:有机物在适当条件下,脱去相当于水的组成的氢氧元素的反应。包括分子内脱水(消去反应)和分子间脱水(取代反应)。 4.消去反应:有机物在适当条件下,从一个分子脱去一个小分子(如水、HX等),而生成不饱和(双键或三键)化合物的反应。包括醇的消去反应和卤代烃的消去反应。 5.水解反应:广义的水解反应,指的凡是与水发生的反应,中学有机化学里能够与水发生水解反应的物质,一般指的卤代烃水解、酯的水解、油脂的水解(含皂化)、糖类的水解、肽及蛋白质的水解等。 6.氧化反应:指的是有机物加氧或去氢的反应。包括: (1)醇被氧化:羟基的O—H键断裂,与羟基相连的碳原子的C—H键断裂,去掉氢原子形成C=O键。注意:叔醇(羟基所在碳原子上无H)不能被氧化: ; (2)醛被氧化:醛基的C—H键断裂,醛基被氧化成羧基: ; (3)乙烯氧化:2CH2=CH2+O22CH3CHO; (4)有机物的燃烧、不饱和烃和苯的同系物使酸性KMnO4溶液褪色等。 (5)醛类及含醛基的化合物与新制碱性Cu(OH)2或银氨溶液的反应; (6)苯酚在空气中放置转化成粉红色物质(醌)。 7.还原反应:指的是有机物加氢或去氧的反应。包括: (1)醛、酮、烯、炔、苯及其同系物、酚、不饱和油脂等的催化加氢。 (2) C6H5-NO2 + 3Fe + 6HCl → C6H5-NH2 + 3FeCl2 + 2H2O 8.酯化反应:酸和醇作用生成酯和水的反应。 9.聚合反应:是指由小分子单体相互发生反应生成高分子化合物的反应。包括加聚反应和缩聚反应。 10.裂化反应:在一定条件下,把相对分子质量大、沸点高的长链烃,断裂为相对分子质量小、沸点低的短链烃的反应。深度裂化叫裂解。 11.显色反应、颜色反应: (1)苯酚溶液滴加氯化铁溶液——显紫色。 (2)淀粉溶液加碘水——显蓝色。 (3)蛋白质(分子中含苯环的)加浓硝酸——显黄色 二、官能团之间的转化知识梳理
有机合成中有机物官能团的引入、消除和转化方法 1.官能团的引入 2.官能团的消去 (1)通过加成反应消除不饱和键。 (2)通过消去反应、氧化反应或酯化反应消除羟基(—OH)。 (3)通过加成反应或氧化反应消除醛基(—CHO)。 (4)通过消去反应或水解反应消除卤素原子。 3.官能团的转化 (1)利用衍变关系引入官能团,如卤代烃水解取代伯醇(RCH 2OH)氧化还原醛――→氧化 羧酸。 (2)通过不同的反应途径增加官能团的个数,如 (3)通过不同的反应,改变官能团的位置,如 有机合成中碳架的构建 1.有机成环反应 (1)有机成环:一种是通过加成反应、聚合反应来实现的;另一种是通过至少含有两个相同或不同官能团的有机物脱去小分子物质来实现的。如多元醇、羟基酸、氨基酸通过分子内或分子间脱去小分子水等而成环。 (2)成环反应生成的五元环或六元环比较稳定。 2.碳链的增长 有机合成题中碳链的增长,一般会以信息形式给出,常见的方式如下所示。 (1)与HCN 的加成反应 (2)加聚或缩聚反应,如n CH 2 (3)酯化反应,如CH 3CH 2OH +CH 3COOH 浓 CH 3COOCH 2CH 3+H 2O 。 3.碳链的减短 (1)脱羧反应:R —COONa +NaOH ――→CaO △R —H +Na 2CO 3。
(3)水解反应:主要包括酯的水解、蛋白质的水解和多糖的水解。 (4)烃的裂化或裂解反应:C 16H 34――→高温C 8H 18+C 8H 16; C 8H 18――→高温 C 4H 10+C 4H 8。 合成路线的选择 1.中学常见的有机合成路线 (2)一元合成路线 R —CH=CH 2――→HX 卤代烃――→NaOH 水溶液△一元醇――→氧化一元醛――→氧化一元羧酸―→酯 (3)二元合成路线 CH 2=CH 2――→X 2CH 2X-CH 2X ――→NaOH 水溶液△二元醇――→氧化二元醛――→氧化二元羧酸→???? ? 链酯环酯 高聚酯 (3)芳香化合物合成路线: 2.有机合成中常见官能团的保护 (1)酚羟基的保护:因酚羟基易被氧化,所以在氧化其他基团前可以先使其与NaOH 反应,把—OH 变为—ONa(或—OCH 3)将其保护起来,待氧化后再酸化将其转变为—OH 。 (2)碳碳双键的保护:碳碳双键也容易被氧化,在氧化其他基团前可以利用其与HCl 等的加成反应将其保护起来,待氧化后再利用消去反应转变为碳碳双键。 (3)氨基(—NH 2)的保护:如在对硝基甲苯――→合成 对氨基苯甲酸的过程中应先把—CH 3氧化成—COOH 之后,再把—NO 2还原为—NH 2。防止当KMnO 4氧化—CH 3时,—NH 2(具有还原性)也被氧化。 有机合成中有机物官能团的引入、消除和转化方法 练习 【例1】 工业上用甲苯生产对羟基苯甲酸乙酯( ),其过程如下: 据合成路线填写下列空白: (1)有机物A 的结构简式:____________________________________________________, B 的结构简式:_____________________________________________________________。 (2)反应④属于__________反应,反应⑤属于____________反应。 (3)③和⑥的目的是__________________________________________________________。 (4)写出反应⑥的化学方程式:_________________________________________________。 【例2】 由环己烷可制备1,4-环己醇二醋酸酯。下面是有关的8步反应(其中所有无机产物都已略去)。
i 5-7-g f e d c b a e d c b a i h g f e d c b a h g f e d c b a h g f e d c b a 6-4-3-1-2-i h g f e d c b a C=C -C(O)-CH 3 CH-CH CH-CX F u n c t i o n a l G r o u p I n t e r c o n v e r s i o n C=C C C C=C C C RCH 2-SO 2Ph RC CH C C C-NH 2; C-NO 2C-OH C(OR)2; C(SR)2C=C-OR; C=C-SR C C C N C=N-OH, C=N-H C=S C=O C=O C-C(O)Z C=C C=O C-OH C-X C-N C-H C-N C=O C---OH C-OC(O)R C-X C-OCH 2OR C-NH 2 C-OR C-H C-OH C=C C-H C(O)OR C-(OR)2C-OH C-OR C-CHO C-CO 2H C-CN C=C C=O C-S C-X C-OH C-H C=C j C(O)X h C N j k C-H C-Br 8-C-X i C-OH C-OH C(O)Z d c b a e d c b a f C-NH 2C-H j CX-CY C C X C=O h g f i C CH RCH(CO 2H)-CH 3-C(O)-CH 3 O O O X CRR'=CHX j C O C-NH 2C-CN 9-C-CH 3 C-X a e C=O
1-a dry pyridine: from CaH 2 and distilled triflate mesylate tosylate S O O O RCH 2CF 3 S O O O RCH 2CH 3 CH 3 CH 3 CH 3 OH (2). for 3' alcohol: LiAlH 4 (1). for 1', 2' alcohol: 1-i h g f e d c b a C-CHO C-CO 2H C-CN C=C C=O C-S C-NH 2C-X C-OH C-H CH 3 CH 3 CH 3 H n -Bu SnH C S O Ph Cl RCH 2-H CH 3 S O O O RCH 2CH 3 S O O Cl RCH 2OH purification textbook ~ $ 30 / Kg toluenesulfonyl chloride (s)methanesulfonyy chloride (l)~ $ 30 / Kg j C(O)X Ph 2SiHCl / InCl 3 Ph Ph Ph Ph JOC, 2001, 66, 7741. ii. Ph 2SiHCl / InCl 3 i. p -TsCl // LiAlH 4 i. ClC(S)OPh // n -Bu 3SnH Cl 2 via: a unique Lewis acid catalyst, acceleratedeoxgyenation InCl 3 indium trichloride ii. Et 3SiH / Lewis acid J. Org. Chem. 2000, 65, 6179 JOC, 2000, 65, 6179. CHCl 2rt, 3 hr
有机合成中有机物官能团的引入、消除和转化方法1.官能团的引入
2.官能团的消去 (1)通过加成反应消除不饱和键。 (2)通过消去反应、氧化反应或酯化反应消除羟基(—OH)。 (3)通过加成反应或氧化反应消除醛基(—CHO)。 (4)通过消去反应或水解反应消除卤素原子。 3.官能团的转化 (1)利用衍变关系引入官能团,如卤代烃水解 取代伯醇(RCH2OH) 氧化 还原醛――→ 氧化 羧酸。 (2)通过不同的反应途径增加官能团的个数,如 (3)通过不同的反应,改变官能团的位置,如
有机合成中碳架的构建 1.有机成环反应 (1)有机成环:一种是通过加成反应、聚合反应来实现的;另一种是通过至少含有两个相同或不同官能团的有机 物脱去小分子物质来实现的。如多元醇、羟基酸、氨基酸通过分子内或分子间脱去小分子水等而成环。 (2)成环反应生成的五元环或六元环比较稳定。 2.碳链的增长 有机合成题中碳链的增长,一般会以信息形式给出,常见的方式如下所示。 (1)与HCN的加成反应 (2)加聚或缩聚反应,如n CH2 (3)酯化反应,如CH3CH2OH+CH3COOH浓CH3COOCH2CH3+H2O。
3.碳链的减短 (1)脱羧反应:R —COONa +NaOH ――→CaO △R —H +Na 2CO 3。 (3)水解反应:主要包括酯的水解、蛋白质的水解和多糖的水解。 (4)烃的裂化或裂解反应:C 16H 34――→高温C 8H 18+C 8H 16; C 8H 18――→高温 C 4H 10+C 4H 8。 合成路线的选择 1.中学常见的有机合成路线 (1)一元合成路线: 卤代烃――→NaOH/H 2O △一元醇―→一元醛―→一元羧酸―→酯 (2)二元合成路线: ――→NaOH/H 2O 二元醇―→二元醛―→二元羧酸―→????? 链酯环酯 高聚酯 (3)芳香化合物合成路线: 2.有机合成中常见官能团的保护 (1)酚羟基的保护:因酚羟基易被氧化,所以在氧化其他基团前可以先使其与NaOH 反应,把—OH 变为—ONa(或—OCH 3)将其保护起来,待氧化后再酸化将其转变为—OH 。 (2)碳碳双键的保护:碳碳双键也容易被氧化,在氧化其他基团前可以利用其与HCl 等的加成反应将其保护起来,待氧化后再利用消去反应转变为碳碳双键。 (3)氨基(—NH 2)的保护:如在对硝基甲苯――→合成 对氨基苯甲酸的过程中应先把—CH 3氧化成—COOH 之后,再把—NO 2还原为—NH 2。防止当KMnO 4氧化—CH 3时,—NH 2(具有还原性)也被氧化。 有机合成中有机物官能团的引入、消除和转化方法 练习
JA C S, 1972, 94, 7159. L A H ------------ alm ost all: ald, ketone, acie, ester, acyl X, anhydride N aB H4 --------------- not for acid, ester (but L iB H4 w ork for ester) B2H6 --------------- not for ester, acyl X, anhydride; from top: L iA lH4; N aB H4; N a / N H3 A l (O i Pr)3 / i PrO H ----------- M eerw ein-Pondorf-V erley rxn IrC l4 / i P rO H / P(O M e)3 ------ H enbest rxn L iB H(sec Bu)3 ------------------ H. C. B row n from bottom: (2). stereoselective: (1). regioselective: 3-h (3). H C H O reagent: M e C H O M e O H H C H O JA C S, 1935, 511, 903. C H3C H O C(C H2O H)4 2 O rg.Syn, 1925, 4, 53. H C H O / K O H H C H O / C a(O H)2 S ynthesis, 1994, 1007. Ph N O2 O Ph N O2 H O H B H / SM e JO C, 2001, 66, 7514. JO C, 2003, 68, 2030. O B H3 / T H F 99.5 % trans solvent: T H F, S M e2 3-i R3B, H O C H2C H2O H // H2O2 // N aO H JO C, 1986, 51, 4925. C O R R R3B R R R R R3C B O H O C H2C H2O H R3C B O O H2O2 O H R3 H O B O O R3C H2O R3C O H
用于备课的资料 各类有机物的转化关系图: 1. 常见官能团与性质 官能团结构性质 碳碳双键易加成、易氧化、易聚合 碳碳三键易加成、易氧化、易聚合 卤素(X=Cl、Br等) 易取代(如溴乙烷与NaOH水溶液共热生成乙醇)、易消去(如 溴乙烷与NaOH醇溶液共热生成乙烯) 醇羟基易取代、易消去(如乙醇在浓硫酸、170℃条件下生成乙烯)、易催化氧化(如乙醇在酸性K2Cr2O7溶液中被氧化为乙醛甚至乙酸) 酚羟基极弱酸性(酚羟基中的氢与NaOH溶液反应,但酸性极弱,不能使指示剂变色)、易氧化(如无色的苯酚晶体易被空气中的氧气氧化为粉红色)、显色反应(如苯酚遇FeCl3溶液呈紫色)、苯酚遇浓溴水产生白色沉淀 醛基易氧化(如乙醛与银氨溶液共热生成银镜)
羰基 易还原(如在Cu/Ag 催化加热条件下还原为)羧基 酸性(如乙酸的酸性强于碳酸,乙酸与NaOH溶液反应)、易取 代(如乙酸与乙醇在浓硫酸、加热条件下发生酯化反应) 酯基 易水解(如乙酸乙酯在稀硫酸、加热条件下发生酸性水解, 乙酸乙酯在NaOH溶液、加热条件下发生碱性水解) 烷氧基如环氧乙烷在酸催化下与水一起加热生成乙二醇 硝基还原(如酸性条件下,硝基苯在铁粉催化下还原为苯胺) 2. 有机反应类型与重要的有机反应 反应类型重要的有机反应 取代反应烷烃的卤代:CH4+Cl2CH3Cl+HCl 烯烃的卤代: 卤代烃的水解:CH3CH2Br+NaOH CH3CH2OH+NaBr 皂化反应:+3NaOH3C17H35COONa+ 酯化反应:+C2H5OH+H2O 糖类的水解: 122211 C H O 蔗糖+H2O 6126 C H O 果糖+ 6126 C H O 葡萄糖 二肽的水解:+H2O 取代反应 苯环上的卤代:+Cl2+HCl 苯环上的硝化:++H2O 苯环上的磺化:++H2O (续表)
官能团相互转换 d 7- e 7- i. W C l 6 / R Li ii. LiPPh 2 / C H 3I product retention product inversion N a R C C H C H 2C H 2C H 2O H O C l R iii. N a (special structure): 7-d.1 7-d.S R 1 R 2 R 1 R 2 (E tO )3P use: (E tO )3P Synthesis , 1977, 1134. via : betaine, oxaphosphetane (N M R )O not good for Ph 3P=C H 2function as base: expensive difficult to prepare O E t C N PPh 3 C N PPh 3 H O PPh 3O C O 2M e + not Ph 3P C H E t H C O C O 2M e not Ph 3P C H C O 2M e E t H O + +++stable ylid gives trans (E ) unstable ylid gives cis (Z )w ater soluble, rem oved by extraction (com parison: O =PPh 3 highly soluble in organic solvent) use:L i Ph S O N M e C H 2// A l (H g) M e 3SiC H R -L i + Ph 3SiC H 2-L i + === Ph 3SiC H 2B r + n-B uL i (exchange)M e 3SiC -H -M gB r === M e 3SiC H 2C l + M g (m etal reduction) Ph 3SiC - H C H 2Ph === Ph 3SiC H =C H 2 + PhL i (addition to vinylsilane)M e 3SiC -H C O 2E t === M e 3SiC H 2C O 2E t + L i (m etalation)M e 3SiC H =PPh 3 === M e 3SiC H 2PPh 3+ X - + K H R O = M eO -, E tO -use: (R O )2PO -C H R ' use: Ph 3P-C H R 'vi. Sulfoxim ide (Johnson C.) iii. Silyl W ittig R eaction (Peterson R eaction) ii. Phosphonate W ittig R eaction (H orner-Em m ons M odification) i. W ittig R eaction 7-f 7-f.Synthesis, 1984, 384. TH L, 1981, 2751. JO C , 1968, 33, 780. iv. C H 2(ZnI)2 C hem. L ett, 1995, 259. Synlett, 1988, 12, 1369. H 2 C H 2(Z nI)2 v. C H 2C H B r 2, Sm , SnI 2 / C rC l 3, TH F R O R vii. G rignard reagent: 1. T M SC H 2M gC l use: T M SC H 2M gC l TH L, 1973, 3497. TH L , 1988, 4339. 2. N aO A c, A cO H m ethylenation O R R ' e 3 H advantages over the W ittig: 1. by-products are m ore easily rem oved, 2. reaction suffers less from steric effects. via: (olefination reaction) 1953 discover
官能团转换 利用有机物的化学反应实现官能团转换是制备有机化合物的基本方法。 一、转换成碳-碳双键的方法 1.醇的消除反应 C H C OH C C+ H2O H2SO4 活性顺序:叔醇>仲醇>伯醇;反应遵循札依采夫规律。2.卤代烷的消除反应 C H C X C C+ HX NaOH/ROH 活性顺序:叔卤代烷>仲卤代烷>伯卤代烷;反应遵循札依采夫规律。3.季铵碱的消除反应 C H C NR3OH C C+ NR3 + H2O 反应遵循霍夫曼规律(得到双键上取代最少的烯烃)。 二、转换成碳-碳叁键的方法 二卤代烷或卤代烯烃的消除反应 C H H C X X C C+ HX NaOR/ROH C H C X
三、转换成碳-卤键的方法 1. 烷烃的取代反应 C H hv X 2C X + HX 活性顺序:叔碳H 、烯丙式H 、苄基H > 仲碳H > 伯碳H ; Cl 2>Br 2。 反应条件:光照、高温、过氧化物。 2. 烯烃、炔烃的加成反应 C H C X C C HX C X C X C C X 2 C C HX C C H H X X C C H X HX C C X 2C C X X X X C C X X X 2 3. 芳烃的取代反应 X 2FeX 3 X 4. 醇的取代反应 C OH HX 或PX 3 C X 活性顺序:叔醇>仲醇>伯醇;HI>HBr>HCl 。 5. 重氮盐的取代反应 N N X CuX X :Cl 、Br ,I 取代时用KI 。
四、转换成羟基的反应 1. 卤代烷的水解反应 NaOH/H 2O C OH C X 活性顺序:碘代烷>溴代烷>氯代烷 2. 格氏试剂与醛、酮的加成反应 C O (1)RMgX (2)H 2O C OH R 由甲醛得到伯醇、由其它醛得到仲醇、由酮得到叔醇。 3. 羰基、酯基、羧基的还原反应 C O C OH H H 2/Ni LiAlH 4或 NaBH 4 由醛得到伯醇、由酮得到仲醇。 C R' O OR CH 2OH R'H 2/Ni LiAlH 4 CH 2OH R + C R O OH LiAlH 4 CH 2OH R 4. 烯烃与水的加成反应 C H C OH C C H 2O/H 2SO 4 按马氏规则,烯烃在酸催化下加水得不到伯醇(除乙烯外);端基烯可以通过硼氢化反应得到伯醇。
3 Me2N N N CH3 H Cl 3 hν N CH3 H H N CH3 H H+ N CH3 Cl NHCH C 2 R3C NH2 R C NR2 R C NHR R3C OH R2C OH RC OH R C NH2 tertiary secondary primary Compare nomenclature class: not a very useful reaction C-N C-H C-N C-X C-OH C=O C=C 4-a b c d e f g 4-a SO2NH2Ph I OAc OAc S O O NH S O O N I Ph Fe(TPP)Cl S O O NH2 (insertion) TPP N N N N Ph 2. NaN3 N C O 1. SO2Cl2C O 2 C C O O h i C N C(O)X C-C(O)X
NH 2 2 RC NO 2 RC N 3RC N Me RC N CPh RC N CPh 3RC NH 2 RC NH 2 RC NH 2RC NH 2RC NH 2 i ii iii RC N C O OtBu RC N C O OPh RC NH 2 RC NH 24-b CF 3CO 3H // Fe / HOAc 1. many reducing agents 1. NaBH 4; 2. Al (Hg) H 2O 2 // Ac 2O, heat / H 3O +H 2 / Pd-C 1. HOAc; 2. H 2 / Pd-C 1. TFA; 2. HCl H 2 / Pd-C 4-b.14-b.2 2. organic electrochemistry 1.2.3.4.Fe 3(CO)12 / CH 3OH JOC, 1972, 37, 930.NaBH 4 / Pd-C Na 2S Sn / HCl Vogel's 12.57Vogel's 12.58 Vogel's 12.59NO 2 OCH 3 NH 2 OCH 3Eg-Ni rt. 15 hr JOC, 1999, 64, 2301. Eg-Ni: electrogenerated nickel 5.H 2 / Pt (S)-C JACS, 1965, 87, 2767. sulfided platium not affect: aromatic rings, ketones, halides, nitriles, amide, easters
用于备课的资料 各类有机物的转化关系图:1.常见官能团与性质 官能团碳碳双键碳碳三键 卤素醇羟基酚羟基 醛基 羰基 羧基 结构性质 易加成、易氧化、易聚合 易加成、易氧化、易聚合 易取代 ( 如溴乙烷与 NaOH水溶液共热生成乙醇) 、易消去 ( 如(X=Cl 、 Br等 ) 溴乙烷与 NaOH醇溶液共热生成乙烯) 易取代、易消去 ( 如乙醇在浓硫酸、 170℃条件下生成乙烯 ) 、易 催化氧化 ( 如乙醇在酸性 K2Cr2O7溶液中被氧化为乙醛甚至乙酸 ) 极弱酸性 ( 酚羟基中的氢与 NaOH溶液反应 , 但酸性极弱 , 不能 使指示剂变色 ) 、易氧化 ( 如无色的苯酚晶体易被空气中的氧气 氧化为粉红色 ) 、显色反应 ( 如苯酚遇 FeCl3溶液呈紫色 ) 、苯 酚遇浓溴水产生白色沉淀 易氧化 ( 如乙醛与银氨溶液共热生成银镜) 易还原 ( 如在Cu/Ag催化加热条件下还原为) 酸性 ( 如乙酸的酸性强于碳酸, 乙酸与 NaOH溶液反应 ) 、易取 代 ( 如乙酸与乙醇在浓硫酸、加热条件下发生酯化反应)
易水解 ( 如乙酸乙酯在稀硫酸、加热条件下发生酸性水解, 酯基 乙酸乙酯在 NaOH溶液、加热条件下发生碱性水解 ) 烷氧基如环氧乙烷在酸催化下与水一起加热生成乙二醇 硝基还原 ( 如酸性条件下 , 硝基苯在铁粉催化下还原为苯胺) 2.有机反应类型与重要的有机反应 反应类型重要的有机反应 取代反应 取代反应 反应类型加成反应烷烃的卤代 :CH4+Cl 2CH3Cl+HCl 烯烃的卤代 : 卤代烃的水解 :CH3CH2Br+NaOH CH3CH2OH+NaBr 皂化反应 :+3NaOH3C17H35COONa+ 酯化反应 : +CH OH +H O 2 5 2 糖类的水解 : C 12 H 22 O 11 +HO C 6 H 12 O 6 + C 6 H 12 O 6 蔗糖果糖葡萄糖 2 二肽的水解 :+H2O 苯环上的卤代 :+Cl 2+HCl 苯环上的硝化 :++H2O 苯环上的磺化 :++H2O ( 续表 ) 重要的有机反应 烯烃的加成 :+HCl
1 i 5-7-g f e d c b a e d c b a i h g f e d c b a h g f e d c b a h g f e d c b a 6-4-3-1-2-i h g f e d c b a C =C -C(O )-C H 3C H -C H C H -C X Functiona l G roup Interconversion C =C C C C =C C C R C H 2-SO 2Ph R C C H C C C -N H 2; C -N O 2C -O H C (O R )2; C (SR )2C =C -O R ; C =C -SR C C C N C =N -O H , C =N -H C =S C =O C =O C -C (O )Z C =C C =O C -O H C -X C -N C -H C -N C =O C ---O H C -O C (O )R C -X C -O C H 2O R C -N H 2 C -O R C -H C -O H C =C C -H C (O )O R C -(O R )2C -O H C -O R C -C H O C -C O 2H C -C N C =C C =O C -S C -X C -O H C -H C =C j C (O )X h C N j k C -H C -B r 8-C -X i C -O H C -O H C (O )Z d c b a e d c b a f C -N H 2C -H j C X -C Y C C X C =O h g f i C C H R C H (C O 2H )-C H 3-C(O )-C H 3 O O O X C R R '=C H X j C O C -N H 2C -C N 9-C -C H 3 C -X a e C =O
一、有机物间相互转化关系
二、能与溴水发生化学反应而使溴水褪色或变色的物质 1、有机物: ⑴ 不饱和烃(烯烃、炔烃、二烯烃等) ⑵ 不饱和烃的衍生物(烯醇、烯醛、烯酸、烯酯、油酸、油酸酯等) ⑶ 石油产品(裂化气、裂解气、裂化汽油等) ⑷ 含醛基的化合物(醛、甲酸、甲酸盐、甲酸酯、葡萄糖、麦芽糖等) ⑸ 天然橡胶(聚异戊二烯) 2、无机物: ⑴ -2 价的 S (硫化氢及硫化物) ⑵ + 4 价的 S (二氧化硫、亚硫酸及亚硫酸盐) ⑶ + 2 价的 Fe 6FeSO 4 + 3Br 2 = 2Fe 2(SO 4)3 + 2FeBr 3 6FeCl + 3Br 2 = 4FeCl + 2FeBr 变色 2FeI 2 3 3 + 3Br 2= 2FeBr + 2I 2 2 3 △ ⑷ Zn 、 Mg 等单质 如Mg + Br 2 Mg 与 H + 、Mg 与 HBrO 的反应) === MgBr 2 (其中亦有 ⑸ -1 价的 I (氢碘酸及碘化物)变色 ⑹ NaOH 等强碱、 Na 2CO 3 和 AgNO 3 等盐 Br 2 + H 2O = HBr + HBrO 2HBr + Na 2CO 3 = 2NaBr + CO 2↑+ H 2O HBrO + Na 2CO 3 = NaBrO + NaHCO 3 三、能萃取溴而使溴水褪色的物质 上层变无色的(ρ >1):卤代烃( CCl 4、氯仿、溴苯等)、 CS 2 等; 下层变无色的(ρ <1):直馏汽油、煤焦油、苯及苯的同系物、低级酯、液态环烷烃、液态饱 和烃(如己烷等)等 四、能使酸性高锰酸钾溶液褪色的物质 1、有机物: ⑴ 不饱和烃(烯烃、炔烃、二烯烃等) ⑵ 不饱和烃的衍生物(烯醇、烯醛、烯酸、烯酯、油酸、油酸酯等) ⑶ 石油产品(裂化气、裂解气、裂化汽油等) ⑷ 醇类物质(乙醇等) ⑸ 含醛基的化合物(醛、甲酸、甲酸盐、甲酸酯、葡萄糖、麦芽糖等) ⑹ 天然橡胶(聚异戊二烯) ⑺ 苯的同系物
主题5 有机合成 第 1 讲各类有机物之间的相互转化 【考点直击】 1.掌握各类有机物的化学性质及相互转化关系。 2.掌握有机反应的基本类型。 【三基建构】 一、各类有机物的化学性质。 1.将下列一些有机物可能具有的主要化学性质用编号填入下表中: ⑴酯化⑵卤代⑶硝化⑷水解⑸加成⑹消去⑺催化氧化⑻酸性KMnO4氧化 2 ⑴烯、炔和芳香烃与氢气加成也可认为反应。 ⑵炔烃与烯烃相比,聚合。 ⑶对于苯的同系物卤代时,光照,发生取代反应,有催化剂存在发生取代反应。 ⑷苯被KMnO4酸性溶液氧化,苯的同系物分子中的可被KMnO4酸性溶液氧化。 ⑸醇的卤代不是与卤素单质发生反应,而是与发生反应。 ⑹酚暴露在空气中。 ⑺醛能被等弱氧化剂氧化,当然也能被KMnO4、K2Cr2O7等强氧化剂氧化。 ⑻油脂在酸性条件下水解得到,油脂在氢氧化钠溶液中水解得到_ , 油脂在碱性条件下的水解又称为__。 ⑼不饱和高级脂肪酸甘油酯能与H2作用生成__,该反应又叫_。 ⑽常见的糖中,具有还原性的有。 ⑾淀粉与碘相遇会显,颜色反应一般用于。 二、常见重要有机物的相互转化 1.在物质间用箭号表示其转化关系并注明反应类型
2.根据以上转化关系小结如下内容: ⑴在有机物中引入碳碳双键的方法 ⑵在有机物中引入卤原子的方法 ⑶在有机物中引入羟基的方法 三、影响有机物化学性质的因素 1. 请举例说明官能团之间的影响。 2. 请举例说明反应条件对化学反应的影响。 四、有机合成的过程与分析方法 1.通过练习归纳:从分子结构看,在有机合成中,原料分子与目标分子发生了什么变化? 2.通过练习归纳:有机合成的分析方法。 3.通过练习归纳:在解有机合成有关问题时,通常需要思考哪些问题? 【真题链接】 例1 (1999·上海)下列物质能溶于水的是( ) A .HOCH 2CHCHCHCHCHO OH B .CH 2OH C . O H R D .CH 3CH 2CH 2CH =CH 2
O 有机官能团鉴别大全 引 言 用于定性鉴别官能团的化学反应必须满足下述条件: 1. 化学反应发生前后,有颜色变化。 2. 化学反应发生前后,有相的变化(有气体放出、或有沉淀生成、或沉淀溶解、或反应前成均相反应后分层、或反应发生前分层反应后成均相)。 1. KMnO 4法 [概述] 第一节 烷 烃 无鉴别反应 第二 节 烯 烃 碳碳双键与KMnO 4的酸性或碱性水溶液发生氧化还原反应使KMnO 4溶液颜色褪 去。在中性或碱性介质中,还有黑褐色的MnO 2沉淀产生。例如, ? ? ? ? ? ? ? ? ? ? ? P 4 ? ? ? ? ? ? ? ? ? ? 2 + ? ? ? OP ? ? P ? ? ? ? ? ? ? H + ? H P ) 2C O ? ? 2 2. Br 2 / CCl 4法 [概述] ? ? 3? ? ? 2 ? ? P ? + ? ? ? ? ? + ? ? ? 碳碳双键与Br 2的四氯化碳溶液发生亲电加成反应使溴的红棕色褪色。 [反应式] 3. 冷浓H 2SO 4法 [概述] ? C ? ? ? 2 ? ? P ? ? C ? ? 碳碳双键与冷浓硫酸发生亲电加成反应生成硫酸氢烷基酯而使反应混合液成均相。 [反应式] ? ? ? ? OP 2? 例如, ? ? ? ? P ? ? ? ? P C H ? F ? ? ? OP 2? ? ? ?? F H 4 ? C
2 3 2 本法适合于常温下为液体的烯烃。 第三节 炔 烃 1. KMnO 4/H 2SO 4法 [概述] 碳碳叁键与KMnO 4/H 2SO 4发生氧化- 还原反应,而使KMnO 4紫色褪去,末端炔烃有二氧化碳放出。 [反应式] ? ? nO ? ? ? ? ? ? 4 ? ? ? ' P ? OP 2 H + ? ? P H 2 ? ? KM nO 4/ H 2SO ? ? O P H + ? 2. Br 2 / CCl 4法 [概述] 炔烃与Br 2 / CCl 4发生亲电加成反应,使溴的橙色褪去。 [反应式] 3. Ag(NH 3)2 +法。 ? ? C ? + 2 ? ? ? ? ? P 4 ? C ? ? [概述] 末端炔烃与Ag(NH 3)2 +作用,产生炔银沉淀(白)。 [反应式] ? ? ? ? ? ? ? ? ? P ? ? ? ? ? ? ? P 4. Cu(NH ) + 法 [概述] 末端炔烃与Cu(NH 3)2 +作用,产生炔铜沉淀(棕红色)。 [反应式] ? ? + ? ? H P 3) 2+ ? ? uP [例1] 用化学方法鉴别化合物[1][2][3][4]。 ? ] P ? ] P ? ] P ? ? P ?? ? ?P ? P ? ? P ? ? P ? ? ? ? < ? ? ? ? P ? ? P ? ? P ? ? ?? ? ? ? P ? P ? P ? P ? ? ? ?
有机反应类型与官能团之间的转化 黑龙江省庆安一中孙秀民 一、有机化学反应类型归纳 1.取代反应:有机物分子里的某些原子或原子团被其他原子或原子团所代替的反应。包括:卤代反应、硝化反应、磺化反应、卤代烃的水解反应、酯化反应、酯的水解反应、醇分子间脱水反应等。 2.加成反应:有机物分子中不饱和的碳原子跟其他原子或原子团直接结合生成新的化合物的反应。包括:与氢气的加成反应 (烯、二烯、炔的催化加氢;苯、苯的同系物、苯乙烯催化加氢;醛、酮催化加氢;油脂的加氢硬化)|、与卤素单质的加成反应、与卤化氢的加成反应、与水的加成反应等。 3.脱水反应:有机物在适当条件下,脱去相当于水的组成的氢氧元素的反应。包括分子内脱水(消去反应)和分子间脱水(取代反应)。 4.消去反应:有机物在适当条件下,从一个分子脱去一个小分子(如水、HX等),而生成不饱和(双键或三键)化合物的反应。包括醇的消去反应和卤代烃的消去反应。 5.水解反应:广义的水解反应,指的凡是与水发生的反应,中学有机化学里能够与水发生水解反应的物质,一般指的卤代烃水解、酯的水解、油脂的水解(含皂化)、糖类的水解、肽及蛋白质的水解等。 6.氧化反应:指的是有机物加氧或去氢的反应。包括:
(1)醇被氧化:羟基的O—H键断裂,与羟基相连的碳原子的C—H键断裂,去掉氢原子形成C=O键。注意:叔醇(羟基所在碳原子上无H)不能被氧化: ; (2)醛被氧化:醛基的C—H键断裂,醛基被氧化成羧基: ; (3)乙烯氧化:2CH2=CH2+O22CH3CHO; (4)有机物的燃烧、不饱和烃和苯的同系物使酸性KMnO4溶液褪色等。 (5)醛类及含醛基的化合物与新制碱性Cu(OH)2或银氨溶液的反应; (6)苯酚在空气中放置转化成粉红色物质(醌)。 7.还原反应:指的是有机物加氢或去氧的反应。包括: (1)醛、酮、烯、炔、苯及其同系物、酚、不饱和油脂等的催化加氢。 (2) C6H5-NO2 + 3Fe + 6HCl → C6H5-NH2 + 3FeCl2 + 2H2O 8.酯化反应:酸和醇作用生成酯和水的反应。 9.聚合反应:是指由小分子单体相互发生反应生成高分子化合物的反应。包括加聚反应和缩聚反应。 10.裂化反应:在一定条件下,把相对分子质量大、沸点高的长链烃,断裂为相对分子质量小、沸点低的短链烃的反应。深度裂化叫裂解。 11.显色反应、颜色反应: (1)苯酚溶液滴加氯化铁溶液——显紫色。 (2)淀粉溶液加碘水——显蓝色。
官能团转化全图解
Lemsay 第 2 页 2021-3-8
Lemsay 第 3 页 2021-3-8
Lemsay 第 4 页 2021-3-8 i 5-7-g f e d c b a e d c b a i h g f e d c b a h g f e d c b a h g f e d c b a 6-4-3-1-2-i h g f e d c b a C=C -C(O)-CH 3 CH-CH CH-CX Functional Group Interconversion C=C C C C=C C C RCH 2-SO 2Ph RC CH C C C-NH 2; C-NO 2C-OH C(OR)2 ; C(SR)2C=C-OR; C=C-SR C C C N C=N-OH, C=N-H C=S C=O C=O C-C(O)Z C=C C=O C-OH C-X C-N C-H C-N C=O C---OH C-OC(O)R C-X C-OCH 2OR C-NH 2 C-OR C-H C-OH C=C C-H C(O)OR C-(OR)2C-OH C-OR C-CHO C-CO 2H C-CN C=C C=O C-S C-X C-OH C-H C=C j C(O)X h C N j k C-H C-Br 8-C-X i C-OH C-OH C(O)Z d c b a e d c b a f C-NH 2C-H j CX-CY C C X C=O h g f i C CH RCH(CO 2H)-CH 3-C(O)-CH 3 O O O X CRR'=CHX j C O C-NH 2C-CN 9-C-CH 3 C-X a e C=O
5-f H 3O + Hg 2+ / CH 3CN (aq) C=C-OR C=C-SR OCH 3 O H 3O + SCH 3 O Hg 2+ 3 O H 3O Hg 2+3H 3O +O O O S S S S SR SR O O OR OR 5-g Hg 2+ / H 3O +H 3O + / solv (aq)H 3O + / solv (aq)Hg 2+ / H 3O + OR OR OH OH H 3O + / solv (aq)a very common protecting group, deprotect back to ketone H C OEt OEt OEt RMgX / H 3O + H C OEt OEt OEt RMgX R C H O
N H +2 Cr 2O 7-2 N HCl .CrO 3 Ag 2O: 1. a mild oxidizing agent 2. must be freshly prepared: NaOH into AgNO 3 (aq) 3. may involve surface change, react with CO 2, light Swern oxidation: (DMSO, oxalyl chloride, Et 3N)drawback: react at low T Collins reagent: (CrO 3 - 2 Py)1. drawback: use 6 equivalent, a messy reaction 2. must be very dry, fire easily; purify by CaH 23. an old oxidizing material, isolated by Collin. i. PCC ii. PDC ix. K 2R C OH O aldehyde 1st alcohol 2nd alcohol 1st alcohol R C OH O R C R O R C H O 5-h i. PCC ii. PDC JOC, 1985, 50, 1332. N OCH 3 OH PDC (pyridinium dichormate) (H 2Cr 2O 7 + 2 Py) PCC (pyridinium chlorochromate) (Py-HCl-CrO 3) most widely used use 1 - 1.2 eq. Pfitzner-Moffatt oxidation O O Br DMSO O O O H 360 % Synth. Commun., 1986, 16, 1343. JOC, 1977, 42, 1991. Synthesis, 1981, 165.O I O OAc AcO