
氯化钠注射液灭菌工艺验证项目要求
一、验证背景
我公司申报的氯化钠注射液(10ml:90mg)灭菌工艺变更补充申请被国家局不予批准,理由是:灭菌工艺验证不全面,如未提供各取样点不同时间的温度统计数据、灭菌曲线、灭菌平台期数据等,对灭菌验证结果无法评价。
经讨论,现准备重新做氯化钠灭菌工艺变更的灭菌工艺验证,主要针对变更后的灭菌工艺即121℃15min进行验证。
二、验证对象
普药车间灭菌柜性能确认和氯化钠注射液(10ml:90mg)工艺验证同步进行。
放样产品:氯化钠注射液(10ml:90mg)
批量:1.9万支(灭菌柜10m满载能力为:244支/盘×36盘/车×2车/柜,共约17568支)
批次:三批
灭菌柜:普药车间B236-O003
灭菌条件:121℃15min
进行灯检、不印包
三、验证项目要求
1、普药车间灭菌柜性能确认
同以前做的灭菌柜性能确认相同,空载、满载热分布均运行三次。唯一不同的是此次满载样品采用氯化钠注射液(10ml:90mg)。验证所需项目如下:
1.1热分布(1)每次运行均需列出最高温度,最低温度,平均温度,F0最大值,F
最小值,对应探头位置;计算出最高温度和最低温度的温差,最高温度和平均0
温度的温差,最低温度和平均温度的温差。可列表如下:
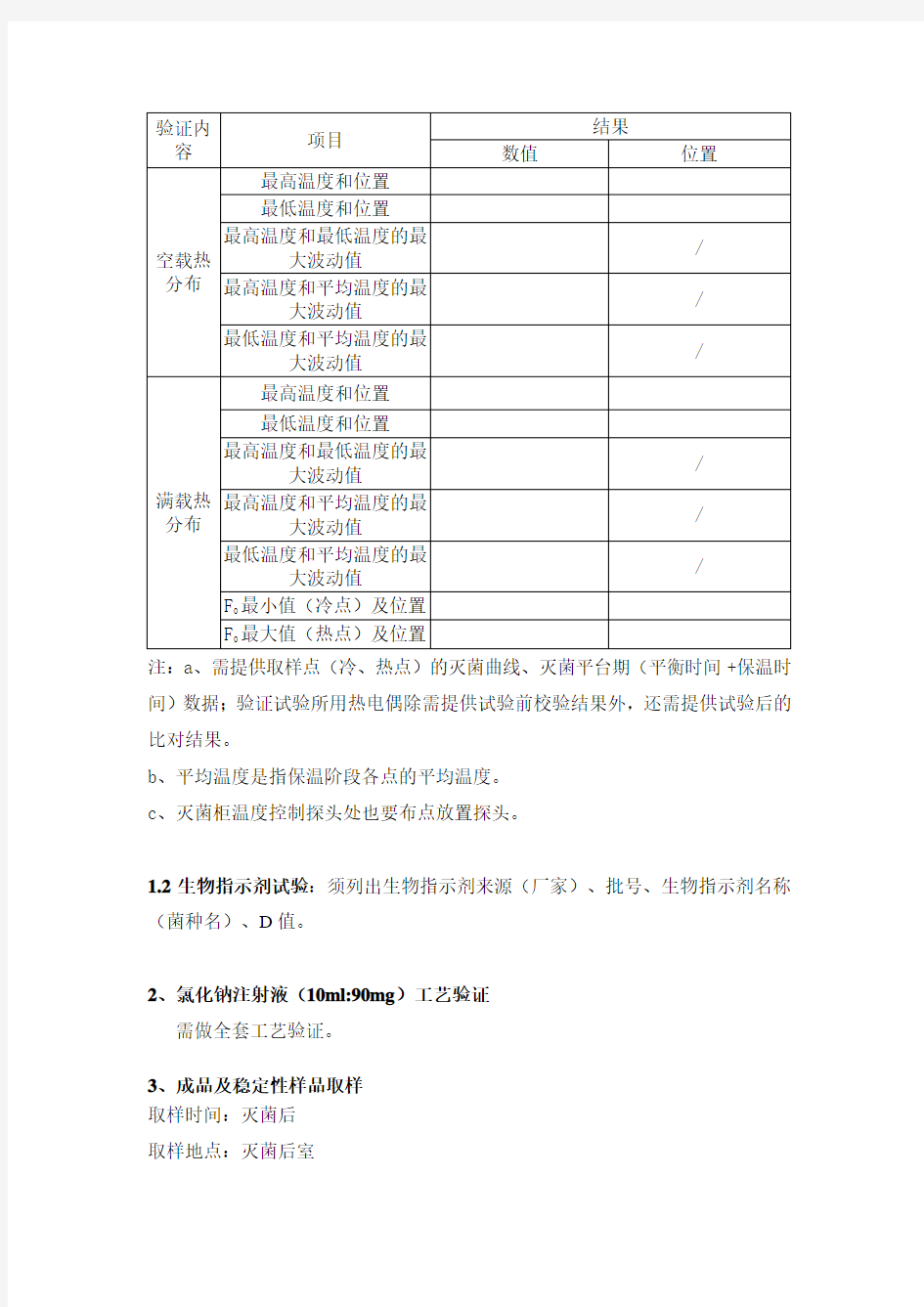
(2)最后将三次运行的数据按照下表进行总结:
验证内容项目
结果
数值位置
空载热分布
最高温度和位置
最低温度和位置
最高温度和最低温度的最
大波动值
/ 最高温度和平均温度的最
大波动值
/ 最低温度和平均温度的最
大波动值
/
满载热分布
最高温度和位置
最低温度和位置
最高温度和最低温度的最
大波动值
/
最高温度和平均温度的最
大波动值
/ 最低温度和平均温度的最
大波动值
/
F
最小值(冷点)及位置
F
最大值(热点)及位置
注:a、需提供取样点(冷、热点)的灭菌曲线、灭菌平台期(平衡时间+保温时间)数据;验证试验所用热电偶除需提供试验前校验结果外,还需提供试验后的比对结果。
b、平均温度是指保温阶段各点的平均温度。
c、灭菌柜温度控制探头处也要布点放置探头。
1.2生物指示剂试验:须列出生物指示剂来源(厂家)、批号、生物指示剂名称(菌种名)、D值。
2、氯化钠注射液(10ml:90mg)工艺验证
需做全套工艺验证。
3、成品及稳定性样品取样
取样时间:灭菌后
取样地点:灭菌后室
取样位置及对象:
位置成品测试稳定性考察样品
冷点化测20支,无菌30支/
热点化测20支,无菌30支加速样品200支,长期样品450支注:鉴于每年10ml规格121℃15min的灭菌柜性能确认的冷热点会漂移,最好将12个探头位置对应的样品取样点标记好,等验证仪数据导出得到冷热点后再取出冷点、热点的样品。
四、准备工作
请金桥设备科提前准备好灭菌柜验证方案,金桥技术科提前准备好批记录、工艺验证方案,并做好培训工作。
五、参考文献
1. 霍秀敏.欧盟灭菌方法选择决策树介绍.国家食品药品监督管理总局药品审评中心网站.2007年1月29日.
2. 已上市化学药品变更研究的技术指导原则(一).国家食品药品监督管理总局药品审评中心网站.2008年6月6日.
3.蒋煜、张豹子.注射制剂变更灭菌工艺的研究思路.国家食品药品监督管理总局药品审评中心网站.2012年4月18日.
4. 石靖、高杨、蒋煜等.注射剂灭菌/除菌工艺验证基本要求及CTD主要研究信息汇总表相关部分撰写建议.国家食品药品监督管理总局药品审评中心网站.2012年12月25日.
5. 殷志勇、王立新、蒋煜.注射剂灭菌工艺变更申请常见问题分析.国家食品药品监督管理总局药品审评中心网站.2013年4月17日.
6. 灭菌/无菌工艺验证指导原则(征求意见稿).国家食品药品监督管理总局药品审评中心网站.2013年8月20日.
7. 糖盐水相关变更的主要研究信息模板.国家食品药品监督管理总局药品审评中心网站.2014年7月15日.
8. 国家食品药品监督管理局.国家食品生产验证指南(2003).化学工业出版社.
药品微生物检验替代方法验证指导原则 本指导原则是为所采用的试验方法能否替代药典规定的方法用于药品微生物的检验提供指导。 随着微生物学的迅速发展,制药领域不断引入了一些新的微生物检验技术,大体可分为三类:(1)基于微生物生长信息的检验技术,如生物发光技术、电化学技术、比浊法等;(2)直接测定被测介质中活微生物的检验技术,如固相细胞技术法、流式细胞计数法等;(3)基于微生物细胞所含有特定组成成分的分析技术,如脂肪酸测定技术、核酸扩增技术、基因指纹分析技术等。这些方法与传统检查方法比较,或简便快速,或具有实时或近实时监控的潜力,使生产早期采取纠正措施及监控和指导优良生产成为可能,同时新技术的使用也促进了生产成本降低及检验水平的提高。 在控制药品微生物质量中,微生物实验室出于各种原因如成本、生产量、快速简便及提高药品质量等需要而采用非药典规定的检验方法(即替代方法)时,应进行替代方法的验证,确认其应用效果优于或等同于药典的方法。 微生物检验的类型及验证参数 药品微生物检验方法主要分两种类型:定性试验和定量试验。定性试验就是测定样品中是否存在活的微生物,如无菌检查及控制菌检査。定量试验就是测定样品中存在的微生物数量,如菌落计数试验。 由于生物试验的特殊性,如微生物检验方法中的抽样误差、稀释误差、操作误差、培养误差和计数误差都会对检验结果造成影响,因此,药品质量标准分析方法验证指导原则(附录XIX A)不完全适宜于微生物替代方法的验证。药品微生物检验替代方法的验证参数见表1。 表1 不同微生物检验类型验证参数 注: 尽管替代方法的验证参数与药品质量标准分析方法验证参数有相似之处,但是其具体的内容是依据微生物检验特点而设立的。替代方法验证的实验结果需进行统计分析,当替代方法属于定性检验时,一般采用非参数的统计技术;当替代方法属于定量检验时,需要采用参数统计技术。 进行微生物替代方法的验证时,若替代方法只是针对药典方法中的某一环节进行技术修改,此时,需要验证的对象仅是该项替代技术而不是整个检验方法。如无菌试验若改为使用含培养基的过滤器,然后通过适宜的技术确认活的微生物存在,那么,验证时仅需验证所用的微生物回收系统而不是整个无菌试验方法。 替代方法验证的一般要求 在开展替代方法对样品检验的适用性验证前,有必要对替代方法有一个全面的了解。首先,所选用的替代方法应具备必要的方法适用性证据,表明在不含样品的情况下,替代方法
无菌工艺模拟试验指南(无菌制剂) (征求意见稿) 国家食品药品监督管理总局 食品药品审核查验中心
二〇一六年十月 目录 1.目的 (1) 2.定义 (1) 3.范围 (1) 4.原则 (2) 5.无菌制剂生产工艺及模拟范围 (2) 6.模拟试验方案的设计及实施过程要求 (3) 6.1. 无菌工艺模拟试验的前提条件 (3) 6.2.基于风险的方案设计 (4) 6.3.模拟介质的选择与评价 (4) 6.4.灌装数量及模拟持续时间 (8) 6.5.容器装量 (9) 6.6. 模拟试验方法的选择 (9) 6.7. 最差条件的选择 (10) 6.8.干预 (12) 6.9.容器规格 (13) 6.10.培养与观察 (14) 6.11. 计数与数量平衡 (15) 6.12. 环境(包括人员)监控 (15) 6.13. 人员因素 (16) 6.14. 不同剂型应考虑的特殊因素 (16) 6.15. 方案的实施 (19) 7.可接受标准与结果评价 (20)
8.污染调查及纠正措施 (21) 9.模拟试验的周期与再验证 (21) 10.无菌工艺模拟试验的局限性 (212) 11.术语 (23) 12. 参考文献 (24)
无菌工艺模拟试验指南(无菌制剂) 1.目的 为指导和规范无菌制剂生产企业开展无菌工艺模拟试验,充分评价无菌制剂产品生产过程的无菌保障水平,确保无菌制剂的安全性,依据《药品生产质量管理规范》(2010版)及附录,制定本指南。 2.定义 本指南所述的无菌工艺模拟试验,是指采用适当的培养基或其他介质,模拟制剂生产中无菌操作的全过程,评价该工艺无菌保障水平的一系列活动。 3.范围 3.1.本指南涵盖了无菌工艺模拟试验的基本要求、不同工艺模式的相应要求、试验的基本流程等内容,适用于无菌制剂的无菌工艺验证。 3.2.本指南所述条款是在现有无菌工艺技术基础上提出的相 关要求,旨在规范企业开展无菌工艺模拟试验活动。在科学的基础上,鼓励新技术、新设备的引入,进一步提高无菌制剂的无菌保障水平。 4.原则 在对无菌生产工艺充分认知和生产经验累积的基础上,应结合工艺、设备、人员和环境等要素定期开展无菌工艺模拟试验,
常用的消毒灭菌操作方法附录 4 一、干热灭菌的操作方法 1.装入待灭菌的物品 将待灭菌的物品,如塞上棉塞的试管、锥形瓶、培养皿、吸管等玻璃仪器,用牛皮纸或干净的报纸 包裹严密后,放人干热灭菌箱。注意,物品不要摆得太挤,以免妨碍热空气流通。同时,灭菌物品也不 要与干热灭菌箱内壁的铁板接触,以防包装纸烤焦起火。 2.灭菌 关好干热灭菌箱的箱门,旋动恒温调节器,设定温度为160~170℃。当温度升到150℃左右时,保持 此温度3~4h。由于干热灭菌温度较高,操作时要注意防止烫伤。 3.降温 关掉电源,自然降温。 4.开箱取物 等温度降到70℃以下后,打开箱门,取出灭菌物品。注意温度未降到70℃以前,切勿打开箱门,以 免玻璃器皿炸裂。 二、高压灭菌的操作方法 1.首先将内层灭菌桶取出,再向外层锅内加入适量的水,使水面与三角搁架平齐。 2.放回灭菌桶,并装入待灭菌物品。注意不要装得太挤,以免妨碍蒸汽流通而影响灭菌效果。锥形瓶 与试管口不要与桶壁接触,以免冷凝水淋湿包裹瓶口的纸而透入棉塞。 3.加盖,并将盖上的排气软管插人内层灭菌桶的排气槽内。拧紧固定盖子的螺栓,注意要同时旋紧相 对的两个螺栓,使螺栓松紧一致,不漏气。 4.加热灭菌锅,打开排气阀,使水沸腾,排除锅内的冷空气。等冷空气完全排尽后,关上排气阀,让 锅内的温度随蒸汽压力增加而逐步上升。当锅内压力升到所需压力时,控制热源,按照灭菌所要求的时 间,维持压力。 5.到灭菌时间后,切断热源,让灭菌锅内温度自然下降,当压力表的压力降到零时,打开排气阀,旋 松螺栓,打开盖子,取出灭菌物品。如果提前打开排气阀,锅内压力突然下降,灭菌容器内的液体会冲 出容器,造成污染。 三、紫外线灭菌的操作方法 紫外线只适用于表面灭菌和空气灭菌。以面积为10 m2的普通小型接种室为例,在工作台上方距地面 2m 处悬挂1~2 只30 W 紫外灯,每次开灯照射30 min ,就能达到室内空气灭菌的目的。照射前,适量喷 洒石炭酸等化学抑菌剂,可以加强灭菌效果。
环境及消毒灭菌效果监测制度 一、监测目的 为有效评价医院消毒设备是否正常,消毒药剂是否有效,消毒方法是否合理,消毒效果是否达标,定期对医院环境及消毒灭菌效果等进行监测,以有效预防医院感染,保证医疗安全。 二、监测范围 对医疗环境、医务人员手、使用中的消毒液、紫外线灯、压力蒸汽灭菌、消毒灭菌后物品等进行监测,并做好监测记录,对不符合要求的立即整改。 三、监测要求 (一) 压力蒸汽灭菌 1.物理监测:每锅登记温度、压力、时间、锅次、物品、消毒员等。 2.化学监测:常规进行包外、包内化学指示物监测。采用快速压力蒸汽灭菌程序灭菌时,应直接将一片包内化学指示物置于待灭菌物品旁边进行化学监测。 3.生物监测:每周一次,有植入物时每锅进行生物监测。 (二) 紫外线灯 1.日常监测:登记照射时间、累计使用时间、使用人签名,每周一次擦拭记录。 2.强度监测:每半年一次,有监测记录。 (三) 消毒剂 1.化学指示卡监测:含氯消毒剂每日监测,戊二醛每周监测,有记录。 2.生物监测:消毒剂每季进行生物学监测。使用中的灭菌用消毒液要求:无细菌生长;使用中皮肤黏膜消毒液染菌量:≤10cfu/ml;其他使用中消毒液染菌量≤100cfu/ml。 (四)医疗环境、医务人员手的清洁消毒效果监测 每季度对感染高风险部门(病房手术室、外科门诊手术室、妇科门诊手术室、口腔科、检验科、供应室、急诊室)、普通科室的治疗室、注射室、换药室等部门进行空气、医务人员手、物体表面、使用中的消毒剂、消毒灭菌后物品的微生物监测一次;当怀疑与医院感染暴发有关时,及时进行监测,并进行相应致病性微生物的检测。 1.灭菌后的物品不得检出任何微生物。消毒后的医疗用品不得检出致病微生物(乙型溶血性链球菌、金黄色葡萄球菌及其他治病微生物)。 2.各治疗室空气中细菌数≤4cfu/(5min·直径9cm平皿),物体表面的细菌菌落总数≤10cfu/ cm2。 3.手术室空气中细菌总数≤4cfu/(15min·直径9cm平皿);物体表面的细菌菌落总数≤5cfu/ cm2。 4.卫生手消毒,监测的细菌菌落总数应≤10cfu/cm2。外科手消毒,监测的细菌菌落总数应≤5cfu/cm2。
消毒灭菌标准操作程序[1].1 消毒灭菌标准操作程序 一、消毒、灭菌基本原则 1、基本要求 (1重复使用的诊疗器械、器具和物品,使用后应先清洁,再进行消毒或灭菌。 (2被朊病毒、气性坏疽及突发不明原因的传染病病原体污染的诊疗器械、器具和物品,应执行本规范第11章的规定。 (3耐热、耐湿的手术器械,应首选压力蒸汽灭菌, 不应采用化学消毒剂浸泡灭菌。 (4环境与物体表面,一般情况下先清洁,再消毒; 当受到患者的血液、体液等污染时,先去除污染物,再清洁与消毒。 (5医疗机构消毒工作中使用的消毒产品应经卫生行政部门批准或符合相应标准技术规范,并应遵循批准使用的范围、方法和注意事项。 二、消毒、灭菌方法的选择原则 1、根据物品污染后导致感染风险高低选择相应的消毒或灭菌方法: (1高度危险性物品,应采用灭菌方法处理;
(2中度危险性物品,应采用达到中水平消毒以上效 果的消毒方法; (3低度危险性物品,宜采用低水平消毒方法,或做清洁处理;遇有病原微生物污染时,针对所污染病原微生物的种类选择有效的消毒方法。 2、根据物品上污染微生物的种类、数量选择消毒或灭菌方法: (1对受到致病菌芽孢、真菌孢子、分枝杆菌和经血传播病原体(乙型肝炎病毒、丙型肝炎病毒、艾滋病病毒等污染的物品,应采用高水平消毒或灭菌; (2对受到真菌、亲水病毒、螺旋体、支原体、衣原体等病原微生物污染的物品,应采用中水平以上的消毒方法; (3对受到一般细菌和亲脂病毒等污染的物品,应采用达到中水平或低水平的消毒方法; (4杀灭被有机物保护的微生物时,应加大消毒剂的使用剂量和(或延长消毒时间。 3、根据消毒物品的性质选择消毒或灭菌方法: (1耐热、耐湿的诊疗器械、器具和物品,应道选压力蒸汽灭菌;耐热的油剂类和干粉类等应采用干热灭菌; (2不耐热、不耐湿的物品,宜采用低温灭菌方法如环氧乙烷灭菌、过氧化氢低温等离子体灭菌或低温甲醛蒸汽灭菌等;
常用消毒与灭菌方法 含氯消毒剂 C.10.1 适用范围 适用于物品、物体表面、分泌物、排泄物等的消毒。 C.10.2 使用方法 C.10.2.1 消毒液配制 根据新产品有效氯含量,按稀释定律,用蒸馏水稀释成所需浓度。具体计算方法及配制步骤按C.9.1.2.1进行。 C.10.2.2 消毒方法 C.10.2.2.1 将待消毒的物品浸没于装有含氯消毒剂溶液的容器中,加盖。对细菌繁殖体污染物品的消毒,用含有效氯500mg/L的消毒液浸泡>10min,对经血传播病原体、分支杆菌和细菌芽孢污染物品的消毒,用含有效氮2000mg/L~5000mg/L消毒液,浸泡>30min。 C.10.2.2.2 擦拭法大件物品或其他不能用浸泡消毒的物品用擦拭消毒,消毒所用的浓度和作用时间同浸泡法。 C10.2.2.3 喷洒法对一般污染的物品表面,用含有效氯400 mg/L~700 mg/L的消毒液均匀喷洒,作用10min~30min;对经血传播病原体、结核杆菌等污染表面的消毒,用含有效氯2000mg/L的消毒液均匀喷洒,作用>60min。喷洒后有强烈的刺激性气味,人员应离开现场。
C10.2.2.4干粉消毒法对分泌物、排泄物的消毒,用含氯消毒剂干粉加入分泌物、排泄物中,使有效氯含量达到10000mg/L,搅拌后作用>2h;对医院污水的消毒,用干粉按有效氯50mg/L用量加入污水中,并搅拌均匀,作用2h后排放。 C10.3 注意事项 C10.3 .1粉剂应于阴凉处避光、防潮、密封保存;水剂应于阴凉处避光、密闭保存。使用液应现配现用,使用时限≤24h。 C10.3.2 配置漂白粉等粉剂溶液时,应戴口罩、手套。 C10.3.3 未加防锈剂的含氯消毒剂对金属有腐蚀性,不应做金属器械的消毒。加防绣剂的含氯消毒剂对金属器械消毒后,应用无菌蒸馏水冲洗干净,干燥后使用。 C10.3.4 对织物有腐蚀和漂白作用,不应做有色织物的消毒。 .16 煮沸消毒 C.16.1 适用范围 适用于金属、玻璃制品、餐饮具、织物或其他耐热、耐湿物品的消毒。 C.16.2 使用方法 将待消毒物品完全浸没水中,加热水沸腾后维持≥15min。
一、准确度 准确度系指采用该方法测定的结果与真实值或参考值接近的程度,一般用回收率(%)表示。准确度应在规定的范围内测定。 1.化学药含量测定方法的准确度 原料药采用对照品进行测定,或用本法所得结果与已知准确度的另一个方法测定的结果进行比较。制剂可在处方量空白辅料中,加入已知量被测物对照品进行测定。如不能得到制剂辅料的全部组分,可向待测制剂中加人已知量的被测物对照品进行测定,或用所建立方法的测定结果与已知准确度的另一种方法测定结果进行比较。准确度也可由所测定的精密度、线性和专属性推算出来。 2.化学药杂质定量测定的准确度 可向原料药或制剂处方量空白辅料中加人已知量杂质进行测定。如不能得到杂质或降解产物对照品,可用所建立方法测定的结果与另一成熟的方法进行比较,如药典标准方法或经过验证的方法。在不能测得杂质或降解产物的校正因子或不能测得对主成分的相对校正因子的情况下,可用不加校正因子的主成分自身对照法计算杂质含量。应明确表明单个杂质和杂质总量相当于主成分的重量比(%) 或面积比(% )。 3.中药化学成分测定方法的准确度 可用对照品进行加样回收率测定,即向已知被测成分含量的供试品中再精密加人一定量的被测成分对照品,依法测定。用实测值与供试品中含有量之差,除以加入对照品量计算回收率。在加样回收试验中须注意对照品的加人量与供试品中被测成分含有量之和必须在标准曲线线性范围之内;加入对照品的量要适当,过小则引起较大的相对误差,过大则干扰成分相对减少,真实性差。 回收率:%= (C - A ) /S X 100% 式中:A为供试品所含被测成分量;B 为加入对照品量; C 为实测值。 4.校正因子的准确度 对色谱方法而言,绝对(或定量)校正因子是指单位面积的色谱峰代表的待测物质的量。待测定物质与所选定的参照物质的绝对校正因子之比,即为相对校正因子。相对校正因子计算法常应用于化学药有关物质的测定、中药材及其复方制剂中多指标成分的测定。校正因子的表示方法很多,本指导原则中的校正因
清洗消毒及灭菌技术操作规范 昭平县中医院院感科 1、范围本标准规定了各级各类医院消毒供应中心central sterile supply department ,CSSD的诊疗器械、器具和物品处理的基本原则、操作流程和被朊毒体、气性坏疽及突发原因不明的传染病病原体污染器械、器具和物品的处理流程。本标准适用于医院的CSSD和为医院提供消毒灭菌服务的社会化消毒灭菌机构。暂未实行消毒供应工作集中管理的医院其手术部室的消毒供应工作应执行本标准。已采取污水集中处理的其他医疗机构可参照使用。 2、规范性引用文件下列文件的条款通过本标准的引用而成为本标准的条款。凡是标注日期的引用文件其随后所有的修改不包括勘误内容或修订版均不适用于本标准然而鼓励根据本标准达成协议的各方研究是否可适用这些文件的最新版本。凡是不注明日期的引用文件其最新版本适用于本标准。GB/T 5750.5 生活饮用水检验标准方法无机非金属指标GB/T 19633 最终灭菌医疗器械的包装WS 310.1 医院消毒供应中心第1部分管理规范WS 310.3 医院消毒供应中心第3部分清洗消毒及灭菌效果监测标准消毒技术规范卫生部 3、术语和定义下列术语和定义适用于本标准。 3.1 清洗cleaning 去除医疗器械、器具和物品上污物的全过程 流程包括冲洗、洗涤、漂洗和终末漂洗。 3.1.1 冲洗flushing 使用流动水去除器械、器具和物品表面污
物的过程。 3.1.2 洗涤washing使用含有化学清洗剂的清洗用水去除器械、器具和物品污染物的过程。 3.1.3 漂洗rinsing 用流动水冲洗洗涤后器械、器具和物品上残留物的过程。 3.1.4 终末漂洗end rinsing 用软洗、纯化水或蒸馏水对漂洗后的器械、器具和物品进行最终处理的过程。 3.2 超声波清洗器ultrasonic cleaner 利用超声波在水中振荡产生“空化效应”进行清洗的设备。 3.3 清洗消毒器washer-disinfector 具有清洗与消毒功能的机器。3.4 闭合closure 用于关闭包装而没有形成密封的方法。例如反复折叠以形成一弯曲路径。 3.5 密封sealing 包装层间链接的结果。注密封可以采用诸如粘合剂或热熔法。 3.6 闭合完好性closure integrity 闭合条件能确保该闭合至少与包装上的其他部分具有相同的阻碍微生物进入的程度。 3.7 包装完好性package integrity 包装未受到物理损坏的状态。3.8 植入物implantable medical device 放置于外科操作造成的或者生理存在的体腔中留存时间为30d或者以上的可植入型物品。 3.9 湿热消毒moist heat disinfection 利用湿热使菌体蛋白质变性或凝固酶失去活性代谢发生障碍致使细胞死亡。包括煮沸消毒法、巴斯德消毒法和低温蒸汽消毒法。
消毒灭菌效果监测制度 This model paper was revised by the Standardization Office on December 10, 2020
消毒灭菌效果监测制度 (一)对使用中的消毒剂、灭菌剂进行染菌量和浓度检测 1.染菌量监测 消毒剂每季度1次,其细菌含量必须<100cfu/ml,不得检出致病性微生物。灭菌剂每月检测1次,不得检出任何微生物。 2.浓度检测 应根据消毒、灭菌剂的性能定期检测、如含氯消毒剂、过氧乙酸等应现用现配,每次配制后都应测试浓度,对戊二醛的监测应每周不少于2次,腔镜中心要每日监测。 (二)消毒灭菌物品进行消毒灭菌效果监测 1.消毒物品每季度监测1次,不得检出致病性微生物。 2.灭菌物品每月检测1次,不得检出任何微生物。 3.消毒后的内镜(如胃镜、肠镜、喉镜、气管镜),细菌总数≤20cfu/件,并未检出致病菌为合格。 4.灭菌后内镜(如腹腔镜、关节镜、胆道镜、膀胱镜、胸腔镜)未检出任何微生物为合格。 (三)紫外线消毒:应进行照射强度检测和生物检测。 1.照射强度检测 各科室应做好每支灯管应用时间、累计时间和使用人、监督人签名的登记。检测灯管照射强度,新灯管的照射强度50≧W/cm2,使用中的灯管照射强度≧70W/cm2。 2.生物检测 必要时进行
(四)环境卫生学检测 1.各科室按照要求每季度对本科重点区域的空气、物体表面及医护人员的手进行消毒灭菌效果监测。 2.医院感染管理科应每季度对重点科室及病房等进行环境卫生学检测,并做好检测统计分析。 3.判定标准:医院内感染检测监控目标 医院感染发病率(现患率)≤10%。 医院感染现患率实查率≧96%。 ③医院感染漏报率≤20%。 ④抗菌药物使用率≤60%。 ⑤清洁手术切口感染率≤%。 ⑥医疗器械消毒灭菌合格率100%。 ⑦卫生手消毒后医务人员手表面菌落数应≤10cfu/cm2;外科手消毒后医务人员手表面菌落数应≤5cfu/cm2 ⑧Ⅰ、Ⅱ类环境科室物体表面细菌总数≤5cfu/cm2;Ⅲ、Ⅳ类环境科室物体表面细菌总数≤10cfu/cm2。 ⑨Ⅰ类环境科室空气细菌总数≤皿(30min),Ⅱ类环境科室空气细菌总数≤皿(15min),Ⅲ、Ⅳ类环境科室空气细菌总数≤皿(5min)。 ⑩消毒后内镜细菌总数20cfu/件,并未检出致病菌。 使用中的灭菌用消毒液为无菌生长;使用中的皮肤粘膜消毒液染菌量≤10cfu/ ml,其他使用中消毒液染菌量≤100cfu/ml吗,不得检出致病性微生物。
严格的消毒灭菌对细胞与胚胎工程研究与应用工作极为重要,直接影响着整个实验能否顺利进行。 (一)消毒灭菌方法 目前常用的消毒灭菌方法多采用物理方法(如干热灭菌法、湿热灭菌法、过滤除菌法、射线杀菌法等)和化学方法(消毒剂、抗生素)两大类。 1.干热灭菌法 是利用恒温干燥箱内120 oC~150 oC的高热,并保持90~120分钟,杀死细菌和芽孢,达到灭菌目的的一种方法。主要适用于不便在压力蒸汽灭菌器中进行灭菌,且不易被高温损坏的玻璃器皿、金属器械以及不能和蒸汽接触的物品的灭菌。用此方法灭菌的物品干燥,易于贮存。酒精灯火焰烧灼灭菌法也是属于干热灭菌的方法之一,在进行动物细胞体外培养工作时,常须利用工作台面上的酒精灯火焰对金属器具及玻璃器皿口缘进行补充灭菌。 2.湿热灭菌法 压力蒸汽湿热灭菌法是目前最常用的一种灭菌方法。它利用高压蒸汽以及在蒸汽环境中存在的潜热作用和良好的穿透力,使菌体蛋白质凝固变性而使微生物死亡。适合于布类工作衣、各种器皿、金属器械、胶塞、蒸馏水、棉塞、纸和某些培养液的灭菌。高压蒸汽灭菌器的蒸汽压力一般调整为1.0~1.1 kg/cm2,维持20~30 min即可达到灭菌效果。 3.射线灭菌法 利用紫外线灯进行照射灭菌的方法。紫外线是一种低能量的电磁辐射,可以杀灭多种微生物。紫外线的作用机制是通过对微生物的核酸及蛋白质等的破坏作用而使其灭活。适合于实验室空气、地面、操作台面灭菌。灭菌时间为30 min。用紫外线杀菌时应注意,不能边照射边进行实验操作,因为紫外线不仅对人体皮肤有伤害,而且对培养物及一些试剂等也会产生不良影响。 4.过滤除菌法 是将液体或气体通过有微孔的滤膜过滤,使大于滤膜孔径的细菌等微生物颗粒阻留,从而达
消毒灭菌效果监测制度 医院必须对消毒、灭菌效果定期进行监测并做好记录备查。灭菌合格率必须达到100%, 不合格物品不得进入临床使用。监测方法见中华人民共和国卫生部《消毒技术规范》(2002 年版) 。 1、对使用中消毒剂、灭菌剂进行生物和化学监测。 (1)生物监测: 消毒剂每季度一次, 其含菌量必须〈100 时, 不得检出致病原性微生物; 灭菌剂每月监测一次, 不得检出任何微生物 (2)化学监测: 根据消毒、灭菌剂的性能定期监测, 如含氯消毒剂、过氧乙酸等应每日监测,戍二醒的监测, 每周不少于一次 (3)对消毒、灭菌物品进行效果监测, 消毒物品不得检出致病性微生物, 灭菌物品不得检出任何微生物。 (4)必须对压力蒸汽灭菌器进行工艺监测、化学监测、和生物监测。 (5)工艺监测应每锅进行, 并详细记录。 (6)化学监测应每包进行, 手术包尚需进行中心部位的化学监测。预真空压力蒸汽灭菌器每天灭菌前第一锅需进行试验。 (7)生物监测应每月进行, 新灭菌器使用前必须先进行
生物监测, 合格后才能使用; 对拟采用的新包装容器、摆放方式、排气方式及特殊灭菌工艺, 也必须进行生物监测, 合格后才能采用。 (8)环氧乙: 院气体灭菌: 必须每锅进行工艺监测、每包进行化学监测, 每月进行生物监测。 (9)紫外线消毒: 应进行日常照射强度和生物监测。日常监测包括灯管应用时间、累积照射时间、使用人签名和新灯管照射强度监测, 新灯管的照射强度不低于100 μ2, 使用中灯管不得低于70 μ2 。照射强度监测应每半年一次, 生物监测必要时进行。 (10)各种消毒后的内镜( 如胃镜、肠镜、喉镜等) 及其它消毒物品应每季度进行监测, 不得检出致病性微生物。 (11)各种灭菌后内镜( 如腹腔镜、关节镜、胆道镜、膀脱镜、胸腔镜等) 、活检钳和灭菌物品,必须每月进行监测, 不得检出任何微生物。 2、进入人体无菌组织、器官或接触破损皮肤、粘膜的医疗用品和接触皮肤、粘膜的医疗用品卫生标准: 应符合《医院消毒卫生标准》(15982-1995)( 附录三) 中4.2 规定。监测方法见《医院消毒卫生标准》( 15982-1995) 。
9012 生物样品定量分析方法验证指导原则
1. 范围
准确测定生物基质(如全血、血清、血浆、尿)中的药物浓度,对于药物和 制剂研发非常重要。这些数据可被用于支持药品的安全性和有效性,或根据毒动 学、药动学和生物等效性试验的结果做出关键性决定。因此,必须完整地验证和 记录应用的生物分析方法,以获得可靠的结果。
本指导原则提供生物分析方法验证的要求,也涉及非临床或临床试验样品实 际分析的基本要求,以及何时可以使用部分验证或交叉验证,来替代完整验证。
生物样品定量分析方法验证和试验样品分析应符合本指导原则的技术要求。 应该在相应的生物样品分析中遵守 GLP 原则或 GCP 原则。
2. 生物分析方法验证
2.1 分析方法的完整验证
分析方法验证的主要目的是,证明特定方法对于测定在某种生物基质中分析 物浓度的可靠性。此外,方法验证应采用与试验样品相同的抗凝剂。一般应对每 个物种和每种基质进行完整验证。当难于获得相同的基质时,可以采用适当基质 替代,但要说明理由。
一个生物分析方法的主要特征包括:选择性、定量下限、响应函数和校正范 围(标准曲线性能)、准确度、精密度、基质效应、分析物在生物基质以及溶液 中储存和处理全过程中的稳定性。
有时可能需要测定多个分析物。这可能涉及两种不同的药物,也可能涉及一 个母体药物及其代谢物,或一个药物的对映体或异构体。在这些情况下,验证和 分析的原则适用于所有涉及的分析物。
对照标准物质 在方法验证中,含有分析物对照标准物质的溶液将被加入到空白生物基质 中。此外,色谱方法通常使用适当的内标。 应该从可追溯的来源获得对照标准物质。应该科学论证对照标准物质的适用 性。分析证书应该确认对照标准物质的纯度,并提供储存条件、失效日期和批号。 对于内标,只要能证明其适用性即可,例如显示该物质本身或其相关的任何杂质 不产生干扰。 当在生物分析方法中使用质谱检测时,推荐尽可能使用稳定同位素标记的内 标。它们必须具有足够高的同位素纯度,并且不发生同位素交换反应,以避免结 果的偏差。
1
常用的消毒灭菌操作方法附录4 一、干热灭菌的操作方法 1.装入待灭菌的物品 将待灭菌的物品,如塞上棉塞的试管、锥形瓶、培养皿、吸管等玻璃仪器,用牛皮纸或干净的报纸包裹严密后,放人干热灭菌箱。注意,物品不要摆得太挤,以免妨碍热空气流通。同时,灭菌物品也不要与干热灭菌箱内壁的铁板接触,以防包装纸烤焦起火。 2.灭菌 关好干热灭菌箱的箱门,旋动恒温调节器,设定温度为160~170℃。当温度升到150℃左右时,保持此温度3~4h。由于干热灭菌温度较高,操作时要注意防止烫伤。 3.降温 关掉电源,自然降温。 4.开箱取物 等温度降到70℃以下后,打开箱门,取出灭菌物品。注意温度未降到70℃以前,切勿打开箱门,以免玻璃器皿炸裂。 二、高压灭菌的操作方法 1.首先将内层灭菌桶取出,再向外层锅内加入适量的水,使水面与三角搁架平齐。 2.放回灭菌桶,并装入待灭菌物品。注意不要装得太挤,以免妨碍蒸汽流通而影响灭菌效果。锥形瓶与试管口不要与桶壁接触,以免冷凝水淋湿包裹瓶口的纸而透入棉塞。 3.加盖,并将盖上的排气软管插人内层灭菌桶的排气槽内。拧紧固定盖子的螺栓,注意要同时旋紧相对的两个螺栓,使螺栓松紧一致,不漏气。 4.加热灭菌锅,打开排气阀,使水沸腾,排除锅内的冷空气。等冷空气完全排尽后,关上排气阀,让锅内的温度随蒸汽压力增加而逐步上升。当锅内压力升到所需压力时,控制热源,按照灭菌所要求的时间,维持压力。 5.到灭菌时间后,切断热源,让灭菌锅内温度自然下降,当压力表的压力降到零时,打开排气阀,旋松螺栓,打开盖子,取出灭菌物品。如果提前打开排气阀,锅内压力突然下降,灭菌容器内的液体会冲出容器,造成污染。 三、紫外线灭菌的操作方法 紫外线只适用于表面灭菌和空气灭菌。以面积为10 m2的普通小型接种室为例,在工作台上方距地面2m处悬挂1~2只30 W紫外灯,每次开灯照射30 min,就能达到室内空气灭菌的目的。照射前,适量喷洒石炭酸等化学抑菌剂,可以加强灭菌效果。
消毒灭菌效果监测实施方 案 This manuscript was revised by the office on December 10, 2020.
吐哈石油医院2015年消毒灭菌效果监测 实施方案 医院消毒是预防医院内感染的重要措施之一,消毒效果的监测是评价其消毒设备运转是否正常、消毒药剂是否有效、消毒方法是否合理、消毒效果是否达标的唯一手段。为规范消毒效果监测,依据卫计委《医院感染管理办法》、《医院感染监测规范》、《医院消毒技术规范规范(2012版)》特制定哈密地区中心医院消毒灭菌效果监测实施方案。 一、监测项目: 1. 空气消毒效果的监测; 2. 手和物体表面的消毒效果监测; 3. 牙科用水的监测; 4. 内镜消毒及灭菌效果的监测; 5. 使用中消毒剂及灭菌剂的监测; 6. 压力蒸汽灭菌效果监测; 7. 血液透析用水和透析液的监测 8. 灭菌物品监测 二、监测单的填写: 1.空气监测:采样地点、样品名称(空气)、采样时间、采样人,检验项目:细菌总数、致病菌(如金黄色葡萄球菌、溶血性链球菌等)。 2.物表监测:采样地点、物表名称(注明所采物品的名称和部位)、采样人、采样时间、检验项目、细菌总数、致病菌(如金黄色葡萄球菌等)。 3.手监测:采样地点、被监测人姓名、采样人、采样时间、检验项目:细菌总数、致病菌(如金黄色葡萄球菌等)。 4.其他物品的监测:采样地点、样品名称、检验项目、采样人、采样时间等。 (一)空气消毒效果的监测 1.监测科室:非洁净手术室、产房、血透室、消毒供应室等。 2.监测频次:重点科室每季度一次,如有疑似感染发生随时采样。 3.采样(沉降法) ⑴采样时间:空气消毒后4小时内、操作前。 ⑵平板暴露法:(非洁净手术室)暴露前先检查平板是否污染,是否有气泡及霉点。将普通营养琼脂平板(直径为 9cm)放在室内各采样点处,采样高度为距地面0.8m-- 1.5m,采样时将平板盖打开,斜扣放于平板旁,暴露 15min,在放置、收取平皿时,手不能在暴露平皿的正上方移动。
灭菌/无菌工艺验证指导原则(第二稿) 目录 1概述 (2) 2制剂湿热灭菌工艺 (3) 2.1湿热灭菌工艺的研究 (3) 2.1.1 湿热灭菌工艺的确定依据 (3) 2.1.2过度杀灭法的工艺研究 (5) 2.1.3残存概率法的工艺研究 (5) 2.2湿热灭菌工艺的验证 (7) 2.2.1物理确认 (7) 2.2.2 生物学确认 (9) 3制剂无菌生产工艺 (10) 3.1无菌生产工艺的研究 (10) 3.1.1无菌分装生产工艺的研究 (10) 3.1.2 过滤除菌生产工艺的研究 (11) 3.2 无菌生产工艺的验证 (12) 3.2.1培养基模拟灌装试验 (12) 3.2.2 除菌过滤系统的验证 (14) 4原料药无菌生产工艺 (17) 4.1 无菌原料药生产工艺特点 (18) 4.1.1 溶媒结晶工艺 (18) 4.1.2 冷冻干燥工艺 (19) 4.2 无菌原料药工艺验证 (19) 4.2.1 验证批量 (19) 4.2.2 最差条件 (19)
1概述 无菌药品是指法定药品标准中列有无菌检查项目的制剂和原料药,一般包括注射剂、无菌原料药及滴眼剂等。从严格意义上讲,无菌药品应完全不含有任何活的微生物,但由于目前检验手段的局限性,绝对无菌的概念不能适用于对整批产品的无菌性评价,因此目前所使用的“无菌”概念,是概率意义上的“无菌”。一批药品的无菌特性只能通过该批药品中活微生物存在的概率低至某个可接受的水平,即无菌保证水平(Sterility Assurance Level, SAL)来表征。而这种概率意义上的无菌保证取决于合理且经过验证的灭菌工艺过程、良好的无菌保证体系以及生产过程中严格的GMP管理。 无菌药品通常的灭菌方式可分为:1)湿热灭菌;2)干热灭菌;3)辐射灭菌;4)气体灭菌;5)除菌过滤。按工艺的不同分为最终灭菌工艺(sterilizing process)和无菌生产工艺(aseptic processing)。其中最终灭菌工艺系指将完成最终密封的产品进行适当灭菌的工艺,由此生产的无菌制剂称为最终灭菌无菌药品,湿热灭菌和辐射灭菌均属于此范畴。无菌生产工艺系指在无菌环境条件下,通过无菌操作来生产无菌药品的方法,除菌过滤和无菌生产均属于无菌生产工艺。部分或全部工序采用无菌生产工艺的药品称为非最终灭菌无菌药品。基于无菌药品灭菌/除菌生产工艺的现状,本指导原则主要对在注射剂与无菌原料药的生产中比较常用的湿热灭菌与无菌生产工艺进行讨论。本指导原则中的湿热灭菌工艺验证主要包括灭菌条件的筛选和研究,湿热灭菌的物理确认,生物指示剂确认等内容;无菌生产工艺验证主要包括无菌分装、除菌过滤、培养基模拟灌装、过滤系统的验证等验证内容。 最终灭菌工艺和无菌生产工艺实现产品无菌的方法有本质上的差异,从而决定了由这两类工艺生产的产品应该达到的最低无菌保证水平的巨大差异。最终灭菌无菌产品的无菌保证水平为残存微生物污染概率≤10-6,非最终灭菌无菌产品的无菌保证水平至少应达到95%置信限下的污染概率<0.1%。由此可见,非最终灭菌无菌产品存在微生物污染的概率远远高于最终灭菌无菌产品,为尽量减少非最终灭菌无菌产品污染微生物的概率,鼓励企业在生产中采用隔离舱等先进技术设备。 基于质量源于设计的药品研发与质量控制的理念,为保证无菌药品的无菌保证水平符合要求,研发者在产品的研发过程中应根据药品的特性选择合适的灭
医院消毒供应中心消毒灭菌工作流程 一、第一个工作流程:污染器械回收 (一)器械使用科室污染器械回收步骤 重要使用的医疗器械应由消毒灭菌部门进行集中的回收处理,包括门诊、病区或手术室等临床科室室使用的污染器械。 (二)对回收的污染器械进行清点核查并确认登记 1. 污染回收时,污染器械应放在有盖的容器中或使用封闭专用车,运送至消毒供应中心污染区进行处理。运送车为封闭式。 2. 沾染较多血液和污物的器械应在使用部门进行初步处理,或者采用保温和封闭的方法,送到消毒供应中心处理。一些物品必须由使用科室在使用后就地进行预处理,例如阴道窥器、直肠窥镜等器械。 3. 精密器械应单独放置在容器中运送,防止损坏。例如内镜、电钻、动力电源线、剪刀。 4. 使用后的医疗废弃物品和材料,不能不能进入供应中心处理转运。 二、第二个工作流程:污染物品接受分类 消毒部门将收回后的污染器械进行清点接受和分类等操作步骤 1. 根据器械部门的材质分为金属、橡胶、玻璃、塑胶等,根据形状为尖锐器械、单管腔类器械、套管强类器械、轴节器械、卡锁器械、盆、盘、瓶等。各种分类的物品应放置在不同的容器中或清洗装置上,注明标记防止混乱。 2. 标明“特殊感染“的器械,需要根据清洗消毒条件,选择处理方法。 3. 一些专科机械可根据使用科室不同,进行分别处理。 三.第三个工作流程: 清洗、消毒 (一)对分类后的器械进行预清洗步骤 根据卫生部WS 310.2-2009 的要求,现代医院消毒供应中心清洗操作程序包括冲洗、洗涤、漂洗和终末漂洗 4 个步骤: 1、冲洗: 将器械、器具和物品置于流动水下冲洗,初步除去污染物。 (1)操作人员必须穿着有防水功能的隔离服装、戴口罩、眼罩或面罩,戴手套、工作帽、穿工作鞋。
清洗消毒及灭菌效果监测标准 基本信息 中文名称清洗消毒及灭菌效果监测标准 外文名称surveillance standardfor cleaning, disinfection and steriliztion 引用文件GB15982 医院消毒卫生标准 前言 根据《中华人民共和国传染病防治法》和《医院感染管理办法》制定本标准。 本标准第4.2.2.2.1、4.4.1.6、4.4.2.3.2为推荐性,其余为强制性条款。 附录A、附录B、附录C为规范性附录。 本标准由卫生部医院感染控制标准专业委员会提出。 本标准主要起草单位:北京大学第一医院、卫生部医院管理研究所、北京协和医院、中国疾病预防控制中心、上海瑞金医院、广州市第一人民医院、江苏省南京市卫生局、煤炭总医院、北京大学人民医院。 本标准主要起草人:李六亿、巩玉秀、么莉、任伍爱、张青、张流波、李新武、钱黎明、冯秀兰、王易非、钟秀玲、武迎宏、张宇、黄靖雄。 1 范围
本标准规定了医院消毒供应中心(central sterile supply department ,CSSD)消毒与灭菌效果监测的要求与方法和质量控制过程的记录与可追溯要求。 本标准适用于医院CSSD和为医院提供消毒灭菌服务的社会化消毒灭菌机构。暂未实行消毒供应工作集中管理的医院,其手术部(室)的消毒供应工作应执行本标准。 已采取污水集中处理的其他医疗机构可参照使用。 2 规范性引用文件 下列文件中的条款通过本标准的引用而成为本标准的条款。凡是标注日期的引用文件,其随后所有的修改(不包括勘误内容)或修订版均不适用于本标准,然而,鼓励根据本标准达成协议的各方研究是否可使用这些文件的最新版本。凡是不注明日期的引用文件,其最新版本适用于本标准。 GB15982 医院消毒卫生标准 GB 18278 医疗保健产品灭菌确认和常规控制要求(工业湿热灭菌第1篇压力蒸汽灭菌效果评价方法与标准) WS310.1 医院消毒供应中心第1部分:管理规范 WS 310.2 医院消毒供应中心第2部分:清洗消毒及灭菌技术操作规范 消毒技术规范卫生部 3 术语和定义 WS310.1和WS 310.2的术语和定义以及下列术语和定义适用于本标准。 3.1可追溯traceability 对影响灭菌过程和结果的关键要素进行记录,保存备查,实现可追踪。 3.2灭菌过程验证装置process challenge device,PCD
物理消毒灭菌法 (一)物理消毒灭菌法 1.热力消毒灭菌法:利用热力作用破坏微生物的蛋白质、核酸、细胞壁、细胞膜,导致其死亡,可分为干热法和湿热法。 (1)燃烧法:属于干热法,是一种简单、迅速、彻底的灭菌方法。 1)用途:①无保留价值的污染物品②金属器械及搪瓷类物品急用,或无条件消毒时,锐利刀剪除外,以免锋刃变钝。 2)方法:①金属器械可在火焰上烧20秒②搪瓷类容器可倒入少量95%乙醇 (2)干烤法:利用特制的烤箱,热力通过空气对流和介质传导进行灭菌,效果可靠。 (3)煮沸消毒法:属于湿热法,用于耐湿、耐高温的搪瓷、金属、玻璃,橡胶类物品,不能用于外科手术器械的灭菌。从水煮开始计时,5-10分钟可杀灭繁殖体,15分钟可将多数细菌芽胞杀灭,如破伤风杆菌芽胞需煮60分钟才可杀灭,在水中加入碳酸氢钠,配成浓度为1%-2%的溶液时,沸点可达105度,即可增强杀菌作用,又可去除防锈。 注意事项:①物品需全部侵入在水中,物品盖子打开,轴节打开,空腔导管预先灌水,各种大小及形状相同的容器不能重叠②玻璃类物品需用纱布包裹,并在冷水或温水中放入③橡胶类物品需用纱布包好,水沸后放入④如中途加入其它物品,需等再次水沸后开始计时⑤高原地区气压低,沸点低,需适当延长煮沸时间,一般海拔每增高300m,煮沸时间延长2分钟。 (4)压力蒸汽灭菌法:属于湿热法,是一种临床上应用最广泛,效果最为可靠的首选灭菌方法 2.光照消毒法(又称辐射消毒)主要是通过紫外线的杀菌作用,使菌体蛋白发生光解、变性,导致细菌死亡。 (1)日光暴晒法:利用日光的热、干燥、紫外线的作用来杀菌,将床垫、毛毯、书籍、衣服等放在阳光下直射,暴晒6小时可达到消毒效果,中间要定时翻动。 (2)紫外线灯管消毒法:紫外线属于电磁波辐射,常用于空气、物品表面的消毒,杀菌最强的波长范围250-270nm从灯亮5-7分钟开始计时。①空气消毒:有效距离不超过2m,照射时间20-30分钟②物品消毒:有效距离不超过25-60cm,照射时间20-30分钟。 3)注意事项:①保持室内清洁、干燥,室内温度20-40度,相对湿度40%-60%时,紫外线消毒最为宜 ②保持紫外线灯管清洁,一般每2周用无水乙醇擦拭1次,发现有污洉应随时擦拭③保护眼睛和皮肤:紫外线对眼睛和皮肤有刺激作用,易引起眼炎、皮炎且臭氧对人体不利,因此一般不在有人的环境中使用,必须使用时应带防护镜,穿防护衣,或用被单遮盖肢体④紫外线穿透力较差,消毒时物品应摊开或挂起,且定时翻动及保证各表面均受到直接照射⑤如需再次开启,应间隔3-4分钟⑥定期检测紫外线灯管照射强度,一般每隔3-6个月1次,或建立登记卡,使用时间超过1000小时应予以更换⑦定期做空气培养检测消毒效果 (3)臭氧灭菌消毒法:利用臭氧强大的氧化作用进行杀菌。 1)用途:主要用于空气、医院污水、诊疗用水、物品表面的消毒。 2)方法:使用时应关闭门窗,人员离开房间,消毒结束后30分钟方可进入。 3.电离辐射灭菌法(又称冷灭菌)适用于不耐热的物品消毒,如橡胶、塑料、高分子聚合物(一次性注射器、输液输血器等)、紧密医疗仪器、生物医学制品、节育用具及金属等。 4.微波消毒灭菌法微波可杀灭细菌繁殖体、真菌、病毒、细菌芽胞、真菌孢子等各种微生物。常用于食品、餐具的处理,化验单据、票证的消毒,医疗药品、耐热非金属材料及器械的消毒灭菌。不能用于金属物品的消毒。 化学消毒灭菌法 化学消毒灭菌法是利用液体或气体的化学药物渗透到菌体内,使菌体蛋白凝固变性,细菌酶失去活性,导致微生物代谢障碍而死亡,或破坏细胞膜结构,改变其通透性,导致细胞膜破裂、溶解,以达到消毒灭菌的目的。 1.化学消毒剂的使用原则 (1)待消毒的物品的物品须先洗净、擦干 (2)根据不同物品的性能及各种微生物的特性,选择恰当的消毒剂。 (3)严格掌握消毒剂的有效浓度、使用方法及消毒时间 (4)消毒液中一般不放置纱布、棉花等物,以免因吸附消毒剂而降低消毒效力。 (5)消毒物品应全部侵没在消毒液内,器械的轴节应打开,套盖应掀开,管腔挂满消毒液。 (6)浸泡消毒后的物品使用前应先用无菌生理盐水冲洗,气体消毒后的物品使用前应待气体散发后,以免残留消毒剂刺激组织。 (7)消毒剂应定期检测,调整浓度,进行更换,易挥发的要加盖。 2.化学消毒剂的使用方法 (1)浸泡法:常用于耐湿、不耐热的物品,如锐利器械、精密器材等的消毒
医院消毒供应中心第二部分清洗消毒及灭菌技术操 作规范 The latest revision on November 22, 2020
卫生部医院消毒供应中心管理第2部分 清洗消毒及灭菌技术操作规范 医院消毒供应中心 第2部分:清洗消毒及灭菌技术操作规范 根据《中华人民共和国传染病防治法》、《医院感染管理办法》制定本标准。本标准清洗、消毒、灭菌流程的技术操作部分参照了美国ANSI/AAMI ST79-2006医疗设备中蒸汽消毒和灭菌保证综合指南(ANSI/AAMI ST79-2006 comprehensive guide to steam sterilization and stearility assurance in health care facilities)EN ISO 15883-1.:2006《清洗消毒器》(EN ISO15833-1:2006《washer disinfector》)和EN285:2006《大型蒸汽灭菌器》(EN 285:2006 Sterilization steam sterilizers Large sterilizers)。 本标准第、、、、)和e)、、、、为推荐性,其余为强制性条款。 附录A、附录B、附录C为规范性附录,附录D为资料性附录。 本标准由卫生部医院感染控制标准专业委员会提出。 医院消毒供应中心 第2部分:清洗消毒及灭菌技术操作规范 1、范围 本标准规定了各级各类医院消毒供应中心(central sterile supply department ,CSSD)的诊疗器械、器具和物品处理的基本原则、操作流程和被朊毒体、气性坏疽及突发原因不明的传染病病原体污染器械、器具和物品的处理流程。 本标准适用于医院的CSSD和为医院提供消毒灭菌服务的社会化消毒灭菌机构。暂未实行消毒供应工作集中管理的医院,其手术部(室)的消毒供应工作应执行本标准。已采取污水集中处理的其他医疗机构可参照使用。 2、规范性引用文件 下列文件的条款通过本标准的引用而成为本标准的条款。凡是标注日期的引用文件,其随后所有的修改(不包括勘误内容)或修订版均不适用于本标准,然而,鼓励根据本标准达成协议的各方研究是否可适用这些文件的最新版本。凡是不注明日期的引用文件,其最新版本适用于本标准。 GB/T 生活饮用水检验标准方法无机非金属指标 GB/T 19633 最终灭菌医疗器械的包装 WS 医院消毒供应中心第1部分:管理规范 WS 医院消毒供应中心第3部分:清洗消毒及灭菌效果监测标准消毒技术规范卫生部 3、术语和定义 下列术语和定义适用于本标准。 清洗cleaning 去除医疗器械、器具和物品上污物的全过程,流程包括冲洗、洗 涤、漂洗和终末漂洗。 冲洗 flushing