
2012届高三二模化学题
一、单项选择题(本题包括6小题,每小题4分,共24分。每小题只有一个
....选项符合题意)7.下列说法正确的是
A.乙烯和苯都能与溴水发生反应
B.溴乙烷和乙醇都能发生消去反应
C.淀粉和蛋白质均可作为生产葡萄糖的原料
D.乙酸乙酯和纤维素乙酸酯均可水解生成乙醇
8
9
10
11
4432
12.短周期元素甲、乙、丙、丁的原子序数依次增大。甲的最高价氧化物与乙的氢化物同时通入水中,得到的生成物既可与酸反应又可与碱反应。丙位于第ⅠA族,丁原子的核外电子总数是其最外层电子数的3倍。则
A.气态氢化物的稳定性:乙< 丁
B.原子半径:甲< 乙
C.丙的两种氧化物都是离子化合物
D.甲、乙、丁的最高价氧化物对应的水化物酸性依次增强
二、双项选择题(本题包括2小题,每小题6分,共12分。每小题有两个选项符合题意。若只选一个且正确得3分,但只要选错就得0分)
22.Li-SOCl 2电池可用于心脏起搏器。电极材料分别为锂和碳,电解液是LiAlCl 4—SOCl 2。电池的总反应可表示为:4Li+2SOCl 2=4LiCl +S +SO 2。电池工作时,下列说法正确的是
A .锂电极发生还原反应
B .电子通过外电路从锂电极流向碳电极
C .每生成1mol SO 2转移4mol 电子
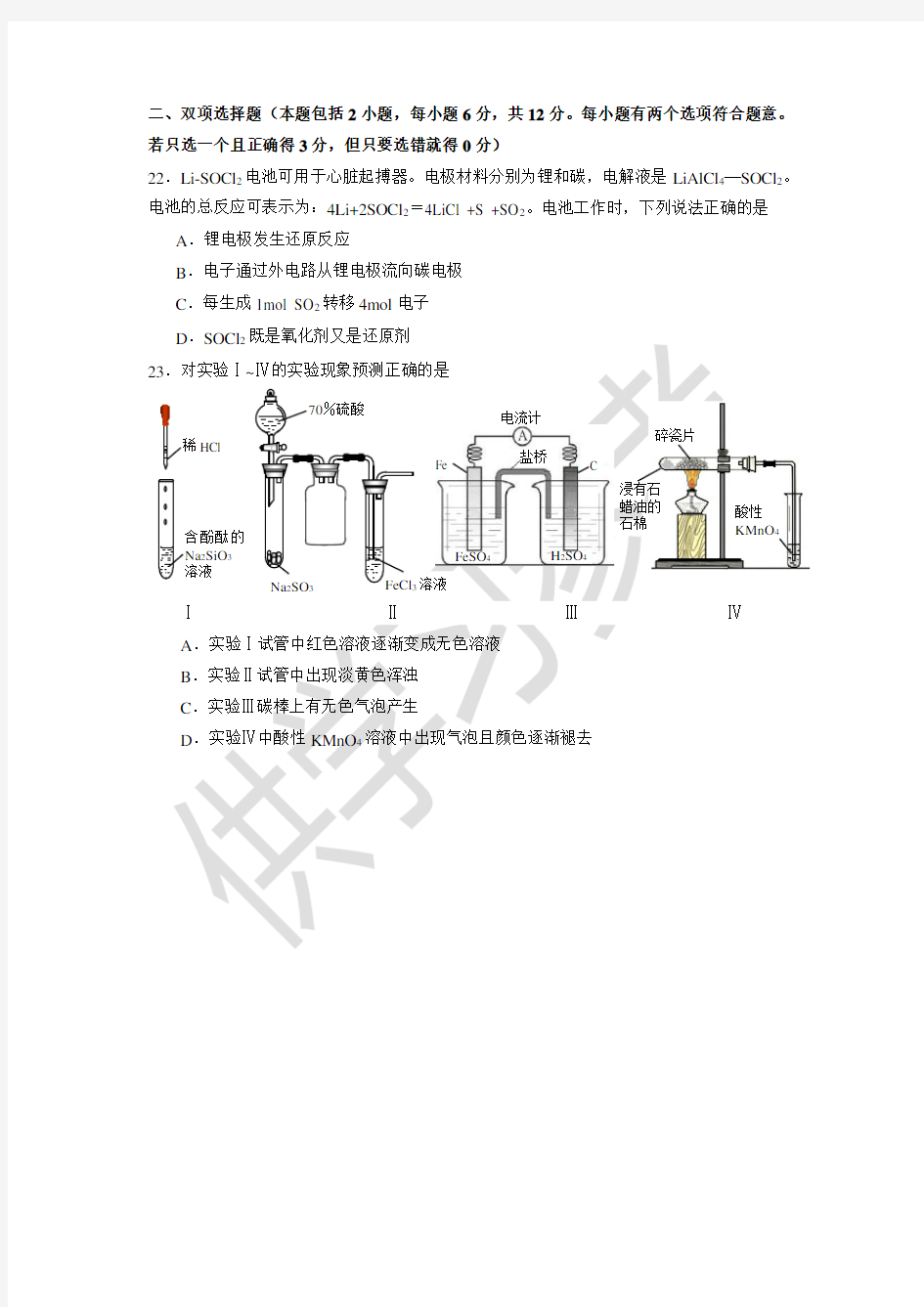
D .SOCl 2既是氧化剂又是还原剂 .对实验Ⅰ~Ⅳ的实验现象预测正确的是
A .实验Ⅰ试管中红色溶液逐渐变成无色溶液
B .实验Ⅱ试管中出现淡黄色浑浊
C .实验Ⅲ碳棒上有无色气泡产生
D .实验Ⅳ中酸性KMnO 4溶液中出现气泡且颜色逐渐褪去
Ⅰ Ⅱ Ⅲ Ⅳ 碎瓷片
浸有石蜡油的石棉
酸性KMnO 4
盐桥
电流计
C
Fe
FeSO 4
H 2SO 4
稀HCl
含酚酞的Na 2SiO 3溶液
FeCl 3溶液
Na 2SO 3
70%硫酸
30.(16分)共轭双烯与含有双键的化合物相互作用,能生成六元环状化合物,常用于有机合成,例如:
化合物Ⅱ可发生以下反应:
(1)化合物Ⅰ的分子式为____________,1 mol 该物质完全燃烧需消耗__________mol O 2。 (2)反应②的化学方程式为______________。
(3)反应③是缩聚反应,化合物Ⅳ的结构简式为______________。 (4)在一定条件下,化合物Ⅴ和化合物Ⅵ能发生类似
反应①的反应,生成两种化合物(互为同分异构体),其结构简式分别为 、_________。
(5)下列关于化合物Ⅰ、Ⅱ、Ⅴ、Ⅵ的说法正确的有_________(填字母)。
A .Ⅰ属于芳香烃
B .Ⅰ、Ⅱ、Ⅴ均能使溴的四氯化碳溶液褪色
C .Ⅴ与足量H 2加成后的产物是3-甲基戊烷
D .加热条件下Ⅵ能与新制Cu(OH)2反应生成红色沉淀
反应①:
(Ⅰ)
COOCH 3
COOCH 3 +
一定条件
COOCH 3
COOCH 3
(Ⅱ)
Ⅱ
Ⅲ(分子式为C 4H 4O 4) HOCH 2CH 2OH/催化剂 Ⅳ(高分子化合物)
稀H 2SO 4/△
反应②
反应③ CH 3CH 2
(Ⅴ)
(Ⅵ)
COOCH 2CH 3 O
31.(16分)工业上常利用醋酸和乙醇合成有机溶剂乙酸乙酯: CH 3COOH(l)+C 2H 5OH(l)
△
浓H 2SO 4CH 3COOC 2H 5(l)+H 2O(l) ΔH =-8.62kJ·mol -
1
已知CH 3COOH 、C 2H 5OH 和CH 3COOC 2H 5的沸点依次为118℃、78℃和77℃。在其他条件相同时,某研究小组进行了多次实验,实验结果如图所示。 (1)该研究小组的实验目的是__________________。 (2)60℃下反应40min 与70℃下反应
20min 相比,前者的平均反应速率___________后者(填“小于”、“等于”或“大于”)。
(3)如图所示,反应时间为40min 、温
度超过80℃时,乙酸乙酯产率下降的原因可能是______(写出两条)。
(4)某温度下,将0.10 mol CH 3COOH 溶于水配成1 L 溶液。
①实验测得已电离的醋酸分子占原有醋酸分子总数的1.3%,求该温度下CH 3COOH 的电离平衡常数K 。(水的电离忽略不计,醋酸电离对醋酸分子浓度的影响忽略不计) ②向该溶液中再加入__________mol CH 3COONa 可使溶液的pH 约为4。(溶液体积变化忽略不计)
乙酸乙酯产率/ %
温度 /℃
32.(16分)硫酸铅广泛应用于制造蓄电池、白色颜料等。利用锌冶炼过程中的铅浮渣生产硫酸铅的流程如下:
已知铅浮渣的主要成分是PbO 、Pb ,还含有少量Ag 、Zn 、CaO 和其他不溶于硝酸的杂质。25℃时,K sp (CaSO 4)=4.9×10-
5,K sp (PbSO 4)=1.6×10-
8。
(1)已知步骤Ⅰ有NO 产生,浸出液中含量最多的阳离子是Pb 2+。分别写出PbO 、Pb 参加
反应的化学方程式_________________、________________。
(2)步骤Ⅰ需控制硝酸的用量并使Pb 稍有剩余,目的是_______________。
(3)母液可循环利用于步骤Ⅰ,其溶质主要是____________(填一种物质化学式),若母液
中残留的SO 42-
过多,循环利用时可能出现的问题是_____________________。 (4)产品PbSO 4还需用Pb(NO 3)2溶液多次洗涤,目的是除去____________。
(5)铅蓄电池的电解液是硫酸,充电后两个电极上沉积的PbSO 4分别转化为PbO 2和Pb ,
充电时阴极的电极反应式为________________。
40%硫酸 PbSO 4
Ⅰ
Ⅱ
Ⅲ
33.(16分)某研究小组在实验室中以铜粉(含铁粉5%以上)为原料制取胆矾(CuSO4·5H2O)并检测其纯度。本题限选试剂:3 mol·L-1 H2SO4、浓硝酸、3%H2O2、0.2mol·L-1 NaOH、20% KSCN。有关物质溶解度如下表(单位:g/100gH2O)。
参考答案和评分标准
7、B 8、D 9、A 10、C 11、B 12、C 22、BC 23、CD 30.(16分)
(1)C 13H 20 (2分) 18(2分)
(2)
(3分)
(漏条件、不配平各扣1分。用可逆符号也正确)
(3)
(2分)
(有错误但只要链节正确,给1分。链节有误得0分)
(4)
(4分)
(书写明显不规范酌情扣分) (5)BCD (3分) (“B ”“C ”“D ”得1分,“BC ”“CD ”“BD ”得2分,其余得0分) 31.(16分)
(1)探究反应温度、反应时间对乙酸乙酯产率的影响 (2分) (自变量、因变量有遗漏或表达不清,扣1分) (2)小于(3分) (“<”得2分) (3)反应可能..已达平衡状态......,温度升高平衡向逆反应方向移动..............;温度过高,乙醇..和乙酸大量挥发..
使反应物利用率下降(4分) (两种可能的原因各占2分。加点部分为得分点,意义相近即可给分。多答其他原因不给分,也不扣分)
(4)① CH 3COOH CH 3COO -
+ H +
初始浓度/ mol·L -
1: 0.10 0 0
浓度变化/ mol·L -
1: 0.10×1.3% 0.10×1.3% 0.10×1.3%
平衡浓度/ mol·L -
1: ≈0.10 0.10×1.3% 0.10×1.3% (2分)
(3分) (K 的表达式正确得1分,算式正确得1分,计算结果正确得1分。因计算时未作近
似处理使小数在1.69~1.71之间均不扣分。用分数表示计算结果不给分)
COOCH 3 COOCH 3
+ 2H 2O
稀H 2SO 4
COOH
COOH
+ 2CH 3OH
△
CH 3CH 2
O
COOCH 2CH 3
O
COOCH 2CH 3
CH 3CH 2
HO C -CH =CH -C -O -CH 2CH 2-O n
H
O
O
c (CH 3COOH)
c (CH 3COO -
) · c (H +) K = = =1.7×10-
5
(0.10×1.3%)2 0.10
②1.7×10-2 (2分)
(“1.68~1.71×10-2”“169/9870”或用小数表示均给分)
32.(16分)
(1)PbO+2HNO3=Pb(NO3)2+H2O (2分)
3Pb+8HNO3=3Pb(NO3)2+2NO↑+4H2O (3分)
(配平错误、漏气体符号各扣1分)
(2)防止Ag被溶解进入溶液(或使Ag留在浸出渣中)(2分)
(“置换Ag”“除去Ag”等得1分。多答其他不给分,也不扣分。)
(3)HNO3(2分)
浸出时部分铅离子生成PbSO4随浸出渣排出,降低PbSO4的产率(2分)
1
红棕色气体生成,该得分点为2分)
(2)取少量铜粉于试管中,加入少量3 mol·L-1 H2SO4溶液,充分振荡后取上层溶液于另一试管中,滴加少量3%H2O2溶液,再滴加几滴20%KSCN溶液。(4分)
(4个得分点,得分点不株连。除注明外其他试剂用量不作要求)
第一个得分点1分:加H2SO4溶解可能存在的铁粉
第二个得分点1分:分离溶液和铜粉
第三个得分点1分:加入氧化剂H2O2(若用HNO3而未强调少量,不给分)
第四个得分点1分:加入KSCN
250 m2
233 m1×100%
(3)(2分)
a P 广东省广州市2018届高三4月综合测试物理(二模) 二、选择题:本题共8小题,每小题6分,共48分。在每小题给出的四个选项中,第 14~18题只有一项符合题目要求,第19~21题有多项符合题目要求。全部选对的得6分,选对但不全的得3分,有选错的得0分。 14.a 、b 两离子从平行板电容器两板间P 处垂直电场入射,运动轨迹如图。若a 、b 的 偏转时间相同,则a 、b 一定相同的物理量是 A .荷质比 B .入射速度 C .入射动能 D .入射动量 15.如图,轻绳的一端系在固定光滑斜面上的O 点,另一端系一小球。给小球一个初速 度使它在斜面上做完整的圆周运动,a 、b 分别为最低点和最高点,则小球 A .重力的瞬时功率始终为零 B .所受的向心力大小不变 C .在b 点的速度不可能为零 D .在a 点所受轻绳拉力一定大于小球重力 16.小球在光滑水平面上以速度v 0做匀速直线运动。某时刻开始小球受到水平恒力F 的作用,速度先减小后增大,最小速度v 的大小为0.5v 0,则小球 A .可能做圆周运动 B .速度变化越来越快 C .初速度v 0与F 的夹角为60° D .速度最小时,v 与F 垂直 17.如图,同一平面内有两根互相平行的长直导线M 和N ,通有等大反向的电流,该 平面内的a 、b 两点关于导线N 对称,且a 点与两导线的距离相等。若a 点的磁感应强度大小为B ,则下列关于b 点磁感应强度B b 的判断正确的是 A .B B 2b >,方向垂直该平面向里 B .B B 2 1b <,方向垂直该平面向外 C .B B B <2013广州二模地理试题及参考答案
1. 因纽特人告别冬季、迎接春天到来的“春节”在 A. 12月25日 B.1月1日 C. 3月最后一个周末 D.6月第一个周末 读“某河流年径流变化示意图”,完成2?3题。 2. 该河流位于 A.乞力马扎罗山 B.塔里木盆地 C.苔原地区 D.赤道地区 3. 该流域的地理环境是 A.有极昼极夜 B.沙漠遍布 C.垂直地带性明显 D.人口稠密 读“我国距今2300万年前植被带分布示意图”,完成4?5题。 4.中部自然带的主要成因是受 A.副热带高气压带影响 B.副极地低气压带影响 C.赤道低气压带影响 D.季风环流影响 5. 自然带分布的格局反映了 A.经度地带性规律 B.纬度地带性规律 C.垂直地带性规律 D.非地带性规律 读“我国15?64岁年龄段人口变化图”,完成6?7题。
6. 2015年后,我国人口变化的特点是 A.少儿人口比重上升 B.总人口数量不断减少 C.老年人口比重下降 D.劳动力数量不断减少 7. 影响图中人口变化的最主要因素是 A.出生率 B.医疗卫生 C.死亡率 D.自然环境 读“世界某农作物产区分布示意图”,完成8?9题。 8. 该农作物是 A.水稻 B.玉米 C.小麦 D.棉花 9. 该作物在西半球主要的农业地域类型是 A.水稻种植业 B.商品谷物农业 C.种植园农业 D.大牧场放牧业 读“20世纪死亡千人以上的灾害分布示意图”,完成10?ll题。
10. 这种灾害是 A.台风 B.滑坡 C.洪涝 D.地震 11.造成图示状况的最主要区位因素是 A.经济水平 B.人口密度 C.地貌形态 D.季风气候 40. (28分)我国30多年的经济高速发展,取得了令世界惊叹的经济奇迹,成为了“世界工厂”。根据以下材料,结合所学知识,完成(1)?(5)题。 材料一:“世界工厂”示意图。 材料二:中国“挖动”了大半个地球。
2019年广州市普通高中毕业班综合测试(二) 理科综合-生物部分 2019.4.25 1.下列关于细胞及其产生的物质的叙述,正确的是 A.细胞中大多数无机盐以离子的形式存在,对维持生命活动有重要作用 B.同一个体不同细胞功能的差异主要是因为不同细胞携带不同遗传信息 C.再次接触到同种抗原时,抗体能迅速通过分裂增殖产生大量新的抗体 D.血糖下降时,肌细胞中的糖原能被分解成葡萄糖,从而维持血糖平衡 2.青霉素药理作用是干扰细菌细胞壁的形成,万古霉素是一种新型的抗生素,其结构与作用原理类似于青霉素。以下分析错误的是 A.万古霉素因干扰细菌增殖而发挥抗菌功效 B.万古霉素的使用使细菌产生抗万古霉素变异 C.青霉素过敏者不适合使用万古霉素 D.万古霉素的使用会使细菌群体中抗万古霉素基因的基因频率提高 3.下列关于细胞癌变的说法,错误的是 A.癌症的发生是细胞中多个基因发生突变的结果 B.癌变细胞的表面物质、形态结构会发生一定的变化 C.香烟烟雾中只有尼古丁这一种化学致癌因子 D.提高免疫系统的监控和清除功能是治疗癌症的一种思路 4.某学习小组用光学显微镜对有关实验材料进行观察和研究,结果记录如下,正确的是 研究证实DELLA蛋白通过阻遏某些基因的转录从而抑制植物生长发育,而赤霉素能解除细胞中已经存在的DELLA蛋白的阻遏效果。以下叙述不合理的是 A.植物合成赤霉素的部位主要是未成熟的种子、幼根和幼芽 B.赤霉素与脱落酸在调控种子萌发与休眠中的作用相互拮抗 C.赤霉素通过抑制DELLA蛋白基因的表达解除其阻遏效果 D.DELLA蛋白分子上可能存在具有不同生物学功能的区域 6.某种家禽(2n=78,性别决定为ZW型)幼体雌雄不易区分,其眼型由Z 染色体上的正常眼基因(B)和豁眼基因(b)控制,雌禽中豁眼个体产蛋能力强。以下叙述错误的是 A.雌禽卵原细胞在进行减数分裂过程中会形成39个四分体 B.正常眼基因和豁眼基因的本质区别在于碱基序列的不同 C.为得到产蛋能力强的雌禽子代,应确保亲本雌禽为豁眼 D.在豁眼雄禽与正常眼雌禽的子代幼体中,雌雄较易区分 29.(9分) 在一项探究土壤细菌对植物X生长效应影响的实验中,将多株生理条件相同的植物X随 1
2013年市高考二模化学试题及答案 本卷可能用到的相对原子质量:H-1 C-12 N-14 O-16 S-32 Fe-56 7.下列实验能达到实验目的的是 A.用乙醇萃取碘水中的碘 B.用饱和NaHCO3中除去CO2混有的HCl C.用Ba(NO3)2溶液鉴别SO32-和SO42-D.用淀粉KI溶液鉴别FeCl3溶液和溴水 8.下列说确的是 A.溴乙烷和甲醇都能发生消去反应 B.乙烯和苯都能与酸性KMnO4溶液发生反应 C.糖类和蛋白质都是人体需要的营养物质 D.纤维素和油脂的水解产物都是葡萄糖 9.设n A为阿伏加德罗常数的数值,下列说确的是 A.常温下,18g H2O中含有2n A个氢原子 B.标准状况下,22.4L 苯含有n A个苯分子 C.1mol Na与足量水反应转移2n A个电子 D.0.1 mol·L-1CH3COOH中含有0.1n A个CH3COO-10.下列物质的制取,实验操作正确的是 A.将CuCl2溶液置于蒸发皿中加热蒸干,可制取无水CuCl2固体 B.将NH4HCO3饱和溶液在蒸发皿中加热蒸干,可制取NH4 HCO3固体 C.向FeCl3饱和溶液缓慢滴入过量氨水加热,可制取Fe(OH)3胶体 D.向电石中缓慢滴入饱和食盐水,可制取C2H2 11.下列离子方程式正确的是 A.铝溶于NaOH溶液:Al + 2OH-=AlO2- + H2↑ B.铜溶于稀硝酸:3Cu + 8H++2NO3-=3Cu2+ +2NO↑+ 4H2O C.碳酸镁中滴加稀盐酸:CO32-+2H+=CO2↑ + H2O D.稀硫酸中滴加氧化钡溶液:H++ OH-=H2O 12.短周期元素甲、乙、丙、丁、戊的原子序数依次增大,甲是周期表中原子半径最小的元素,乙形成的气态氢化物的水溶液呈碱性,乙与丁同族,丙、丁、戊同周期,丙单质可制成半导体材料,戊的最高化合价为+7,则 A.原子半径:乙>丁>丙 B.非金属性:丙>丁>戊 C.甲与戊形成的化合物是共价化合物 D.乙、丙、丁最高价氧化物对应的水化物均是强酸 22.HA为酸性略强于醋酸的一元弱酸,常温下叙述正确的是 A.0.1 mol·L-1 HA中c(H+)=c(OH-)+ c(A-) B.0.1 mol·L-1 HA与0.1 mol·L-1NaOH混合至溶液呈中性:c(Na +)=c(A-) C.0.1 mol·L-1 NaA中c(Na +)>c(OH-) >c(A-)>c(H+) D.0.1 mol·L-1 HA中加入少量NaA固体,HA的电离常数减小 23.下列对实验I~IV电化学的装置正确,且实验现象预测正确的是
2012届高三二模化学题 一、单项选择题(本题包括6小题,每小题4分,共24分。每小题只有一个 ....选项符合题意)7.下列说法正确的是 A.乙烯和苯都能与溴水发生反应 B.溴乙烷和乙醇都能发生消去反应 C.淀粉和蛋白质均可作为生产葡萄糖的原料 D.乙酸乙酯和纤维素乙酸酯均可水解生成乙醇 8 9 10 11 4432 12.短周期元素甲、乙、丙、丁的原子序数依次增大。甲的最高价氧化物与乙的氢化物同时通入水中,得到的生成物既可与酸反应又可与碱反应。丙位于第ⅠA族,丁原子的核外电子总数是其最外层电子数的3倍。则 A.气态氢化物的稳定性:乙< 丁 B.原子半径:甲< 乙 C.丙的两种氧化物都是离子化合物 D.甲、乙、丁的最高价氧化物对应的水化物酸性依次增强
二、双项选择题(本题包括2小题,每小题6分,共12分。每小题有两个选项符合题意。若只选一个且正确得3分,但只要选错就得0分) 22.Li-SOCl 2电池可用于心脏起搏器。电极材料分别为锂和碳,电解液是LiAlCl 4—SOCl 2。电池的总反应可表示为:4Li+2SOCl 2=4LiCl +S +SO 2。电池工作时,下列说法正确的是 A .锂电极发生还原反应 B .电子通过外电路从锂电极流向碳电极 C .每生成1mol SO 2转移4mol 电子 D .SOCl 2既是氧化剂又是还原剂 .对实验Ⅰ~Ⅳ的实验现象预测正确的是 A .实验Ⅰ试管中红色溶液逐渐变成无色溶液 B .实验Ⅱ试管中出现淡黄色浑浊 C .实验Ⅲ碳棒上有无色气泡产生 D .实验Ⅳ中酸性KMnO 4溶液中出现气泡且颜色逐渐褪去 Ⅰ Ⅱ Ⅲ Ⅳ 碎瓷片 浸有石蜡油的石棉 酸性KMnO 4 盐桥 电流计 C Fe FeSO 4 H 2SO 4 稀HCl 含酚酞的Na 2SiO 3溶液 FeCl 3溶液 Na 2SO 3 70%硫酸
2018年广州市普通高中毕业班综合测试(二) 理科综合 2018.4 一、选择题: 1.下列对人体浆细胞有关物质迁移途径的描述,错误的是 A.抗体:核糖体→内质网→高尔基体→细胞膜→细胞外 B.编码抗体的mRNA:细胞核→细胞质基质→核糖体 C.葡萄糖:细胞外→细胞膜→细胞质基质→线粒体 D.O2:细胞外→细胞膜→细胞质基质→线粒体 2.右下图表示土壤中甲、乙两种矿质元素的含量变化与某植物生长速率的关系,下列分析合理的是A.该植物生长所需要甲元素的量比乙元素的量多 B.施含乙元素的肥料比施含甲元素的肥料更有利 于该植物生长 C.种植该植物时,应在早期施用含甲元素的肥料, 后期施用含乙元素的肥料 D.当土壤中乙元素的含量为I时,适当增施含乙元素的肥料能促进该植物生长 3.乘坐过山车朝下疾驰时,不少游客会呼吸加快并感到心怦怦直跳。下列叙述正确的是A.游客在短时间内的上述反应只是神经调节的结果 B.此现象与肾上腺髓质分泌的肾上腺素有关 C.控制呼吸和心跳的中枢位于大脑皮层 D.过程中游客体内的糖原合成速度会加快 4.研究人员测试不同浓度的甲、乙两种生长素类似物对莴苣幼根生长的影响,部分结果如下表。下列分析正确的是 A.甲、乙浓度为0ppm条件下,莴苣幼根不生长 B.甲、乙两种生长素类似物的生理作用与乙烯相似 C.甲促进莴苣幼根生长的最适浓度在10~35ppm之间 D.在0~50 ppm范围内,甲、乙对莴苣幼根生长的影响均体现出两重性 5.某同学取三支试管编号为①、②、③,各加入2ml稀淀粉糊和5滴碘液。试管①内加入2ml唾液,
试管②内加入2ml煮沸的唾液,试管③内加入2ml胰液,将三支试管37℃水浴15分钟后,观察现象。下列关于该实验的叙述错误的是 A.试管①中溶液蓝色褪去,因为唾液中有淀粉酶将淀粉分解 B.试管②中溶液不褪色,因为其中的淀粉酶结构被破坏 C.试管③中溶液蓝色褪去,推测胰液中可能含有淀粉酶 D.实验中应增加对照组,试管中加入4ml蒸馏水和5滴碘液 6.下图为某种单基因遗传病的家系图,在不考虑基因突变等变异的前提下,下列分析错误的是 A.该遗传病不可能是伴Y染色体遗传病 B.III10细胞中的染色体最多有23条源自I1 C.若致病基因在常染色体上,则II4与II6的基因型相同 D.若为隐性基因决定的遗传病,则该病的致病基因可能位于X染色体上 7.化学与生活密切相关。下列对化学事实的解释错误的是 8.N A为阿伏加德罗常数的值。下列说法正确的是 A.25℃时,pH=1 的CH3COOH 溶液中含有H+的数目为0.1N A B.0.1mol H2(g)和0.2mol I2(g)于密闭容器中充分反应后,其分子总数为0.3N A C.0.1mol CH3OH 分子中含有C-H 键的数目为0.4N A D.1.1g 的11B 中含有的中子数0.5N A 9.下列关于(I)、(II)、(III)、(IV)化合物的说法正确的是
2019年高考广州二模物理试题及答案 一、单项选择题(每小题给出的四个选项中,只有一个选项符合题目的要求;每题4分) 13.装有半瓶开水的热水瓶,经过一晚,瓶塞不易拔出,主要原因是 A. 瓶内气体因温度降低而压强减小 B.瓶外因气温高而大气压强变大 C.瓶内气体因体积减小而压强增大 D.瓶内气体因体积增大而压强减小 14.图1是氧气分子在0℃和100℃下的速率分布图线,由图可知 A.随着温度的升高,氧气分子的平均速率变小 B.随着温度的升高,每一个氧气分子的速率都增大 C.随着温度的升高,氧气分子中速率小的分子所占比例高 D.同一温度下,氧气分子速率分布呈现“中间多,两头少”的规律 15.用于治疗肿瘤的放射源必须满足:①放射线具有较强的穿透力,以辐射到体内的肿瘤处;②要在较长时间内具有相对稳定的辐射强度。表中给出的四种放射性同位素,适合用于治疗肿瘤的放射源是 A.钋210 B.锝99 C.钴60 D.锶90 16.频率为υ的光照射某金属时,产生光电子的最大初动能为E km.改用频率为2υ的光照射同一金属,所产生光电子的最大初动能为(h为普朗克常量) A.E km-hυB.2E km C. E km+hυ D. E km+2hυ 二、双项选择题(每小题给出的四个选项中,有两个选项符合题目的要求;每题6分,全选对得6分,只选1个且正确得3分,错选、不选得0分) 17.某交流电的u—t图象如图2所示,则该交流电 A.周期T=0.01s B.频率f=50Hz C.电压有效值2 220 = U V D.用交流电压表测量时读数为220V 18.小球自由下落,经时间t0竖直反弹到某高度。不计小球与地面接触的时间,则整个过程小球加速度a和速度v随时间变化的图象分别是下图中的 图1 -
广州市2020年高考物理二模试卷(I)卷 姓名:________ 班级:________ 成绩:________ 一、选择题 (共10题;共24分) 1. (2分) (2017高二下·淮北期末) 现有a、b、c三束单色光,其波长关系为λa:λb:λc=1:2:3.当用a光束照射某种金属板时能发生光电效应,飞出的光电子最大动能为Ek ,若改用b光束照射该金属板,飞出的光电子最大动能为 Ek ,当改用c光束照射该金属板时() A . 能发生光电效应,飞出的光电子最大动能为 Ek B . 能发生光电效应,飞出的光电子最大动能为 Ek C . 能发生光电效应,飞出的光电子最大动能为 Ek D . 由于c光束光子能量较小,该金属板不会发生光电效应 2. (2分) (2018高一下·阿拉善左旗期末) 下列说法正确的是() A . 动量为零时,物体一定处于平衡状态 B . 动能不变,物体的动量一定不变 C . 物体受到恒力的冲量也可能做曲线运动 D . 物体所受合外力大小不变,但方向改变时,其动量大小一定要发生改变 3. (2分)一电子以初速度v0沿垂直电场强度方向射入两平行金属板间的匀强电场中,现减小两板间的电压,则电子穿越两平行金属板所需的时间() A . 随电压的减小而减少 B . 随电压的减小而增加 C . 与电压无关 D . 随两板间距离的增大而减少
4. (3分) (2019高三上·太原月考) 如图所示,光滑绝缘水平面上有甲、乙两个点电荷。时,甲静止,乙以的初速度向甲运动。此后,它们仅在静电力的作用下沿同一直线运动整个运动过程中没有接触 ,它们运动的图像分别如图中甲、乙两曲线所示。则由图线可知() A . 两电荷的电性一定相反 B . 甲、乙两个点电荷的质量之比为2:1 C . 在时间内,两电荷的静电力先减小后增大 D . 在时间内,甲的动能一直增大,乙的动能先减小后增大 5. (2分)在物理学的发展历程中,下面的哪位科学家首先建立了平均速度、瞬时速度和加速度等概念用来描述物体的运动。并首先采用了实验检验猜想和假设的科学方法,把实验和逻辑推理(包括数学演算)和谐地结合起来,从而有力地推进了人类科学的发展 A . 笛卡尔 B . 牛顿 C . 伽利略 D . 亚里士多德 6. (2分)下面的各种说法中正确的是() A . 在实验室可以做“声波碎杯”的实验,若要使杯子碎掉,操作人员一定是把声波发生器的功率调到很大 B . 关于气体的压强,气体的压强是由气体分子间的吸引和排斥产生的 C . 对爱因斯坦光电效应方程EK=hν﹣W可理解为光电子的最大初动能和入射光的频率成正比
2012初三英语二模模拟试题(六) 二、语言知识及运用(共两节,满分20分) 第一节单项选择(共10小题;每小题1分,满分10分) 从16~25各题所给的A、B、C和D项中,选出可以填入空白处的最佳选项,并在答题卡上将该项涂黑。 16. She often _________ new words in the dictionary. That’s good for her. A. looks after B. looks up C. looks down D. looks out 17. —I’m sorry to have kept you waiting. —Oh, not at all. I ________ here for only a few minutes. A. have come B. had been C. has gone D. have been 18. —__________ will the train come, do you know? — In twenty minutes. A. How soon B. How many C. How long D. How much 19. —Is that our headmaster? — No, it _______ be him. He flew to London yesterday. A. mustn’t B. can’t C. may not D. needn’t 20. _________ exciting news. We will have ________ long holiday after the exam A. How; the B. What; a C. How an; the D. What an; a 21. Our teachers are having a meeting in the next room. Miss Li asked us _______ loudly there. A. to not speak B. don’t speak C. not speak D. not to speak 22. Jamie is a young cook _______ wants to improve school dinners. A. whose B. who C. which D. whom 23. _________he is old, ________he walks as fast as a young man. A. As; / B. When; but C. Though; / D. Although; and 24. —What do you think about Tom’s driving skill ? — He drives ___________than he did three years ago. A. much careful B. more carefully C. more careful D. much carefully 25. —Tom, your father went to Hong Kong last week. Do you know _________? — Next month. A. when he will come back B. where will he come back C. when will he come back D. where he will come back 第二节语法选择(共10小题;每小题1分,满分10分) 阅读下面短文,按照句子结构的语法性和上下文连贯的要求,从26~35各题所给的A、
2020年广东省广州市天河区高考化学二模试卷 题号一二三总分 得分 一、单选题(本大题共6小题,共36.0分) 1.化学与生产、生活、科技、环境等密切相关。下列说法正确的是() A. “华为麒麟980”手机中芯片的主要成分是二氧化硅 B. “复兴号”高铁车厢连接处使用的增强聚四氟乙烯板属于有机高分子材料 C. 《本草纲目》中“冬月灶中所烧薪柴之灰,令人以灰淋汁,取硷浣衣”中的硷 是Na2CO3 D. 《梦溪笔谈》中“方家以磁石磨针锋,则能指南”中的磁石主要成分为Fe2O3 2.某合成有机光电材料的中间体,结构简式如图所示。下列说 法正确的是() A. 属于芳香烃 B. 分子式为C18H16O2 C. 苯环上的二氯取代物有6种 D. 性质稳定,不与强酸、强碱、强氧化剂反应 3.钼(Mo)的主要用途是制造特种钢,用CO还原MoO3(白色粉末,加热时变黄) 制备单质Mo的装置如图。下列说法正确的是() A. 装置②中盛有饱和Na2CO3溶液,装置③中盛有浓硫酸,作用是净化CO2 B. 装置①中的稀盐酸可用稀硫酸代替,石灰石可用碳酸钠粉末代替 C. 装置④的作用是制备CO,装置⑤的作用是CO还原MoO3 D. 装置⑥能达到检验MoO3是否被CO还原的目的 4.NaCl是我们生活中必不可少的物质。将NaCl溶于水配成1mol?L-1的溶液,溶解过 程如图所示,下列说法正确的是() A. a离子为Na+ B. 溶液中存在NaCl?Na++Cl- C. 溶液中含有N A个水合Na+和N A个水合Cl- D. 在水分子的作用下,NaCl溶解的同时发生了电离
5.由W、X、Y、Z四种短周期元素组成化合物如图。其中 W、Y、Z分别位于三个不同周期,Y核外最外层电子数 是W核外最外层电子数的二倍,W、X、Y三种简单离 子的核外电子排布相同。下列说法不正确的是() A. 原子半径:W>X>Y>Z B. 常温常压下熔点:W2Y3>X2Y>Z2Y C. X与Y、Y与Z均可形成具有漂白性的化合物 D. W与X的最高价氧化物的水化物可相互反应 6.25℃时,将浓度均为0.1mol/L、体积分别为V a和V b的HA溶液与BOH溶液按不 同体积比混合,保持V a+V b=100mL,V a、V b与混合液的pH的关系如图所示.下列说法正确的是() A. K a(HA)的值与 K b(BOH)的值不相等 B. b 点时,水电离出的 c(H+)=10-7mol/L C. c 点时,c(A-)>c(B+) D. a→c过程中不变 二、双选题(本大题共1小题,共6.0分) 7.一种“固定CO2”的电化学装置如图。该电化学装置放电时可将CO2转化为C和 Li2CO3,充电时仅使Li2CO3发生氧化反应释放出CO2和O2.下列说法正确的是() A. 放电时,Li+向电极X方向移动 B. 放电时,每转移4mole-,理论上生成 1mol c C. 充电时,阳极反应:C+2Li2CO3-4e-=3CO2↑+4Li+ D. 充电时,电极Y与外接直流电源的负极相连 三、简答题(本大题共5小题,共63.0分) 8.氮化镓(GaN)被称为第三代半导体材料,其应用取得了突破性的进展。一种镍催 化法生产GaN的工艺如图:
2017年广州市普通高中毕业班综合测试(二) 理科数学 第Ⅰ卷(共60分) 一、选择题:本大题共12个小题,每小题5分,共60分.在每小题给出的四个选项中,只有一项是符合题目要求的. 1.已知集合{}11A x x =-<,110B x x ? ?=-≥???? ,则A B =∩( ) A .{}12x x ≤< B .{}02x x < 7.已知点()4,4A 在抛物线2 2y px =(()0p >)上,该抛物线的焦点为F ,过点A 作该抛物线准线的垂线,垂足为E ,则EAF ∠的平分线所在的直线方程为( ) A .2120x y +-= B .2120x y +-= C .240x y --= D .240x y -+= 8.在棱长为2的正方体1111ABCD A B C D -中,M 是棱11A D 的中点,过1C ,B ,M 作正方体的截面,则这个截面的面积为( ) A .35 B .35 C .92 D .98 9.已知R k ∈,点(),P a b 是直线2x y k +=与圆22223x y k k +=-+的公共点,则ab 的 最大值为( ) A .15 B .9 C .1 D .53- 10.已知函数()2sin 4f x x πω? ?=+ ??? (0ω>)的图象在区间[]0,1上恰有3个最高点,则ω的取值范围为( ) A .1927,44ππ?????? B .913,22ππ?????? C .1725,4 4ππ?????? D .[)4,6ππ 11.如图,网格纸上小正方形的边长为1,粗线画出的是某三棱锥的三视图,则该三棱锥的体积为( ) A .83 B .163 C .323 D .16 12.定义在R 上的奇函数()y f x =为减函数,若m ,n 满足 ()22f m m -+()220f n n -≥,则当1n ≤32≤ 时,m n 的取值范围为( ) A .2,13??-???? B .31,2?????? C .13,32?????? D .1,13?????? 语法填空的分类练习 考查范围:1 语境(上下文);2 语法:动词(时态、语态、主谓一致、非谓语形式)、名词、代词、冠词、介词、固定搭配、情态动词、复合句、形容词和副词的比较级最高级及构词法、倒装等。 语法填空的能力要求:1.阅读/理解语篇的能力 2.分析句子结构的能力3.熟练运用语法的能力 4.单词拼写能力 一、动词(谓语/非谓语) 给出动词的原形,根据句子结构的需要给出其适当的形式。填动词形式,首先抓住主谓结构,确定主句,剩下的部分,如有连词,则是句子,仍然有主谓结构,否则就用非谓语;是谓语就思考时态,语态,主谓一致,是非谓语就看主动被动,有否先后关系。 1.…The exam, which was originally to be held in our classroom,____(change) to the library at the last minute.(广州二模) 2. The child, Nicole Hobson,________ (take) by her mother to Children's Memorial Hospital about 11 p.m., Wednesday to check …(汕头二模) 3. A transit spokesman said the driver should ______(make) radio call to the control center for help. (汕头二模) 4. One of them was a visitor, saying he wouldn’t have been there if he ______ (watch)the weather forecast the day before. (梅州二模) 5. We must also consider the reaction of the person ______ (receive) the gift. (广州一模) 6 … With the problem ________(solve), I f elt proud of my achievement. .(广州二模) 2014年广州市二模试题与答案 7.化学与生活密切相关,下列说法正确的是 A.蛋白质和油脂都是天然高分子化合物 B.CO2和CH4都是造成温室效应气体 C.蔗糖和麦芽糖水解产物均为葡萄糖 D.苯酚和甲苯遇FeCl3均显紫色 8.下列叙述Ⅰ和叙述Ⅱ均正确并且有因果关系的是 9.设n A为阿伏加德罗常数的数值,下列说法正确的是 A.1mol Cl2与过量的镁铁反应,转移2n A个电子 B.常温下,16g CH4含有8n A个电子 C.1L 0.5 mol·L-1Na2SO4溶液中含有n A个SO42- D.常温常压下,22.4LCO2含有n A个CO2分子 10.水溶液中能大量共存的一组离子是 A.H+、NO3-、I-、Cl- B.Cu2+、Br-、H+、SO42- C.Al3+、Mg2+、CO32-、NO3- D.NH4+、Cl-、OH-、HCO3- 11.短周期元素X、Y、Z、W、R的原子序数依次增大,X单质在暗处与H2剧烈化合并发生爆炸,Y位于第IA族,Z所处的周期序数与族序数相等,W元素最高正价与最低负价之和为0,R与X同族,则 A.原子半径:Z>Y>X B.X与R的核电荷数相差18 C.气态氢化物稳定性:W>R D.Y与Z两者最高价氧化物对应的水化物能相互反应 12.下列实验的现象与对应结论均正确的是 22.室温下,将一元酸HA 溶液和NaOH 溶液等体积混合,实验数据如表: 下列说法正确的是 A .实验①反应前HA 溶液中c (H +)=c (OH - )+ c (A - ) B .实验①反应后溶液中c (A - )>c (Na +) C .实验②反应前HA 溶液浓度x >0.2 mol·L - 1 D .实验②反应后溶液中c (A - )+ c (HA)= c (Na +) 23.某小组为研究原电池原理,设计如图装置,下列叙述正确的是 A .装置I ,铜片上有O 2逸出 B .装置I ,锌片溶解,发生还原反应 C .装置 II ,电池反应为:Zn+ Cu 2+= Zn 2++ Cu D .装置II ,外电路中,电子从锌电极流向铜电极 CuSO 4溶液 H 2SO 4溶液 I II 2020年广东省广州市高考化学二模试卷 一、单选题(本大题共7小题,共42.0分) 1.处理锂离子二次电池正极废料铝钴膜(含有LiCoO2、Al等)的一种工艺如下,下列有关说法不正 确的是 A. 碱浸的目的是溶解铝 B. 酸溶时H2O2被还原 C. H2SO4/H2O2可改用浓盐酸 D. 铝、钴产物可再利用 2.设N A为阿伏加德罗常数的值,下列说法正确的是() A. 标准状况下,1.12LCCl4含有Cl原子数目为0.4N A B. 7.1g氯气与足量NaOH溶液反应转移电子数为0.2N A C. 常温常压下,4.4gCO2与N2O混合气体中含有的原子总数为0.3N A D. 常温常压下,1mol任何物质都含有阿伏加德罗常数个分子 3.下列实验操作能达到实验目的是() 选项实验目的实验操作 A 探究反应物浓度对反应 速率的影响 向2支盛有10mL不同浓度NaHSO3溶液的试管中同 时加入3mL8%H2O2溶液 B 判断苯酚与碳酸的酸性 强弱 向C6H5ONa溶液中通入CO2看溶液是否变浑浊 C制备Fe(OH)3胶体将NaOH浓溶液滴加到饱和FeCl3溶液中 D 配制0.2000mol/L的 NaOH溶液 称取2.0g固体NaOH于烧杯中,加入少量蒸馏水溶 解,转移至250mL容量瓶中定容 4.下列关于2,3?二甲基?1?丁烯()的说法错误的是() A. 其一氯代物有四种(不考虑立体异构) B. 与氢气加成的产物为异丁烷的同系物 C. 所有碳原子可能在同一平面 D. 与甲基环戊烷()互为同分异构体 5.W、X、Y、Z均是短周期元素,X、Y、Z处于同一周期,W、X、Z的简单离子具有相同的电 子层结构,W的最高氧化物的水化物可与其最简单的气态氢化物反应生成易溶于水的盐,X的氧化物具有两性,Y的最高正价与最低负价的代数和为0,下列说法正确的是() A. 离子半径:W>Z>X B. 单质熔点:W>Z C. 最高正价:W>X>Y>Z D. 原子序数:Z>W>X>Y 6.25℃时,0.1mol·L?1的NaHC2O4溶液的pH<7,下列关系正确的是() A. c(H+) 1 2017年广州市普通高中毕业班综合测试(二) 理综物理 2017.04 第Ⅰ卷 二、选择题:本题共8小题,每小题6分。在每小题给出的四个选项中,第14~17题只有一项符合题目要求,第18~21题有多项符合题目要求。全部选对的得6分,选对但不全的得3分,有选错的得0分。 14.同一位置同向先后开出甲、乙两汽车,甲先以初速度v 、加速度a 做匀加速直线运动;乙 在甲开出t 0时间后,以同样的加速度a 由静止开始做匀加速直线运动。在乙开出后,若以乙为参考系,则甲 A .以速度v 做匀速直线运动 B .以速度at 0做匀速直线运动 C .以速度v +at 0做匀速直线运动 D .停在乙车前方距离为2 002 1at vt + 的地方 15.如图,小木块以某一竖直向下的初速度从半球形碗口向下滑到碗底,木块下滑过程中速 率不变,则木块 A .下滑过程的加速度不变 B .所受的合外力大小不变 C .对碗壁的压力大小不变 D .所受的摩擦力大小不变 16.有一钚的同位素Pu 23994核静止在匀强磁场中,该核沿与磁场垂直的方向放出x 粒子后,变成 铀(U )的一个同位素原子核。铀核与x 粒子在该磁场中的旋转半径之比为1∶46,则 A .放出的x 粒子是He 42 B .放出的x 粒子是e 0 1- C .该核反应是核裂变反应 D .x 粒子与铀核在磁场中的旋转周期相等 17.如图,带电粒子由静止开始,经电压为U 1的加速电场加速后,垂直电场方向进入电压为 U 2的平行板电容器,经偏转落在下板的中间位置。为使同样的带电粒子, 从同样的初始位 2 置由静止加速、偏转后能穿出平行板电容器,下列措施可行的是 A .保持U 2和平行板间距不变,减小U 1 B .保持U 1和平行板间距不变,增大U 2 C .保持U 1、U 2和下板位置不变,向下平移上板 D .保持U 1、U 2和下板位置不变,向上平移上板 18.如图a ,物体在水平恒力F 作用下沿粗糙水平地面由静止开始运动,在t=1s 时刻撤去恒 力F 。物体运动的v -t 图象如图b 。重力加速度g =10m/s 2 ,则 A .物体在3s 内的位移s =3m B .恒力F 与摩擦力f 大小之比F :f =3:1 C .物体与地面的动摩擦因数为30.=μ D .3s 内恒力做功W F 与克服摩擦力做功W f 之比W F :W f =3:2 19.在同一平面内有①、②、③三根等间距平行放置的长直导线,通入的电流强度分别为1A 、 2A 、1A ,②的电流方向为d c →且受到安培力的合力方向水平向右,则 A .①的电流方向为b a → B .③的电流方向为f e → C .①受到安培力的合力方向水平向左 D .③受到安培力的合力方向水平向左 20.如图, a 、b 两个带电小球分别用绝缘细线系住,并悬挂在 它们恰好在同一水平面上,此时两细线与竖直方向夹角α<下落过程中 A .两球始终处在同一水平面上 A 1a b e f ① ③ 2A 1左右 2017年广东省广州市高考化学二模试卷(J) 副标题 一、单选题(本大题共7小题,共7.0分) 1.化学与航空、航天密切相关,下列说法错误的是 A. 镁用于制造轻合金,是制造飞机、火箭的重要材料 B. 高纯度硅制成的光电池,可用作火星探测器的动力 C. 聚脂纤维属于新型无机非金属材料,可制作宇航服 D. 高温结构陶瓷耐高温、耐氧化,是喷气发动机的理想材料 【答案】C 【解析】解:镁合金硬度大,密度小,可用于制造汽车、飞机、火箭,故A正确; B.硅属于半导体材料,高纯度硅制成的光电池,可用作火星探测器的动力,故B正确; C.制作航天服的聚酯纤维属于有机物,不是无机材料,属于合成有机高分子材料,故C 错误; D.高温结构陶瓷耐高温,不怕氧化、密度小,所以高温结构陶瓷时喷气发动机的理想材料,故D正确。 故选:C。 A.镁合金硬度大,密度小; B.硅属于半导体材料; C.聚酯纤维为有机高分子材料 D.高温结构陶瓷耐高温,不怕氧化、密度小. 本题考查较为综合,侧重于化学与生活、生产的考查,有利于培养学生的良好的科学素养、提高学生学习的积极性,注意相关基础知识的积累,难度不大. 2.下列关于有机化合物的说法正确的是 A. 氯乙烯和溴乙烷均能发生加成反应 B. 花生油和玉米油都是可皂化的饱和酯类 C. 天然气和水煤气的主要成分都是烃类 D. 分子式为的单取代芳烃,其可能的结构有4种 【答案】D 【解析】解:溴乙烷不能发生加成反应,故A错误; B.植物油多为不饱和酯类,故B错误; C.水煤气的主要成分为CO、氢气,不属于烃类,故C错误; D.分子中含有一个苯环,侧链是烷基,为,的异构体有:、 、、,故符合条件的结构有4种,故D正确。故选:D。 A.含有不饱和键的有机物,一般可发生加成反应; B.植物油多为不饱和酯类; C.水煤气的主要成分为CO、氢气; D.分子中含有一个苯环,侧链是烷基,为,书写的异构体,确定符合条件的同分异构体数目. 本题考查有机物的结构和性质,为高频考点,侧重考查学生的分析能力,注意把握有机 广东省广州市中考数学二模试卷 姓名:________ 班级:________ 成绩:________ 一、选择题(满分24分) (共6题;共24分) 1. (4分)(2019·黄浦模拟) 下列自然数中,素数是() A . 1 B . 2 C . 4 D . 9 2. (4分)(2019·湖南模拟) 下列计算正确的是() A . B . C . D . 3. (4分)(2017·蒸湘模拟) 如图,边长为1的正方形ABCD中,点E在CB的延长线上,连接ED交AB于点F,AF=x(0.2≤x≤0.8),EC=y.则在下面函数图象中,大致能反映y与x之间函数关系的是() A . B . C . D . 4. (4分)(2017·微山模拟) 今年某县有1万名初中和小学生参加全国义务教育质量抽测,为了了解1万名学生的抽测成绩,从中抽取500名学生抽测成绩进行统计分析,在这个问题中数据500是() A . 总体 B . 个体 C . 一个样本 D . 样本容量 5. (4分) (2019九上·黄浦期末) 已知、、都是非零向量.下列条件中,不能判定∥ 的是() A . | |=| | B . =3 C . ∥ ,∥ D . =2 ,=-2 6. (4分)⊙O1的半径为1, ⊙O2的半径为8,两圆的圆心距为7,则两圆的位置关系为() A . 相交 B . 内切 C . 相切 D . 外切 二、填空题:(满分48分) (共12题;共48分) 7. (4分)(2020·信阳模拟) 计算:-(-)=________. 8. (4分) (2011·成都) 分解因式:x2+2x+1=________. 9. (4分) (2016七上·萧山期中) 能够说明“ =x不成立”的x的值是________(写出一个即可). 10. (4分)已知,平面直角坐标系中,O为坐标原点,一次函数y= x+2的图象交x轴于点A,交y轴于点B,则△AOB的面积=________. 11. (4分)(2018·广东模拟) 不等式组的解集是________ 12. (4分)(2019·中山模拟) 关于x的一元二次方程x2-2x+m=0有两个不相等的实数根,则实数m的取值范围为________ 13. (4分) (2019·岳阳) 分别写有数字、﹣1、0、π的五张大小和质地均相同的卡片,从中任意1高考语法填空分类练习
2014年广州二模理综化学试题及答案
2020年广东省广州市高考化学二模试卷 (含答案解析)
2017年广州市二模物理试卷
2017年广东省广州市高考化学二模试卷(J)
广东省广州市中考数学二模试卷