
必修一-第三章-第三节-铁及其化合物
【要点梳理】
要点一、铁
1.铁的存在
铁元素在地壳中的含量仅次于O、Si、Al,主要以+2价和+3价化合物的形式存在。
2.物理性质
常温下,纯铁是银白色具有金属光泽的金属(纯铁的抗蚀力很强),易导电、导热,有延展性;铁粉为黑色。铁的熔沸点都很高:熔点1535℃,沸点2750℃。铁能被磁体吸引,在磁场的作用下,自身也能产生磁性
3.化学性质
当跟弱氧化剂反应时:Fe - 2e-= Fe2+
当跟强氧化剂反应时:Fe - 3e-= Fe3+
(1)与非金属的反应:
3Fe + 2O2Fe3O4 2Fe + 3Cl22FeCl3 2Fe + 3Br2= 2FeBr3
Fe + I2= FeI2 Fe + S FeS
(2)与某些盐(如CuSO4)溶液的反应:
Fe+Cu2+= Fe2++Cu
(3)与酸的反应:
与非氧化性酸:Fe+2H+= Fe2++H2↑
(4)与水蒸汽的反应:3Fe + 4H2O(g)Fe3O4 + 4H2
注意:
①现象:用火柴点燃肥皂泡,听到爆鸣声
②湿棉花的作用:提供反应所需水蒸气
③肥皂液的作用:“收集”H2
要点二、铁的化合物
1.铁的氧化物
(1)FeO不稳定,在空气里受热,就迅速被氧化成Fe3O4
(2)Fe2O3常用作红色油漆和涂料,赤铁矿(主要成分是Fe2O3)是炼铁的原料
(3)Fe3O4可以看成由FeO和Fe2O3按物质的量之比1∶1组合而成的复杂氧化物,通常也可写成FeO·Fe2O3的形式。FeO、Fe2O3属于碱性氧化物,Fe3O4不属于碱性氧化物
(4)铁的氧化物比较
铁的氧化物氧化亚铁氧化铁四氧化三铁
化学式FeO Fe2O3Fe3O4
铁元素化合价+2 +3 +2、+3
颜色、状态黑色粉末红色粉末黑色晶体
俗称铁红
溶解性均不溶于水
与HCl反应离子方程式FeO + 2H+ = Fe2+ + H2O Fe2O3+ 6H+ = 2Fe3+ + 3H2O Fe3O4 + 8H+ = 2Fe3+ + Fe2+ + 4H2O
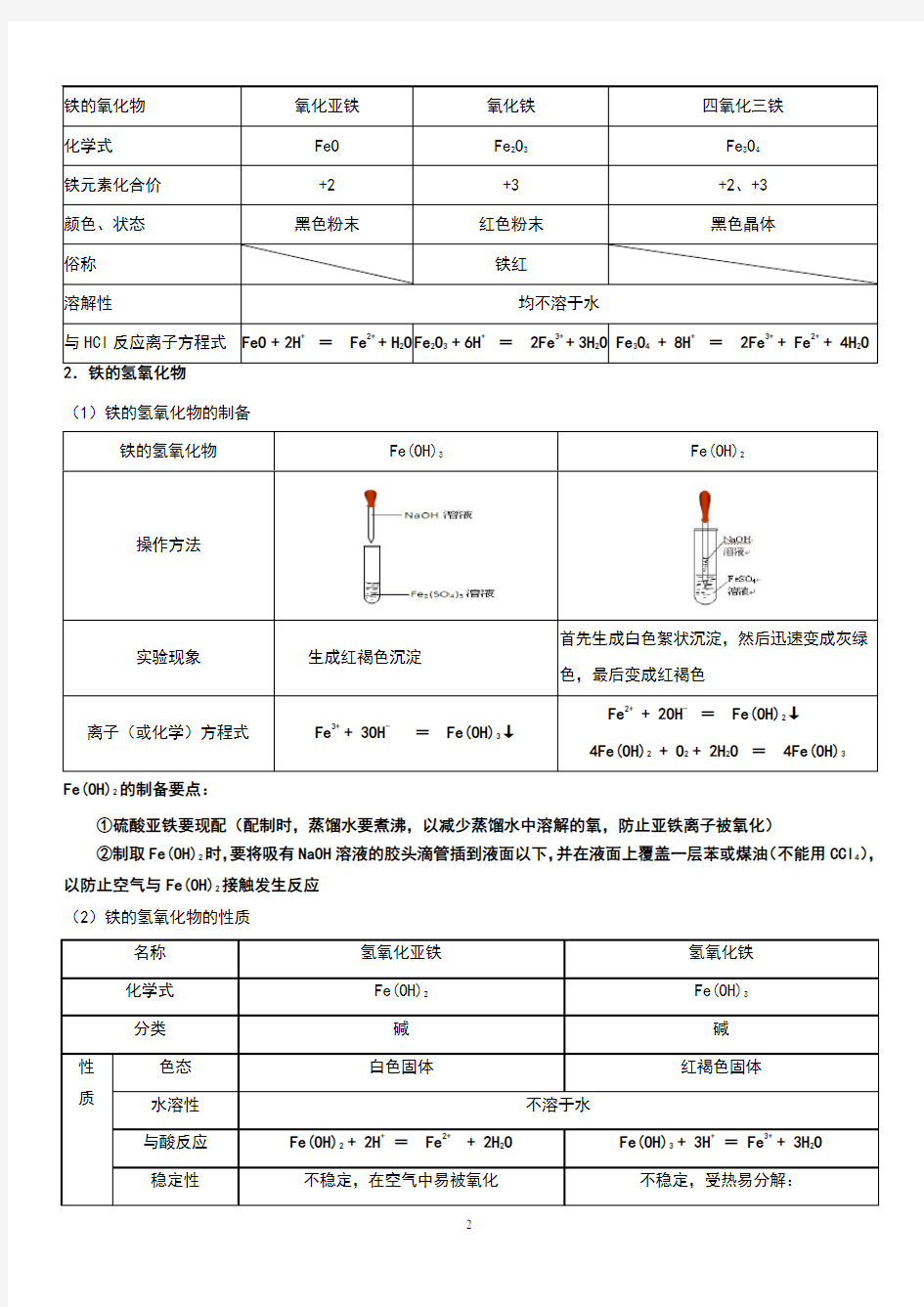
(1)铁的氢氧化物的制备
铁的氢氧化物Fe(OH)3Fe(OH)2
操作方法
实验现象生成红褐色沉淀
首先生成白色絮状沉淀,然后迅速变成灰绿
色,最后变成红褐色离子(或化学)方程式Fe3+ + 3OH-= Fe(OH)3↓
Fe2+ + 2OH- = Fe(OH)2↓
4Fe(OH)2 + O2 + 2H2O= 4Fe(OH)3
Fe(OH)2的制备要点:
①硫酸亚铁要现配(配制时,蒸馏水要煮沸,以减少蒸馏水中溶解的氧,防止亚铁离子被氧化)
②制取Fe(OH)2时,要将吸有NaOH溶液的胶头滴管插到液面以下,并在液面上覆盖一层苯或煤油(不能用CCl4),以防止空气与Fe(OH)2接触发生反应
(2)铁的氢氧化物的性质
名称氢氧化亚铁氢氧化铁
化学式Fe(OH)2Fe(OH)3
分类碱碱
性质
色态白色固体红褐色固体
水溶性不溶于水
与酸反应Fe(OH)2 + 2H+= Fe2++ 2H2O Fe(OH)3 + 3H+= Fe3+ + 3H2O 稳定性不稳定,在空气中易被氧化不稳定,受热易分解:
2Fe(OH)3Fe2O3 +3H2O 转化4Fe(OH)2 + O2+ 2H2O = 4Fe(OH)3
常见的亚铁盐主要有FeSO4·7H2O(绿矾),铁盐有FeCl3、Fe2(SO4)3等
Fe2+、Fe3+的性质及检验方法:
离子Fe3+Fe2+
颜色黄色淡绿色
与碱反应Fe3++3OH—= Fe(OH)3↓Fe2++2OH—= Fe(OH)2↓
氧化性、还原性氧化性:2Fe3++Fe = 3Fe2+氧化性:Fe2+ + Zn = Zn2+ + Fe
还原性:2Fe2 ++ Cl2= 2Fe3+ + 2Cl—
检验方法加碱(NaOH)法
①现象:红褐色沉淀
②反应:Fe3+ + 3OH-= Fe(OH)3↓
①现象:白色沉淀???→
迅速灰绿色???→
最终红褐色沉淀
②反应:Fe2++2OH-= Fe(OH)2↓
4Fe(OH)2 + O2 + 2H2O = 4Fe(OH)3
加盐(SCN-)法
(显色反应)
①现象:加入KSCN溶液,溶液变为红色
②反应:Fe3+ + 3SCN-= Fe(SCN)3(红
色)
①现象:加入KSCN溶液无明显现象,再滴入氯水
变成红色溶液
②反应:2Fe2+ + Cl2= 2Fe3+ + 2Cl-
Fe3+ + 3SCN-= Fe(SCN)3(红色)
利用氧化性及还原性加入淀粉KI溶液,变为蓝色加入酸性KMnO4溶液,紫色褪去
要点三、Fe2+、Fe3+、Fe的相互转变——“铁三角”
1.Fe只具有还原性,可以被氧化剂氧化成Fe2+、Fe3+(1)Fe能被S、Fe3+、Cu2+、H+等较弱氧化剂氧化为Fe2+
如Fe + S △
FeS,Fe + 2Fe3+= 3Fe2+
(2)Fe能被Cl2、Br2、HNO3、浓H2SO4等强氧化剂氧化为Fe3+
如2Fe + 3Cl2点燃
2FeCl3
2.Fe2+既具有还原性又具有氧化性,可以被氧化为Fe3+,也可以被还原为Fe (1)当Fe2+遇到强氧化剂O2、Cl2、HNO3、KMnO4等时,被氧化为Fe3+,如2Fe2+ + Cl2= 2Fe3+ + 2Cl-
(2)当Fe2+遇到C、Al、Zn、CO等还原剂时,可以被还原为Fe
如Fe2+ + Zn = Zn2+ + Fe,FeO + CO △
Fe + CO2
3.Fe3+具有较强氧化性,可被还原为Fe2+或Fe
(1)Fe3+被C、CO、活泼的金属(钾、钠、钙除外)还原为Fe 如Fe2O3 + 3CO2Fe + 3CO2,Fe2O3 + 2Al2Fe + Al2O3。
(2)Fe3+被KI、H2S、Fe、Cu、SO2等还原为Fe2+
如2Fe3+ + Cu = 2Fe2+ + Cu2+