
O2选择氧化烷烃新进展
王荣民1,2 王云普1 李树本2
(1西北师范大学化学系 兰州 730070)
(2中国科学院兰州化学物理研究所羰基合成与选择氧化国家重点实验室 730000)
摘 要 综述了90年代以来有关金属络合物催化O2选择氧化烷烃研究的进展。如:卤代卟啉铁络合物在无还原剂存在下催化烷烃羟基化,类卟啉金属络合物催化烷烃氧化及高分子或固载化金属络合物的催化性能。
催化氧化作用 金属络合物 分子氧 烷烃
Abstract R esearches on the aerob ic ox idati on of alkane catalyzed by m etal comp lexes w ere re2 view ed.
Key words A lkane,A erob ic ox idati on,M etal comp lexes,Catalyzing
分子氧对于地球上所有动物,包括人类来说都是至关重要的,由于它为生命提供能量、促进新陈代谢。在化学工业中也同样重要,作为最通用的氧化剂,分子氧已用于大规模生产:如最大商业化的匀相催化氧化—在水溶性钴盐或锰盐催化下由对二甲苯空气氧化生产对苯二甲酸;以及异丙苯氧化制苯酚等。这些成功的过程,由于操作中的温度或压力的因素而受到限制。因此,化学家们热切地寻求一些在温和条件下能有效进行的氧化反应。在环境保护日益受到重视的今天,使用分子氧作氧化剂更具现实意义。
由于生物生命活动体系中的氧化反应是在十分温和的条件下进行的,因此,生物模拟研究主要集中在配体结构的改进以模拟血蓝蛋白(hem ocyan in)和血红蛋白的功能。细胞色素P2450(一个含血红蛋白的典型的铁络合物)催化氧化机理已得到证实(如图1所示)。
已进行了大量的研究工作来模拟生物氧化反应[1]。90年代以来,有关卟啉类和非卟啉类金属络合物活化分子氧及在催化氧化反应中的应用有了长足的进步,在此,只对金属络合物活化分子氧及在催化O2氧化烷烃做一综述。
1 金属卟啉催化烷烃羟基化
金属卟啉络合物按模拟生物形式催化烷烃羟基化,一般需要(a)化学计量氧原子给体;(b)消耗助还原剂;(c)由电化学还原;(d)光助催化。
111 高卤代金属卟啉催化氧化性能
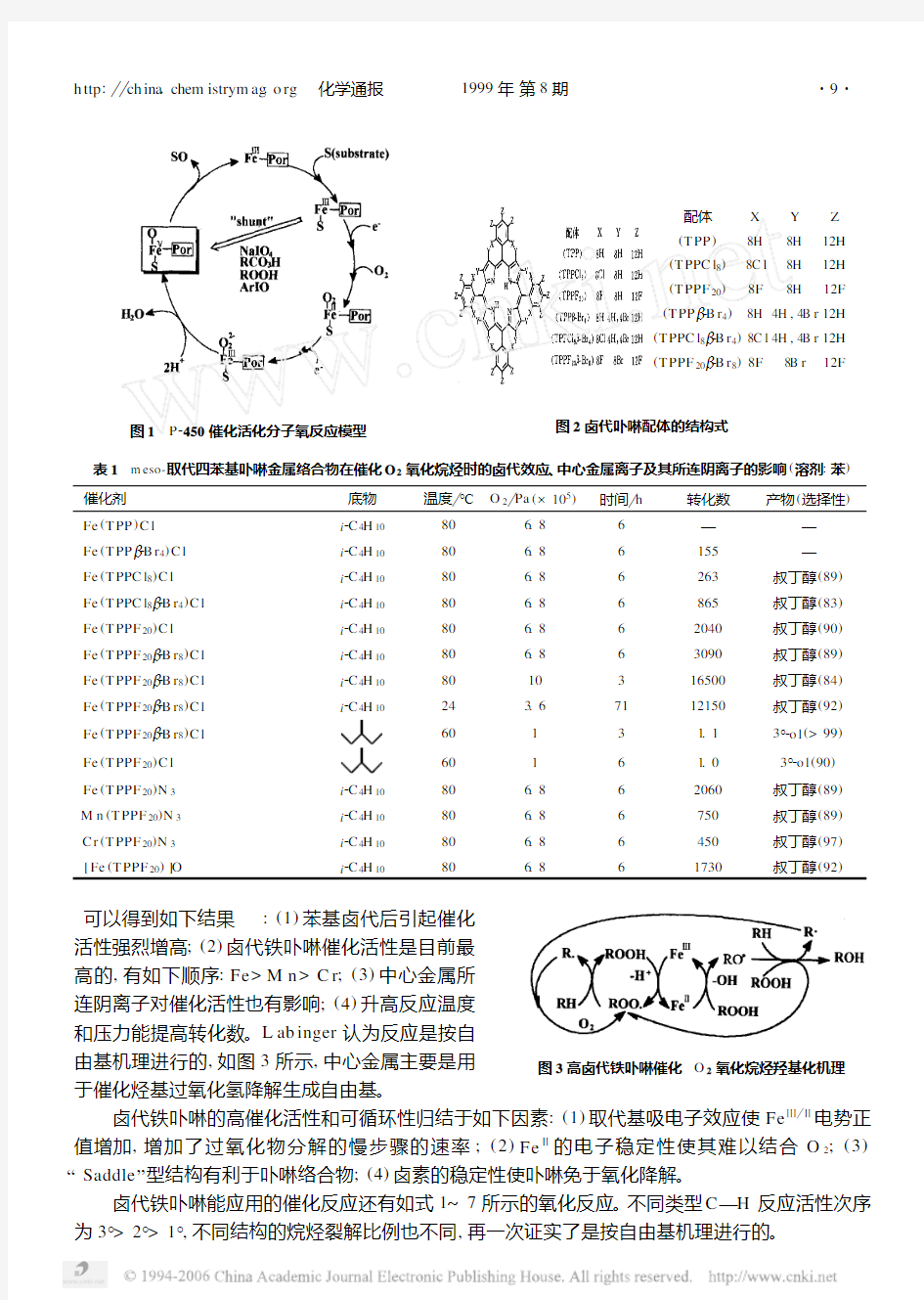
L yon s[2]和L ab inger[3]以及M an suy[4]小组的最新研究表明,卤代金属卟啉是用O2直接氧化烷基生成醇和羰基化合物有效的催化剂,而无需助还原剂、化学计量氧或光、电化学技术辅助,产率可达90%。其中,卤代卟啉的结构如图2所示。表1列出了典型的一些结果。
王荣民 男,33岁,理学博士,教授,主要从事高分子金属络合物的性能研究和有机化学的教学工作
国家自然科学基金资助项目
1998204215收稿,1998210210修回
图1 P 2450催化活化分子氧反应模型
配体
X Y Z (T PP )8H 8H 12H (T PPC l 8)8C l 8H 12H (T PPF 20)8F
8H
12F
(T PP Β2B r 4)
8H 4H ,4B r 12H
(T PPC l 8Β2B r 4)
8C l
4H ,4B r
12H (T PPF 20Β2B r 8)8F
8B r
12F
图2 卤代卟啉配体的结构式
表1 m eso -取代四苯基卟啉金属络合物在催化O 2氧化烷烃时的卤代效应、中心金属离子及其所连阴离子的影响(溶剂:苯)催化剂
底物
温度 ℃
O 2 Pa (×105)
时间 h
转化数产物(选择性)
Fe (T PP )C l
i 2C 4H 10806.86—
—Fe (T PP Β2B r 4)C l
i 2C 4H 10806.86155—Fe (T PPC l 8)C l
i 2C 4H 10806.86263叔丁醇(89)Fe (T PPC l 8Β2B r 4)C l
i 2C 4H 10806.86865叔丁醇(83)Fe (T PPF 20)C l
i 2C 4H 10806.862040叔丁醇(90)Fe (T PPF 20Β2B r 8)C l i 2C 4H 10806.863090叔丁醇(89)Fe (T PPF 20Β2B r 8)C l i 2C 4H 108010316500叔丁醇(84)Fe (T PPF 20Β2B r 8)C l i 2C 4H 10
243.67112150叔丁醇(92)
Fe (T PPF 20Β2B r 8)C l
60131.13°2o l (>99)Fe (T PPF 20)C l 60
161.03°2o
l (90)
Fe (T PPF 20)N 3i 2C 4H 10806.862060叔丁醇(89)M n (T PPF 20)N 3i 2C 4H 10806.86750叔丁醇(89)C r (T PPF 20)N 3i 2C 4H 10806.86450叔丁醇(97)[Fe (T PPF 20)]O
i 2C 4H 10
80
6.8
6
1730
叔丁醇(92)
图3 高卤代铁卟啉催化O 2氧化烷烃羟基化机理 可以得到如下结果:(1)苯基卤代后引起催化活性强烈增高;(2)卤代铁卟啉催化活性是目前最高的,有如下顺序:Fe >M n >C r ;(3)中心金属所连阴离子对催化活性也有影响;(4)升高反应温度
和压力能提高转化数。L ab inger 认为反应是按自由基机理进行的,如图3所示,中心金属主要是用于催化烃基过氧化氢降解生成自由基。
卤代铁卟啉的高催化活性和可循环性归结于如下因素:(1)取代基吸电子效应使Fe
电势正值增加,增加了过氧化物分解的慢步骤的速率;(2)Fe 的电子稳定性使其难以结合O 2;(3)“Saddle ”型结构有利于卟啉络合物;(4)卤素的稳定性使卟啉免于氧化降解。卤代铁卟啉能应用的催化反应还有如式1~7所示的氧化反应。不同类型C —H 反应活性次序为3°>2°>1°,不同结构的烷烃裂解比例也不同,再一次证实了是按自由基机理进行的。
高卤代铁卟啉催化烷烃氧化反应式 在无助催化剂时,多氟卟啉络合物催化体系需
一定的压力和温度。当有还原剂如乙醛存在下氧化烷烃[5],如环己烷、正己烷、金刚烷及乙苯时,Co (T PPF 20)的催化活性要比M n (T PPF 20)C l 、R u (T PPF 20)(CO )高,氧化金刚烷的转化数分别为270、240、190。
112 高分子固载金属卟啉
高卤代铁卟啉由于卤素原子对卟啉骨架环的保护作用,使其不能被其它卤代铁卟啉分子催化氧化,因此十分稳定,表现出高活性及可循环性。当金属卟啉固载于有机高分子或无机高分子后,也能达到类似的效果。计亮年等以高分子担载金属卟啉[6]、分子氧、抗坏血酸和底物细胞色素P 2450模拟体系,也实现了在常温常压下环己烷选择氧化为环己醇和环己酮,其中聚苯乙烯担载铁(III )卟啉转化数可达2617。沸石分子筛微孔也具有稳定作用[7],当m eso 2
四(2,4,62三甲基苯基)卟啉钴(CoTM PP )包封于沸
石后用于催化O 2氧化环己烷时,催化活性与多氟卟啉钴络合物(CoT
PPF 20)相当。但是,铁卟啉和锰卟啉包封于沸石后,催化活性不如多氟卟啉钴络合物(CoT PPF 20)。这是由于铁卟啉和锰卟啉的氧化电势比钴卟啉低,催化氧化受到高价金属氧化物(M O )的影响。
2 类卟啉金属络合物催化体系
金属卟啉由于其结构核心与细胞色素P 2450相同而表现出高的催化活性,但因成本较高、难以制备手性络合物等使其受到限制,因此,研究结构与其相似的类卟啉金属络合物受到关注。
图4 几种用于氧化的催化剂的结构
211 水杨醛希夫碱络合物
在Co 2SB O 2 异丁醛体系中[8],环己烷、环辛烷室温氧化生成醇和酮,转化率在13%~20%,醇 酮比分别为21 79、33 67,甲基环己烷室温氧化生成醇。交联聚苯乙烯共价键担载L 2酪氨酸水
杨醛希夫碱钴络合物(PS 2SB 2Co )[9]催化环己烷氧化,在150℃,5144×105
Pa O 2下转化率为14115%,对环己醇和环己酮选择性分别为6619%和3311%。212 冠醚络合物
冠醚铜络合物[10]作为金属卟啉的替代物,与乙醛共同作用下,能高效催化分子氧氧化烷烃,产
物为相应的醇和酮,转化数高达16200。对乙苯氧化可在室温下进行。
213 Β2二酮类络合物
可溶性Β2二酮酯的铁(III)、镍(II)、钴(II)络合物[11],在室温、常压、O22异戊醛催化体系,氧化金刚烷高选择性得到金刚醇,但对环烷烃催化氧化活性很低,转化率Φ3%。
214 氮杂环络合物
江英彦[12]等将N,N′2双[222(苯并咪唑甲基)]胺2铁(I V)络合物固载于Si O2,得到Si O22BBA2 Fe,在亚甲基兰2HOA c2Zn2O2氧化体系,室温催化氧化环己烷得到环己醇和环己酮,转化数可达11156(m o l m o l.Fe.h)。Ku ru su[13]以32二甲氨基丙基硅氧烷改性硅胶后与铁、铜形成的络合物催化室温下氧化环己烷和甲基环己烷,产率在0145%~27%之间,对醇的选择性在70%~94%之间。
3 Gif体系
基于模拟10亿年前地球自然环境中催化氧化反应的Gif体系[14],是催化烷烃分子氧氧化的非卟啉体系,主要组分为:乙酸或其它酸(质子源)、吡啶(溶剂)、铁粉(电子源)及铁催化剂前体。在温和条件下进行分子氧氧化饱和烃,如金刚烷、取代环烷烃,酮的产率在3~26%,而醇的产率大约在015~215%范围。B arton提出在H2O2为氧化剂,反应历程中有分子氧参与,如式28所示。另外Zn、H2 Pd都可做电子源。R u络合物催化环己烷氧化生成环己酮(选择性66%,转化率11%)和环己醇(选择性29%)、金刚烷氧化生成金刚醇(选择性75%,转化率36%)。
Fe V=O→Fe V—CH H2O2
Fe —CH+O2
O2
Inserti on
Fe —O—O—CH
H2O
H—O—O—CH→O(8)
Fe —OH
4 烷基芳香烃侧连的氧化
烷基芳香烃用强氧化剂如K2C r2O7、K M nO4等氧化时,侧连彻底氧化为苯甲酸。当采用催化剂存在下的分子氧选择氧化,可得到所需的部分氧化产物(如醇、酮)。
411 高分子担载金属盐
醋酸钴的醋酸溶液能催化异丙苯自氧化,对苯基异丙基过氧化氢(CH P)的选择性在90%~96%范围内。徐樱芳等[15]将金属盐担载于聚丙烯酸微粒(B i o2R ex70),90℃能很有效的催化异丙苯自氧化,对异丙苯过氧化氢的选择性高达99%金属离子催化活性次序为:M n(II)>Cu(II)>Co (II)>N i(II)>Fe(II)。这对高产率制备苯酚十分有利。
412 水杨醛希夫碱络合物
水杨醛希夫碱(Co2SB)在22氧代环戊甲酸乙酯做还原剂时[16],催化芳基侧连氧化得到酮。如表2所示。苄基碳为叔碳时发生消除反应。
表2 Co-SANSE催化苄基O2氧化(60℃,15h,CH3CN)
Sub.P rod.y %Sub.P rod.y %
Ph Ph
O
Ph Ph
69
O
61
Ph
O
Ph
45
Ph Ph47
O
66
413 高分子卟啉及类卟啉金属络合物
作为模拟细胞色素P2450的一个新方向,卟啉金属络合物与高分子相结合,出现一些不同的特性,在催化氧化反应中所使用的氧化剂也有多种[17]。王云普等[18]合成了平面聚合的高分子卟啉金属络合物及一系列高分子类卟啉金属络合物,能催化乙苯O2氧化生成苯乙醇和苯乙酮,异丙苯O2氧化生成22苯基22丙醇、苯乙酮、对甲基苯乙酮。选择性可达99%,不同金属离子催化活性次序为: Co>M n>Cu。
CH2CH3
O2 PPo r2M
CHCH3
OH
+
COCH3
(9
)
O2
PPo r2M
OH
+
COCH3
+
CH3
COCH3
(10)
末端以乙酰丙酮功能化的聚乙二醇钴络合物在O2氧化乙苯时表现出明显活性(与非高分子类相比)[19],产物仅为苯乙酮。E rn st[20]将CoPc以“sh i p2in2bo ttle”形式固载于沸石分子筛E M T,可催化乙苯氧化生成苯乙酮和苯乙醇,最大转化数为22000。Ku ru su将蒙脱土改性后制得钴络合物[M on tm2Co]1和[M on tm2Co]2,[m on tm2Co]1催化乙苯转化率为73%,对苯乙酮的选择性为67%。[M on tm2Co]2只有H2O2(底物的1 16)参与下,24h r后催化乙苯转化率为40%,对苯乙酮的选择性为70%。
图5 改性蒙脱土
5 结束语
作为O2氧化烷烃的催化剂,多卤代铁卟啉络合物由于在相对温和的条件下具有很高的催化活性且无须消耗助还原剂而受到注目。但其缺点是成本高、反应压力由6189×109Pa降到常压时,转化数也随之迅速降低。通过研究取代卟啉络合物催化氧化机理和取代效应,能给我们一些启示来合成更有前途的催化剂,如配体的卤化、络合物的高分子化或固载化都有可能起到稳定作用及提高催化活性的作用。类卟啉金属络合物,尤其是高分子类卟啉金属络合物由于较高的催化活性和选择性以及易于合成也受到广泛关注,这些研究方向正在得到重视。
(下转第7页)
[32] H aas L A,Khalafalla S E.K inetic Evidence of a R eactive Interm ediate in R educti on of SO2w ith CO.J.Catal.,1973,29:264
~269.
[33] H appel J,H natow M A,Bajars L et al.L anthanum T itanate Catalyst2SO2R educti on.Ind.Eng.Chem.,P rod.R es.D ev.,
1975,14(3):154~158.
[34] Bazes J G,Caretto L S,N obe K.Catalytic R educti on of SO2w ith CO on Cobalt O xides.Ind.Eng.Chem.,P rod.R es.D ev.,
1975,14(4):264~268.
[35] H ibbert D B,Campbell R H.F lue Gas D esulphurisati on:R emoval of SO2by CO on Sulph ided L a1-x Sr x CoO3.A pp l.Catal.,
1988,41:289~299.
[36] H ibbert D B,T seung A C C.T he R educti on of SO2by CO on a L a0.5Sr0.5CoO3Catalyst.J.Chem.T ech.B i o techno l.,1979,
29:713~722.
[37] Bagllo J A.L anthanum O xysulfide as a Catalyst fo r O xidati on of CO and CO S by SO2.Ind.Eng.Chem.,P rod.R es.
D ev.,1982,21(1):38~41.
[38] M a J X,Fang M,L au N T.O n the Synergis m betw een L a2O2S and CoS2in the R ducti on of SO2by CO.J.Catal.,1996,158:
251~259.
[39] L iu W,Sarofi m A F,Stephanopoulo s M F.R educti on of SO2by CO to E lem ental Sulfur over Compo site O xide Catalysts.
A pp l.Catal.B,1994,4:167~186.
[40] M a J X,Fang M,L au N T.A ctivati on of L a2O3fo r the Catalytic R educti on of SO2by CO.J.Catal.,1996,163:271~278.
[41] M a J X,Fang M,L au N T.T he Catalytic R educti on of SO2by CO over L a2O2S.A pp l.Catal.,1997,150:253~268.
[42] Karl P S,H illN J,Peter E D.Catalytic D ecompo siti on of Ammonia from Coke2oven Gas.Iron and Steel Eng.,1990,(12):42
~46
(上接第12页)
参考文献
[1] M ontanari F,Casella L.M etallopo rphyrins Catalyzed O xidati on,L ondon:K luw er A cadem ic Publisher,1994.
[2] L yons J E,E llis P E,M ayers H K.J.Catal.1995,155:59~73.
[3] Grinstaff M W,H ill M G,L abinger J et al.Science,1994,264:1311~1313.
[4] Barto li J f,Batti oni P,D efoo r W R et https://www.doczj.com/doc/0a1571740.html,m un.,1994:23~24.
[5] M urahash i S I,N ao ta T,Kom iya N.T erahedron L ett.,1995,36:8059~8062.
[6] 刘展良,黄锦汪,计亮年等1离子交换与吸附,1996,12(3):217~222.
[7] Batti oni P,I w anejko R,M ansuy D et al.J.M o l.Catal.A:Chem.,1996,109:91~98.
[8] Puniyam urthy T,R eddy M M,Kalra S J S et al.Pure&A pp l.Chem.,1996,68(3):619~622.
[9] Kulkarni S,A lurkar M,Kum ar A.A pp l.Catal.,A:General,1996,142:243~254.
[10] Kom iya N,N ao ta T,M urahash i,S I.T erahedron L ett.,1996,37(10):1633~1636.
[11] Giannandrea M P,N obile C F,Suranna G P.J.mo l.Catal.,1994,94:27~32.
[12] W ang T J,M a Z H,H uang M Y,J iang Y Y.Ch in.Chem.L ett.,1996,7(1):47~50.
[13] Kurusu Y.R eactive Po lym er,1995,25:63~68.
[14] Barton D H R,T aylo r D K.Pure&A pp l.Chem.,1996,68(3):497~504;Singh B,L ong J R,Papaefthym i ou G C,et al.J.
Am.Chem.Soc.,1996,118:5824~5825.
[15] H su Y F,Cheng C P.J.M o l.Catal.,1997,120:109~116.
[16] Puniyam urthy T,Iqbal J.T etrehedron L ett.,1994,35:4003~4006.
[17] 王荣民,王云普,高分子通报,1994,(1):18~25.
[18] L ei Z Q,Hon X N,W ang Y P et al,Po lym.2P last.T echno l,Eng.,1999,38:159~165.
[19] Karakhanov E A,Kardasheva Y S,M ak si m ov A L et al.J.M o l.Catal.A:Chem.,1996,107:235~240.
[20] E rnst S,T raa Y,D eeg U.Studies in surface science and catalysis,V o l84,(Ed byW eitkap J et al),N ew yo rk:E lsevier,1994:
925~930.
NHPI催化空气氧化反应的研究 近年来,分子氧选择性氧化碳氢化合物制备含氧精细化学品的研究引起了工业界和学术界的广泛关注。ε-己内酯是一种重要的有机中间体和高分子聚合单体,在工业生产中广泛应用于精细化工、石油化工、有机合成及医用材料等领域。尽管近年该生产领域得到了迅速的发展,但依然面临不少的困难与挑战,主要包 括以下三个方面:第一,目前ε-己内酯工业生产的氧化剂主要是双氧水和过氧酸。 然而,它们的不稳定性、冲击敏感性和潜在爆炸性严重限制了运输和储存, 也限制了它们的商业应用。空气氧化技术还只是处于实验室研发阶段,并未工业化应用。第二,空气氧化技术中不可避免地使用过量的苯甲醛做牺牲剂,经济效应低,且生成的有机酸难以分离。 第三,工业上环己酮主要是通过环己烷氧化的方法得到,而环己烷的转化效 率太低,转化率一般维持在3.5-4%,选择性80-85%。本论文主要以空气氧化制备ε-己内酯为研究,从绿色化学的角度出发寻找高效、高选择性且环境友好的催化剂。将分三个部分来进行阐述:第一部分是N-羟基邻苯二甲酰亚胺(NHPI)催化环己酮Baeyer-Villiger氧化生成ε-己内酯的研究,主要包括反应条件的优化及 机理探究。 首先,通过考察催化剂的种类、用量及溶剂体系来筛选优化反应,在最优条件下,环己酮的转化率为100%,ε-己内酯的选择性为96%。然后,结合谱学方法和理论计算对反应机理提出可能的反应机理。实验结果和理论计算表明,NHPI在反应中起的主要作用是促进苯甲醛的氧化生成过氧苯甲酸。 NHPI拔氢后形成的PINO自由基可以稳定反应体系中的各种自由基,增强苯 甲醛的使用效率。第二部分是NHPI催化氧化环己烷一锅法生成ε-己内酯的研究。
?防治技术? 催化氧化法处理有机废水催化剂的选择应用 李启良,陈建林 (南京大学环境学院,江苏南京 210093) 摘 要:催化氧化法是处理难降解有机废水的一项重要的新技术。在对化学氧化法的不断改进中,逐步发展出湿式催化氧化法、光催化氧化法、均相催化氧化法和多相催化氧化法。不同的氧化方法所用的催化剂不相同,有机化合物的种类和结构不同,催化剂与氧化剂之间存在匹配问题,因此对催化剂要进行筛选评价。 关键词:废水处理;催化氧化;催化剂 中图分类号:X703.5;O643.36 文献标识码:A 文章编号:1004-695X(2003)02-0034-03 R evie w on Selection of C atalysis in C atalytic Oxidation LI Qi2liang,CHE N Jian2lin (School o f the Environmental,Nanjing Univer sity,Nanjing,Jiangsu210093,China) Abstract:The treatment of organic wastewater with catalytic oxidation methods is a totally new technology.The paper introduces the progress in the selection of catalysts in the treatment of organic wastewater with four basic catalytic oxidation methods(wet catalytic oxida2 tion,photo catalytic oxidation,hom ogeneous catalytic oxidation and heterogeneous catalytic oxidation).The different kinds and different compositions of organic wastewater should be treated with different catalytic oxidation method,s o it is necessary to study on catalysts match2 ing with different oxidants in treating with specific organic wastewater. K ey w ords:Wastewater treatment;Catalytic oxidation;Catalysts review 对有机化工行业每天排放大量有机废水的处理中,催化氧化法具有独有的优势而成为研究的重点。该法不仅可以改善废水的可生化降解性,在物化和生化处理之间架设了一座桥梁,而且可以作为单独处理工艺来应用,是废水处理的一项新技术,国内外已进行了广泛深入的研究。其中,研究较多的是寻找新型、高效、稳定性好、成本低廉的催化剂。 在对化学氧化法不断改进的过程中,逐步发展了湿式催化氧化等方法[1]。不同的氧化方法应用的催化剂不相同,而且由于氧化催化剂具有选择性,有机化合物的结构和种类不同以及催化剂与氧化剂存在匹配问题,因此要对催化剂进行筛选评价。催化剂一般分为光敏化半导体材料、过渡金属盐及其氧化物和复合氧化物四大类(表1)。在形态上可分为均相和非均相两种;从催化剂的组成又分贵金属和非贵金属两种。作者将分别作评述,并简介催化作用的机理。 1 湿式催化氧化催化剂 湿式催化氧化技术始于20世纪70年代。它 表1 催化氧化法常用催化剂[2] 类 别催化剂 金属盐 PCl2,RuCl3,RbCl3,IrCl4,K2PtO4,NaAuCl4,NH4ReO4, AgNO3,Na2CrO7,Cu(NO3)2,CuS O4,C oCl2,NiS O4, FeS O4,MnS O4,ZnS O4,SnCl2,Na2CO3,Cu(OH)2, Cu(Ⅱ),CuCl2,FeCl2,CuS O4-(NH4)2S O4,MnCl2, Cu(BF4)2,Mn(AC)2 氧化物 W O3,V2O5,M oO3,Z rO4,T aO2,Nb2O5,H fO2ΠOsO4,CuO, Cu2O,C o2O3,NiO,Mn2O3,CeO2,SnO2,Fe2O3 复合 氧化物 CuO-Al2O3,MnO2-Al2O3,CuO-S iO2,CuO-ZnO- Al2O3,RuO2-CeO2,RuO2-Al2O3,RuO2-Z rO2,RuO2 -T iO2,Mn2O3-CeO2,Rh2O-CeO2,PtO-CeO2,IrO2- CeO2,PdO-T iO2,C o3O4-BiO(OH),C o3O4-CeO2, C o3O4-BiO(OH)-CeO2,C o3O4-BiO(OH)-Ln2O3, CuO-ZnO,“OG”,SnO2-Sb2O4,SnO3-M oO3,Fe2O3- Sb2O4,SnO2-FeO3,Fe2O3-Cr2O3,Fe2O3-P2O5,Cu- Mn-Fe氧化物,Cu-Mn氧化物,Cu-Mn-Zn氧化 物,C o-Mn-Zn氧化物,C o-Cu氧化物,Cu-Mn-C o 氧化物 光敏化 半导体T iO2,ZnO,CdS,W O3,Fe2O3 是在高温高压和催化剂作用下,使氧化剂迅速反应分解出活性基团(自由基),进而氧化分解有机物, 最终产物为C O 2 ,H2O及N2等无害物质。其技术的关键是研制高氧化活性、高稳定性的催化剂。 收稿日期:2002-12-13;修订日期:2003-02-18 作者简介:李启良(1973—),男,湖北黄岗人,南京大学在读硕士研究生,主要研究废水处理技术与资源化。 43 第16卷 第2期污染防治技术2003年6月
光催化氧化技术在水处理领域的应用及存在的问题 摘要:本文主要介绍光催化氧化反应机理、及其在处理染料废水、农药废水、含油废水、造纸废水、含表面活性剂废水等方面的应用, 并对其目前存在的问题进行了简单的阐述。 关键词:光催化氧化氧化技术 1前言 随着科技的高速发展和人类文明的进步,各种环境污染越来越严重,其中水污染尤为引起全球范围内的广泛重视。目前许多国家的地表水和地下水均受到不同程度的污染,水污染物主要来自工业、农业以及生活污水。当前水处理中常采用的方法是物化法和生化法,具有工艺成熟,易于大规模工业化应用的优点。然而,这些方法只是将污染物从一相转移到另一相,或是将污染物分离、浓缩,并没有使污染物得到破坏而实现无害化。这不可避免地带来废料和二次污染, 而且适用范围有限, 成本也比较高。近年来, 有关污染物治理研究方面已逐步转向化学转化法, 即通过化学反应使污染物受到破坏而实现无害化。因此, 开发能将各种化学污染物降解至无害化的实用技术( 尤其是污水处理和空气净化) 成为各国科研工作者 的重要研究内容。 光催化氧化技术( Photocatalytic Oxidation )是一种高级氧化技术( advanced oxidation process,AOP) 。光催化剂在光照的条件下能够产生强氧化性的自由基, 该自由基能彻底降解几乎所有的有机物,并最终生成H2O、CO2 等无机小分子,加上光催化反应还具有反应条件温和, 反应设备简单, 二次污染小,操作易于控制, 催化材料易得, 运行成本低, 可望用太阳光为反应光源等优点, 因而近年来受到广泛关注。 1972 年, Fujishima 等在《Nature 》上发表了“Electrochemical potolysis of water at asemiconductor electrode”一文, 揭开了光催化氧化技术的序幕。1976 年, Cr aey [ 4] 等发现, 在TiO2 光催化剂存在的条件下, 多氯联苯、卤代烷烃等可发生有效的光催化降解. 这一研究成果使人们认识到半导体催化剂对有机污染物具有矿化功能, 同时也为治理环境 污染提供了一种新方法, 立即成为半导体光催化研究中 最为活跃的领域。近30 年来, 光催化氧化技术在有机污染物处理方面得到了广泛的研究,几乎所有在水中可能存在的有机污染物都可被光催化氧化法降解并矿化。将光催化工艺与混凝、生物处理等常规水处理工艺结合起来可达到优势互补的效果。近年来, 人们围绕光催化剂活性的提高以及降低反应成本等方面进行了大量的研究, 相关文献每年都有150 篇 以上。 2光催化氧化反应的机理 Sch iavello等认为, 光触媒表面的光催化反应基 本包括4个步骤: (1)光激发催化剂表面形成电子- 电洞对; (2)电子- 电洞对必须能有效地分离; (3)电子- 电洞对在催化剂表面与被吸附物质发生氧化还原反应; ( 4) 光催化剂表面产物的脱附与再吸附。
化学试剂,2005,27(8),459~463;499 专论与综述 催化分子氧氧化醇类的研究进展 李长辉3,李容,郑国钧,赵秀芳 (中国医学科学院中国协和医科大学药物研究所,北京 100050) 摘要:综述了用氧气或空气(分子氧)作为化学计量氧化剂,在催化剂作用下氧化醇类的研究进展,并对某些代表性的催化氧化反应的特点和选择性进行了讨论。 关键词:醇;催化氧化;分子氧;氧气;空气;均相催化;非均相催化 中图分类号:T Q224;O643.322 文献标识码:A 文章编号:025823283(2005)0820459205 收稿日期:2004210213作者简介:李长辉(19752),男,四川泸州人,硕士,实习研究员,主要研究方向为生物活性天然产物的全合成。 醇的氧化是有机合成和工业生产中制备羰基化合物的重要方法,应用化学剂量的氧化剂对醇进行氧化的方法沿用已久,所用的氧化剂包括无 机过渡金属氧化物和盐类,以及一些金属配合物等[1]。使用化学计量氧化剂的方法至今仍然在有机合成领域广泛应用,并在许多方面取得不小进步,但是从经济学以及环境学方面考虑,迫切需要使用氧气、空气等环保、清洁、符合原子经济性的氧化剂,在此过程中,除目标产物外,水为惟一副产物。 R R ′ OH 催化剂O 2(或空气) R R ′ O +H 2O 其中:R ,R ′=烷基,芳基或H 本文分均相催化氧化和非均相催化氧化两大 类,概要的介绍这一领域的最新进展,并对某些催化氧化反应的特点和选择性进行讨论。1 均相催化氧化 由于反应物和催化剂存在于同一相中,均相 催化体现出活性高、选择性好等优点。111 金属/TE MPO 催化体系 氮氧自由基类作为比较成熟的氧化剂(或催化剂),无论在实验室还是工业生产中,都已广泛地用于醇的氧化,2,2,6,62四甲基哌啶2N 2氧化物(TE MPO )是其中最重要的一个。TE MPO (1)是一个氮氧自由基,本身的氧化作用并不强,但其分解产物中的氮氧正离子(2)却是强的氧化剂,可以氧化各种醇成相应的羰基化合物,而自身被还原成为氮羟基化合物(3),继而重新被氧化成自由基形态。 自1984年Semmelhack 等 [2] 首次报道CuCl/ TE MPO 体系催化氧气进行伯醇的氧化以来,这一 体系在近年来取得许多进展。最近,Sheldon 等[3] 报道[Cu (Ⅱ)2(2,2′2二吡啶)]/TE MPO 体系以碱作为共催化剂,在室温下催化氧气将伯醇选择性地氧化成醛,对仲醇没有影响。Marko 等[4]也报 道了CuCl/1,102菲咯啉/二叔丁基胺二乙酸盐在温和条件下催化伯醇的选择性氧化取得很好效果。 TE MPO 催化氧化历程 研究发现,用其他金属化合物替代CuCl ,可 以取得更好的效果,Sheldon 等[5]使用Ru (PPh 3)32Cl 2/TE MPO 体系,顺利地催化活泼和不活泼的醇 高选择性(>99%)地氧化成相应的醛酮。使用12辛醇和22辛醇进行竞争实验表明,对伯醇的选择性高于仲醇(混合反应,二者的转化率分别为80%和10%)。其缺点是较高的氧气压力(1MPa ),反应温度(100℃)及三苯基膦配体自身的热不稳定性。此外,底物中的S ,N ,O 等原子会与Ru 离子配合而导致催化剂失活。Minisci 等[6]报 道了双金属的Mn (Ⅱ )2C o (Ⅱ)/TE MPO 体系,近室温条件高收率(>95%)地催化了一系列苄醇、脂肪伯醇和仲醇的氧化。此反应以醋酸作为溶剂,需使用大量价格昂贵的TE MPO (>10m ol %)。 112 Pd (Ⅱ )类催化剂9 54第27卷第8期李长辉等:催化分子氧氧化醇类的研究进展
第14卷第6期分 子 催 化V ol.14,N o.6 2000年12月J O U RN A L O F M O L ECU L A R CA T A L YSI S(CHIN A)Dec. 2000 文章编号:1001-3555(2000)06-0477-06 低碳烷烃的多相光催化选择氧化 陈希慧1,2),李树本1)* (1.中国科学院兰州化学物理研究所 羰基合成与选择氧化国家重点实验室,兰州730000; 2.广西大学 化学化工学院,南宁530004) 关 键 词:光催化;烷烃;选择氧化 中图分类号:O643.32 文献标识码:A 许多含氧有机物如醇、醛、酮等,是化学工业的重要原料.利用分子氧氧化烷烃生产含氧有机物,是化学工业的一个重要过程.低碳烷烃催化部分氧化的过程往往伴随着初级产物的自氧化,从而导致选择性降低.为了减少反应初级产物的自氧化,反应必须维持在烷烃低转化的条件下进行[1].设计并合成直接将低碳烷烃中的C-H键有效地选择活化的催化剂,是目前催化学科面临的一个艰巨任务[2,3].对于光催化来说,一度被寄于厚望的、以金属有机复合物及盐类[4~6]催化低碳烷烃选择氧化为含氧有机物的需氧氧化过程也面临许多困难[7],作为研究克服需氧氧化过程存在问题的一种方法,以氧化物或负载在多孔载体上的氧化物半导体光催化低碳烷烃选择氧化,近年来取得了一定的进展.我们将介绍近年来氧化物半导体光催化低碳烷烃选择氧化研究方面的进展. 1环己烷的光催化选择氧化 Mu[8]、李树本[9]等用TiO2(P25)、Pt/P25及TiO2/TS-1(Si/Ti=44),在室温下催化环己烷光氧化,其产物分布随催化剂的不同而改变(见表1). Mu等人认为,TiO2(P25)光催化氧化环己烷,在反应条件下初级产物环己醇高选择性被光氧化为环己酮(环己醇光氧化速率为环己酮的 1.3倍);在P25上负载Pt,可使催化环己烷光氧化为环己醇的选择性增加.Pt的负载,可使吸附于TiO2表面的O-ads 物种的量增加,而该物种在环己烷氧化为环己醇的反应步骤中起决定性作用. 表1环己烷在TiO2和TiO2/TS-1催化剂上光氧化的选择性Table1Selectiv ity fo r pho to ox idation of cyclohex ane o v er TiO2a nd TiO2/T S-1catalysts Catalyst Selectivity(%) Cyclohex anol Cy cloh ex ano ne CO2 TiO2(P25)58312 0.5%Pt/P252476 - TiO2/T S-1a ca.45ca.50ca.5 Reactio n co nditions:P2570mg;TiO2/T S-180mg; T iO2∶T S-1(mass ratio)=3∶5;U V light;ro om temperatur e a:CH3CN a s so lv ent; C6H12∶C H3CN(v o lume ra tio)=1∶1 2丙烷的光催化选择氧化 Ro berg e[10]、Wada[7,11,12]及Yoshida[13~16]等将M oO3、V2O5、TiO2负载在多孔的SiO2上,制得M oO3/SiO2、V2O5/SiO2、M2O-V2O5/SiO2(M= Na+、K+、Rb+)、TiO2/SiO2催化剂,并用于光催化丙烷的选择氧化(表2).对于M oO3/SiO2, Ro berg e[10]根据催化剂的紫外漫反射光谱及反应结果,提出了如Scheme1所示的反应机理.他们认为,丙烷选择氧化产物的选择性与催化剂中MoO3的含量有关.当Mo O3的含量低于2%(质量分数)时,M oO3分散于SiO2表面,形成配位数不饱和的M o-O物种,该物种吸收250~290nm的光并激发,催化丙烷氧化为CH3(CO·)CH3和·O(CH2)-C H3自由基,最终产物为丙酮和丙醇;当M oO3的 收稿日期:1998-09-27;修回日期:1999-08-02. 作者简介:陈希慧,女,40岁,博士研究生,副教授. *通讯联系人.
光催化氧化技术及其在水处理中的应用 摘要:介绍了光催化氧化的机理及光催化氧化反应的主要影响因素,就TiO2固定化制备、改性、光催化氧化在工业废水以及饮用水处理中的应用进行了阐述。 关键词:光催化氧化Ti02光催化剂水处理 1 引言 光催化氧化法是近二十年才出现的水处理技术,1972年,Fu—jishima和Honda报道了在光电池中光辐射Ti02可持续发生水的氧化还原反应,标志着光催化氧化水处理时代的开始。1976年,Carey等在光催化降解水中污染物方面进行了开拓性的工作。光催化技术具有反应条件温和、能耗低、操作简便、能矿化绝大多数有机物、可减少二次污染及可以用太阳光作为反应光源等突出优点[1],在难降解有机物、水体微污染等处理中具有其他传统水处理工艺所无法比拟的优势,是一种极具发展前途的水处理技术,对太阳能的利用和环境保护有着重大意义。 2 光催化氧化原理 光催化氧化还原以n型半导体为催化剂,如TiO2、ZnO、Fe2O3、SnO2、WO3等。TiO2由于化学性质和光化学性质均十分稳定,且无毒价廉,货源充分,所以光催化氧化还原去除污染物通常以TiO2作为光催化剂。光催化剂氧化还原机理主要是催化剂受光照射,吸收光能,发生电子跃迁,生成“电子—空穴”对,对吸附于表面的污染物,直接进行氧化还原,或氧化表面吸附的羟基OH-,生成强氧化性的羟基自由基(OH)将污染物氧化[2]。当用光照射半导体光催化剂时,如果光子的能量高于半导体的禁带宽度,则半导体的价带电子从价带跃迁到导带,产生光致电子和空穴。水溶液中的OH- 、水分子及有机物均可以充当光致空穴的俘获剂,具体的反应机理[3]如下(以TiO2为例): TiO2 + hν→h+ + eh++ e- →热量 H2O →OH- + H+ h+ + OH-→OH h+ + H2O + O2- →·OH + H+ + O2- h+ + H2O →·OH + H+ e- + O2 →O2- O2- + H+ →HO2· 2 HO2·→O2 + H2O2 H2O2 + O2- →OH + OH- + O2 H2O2 + hν→2 OH Mn+(金属离子) + ne+ →M 3 光催化氧化反应的主要影响因素 3.1催化剂性质及用量 可用于光催化氧化的催化剂大多是金属氧化物或硫化物等半导体材料,如TiO2、ZnO、CeO2、CdS、ZnS等.在众多光催化剂中,Ti02是目前公认的最有效的半导体催化剂,其特点有:化学性质稳定,能有效吸收太阳光谱中弱紫外辐射部分,氧化还原性极强,耐酸碱和光化学腐
教学目标:1.掌握不同的醇氧化时,产物的对应性。 2.掌握选择性或控制性氧化剂的使用。 3.掌握邻位二醇HIO4氧化及应用。 4.了解醇的催化脱氢 教学重点:选择性氧化剂的应用 教学安排:I ;20min; 1--I7 一、醇的氧化 1.伯醇的氧化 由于羟基的影响,醇的α-氢原子比较活泼,容易被氧化。伯醇被氧化剂氧化时(如K2Cr2O7、KMnO4、浓HNO3等),先是生成醛,然后进一步被氧化,生成羧酸。 在从伯醇氧化制备醛时,应把生成的醛尽快地从反应体系中移出,以避免被进一步氧化。另外,选用氧化剂的种类也是重要的,重铬酸钠(钾)虽然是常用的氧化刘,但用于氧化醇时却得不到很高收率的醛,因为它可使生成的醛进一步被氧化成酸。采用一种称为PCC的氧化剂,用于氧化伯醇制取醛是比较好的氧化方法之一。PCC(pyridinium chlorochromate) Sarrett试剂,是橙红色晶体,它溶于CH2Cl2,是吡啶和CrO 3在盐酸溶液中的络合盐,又称 使用很方便,在室温下便可将伯醇氧化为醛,而且基本上不发生进一步氧化作用。如: PCC氧化剂中的吡啶是碱性的,因此对于在酸性介质中不稳定的醇类氧化为醛(或酮)时,是很好的方法,不但产率高,而且对分子中的C=C、C=O、C=N等不饱和键不发生破坏作用。 若将不饱和伯醇氧化成不饱和醛,还可以选用新生的MnO2或K2FeO4, 例如:
新生的MnO2主要是氧化活泼的烯丙醇或苄醇,有很好的选择性氧化作用。 2.仲醇和叔醇的氧化 仲醇由于其α-C上只有一个氢原子,所以它被氧化的产物为酮。 醇的氧化是放热反应。仲醇氧化生成酮,要控制好反应温度,不然会有深度氧化反应发生(酮被进一步氧化成酸)。 CrO3在醋酸中对仲醇的氧化反应可以比较平缓地进行: CrO3的稀硫酸溶液称为Jones试剂,不能氧化烯、炔烃,而伯、仲醇则可被氧化,常用于比较特殊的酮类化合物的制备。例如: 次卤酸钠可将仲醇氧化成酮。例如: 由于叔醇的α-C上没有氢原子,所以叔醇较难进行氧化反应。在碱性条件下,叔醇不被KMnO4氧化;在酸性条件下,叔醇可以被KMnO4氧化,生成小分子产物。例如: 3、邻位二醇的氧化 多元醇也容易被氧化,但产物比较复杂,最简单的多元醇是乙二醇,它也是邻位二元醇,在不同的氧化条件下,生成的氧化产物是不同的;如下所示:
金属氧化物催化剂与选择性氧化催化剂设计理论基础、作用机理
金属氧化物催化剂 金属氧化物催化剂通常为复合氧化物(complex oxides),即多组分的氧化物。如V 2532V 2O 5-P 2O 5,V 2O 5-MoO 3-Al 2O 3。组分中至少有一个组分是过渡金属氧化物。组分与组分之间可能相互作用,作用的情况因条件而异。复合氧化物系通常是多相共存,如MoO 3-Al 2O 3,就有α-、β-、复杂,有固溶体、有杂多酸、有混晶等。 就催化作用与功能来说,有的组分是主催化剂,有的组分为助催化剂或者是载体。
金属氧化物催化剂的结构化学z具有某种特定晶格结构的新化合物生成,需要满足三个方面的要求:1 控制化学计量关系的价态平衡;2 控制离子间大小相互取代的可能;3修饰理想结构的配位情况变化。这种理想结构是基于假定离子是刚性的、不可穿透的、非崎变的球体。 z对于复合金属氧化物,实际结构常有晶格缺陷、非化学计量的情况,而且离子是可变形的。 z任何稳定的化合物。无论它是晶态结构或无定形态结构,必须满足化学价态的平衡。当晶格中发生高价离子取代低价离子时,就要结合高价离子和因取代而需要的晶格阳离子空位以满足这种要求。
金属氧化物催化剂的结构特征z 尖晶石结构(AB 2O 4,LiMn 2O 4, MoAg 2O 4, MoLi 2O 4,WLi 2O 4)A 8B 16O 32z 钙钛矿型结构(ABO 3, LaMnO 3, LaFeO 3, LaCrO 3, LaCoO 3)z 层状结构LiCoO 2, LiNiO 2, LiMn 2O 4, LiNi x Co 1-x O 2z 新型介孔材料TiO 2, Al 2O 3、PbO 2、Fe 2O 3、WO 3、V 2O 5、MoO 3、ZrO 2 、TiO 2 、Mn 2O 4
第二章光催化氧化技术 第1节光催化概述 光催化(Phntocatalv}i} }是在光的照射下产生类似光合作用的光催化反应,产生出氧化能力极强的自山氢氧基和活性氧,具有很}},的光氧化还原功能,可氧化分解各种有机化合物 和部分无机物,能破坏细菌的细胞膜和固化病毒的蛋白质,可杀灭细菌和分解有机污染物,把有机污染物分解成无污染的水和.二氧化碳,因而具有极强的杀菌、除臭、防霉、防r} ;自 洁、字泞除甲醛和净化空气功能。 光催化的特性为利用空气中的氧分子及水分子将所接触的有机物转换为二氧化碳和水,自身不起变化,却可以促进化学反应的物质,理论.r-有效期较长、维护费用低。同时,二氧化钦本身无毒无害。已广泛用于食品、民药、化妆品等各种领域。 光催化在光的照射下产生氧化能力极强的 氢氧自由基和活性氧,具有很强的光氧化还原 功能。可氧化分解各种有机化合物和部分无机物,能破坏细菌的细胞膜和固化病毒的蛋臼质,可杀灭细菌和分解有机污染物,把有机污染物分解成无污染的水(HZO)和二氧化碳 }co}),因而具有极强的杀菌、除臭、防霉、防污自洁及净化空气的功能。 (川光催化基本原理光催化的原理是光催化剂纳米材料被太阳光、灯光(紫外线) 照射后,表面电子(e)被激励,同时生成带电的正孔(h+},正孔(h+)和空气中的氧 (o:)、水(HZo)发生反应,产生具有极强氧化作用的活性氧。有机物污染物、臭气、细 菌等被氧化分解,而电子(e)还原成空气中的氧。 光催化反应可分为下列几个步骤: ①反应物、氧气及水分子吸附于二氧化钦表而;②经光照射后。二氧化钦产生电子及空穴;③电子和空穴分别扩散到二氧化钦粒子表面;④电子、空穴和氧及水分子形成氢氧自由基;⑤氢氧自由基和反应物进行氧化反应; 光催化是利用特定波长光源的能量产生催化作用,使周围氧及水分子激发成极具活性的OH一及02一自由离子基,这些氧化力极强的自由基儿乎可分解所有对人体或环境有害的有机物质及部分无机物质 第2节光催化氧化技术在污水处理中的应用 }.光催化叙化技术的应用 光催化技术的研究始于20世纪70年代的后半期,用作催化的化学物有T1}} ,硫化锅、硫化亚铅、妮或钦系层状复合氧化物、二氧化铁等。用光照射催化剂时山于光生成空穴。氧化力强。大都采用不溶解的、稳定的半导体粉末二氧化钦,与水分解成氧和氢。从含乙醇的水溶液中生成氢,因水和氮合成氨,还原二氧化碳。含氨和.二氧化碳的水溶液合成氨基酸,氰基化离子或酪酸离子,变为纳米Tif}.}能处理多种有毒化合物。包括工业有毒溶剂、化学杀虫剂、木材光催化技术也被用于无机污染物的处理。利用光催化法在柠檬酸根离子存在下,可以使H}}被还原成Hg而沉积在TiO}表面;此法同样适川于铅。`Ti0:光催化可能降 解的尤机污染物还有氰化物,5}1}、I} }S , LV}和No:等有害气休也能被吸附在}'i。}表面,在光的作用下转化成无毒无害物质,井可回收贵金属。水污染有机物的分解研究儿乎都涉及到'}'i(}}光催化。 光催化是与常规热能催化相对应的催化技术,.光催化主要是有机盒属络合物和半导体。现在商用的光催化剂儿乎都是二氧化钦(Ti}} }可以说是半导体光催化。半甘体光催化的 一般机能是脱臭、抗菌、灭菌、防污、去除有害物等:.
选择性催化还原法(SCR)烟气脱硝技术概述 王清栋 (能源与动力工程1302班1306030217) 摘要:对选择性催化还原脱硝技术进行概述,分析了其机理,并简要介绍催化剂的种类及钝化与中毒机理.最后,对SCR技术进行总结与展望. 关键词:选择性催化还原;烟气脱硝;氮氧化物 Overview of Selective catalytic reduction (SCR) flue gas denitration Wang Qingdong (Power and Energy Engineering, class 1302 1306030217) Abstract: selective catalyst reduction flue gas denitration is reviewed. Its mechanism is analysed and catalyst is given a brief introduction. Catalyst passivation and poisoning mechanism is analysed. Finally, the summary and prospect of the technology are given. Keywords: SCR; NO x; flue gas denitration. 1.前言 氮氧化物是造成酸雨的主要酸性物质之一,是形成区域微细颗粒物污染和灰霾的主要原因,也是形成光化学烟雾的主要污染物,会引起多种呼吸道疾病,是“十二五”期间重点控制的空气污染物之一.2011年初通过的“十二五”规划纲要,要求NO x减少 10%,从而使NO x成为我国下一阶段污染减排的重点.烟气脱硝技术与NO的氧化、还原及吸附特性有关.根据反应介质状态的不同,分为干法脱硝和湿法脱硝.目前,已经在火力发电厂采用的烟气脱氮技术主要是选择性催化还原(SCR)和选择性非催化还原 (SNCR),其中采用最多的主流工艺是选择性催化还原法. 2.SCR反应原理 选择性催化还原脱氮是在一定温度和有催化剂存在的情况下,利用还原剂把烟气中的NO x还原为无毒无污染的N2和H2O.这一原理与1957年在美国发现,该工艺最早却在20世纪70年代的日本发展起来的. SCR 原理图如图一所示 氨气被稀释到空气或者蒸汽中,然后注入到烟气中脱硝,在催化剂表面,氨与NO x 生成氨气和水.SCR过程中的主要反应如下: 4NO+4NH3+O24N2+6H2O 基于V2O5的催化剂在有氧的条件下还对NO2的减少有催化作用,其反应式为 2NO2+4NH3+O23N2+6H2O
第七节选择性催化氧化 一、烃类晶格氧选择性催化氧化概念 烃类的选择性催化氧化,在工业上一般以氧气或空气为氧化剂,催化剂多为可变价过渡金属复合氧化物。就反应机理而言,大多符合Redox机理,它包括两个主要的过程:①气相的烃分子与高价态金属氧化物催化剂表面上的晶格氧(或吸附氧)作用,烃分子被氧化为目的产物,晶格氧参与反应后,催化剂的金属氧化物被还原为较低价态;②气相氧将低价金属氧化物氧化到初始高价态,补充晶格氧,完成Redox循环。按Mars和Van Krevenlen提出的Redox模型,选择氧化反应: C n H m+O2→C n H m-2+H2O (1) 可写成两个基元反应: C n H m+2OM→C n H m -2O+H2O+2M (2) 2M+O2→2OM (3)式中,M——低价态的活性位; OM——有晶格氧的活性位。 但是总反应(1)的速率,实际上是受两个基元反应(2)和(3)中速率较慢的反应所控制。在通常情况下,催化剂被烃分子还原的反应(2)是慢步骤。烃类催化氧化反应动力学的研究结果表明,副反应对氧气的反应级数比主反应对氧气的反应级数高,所以提高氧分压通常不能有效增加反应(1)的速率,反而会导致选择性下降。这是因为提高气相氧分压,一方面会增加与气相氧出于平衡的可逆吸附氧物种(如O2-、O22-、或O-)的表面浓度,这种高活性的可逆吸附氧物种,一般认为主要参与非选择性氧化反应;另一方面对于高温(>900K)的烃类氧化过程表面催化反应外,还伴随有气相自由基反应发生,气相氧的存在也会加快气相深度氧化反应,导致选择性下降。 为了避免气相氧对烃类分子的深度氧化,提高目的产物的选择性,人们在不断改进催化剂性能的同时,尝试了采用催化剂晶格氧作为氧源的反应新工艺。该工艺按Redox 模型将烃分子与氧气或空气分开进行反应,以便从根本上排除气相深度氧化反应。目前有两种反应工艺可用于烃类晶格氧选择氧化,一种是膜反应器,另一种是循环流化床。(1)膜反应器 对烃类选择氧化而言,所用的催化膜通常由具有氧离子/电子导体性能和催化活性的金属氧化物材料制得。其反应机制如下图所示,烃分子与催化膜左侧的晶格氧反应生成
催化氧化法工艺在我公司的应用 1、前言 随着化工工业的迅猛发展,煤、石油、天然气的大量开采、加工及使用,环境污染日益严重,人们也意识到环保的重要性,如不下大力气保护地球环境,人类将面临自己毁灭自己。为遏制全球气候不断变暖,各国都在限制H2S、SO2及有机硫化物等有毒有害气体的排放。10年前150多个国家在日本东京制定了《京都协议书》,2007年12月15日,180多个国家代表在印尼巴厘岛又通过了《巴厘岛路线图》,这肯定了全球有关各方已为控制全球气候变化所做的种种努力。围绕着工业气体、化工废气脱硫并回收硫磺技术,世界各国进行了大量的研究和开发工作。 目前,在煤化工脱硫领域中,脱硫方法有: 1.1 喷射再生法: 喷射再生法回收硫磺主要应用于固定床造气脱硫,且要求H2S≤0.5%,主要有栲胶法、络合铁法、888、PDS、ADA、MSQ法等。 1.1.1 栲胶法脱硫,其主要用于半水煤气脱硫,如CO2过高,碱耗增大,PH值不易调节,Na2CO3与NaHCO3比例失调,造成设备堵塞。如果过高,需加大循环量,相应成分也需提高,设备费用随之增大。 1.1.2 肽菁钴系列硫容低,且易造成设备腐蚀。 1.1.3 络合铁法脱硫,应用于再生气脱硫,其消耗高,易造成设备腐蚀,且工艺不太成熟。 1.2 克劳斯法: 对于胺法、砜胺法、低温甲醇洗等脱硫溶液再生析出的含H S酸气,其大多 2 采用克劳斯装置回收硫磺。克劳斯法要求H2S≥25%,其转化率为95~98%左右,出口尾气硫化物含量高达800~1500mg/Nm3,难以达到环保排放标准,后面还需配套尾气回收装置, 不符合我公司的实际情况(H2S浓度0.5~2%左右)。 1.3 林德直接氧化工艺: S浓度为0.5~3%)处理—Clinsulf-DO Linda公司开发出的低浓度酸性气(H 2 直接氧化工艺,该技术核心是林德公司的内冷式反应器。该反应器分为两部分,入口部分设置一个非冷却绝热床,允许反应温度迅速上升以提高反应速度。下面
催化氧化反应新进展综述 (常熟理工学院化学与材料工程学院,江苏常熟215500) 摘要:本文主要总结了烯烃、烷烃、醇等在催化剂存在的条件下发生催化反应的新进展。 关键字:催化氧化;催化剂;烷烃;烯烃;醇 物质失去电子的反应叫氧化反应。在有机反应中,把有机物引入氧或脱去氢的反应叫做氧化反应。催化氧化反应是指在一定的压力和一定的温度条件下,在以金属材料(如Pt、Pd、Ni等)或非金属材料为催化剂的情况下,与空气、氧气、臭氧等氧化剂进行反应的氧化反应。 催化剂是指一种能够与反应物相互作用,改变反应速率而不改变反应标准自由焓,反应结束时本身依旧保持不变的物质。我们通常把加速化学反应速率的催化剂叫正催化剂,延缓化学反应速率的物质叫负催化剂。催化剂具有专一性和高效性,即不同催化剂对特定的反应体系具有选择性(机理选择性)和加速反应趋于平衡而不改变平衡位置的性能。 1 稀烃催化氧化 1.1 气固相催化 Leals[1]等开发研究双金属催化剂体系,将u-过五氰合钴(Ⅲ)五氰合水合氧化钼(Ⅵ)双(三苯基磷)亚铵盐负载到的硅胶上,在170℃时催化环己烯和氧气进行环氧化反应, 反应产物是氧化环基烯和环己酮,环己烯的选择性最高可以达到58%。 1.2 液相催化 Lunsford等将负载钼的沸石催化剂和钴离子交换后得到的沸石或氢型沸石催化剂催化环己烯的液相反应,环己烯的转化率可以达到50%时,生成环氧化物的选择性可达到50% [2]。此外,Mo-Mn氧化物、过渡金属硼酸盐、重金属络合物也可以作为烯烃液相环氧化的催化剂。 1.3 模拟酶催化 Tabushi[3]最先用锰卟啉络合物-氧化-还原体系来进行环已烯的氧化反应,生
光催化氧化法简介 光催化氧化法是近20年才出现的水处理技术,在足够的反应时间内通常可以将有机物完全矿化为CO2和H2O 等简单无机物,避免了二次污染,简单高效而有发展前途。所谓光催化反应,就是在光的作用下进行的化学反应。光化学反应需要分子吸收特定波长的电磁辐射,受激产生分子激发态,然后会发生化学反应生成新的物质,或者变成引发热反应的中间化学产物。光化学反应的活化能来源于光子的能量,在太阳能的利用中光电转化以及光化学转化一直是十分活跃的研究领域。由于以二氧化钛粉末为催化剂的光催化氧化法存在催化剂分离回收的问题,影响了该技术在实际中的应用,因此将催化剂固定在某些载体上以避免或更容易使其分离回收的技术引起了国内外学者的广泛兴趣。 在我国工业废水中,印染废水因其有机物含量高、色度深、水质复杂、排放量大而成为难处理的工业废水之一。印染废水中含有大量卤化物、硝基物、氨基物、苯胺、酚类及各种染料等有机物,主要来自纤维、纺织浆料和印染加工所使用的染料、化学药剂、表面活性剂和各类整理剂。其COD浓度达数千至数万mg/L,色度也高达数千至数万倍,可生化性差,很多废水还含有高浓度无机盐:如氯化钠、硫化物等,严重污染水环境。国内处理染料废水普遍以生物法为主,同时辅以化学法,但脱色及COD去除效果差,出水难以稳定达到国家规定的排放标准。光催化氧化法是近年来水处理研究的热点之一,实验证明,此方法对印染废水有较好的处理效果。当进水COD Cr为1300 mg/L左右,色度为800倍时,经本法处理的废水,出水COD Cr达188 mg/L,色度为0~10倍,COD Cr 去除率达92%,脱色率几近100%。主要水质指标达到了GB8978—1996《污水综合排放标准》中染料工业的二级标准。本法可取代常规的生物法,适合中小型印染厂的废水处理。 光催化氧化法原理 光降解通常是指有机物在光的作用下,逐步氧化成低分子中间产物最终生成CO2、H2O及其他的离子如NO3-、PO43-、Cl-等。有机物的光降解可分为直接光降解、间接光降解。前者是指有机物分子吸收光能后进一步发生的化学反应。后者是周围环境存在的某些物质吸收光能成激发态,再诱导一系列有机污染的反应。间接光降解对环境中难生物降解的有机污染物更为重要。 利用光化学反应降解污染物的途径,包括无催化剂和有催化剂参与的光化学氧化过程。前者多采用氧和过氧化氢作为氧化剂,在紫外光的照射下使污染物氧化分解;后者又称光催化氧化,一般可分为均相和非均相催化两种类型。均相光催化降解中较常见的是以Fe2+或Fe3+及H2O2为介质,通过photo-Fenton 反应产生?HO使污染物得到降解,非均相光催化降解中较常见的是在污染体系中投加一定量的光敏半导体材料,同时结合一定量的光辐射,使光敏半导体在光的照射下激发产生电子-空穴对,吸附在半导体上的溶解氧、水分子等与电子-空穴作用,产生?HO等氧化性极强的自由基,再通过与污染物之间的羟基加和、取代、电子转移等使污染物全部或接近全部矿化。 新型高效光催化氧化的原理 新型高效光催化氧化的原理就是在表面催化剂存在的条件下,利用一定波长的紫外光波在常温常压下催化、通过一定量的曝气来氧化废水中的有机污染物,或直接氧化有机污染物,或将大分子有机污染物氧化成小分子有机污染物,提高废水的可生化性,较好的去除有机污染物。在降解COD的过程中,通过催化氧化来打断有机分子中的双键发色团,如偶氮基,硝基,硫化羟基,碳亚氨基等,达到脱色的目的,同时有效地降低BOD/COD值,使之易与生化降解。这样,光催化氧化反应在高浓度,高毒性,高含盐量废水中充当常规物化预处理和生化处理之间的桥梁。 该技术的核心为三相催化氧化。这三相分别是:由风机送入罐内的压缩空气曝气(气相),一定波长
·防治技术· 催化氧化法处理有机废水催化剂的选择应用 李启良,陈建林 (南京大学环境学院,江苏南京 210093) 摘 要:催化氧化法是处理难降解有机废水的一项重要的新技术。在对化学氧化法的不断改进中,逐步发展出湿式催化氧化法、光催化氧化法、均相催化氧化法和多相催化氧化法。不同的氧化方法所用的催化剂不相同,有机化合物的种类和结构不同,催化剂与氧化剂之间存在匹配问题,因此对催化剂要进行筛选评价。 关键词:废水处理;催化氧化;催化剂 中图分类号:X703.5;O643.36 文献标识码:A 文章编号:1004-695X(2003)02-0034-03 Review on Selection of Catalysis in Catalytic Oxidation LI Qi-liang,CHEN Jian-lin (Sc hool of the Environmental,Nanjing University,Nanjing,J iangsu210093,China) A bstract:The treatment of organic wastewater with catal ytic oxidation methods is a totall y new technology.The paper introduces the progress in the selection of catal ysts in the treatment of organic wastewater with four basic catalytic oxidation methods(wet catalytic oxida-tion,photo catalytic oxidation,homogeneous catalytic oxidation and heterogeneous catalytic oxidation).The different kinds and different compositions of organ ic wastewater should be treated with different catal ytic oxidation method,so it is necessary to study on catalysts match-ing with different oxidants in treating with specific organic wastewater. Key words:Wastewater treatment;Catalytic oxidation;Catalysts review 对有机化工行业每天排放大量有机废水的处理中,催化氧化法具有独有的优势而成为研究的重点。该法不仅可以改善废水的可生化降解性,在物化和生化处理之间架设了一座桥梁,而且可以作为单独处理工艺来应用,是废水处理的一项新技术,国内外已进行了广泛深入的研究。其中,研究较多的是寻找新型、高效、稳定性好、成本低廉的催化剂。 在对化学氧化法不断改进的过程中,逐步发展了湿式催化氧化等方法[1]。不同的氧化方法应用的催化剂不相同,而且由于氧化催化剂具有选择性,有机化合物的结构和种类不同以及催化剂与氧化剂存在匹配问题,因此要对催化剂进行筛选评价。催化剂一般分为光敏化半导体材料、过渡金属盐及其氧化物和复合氧化物四大类(表1)。在形态上可分为均相和非均相两种;从催化剂的组成又分贵金属和非贵金属两种。作者将分别作评述,并简介催化作用的机理。 1 湿式催化氧化催化剂 湿式催化氧化技术始于20世纪70年代。它 表1 催化氧化法常用催化剂[2] 类 别催化剂 金属盐 PCl2,R uCl3,RbCl3,IrCl4,K2PtO4,NaAuCl4,N H4R eO4, AgNO3,Na2CrO7,Cu(NO3)2,CuSO4,CoCl2,NiSO4, FeSO4,MnSO4,ZnSO4,SnCl2,Na2CO3,Cu(OH)2, Cu(Ⅱ),CuCl2,FeCl2,CuSO4-(NH4)2SO4,MnCl2, Cu(BF4)2,Mn(AC)2 氧化物 WO3,V2O5,MoO3,ZrO4,TaO2,Nb2O5,HfO2OsO4,CuO, Cu2O,Co2O3,NiO,Mn2O3,CeO2,SnO2,Fe2O3 复合 氧化物 CuO-Al2O3,MnO2-Al2O3,CuO-SiO2,CuO-ZnO- Al2O3,RuO2-Ce O2,R uO2-Al2O3,RuO2-ZrO2,RuO2 -TiO 2 ,Mn 2 O3-CeO2,R h2O-CeO2,PtO-CeO2,IrO2-CeO2,PdO-Ti O2,Co3O4-BiO(OH),Co3O4-CeO2, Co3O4-BiO(OH)-CeO2,Co3O4-Bi O(OH)-Ln2O3, CuO-ZnO,“O G”,SnO2-Sb2O4,SnO3-MoO3,Fe2O3- Sb2O4,SnO2-Fe O3,Fe2O3-Cr2O3,Fe2O3-P2O5,Cu- Mn-Fe氧化物,Cu-Mn氧化物,Cu-Mn-Zn氧化 物,Co-Mn-Zn氧化物,Co-Cu氧化物,Cu-Mn-Co 氧化物 光敏化 半导体 TiO2,ZnO,CdS,WO3,Fe2O3 是在高温高压和催化剂作用下,使氧化剂迅速反应分解出活性基团(自由基),进而氧化分解有机物,最终产物为CO2,H2O及N2等无害物质。其技术的关键是研制高氧化活性、高稳定性的催化剂。 收稿日期:2002-12-13;修订日期:2003-02-18 作者简介:李启良(1973—),男,湖北黄岗人,南京大学在读硕士研究生,主要研究废水处理技术与资源化。 34 第16卷 第2期污染防治技术2003年6月