遗传性痉挛性截瘫
- 格式:doc
- 大小:41.00 KB
- 文档页数:9
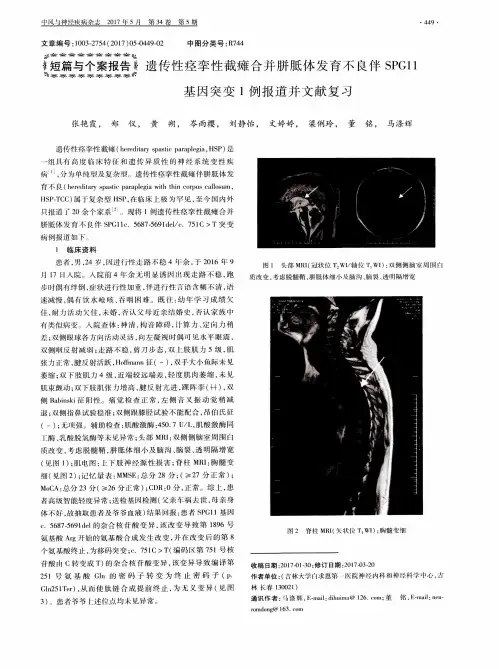

遗传性痉挛性截瘫病因是什么*导读:遗传性痉挛性截瘫是一种什么病,相信很多人都不清楚,因为人们在日常生活中除了了解常见疾病外,很少去了解这种一床疾病。
遗传性痉挛性截瘫是一种以膝、踝阵挛、肌张力增高、双下肢痉挛性肌无力为临床症状的以双侧皮质脊髓束的轴索变性为病例改变的神经系统疾病。
遗传性痉挛性截瘫病因是什么,下面我们来探讨一下。
……遗传性痉挛性截瘫是一种什么病,相信很多人都不清楚,因为人们在日常生活中除了了解常见疾病外,很少去了解这种一床疾病。
遗传性痉挛性截瘫是一种以膝、踝阵挛、肌张力增高、双下肢痉挛性肌无力为临床症状的以双侧皮质脊髓束的轴索变性为病例改变的神经系统疾病。
遗传性痉挛性截瘫病因是什么,下面我们来探讨一下。
*遗传性痉挛性截瘫病因遗传因素是遗传性痉挛性截瘫的主要病因,常见为常染色体显性遗传,也可为X连锁遗传或隐性遗传。
其发病机制尚不明确,以慢性痉挛性下肢瘫痪和双下肢痉挛性肌无力为特征。
*遗传性痉挛性截瘫临床表现了解遗传性痉挛性截瘫病因是什么,还要了解遗传性痉挛性截瘫临床表现。
儿童或成年人是遗传性痉挛性截瘫的高发人群,发病时患者不仅会出现肌张力增高、膝、踝阵挛、剪刀样步态的临床表现,还会出现双下肢痉挛性肌无力、腱反射活跃亢进锥体外系症状、痴呆、精神发育迟滞、弓形足畸形等临床表现,还可伴有视神经萎缩、视网膜色素变性、小脑性共济失调、耳聋、肌萎缩。
*遗传性痉挛性截瘫治疗一旦出现明显的临床症状,患者要及早到医院就诊,根据医生指导采取治疗方法进行治疗。
日常患者还可自行做肌肉力训练,减缓肌肉萎缩;做有氧训练,提高耐力,改善心血管适应性;做伸展训练,提高肌肉力量,减少并发症。
由于遗传性痉挛性截瘫是一种难治疗的疾病,暂时没有任何一种特异性治疗法能够治愈疾病,因此预防非常重要。
预防方法为患者尽量不结婚,因为结婚后患者可能想要生孩子,但这种疾病具有遗传性,会影响后代,因此不要结婚或结婚后不要生育。
在治疗期间,患者应加强体育锻炼,做好护理,防止残废。



小儿遗传性痉挛性截瘫怎样治疗?
*导读:本文向您详细介绍小儿遗传性痉挛性截瘫的治疗方法,治疗小儿遗传性痉挛性截瘫常用的西医疗法和中医疗法。
小儿遗传性痉挛性截瘫应该吃什么药。
*小儿遗传性痉挛性截瘫怎么治疗?
*一、西医
*1、治疗:
本病目前无特效治疗方法。
根据病情可对患者进行跟腱延长或内收肌松解术,虽然病情仍在进展,但手术治疗后可以延缓病程进展数年。
*2、预后:
本病预后与发病早晚和分型有关。
早发病组(3~5岁发病)为单纯型HSP,病情进展缓慢,多在起病约30年后才不能行走,一般不危及生命。
晚发病组(30岁后发病)病情进展较快。
复杂型HSP患者则预后较差。
*温馨提示:上面就是对于小儿遗传性痉挛性截瘫怎么治疗,小儿遗传性痉挛性截瘫中西医治疗方法的相关内容介绍,更多更详尽的有关小儿遗传性痉挛性截瘫方面的知识,请关注疾病库,也可以在站内搜索“小儿遗传性痉挛性截瘫”找到更多扩展资料,
希望以上内容对大家有帮助!。

遗传性痉挛性截瘫应该做哪些检查?
*导读:本文向您详细介遗传性痉挛性截瘫应该做哪些检查,常用的遗传性痉挛性截瘫检查项目有哪些。
以及遗传性痉挛性截瘫如何诊断鉴别,遗传性痉挛性截瘫易混淆疾病等方面内容。
*遗传性痉挛性截瘫常见检查:
常见检查:肌电图、核磁共振成像(MRI)、CT检查、脑脊液检查-化学检查-蛋白质检查
*一、检查
本病血、尿、便、脑脊液常规化验均正常。
1.CT与MRI可能有脊髓变细、萎缩。
2.由于脊髓后索损害,下肢皮层体感诱发电位异常,潜伏期延长,波幅降低,提示神经传导速度减慢。
*以上是对于遗传性痉挛性截瘫应该做哪些检查方面内容的相关叙述,下面再来看看遗传性痉挛性截瘫应该如何鉴别诊断,遗传性痉挛性截瘫易混淆疾病。
*遗传性痉挛性截瘫如何鉴别?:
*一、鉴别
本病须与Arnold-Chiari畸形、多发性硬化、脑性瘫痪、遗传性运动神经元病、多系统萎缩、小脑性共济失调、亚急性联合变性、脊髓压迫症等鉴别。
*温馨提示:以上内容就是为您介绍的遗传性痉挛性截瘫应该做哪些检查,遗传性痉挛性截瘫如何鉴别等方面内容,更多更详细资料请关注疾病库,或者在站内搜索“遗传性痉挛性截瘫”了解更多,希望以上内容可以帮助到大家!。

遗传性痉孪性截瘫1例分析遗传性痉孪性截瘫(hereditary spasticparaplegia)是一种比较少见的家族遗传性变性病,以慢性进行性无力与慢性痉挛性下肢瘫痪为特征。
病理特点为皮质脊髓束变性,该病有遗传家族史,发病机制至今仍不清楚。
有人认为是基因遗传与酶系统缺陷有关。
下面就一例患者的病情加以分析。
患者,女,27岁。
2006年7月无明显诱因开始出现步态异常,走路时双下肢发僵,以右下肢为著,右脚用足尖走路,脚后跟不能着地,且经常在走路时出现摔倒现象,以身体向后倾倒次数为多,摔倒前后都意识清楚,双上肢活动正常。
于2006年11月去北京地区301解放军总医院就诊,给予口服美多巴从小剂量开始治疗,开始服用一个月患者自觉症状有所缓解,即觉得双下肢发僵有所减轻,而且摔倒现象也减少了,但是一个月后继续服用时患者自觉不再有明显的改善,且症状呈进行性加重,并同时伴有小便失禁,饮食水呛咳,且上述症状呈晨轻暮重的特点,为进一步诊治来我院就诊。
家族史:患者母亲大约30岁左右发病,双下肢发僵,双足尖走路,后渐渐不能自行走路。
其三个舅舅均因同样症状不能走路而瘫痪在床,且均有小便失禁及饮食水呛咳,均在大约30岁左右发病,而且患者及其家人智力及记忆力反应力都正常。
入院后体格检查:BP110/70mmHg,神志清楚,语言流利,颅神经检查正常,四肢肌张力高,尤以双下肢为著,腱反射活跃,以下肢明显,肌力尚正常,可引出病理征,感觉共济正常。
辅助检查:头颅MRI未见明显异常。
四肢肌电图尚正常,血肝肾功能正常,血钾化验正常,血钙略低,胸片心电图正常。
请北京专家会诊,考虑定位于锥体束,临床表现以双下肢肌张力增高明显,结合其家族史,考虑定性诊断为遗传性痉挛性截瘫,为常染色体显性遗传,该病人为单纯型,治疗给予巴氯酚口服对症治疗减轻症状。
治疗效果:用药治疗五日后患者自觉症状有所减轻,肢体发僵有改善,身体不自主倾倒现象亦有所减少,查体肌张力有所降低。




遗传性痉挛性截瘫(HSP)临床表现HSP临床共性特征,发病年龄广,可婴幼儿发病亦可成年发病乃至老年发病,一般多在少年发病,同一个家族病情轻重也有明显差别。
男女均可发病,但男性似乎多于女性;双下肢进展性痉挛性截瘫,但进展速度多样化;运动系统功能障碍普遍,但可合并其他多种病症;往往存在家族史,但家系内不同患者病情不尽相同;不同基因分型HSP,临床表现、病情严重程度及病程进展不同。
因此HSP 临床可划分为单纯型和复杂型,前者又可划分为早发和晚发型。
1.单纯型是临床最常见类型,主要临床表现是双下肢痉挛性截瘫、肌张力增高、腱反射亢进,肌力正常或稍减低,患病最初自我感觉双下肢僵硬、走路易跌绊、上楼困难,其他表现为:约10%~65%的患者感觉障碍(主要为下肢远端位置觉和震动觉消失),约50%的患者可有尿频与尿急等括约肌功能障碍现象,约33%的患者可在发病后数年出现足畸形(如足尖着地步态或弓形足),少数患者可出现肢体远端肌肉萎缩(一般在起病10余年后展现下肢远端肌肉轻度萎缩)、少数患者上肢亦可受累而在发病早期呈现上肢痉挛和双手僵硬与动作笨拙、罕见轻度构音障碍。
其中,早发型在35岁前发病,不乏幼儿期发病,是HSP最常见临床类型,病情进展缓慢,多在数十年后亦无明显进展,仅有极少数晚年需要轮椅;晚发型35岁后发病,病情进展快,常于40~65岁出现行走困难,多见60岁左右就丧失行走能力而需轮椅辅助移动。
2.复杂型临床相对少见,除外上述单纯型临床表现还可合并多种病症而形成多种临床综合征。
①Ferguson-Critchley综合征:临床特征为中年发病,出现四肢锥体系症状、协调障碍、深感觉减退,眼部症状可展现眼球震颤、侧向及垂直注视受限、假性眼肌麻痹、视神经萎缩、复视等,可伴有四肢僵硬、面无表情、前冲步态和不自主运动等锥体外系症状,呈常染色体显性遗传。
②Kjellin综合征:20岁左右发病,痉挛性截瘫伴下肢肌肉进行性萎缩、小脑性构音障碍、精神发育迟滞、视网膜色素变性,呈常染色体隐性遗传。
遗传性痉挛性截瘫怎样治疗?
*导读:本文向您详细介绍遗传性痉挛性截瘫的治疗方法,治疗遗传性痉挛性截瘫常用的西医疗法和中医疗法。
遗传性痉挛性截瘫应该吃什么药。
*遗传性痉挛性截瘫怎么治疗?
*一、西医
*1、治疗
本病迄今为止尚无有效的预防和治疗方法,也无延缓其发展进程的方法。
主要采取对症治疗,左旋多巴、巴氯芬可减轻症状,理疗和适当运动也有帮助。
*2、预后
病情缓慢进展,最终卧床不起,因合并其他疾病而死亡。
*温馨提示:上面就是对于遗传性痉挛性截瘫怎么治疗,遗传性痉挛性截瘫中西医治疗方法的相关内容介绍,更多更详尽的有关遗传性痉挛性截瘫方面的知识,请关注疾病库,也可以在站内搜索“遗传性痉挛性截瘫”找到更多扩展资料,希望以上内容对大家有帮助!。
第 1 页 什么是遗传性痉挛性截瘫 *导读:遗传性痉挛性截瘫也叫做家族性痉挛性截瘫,是一种神经系统退行性变性疾病。遗传性痉挛性截瘫,顾名思义,是一种家族性遗传疾病,大部分患者都是常染色体的显性遗传,也有少部分病人属于常染色体隐性遗传及X连锁遗传。本病发病和引起遗传的原因目前尚未明确。……
遗传性痉挛性截瘫也叫做家族性痉挛性截瘫,是一种神经系统退行性变性疾病。遗传性痉挛性截瘫,顾名思义,是一种家族性遗传疾病,大部分患者都是常染色体的显性遗传,也有少部分病人属于常染色体隐性遗传及X连锁遗传。本病发病和引起遗传的原因目前尚未明确。 遗传性痉挛性截瘫的主要发病年龄是儿童时期和青春期,少部分病人会出现在其他年龄段,男性患者多于女性,患者常有阳性遗传家族史。主要临床表现是缓慢进展的双下肢痉挛性肌无力,肌张力增高,腱反射活跃亢进,膝、踝阵挛,患者可能会出现剪刀样步态等。除了肌肉和关节的症状,患者还会出现视力和智力和听力的障碍,常见的症状有有视神经萎缩、视网膜色素变性、锥体外系症状、小脑性共济失调、感觉障碍、痴呆、精神发育迟滞、耳聋、肌萎缩、自主神经功能障碍等,还可有弓形足畸形。 目前没有有效的方法能够治疗遗传性痉挛性截瘫,只能够进行预防,延缓病情的训练。药物治疗以减少残疾和预防并发症为 第 2 页
目的。患者可进行肌力训练,提高未受损肌肉的力量,代偿无力肌的肌力。减缓肌肉的萎缩,尤其是小腿肌。此外,肌肉训练也能够缓解背部的疼痛,减轻并发症,如肌腱炎、滑囊炎和抽筋。 有氧训练能够改善心血管适应症,减轻患者的疲劳,提高肌肉和身体的耐力。此外,患者还可以多做步行、骑自行车、游泳、水上健身操等运动,也有利于减缓病情的发展。 因为遗传性痉挛性截瘫是一种遗传病,而且没有有效的治疗方法,因此建立遗传性痉挛性截瘫患者尽量不要结婚,或者婚后不要生育,以免遗传给下一代。
第 1 页 遗传性痉挛性截瘫的症状有哪些表现 *导读:很多报道上都说,很多的遗传性痉挛性截瘫患者在患病初期,由于对遗传性痉挛性截瘫的症状不是很了解,而错过了最佳治疗时期,给患者日后的生活甚至一生都造成了严重的影响。因此,这对我们敲响了一记警钟,我们这才知道了解遗传性痉挛性截瘫的症状是多么的重要。那么,遗传性痉挛性截瘫的症状有哪些变现呢?……
遗传性痉挛性截瘫通常又被称作家族性痉挛性截瘫,因为这种病几乎都是带有家族遗传的特点。 很多报道上都说,很多的遗传性痉挛性截瘫患者在患病初期,由于对遗传性痉挛性截瘫的症状不是很了解,而错过了最佳治疗时期,给患者日后的生活甚至一生都造成了严重的影响。因此,这对我们敲响了一记警钟,我们这才知道了解遗传性痉挛性截瘫的症状是多么的重要。那么,遗传性痉挛性截瘫的症状有哪些变现呢? 专家指出,遗传性痉挛性截瘫可见于任何年龄,但好发于儿童期和青春期,且男性较女性多见。该病的首发症状表现是患者走路不便,双下肢僵硬,跑步易跌,上下楼梯困难。临床表现主要是缓慢进展的双下肢痉挛性截瘫。体检时候可发现双下肢呈剪刀步态,双下肢肌张力增高,腱反射亢进,膝、踝震挛阳性,病理征阳性。还可伴有视神经萎缩视网膜色素变性锥体外系症状小 第 2 页
脑性共济失调深感觉障碍痴呆精神发育迟滞耳聋肌萎缩自主神经功能障碍等。1.单纯型遗传性痉挛性截瘫:临床上将只有痉挛性截瘫者称为单纯型遗传性痉挛性截瘫,这类型较为常见。 ①单纯型遗传性痉挛性截瘫Ⅰ型:单纯型遗传性痉挛性截瘫Ⅰ型患者于三十五岁前发病,单纯型遗传性痉挛性截瘫Ⅰ型患者大多数为男性,常染色体隐性遗传性痉挛性截瘫发病年龄常在三到六岁或者十岁以内。 ②单纯型遗传性痉挛性截瘫Ⅱ型:单纯型遗传性痉挛性截瘫Ⅱ型患者于三十五岁以后发病。常染色体显性遗传性痉挛性截瘫发病年龄较晚,平均年龄十八岁,锥体束征明显,常有感觉障碍和括约肌障碍。 2.复杂型遗传性痉挛性截瘫:临床上将痉挛性截瘫合并脊髓外损害的患者称为复杂型遗传性痉挛性截瘫。发病年龄一般为三到五岁,均为男性。除痉挛性截瘫外,并有脊髓外受损表现。根据合并症状的不同,构成几种类型。 3.少数患者开始表现为单纯型,数十年后出现脊髓外受损。 以上这些就是关于遗传性痉挛性截瘫的症状有哪些表现的简单介绍,希望对大家对疾病的认识和学习有一定的帮助,我们在了解了该病的症状之后才能有效地认识疾病和预防疾病,及早发现病及时治疗。 第 3 页
遗传性痉挛性截瘫遗传性痉挛性截瘫(hereditary spastic paraplegia,HSP)是一种神经系统退行性变性疾病,病理改变主要在脊髓中双侧皮质脊髓束的轴索变性和(或)脱髓鞘,以胸段最重。
临床表现为双下肢肌张力增高,腱反射活跃亢进,病理反射阳性,呈剪刀步态。
许多学者认为HSP也属于遗传性共济失调疾病(IAs)的范畴。
由Seeligmuller(1876)首报,strumpell(1880)和Lorrain(1898)将之定为独立疾病单元,故也称Striampell-Lorrain病。
流行病学调查,发病率为2~10/10万人口,约占遗传性共济失调的25%,是遗传性共济失调中较多见的类型。
目录遗传形式遗传学和发病机制病理临床表现HSP分型1、单纯型HSP2、复杂型HSPHSP伴黄斑变性(Kjellin综合征)HSP伴早老性痴呆(Mast综合征)HSP伴精神发育迟滞或痴呆HSP伴远端肌萎缩(Tyorer综合征)HSP伴视神经萎缩(Behr综合征)HSP伴多发性神经病Charlevoix-Sageunay综合征辅助检查诊断鉴别诊断治疗预防遗传形式遗传学和发病机制病理临床表现HSP分型1、单纯型HSP2、复杂型HSPHSP伴黄斑变性(Kjellin综合征)HSP伴早老性痴呆(Mast综合征)HSP伴精神发育迟滞或痴呆HSP伴远端肌萎缩(Tyorer综合征)HSP伴视神经萎缩(Behr综合征)HSP伴多发性神经病Charlevoix-Sageunay综合征辅助检查诊断鉴别诊断治疗预防展开编辑本段遗传形式国内外研究报道,HSP的遗传形式可呈常染色体显性遗传(AD)和常染色体隐性遗传(AR),少见X-连锁隐性遗传(XR),散发病例也不少见。
国内学者总结国内文献报道的HSP(共117个家系,435例患者)的遗传特点,发现常染色体显性、常染色体隐性、X-连锁隐性遗传分别为41、13、2个家系,约占HSP的35.04%、11.11%、1.71%,与国外报道遗传形式基本一致。
遗传性痉挛性截瘫是一种比较少见的家族遗传性变性病,最常见为常染色体显性遗传、也有常染色体隐性遗传及x链锁遗传。
以慢性进性无力与慢性痉挛性下肢瘫痪为特征。
发病机制至今仍不清楚。
编辑本段遗传学和发病机制HSP有明显的遗传异质性,目前分子遗传学研究发现,HSP的基因分型至少有16型,已有4型疾病基因被克隆。
16型分别为:①X-连锁隐性遗传(XR)3型,分别是HSP -1,定位于Xq28,疾病基因已克隆,为神经细胞粘附分子L1基因,即LICAM基因;HSP -2定位于Xq22,疾病基因已克隆,为髓鞘蛋白脂蛋白基因,即PLP基因;HSP -16定位于Xqll。
②常染色体显性遗传(AD)8型,分别是HSP -3A定位于14q11.2~q24.3;HSP -4定位于2p22~21,疾病基因为痉挛蛋白基因(Spastin基因);HSP -6定位于15q11.1;HSP -8定位于8q23~q24;HSP-9定位于10q23.3~q24.1;HSP-10定位于12q13;HSP-12定位于19q13;HSP-13定位于2q24;HSP-17定位于llql2。
③常染色体隐性遗传(AR)5型,分别是HSP-5A定位于8q12~13;HSP-5B尚未定位;HSP-7定位于16q24.3,疾病基因为截瘫蛋白基因(Paraplegin基因);HSP-11定位于15q13~q15;HSP-14定位于3q27~q28;HSP-15定位于14q。
L1CAM基因编码的神经细胞粘附分子L1是粘附分子免疫球蛋白G超家族中的一员,主要在神经细胞中表达,与神经元一神经元粘附以及其他一些重要的神经元相互作用有关。
Jouet等(1994),在HSP-1研究中发现了LICAM 基因突变与HSP-1发病相关,突变形式可表现为错义突变、无义突变及缺失突变。
另外,LICAM基因突变还可引起X-连锁的MASA综合征(Mental Retardation,Aphasia Shuffling gait,Adducted Thumb Syndrome)、X-连锁的脑积水及X-连锁的胼胝体发育不全。
因此,我们称这4种病为等位基因病(allelic diseases)。
由于这4种病的临床特征显示有相当大的重叠,以胼胝体发育不全(corpus callosum hypoplasia)、精神发育迟滞(mental retardation)、拇指内收(Adducted thumbs)、遗传性痉挛性截瘫(hereditary spastic paraplegia)和脑积水(Hydrocephalus)为特征,最近将这些疾病概括在一起,命名为CRASH综合征。
髓鞘蛋白脂蛋白(PLP)基因编码两个主要髓鞘蛋白:PLP及其异构体DM20蛋白。
PLP的mRNA特异性表达于中枢神经系统(CNS)组织,而DM20的mRNA 可见于CNS、心脏及其他组织。
PLP约占CNS髓鞘总蛋白含量的50%,其生物功能主要是在髓鞘形成及保持功能结构中发挥作用。
Saugier-Veber等(1994)突变分析研究发现在HSP-2患者有PLP基因突变,确定PLP基因是HSP-2的疾病基因。
有趣的是PLP基因突变还与佩-梅病(Pelizaeus-Merzbacher disease,PMD)发病有关。
因此,HSP-2和PMD 也为等位基因病。
已发现PLP基因突变有30余种,点突变约占突变的15%~20%,常见于HSP-2;重复突变多见于PMD。
Hazan等(1999)研究发现Spastin基因突变引起HSP-4。
Spastin是一种氨基酸ATP酶(Amino Acid ATPase,AAA)蛋白家族的一个成员。
HSP-4广泛表达于人类成人及胎儿组织,定位于核中,与26S蛋白酶同源,可能与核蛋白生物功能和聚集有关。
到目前为止,40%~50%HSP-4被发现有spastin基因的突变,约有39种,包括11种错义突变、6种无义突变、10种剪接位点突变、8种小缺失突变、3 发病遗传家族图(2张)种插入突变和1种大缺失突变等。
Ciorgio Lasari等(1998)在HSP-7病人中发现了Paraplegin基因的一种9.5kb缺失的杂合突变,另外他们还发现了两种移码突变,导致截短的Paraplegin蛋白的产生,确定paraplegin基因是HSP-7的疾病基因。
Paraplegin是一种线粒体金属蛋白酶,与酵母线粒体ATP酶高度同源,转染的Cos-7细胞免疫荧光分析和体外线粒体表达实验表明,Paraplegin蛋白存在于线粒体内膜,它有线粒体膜内蛋白水解作用,分子伴侣(chaperone)样活性,线粒体蛋白翻译后的装配,多肽链的错误折叠或翻译等功能有关。
在有Paraplegin突变的两个病人的肌活检分析中发现存在典型的线粒体氧化磷酸化缺陷,提示此缺陷可能是HSP-7型疾病神经变性的一种发病机制。
编辑本段病理基本的病理形态改变主要是双侧皮质脊髓侧束的轴索变性和脱髓鞘,以胸段最重;皮质脊髓前束脱髓鞘往往不很严重;双侧脊髓小脑束和薄束也有脱髓鞘改变。
此外,前角细胞、巨锥体细胞、基底节、脑干、小脑、视神经等也可有病理改变。
Behan和Maia两次尸检研究后认为在脊髓中上行和下行长束远端的轴索变性是HSP的特征性表现,最近在有para ptegin基因突变的HSP病人的股四头肌肌肉活检时发现有破碎红纤维(RRF)及细胞色素C 氧化酶(COX)阴性纤维,这显示有线粒体功能异常。
至于线病理图片(4张)粒体异常仅仅与HSP-7有关还是在其他基因型HSP中都存在仍不清楚。
目前仅有少量病理研究,可见脊髓的皮质脊髓侧束变性,胸髓较重,皮质脊髓前束、脊髓小脑束、薄束有不同程度病变,脊髓前角、基底节、小脑、脑干、视神经也受累。
Paraplegin 基因突变所致SPG7患者肌活检可发现蓬毛样红纤维(RRF)。
编辑本段临床表现HSP的发病年龄多见于儿童期或青春期,但也可见于其他年龄段。
男性略多于女性。
常有阳性遗传家族史。
临床表现为缓慢进展的双下肢痉挛性肌无力,肌张力增高,腱反射活跃亢进,膝、踝阵挛,病理征阳性,呈剪刀样步态等。
可伴有视神经萎缩、视网膜色素变性、锥体外系症状、小脑性共济失调、感觉障碍、痴呆、精神发育迟滞、耳聋、肌萎缩、自主神经功能障碍等。
还可有弓形足畸形。
部分HSP家族有遗传早现(Anticipation)现象。
编辑本段HSP分型Harding(1984)的分型方法为大多数学者接受。
Harding按临床表现分为两型:1、单纯型HSP是临床最常见的HSP。
主要表现为痉挛性截瘫,也有遗传异质性,呈常染色体显性遗传,或常染色体隐性遗传,病理改变主要在脊髓锥体束变性,而脊髓小脑束、后索改变不明显。
显性遗传的HSP又按年龄分为早发型和晚发型。
早发型最多见,常于35岁前发病,这型HSP患者行走较迟,双下肢僵硬,不灵活,痉挛性瘫痪,腱反射亢进、膝踝阵挛阳性,病理征阳性。
双上肢可有轻微手指活动不灵活,腱反射活跃,深感觉障碍随病程进展而越来越明显。
括约肌障碍和弓形足也可见。
晚发型患者常于40~65岁出现行走困难,临床表现类似早发型,但双下肢肌无力、深感觉障碍、括约肌障碍更常见。
2、复杂型HSP临床上较少见,除痉挛性截瘫表现外,常伴有脊髓病损外的伴发症状体征,遗传异质性更明显。
Ferguson-Critchley综合征:临床特点是中年起病,四肢锥体束征,踝反射减弱或消失,其他腱反射亢进。
四肢协调障碍,深感觉略减退。
眼部症状主要是眼球震颤,侧向及垂直注视受限,假性眼肌麻痹。
锥体外系损害表现四肢僵硬,不自主运动,面部表情少,可有前冲步态。
呈常染色体显性遗传。
HSP伴黄斑变性(Kjellin综合征)于20岁左右开始发生痉挛性截瘫,伴小脑性构音障碍,精神运动发育迟滞,视网膜色素变性。
呈常染色体隐性遗传。
HSP伴早老性痴呆(Mast综合征)起病于20岁左右,痉挛性截瘫,伴有构音障碍,痴呆,手足徐动症。
呈常染色体隐性遗传。
痉挛性无力伴双手和腿部小肌肉进行性萎缩、精神发育迟滞和中心性视网膜变性等;合并眼肌麻痹称为Barnard-Scholz综合征。
HSP伴精神发育迟滞或痴呆又称鱼鳞癣样红-痉挛样截瘫-精神发育迟滞(Siogren-Larsson)综合征:幼儿期发病或生后不久出现颈、腋窝、肘窝、下腹部及腹股沟等皮肤弥漫性潮红和增厚,随后皮肤角化脱屑,呈暗红色鳞癣,痉挛性截瘫或四肢瘫(下肢重),常伴假性球麻痹、癫痫大发作或小发作、手足徐动、轻至重度精神发育迟滞等;1/3的病例视网膜黄斑色素变性导致视力,可见视神经萎缩或审神经炎,但不失明;患儿身材矮小,牙釉质发育不全,指(趾)生长不整齐。