试验八极化曲线评选缓蚀剂
- 格式:doc
- 大小:829.50 KB
- 文档页数:3

一种新型酸洗缓蚀剂的应用研究现状及未来发展趋势摘要:利用电化学测试技术研究了一种新型酸洗缓蚀剂,即2,5-二氯苯乙酮-O-1-(1,3,4-三氮唑)亚甲基肟在l mol/L HCl介质中对碳钢的缓蚀作用和吸附行为。
结果表明:合成的三唑类化合物是一种性能优异的缓蚀剂。
从而也从大方向上把握了未来酸洗缓蚀剂的发展趋势。
关键词:三唑化合物;缓蚀剂;电化学实验;热力设备1.前言酸洗广泛应用于各个工业部门中的换热设备、传热设备和冷却设备等的水垢清洗,特别是电力部门的热力设备(如锅炉)的酸洗尤其重要。
从社会经济的角度来看,可减少因污垢带来的燃料耗费;从环境保护的角度来看,减少了燃料废气和大气污染【1】;从安全角度来看,锅炉和换热器等热力设备在使用过程中逐渐形成各类污垢,而这些污垢导热不良致使炉管局部温度升高,降低了钢材的强度,常常发生爆管事故,影响锅炉运行。
因此酸洗对于电厂的锅炉运行起着非常重要的作用。
酸洗常用的酸有盐酸、硫酸、磷酸、氢氟酸、氨基磺酸等无机酸,和柠檬酸、EDTA 等有机酸。
但由于酸对金属设备均有腐蚀作用,尤其无机酸的腐蚀更为严重,同时所放出的氢会向金属内部扩散,使被洗设备发生氢脆。
各种酸对铁的溶解能力由大到小如表1 所示。
另外所析出的大量的酸性气体,会使劳动条件恶化。
由于强酸的腐蚀性,酸洗过程常出现“过蚀”的现象,即清洗过程中不仅清除了金属表面的锈蚀和污垢,同时也将部分金属基材一并清洗掉。
因此,酸洗过程既造成金属材料、酸洗液的极大浪费,同时还产生大量的酸洗废液,造成严重的环境污染。
因此在酸洗时要加入缓蚀剂,以抑制金属在酸性介质中的腐蚀,减少酸的使用量,提高酸洗效果,延长热力设备的使用寿命。
酸洗时不仅要考虑酸的溶铁能力,还应考虑垢成分、金属材质、废液处理方法等因素【2】。
故选择一种质量好的缓蚀剂是酸洗的重要环节,而了解各类缓蚀剂的缓蚀性能可以更好的进行防腐工作。
1.1 酸洗缓蚀剂的发展历史关于酸性介质缓蚀剂的研究报道很多,根据有关文献记录,酸洗缓蚀剂第一个专利是1860年英国公布用糖浆及植物油的混合物作为酸洗铁板时的缓蚀剂。


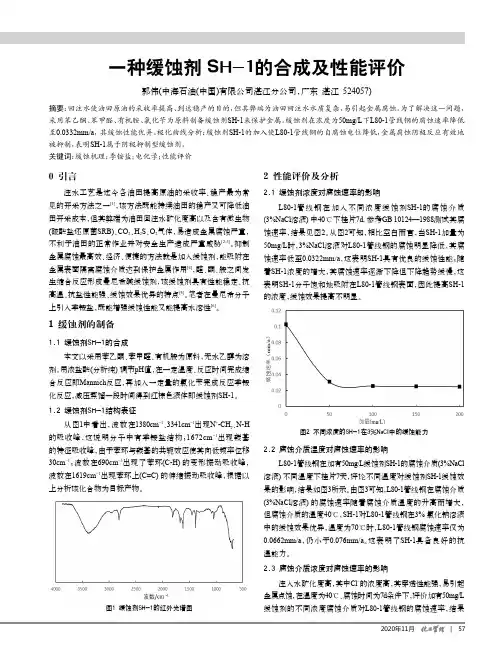
2 性能评价及分析2.1 缓蚀剂浓度对腐蚀速率的影响L80-1管线钢在加入不同浓度缓蚀剂SH-1的腐蚀介质(3%NaCl溶液)中40℃下挂片7d, 参考GB 10124—1988测试其腐蚀速率,结果见图2。
从图2可知,相比空白而言,当SH-1加量为50mg/L时,3%NaCl溶液对L80-1管线钢的腐蚀明显降低,其腐蚀速率低至0.0322mm/a,这表明SH-1具有优良的缓蚀性能;随着SH-1浓度的增大,其腐蚀速率逐渐下降但下降趋势缓慢,这表明SH-1分子饱和地吸附在L80-1管线钢表面,因此提高SH-1的浓度,缓蚀效果提高不明显。
图2 不同浓度的SH-1在3%NaCl中的缓蚀能力2.2 腐蚀介质温度对腐蚀速率的影响L80-1管线钢在加有50mg/L缓蚀剂SH-1的腐蚀介质(3%NaCl溶液)不同温度下挂片7天,评论不同温度对缓蚀剂SH-1缓蚀效果的影响,结果如图3所示。
由图3可知,L80-1管线钢在腐蚀介质(3%NaCl溶液)的腐蚀速率随着腐蚀介质温度的升高而增大,但腐蚀介质的温度40℃,SH-1对L80-1管线钢在3%氯化钠溶液中的缓蚀效果优异,温度为70℃时,L80-1管线钢腐蚀速率仅为0.0662mm/a,仍小于0.076mm/a。
这表明了SH-1具备良好的抗温能力。
2.3 腐蚀介质浓度对腐蚀速率的影响注入水矿化度高,其中Cl-的浓度高,其穿透性能强,易引起金属点蚀,在温度为40℃、腐蚀时间为7d条件下,评价加有50mg/L缓蚀剂的不同浓度腐蚀介质对L80-1管线钢的腐蚀速率,结果0 引言注水工艺是迄今各油田提高原油的采收率、稳产最为常见的开采方法之一[1],该方法既能持续油田的稳产又可降低油田开采成本,但其弊端为油田回注水矿化度高以及含有微生物(硫酸盐还原菌SRB)、CO2、H2S、O2气体,易造成金属腐蚀严重,不利于油田的正常作业并对安全生产造成严重威胁[2-3]。
抑制金属腐蚀最高效、经济、便捷的方法就是加入缓蚀剂,能吸附在金属表面隔离腐蚀介质达到保护金属作用[4],醛、酮、胺之间发生缩合反应形成曼尼希碱缓蚀剂,该缓蚀剂具有性能稳定、抗高温、抗盐性能强、缓蚀效果优异的特点[5]。


电化学方法筛选海水介质中的碳钢缓蚀剂罗帆;朱承飞;贾景龙【摘要】采用电化学交流阻抗谱法(EIS)以及动电位极化曲线法研究了6种缓蚀剂在海水中对碳钢的缓蚀效果.通过等效电路拟合得到电极的腐蚀速率,使用外推法求出腐蚀电流密度.结果表明:缓蚀效率由大到小为Na2MoO4、苯并三氮唑、Ce(NO3)2、葡萄糖酸钙、硫脲、ZnSO4.Na2MoO4能较好地抑制碳钢腐蚀,由于MoO42-在金属基底上产生一层缓蚀剂膜,有效地抑制了碳钢孔蚀的加剧,减缓了金属的腐蚀,缓蚀效率高达80.67%.【期刊名称】《南京工业大学学报(自然科学版)》【年(卷),期】2015(037)005【总页数】5页(P113-117)【关键词】缓蚀剂;海水;极化曲线;电化学阻抗谱【作者】罗帆;朱承飞;贾景龙【作者单位】南京工业大学材料科学与工程学院,江苏南京210009;南京工业大学材料科学与工程学院,江苏南京210009;南京工业大学材料科学与工程学院,江苏南京210009【正文语种】中文【中图分类】TG174.42作为地球生态系统中重要的组成部分,海洋蕴藏了巨大的资源,随着人类对能源需求的增大以及陆地资源的日益减少,开发海洋资源已成为解决能源问题、促进经济发展的重要途径。
由于海水中含有多种强电解质,以3.5% NaCl为主,并溶解有一定量的O2,绝大部分金属材料在海水中都存在着严重的氧去极化腐蚀[1]。
碳钢由于具有优良的力学性能和工艺性能使其成为海水中应用最广泛的材料之一,它在各海域的腐蚀数据和海水腐蚀性已成为世界各国的基本腐蚀数据资料[2]。
在众多防腐蚀方法中缓蚀剂由于其方便经济的特点备受关注。
不同于大部分缓蚀剂的快速发展,针对海水介质的缓蚀剂研究相对缓慢。
关于缓蚀剂的应用研究多集中于密闭体系中,然而作为一个敞开的复杂体系,环境的不稳定性使得海水中的碳钢缓蚀剂研究较少。
近年来对缓蚀剂的研究发现,在敞开体系中单独使用缓蚀剂所需浓度偏高,成本昂贵,但与其他保护技术联合防腐被越来越多地应用,可见,有必要进行缓蚀剂的筛选工作,为联合保护工作做指导。


图1 1号咪唑啉化合物的红外谱图咪唑啉抗CO
腐蚀性能评价
2
通过改变影响缓蚀性能的几个因素:缓蚀剂浓度、腐蚀温度以及腐蚀时间,在常压下,模拟饱和腐蚀介质中对1号缓蚀剂做进一步评价。
最后通过极化曲线测试来对缓蚀机理做初步探讨。
缓蚀性能研究
缓蚀剂浓度的影响
图2 缓蚀剂浓度对极化曲线的影响
从图2可知,添加缓蚀剂后金属的自腐蚀电位发生了正移,有可能是随着缓蚀剂浓度的增加铁离子
进入溶液克服的表面能增加,从而单位时间内进入
溶液的铁离子减少。
(2)在饱和CO
2
模拟采出水中加入70mg/L的缓蚀剂,考察了在30℃、50℃、70℃、90℃时的极化曲
线,结果如图3所示。
图3 温度对极化曲线的影响
从图3可知,随着温度的升高,金属的自腐蚀电位呈下降趋势,腐蚀电流增加,这有可能是温度的温度对缓蚀效率的影响
平均腐蚀速率(mm/a)合成缓蚀剂
缓蚀效率(%)
0.07 0.098 0.172 0.28181.53 74.14 54.62 25.86
腐蚀时间对缓蚀效率的影响
钢失重(g)平均腐蚀速率
(mm/a)
合成缓蚀剂。



线性极化法测定金属的腐蚀速度实验报告一、 实验目的1.了解线性极化法测量金属腐蚀速度的基本原理。
2.掌握PS-1型恒电位仪的使用方法。
二、 实验原理线性极化法也称极化电阻法,是基于金属腐蚀过程的电化学本质而建立起来的一种快速测定腐蚀速度的电化学方法。
由金属腐蚀动力学基本方程式(1-1) :⎥⎦⎤⎢⎣⎡--⎩⎨⎧⎥⎦⎤⎢⎣⎡=A c c c C 3.2exp 3.2exp corr b b i i ηη外(1-1)通过微分和适当的数学处理可导出:c A c A c c c C corrcorr )3.23.2()3.23.2(ηηηi b b b b i i +=+=外 可知 c外C A c Ac )b (3.2b bcorr ηi b i•+=可见i c 外与ηC 成正比,即在η<10mV 内极化曲线为直线。
直线的斜率称为极化电阻R P ,即0d d C C →⎪⎪⎭⎫⎝⎛=ηηη外p R 可得 ()c a c a b b b b +⋅⋅=3.2R 1i P corr 式中p R ——极化电阻,Ωcm 2;corr i ——金属自腐蚀电流,A /cm 2;a b 、c b ——常用对数,阳极、阴极塔菲尔(Tafel)常数,V ;若令 ()c a ca b b b b B +⋅=3.2则有 corri B R p =pR B i =corr 式(1-1)即为活化极化控制下的腐蚀体系其极化电阻与腐蚀电流之间存在的线性极化关系的基本公式(Stern 公式)。
很显然极化电阻p R 与腐蚀电流corr i 成反比。
当实验测得p R 和a b 、c b 后就可以求得腐蚀电流corr i 。
对于大多数体系可以认为腐蚀过程中a b 和c b 是一个常数。
确定a b 和c b 的方法有以下几种:1.极化曲线法:在极化曲线的塔菲尔直线段求直线斜率a b 、c b 。
2.根据电极过程动力学基本原理,由Fn a RTb a a )1(3.2-=和Fan RTb c c 3.2=等公式求a b 、c b ,该法的关键是要正确选择传递系数a 值(a 值为0~l 之间的数值),这要求对体系的电化学特征了解得比较清楚,例如,析2H 反应,在20℃各种金属上反应a≈0.5,所以c b 值都在0.1~0.12V 之间。
#分析检测#羧酸类铜缓蚀剂的制备及性能测试大连理工大学化工学院电化学工程系(116012) 董泉玉 陈号卫 杨从贵 王志琨 单 耕 卢家成[摘 要] 介绍了新型羧酸类铜缓蚀剂的制备方法,用挂片失重法和测试电化学极化曲线的方法,研究了其对铜在海水中的缓蚀性能,并同B TA 的缓蚀性能进行了对比;结果表明,该类缓蚀剂制备工艺简单,且具有比BTA 更好的缓蚀性能。
[关键词] 苯骈三氮唑; 铜缓蚀剂; 羧酸类缓蚀剂; 性能测试[中图分类号] TG174.42 [文献标识码] A [文章编号] 1001-1560(2001)03-0049-02[收稿日期] 2000-10-121 引 言羧酸类缓蚀剂的生产合成比较简单,它对铜及铜合金具有突出的缓蚀性能,特别是在海水介质中。
目前,国外的有关文献都是关于它作为树脂增塑剂方面的报道,还未曾有把它用作铜系金属缓蚀剂方面的报道,国内至今尚未有这方面的报道。
所以,对于它的合成开发有着重要的意义,也有很好的发展潜力和应用前景。
该类缓蚀剂是把多元酚末端的羟基置换成羧基而生成的,所以它具有二碱基酸的性质,可以用碱性物质(如苛性钠)将其末端的羧基中和,因此它易溶于水,这为它作为缓蚀剂提供了有利的条件。
铜广泛应用于发电站的凝汽器,空调机的冷凝管等设备中。
国内许多发电站都用海水作凝汽器黄铜管的冷却水,因此开发更加有效的海水介质用铜缓蚀剂具有很好的应用前景。
此外,汽车发动机不冻液中混有金属防腐剂、消泡剂、色素等添加剂,该类缓蚀剂与这些添加剂混合使用都不会产生任何影响,因此在汽车工业中也有很好的应用前景。
日本已将这种缓蚀剂广泛应用于汽车内燃机的冷却液中,它可有效防止冬季冷却水的冻结和金属铜管的腐蚀,同时解决了防冻和防锈问题。
2 制备方法羧酸类缓蚀剂的结构为:HO 2CROq(R 2)XZq(R 3)YOR c CO 2H 其中,R 和R c 是含有1~6个碳原子的碳氢化合物;R 2和R 3是含有1~4个碳原子的碳氢化合物或含有芳香环的化合物;X \0,Y [3;Z 是氧、硫、二氧化硫、一氧化碳或是含有1~9个碳原子的碳氢化合物。
1
实验8 极化曲线评选缓蚀剂
一. 目的要求:
1.掌握用极化曲线Tafel区外推法测定金属腐蚀速度的原理及方法。
2.掌握评选缓蚀剂的原理及方法。
3.评定乌洛托品在盐酸中的缓蚀效率。
二.基本原理:
利用近代的电化学测试技术,可以测得以自然腐蚀电位为起点的完整的极化曲线。如图8—1
所示:
图8—1 外加电流的活化激化曲线
在开始时,把极化电位控制的很低,然后逐渐提高极化电位,这样的极化曲线可以分三个区:
(1)线性区——直线AB段
(2)弱极化区——曲线BC段
(3)Tafel区——直线CD段
把Tafel区CD段(在ф——㏒I图上)的切线外推与自然腐蚀电位фc的水平线相交于O点,
此点所对应的电流密度即为金属的自然腐蚀电流密度ic,根据法拉第定律,即可以把ic换算为腐
蚀重量或腐蚀深度。
对于阳极极化曲线不易测准的体系,常常只由阴极极化曲线的Tafel直线外推与фc的水平线相交以求出ic
这种以利用极化曲线的Tafel区直线外推以求腐蚀速度的方法称之为极化曲线法或Tafel线外推法。它有许多
局限性 :它只适用于在Tafel区的电极过程服从于指数定律的腐蚀体系,如放氢型的腐蚀。对于浓差极化较大的
体系,对于电阻较大的溶液在强烈激化时金属表面发生较大变化(如膜的生成或溶解)的情况就不适用。此外,
在外推做图时也回引入较大的误差。
用极化曲线评选缓蚀剂是基于缓蚀剂回阻滞腐蚀的电极过程,降低腐蚀速度,从而改变受阻滞的电极过程的
极化曲线的走向,见图8—2
2
图8—2缓蚀剂阻滞电极过程的极化曲线
由图8—2可见,未加缓蚀剂时,阴极阳极极化曲线相交于S0点,腐蚀电流为I0,加缓蚀剂
之后,阴极阳极极化曲线相交于S点,腐蚀电流为I,而I比I0要小的多。可见缓蚀剂明显地减
缓了腐蚀。根据缓蚀剂所阻滞的电极过程,可以把缓蚀剂分为阴极型,阳极型和混合型。
缓蚀剂的缓蚀率也可以直接用腐蚀电流来计算:
Z=(I0-I)/I0×100%
式中:Z——缓蚀剂的缓蚀效率(%)
I0——不加缓蚀剂时金属在介质中的腐蚀电流
I——加缓蚀剂之后在腐蚀介质中的腐蚀电流(也可以用电流密度来表示)。
本实验用恒定电位法测定碳钢在1NHCl,1NHCl加0.5%乌洛托品的极化曲线,评定其缓蚀
率。
三.仪器,药品及实验装置
1.恒定电仪(HDV——7型或JH——2C型) 一台
2.饱和甘汞电极,液桥,盐桥 各1支
3.铂电极 1支
4.碳钢试件 2个
5.电介质 各一个
6.1N盐酸 1升
7.乌洛托品0.5%(1N盐) 1升
8.试件夹具,试件预处理用品 若干
四.操作步骤:
1.准备好待测试件,打磨,测量,安装到聚四氟乙烯夹具上,脱脂,冲洗并安装于电介池中。
2.按图8—3接好路线,装好仪器,按恒电位仪操作规程,在电解池中注入足够的实验溶液,
恒电位仪的“电流测量”置于最大量程,预热调零,测量待测电极的自然腐蚀电位,调节“给定
3
电位”,“电流测量”置于适当的量程,进行极化测量,即从自然腐蚀电位开始,由小到大增加极
化电位,电位调节幅度可由10,20,30mV……..直至80mV左右。同一幅度可连续调节若干次,
每调节一次电位值1~2分钟后读取电流值,再调一次电位值,再读相应电流值,如此反复。
3.按步骤2进行如下测量:测碳钢在1N盐酸中阴极极化曲线,重测自然腐蚀电位,再测极化
曲线;更换或重新处理试件,在上述介质中加入0.5%乌洛托品,测定其系统中的自然腐蚀电位及
阴极,阳极极化曲线。
4.关机,结束实验。
五.数据处理:
试件材质( ) 介质成分( ) 介质温度( )℃
试件尺寸( ) 试件暴露面积( ) 参比电极( )
参比电极电位( )mV 辅助电极( ) 试件自然腐蚀电位( )mV
极化电位(mV) 极化电流 备注
Φt Φt—Φc
I
六.结果处理:
在同一张半对数坐标纸上分别绘出碳钢在二组溶液阴极和阳极极化曲线(△Φ~㏒I),并求
出自然腐蚀电流密度(mA/cm2)及乌洛托品的缓蚀率。
七.思考与讨论:
1.为什么可以用自然腐蚀电流密度
ic 代表金属的腐蚀速度?如何由ic换算出腐蚀重
量与腐蚀深度?
2.本实验方法的误差来源有哪些?