一等奖九年级化学教案大全5篇
- 格式:docx
- 大小:26.18 KB
- 文档页数:14
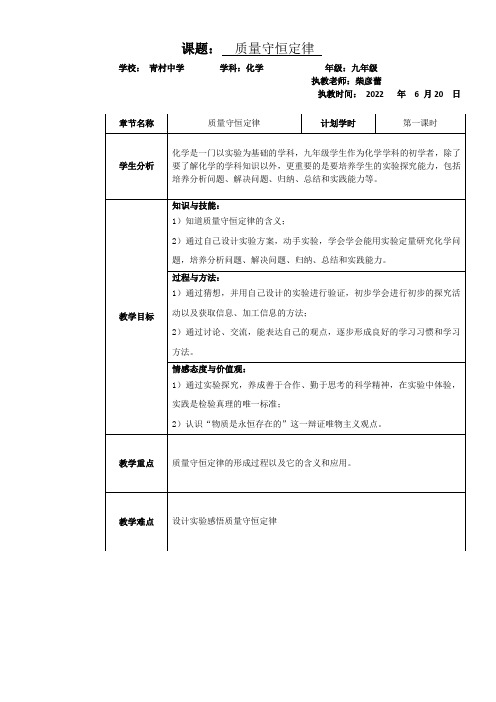
课题:质量守恒定律学校:青村中学学科:化学年级:九年级执教老师:柴彦蕾执教时间:2022 年 6 月20 日实验结论:猜想______正确,说明_______________________________________________实验反思:1、实验化学方程式:_________________________________________________________2、实验现象:____________________________________________________________【导学】1、质量守恒定律定义:_____________________________________________________2、注意事项:1)_____________________________________________________________________2_______________________________________________________________________3_______________________________________________________________________质量守恒定律导学案【探究实验的设计方案(组2)】实验目的:探究反应前物质的总质量与反应后物质的总质量的关系实验猜想:猜想1 反应前物质的总质量_____________反应后物质的总质量猜想2 反应前物质的总质量_____________反应后物质的总质量猜想3 _________________________________________实验仪器:___________________________________________________________________实验药品:硫酸铜溶液、铁丝实验步骤:__________________________________________________________________________________________________________________________________________________________________________________________________________________实验记录:反应后质量的变化情况实验结论:猜想______正确,说明_______________________________________________实验反思:3、实验化学方程式:_________________________________________________________4、实验现象:____________________________________________________________【导学】1、质量守恒定律定义:_____________________________________________________2、注意事项:1)_____________________________________________________________________2_______________________________________________________________________3_______________________________________________________________________质量守恒定律导学案【探究实验的设计方案(组3)】实验目的:探究反应前物质的总质量与反应后物质的总质量的关系实验猜想:猜想1 反应前物质的总质量_____________反应后物质的总质量猜想2 反应前物质的总质量_____________反应后物质的总质量猜想3 _________________________________________实验仪器:___________________________________________________________________实验药品:氯化钠溶液、硝酸银溶液实验步骤:__________________________________________________________________________________________________________________________________________________________________________________________________________________实验记录:反应后质量的变化情况实验结论:猜想______正确,说明_______________________________________________实验反思:1、实验化学方程式:_________________________________________________________2、实验现象:____________________________________________________________【导学】1、质量守恒定律定义:_____________________________________________________2、注意事项:1)_____________________________________________________________________2_______________________________________________________________________3_______________________________________________________________________质量守恒定律导学案【探究实验的设计方案(组4)】实验目的:探究反应前物质的总质量与反应后物质的总质量的关系实验猜想:猜想1 反应前物质的总质量_____________反应后物质的总质量猜想2 反应前物质的总质量_____________反应后物质的总质量猜想3 _________________________________________实验仪器:___________________________________________________________________实验药品:碳酸钠粉末、稀盐酸实验步骤:__________________________________________________________________________________________________________________________________________________________________________________________________________________实验记录:反应后质量的变化情况实验结论:猜想______正确,说明_______________________________________________实验反思:1、实验化学方程式:_________________________________________________________2、实验现象:____________________________________________________________【导学】1、质量守恒定律定义:_____________________________________________________2、注意事项:1)_____________________________________________________________________2_______________________________________________________________________3_______________________________________________________________________附录2:分类导航一级二级三级四级五级六级学科年级学期章节课题课时化学九年级第一学期二质量守恒定律1目标最低达成度:知道化学反应前后,参加反应的总质量等于生成物的总质量。

九年级下册化学教案一、教学目标1. 知识目标:1) 掌握有关化学反应和化学方程式的基本概念和基本原理;2) 掌握化学反应类型和化学方程式的书写规则;3) 了解一些常见的化学反应和它们的应用领域。
2. 能力目标:1) 能够正确理解和使用化学反应类型和化学方程式的概念,能够运用所学知识分析和解决相关问题;2) 能够合理设计和进行一些简单的化学实验,并能够正确记录实验数据和结果;3) 能够运用科学的思维方式,培养观察、实验、分析和推理的能力。
3. 情感态度目标:1) 培养学生对化学科学的兴趣和热爱,提高他们对科学事物的好奇心和探索精神;2) 培养学生的团队合作意识和实验安全意识,增强他们的自我保护意识;3) 培养学生的创新意识和实践能力,培养他们的批判性思维和解决问题的能力。
二、教学内容1. 化学反应和化学方程式的基本概念;2. 化学反应类型和化学方程式的书写规则;3. 常见化学反应及其应用领域。
三、教学重点1. 掌握化学反应和化学方程式的基本概念;2. 熟练掌握化学反应类型和化学方程式的书写规则。
四、教学难点1. 熟练掌握化学反应类型和化学方程式的书写规则;2. 能够正确理解和应用所学知识进行相关问题的解答和分析。
五、教学方法1. 探究式教学法:通过示例和实验引导学生主动探索化学反应和化学方程式的基本概念和规律;2. 讨论式教学法:引导学生通过小组讨论和思维导图的方式,提高他们的思维能力和解决问题的能力;3. 实验教学法:通过设计和进行简单的化学实验,加深学生对所学知识的理解和应用能力。
六、教学过程1. 导入(5分钟)通过展示一些日常生活中的化学反应现象(如:酸碱反应、氧化还原反应等),引起学生的兴趣和思考,为本节课的学习内容做铺垫。
2. 知识讲解(25分钟)a. 介绍化学反应和化学方程式的基本概念,引导学生理解分子、离子和原子之间的反应关系;b. 讲解化学反应的常见类型和化学方程式的书写规则,通过示例引导学生掌握正确的书写方法。

第五单元化学方程式课题1 质量守恒定律(2课时)第一课时)广南县第五中学校陆秋伶课标要求与分析要求:认识质量守恒定律,能说明化学反应中的质量关系。
分析:这是一条知识目标,通过实验探究完成化学反应前后的质量关系。
用微粒的观点对质量守恒定律做出解释。
本课要求达到了解、理解的水平教材分析本节内容节选自人教版九年级化学上册第五单元课题1,《质量守恒定律》第1课时,它包含质量守恒定律的含义,原因和应用,是初中化学一个重要的化学规律,它的运用贯穿于整个中学化学。
在本节之前,学生已经知道了物质经过化学反应可以生成新的物质,但是并没有涉及反应物与生成物质量之间的问题。
本课题主要通过实验来探讨化学反应过程中反应物总质量与生成物总质量之间的关系,开始了从生成何种物质向生成多少物质方面的过渡,引导学生从量的方面去研究化学反应的客观规律,为化学方程式的书写和有关计算的教学做好理论准备。
所以,本节内容在初中化学里有着承上启下的作用,它不仅是本单元的一个重点,也是整个初中化学的教学重点。
教学目标1知识与技能(1)通过实验探究理解质量守恒定律,了解常见化学反应中的质量关系。
(2)从微观角度认识在一切化学反应中,反应前后原子的种类和原子的数目没有增减。
2过程与方法通过探究性学习,让学生了解科学探究的基本思路,培养学生发现问题、探究问题的能力;3情感、态度、价值观通过探究学习,培养学生热爱科学、善于合作、实事求是的科学精神和态度;重点难点教学重点:质量守恒定律的含义及应用。
教学难点:1质量守恒定律的理解。
2从微观角度认识在一切化学反应中,反应前后原子的种类和原子的数目没有增减。
学情分析1学生的知识状况:学习了元素符号、化学式、化学反应的实质,初步掌握了一些简单的化学反应;2学生的能力状况:初步掌握了简单的化学实验基本操作技能,而对化学探究学习方法的了解尚处于启蒙阶段;3学生的心理状况:学生刚开始化学学习,情绪和心理都处于比较兴奋、好奇的状态;4学生存在的问题:从“定性”到“定量”,从“宏观”到“微观”;从“开放体系”到“密闭体系”的思维转换上还存在着一定的认知障碍。

初三化学第一课教案一、教学目标1. 知识与技能目标:a. 理解化学的基本概念和化学实验的基本步骤;b. 掌握化学实验中的安全操作规范;c. 理解化学实验中的常用仪器和玻璃器皿的使用方法;d. 能够进行简单的化学实验,并正确观察、记录和分析实验现象。
2. 过程与方法目标:a. 培养学生的实验操作能力和观察分析能力;b. 培养学生的合作意识和团队精神;c. 引导学生积极参与化学实验,善于发现问题和解决问题的能力。
3. 情感态度价值目标:a. 培养学生对化学实验的兴趣和好奇心;b. 培养学生的实验精神,注重实践探究;c. 培养学生的安全意识和环境保护意识。
二、教学重点与难点1. 教学重点:a. 理解化学实验的基本概念和步骤;b. 掌握化学实验中常用仪器和玻璃器皿的使用方法。
2. 教学难点:a. 引导学生正确观察实验现象,并进行分析和解释;b. 培养学生的实验操作能力和团队合作能力。
三、教学准备1. 教师准备:a. 整理教案;b. 准备化学实验所需的物品和仪器。
2. 学生准备:a. 阅读相关化学知识,了解基本概念和实验步骤;b. 准备好实验所需的实验器材和化学试剂。
四、教学过程1. 导入(5分钟)a. 引导学生回顾初中阶段学习的化学知识,回答问题,复习基本概念和实验步骤。
2. 初中化学实验基本概念讲解(15分钟)a. 讲解化学实验的定义和目的;b. 介绍化学实验中的基本步骤:观察、记录、分析、总结;c. 引导学生分析化学实验中的实验现象和实验结果,并进行解释。
3. 化学实验中的安全操作规范(15分钟)a. 讲解化学实验中的安全注意事项,包括佩戴实验服、戴眼镜、戴手套等;b. 引导学生了解化学实验中的危险物质和防护措施;c. 组织学生进行安全操作演示,并强调实验中的安全注意事项。
4. 化学实验中常用仪器和玻璃器皿的使用方法(15分钟)a. 介绍化学实验中常用的仪器和玻璃器皿,如量筒、试管、烧杯等;b. 演示仪器使用方法,并引导学生进行实验操作训练。

鲁教版初三化学教案一等奖初三化学第七单元教案一等奖《鲁教版初三化学教案一等奖初三化学第七单元教案一等奖》这是优秀的教案文章,希望可以对您的学习工作中带来帮助!1、鲁教版初三化学教案一等奖初三化学第七单元教案一等奖第七单元常见的酸和碱第一节酸及其性质教学目标:1.掌握盐酸、硫酸的化学性质及有关的化学方程式,掌握其性质和用途。
2.理解复分解反应。
3.了解酸碱指示剂、浓硫酸的特性及稀释。
4.通过展示样品及演示实验,培养学生的观察能力和分析实验现象的能力。
重点:盐酸、稀硫酸的化学性质。
难点:化学方程式的书写。
课时安排:三课时教学用品:纯净浓盐酸、工业浓盐酸、稀盐酸、NaOH溶液、Zn粒、铁丝段、锈铁钉、Cu(OH)2、CuO、AgNO3溶液、浓H2SO4、稀H2SO4、BaCl2溶液,浓HNO3、稀HNO3、石蕊试液、酚酞试液、水、玻璃棒、试管架、试管、烧杯、酒精灯、火柴等。
教学过程:第一课时(总第1课时)一、[引言]不同的酸在水溶液中电离出的阳离子全部为H+,决定它们必有相同的化学性质,但因酸根离子不同,必然又有各自的特性,即共性与个性的并存。
我们分别学习几种常见的、重要的酸。
【提问】什么叫酸?写出盐酸、硫酸、硝酸的电离方程式【板书】一、盐酸(HCl)盐酸是氯化氢的水溶液。
【演示】浓盐酸的物理性质:展示纯净浓盐酸和工业盐酸各一瓶,要求学生注意观察其色、态、闻气味(注意煽风闻味)。
待学生观察后,请一个学生回答浓盐酸的颜色、状态、气味。
【阅读】课本相关内容。
学生思考、师生互动、教师归纳:1.瓶口的白雾是什么?如何形成的?说明浓盐酸具有什么性质?2.如何保存浓盐酸?敞口放置后的浓盐酸质量和溶质的质量分数有何改变?【板书】1.盐酸的物理性质无色、有刺激性气味液体;有挥发性,常用浓盐酸密度1.19g/cm3,HCl的质量分数37%左右。
烟与雾的区别。
烟是固体小颗粒,雾为液体小液滴。
二、硫酸(H2SO4)展示浓H2SO4样品(请学生回答色、嗅、态)【板书】1.浓H2SO4(1)物理性质:无色、粘稠、油状液体,难挥发,高沸点(338℃)。
课题1《燃烧和灭火》教学设计一、教学目标本节课着重体现化学学习内容的现实性,培养学生对化学知识的应用意识。
具体三维目标如下:(1)知识与技能:①认识燃烧的条件、灭火的原理和方法;②会运用相关的知识解释和解决日常生活中的相关问题(2)过程与方法:①通过研究燃烧的条件,认识探究问题的方法;②利用实验学习对比在化学学习中的作用;③通过活动和探究,体会对获得的事实运用比较归纳等方法进行分析得出结论的科学方法。
(3)情感态度与价值观:①培养学生合作交流意识和探索精神;②激发学生热爱生活,关注社会的责任感;③使学生学会用辩证唯物主义的观点去认识事物,用发展的眼光看待事物教学重点、难点①重点:燃烧的条件和灭火的原理②难点:对着火点的理解课时安排本课题共需两课时,本节课为第一课时二、教法分析1、三力教学法:具体模式为:导→ 习→ 评。
2、多媒体辅助教学法:利用多媒体技术既能营造良好的课堂氛围,又能将探究的方案,讨论的情景提前准备好,给学生更多的时间动手、思考和讨论。
三、学法指导1、实验探究法:通过实验探究出燃烧的条件和灭火的原理,从探究中发现问题,分析问题,从而提高学生解决问题的能力。
2、合作学习法:让学生在讨论中取长补短,培养学生的合作竞争意识。
四、学情分析在学习本课题前学生的情况:1、已有的知识:(1)燃烧的本质;(2)一些物质在空气或氧气中燃烧的现象;(3)生活中关于燃烧的常识。
2、欠缺的东西:(1)对“着火点”、“可燃物”等概念的理解和运用还比较模糊;(2)知道灭火的方法,但不知道原理,即“知其然而不知其所以然”;3、学习的困难:在探究性实验中对于变量的控制问题,如“在什么情况下才需要使用控制变量”、“如何使用控制变量”、“控制变量是应注意哪些事项”等。
五、教学过程导(一)教师表演烧不坏的手帕,导入新课第七单元燃料及其利用,课题1燃烧和灭火(1)(二)【投影展示】学习目标请一名同学读出学习目标。
习首先,通过图片帮助同学们回忆学习过的燃烧事例,回忆燃烧现象。
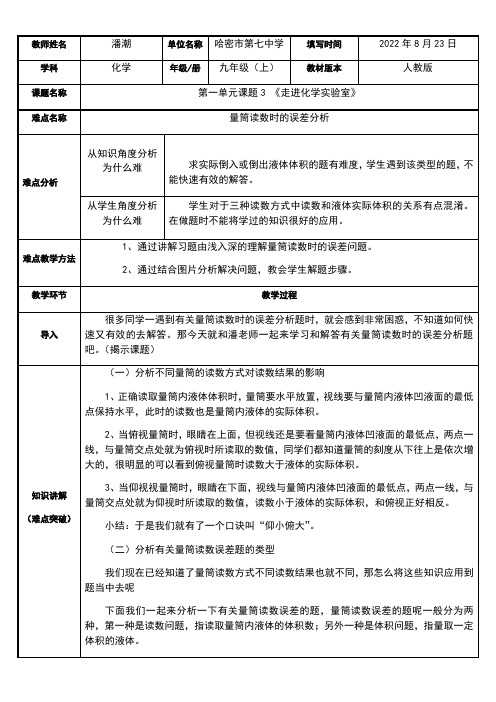
过滤实验教学设计哈密市巴里坤县奎苏镇中学路励尚一、教学目标1知识与技能了解过滤是使不溶性固体和液体分离的一种常用方法,了解过滤的适用程与方法通过动手实验、观察、协作等过程,学生能进行过滤操作及对失误进行简单分析。
3情感态度价值观通过实验操作渗透科学素质和实事求是精神的培养,培养学生的动手能力,体验实验操作的乐趣,激发学生学习化学的兴趣。
二、教学重点利用过滤分离混合物的原理以及注意事项。
三、教学难点过滤及过滤中注意事项。
四、教具准备自来水、玻璃棒、铁架台、烧杯、漏斗、玻璃棒、滤纸、小剪刀五、教学过程复习:什么叫纯净物什么叫混合物在日常生产和生活中,我们所接触到的物质很多是混合物,如河水,江水,自来水,粗盐水,石油等,为了适应各种不同需要,常常要将这些混合物中的几种物质分开,得到较纯净的物质,这就叫对混合物的分离。
其原理就是利用混合物中各组份物质性质的差异,将混合物中各组份转换为不同的状态而分离开来。
对混合物的分离方法很多,本节首先学习过滤方法分离混合物。
说到过滤,其实大家并不陌生,在我们日常生活中,经常会用到过滤的方法为我们生活服务。
例如家里制作豆腐时,用纱布将豆腐与豆浆水分开;煮饺子时,用沙漏勺子将煮熟饺子与汤分开;熬中药时,用一块布将药渣与药水分开;打鱼时,用渔网将鱼与水分开,再如卫生间里设有地漏盖子,将固体垃圾与水分开等等。
从这些可以看出,什么是过滤过滤的原理是什么1定义:过滤就是将液体中不溶性固体物质与液体彻底分离的一种方法。
2原理:过滤时,液体穿过滤纸上的小孔下来,而不能穿过小孔的固体物质就留在滤纸上,从而实现了对不溶性固体物质与液体彻底的分离。
3这个实验需要哪些实验仪器呢铁架台(带铁圈的)、烧杯、玻璃棒、漏斗下面大家就看看我过滤粗盐水的演示实验。
大家在观看过程中,注意实验步骤和实验注意事项。
4.步骤:①制作过滤器注意:A、滤纸紧贴漏斗内壁,润湿,中间不留有气泡----加快过滤速度B、滤纸边缘低于漏斗边缘----防止滤纸破损②架漏斗C、漏斗下端紧靠烧杯内壁----防液体溅出③过滤液体D、烧杯紧靠玻璃棒----防液体溅出思考:玻璃棒作用:引流E、漏斗内液面低于滤纸边缘----防过滤不充分F、玻璃棒下端紧靠三层滤纸一边----防弄破滤纸5.小结:简称:“一贴二低三靠”六、板书设计过滤操作要点:一贴、二低、三靠七、教学反思过滤操作是化学实验操作的重点,也是基础,过滤操作更是和我们的生活息息相关,因此,掌握过滤的操作方法可以为以后的化学学习打下坚硬的基础,而过滤过程中的一些操作要领对于过滤成功与否显得至关重要,对于操作要领要特别注意,规范实验操作是实验成功的保障。
化学《酸的通性》教案一等奖化学《酸的通性》教案一等奖1教学目标:一、知识目标:1、了解酸的分类方法和命名。
2、了解酸的通性,能熟练书写一些典型反应的化学方程式。
3、了解并记住金属活动顺序表,并能用它来判断金属能否与酸发生置换反应。
二、科学素养目标:从电离角度了解酸的通性,使学生逐渐懂得从个别到一般认识事物的过程。
教学重点:酸的通性及方程式的书写。
教学难点:金属活动顺序表的应用。
教学方法:比较归纳法、讨论法、练习法。
实验与电教:[实验8-19、8-20]投影仪、胶片教学过程:[复习提问]什么叫酸,写出已学过的酸的化学式。
[引入新课]略[讲授新课]一、出示教学目标(投影)二、酸的分类和命名引学生阅读课文P161,相应内容,分组讨论下列问题:1、酸有几种分类方法?根据是什么?2、酸是如何命名的?3、硫酸和氢硫酸是不是同一种酸?为什么?(由学生代表总结,教师归纳并板书)练习:说出下列各种酸所属类别和名称:HF、HBr、HCl、HClO3、H3BO3三、酸的通性(小组讨论)根据盐酸、稀硫酸的化学性质归纳,酸具有哪些相似的化学性质?学生回答后小结(投影)石蕊:变红指示剂─→使│酚酞:不变色酸金属金属氧化物碱盐↓ ↓ ↓ ↓(提问)酸为什么会具有相似的化学性质呢?请写出HCl、H2SO4、 HNO3的电离方程式,并找出它们电离产物的共同点。
(小结)酸的水溶液中都存在相同的.阳离子──H+,故它们有相似的化学性质,我们称之为酸的通性。
以下由学生阅读,师生共同总结出酸的通性1、紫色石蕊试液遇酸变红色,无色酚酞遇酸不变色2、活泼金属+酸→盐+H2(提问)为何要强调活泼二字?是否有些金属不能与酸反应生成氢气?(学生分组探究)[实验8-19]结论:铜及银跟酸不反应小结:并非所有的金属都能跟酸反应生成盐和氢气,金属能否与酸反应与金属本身的活动性有关。
(投影)金属活动性顺序并分析K Ca Na Mg Al,Zn Fe Sn Pb(H),Cu Hg Ag Pt Au失电子能力强─────→弱活动性强─────→弱(讲解)①金属跟酸反应的条件:只有排在氢前面的金属才能置换出酸中的氢。
课题3二氧化碳的实验室制法一、教学目标知识与技能1、了解实验室制取二氧化碳的药品和反应原理。
2、探究实验室制取并收集二氧化碳的方法;以及验证和验满的方法。
3、了解实验室中制取气体的思路和方法。
过程与方法1、探究实验室制,取二氧化碳的药品、装置,并利用设计的装置制取二氧化碳。
2、通过探究活动过程,体验化学实验的科学性,了解实验室制取气体的思路和方法。
3、初步认识观察、分析、讨论、归纳、总结、理解以及运用的科学方法过程。
情感态度理解与价值观1、激发学生的探究兴趣和学习化学的动机。
二、教学重难点重点:了解实验室制取二氧化碳的化学反应原理和装置设计以及制取方法。
难点:通过活动和探究,研究实验室中制取二氧化碳的装置,并利用设计的装置制取二氧化碳。
三、教学准备多媒体课件、实验室制取二氧化碳的相关药品和仪器。
四、教学过程一、故事导入学生讲故事:很早以前,在西德的一个州,有一片奇异的泽地:每当猎人牵着狗通过的时候,猎人安然无恙,狗却死了。
当时那里人们都传说这泽地上有魔鬼,它最嗜好吃狗。
在意大利那不勒斯山中有一个著名的屠狗洞,传说洞中有一个屠狗妖,人进入洞中安然无恙,狗却死亡。
老师提问:大家知道这妖怪是什么吗大家想不想抓住这妖怪呢学生回答:二氧化碳,想老师引入课题:今天我们就一起来学习二氧化碳制取的研究(二)合作探究1、PPT展示制取二氧化碳的药品选取原则:①反应条件是否容易达到。
②产生气体的量的多少。
③收集的气体是否纯净。
④装置、操作是否简单。
⑤原料是否易得、价廉。
⑥产生的气体是否利于收集。
⑦反应速度是否适中。
2、制取二氧化碳药品的选择及反应原理老师演示实验:(1)(Na2CO3粉末和稀盐酸(2)CaCO3粉末和稀盐酸(3)块状石灰石和稀盐酸(4)块状石灰石和稀硫酸学生:观察并记录实验现象,得出实验结论,组内讨论,分组表达。
师生归纳得出:实验室制取二氧化碳药品以及反应原理药品:块状石灰石和稀盐酸,因为产生气泡速率比较适中有利于气体的收集。
一等奖九年级化学教案大全5篇一等奖九年级化学教案大全5篇化学是一门研究物质的组成、性质和变化的科学,探索着万物的基本构造、反应过程和能量转化。
这里给大家分享一些关于一等奖九年级化学教案,供大家参考学习。
一等奖九年级化学教案(篇1)教学目标:1.经历从具体情境中抽象出比的过程,理解比的意义,氧气教学设计。
2.能正确读写比,记住比各部分的名称,会正确求比值。
3.初步理解比与分数、除法之间的关系。
4.能利用比的知识结合一些简单的生活现象,感受比在生活中的广泛应用。
教学重点:理解比的意义,会求比值。
教学难点:理解比与除法、分数的关系。
教学准备:电脑PPT课件教学过程:一、创设情境,导入新课1、投影出示淘气的相片。
师:这是我们熟悉的小伙伴——淘气。
同学们仔细观赏图片,在这些照片中,你觉得哪些看起来更美观,更舒服?看看哪几张和图A比较像?为什么?师:刚才同学们是用眼睛观察到的,用数学知识怎样解释呢?师:这些图片都是什么形状?下面我们研究一下这些长方形。
研究长方形我们通常从哪些方面入手?那么上面这些长方形的长和宽之间有什么关系?师:为了准确地判断它们为什么那么“像”,我们可以把它们放在方格纸上来研究。
如,图A的一条边是4份,另一条边是6份。
剩下的图形请大家仔细观察每一个长方形,自己数一数长和宽的份数,填一填、比一比。
小组讨论:学生观察、讨论,动笔计算。
分别找出图中长和宽的倍数(或分数)关系。
教师巡视,了解各小组讨论的情况,并加以引导。
学生汇报讨论成果。
师:你是怎么得出的?师:谁说一下其他几个长方形长和宽的关系。
师:你们还发现了什么?师:根据上面的计算,请同学们解释一下为什么图片A和图片B、D比较像?师:那谁能说说C和E为什么不像?小结:长方形的长和宽同时扩大或缩小相同的倍数,图形的大小变化了,但不变形。
长与宽的倍数关系不变,照片看起来就像;长与宽的关系发生变化,照片看起来就不像。
2、生活实例(1)出示情境图师:你喜欢吃苹果吗?现在有三个卖苹果的摊位,据我观察,质量上没什么差别。
你认为该去哪个摊位买呢?应该考虑什么问题?①学生独立思考。
②全班反馈交流:A:15÷3=5(元) B:9÷2=4.5(元) C:12÷3=4(元)(2)出示情境图马拉松选手跑40千米,大约需2时。
小刚骑车3时可以行45千米。
谁快?师:要比谁快,比什么呢?要比速度,也就是要求哪个量与哪个量的比?汇报交流,老师板书:40 :2=40÷2=20(千米)45 :3=45÷3=15(千米)二、探究新知,构建模型1、揭示课题:刚才我们研究长方形的长与宽的关系、苹果单价,跑步和骑自行车的速度时运用的都是除法算式,像上面那样,两个数相除,又叫做这两个数的比。
这就是我们今天要学习的内容:“生活中的比”2、请同学们自学P50的“认一认”,然后交流你从中知道了哪些关于比的知识(1)意义:两个数相除,又叫做这两个数的比。
(2)比号、前项、后项、比值、写法、读法。
三、拓展运用,巩固新知1、同学们,我们对比已经有了一定的认识,生活中还有很多的事情是和比密切相关的,我们生活中有哪些比?①教室里有四个窗户、两扇门。
窗户和门的数量的比是4 :2②我的身高是153厘米,我爸爸身高是178厘米,我的身高和爸爸身高的比是153厘米:178厘米。
③我有1支钢笔,3支圆珠笔。
我的钢笔数量和铅笔数量的比是1 :3。
④我们小组有男生4人,女生2人。
男生人数和女生人数的比是4:2。
2、你觉得比和我们以前学习的哪些知识有关?(除法、分数)四、质疑问难,归纳总结1、各类比赛中的比和我们今天学的比一样吗?它只是一种计分形式,是比较大小的,是相差关系,不是相除关系。
2、人的脚长与身高的比1∶7。
福尔摩斯发现一个脚印长25厘米,他可以做出什么样的推断?3、今天我们认识了谁?它表示什么意思?课后继续找一找哪些地方还用到了比?一等奖九年级化学教案(篇2)教学目的:1、使学生了解空气的组成。
2、使学生认识空气是一种宝贵的自然资源。
3、使学生初步了解空气污染的后果和防止污染的重要意义。
4、初步培养学生的观察能力;查阅搜集资料的技能;表达与交流能力;为学生提供展示特长和才干的机会。
重点:增强环保意识。
课时:1课时准备:1、搜集资料在本课前2~3周动员学生多方面搜集有关空气的素材,包括课外读物、科普书籍、杂志、报纸、照片、录像、漫画、实物等。
例如:课外读物:环境知识读本、关于空气的知识、大气污染方面的文章。
照片:风景地的蓝天、本地的晴天和污染天气、学生外出旅游、交通堵塞、工厂烟囱冒烟,杂志(或照片):酸雨、太空、臭氧层空洞、水灾等照片。
漫画:大气污染的严重后果。
剪报:某一期的《大气质量周报》或《大气质量日报》、大气污染报道等。
录像:空气、酸雨、保护臭氧层、温室效应。
2、课外预习和调查结合搜集的素材,阅读课文,查阅有关资料,为在课堂上介绍有关知识做准备。
3、课前活动(见学生页)(1)[观察]烟气观测活动。
(2) [小实验] 哪儿的尘土多?(3)[调查活动]交通流量与空气质量的关系。
4、布置教学环境组织学生编写环境墙报、图片、漫画、小论文等,布置教室。
教学过程:1、引言教师用简明的语言说明本节课的意义及教学活动的方法。
2、观看录像《空气》。
3、课堂展示。
学生按自选专题,根据课前的准备发言、讨论(一人中心发言,其他人补充)。
4、讨论(选择以下部分题目讨论)● 你愿意在树林里还是愿意在室内活动?● 吸烟会不会污染空气?● 焚烧树叶、庄稼秸秆会不会污染空气?● 有哪些减少空气污染的方法?● 家庭最主要的空气污染来自哪些活动?● 每天开窗通风换气有什么好处?● 新装修的居室有没有刺激性气味?● 你能为保护空气质量做哪些事?5、专题讨论“造成空气污染的原因”6、课堂小结教师对学生发言及讨论作必要的补充,鼓励、表扬学生认真自学,积极探索,独立思考、勤于实践态度和方法。
实验的结果和结论并不重要,不要求有统一的结论,重要的是每个学生积极参与及在活动中受到教育和启发。
7、布置作业指导举办关于大气的环境专刊、演讲比赛,组织野外活动、参观等。
一等奖九年级化学教案(篇3)【教材分析】从知识结构来说:空气是学生在化学课上接触到的第一种物质,而学生们在生活中可以从不同的途径获取有关空气的知识,因此本课题教学是很容易引起学生学习兴趣。
选择以空气为主题,开始这一单元的教学活动,是符合“从学生熟悉的事物入手,进行科学教育”的原则。
从能力培养来说:从看图了解拉瓦锡研究空气成分开始,到做仿照实验来测定空气里O2的含量,再到学生自主设计实验,可以说教材深入浅出,为以后的学习提供一个合理的思维方式。
从感情培养来说:通过本课题的学习,让学生充分体验到探究的乐趣,对化学学习充满兴趣。
【学情分析】初中的学习要求学生的思维方式要求逐步由形象思维向抽象思维过渡,因此在教学过程中应注意积极引导学生应用已掌握的基础知识,通过理论分析和推理判断来获得新知识,发展抽象思维能力。
当然在此过程仍需要以一些感性认识作为依托,可以借助实验或多媒体电教手段,加强直观性和形象性,以便学生理解和掌握。
因此做好每一个演示实验和调动好学生的积极性,不断提供动脑的问题情景,提供动手的练习机会,让每个学生参与到学习中来。
【教学目标】1、知识与技能(1)了解空气的主要成分;(2)了解氧气、氮气、稀有气体的主要物理性质和用途;(3)初步认识纯净物、混合物的概念,能区分—些常见的纯净物和混合物。
2、过程与方法(1)通过对“测定空气里氧气含量”实验的操作、观察、分析,培养学生能够设计和完成简单化学实验的能力。
(2)通过对空气、氧气等几种常见物质的比较,了解混合物和纯净物的概念。
(3)通过对空气污染情况的调查,知道空气污染的危害,学会一些简单的防治方法。
3、情感、态度与价值观(1)产生对化学学科的热爱,培养学生实事求是的科学态度,感受科学发现的过程和所运用的方法,发展相互交流,共同协作的科学精神,初步具备创新意识。
(2)养成关注环境、热爱自然的情感。
【教学过程设计】新的课程改革倡导从学生和社会的发展需要出发,将科学探究引入课堂,激发学生的主动性,让学生通过亲自经历来体验获取知识的过程,初步形成科学探究的方法。
所以本节课我以学生自主解决“测定空气中氧气含量” 的实验问题为中心展开学习,把本课分为以下几个环节:1、目的:创设和谐、轻松的学习氛围,培养学生学习化学的兴趣。
内容:引导学生从日常生活经验和第一单元的知识出发,先是让学生用多种方式感知空气的存在,接着由学生举实例证明空气含有的多种物质,进而提出探究空气中多种成分(主要是氧气)含量的任务。
这样就创设了一个生动而真实的问题情境。
2、目的:通过抢答,巩固旧知识,为新知识的学习奠定基础。
同时活跃课堂气氛,通过学生自主实验调动学生的积极性。
内容:讲述空气的发现史,然后出示拉瓦锡的照片以及拉瓦锡研究空气成分所用装置的图片,并讲述拉瓦锡发现空气组成的故事。
从而提出问题:拉瓦锡实验的原理仿照拉瓦锡实验的原则,我们也来测定空气里氧气的含量。
展示实验所需的仪器,并组织学生抢答下列问题:(1)有关仪器的名称;(2)集气瓶中有物质吗(3)谁能说出空气的成分有哪些要求学生按教材中图2-3连接装置并实验,适时指导学生观察实验现象、记录实验结果。
3、目的:让学生在观察与讨论中发现问题、提出问题、解决问题,从中培养科学观察、规范表达和分析问题的能力。
树立实事求是、严谨务实的科学态度。
内容:同组讨论:实验过程中观察到什么现象分析原因引导学生从两方面来分析:(1)实验成功,描述现象;(2)实验失败,寻找原因。
小结:由于红磷燃烧消耗瓶内的氧气,导致集气瓶内的气压减小,因而水倒流。
4、目的:对实验现象作进一步的分析、探究,培养学生的探索精神。
内容:讨论与思考:为什么要用红磷能否用木炭或硫粉然后进行分组实验:两组同学分别用木炭和硫粉重复上述实验,比较两次实验的不同,分析原因。
并自由发言。
5、目的:引导学生对所获得的事实与证据进行归纳,得出结论。
培养学生的规范表达能力。
内容:在上述探究活动的基础上,阅读教材有关内容,师生共同归纳空气的主要成分:由与红磷反应的气体(氧气)和与红磷不反应的气体(氮气)组成。
6、目的:拓宽学生的创新思维,扩大学生自主探究的空间。
内容:引导学生对以上实验进行回顾与反思,并思索对本实验是否有改进方法。
对较好的改进方案给予充分的肯定和鼓励。
及时提供其实验设备,让学生利用自己所设计的方案完成实验。
7、目的:让学生学会运用比较的方法,通过比较,可清晰地掌握概念。
内容:比较:氮气、二氧化碳、红磷、空气、河水、矿泉水等物质,从而得出混合物和纯净物的概念。
一等奖九年级化学教案(篇4)【教学目标】1.知识与技能⑴进一步了解化学是一门研究物质的组成、结构、性质以及变化规律的自然科学,它与人类进步和社会发展的关系非常密切。